Microesferas de silicio mesoporosas producidas a partir de la reducción magnetotérmica in situ de óxido de silicio para material anódico de alto rendimiento en baterías de iones de sodio
Resumen
Las baterías de iones de sodio se han utilizado ampliamente en el almacenamiento de energía debido a su alto contenido de sodio y su bajo costo. Este estudio demuestra que las microesferas de silicio mesoporosas (MSM) con los mesoporos distribuidos homogéneamente que van de 1 a 10 nm se pueden utilizar como ánodos de NIB. Se llevó a cabo una reducción magnesiotérmica in situ de óxido de silicio para sintetizar las muestras de MSM. Se probó un ánodo en NIB y se observó que la muestra de MSM que se calcinó a 650 ° C tenía un buen rendimiento de velocidad de 160 mAh g −1 a 1000 mAg −1 y una alta capacidad reversible de 390 mAh g −1 a 100 mAg −1 después de 100 ciclos. Además, su rendimiento de ciclismo a largo plazo fue de 0,08 mAh g −1 decaimiento por ciclo durante 100 ciclos, que fue bastante excelente. Los MSM tienen alta reversibilidad, buen rendimiento cíclico y excelente capacidad de velocidad, que están relacionados con su tamaño de partícula ultrafina y morfología mesoporosa.
Antecedentes
La batería de iones de litio es la primera opción para que los equipos electrónicos portátiles y los vehículos eléctricos almacenen energía debido a su alta densidad energética. Sin embargo, el alto costo, los recursos limitados y la distribución irregular del litio en el suelo son los principales problemas encontrados en el desarrollo de sistemas de almacenamiento de energía a escala de red. Debido al bajo costo y la gran abundancia de Na, las baterías de iones de sodio a temperatura ambiente con iones de sodio como portador de energía son uno de los sustitutos más prometedores de las baterías de iones de litio (LIBS) [1,2,3,4, 5]. Sin embargo, se debe desarrollar un nuevo concepto de diseño de materiales de electrodos porque Li + (0,69 Å) y Na + (0,98 Å) son diferentes en el radio iónico [6, 7]. Por ejemplo, debido al gran radio iónico de Na, es imposible absorber una gran cantidad de Na en el espacio entre capas por material de electrodo de grafito comercial para ánodos en LIB con la capacidad teórica de 372 mAh g −1 . El diagrama de fase Na-Si [8, 9] y la predicción de Ceder y Chevrier [10] y Chou et al. [11] señalan que la fase más rica en Na para los compuestos binarios de Na-Si es NaSi cuando se utiliza Si como ánodo en baterías de iones de sodio (NIB), de modo que la capacidad teórica es 954 mAh g −1 , y el Si puede ser un material prometedor para los ánodos de baterías de iones de sodio. Los experimentos también estudiaron la sodiación electroquímica [12,13,14,15,16] de Si de tamaño micrométrico [17] y Si de tamaño nanométrico (100 nm) [18]. Mulder usa nanopartículas de Si como ánodo en NIB, la capacidad específica es de aproximadamente 300 mAh g - 1 después de 100 círculos [9]. Y Mukhopadhyay estudió la capacidad específica de nanocables de silicio estructurados con estructura de capa amorfa / núcleo cristalino de hasta 390 mAh g −1 después de 200 círculos [19]. Dado que el Si amorfo es conductor para la inserción de Na y la nanoescala es favorable para la cinética de inserción y extracción de iones, se exploraron a fondo partículas de Si con un tamaño más pequeño y una gran fracción de Si amorfo obtenidas expandiendo el silano [20, 21].
Sin embargo, el elevado coste y la complicada síntesis de los métodos de composición pueden dificultar la realización de una producción a gran escala. Por lo tanto, es muy urgente desarrollar un método simple y eficiente para sintetizar el material del ánodo de Si con buen desempeño [22,23,24]. Mediante el uso de reducción magnesiotérmica in situ de óxido de silicio, se estudiaron microesferas de silicio mesoporosas (MSM) con diámetros que van desde 1 a 10 nm distribuidas homogéneamente en las microesferas de silicio. Los resultados experimentales muestran que se puede lograr una absorción electroquímica reversible de iones de Na en Si, y se obtiene una capacidad notable. Se utilizaron microscopía electrónica de transmisión (TEM), microscopía electrónica de barrido (SEM) y difracción de rayos X (XRD) para caracterizar el producto final, que se evaluó adicionalmente mediante una prueba cíclica. Cuando la densidad de corriente se incrementó a 1000 mAg −1 , más del 40% de la capacidad se puede retener a través de NIB; por lo tanto, las microesferas se utilizan como materiales de ánodo.
Métodos / Experimental
El proceso de Stöber modificado se utilizó para sintetizar SiO 2 microesferas. Se agregaron veinte mililitros de ortosilicato de tetraetilo a 100 ml de H 2 desionizado O. Veinte mililitros de NH 3 · H 2 Se añadieron O y 80 ml de 2-propanol a la mezcla y se agitó magnéticamente a temperatura ambiente. Después de que la reacción duró 2 h, el SiO 2 coloidal Las esferas se recogieron mediante centrifugación, se lavaron con agua desionizada y etanol y se secaron a 100ºC. Quinientos sesenta miligramos de SiO 2 preparado Se colocaron microesferas y 600 mg de magnesio en polvo en dos recipientes de acero inoxidable por separado. Posteriormente, los recipientes se colocaron en un horno de acero inoxidable sellado y se calentaron a 650 ° C durante 2 h bajo protección de Ar. El mecanismo de reacción es el siguiente:
$$ 2 \ mathrm {Mg} + {\ mathrm {SiO}} _ 2 \ to \ mathrm {Si} +2 \ mathrm {Mg} \ mathrm {O} $$ (1)Los compuestos de magnesio y el magnesio restante se disolvieron almacenando el polvo de color marrón amarillento en una solución de ácido clorhídrico (HCl) 1 M (200 ml, 1 M) durante 12 h. La mezcla se filtró a través de agua destilada y el polvo se secó al vacío durante 12 ha 80ºC. El polvo de microesferas de Si se adquirió de Sigma-Aldrich Co. LLC para una comparación adicional. Se utilizaron pilas de botón tipo 2032 para realizar mediciones electroquímicas. Se formó una suspensión mediante la adición de polivinildifluoruro (10% en peso), negro de acetileno (20% en peso) y material activo (70% en peso) a N -metilpirrolidona. Se adoptó el método de raspado para pegar la lechada en un colector de corriente de lámina de cobre, que se secó al vacío hasta un peso final de 2 mg / cm 2 . Montamos las baterías de iones de sodio de media celda en una caja de guantes llena de Ar con Celgard2250 como separador, NaClO 1 M 4 disuelto en una mezcla de carbonato de etileno y carbonato de dietilo (1:1 en volumen) como electrolito, lámina de Na como contraelectrodo y MSM como electrodo de trabajo. Se llevaron a cabo experimentos de carga y descarga galvanostática de las celdas en un sistema de prueba de baterías (LAND, Wuhan Jinnuo Electronics Ltd.) a diferentes densidades de corriente de 0,01 a 2,5 V.
Resultados y discusión
Los patrones de XRD del nanocompuesto de MgO-Si tal como se forma, los MSM y las microesferas de Si se muestran en la Fig. 1. Los picos de difracción principal a 2 θ =28,4 °, 47,4 °, 56,2 °, 69,2 ° y 76,4 ° presentados por HSH pueden ser índices como (1 1 1), (2 2 0), (3 1 1), (4 0 0) y (3 3 1) planos de cristalitos de Si (JCPDS 772107). No hubo ningún pico adicional relevante con la impureza en los patrones de XRD. La solución de HCl podría lavar completamente el MgO en el nanocompuesto de MgO – Si.
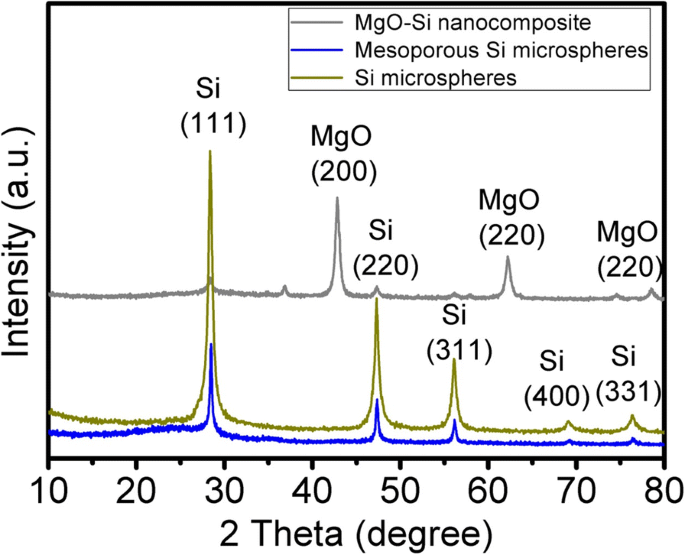
Patrones XRD de las muestras
Se adoptaron SEM y TEM para examinar las morfologías de microesferas de Si mesoporosas y microesferas de Si. Las imágenes típicas de TEM y SEM de la esfera de Si se muestran en la Fig. 2a. Las imágenes SEM de microesferas de Si mesoporosas a varios aumentos se muestran en la Fig. 2b. Hay abundantes mesoporos en las microesferas de Si. Las imágenes TEM de los MSM se muestran en la Fig. 2c, d. Los diámetros de la estructura mesoporosa de las microesferas de Si son de 1 a 10 nm. La Figura 2e es la imagen TEM de los círculos de MSM con una densidad de 100 mAg −1 . Se puede observar una isoterma de tipo IV típica con un bucle de histéresis de tipo H3 en la curva de adsorción-desorción (Fig. 2f), que indica los mesoporos desordenados en los HSH. De acuerdo con la curva de distribución del tamaño de poro de Barrett-Joyner-Halenda (BJH) de la rama de adsorción, la distribución de poros está por debajo de 6 nm, lo que concuerda con el resultado de TEM. El volumen de los poros y el área de la superficie BET fueron de 0,25 cm 3 g −1 y 200 m 2 g −1 . Dado que los mesoporos sirven como zona de amortiguación, las variaciones de volumen de silicio son acomodadas de manera efectiva por los MSM que pueden mantener la estructura en el proceso de carga y descarga. Se pueden mantener buenas conductividades electrónicas agregando carbono conductor, que es conductor de los materiales de los electrodos en las NIB.
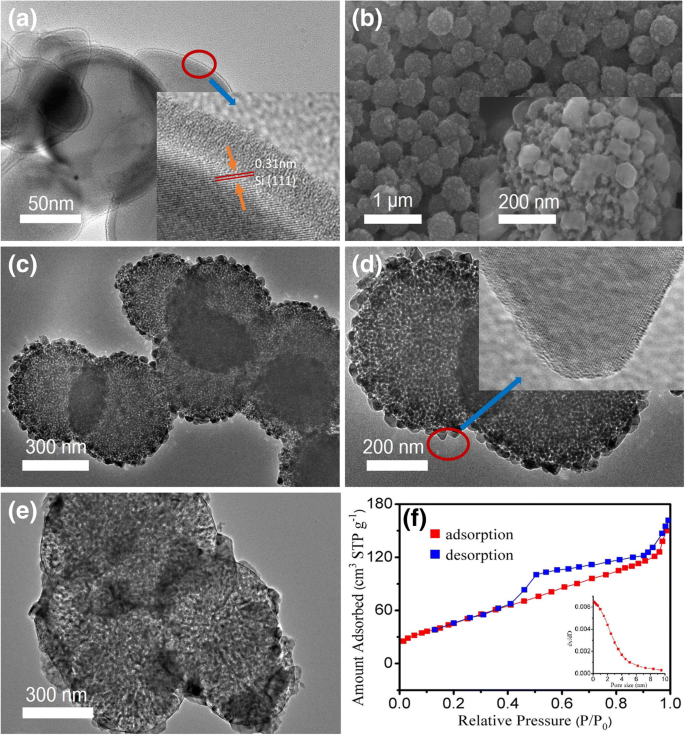
SEM ( a ) y TEM insertado ( a ) imágenes de microesferas de silicio. SEM ( b ) y TEM ( c y d ) imágenes de HSH. TEM ( e ) 100 después de círculos en 100 mAg - 1 . La curva de adsorción-desorción ( f ) de los HSH, recuadro:distribución del tamaño de partícula de los HSH
Llevamos a cabo mediciones de voltamperometría cíclica (CV) de 0,01 a 2,5 V a varias velocidades de exploración. Como se muestra en la Fig. 3a, cuando la velocidad de exploración es de 0,2 mV s −1 , hay un pico catódico obvio en 0.04, que se puede atribuir a la inserción del ion Na en el Si cristalino. El Si cristalino se extrae a 0,08 V a través del barrido anódico. La absorción de Na en el Si amorfo ocurre en un rango de voltaje más amplio y más alto (<0,8 V) [9]. Con el aumento de la velocidad de exploración, el pico de potencial se desplaza gradualmente hacia el voltaje alcalino más bajo y el potencial de descarbonización más alto, que es causado por el sobrepotencial cada vez más significativo. La Figura 3b muestra las curvas típicas de carga-descarga de microesferas de Si mesoporosas a las densidades de corriente de 0.01 V y 2.5 V versus Na + /N / A. La formación de NaSi provoca la meseta a 0,6 V en la primera curva de descarga. El aumento de la densidad de corriente conduce a la disminución del potencial de descarga y al aumento del potencial de carga de los MSM. Como resultado, se producen sobrepotenciales elevados. La celda se cicló durante 10 ciclos a la baja densidad de corriente de 100 mAg −1 , y la capacidad específica estable fue de aproximadamente 400 mAh g −1 . La proporción de la capacidad retenida es superior al 40% a 1000 mAg −1 , que indica la excelente capacidad de frecuencia de los HSH. Después de 60 ciclos de carga y descarga, la capacidad de aproximadamente 390 mAh g −1 fue retenido a diferentes densidades de corriente (Fig. 3c). Por tanto, la estabilidad del ciclismo es buena. Las curvas de capacidad de carga / descarga de los electrodos que están hechos de MSM versus el número de ciclo a la densidad de corriente de carga-descarga de 100 mAg −1 a 25 ° C se muestran en la Fig. 3d. La capacidad del silicio para la primera carga y descarga de las baterías de iones de sodio es mayor que la de la segunda carga y descarga, lo que se debe principalmente a la intercalación irreversible de iones de sodio y a la formación de una película SEI durante la primera carga y descarga. Después de 100 ciclos, la capacidad es de aproximadamente 390 mAh g −1 , y el electrodo MSMs tiene un excelente rendimiento cíclico a largo plazo de 0.08 mAh g −1 decaimiento por ciclo, lo que indica la buena estabilidad cíclica del electrodo. En cuanto a las microesferas de Si puro, el electrodo solo retuvo 30 mAh g −1 después de 100 ciclos con una densidad de corriente de carga-descarga de 100 mAg - 1 . Se mejoró la estabilidad cíclica de los HSH.
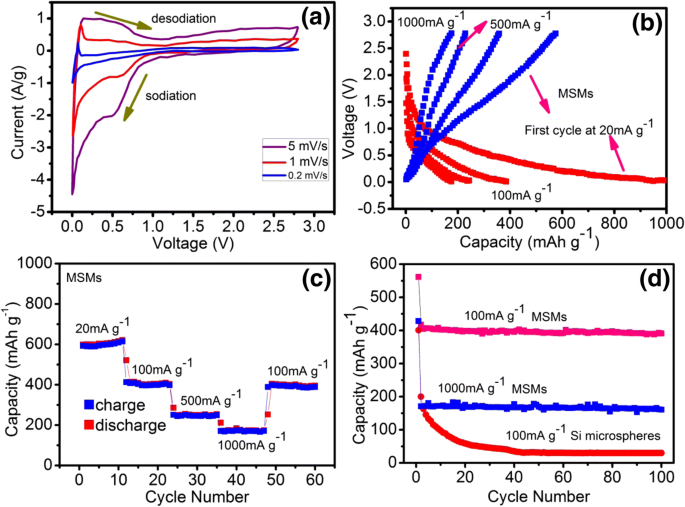
un Mediciones de voltamperometría cíclica de MSM a diferentes densidades de corriente, b Curvas representativas de carga-descarga de MSM a diversas densidades de corriente, c capacidad de retención de los HSH en diversas densidades de corriente, y ( d ) retención de capacidad de descarga de MSM y nanoesferas de silicio a una densidad de corriente de 1000 mAg −1 y 100 mAg −1
La Figura 4 muestra el proceso de síntesis típico de los HSH. Las microesferas de sílice tienen una gran superficie específica y pueden considerarse una fuente de silicio adecuada. Por lo tanto, los MSM se sintetizaron utilizando microesferas de Si como fuente de silicio en el proceso de reducción magnesiotermica. El vapor de magnesio fundido reacciona en microesferas de sílice y forma nanocompuestos de MgO-Si a 650 ° C. El MgO se elimina aún más mediante el tratamiento de nanocompuestos a través de una solución de HCl en el proceso de grabado. Los 3D MSM están formados por los nanocristales de silicio residuales, y las variaciones de volumen de silicio durante los ciclos repetidos de aleación y desaleación se acomodan tomando los mesoporos bien dispersos como zona de amortiguación. Se suprime la exfoliación y agregación de partículas de Si. Tanto el Si cristalino como el amorfo juegan un papel activo en la alcalinización electroquímica. NaSi y Si pueden coexistir cuando se inserta Na en Si amorfos y cristalitos de Si. Cuando se extrae Na, se confirma la reacción de desoxidación de la solución sólida. Mesoporoso también proporciona un canal de electrolitos útil para la transferencia de iones de sodio, lo que explica la mejora del rendimiento electroquímico de los HSH.
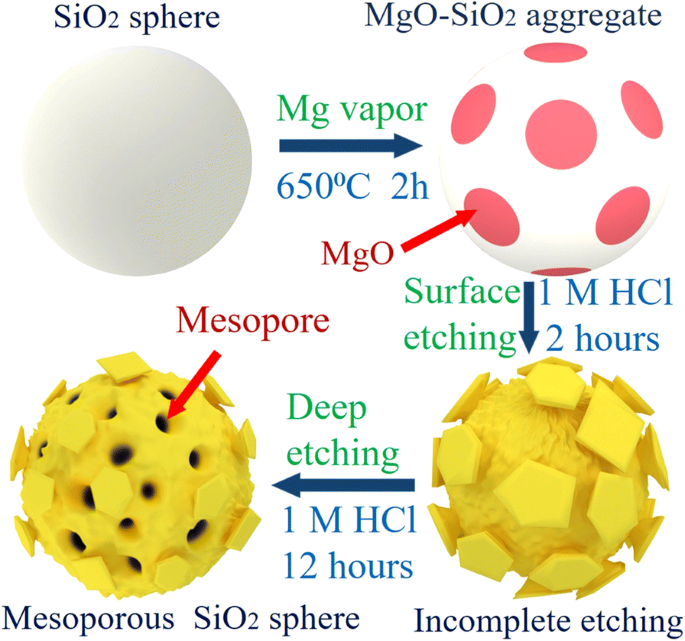
Ilustración esquemática de los HSH
Conclusiones
Se utilizó el método de reducción magnesiotermica para preparar un material de silicio mesoporoso 3D. Los resultados de la investigación demuestran que la absorción electroquímica reversible de iones de sodio puede realizarse a temperatura ambiente. Esta mejora se puede atribuir a nanoestructuras optimizadas relevantes con las estructuras mesoporosas distribuidas uniformemente.
Abreviaturas
- 3D:
-
Tres dimensiones
- BJH:
-
Barrett – Joyner – Halenda
- CV:
-
Voltamperometría cíclica
- HCl:
-
Ácido clorhídrico
- LIB:
-
Baterías de iones de litio
- MgO:
-
Óxido de magnesio
- HSH:
-
Microesferas de silicio mesoporosas
- NaSi:
-
Siliciuro de sodio
- NIB:
-
Baterías de iones de sodio
- SEM:
-
Microscopía electrónica de barrido
- Si:
-
Silicio
- TEM:
-
Microscopía electrónica de transmisión
- XRD:
-
Difracción de rayos X
Nanomateriales
- Síntesis fácil de nanopartículas de SiO2 @ C ancladas en MWNT como materiales de ánodo de alto rendimiento para baterías de iones de litio
- Compuesto negro de acetileno / MoS2 de pocas capas como material de ánodo eficiente para baterías de iones de litio
- Microesferas de carbono magnéticas como adsorbente reutilizable para la eliminación de sulfonamidas del agua
- Efecto de diferentes aglutinantes sobre el rendimiento electroquímico del ánodo de óxido metálico para baterías de iones de litio
- Na4Mn9O18 / Compuesto de nanotubos de carbono como material de alto rendimiento electroquímico para baterías acuosas de iones de sodio
- Nanopétalos mesoporosos de óxido de níquel (NiO) para detección de glucosa ultrasensible
- Compuesto de grafeno / Si integrado fabricado por reducción térmica de magnesio como material anódico para baterías de iones de litio
- Un ánodo de película de Fe2O3 nanocristalino preparado por deposición de láser pulsado para baterías de iones de litio
- Sintetizado hidrotermal de microesferas de CoMoO4 como excelente material de electrodo para supercondensador
- Microarreglos mesoporosos de VO2 bidimensionales para supercondensadores de alto rendimiento
- Reducción de óxido de grafeno a baja temperatura:Conductancia eléctrica y microscopía de fuerza de sonda Kelvin de barrido



