Sintetizado hidrotermal de microesferas de CoMoO4 como excelente material de electrodo para supercondensador
Resumen
El CoMoO 4 monofásico se preparó mediante un método hidrotermal fácil junto con un tratamiento de calcinación a 400 ° C. Se investigaron las estructuras, morfologías y propiedades electroquímicas de muestras con diferentes tiempos de reacción hidrotermal. La estructura de la microesfera, que consistía en nanoflakes, se observó en las muestras. Las capacitancias específicas a 1 A g −1 son 151, 182, 243, 384 y 186 F g −1 para muestras con tiempos hidrotermales de 1, 4, 8, 12 y 24 h, respectivamente. Además, la muestra con el tiempo hidrotermal de 12 h muestra una buena capacidad de velocidad, y hay un 45% de retención de la capacitancia inicial cuando la densidad de corriente aumenta de 1 a 8 A g −1 . Las altas capacidades de retención de las muestras muestran la fina estabilidad de ciclo largo después de 1000 ciclos de carga y descarga a una densidad de corriente de 8 A g −1 . Los resultados indican que CoMoO 4 Las muestras podrían ser una elección de excelentes materiales de electrodos para supercondensadores.
Antecedentes
Es importante desarrollar la conversión y el almacenamiento de energías alternativas renovables debido a la rápida descomposición de los combustibles fósiles. El supercondensador, como una especie de dispositivo de almacenamiento de energía, ha atraído mucha atención en los últimos años [1, 2, 3, 4, 5]. Los supercondensadores muestran un rendimiento deseable, como una alta densidad de potencia, un tiempo de carga corto y un ciclo de vida prolongado [6,7,8]. Según el mecanismo de almacenamiento de carga, los supercondensadores podrían clasificarse en condensadores electroquímicos de doble capa (EDLC) y condensadores electroquímicos redox (es decir, pseudocapacitancia (PC)). El mecanismo de almacenamiento de carga de los EDLC está relacionado con la adsorción y desorción reversibles de iones electrolitos en la superficie del electrodo / electrolito, mientras que el de los PC está relacionado con las reacciones redox en la superficie del electrodo [4, 6, 8, 9]. Por lo tanto, ya sea para EDLC o PC, los electrodos son muy importantes y es necesario encontrar un material de electrodo interesante para la aplicación de supercondensadores. Generalmente, la densidad de energía de los PC es más alta que la de los EDLC [10, 11]. Muchos materiales de óxidos metálicos, como NiO [12, 13], Co 3 O 4 [3], CuO [14], MnO 2 [15] y SnO 2 [16], han atraído mucha atención por su uso como electrodos supercondensadores. Entre estos óxidos metálicos, los óxidos de molibdeno y los óxidos de cobalto son los candidatos prometedores para aplicaciones debido a su alta actividad redox, múltiples estados de oxidación, alta capacitancia específica teórica, almacenamiento reversible de iones pequeños y bajo costo [11]. Zhou y col. preparado MoO 2 nanopartículas, y la muestra muestra una alta capacitancia específica de 621 F g −1 [17] y Wu et al. investigó las propiedades de MoO 2 / CNT con capacitancia de 467,4 F g −1 [18].
Los óxidos metálicos mixtos han atraído mucha atención debido a su alta actividad redox, buena conductividad eléctrica, almacenamiento reversible de iones pequeños y bajo costo [11]. Entre ellos, los molibdatos metálicos han atraído mucha atención para la aplicación de almacenamiento de energía. Como NiMoO 4 [19,20,21], MnMoO 4 [22, 23], CoMoO 4 [6, 8, 11, 24, 25] y otros molibdatos metálicos se han investigado extensamente como excelentes materiales de electrodos para supercondensadores. Como se informa en las Refs. [26,27,28], CoMoO 4 es ventajoso debido a su bajo costo y no toxicidad y exhibe propiedades electroquímicas mejoradas. Veerasubramani et al. preparó el CoMoO 4 en forma de plato con una capacitancia específica de aproximadamente 133 F g −1 a 1 mA cm −2 [26]. Padmanathan y col. sintetizó el α-CoMoO 4 nanoflakes / CFC utilizados como supercondensador simétrico con una capacitancia específica de 8,3 F g −1 a una densidad de corriente de 1 A g −1 en electrolito orgánico [29]. Además, Kazemi et al. obtuvo el CoMoO 4 en forma de diente de león con una excelente capacitancia específica de 2100 F g −1 a una densidad de corriente de 1 A g −1 [8]. Xia y col. informó que el CoMoO 4 / los compuestos de grafeno muestran una capacitancia específica de 394,5 F g −1 (a la velocidad de escaneo de 1 mV s −1 ), que es aproximadamente 5,4 veces el valor de CoMoO puro 4 [30].
En este artículo, CoMoO 4 Los nanoflakes se sintetizaron mediante un método hidrotermal simple en diferentes tiempos de reacción hidrotermal, seguido de calcinación a 400 ° C en horno de mufla. Las propiedades electroquímicas de las muestras se investigaron utilizando los métodos de voltamperometría cíclica (CV), descarga de carga galvanostática (GCD) y espectroscopia de impedancia electroquímica (EIS). Según los resultados de la prueba GCD, las muestras muestran capacitancias específicas de 151, 182, 243, 384 y 186 F g −1 a una densidad de corriente de 1 A g −1 en electrolito de KOH 2 M. La muestra CMO-12 presenta una propiedad electroquímica interesante.
Experimental
Síntesis de CoMoO 4
El CoMoO 4 Las muestras se sintetizaron mediante un método hidrotermal simple. En primer lugar, 0,4410 g Co (NO 3 ) 2 · 6H 2 O y 0,2675 g (NH 4 ) 6 Mo 7 O 24 · 4H 2 Se disolvieron O (AHM) en 30 ml de agua destilada con agitación magnética durante 10 min a temperatura ambiente para obtener una solución mixta transparente. En segundo lugar, se añadieron lentamente 0,3621 g de urea a la solución mixta de Co (NO 3 ) 2 · 6H 2 O y AHM bajo agitación magnética. La mezcla se agitó durante 1 h para formar una solución homogénea. A continuación, la solución homogénea se transfirió a un autoclave de acero inoxidable revestido con teflón de 50 ml y se mantuvo a 180 ° C en un horno eléctrico durante 1 h. Otras muestras se prepararon con los tiempos hidrotermales de 4, 8, 12 y 24 h, respectivamente. Los productos sintetizados se enfriaron a temperatura ambiente con el horno. Luego, la solución resultante se centrifugó con agua destilada y etanol. El precipitado obtenido se secó a 60 ° C en un horno de vacío durante 10 h. Finalmente, el precipitado seco se calcinó a 400 ° C en horno de mufla durante 2 h para obtener los productos finales. Los productos finales se marcaron como CMO-1, CMO-4, CMO-8, CMO-12 y CMO-24, respectivamente.
Caracterización del material
Las estructuras cristalinas de las muestras se determinaron mediante difracción de rayos X (XRD; Bruker, D8 Discover) a 40 kV y 40 mA. Las morfologías de las muestras se examinaron mediante microscopía electrónica de barrido de emisión de campo (FE-SEM; Zeiss, SUPRA 40) y microscopía electrónica de transmisión (TEM; JEM-2100). Las isotermas de adsorción-desorción de nitrógeno de las muestras se obtuvieron utilizando el aparato de adsorción física Autosorb-iQ. Luego, las áreas de superficie específicas y la distribución del tamaño de los poros de las muestras se obtuvieron mediante los métodos Brunauer-Emmett-Teller (BET) y Barrett-Joyner-Halenda (BJH).
Preparación del electrodo de trabajo y mediciones electroquímicas
Los electrodos de trabajo se prepararon de acuerdo con el método descrito en la literatura [31]. Los productos sintetizados, negros de acetileno y politetrafluoroetileno (PTFE) se mezclaron con una relación en peso de 70:20:10 para formar una pasta homogénea. Luego, se revistió sobre la espuma de níquel limpia con un área de 1 cm x 1 cm. Después de secar en un horno de vacío a 50 ° C durante 6 h para eliminar el disolvente, la espuma de níquel se prensó a continuación a 10 MPa durante 2 min mediante una máquina de perlas. La masa del material activo en el electrodo fue de aproximadamente 3 a 5 mg.
Las propiedades electroquímicas de las muestras se caracterizaron mediante el uso de una estación de trabajo electroquímica CS 350 (CorrTest, Wuhan) a temperatura ambiente. Se usaron dos moles por litro de soluciones de KOH como solución de electrolito, y se usó un sistema de tres electrodos en la medición. CoMoO 4 , platino y un electrodo de calomelanos saturado (SCE) sirvieron como electrodo de trabajo, contraelectrodo y electrodo de referencia, respectivamente. Las curvas CV se realizaron en el rango de potencial de - 0,2 a + 0,6 V a diferentes velocidades de exploración de 5, 10, 20, 40, 50 y 100 mV s −1 . Las curvas de GCD se probaron a diferentes densidades de corriente de 1, 1,5, 2, 3, 5 y 8 A g −1 . La EIS de las muestras se investigó desde 0,01 Hz hasta 100 kHz.
Resultados y discusión
Caracterización estructural y morfológica
Como se muestra en la Fig.1, los patrones XRD de las muestras son consistentes con el patrón estándar de CoMoO 4 (JCPDS No. 21-0868), y son similares a los reportados en anteriores [6, 8, 32, 33]. Los picos de difracción a 13,1 °, 19,1 °, 23,3 °, 26,5 °, 27,2 °, 28,3 °, 32,0 °, 33,6 °, 36,7 °, 40,2 °, 43,6 °, 47,0 °, 52,1 °, 53,7 °, 58,4 ° y 64,5 ° corresponden a las reflexiones de (001), (\ (\ overline {2} \) 01), (021), (002), (\ (\ overline {1} \) 12), (\ (\ overline {3} \) 11), (\ (\ overline {1} \) 31), (\ (\ overline {2} \) 22), (400), (003), (\ (\ overline {2 } \) 41), (241), (\ (\ overline {2} \) 04), (\ (\ overline {4} \) 41), (024) y (243) planos, respectivamente. Como se muestra en la Fig.1, los picos de difracción más amplios y más débiles de los patrones XRD para CoMoO 4 Se observaron muestras, lo que indica la cristalización más débil en las muestras. Como se informa en las Refs. [8, 34], la cristalinidad más débil juega un papel crítico para mejorar el comportamiento electroquímico en aplicaciones de supercondensadores.
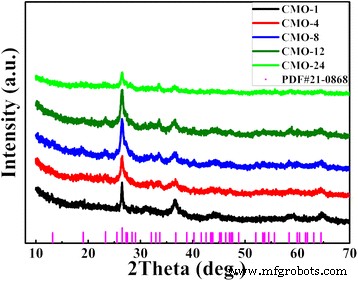
Patrones XRD de cinco muestras
Las morfologías superficiales de CoMoO 4 las muestras se caracterizaron por SEM y TEM. Como se muestra en la Fig. 2, se observaron estructuras de microesferas para todas las muestras, y la microesfera estaba formada por nanoflakes. Con el aumento del tiempo hidrotermal, el grosor de las nanohojas aumenta primero y luego disminuye, y las nanoflakes más gruesas se obtuvieron en la muestra con el tiempo hidrotermal de 12 h. Las figuras 3a, b muestran las imágenes de mapeo de elementos de espectroscopía de dispersión de energía (EDS) y el espectro de EDS de CMO-12. Según las imágenes de mapeo de elementos, los elementos Co, Mo y O se distribuyen uniformemente en la microesfera. La relación molar de elementos de Co, Mo y O es aproximadamente 1:1:4, que corresponde a la composición de CoMoO 4 . La Figura 3c, d muestra las imágenes TEM del CMO-12. Como se muestra en el recuadro de la Fig. 3c, los patrones de difracción de electrones de área seleccionada (SAED) revelan la naturaleza monocristalina del CoMoO 4 . Los puntos de difracción claros podrían asignarse a los planos cristalinos (\ (\ overline {2} \) 22), (024), (\ (\ overline {1} \) 31) y (002) del CoMoO 4 . La figura 3d es la imagen HRTEM; muestra el espaciado de celosía de 0.34 y 0.27 nm, que podría estar relacionado con los planos (002) y (\ (\ overline {1} \) 31) de CoMoO 4 , respectivamente.
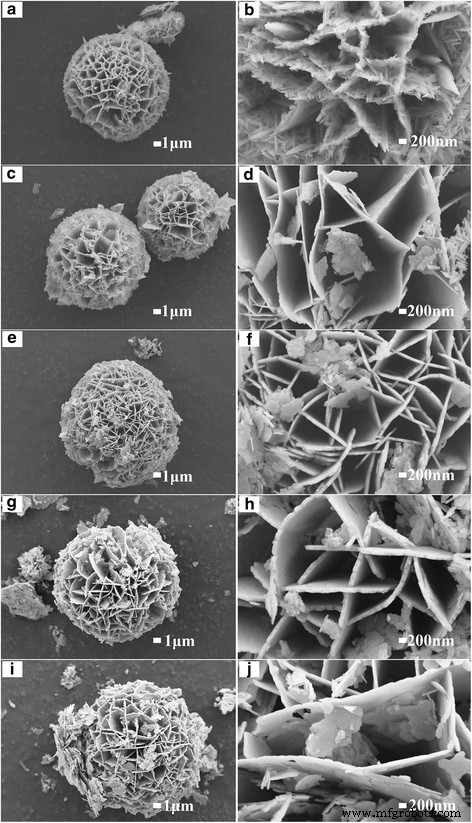
Las imágenes SEM de baja y alta ampliación de las muestras. un , b CMO-1. c , d CMO-4. e , f CMO-8. g , h CMO-12. yo , j CMO-24
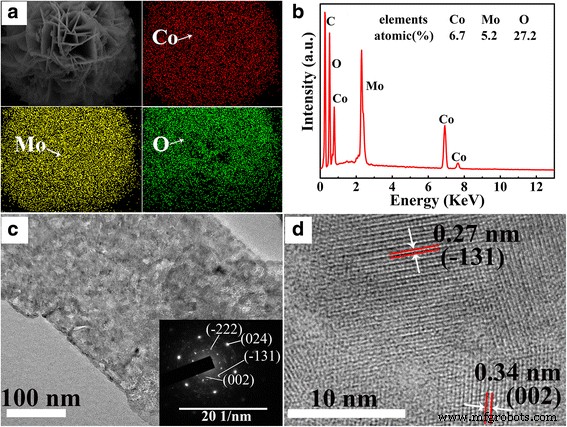
un Imagen de mapeo de elementos de espectroscopía de dispersión de energía (EDS) y distribución de Co, Mo y O. b El espectro y el recuadro de EDS son el porcentaje molar de los elementos Co, Mo y O. c El TEM de gran aumento y el recuadro son el patrón de difracción de electrones del área seleccionada. d La imagen HRTEM de la muestra CMO-12
La Figura 4 muestra las distribuciones del tamaño de los poros y N 2 isotermas de adsorción-desorción de CoMoO 4 muestras. Según el N 2 isotermas de adsorción-desorción de muestras, todas las isotermas muestran la característica del tipo IV con H 3 -tipo bucles de histéresis. Las áreas de superficie específicas BET de CMO-1, CMO-4, CMO-8, CMO-12 y CMO-24 se calcularon en 18,4, 29,2, 42,8, 74,1 y 26,2 m 2 g −1 , respectivamente. La muestra CMO-12 muestra el área de superficie BET más alta, y el área de superficie BET alta podría aumentar el área de contacto del electrodo / electrolito y proporcionar sitios más activos para el transporte eficiente de electrones e iones en el sistema de electrodos [35]. Como se muestra en la Fig. 4, los picos agudos en las distribuciones del tamaño de los poros de las muestras se encuentran a 145,9, 74,1, 22,6, 27,9 y 75,3 nm, respectivamente. Indica que hay mesoporos en CMO-8 y CMO-24. Sin embargo, se detectan algunos macroporos en las muestras CMO-1, CMO-4 y CMO-24. Cuando se utilizan materiales en supercondensadores, las estructuras de mesoporos de los materiales también podrían aumentar el área de contacto entre el electrodo y el electrolito; hay sitios activos más suficientes para el transporte eficiente de electrones e iones en el sistema de electrodos [36,37,38]. Por lo tanto, CMO-12 con mayor área de superficie BET y estructura de mesoporo podría mostrar mejores propiedades electroquímicas que otras muestras.
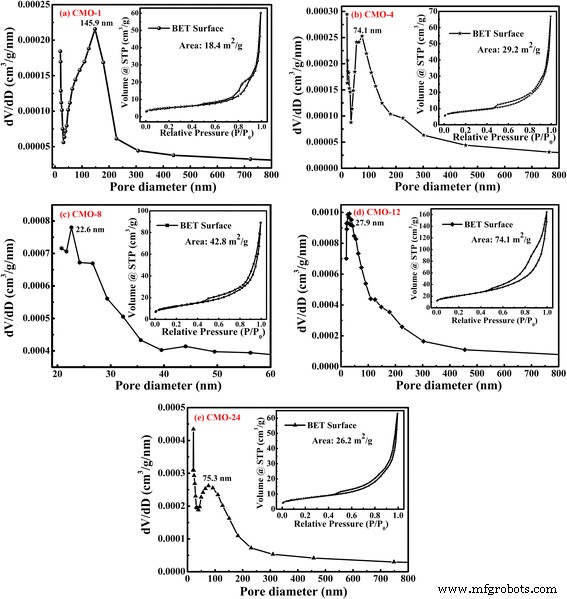
Distribuciones de tamaño de poro y N 2 isotermas de adsorción-desorción de muestras
Caracterización electroquímica
Curvas CV de CoMoO 4 muestras a diferentes velocidades de escaneo de 5 a 100 mV s −1 en electrolito de KOH 2 M con rango de potencial de - 0.2 V a + 0.6 V (vs. Hg / HgO) se muestran en la Fig. 5a –e. Los picos típicos de reacción farádica se pueden ver claramente en todas las curvas, lo que indica que el CoMoO 4 los electrodos son electrodos pseudocondensadores. El pico redox observado se debe a la cinética de transferencia de carga de Co 2+ y Co 3+ asociado con el OH - en electrolito [8, 26]. La reacción redox de Co 2+ / Co 3+ se enumera de la siguiente manera [39, 40]:
$$ {\ mathrm {CoMoO}} _ 4 + {\ mathrm {OH}} ^ {-} \ to \ mathrm {CoOOH} + {\ mathrm {MoO}} _ 3 + {\ mathrm {e}} ^ {-} $$ (1) $$ \ mathrm {CoOOH} + {\ mathrm {OH}} ^ {-} \ kern0.28em \ iff \ kern0.28em {\ mathrm {CoO}} _ 2 + {\ mathrm {H}} _ 2 \ mathrm {O} + {\ mathrm {e}} ^ {-} $$ (2) $$ \ mathrm {CoOOH} + {\ mathrm {H}} _ 2 \ mathrm {O} + {\ mathrm {e}} ^ {-} \ kern0.28em \ iff \ kern0.28em \ mathrm {Co} {\ left (\ mathrm {OH} \ right)} _ 2 + {\ mathrm {OH}} ^ {-} $$ (3)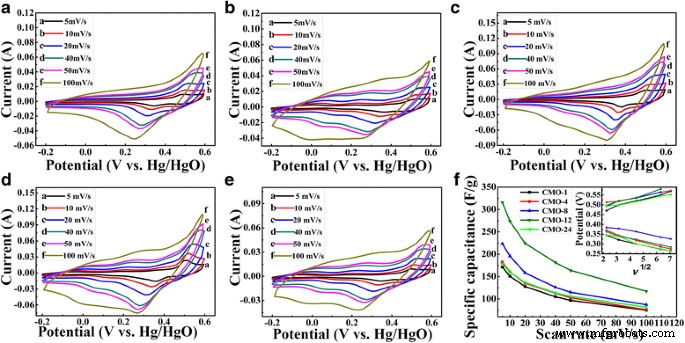
Las curvas CV bajo diferentes velocidades de escaneo de 5, 10, 20, 40, 50 y 100 mV s −1 de muestras a CMO-1, b CMO-4, c CMO-8, d CMO-12 y e CMO-24 en la ventana potencial osciló entre - 0,2 y + 0,6 V. f La capacitancia específica de muestras bajo diferentes velocidades de escaneo de 5 a 100 mV s −1 . El recuadro en f son las gráficas de la corriente máxima anódica y catódica contra la raíz cuadrada de la velocidad de escaneo
Como se muestra en la Fig. 5a-e, con el aumento de las velocidades de exploración, los picos redox cambian a potenciales más altos y más bajos, respectivamente. La diferencia de potencial entre los picos de oxidación y los picos de reducción también aumentó con el aumento de la velocidad de exploración. Indica que el grado irreversible y la reacción cuasi-reversible aumentan con el aumento de la velocidad de exploración [36, 41]. El cambio está relacionado principalmente con la resistencia interna del electrodo y la polarización causada por la alta frecuencia de exploración [36, 42]. Se observó una relación casi lineal entre los potenciales de los picos redox y la raíz cuadrada de la velocidad de exploración, que se puede ver en el recuadro de la Fig. 5f. La relación aproximadamente lineal también indica que la cinética de reacción durante el proceso redox probablemente está controlada por el proceso de difusión de iones [6].
Según las curvas CV, la capacitancia específica de las muestras se puede calcular mediante la siguiente ecuación:
$$ {C} _ {\ mathrm {sp}} =\ frac {\ int_ {V_1} ^ {V_2} IdV} {m \ times v \ times \ Delta V}, $$ (4)donde C sp (F g −1 ) es la capacitancia específica, V 1 y V 2 son el voltaje inicial y final, ∫ IdV es el área integral de las curvas CV, m (g) es la masa de materiales activos que se cargan en el electrodo, v (mV s −1 ) es la frecuencia de exploración potencial y ∆ V (V) es la ventana de potencial de barrido. Las capacitancias específicas de las muestras se calcularon con base en las curvas CV usando la Ec. (4), que se muestran en la Fig. 5f. Las capacitancias específicas de todas las muestras disminuyen a medida que aumentan las velocidades de exploración. Más OH - puede llegar al sitio activo en condiciones más favorables a una tasa de exploración potencial baja [31, 43]. Además, una tasa de exploración más alta conduce al agotamiento o la saturación de los protones en el electrolito dentro del electrodo durante el proceso redox, y solo la superficie exterior podría utilizarse para el almacenamiento de carga [41, 43, 44]. Cuando el tiempo de síntesis hidrotermal aumenta de 1 a 12 h, las capacitancias específicas de las muestras muestran un aumento obvio de 171,3 a 315,7 F g −1 a una velocidad de exploración de 5 mV s −1 . Sin embargo, la capacitancia específica disminuye de 315,7 a 178,7 F g −1 cuando el tiempo hidrotermal aumenta de 12 a 24 h. Por lo tanto, la muestra CMO-12 (es decir, el tiempo hidrotermal es de 12 h) muestra una excelente capacitancia específica. La capacitancia específica de 315,7 F g −1 a 5 mV s −1 es mejor que el de 286 F g −1 para CoMoO 4 nanovarillas [11] y 95.0 F g −1 para CoMoO puro 4 [45] y comparable con 322,5 F g - 1 para RGO / CoMoO 4 [45].
Esta propiedad electroquímica mejorada puede confirmarse mediante las siguientes pruebas de carga-descarga galvanostática. Las pruebas GCD de las muestras se realizaron a diferentes densidades de corriente de 1, 1,5, 2, 3, 5 y 8 A g −1 en electrolito de KOH 2 M, y los resultados se muestran en la figura 6a-e. Las curvas GCD no lineales podrían atribuirse a la reacción redox [46], y esto es coherente con las curvas CV. Como se muestra en estas curvas, el tiempo de descarga de CMO-12 es significativamente más largo que el de otras muestras, lo que indica una capacitancia específica mucho más alta en CMO-12. Esto podría confirmarse aún más mediante los siguientes resultados calculados. Las capacidades específicas de CoMoO 4 El electrodo se puede calcular utilizando la siguiente ecuación:
$$ C =\ frac {I \ times \ Delta t} {m \ times \ Delta V}, $$ (5)donde C (F g −1 ) es la capacitancia específica, I (A) es la corriente de descarga, ∆ t (s) se refiere a tiempos de descarga, m (g) es la masa de material activo que se carga en la superficie del electrodo, y ∆ V (V) es la ventana de potencial aplicada [6, 8, 26]. La Figura 6f muestra la capacitancia específica calculada de muestras a diferentes densidades de corriente. Con el aumento de la densidad de corriente, se reducen las capacidades específicas de las muestras. Esto se puede atribuir al contacto efectivo entre los iones y los sitios electroactivos del electrodo. A alta densidad de corriente, solo hay una parte del total de sitios de reacción disponibles porque los iones de electrolito sufren de baja difusión, lo que conduce a una reacción de inserción incompleta y una baja capacitancia específica [19, 45]. De la Fig. 6f, podemos ver que el CMO-12 tiene la capacitancia específica más alta, que son 384, 337, 307, 269, 229 y 172 F g −1 a la densidad de corriente de 1, 1.5, 2, 3, 5 y 8 A g −1 , respectivamente. La capacitancia específica de CMO-12 muestra una buena capacidad de velocidad. Además, la capacitancia específica de CMO-12 también es más alta que la informada en algunas publicaciones anteriores. Según lo informado por Tian et al. [39], la capacitancia específica del Co-Mo-O en forma de aguja es 302 F g −1 a una densidad de corriente de 1 A g −1 . La capacitancia específica máxima de CoMoO 4 era de aproximadamente 133 F g −1 a 1 mA cm −2 en el artículo de Veerasubramani [26]. En Ref. [29], la capacitancia específica de α-CoMoO 4 nanoflakes / CFC usado como supercondensador simétrico es solo 8.3 F g −1 a una densidad de corriente de 1 A g −1 . Además, una alta tasa de descarga o una alta densidad de corriente es muy importante para un dispositivo supercondensador real, que implica un proceso de carga-descarga rápido [43]. A una alta densidad de corriente de 8 A g −1 , las capacitancias específicas para las cinco muestras son 97, 109, 148, 172 y 98 F g −1 , respectivamente.
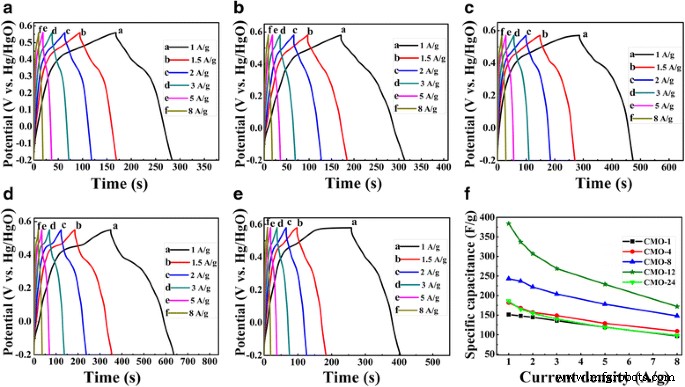
Las curvas de GCD bajo diferentes densidades de corriente de 1, 1.5, 2, 3, 5 y 8 A g −1 de muestras a CMO-1, b CMO-4, c CMO-8, d CMO-12 y e CMO-24 en la ventana potencial osciló entre - 0,2 y + 0,58 V. f La capacitancia específica de las muestras calculada por los resultados de GCD
Las estabilidades del CoMoO 4 Los electrodos se detectaron en un electrolito de KOH 2 M a una densidad de corriente de 8 A g −1 para 1000 ciclos, que se muestran en la Fig. 7. Después de 1000 ciclos, las cinco muestras muestran la retención de 102,9, 87,8, 101,5, 94,2 y 100,5%, respectivamente. Para el aumento de capacitancia específica durante el proceso de carga-descarga cíclica, podría atribuirse a la activación del CoMoO 4 superficie con el tiempo [6]. Hace que la superficie de CoMoO 4 entrar en contacto completo con el electrolito, lo que conduce a la mejora de la propiedad electroquímica [6, 47, 48]. La Figura 7b muestra la eficiencia culómbica de CoMoO 4 muestras durante los 1000 ciclos de carga-descarga, que también muestra una alta capacitancia específica. Los resultados indican que todas estas muestras tienen una excelente estabilidad de ciclo largo. La capacitancia altamente específica, la gran capacidad de velocidad y la fina estabilidad de ciclo largo indican que la muestra CMO-12 tiene una excelente propiedad electroquímica.
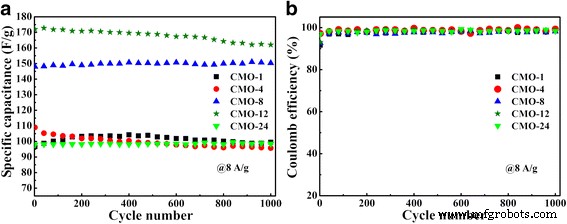
un Rendimiento cíclico de los electrodos a 8 A g −1 . b La correspondiente eficiencia culómbica de las muestras durante la prueba cíclica
Para evaluar más a fondo la propiedad electroquímica de CoMoO 4 electrodo, el EIS de cinco muestras se registra en electrolito KOH 2 M. La Figura 8 son los gráficos de Nyquist de cinco muestras. Los gráficos de Nyquist representan la respuesta de frecuencia del sistema electrodo / electrolito [26, 49]. Los espectros EIS pueden ajustarse mediante el diagrama de circuito equivalente, que se insertó en la Fig. 8. La gráfica de Nyquist se compone de un semicírculo a alta frecuencia y una línea recta a baja frecuencia. El diámetro del semicírculo a alta frecuencia representa la resistencia de transferencia de carga de la interfaz de Faraday ( R ct ), y la pendiente de la línea recta a baja frecuencia es representativa de la resistencia típica de Warburg (W 0 ) [41], respectivamente. CPE1 es un elemento de fase constante, que representa la capacitancia de doble capa [43]. Además, la resistencia en serie R s es la resistencia interna, que podría obtenerse de la intersección de las parcelas en el eje real [11]. La R medida s los valores son 2,83, 2,41, 1,51, 1,22 y 2,26 Ω para las cinco muestras, respectivamente. Y la R ajustada ct Los valores de las cinco muestras son 1,69, 1,48, 0,72, 0,23 y 1,28 Ω. Los resultados de la EIS muestran que la muestra CMO-12 tiene valores más bajos de R s y R ct que las otras cuatro muestras. Esto indica que la muestra de CMO-12 tiene conductividades electrónicas e iónicas más altas que las otras muestras [35, 50, 51]. Además, CMO-12 con estructura de mesoporos tiene un área de superficie BET más alta que las otras muestras. La alta superficie BET y la buena conductividad son beneficiosas para la reacción redox en el sistema de electrodo / electrolito.
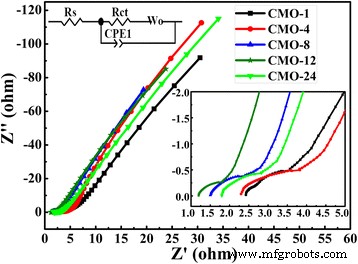
Espectros EIS de muestras obtenidas en la frecuencia que va desde 0,01 Hz a 100 KHz. El recuadro es la amplificación local de los espectros EIS y el diagrama de circuito equivalente
Conclusiones
En resumen, CoMoO 4 Las microesferas se han sintetizado con éxito mediante un proceso de crecimiento hidrotermal junto con un tratamiento de calcinaciones. Los tiempos de síntesis hidrotermal son 1, 4, 8, 12 y 24 h, respectivamente. Los patrones XRD indican que el CoMoO 4 monofásico se obtuvo la estructura. Las imágenes SEM muestran que las microesferas estaban compuestas por nanoflakes. El CMO-12, que se preparó con el tiempo hidrotermal de 12 h, ha demostrado un excelente rendimiento de supercondensador. Según las pruebas de GCD, las capacitancias específicas de CMO-12 son 384, 337, 307, 269, 229 y 172 F g −1 a densidades de corriente de 1, 1,5, 2, 3, 5 y 8 A g −1 , respectivamente, mientras que acaba de llegar a 151, 182, 243 o 186 F g −1 a la densidad de corriente 1 A g −1 para otras muestras con diferentes tiempos hidrotermales. Las capacidades de retención de la muestra CMO-12 después de 1000 ciclos de carga y descarga a una densidad de corriente de 8 A g −1 muestran la fina estabilidad de ciclo largo. Este excelente comportamiento capacitivo podría atribuirse a la estructura de la microesfera y al área de superficie BET alta, y la buena conductividad en el electrodo CMO-12 también es útil para mejorar el comportamiento capacitivo. La alta capacitancia específica, la buena capacidad de velocidad y la excelente estabilidad cíclica promueven la aplicación práctica de CoMoO 4 materiales en supercondensadores.
Abreviaturas
- APUESTA:
-
Brunauer-Emmett-Teller
- CV:
-
Voltamperometría cíclica
- EDS:
-
Espectroscopía de dispersión de energía
- EIS:
-
Espectroscopia de impedancia electroquímica
- FE-SEM:
-
Microscopía electrónica de barrido por emisión de campo
- GCD:
-
Carga-descarga galvanostática
- PTFE:
-
Politetrafluoroetileno
- SAED:
-
Difracción de electrones de área seleccionada
- SCE:
-
Electrodo de calomelanos saturado
- TEM:
-
Microscopía electrónica de transmisión
- XRD:
-
Difracción de rayos X
Nanomateriales
- Compuestos de grafeno y polímeros para aplicaciones de supercapacitores:una revisión
- Nanoesferas de carbono monodispersas con estructura porosa jerárquica como material de electrodo para supercondensador
- Síntesis de material de ánodo de Li4Ti5O12 esférico recubierto de plata mediante un método hidrotermal asistido por sol-gel
- Microarreglos mesoporosos de VO2 bidimensionales para supercondensadores de alto rendimiento
- Silicio poroso pasivado con láminas de grafeno de pocas capas hacia un excelente electrodo supercondensador electroquímico de doble capa
- Microesferas de silicio mesoporosas producidas a partir de la reducción magnetotérmica in situ de óxido de silicio para material anódico de alto rendimiento en baterías de iones de sodio
- Electrodo de grafeno de transferencia secundaria para FOLED estable
- Guía de selección de materiales para mecanizado CNC
- Electrodo de estaño amplifica supercondensadores
- El material de electrodo adecuado para su aplicación de soldadura por resistencia
- Las propiedades de cobre y tungsteno lo convierten en un material de electrodo EDM ideal



