Síntesis de material de ánodo de Li4Ti5O12 esférico recubierto de plata mediante un método hidrotermal asistido por sol-gel
Resumen
ᅟ
Li 4 esférico recubierto de Ag Ti 5 O 12 El compuesto se sintetizó con éxito mediante un método hidrotermal asistido por sol-gel utilizando una mezcla de etilenglicol y nitrato de plata como precursor, y se investigó exhaustivamente la influencia del contenido del recubrimiento de Ag en las propiedades electroquímicas de su compuesto. El análisis de difracción de rayos X (XRD) indicó que el recubrimiento de Ag no cambia la estructura de la espinela de Li 4 Ti 5 O 12 . Los análisis de espectroscopía de impedancia electroquímica (EIS) demostraron que la excelente conductividad eléctrica del Li 4 Ti 5 O 12 / Ag resultó de la presencia de la capa de recubrimiento de plata altamente conductora. Además, la capa de plata nanogruesa, que se recubre uniformemente sobre las partículas, mejoró significativamente la capacidad de velocidad de este material. Como consecuencia, el Li 4 esférico de tamaño micrométrico recubierto de plata Ti 5 O 12 exhibió un excelente rendimiento electroquímico. Por tanto, con un contenido de plata apropiado del 5% en peso, el Li 4 Ti 5 O 12 / Ag entregó la capacidad más alta de 186,34 mAh g −1 a 0,5 ° C, que es más alta que la de otras muestras, y mantuvo el 92,69% de su capacidad inicial a 5 ° C después de 100 ciclos. Incluso a 10 ° C después de 100 ciclos, todavía tenía una capacidad de retención del 89,17%, lo que demuestra una estabilidad cíclica notable.
Registro de prueba
ISRCTN NARL-D-17-00568
Aspectos destacados
- 1.
Li 4 esférico Ti 5 O 12 / Los compuestos de Ag se sintetizaron mediante un método hidrotermal asistido por sol-gel utilizando etilenglicol y una mezcla de nitrato de plata como precursor de la capa de recubrimiento, lo que mejoró significativamente la conductividad electrónica y el rendimiento electroquímico de Li 4 Ti 5 O 12 .
- 2.
La morfología esférica podría inducir una gran densidad de grifo y, en consecuencia, mejorar la densidad de energía volumétrica.
Antecedentes
Durante la última década, las baterías recargables de iones de litio (LIB) han demostrado muchas ventajas. Son de peso ligero; tener un tamaño pequeño, alto voltaje y alta densidad de energía; y han suscitado un gran interés como dispositivo de almacenamiento de energía electroquímica para reducir las emisiones de escape y el ahorro de combustible [1, 2]. Sin embargo, el precio de los precursores de litio, las cuestiones de seguridad y de vida y la baja densidad de potencia son obstáculos para la aplicación de los BIB para el almacenamiento de energía a gran escala en el futuro [3]. Por lo tanto, para desarrollar materiales sustitutos para satisfacer las demandas de seguridad del almacenamiento a gran escala, se han realizado grandes esfuerzos [4].
Titanato de litio en cubos de espinela (Li 4 Ti 5 O 12 ), los materiales del ánodo de las baterías de iones de litio, se han convertido en un material prometedor debido a su característica estructural de deformación cero durante el proceso de intercalación y desintercalación de Li 4 Ti 5 O 12 [5,6,7,8,9]. Este material tiene un voltaje de inserción y extracción de litio de plataforma de ~ 1,55 V (en comparación con Li / Li + ), evitando la formación de películas de interfaz de electrolitos sólidos (SEI) que consumen litio, que deberían ser beneficiosas para mejorar la seguridad y el buen ciclo de los LIB. Por lo tanto, Li 4 Ti 5 O 12 se ha convertido en uno de los materiales potenciales en aplicaciones comerciales e investigación científica. Li 4 Ti 5 O 12 se ha preparado mediante varios métodos, por ejemplo, método de estado sólido, deposición no electrolítica, microondas y sol-gel. Con respecto al método de estado sólido, algunos estudios han demostrado que tiene una ruta de síntesis simple y un bajo costo de síntesis debido a la distancia más corta para Li + difusión y transferencia de electrones, Li 4 Ti 5 O 12 exhibe una excelente capacidad de velocidad, pero la reacción en estado sólido no puede proporcionar una morfología uniforme con un tamaño estrecho. Sin embargo, el proceso de deposición sin electricidad tiene una ruta de síntesis compleja. Para la síntesis sol-gel de Li 4 Ti 5 O 12 , varios investigadores han informado que puede producir productos con una distribución uniformemente homogénea y partículas estrechas con un buen control estequiométrico.
A pesar de estas muchas ventajas, los principales inconvenientes de Li 4 Ti 5 O 12 son su baja conductividad electrónica e iónica y su lento coeficiente de difusión de iones de litio, lo que da como resultado una capacidad de baja velocidad. Se han adoptado numerosas estrategias, incluida la reducción del tamaño de los cristalitos [10], el dopaje con iones metálicos de alta valencia [11,12,13] y el revestimiento con fases conductoras [14,15,16,17] para mejorar el transporte de descarga / carga. propiedades de los electrodos. Además, otra forma de mejorar la conductividad electrónica es sintetizar Li 4 nanoestructurado Ti 5 O 12 . Las nanoestructuras proporcionan un área de contacto electrodo / electrolito más grande para aumentar la cinética de intercalación y reducir las rutas de difusión para acelerar Li + y transporte de electrones [18]. Entre estos enfoques, la forma más eficaz de mejorar las propiedades electroquímicas de Li 4 Ti 5 O 12 es la modificación de la superficie conductora. Aslihan y col. [2] sintetizado Li 4 Ti 5 O 12 a través del método sol-gel, y luego el Li 4 sintetizado Ti 5 O 12 se revistió la superficie con plata mediante deposición no electrolítica. Los resultados mostraron que el recubrimiento de plata (recubrimiento de Ag) proporciona una matriz altamente conductora para Li + inserción, mejorando la conductividad electrónica. Zhu y col. [19] Li 4 nanométrico recubierto de carbono preparado Ti 5 O 12 microesferas nanoporosas con una capacidad de velocidad notable a través de un proceso de prerrevestimiento de carbono en combinación con un método de secado por aspersión, e indicaron que las partículas esféricas del tamaño de un micrón inducen una gran densidad de grifo, lo que resulta en una mejora de la densidad de energía volumétrica. Sin embargo, cómo sintetizar Li 4 de tamaño micrométrico recubierto de Ag Ti 5 O 12 No se ha informado de partículas esféricas a través de un método hidrotermal asistido por sol-gel.
En este documento, informamos sobre un método hidrotermal asistido por sol-gel para sintetizar el Li 4 esférico de tamaño micrométrico Ti 5 O 12 / Ag compuesto usando etilenglicol y una mezcla de nitrato de plata como precursor, y el contenido del revestimiento de Ag se ajustó controlando la cantidad de elemento plata en el precursor. Las propiedades electroquímicas del Li 4 Ti 5 O 12 / Ag con morfología esférica se investigaron en detalle.
Experimental
Síntesis de Pristine Li 4 Ti 5 O 12 y modificación de su superficie con Ag
Síntesis del precursor esférico mediante el método Sol-Gel
El precursor esférico de glicolato de titanio (TG) se sintetizó mediante el método sol-gel. Primero, se agregaron lentamente 2 mL de titanato de tetrabutilo a la solución, que contenía AgNO 3 (en una cantidad apropiada para que sea soluble en 50 mL de glicol), bajo vigorosa agitación para formar la solución precursora. En segundo lugar, se añadió la solución precursora a 150 ml de mezcla de acetona que contenía 0,1 ml de Tween 80 y se continuó agitando durante 1 ha temperatura ambiente para formar precipitados. Luego, los precipitados se envejecieron durante 8 h, se separaron por filtración y se lavaron dos veces con alcohol anhidro. Finalmente, los polvos precursores se obtuvieron mediante tratamiento térmico a 80 ° C durante 6 h en un horno seguido de molienda.
Síntesis de Li esférico 4 Ti 5 O 12 / Ag
El esférico Li 4 Ti 5 O 12 / Ag se preparó mediante el método hidrotermal. Primero, LiOH · H 2 O y el precursor en una proporción molar de 3.9:1 se mezclaron homogéneamente agitando con 40 mL de alcohol como medio durante 1 h para formar una mezcla, que luego se calentó a 180 ° C durante 12 h en recipientes de teflón sellados hasta que precipitó. se obtuvieron. En segundo lugar, los precipitados se recogieron mediante centrifugación (5000 rpm, 5 min) y se lavaron adicionalmente con etanol anhidro varias veces. Luego, se secaron en estufa a 80 ° C durante 2 h. Finalmente, los precipitados se calentaron en un horno de mufla a 700 ° C durante 2 h (velocidad de calentamiento de 5 ° C · min −1 ) en el aire después de triturarlos y luego enfriarlos naturalmente a temperatura ambiente para obtener Li 4 esférico Ti 5 O 12 / Ag en polvo.
Caracterización del material
La estructura del Li 4 Ti 5 O 12 Las muestras se identificaron mediante difracción de rayos X (XRD, Rigaku D / max-PC2200) utilizando una fuente de radiación Cu Kα (λ =0.15405 nm) con una velocidad de escaneo de 4 ° min −1 de 10 ° a 80 ° y operado a 40 KV y 20 mA. La morfología y el tamaño de partícula de los materiales se exploraron mediante SEM (microscopía electrónica de barrido, Supra 55 Zeiss) y TEM (microscopía electrónica de transmisión, JEOL-2100).
Mediciones electroquímicas
Las prestaciones electroquímicas de los productos se probaron utilizando una celda tipo moneda CR2025. Los electrodos de trabajo se prepararon mezclando 80% en peso de Li 4 Ti 5 O 12 / Ag materiales activos, 10% en peso de Super-P conductor y 10% en peso de aglutinante de fluoruro de polivinilideno (PVDF) en disolvente N-metil-2-pirrolidona (NMP) para formar una suspensión uniforme. Luego, la suspensión se vertió sobre una hoja de aluminio y se secó al vacío a 80ºC durante 12 h para eliminar el disolvente residual. Luego, la lámina se presionó y se cortó en discos. Se utilizó una membrana microporosa de polipropileno Celgard 2400 y una lámina de litio como separador y electrodo negativo, respectivamente. La solución de electrolitos era LiPF 6 1 M en carbonato de etileno (EC), carbonato de dimetilo (DMC) y carbonato de etileno metil (EMC) en una relación volumétrica de 1:1:1. Las células se ensamblaron en una caja de guantes llena de argón, donde los niveles de humedad y oxígeno se mantuvieron por debajo de 1 ppm. Las pruebas electroquímicas de los productos se evaluaron utilizando un sistema de prueba LAND CT2001A (Wuhan, China). Las pruebas de voltamperometría cíclica (CV) se registraron en una estación de trabajo electroquímica CHI600A a 0,1 mV s −1 velocidad de escaneo de 1.0 a 2.5 V (en comparación con Li / Li + ). Las mediciones de EIS se realizaron en el rango de frecuencia de 100 KHz a 10 mHz con una perturbación de 5 mV.
Resultados y discusión
Propiedades estructurales y morfológicas
El efecto de la cantidad de aditivo Ag en el Li 4 Ti 5 O 12 / Se investigaron los polvos de agricultura. Los patrones XRD del Li 4 esférico recubierto de Ag Ti 5 O 12 Los compuestos se muestran en la Fig. 1. Se puede ver fácilmente que los picos de difracción principales de todas las muestras aparecen en 18.4 °, 35.54 °, 43.2 °, 57.2 °, 62.8 ° y 66.1 ° y están indexados como (111), (311), (400), (333), (440) y (531), respectivamente. Que los picos están de acuerdo con el Li 4 Ti 5 O 12 patrón de difracción estándar [20], excepto los patrones característicos del metal Ag (2θ =38,1 °, 44,3 °, 64,4 °). No se detectaron picos de difracción de impurezas en ninguna de las muestras. Además, la intensidad máxima de la plata aumentó de manera correspondiente a medida que aumentaba la cantidad de Ag.
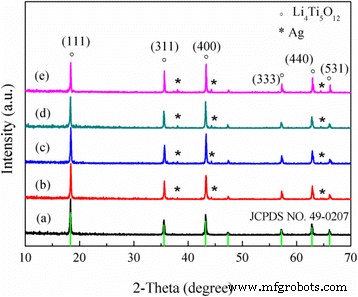
Patrones XRD del Li 4 Ti 5 O 12 / Ag. ( a ) 0% en peso, ( b ) 1% en peso, ( c ) 3% en peso, ( d ) 5% en peso y ( e ) 7% en peso
Parámetros de celosía del Li 4 Ti 5 O 12 / Las muestras de Ag con diferentes recubrimientos de Ag se proporcionan en la Tabla 1. No se observaron cambios significativos con el aumento del contenido de Ag. Por lo tanto, se sugirió que la plata se recubre principalmente en forma de Ag elemental en la superficie de Li 4 Ti 5 O 12 partículas pero que no penetran en la red de espinela Li 4 Ti 5 O 12 . Porque el radio iónico de Ag + (0,126 nm) es sustancialmente más grande que el del Ti 4+ (0.068 nm), el Li 4 sintetizado Ti 5 O 12 / La muestra de Ag era solo un compuesto del metal Ag y el Li 4 Ti 5 O 12 fase.
La Figura 2 muestra las imágenes SEM del precursor preparado (a 1 -e 1 ) y Li 4 Ti 5 O 12 / Ag (a 2 -e 2 ). Como se muestra en la Fig. 2, todas las muestras exhiben una estructura esférica uniforme con una distribución de tamaño estrecha de 5 a 10 μm, lo que es beneficioso para el contacto entre los materiales activos y el electrodo. A partir de las imágenes SEM, el precursor esférico, las partículas de glicolato de titanio (TG), muestra una línea suave, mientras que el Li 4 Ti 5 O 12 / Las partículas de Ag presentan una línea rugosa. Además, una buena dispersión podría agrandar el área de contacto electrodo-electrolito y acelerar significativamente el transporte de Li + y electrón. Sin embargo, la superficie del Li 4 Ti 5 O 12 / Las muestras de Ag no son obviamente más suaves que las del precursor preparado y el glicolato de titanio, y existen hasta cierto punto como una aglomeración. Además, los tamaños de partículas de diferentes Li 4 Ti 5 O 12 / Los compuestos de Ag son mucho más grandes que los de Li 4 sin Ag Ti 5 O 12 ; sin embargo, el fenómeno de la aglomeración se vuelve más obvio con un aumento en el contenido de plata.

Imágenes SEM del precursor y el Li 4 Ti 5 O 12 / Ag. ( a ) 0% en peso, ( b ) 1% en peso, ( c ) 3% en peso, ( d ) 5% en peso, ( e ) 7% en peso
La distribución de plata en el interior de las partículas de tamaño micrométrico se investigó más a fondo, y los análisis TEM y HRTEM se proporcionaron en la Fig. 3. Las imágenes TEM (Fig. 3a) muestran que el tamaño de micras recubierto de Ag al 5% en peso -esférico Li 4 Ti 5 O 12 las partículas están uniformemente recubiertas por una capa de plata con un espesor de 3 ~ 4 nm, lo que indica que la capa de plata construye una red conductora en la superficie de todo el material, lo que facilita el transporte de iones de litio y electrones. Como se muestra en la Fig. 3b, la superficie del Li 4 de tamaño micrométrico Ti 5 O 12 / Las partículas de Ag no son suaves y el d -espaciado del 5% en peso de Li 4 recubierto de Ag Ti 5 O 12 partículas es de 0,484 nm, que coincide bien con la del plano LTO (111). Esto sugiere que no se generó una nueva fase en la superficie de las partículas LTO, pero había una fina capa de recubrimiento sobre las partículas.

( a ) TEM y ( b ) Imágenes HRTEM del 5% en peso de Li 4 recubierto de plata Ti 5 O 12 , en el que la "línea" indica la capa de plata recubierta
Propiedades electroquímicas
La Figura 4 muestra las primeras curvas de carga-descarga del Li 4 esférico de tamaño micrón Ti 5 O 12 / Electrodos de Ag recubiertos con diferentes contenidos de Ag a diferentes velocidades. Como se puede ver en la Fig.4, todos los perfiles exhiben una meseta de voltaje extremadamente plana de 1,55 V (en comparación con Li / Li + ), lo que indica una transición de dos fases entre Li 4 Ti 5 O 12 y Li 7 Ti 5 O 12 para inserción de litio [21]. La plataforma de voltaje de Li 4 Ti 5 O 12 / Ag composites es más largo que el de Li 4 sin Ag Ti 5 O 12 . Con un contenido creciente de Ag, para una plataforma de descarga más larga de Li 4 Ti 5 O 12 / Ag, la capacidad de mantener la plataforma es más fuerte, lo que sugiere que una buena conductividad electrónica puede reducir efectivamente la polarización del material durante el proceso de reacción del electrodo y mejorar la utilización del material.
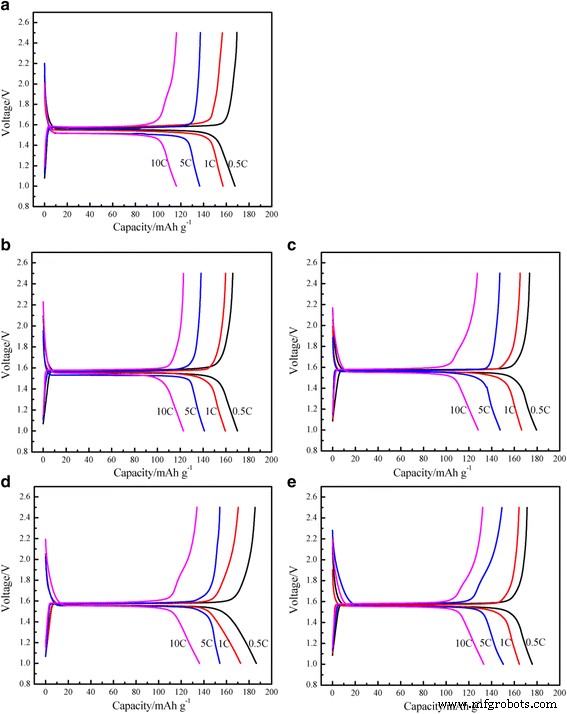
Las curvas de carga-descarga iniciales con varias densidades de corriente del Li 4 Ti 5 O 12 / Ag. ( a ) 0% en peso, ( b ) 1% en peso, ( c ) 3% en peso, ( d ) 5% en peso, ( e ) 7% en peso
Como se muestra en la Fig.4, Li 4 sin Ag Ti 5 O 12 entregó una capacidad inicial específica de descarga de 167,62 mAh g −1 a una velocidad de 0.5C, mientras que la capacidad de entrega del Li 4 esférico de tamaño micrón recubierto de Ag Ti 5 O 12 los compuestos aumentaron al aumentar la cantidad de plata:170,10, 179,54 y 186,34 mAh g −1 para 1, 3 y 5% en peso, respectivamente. Pero 7% en peso de Li 4 recubierto de Ag Ti 5 O 12 exhibió un comportamiento algo diferente. La capacidad específica de descarga entregada disminuyó al aumentar la cantidad de plata:175,86 mAh g −1 al 7% en peso. El 5% en peso de Li 4 recubierto de Ag Ti 5 O 12 obtuvo la capacidad de descarga inicial más alta y las capacidades específicas de descarga inicial alcanzaron 186,34, 172,47, 154,12 y 136,06 mAh g −1 a las corrientes específicas de 0.5, 1, 5 y 10C, respectivamente. Debido a la mala conductividad electrónica y la lentitud de Li + difusión, el material exhibe una gran polarización a altas tasas de carga / descarga. El aditivo Ag altamente conductor puede mejorar significativamente la reacción de intercalación de la superficie y reducir la polarización [20, 22]. Incluso el contenido de Ag más alto (7% en peso) puede proporcionar la meseta de voltaje más larga, y la plata metálica en sí misma no se puede intercalar completamente en el litio. En cambio, el alto contenido de Ag conducirá a una disminución en la capacidad específica de Li 4 Ti 5 O 12 / Ag. Por lo tanto, un contenido de plata adecuado no solo puede mejorar eficazmente la conductividad del Li 4 Ti 5 O 12 y reducir la polarización del Li 4 Ti 5 O 12 en el proceso de reacción, pero también puede reducir la pérdida de capacidad reversible debido al recubrimiento de Ag.
Las capacidades de velocidad del Li 4 sin Ag Ti 5 O 12 y 5% en peso de Li 4 recubierto de Ag Ti 5 O 12 compuesto se analizaron a densidades de corriente de 0,5, 1, 5 y 10 ° C, y los resultados se muestran en la Fig. 5. Como se muestra, la capacidad inicial del 5% en peso de Li 4 recubierto de Ag Ti 5 O 12 compuesto a 5 ° C fue 154,12 mAh g −1 . Después de 30 ciclos, la capacidad aún se mantuvo en 150,50 mAh g −1 , reteniendo más del 97,65% de la capacidad inicial. Cuando se incrementó aún más a 10 ° C, la capacidad de descarga aparentemente se redujo de 136,06 mAh g −1 a 130,81 mAh g −1 después de 30 ciclos. Mientras que la eficiencia de retención de la capacidad aún podría mantenerse en 96,14%. Además, el rendimiento ciclista del Li 4 Ti 5 O 12 / El compuesto de Ag fue significativamente mejor que el del Li 4 sin Ag Ti 5 O 12 a varias tasas de carga y descarga. Como se muestra en la Fig. 6a, con un contenido de plata apropiado del 5% en peso, el Li 4 recubierto de plata Ti 5 O 12 entregó la capacidad más alta de 186,34 mAh g −1 a 0,5 ° C, que es más alta que la de otras muestras, y mantuvo el 92,69% de su capacidad inicial a 5 ° C después de 100 ciclos. Incluso a 10ºC después de 100 ciclos (Fig. 6b), todavía tenía una capacidad de retención del 89,17%, lo que demuestra una estabilidad cíclica notable. Los resultados sugirieron que, en condiciones experimentales favorables, el Li 4 Ti 5 O 12 El revestimiento de superficie Ag no solo mejoró la conductividad iónica y de electrones, sino que obviamente también aumentó el transporte de electrones durante la reacción de inserción / extracción de litio y mejoró significativamente la estabilidad del ciclo del Li 4 Ti 5 O 12 .
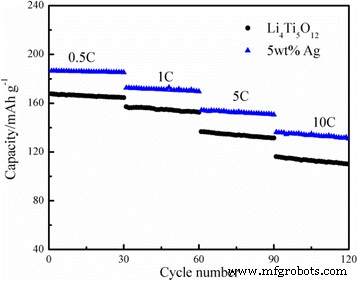
Capacidad de tasa del Li 4 sin Ag y el 5% en peso recubierto de Ag Ti 5 O 12 bajo diferentes tarifas actuales
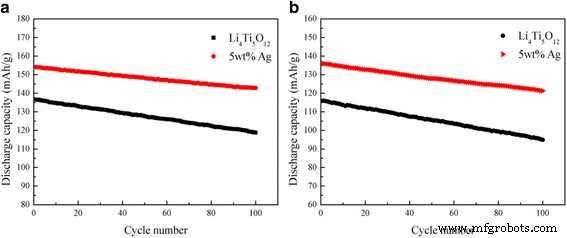
El rendimiento cíclico del Li 4 sin Ag y el 5% en peso recubierto de Ag Ti 5 O 12 a 5 ° C ( a ) y 10 ° C ( b )
La Figura 7 presenta los voltamogramas cíclicos (CV) del Li 4 sin Ag Ti 5 O 12 y 5% en peso de Li 4 recubierto de Ag Ti 5 O 12 compuesto obtenido a una velocidad lenta de 0,1 mV s −1 . Obviamente, se obtuvieron picos redox reversibles entre 1.0 y 2.5 V, que se atribuyen a la inserción y extracción de iones de litio, lo que sugiere que no se forma una fase intermedia durante la inserción y desinserción del litio. Mientras tanto, el área del pico redox de estas dos curvas es casi igual, lo que indica una alta eficiencia culómbica [23]. Las posibles diferencias entre los picos de oxidación y reducción del Li 4 recubierto de Ag al 5% en peso Ti 5 O 12 es de 0,244 V, que es ligeramente inferior a la del Li 4 sin Ag Ti 5 O 12 (0,24 V). Esto sugiere que el recubrimiento apropiado de la superficie del aditivo Ag altamente conductor redujo significativamente la polarización del Li 4 Ti 5 O 12 muestra y mejoró eficazmente su rendimiento electroquímico. Además, los picos redox del 5% en peso de Li 4 recubierto de Ag Ti 5 O 12 son más nítidos y más grandes que los del Li 4 sin Ag Ti 5 O 12 , lo que indica que un recubrimiento de Ag apropiado puede mejorar el desempeño dinámico del electrodo.
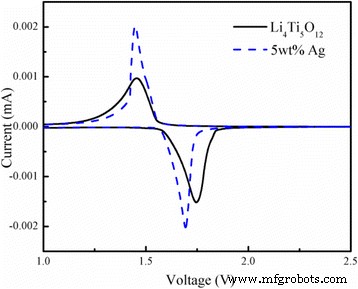
Curvas CV del Li 4 sin Ag y el 5% en peso recubierto de Ag Ti 5 O 12 compuesto
Mediciones de espectroscopía de impedancia electroquímica (EIS) de Li 4 sin Ag Ti 5 O 12 y 5% en peso de Li 4 recubierto de Ag Ti 5 O 12 se realizaron en el rango de frecuencia de 10 5 a 0,01 Hz antes de los ciclos galvanostáticos. Además, el circuito equivalente (recuadro) y los datos de impedancia correspondientes se muestran en la Fig. 8. En el circuito equivalente, Rs representa la resistencia de la solución de electrolito, que refleja la conductividad eléctrica del electrolito, el separador y los electrodos. (intersección con la Z ′ eje a alta frecuencia), R ct muestra la resistencia de transferencia de carga en materiales, CPE es la capacitancia de la película de pasivación y de doble capa, y W es la impedancia de Warburg, que está relacionada con la difusión de iones de litio en la región de baja frecuencia. Los parámetros obtenidos mediante el ajuste se enumeran en la Tabla 2. Como se muestra en la Fig. 8, ambas curvas EIS estaban compuestas por un semicírculo deprimido en la región de alta frecuencia y una línea recta oblicua en la región de baja frecuencia. El diámetro del semicírculo representa la resistencia de transferencia de carga y la línea recta oblicua está relacionada con la impedancia de Warburg [24]. La impedancia de los semicírculos en la región de alta frecuencia corresponde al proceso de transferencia de carga de la interfaz del electrodo y el electrolito líquido, y la línea recta en la región de baja frecuencia se puede expresar como el comportamiento de difusión de los iones de litio en la estructura de óxido [25, 26, 27,28]. Como se muestra en la Fig.8, el diámetro del semicírculo del 5% en peso de Li 4 recubierto de Ag Ti 5 O 12 es más corto que el de Li 4 desnudo Ti 5 O 12 , lo que indica que una cantidad adecuada de recubrimiento de Ag podría mejorar la conductividad electrónica de Li 4 Ti 5 O 12 , y esto tiene que ver con el proceso de transferencia de carga, donde Li + y los electrones alcanzan la superficie del electrodo simultáneamente para completar la reacción. Esto depende principalmente de la reacción redox en la superficie de los materiales activos. La menor resistencia a la transferencia de carga del 5% en peso de Li 4 recubierto de Ag Ti 5 O 12 reflejó reacciones de transferencia de carga más rápidas en sus interfaces electrodo / electrolito.
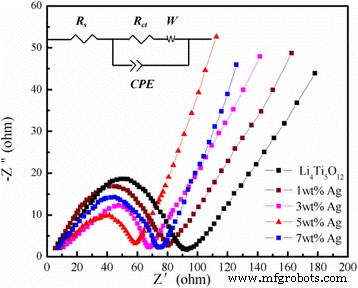
Patrones EIS del Li 4 puro Ti 5 O 12 y el Li 4 Ti 5 O 12 recubierto con diferentes contenidos de Ag
El coeficiente de difusión química de iones de litio se puede calcular a partir del gráfico en la región de baja frecuencia utilizando la siguiente ecuación. (1) [29,30,31,32,33].
$$ {D} _ {{\ mathrm {Li}} ^ {+}} =\ frac {R ^ 2 {T} ^ 2} {2 {A} ^ 2 {n} ^ 4 {F} ^ 4 { C} _ {Li} ^ 2 {\ sigma_w} ^ 2} $$ (1)Aquí, \ ({D} _ {{\ mathrm {Li}} ^ {+}} \) es el coeficiente de difusión de iones de litio, R es la constante de gas (8.314 JK mol −1 ), T es la temperatura absoluta (298 K), A es el área de la superficie del electrodo, n es el número de electrones por molécula que asisten a la reacción de transferencia electrónica, F es la constante de Faraday (96,500 C mol −1 ), C Li es la concentración de iones de litio en el Li 4 Ti 5 O 12 electrodo y σ w es el factor de Warburg, que tiene la siguiente relación con Ζ re :
$$ {Z} _ {\ mathrm {re}} ={R} _S + {R} _ {\ mathrm {ct}} + {\ sigma} _w \ cdot {\ omega} ^ {- 0.5} $$ (2 )Además, la relación entre Z re y la raíz cuadrada recíproca de la frecuencia en la frecuencia baja se muestra en la Fig. 9. Todos los parámetros obtenidos y calculados a partir del EIS se resumen en la Tabla 2. Como se muestra en la Tabla 2, \ ({D} _ {\ mathrm { L} {\ mathrm {i}} ^ {+}} \) del 5% en peso de Li 4 recubierto de Ag Ti 5 O 12 es 6,73 × 10 −11 , que es un orden de magnitud más alto que el de Li 4 Ti 5 O 12 (8,69 × 10 −12 ). El 5% en peso de Li 4 recubierto de Ag Ti 5 O 12 tiene el mayor coeficiente de difusión de litio en comparación con el del Li 4 sin Ag Ti 5 O 12 y 1, 3 y 7% en peso de Li 4 recubierto de Ag Ti 5 O 12 compuestos, lo que indica que el recubrimiento con Ag es una forma eficaz de mejorar la conductividad electrónica. En consecuencia, la capacidad de tasa del 5% en peso de Li 4 recubierto de Ag Ti 5 O 12 se puede mejorar sustancialmente.
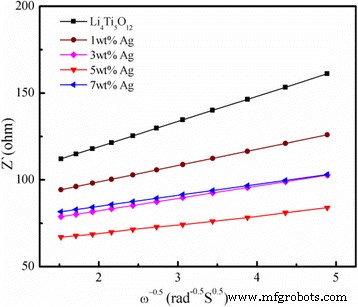
Gráfico de Z re conspirado contra ω −0,5 en la región de baja frecuencia para el Li 4 Ti 5 O 12 y Li 4 Ti 5 O 12 recubierto con diferentes contenidos de Ag
Conclusiones
Materiales anódicos esféricos Li 4 Ti 5 O 12 / Los compuestos de Ag con una alta densidad de grifo se prepararon mediante un método hidrotermal asistido por sol-gel. Las pruebas electroquímicas muestran que la cantidad adecuada de recubrimiento de Ag puede mejorar significativamente la conductividad electrónica de Li 4 Ti 5 O 12 y mejorar la estabilidad del ciclo. El contenido óptimo de plata es 5% en peso, lo que puede obtener un excelente rendimiento electroquímico. Sin embargo, el contenido excesivo de plata empeorará las propiedades electroquímicas del material. Por lo tanto, Li 4 esférico recubierto de Ag apropiado Ti 5 O 12 El compuesto es un material de almacenamiento de litio superior con una alta capacidad y excelente seguridad, y tiene un potencial real como material prometedor en baterías de iones de litio.
Nanomateriales
- Método de preparación del material de contacto de tungsteno de cobre
- Método C#
- Estrategia de sinterización asistida por hidrotermia hacia material de ánodo LiNb3O8 de estructura hueca y porosa
- Síntesis fácil de nanopartículas de SiO2 @ C ancladas en MWNT como materiales de ánodo de alto rendimiento para baterías de iones de litio
- Síntesis hidrotermal de nanopartículas de In2O3, gemelos híbridos, discos hexagonales, heteroestructuras de ZnO para mejorar las actividades fotocatalíticas y la estabilidad
- Compuesto negro de acetileno / MoS2 de pocas capas como material de ánodo eficiente para baterías de iones de litio
- Método de postratamiento para la síntesis de nanopartículas de FePt-Fe3O4 binarias monodispersas
- Efecto del método de síntesis de nanopartículas de manganita La1 - xSr x MnO3 en sus propiedades
- Compuesto de grafeno / Si integrado fabricado por reducción térmica de magnesio como material anódico para baterías de iones de litio
- Sintetizado hidrotermal de microesferas de CoMoO4 como excelente material de electrodo para supercondensador
- Nuevo método crea memoria de computadora a partir de óxido de titanio



