Estrategia de sinterización asistida por hidrotermia hacia material de ánodo LiNb3O8 de estructura hueca y porosa
Resumen
LiNb 3 de estructura porosa y hueca O 8 El material del ánodo se preparó por primera vez mediante una estrategia de sinterización asistida por hidrotermia. Se estudió la evolución de la fase y se propuso el mecanismo de formación de la estructura porosa y hueca. La formación de la estructura única se puede atribuir a la existencia local de fase líquida debido a la volatilización del elemento Li. Como material del ánodo, la capacidad de descarga inicial es 285,1 mAhg −1 a 0,1 C, la mayor capacidad de descarga informada hasta ahora para LiNb 3 O 8 . Incluso después de 50 ciclos, la capacidad reversible aún puede mantener 77,6 mAhg −1 a 0,1 C, aproximadamente 2,5 veces la de LiNb 3 O 8 muestras preparadas por métodos tradicionales de estado sólido. La mejora significativa de la capacidad de almacenamiento de Li se puede atribuir a la estructura especial porosa y hueca, que proporciona una alta densidad de sitios activos y canales paralelos cortos para una rápida intercalación de Li + iones a través de la superficie.
Antecedentes
En los últimos años, se ha prestado mucha atención a las estructuras huecas y porosas debido a sus aplicaciones generalizadas en catálisis, energía, ingeniería ambiental, administración de fármacos y sistemas de sensores [1, 2, 3, 4]. En comparación con otras baterías de nueva energía, las baterías de iones de litio (LIB) han obtenido un éxito comercial como fuente de energía predominante para la electrónica portátil y muestran un gran potencial en aplicaciones a gran escala debido a su alta densidad de energía, larga vida útil y benignidad ambiental [5 ]. Para obtener un alto rendimiento electroquímico, los electrodos de las LIB siempre tienen estructuras abiertas, que pueden proporcionar una alta densidad de sitios activos y canales paralelos para una intercalación más rápida de Li + iones a través de la superficie [6]. Sin embargo, es un desafío sintetizar los nanomateriales con estructuras abiertas, incluidas arquitecturas porosas y huecas.
Para mejorar el rendimiento de los LIB, la gente ha estado buscando materiales para electrodos de alto rendimiento, incluidos materiales de ánodo y cátodo. LiFePO 4 [7], LiCoO 2 [8], LiMn 2 O 4 [9], LiVPO 4 F [10], y varios materiales híbridos [11, 12] se han considerado seriamente como candidatos para materiales catódicos. Para los materiales de ánodo, se han investigado muchos materiales diferentes como alternativas a los materiales de ánodo a base de grafito, como los óxidos de metales de transición (TMO) [13], el disulfuro de molibdeno (MoS 2 ) e híbridos basados en grafeno [14]. En la literatura reciente, se ha demostrado que el niobio tiene un rendimiento electroquímico superior [15]; algunos compuestos tradicionales dopados con elemento Nb y nuevos compuestos basados en Nb están bien desarrollados [16,17,18,19]. Los óxidos a base de Nb se han considerado materiales de ánodos prometedores para los LIB con una seguridad mejorada. Comparado con Li 4 Ti 5 O 12 (con una capacidad teórica de 175 mAhg −1 ), Los óxidos a base de Nb tienen una capacidad teórica relativamente alta de 389 mAhg −1 . Además, es notable que las dos Nb parejas redox, Nb 5+ / Nb 4+ y Nb 4+ / Nb 3+ , puede suprimir la formación de película de interfaz de electrolitos sólidos (SEI) durante el ciclo [19]. LiNb 3 O 8 , un material conocido, siempre aparecen en el proceso de preparación de LiNbO 3 como fase de impureza debido a la volatilización del Li [20]. Jian y col. introdujo por primera vez LiNb 3 O 8 material preparado mediante una reacción en estado sólido como ánodo para LIB. Se encuentra que el LiNb 3 preparado O 8 muestra molida con acetileno negro (LiNb 3 O 8 -BM) mejoró en gran medida las capacidades iniciales de carga / descarga (351 y 212 mAhg −1 ) que los del LiNb 3 preparado O 8 muestra (250 y 170 mAhg −1 ) a 0,05 C; después de 50 ciclos, la capacidad alcanzó 150 mAhg −1 para LiNb 3 O 8 -BM a 0,1 C, solo 30 mAhg −1 para LiNb 3 O 8 muestra [18]. LiNb 3 poroso O 8 Las nanofibras también exhibieron una capacidad mejorada y ciclabilidad en virtud de la gran área de superficie, los pequeños nanocristales y la estructura porosa con la capacidad de descarga inicial de 241.1 mAhg −1 a 0,1 C [19]. Debido a la dificultad para obtener la fase pura, como un nuevo material anódico con alta capacidad teórica, LiNb 3 O 8 rara vez se ha estudiado.
En este artículo, LiNb 3 de estructura porosa y hueca O 8 El material del ánodo se preparó con éxito mediante un proceso de sinterización asistido por hidrotermia. Se estudió la evolución de la fase y se propuso el mecanismo de formación de la estructura porosa y hueca. Las propiedades morfológicas y electroquímicas de LiNb 3 O 8 como el material del ánodo también se estudiaron en detalle.
Métodos
Preparación de muestras
LiNb 3 O 8 los polvos se prepararon mediante el proceso de sinterización asistida hidrotermal. Hidróxido de litio monohidrato (LiOH · H 2 O, Aladdin, ACS, ≥98,0%) y pentóxido de niobio (Nb 2 O 5 , Aladdin, AR, 99,9%) se adquirieron como materias primas sin purificación adicional. Primero, 3,5 mmol de Nb 2 O 5 se dispersó en 35 ml de LiOH · H 2 O solución acuosa transparente (la relación molar de Li:Nb =8:1) con agitación magnética durante 1 h. Luego, la solución de suspensión se colocó en un reactor autoclave de síntesis hidrotermal revestido con teflón de 50 ml. Después de eso, el reactor se selló y se mantuvo a 260 ° C durante 24 hy luego se enfrió a temperatura ambiente de forma natural. Finalmente, los productos preparados se centrifugaron y enjuagaron con agua desionizada y etanol. Después de secar en un horno a 60 ° C durante 12 h, los polvos blancos de Li-Nb-O se recogieron y se calcinaron a varias temperaturas de 500 a 800 ° C durante 2 h con una velocidad de rampa de 5 ° C / min.
Caracterización
La característica de descomposición térmica del polvo de Li-Nb-O se estudió mediante un calorímetro de barrido diferencial y termogravimétrico (TG / DSC, Netzsch STA 409 PC / PG) desde temperatura ambiente hasta 1200 ° C con una velocidad de rampa de 10 ° C / min bajo N 2 atmósfera. Las estructuras cristalinas de los polvos calcinados se analizaron mediante difracción de rayos X en polvo (XRD; Bruker D8 Discover) con Cu Kα radiación. Las morfologías de los polvos calcinados se caracterizaron mediante microscopía electrónica de barrido (SEM; JSM-6700F). El análisis de espectroscopía de fotoelectrones de rayos X (XPS) se realizó en un instrumento Thermo-Fisher Escalab 250Xi.
Mediciones electroquímicas
El LiNb 3 O 8 Los electrodos se prepararon esparciendo una suspensión de LiNb 3 O 8 polvos, negro de humo y fluoruro de polivinilideno (PVDF) con una relación en peso de 8:1:1 sobre una hoja de aluminio. Posteriormente, el electrodo se secó a 120 ° C en un horno de vacío durante la noche. Los ánodos se perforaron en discos con un diámetro de 16 mm. Para las mediciones electroquímicas, se ensamblaron pilas tipo moneda CR2025 en una caja de guantes llena de argón utilizando papel de litio como contraelectrodo y membrana microporosa de polipropileno (Celgard 2320) como separador para aislar los dos electrodos, y luego, el 1.0-M LiPF 6 El electrolito se disolvió en una mezcla de carbonato de etileno y carbonato de dimetilo (1:1 en volumen). Las pruebas de carga-descarga galvanostática de las celdas se realizaron utilizando un sistema de prueba eléctrico Land (Wuhan Land Electronics Co., Ltd., China) entre 0 y 3 V (frente a Li / Li + ) a diferentes densidades de corriente de 0,1 a 1 C (1 C =389 mAhg −1 ). Las curvas de voltametría cíclica (CV) se registraron en una estación de trabajo electroquímica (CHI604E, Shanghai Chenhua Instruments Co., Ltd., China) en el rango de voltaje de 1-3 V.
Resultados y discusión
La Figura 1 traza las curvas TG / DSC del polvo obtenido después de la reacción hidrotermal sin más calcinación. La pérdida de peso del polvo es muy pequeña, alrededor del 5%, incluso cuando la temperatura alcanza los 1100 ° C, pero la pérdida se produce durante todo el proceso de calcinación. Esto se puede atribuir a la evaporación del elemento Li debido a su baja temperatura de fusión, lo que es confirmado por los resultados de DSC con el proceso de reacción endotérmica durante todo el proceso de calcinación. A 330 ° C, se produce un pico endotérmico, que puede originarse por la formación de LiNbO 3 . Se produce una reacción exotérmica a 580 ° C como resultado de la reacción entre LiNbO 3 y Nb 2 O 5 para formar LiNb 3 O 8 . Como se ve en la curva DSC, más allá de 1100 ° C, la reacción exotérmica se vuelve fuerte debido a la descomposición de LiNb 3 O 8 .
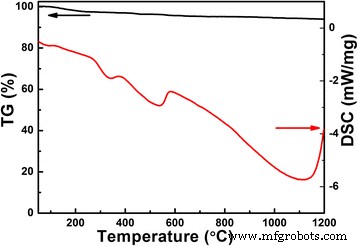
Curvas TG / DSC del polvo de Li-Nb-O desde temperatura ambiente hasta 1200 ° C a una velocidad de calentamiento de 10 ° C / min en N 2
Los patrones de XRD de los polvos de Li-Nb-O calcinados a diferentes temperaturas se muestran en la Fig. 2. Se puede ver que las fases principales son LiNbO 3 y Nb 2 O 5 a 500 ° C. Con el aumento de la temperatura de calcinación, aparece el pico de difracción a 30,26 ° que puede indexarse como el plano (410) del LiNb 3 monoclínico O 8 . La reacción puede describirse mediante la ecuación. (1) no Eq. (2) [21]:
$$ {\ mathrm {LiNb} \ mathrm {O}} _ 3+ {Nb} _2 {\ mathrm {O}} _ 5 \ to {\ mathrm {LiNb}} _ 3 {\ mathrm {O}} _ 8 $$ (1) $$ {\ mathrm {LiNb} \ mathrm {O}} _ 3 \ to {\ mathrm {LiNb}} _ 3 {\ mathrm {O}} _ 8+ {Li} _2 \ mathrm {O} \ uparrow $$ (2)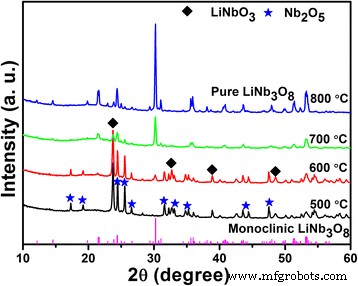
Patrones de XRD del polvo de Li-Nb-O calcinado a diferentes temperaturas durante 2 h
A 700 ° C, el monoclínico LiNb 3 O 8 es la fase predominante con impurezas casi insignificantes. La fase pura de LiNb 3 O 8 se obtiene a 800 ° C con todos los picos de difracción indexados a la fase monoclínica (tarjeta JCPDS nº 36–0307), un grupo espacial de P21 / a. En comparación con el método tradicional de estado sólido, la fase pura de LiNb 3 O 8 se obtiene más fácilmente utilizando el proceso de sinterización asistido por hidrotermia.
Las imágenes SEM de LiNb 3 O 8 El polvo calcinado a 800 ° C con diferentes aumentos se presenta en la Fig. 3. La estructura porosa y hueca que se asemeja a un panal está formada por LiNb 3 O 8 nanopartículas con una longitud de varios micrómetros. La estructura no es plana, con deformaciones obvias, e incluso forma estructuras cerradas parecidas a rechonchas. Es completamente diferente de la agregación de partículas que resulta de las reacciones convencionales en estado sólido. El tamaño del LiNb 3 O 8 La partícula es de aproximadamente 200 nm, como se muestra en la Fig. 3c. El tamaño de partícula pequeño y la estructura única son beneficiosos para la intercalación de iones [6]. La formación de la estructura única se puede atribuir a la volatilización del litio durante el proceso de calcinación, como lo demuestran los resultados de TG-DSC. Como fácil volatilización del elemento Li, el exceso de elemento Li existente en el polvo migra fácilmente a la superficie de las partículas y se convierte en fase líquida. La existencia local de fase líquida conduce a la formación de nuevos LiNb 3 O 8 partículas en el sitio y también fomenta la formación de redes entre las partículas.

un - c Imágenes SEM de LiNb 3 O 8 polvo con diferentes aumentos
Para confirmar aún más las composiciones elementales y el estado electrónico, el LiNb 3 de estructura porosa y hueca O 8 los polvos se analizan por XPS, como se muestra en la Fig. 4. Los datos de XPS se calibraron usando C 1s como referencia con la energía de unión a 284,6 eV. En la Fig. 4a, dos picos en 207,1 y 209,8 eV corresponden a Nb 3d 5/2 y 3d 3/2 , respectivamente, indicando el Nb 5+ estado en LiNb 3 O 8 [22]. Los espectros XPS de O 1 en la Fig. 4b pueden descomponerse en dos picos a 530,3 y 532 eV. El primero se asigna a los enlaces Nb-O, y el último se relaciona con el oxígeno no reticular [22, 23].
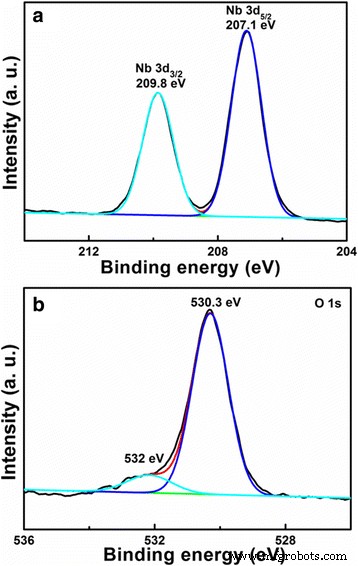
Espectros XPS de ( a ) Nb 3d y ( b ) O 1s para LiNb3O8 de estructura porosa y hueca
Para investigar el rendimiento electroquímico del LiNb 3 preparado O 8 muestra, se realizaron las pruebas de CV y ciclo descarga-carga galvanostática. Las primeras tres curvas CV de LiNb 3 O 8 polvo a una velocidad de barrido de 0,1 mV / s en el intervalo de 3 ~ 1 V se muestran en la Fig. 5. En el primer ciclo, se observan dos picos pronunciados (inserción de Li) a 1,13 y 1,30 V; el primero se puede atribuir a la reducción parcial de Nb 4+ a Nb 3+ , mientras que este último puede estar relacionado con la variación de valencia completa de Nb 5+ a Nb 4+ [18, 19]. Como se ve en la Fig. 5, los ciclos posteriores son bastante diferentes del primer ciclo. La desaparición de los picos a 1,13 y 1,30 V implica que la transición de fase en el primer ciclo es irreversible. Solo los picos de oxidación (extracción de Li) a 1,71 y 1,96 V permanecen estables durante el ciclo, lo que implica el cambio de estructura del LiNb 3 O 8 muestra en ciclos posteriores es reversible.
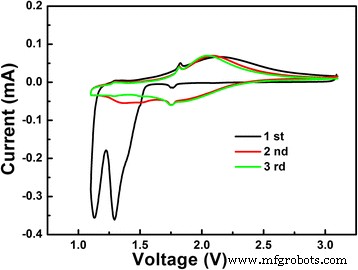
Las tres curvas CV iniciales del LiNb 3 O 8 polvo a una velocidad de escaneo de 0.05 mV / s entre los rangos de voltaje de 3–1 V
La Figura 6 muestra las curvas de descarga-carga del LiNb 3 O 8 polvo a 0,1 C (aquí, 1 C =389 mAhg −1 ) entre 3 y 1 V en el primer, segundo, décimo, trigésimo y quincuagésimo ciclo. En la primera curva de descarga, se pueden observar dos mesetas de potencial obvias a aproximadamente 1,13 y 1,30 V, lo que concuerda bien con los resultados de CV que las reacciones de dos fases, Nb 4+ → Nb 3+ y Nb 5+ → Nb 4+ , tener lugar. Sin embargo, en los ciclos posteriores, las mesetas que existen en el primer ciclo son reemplazadas por curvas inclinadas, lo que implica diferentes reacciones entre el primer ciclo y los posteriores. Al mismo tiempo, la capacidad de descarga inicial del LiNb 3 O 8 la muestra es 285,1 mAhg −1 a 0,1 C, la mayor capacidad de descarga informada hasta ahora para LiNb 3 O 8 materiales de ánodo [18, 19]. La fórmula de 4,4 Li por unidad se puede insertar en LiNb 3 O 8 material, correspondiente a una composición de Li 5.4 Nb 3 O 8 . Sin embargo, la capacidad de carga en el primer ciclo es de 106,4 mAhg −1 , lo que indica que solo 1,6 Li se pueden extraer de forma reversible. La gran pérdida de 2,8 Li es ambigua en la actualidad.
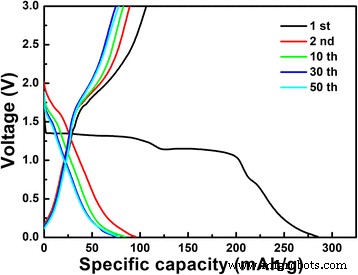
Perfiles de carga-descarga galvanostáticos del LiNb 3 O 8 polvo a 0,1 C entre 3 y 1 V
La Figura 7 muestra el rendimiento de ciclismo de LiNb 3 O 8 muestrear a diferentes velocidades de corriente hasta 50 ciclos. Las capacidades de descarga inicial de LiNb 3 O 8 polvo a velocidades de 0,1, 0,5 y 1 C son 285,1, 250 y 228 mAhg −1 , respectivamente. A una velocidad actual de 0,1 C, la capacidad reversible aún puede mantener 77,6 mAhg −1 , aproximadamente 2,5 veces la de LiNb 3 O 8 muestras preparadas por el método tradicional de estado sólido (aproximadamente 30 mAhg −1 a 0,1 C, Ref. [18]). La mejora significativa de la capacidad de almacenamiento de Li se puede atribuir a la estructura especial porosa y hueca de LiNb 3 O 8 muestra, que proporciona una alta densidad de sitios activos y canales paralelos cortos para una intercalación más rápida de Li + iones a través de la superficie [6]. Cuando las velocidades aumentan a 0,5 y 1 C, las capacidades de descarga después de 50 ciclos permanecen en 39,7 y 29,4 mAhg −1 , respectivamente. Se espera que la estabilidad de la capacidad se pueda mejorar mediante la modificación adecuada de la superficie en LiNb 3 O 8 material.
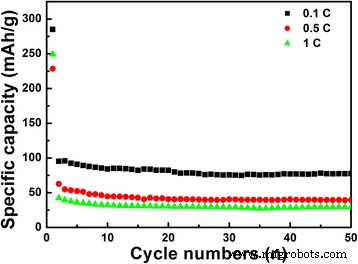
Rendimiento ciclista del LiNb 3 O 8 polvo a diferentes velocidades de corriente de 0,1 C, 0,5 C y 1 C
Conclusiones
En resumen, LiNb 3 de estructura porosa y hueca O 8 El material del ánodo se preparó con éxito mediante la estrategia de sinterización asistida por hidrotermia. Se estudió la evolución de la fase y se propuso el mecanismo de formación de la estructura porosa y hueca. La formación de la estructura única se puede atribuir a la existencia local de fase líquida debido a la volatilización del Li. Como material del ánodo, la capacidad de descarga inicial es 285,1 mAhg −1 a 0,1 C, la mayor capacidad de descarga informada hasta ahora para LiNb 3 O 8 . Después de 50 ciclos, la capacidad reversible aún puede mantener 77,6 mAhg −1 , aproximadamente 2,5 veces la de LiNb 3 O 8 muestras preparadas por métodos tradicionales de estado sólido. La mejora significativa de la capacidad de almacenamiento de Li se puede atribuir a la estructura especial porosa y hueca de LiNb 3 O 8 polvo, que proporciona una alta densidad de sitios activos y canales paralelos cortos para una intercalación rápida de Li + iones a través de la superficie.
Nanomateriales
- Polvo de metal refractario y su proceso de sinterización
- Una guía para construir y medir una estrategia de mantenimiento ajustado
- Arreglando una estrategia de mantenimiento rota:optimización de MP y AMFE
- TOTAL desarrolla la estrategia de inspección y mantenimiento
- Clave de innovación de materiales para 7nm y más allá
- Avances en la estrategia de transformación digital en petróleo y gas
- Nano y ánodo de batería:una revisión
- Los efectos de la relación Li / Nb en la preparación y el rendimiento fotocatalítico de los compuestos Li-Nb-O
- Compuesto negro de acetileno / MoS2 de pocas capas como material de ánodo eficiente para baterías de iones de litio
- Preparación y rendimiento fotocatalítico de fotocatalizadores LiNb3O8 de estructura hueca
- Síntesis de material de ánodo de Li4Ti5O12 esférico recubierto de plata mediante un método hidrotermal asistido por sol-gel



