Síntesis hidrotermal de cuasi-cubos de Co3O4 asistida por albúmina de huevo como material de electrodo superior para supercondensadores con excelentes rendimientos
Resumen
Novela Co 3 O 4 Los cuasicubos con estructura en capas se obtuvieron mediante procedimientos sintéticos de dos pasos. Los precursores se prepararon inicialmente mediante una reacción hidrotermal en presencia de albúmina de huevo, y luego los precursores se recocieron directamente a 300 ° C en aire para convertirlos en Co 3 puro. O 4 polvos. Se encontró que el tamaño y la morfología del Co 3 final O 4 Los productos estuvieron muy influenciados por la cantidad de albúmina de huevo y la duración hidrotermal, respectivamente. Tales capas de Co 3 O 4 los cubos poseían una naturaleza mesoporosa con un tamaño medio de poro de 5,58 nm y una superficie específica total de 80,3 m 2 /gramo. Se empleó un sistema de tres electrodos y 2 M de electrolito acuoso de KOH para evaluar las propiedades electroquímicas de estos Co 3 O 4 cubos. Los resultados indicaron que una capacitancia específica de 754 F g −1 a 1 A g −1 fue logrado. Además, el Co 3 O 4 El electrodo modificado con cubos exhibió un rendimiento de velocidad excelente del 77% a 10 A g −1 y una durabilidad cíclica superior con una retención de capacitancia del 86,7% durante 4000 procesos de carga y descarga repetidos a 5 A g −1 . Un rendimiento electroquímico tan alto sugiere que estos Co 3 mesoporosos O 4 Los cuasicubos pueden servir como un material de electrodo importante para los supercondensadores avanzados de próxima generación en el futuro.
Introducción
Con el rápido desarrollo de la ciencia y la tecnología en la sociedad moderna, depender únicamente de combustibles fósiles con almacenamiento limitado está lejos de cumplir con los crecientes requisitos de energía, por lo que se han desarrollado rápidamente algunos nuevos dispositivos de almacenamiento de energía con tipos benignos para el medio ambiente para resolver este problema. dilema [1, 2, 3]. En la actualidad, las baterías y los supercondensadores son dos tipos de sistemas de almacenamiento de energía más prometedores debido a su alto rendimiento y bajo costo. En particular, los supercondensadores, también conocidos como condensadores electroquímicos, han atraído más atención en términos de su excelencia en densidad de potencia, ciclo de vida a largo plazo, tasa de carga-descarga y otras propiedades [4, 5, 6]. Atribuidos a estas ventajas, los supercondensadores se han aplicado en iluminación de emergencia, vehículos eléctricos híbridos, equipos militares y fuentes de energía a corto plazo [7, 8]. Al mismo tiempo, la energía y la densidad de potencia de los supercondensadores deben aumentarse continuamente para adaptarse a la expansión de sus campos de aplicación; como resultado, se han dedicado enormes esfuerzos a resolver este problema. Lograr mejoras notables en los supercondensadores requiere una comprensión fundamental profunda de los mecanismos de almacenamiento de carga. Se ha descubierto que la forma, la porosidad y las propiedades mecánicas de los materiales de los electrodos tienen un impacto crucial en el rendimiento de los supercondensadores [9,10,11]. Para obtener un material de electrodo ideal, se debe mejorar el número de sitios electroquímicamente activos para la transferencia de carga y se debe controlar el transporte iónico / electrónico a una longitud de difusión pequeña [12].
Los supercondensadores se han diferenciado en las categorías sobre la base de diferentes mecanismos de almacenamiento de energía. Uno de ellos almacena energía por acumulación de carga en la interfaz del electrodo y el electrolito, y se conoce como condensadores eléctricos de doble capa (EDLC). El otro son los pseudocondensadores (PC), que dependen de una rápida reacción farádica que se produce cerca o en la superficie de los materiales de los electrodos para almacenar energía [13,14,15,16]. Los materiales carbonosos, como el carbón activado, el grafeno y los nanotubos de carbono (CNT), que tienen una gran superficie específica y buena conductividad, son materiales de electrodos ideales para los EDLC. Sin embargo, para los materiales a base de carbono, su capacitancia específica inherentemente baja es un defecto severo que no se puede ignorar, lo que conduce a una densidad de energía más baja que la de los PC [17]. Los polímeros conductores, así como los óxidos metálicos, se utilizan comúnmente como materiales de electrodos en los PC, debido a sus favorables características pseudocapacitivas de reacciones redox rápidas y reversibles. Los PC pueden proporcionar una mayor energía y densidad de potencia, una mayor capacitancia específica y han atraído el interés de la investigación en todo el mundo [18]. Hasta la fecha, los óxidos de metales, especialmente los óxidos de metales de transición (TMO), como el MnO 2 [19, 20], NiO [21, 22] y Fe 2 O 3 [23, 24], han atraído mucha atención como candidatos potenciales para materiales de electrodos, ya que pueden proporcionar una rica transferencia de carga redox originada a partir de su variedad de estados de oxidación, lo cual es beneficioso para la reacción de Faraday. A pesar de las virtudes de bajo costo y alta capacitancia específica, los efectos de estos materiales usados como electrodo en PC aún no son satisfactorios, dado que generalmente poseen cambios de volumen dramáticos, capacidad de velocidad inferior y resistencia relativamente alta; Se han realizado enormes esfuerzos para sortear los obstáculos [25]. Entre la serie de TMO, Co 3 O 4 se considera como uno de los materiales de electrodos más prometedores. Este tipo de material posee una capacitancia específica teórica de hasta 3560 F g −1 [26]. Además, es ecológico, económico y rico en actividad redox. Desafortunadamente, en comparación con su valor teórico, la capacitancia específica de Co 3 O 4 electrodo logra en aplicaciones prácticas es significativamente bajo. Atribuido a la transferencia de limitación de electrones causada por la alta resistencia interna del Co 3 O 4 , solo una parte de los sitios activos pueden estar involucrados en la reacción redox, lo que lleva a una baja utilización del material activo y una disminución de la capacitancia específica. Además, el Co 3 O 4 tiene una tendencia de cambio de volumen dramático durante el proceso de reacciones redox rápidas, y el colapso del material del electrodo conduce a una reducción del ciclo de vida [27].
Para abordar estos problemas, Co 3 O 4 Se han preparado con éxito nanoestructuras con diferentes morfologías, incluidas nanovarillas, nanocables, nanoflakes y nanoflores, controlando el proceso de síntesis, con el objetivo de aumentar la superficie y facilitar la reacción redox [28,29,30,31]. Los resultados de la investigación han demostrado que diferentes morfologías tienen un efecto significativo en el rendimiento de Co 3 O 4 electrodo, pero simplemente cambiando la morfología está lejos de ser capaz de mejorar su mala conductividad inherente y sus serios defectos de expansión de volumen. Los investigadores se dedican a combinar Co 3 O 4 con otros materiales altamente conductores para obtener materiales de electrodos con alta capacidad de transferencia de carga. Además, la sinergia entre diferentes materiales puede contribuir a la reacción redox al mismo tiempo, para lograr el propósito de aumentar la capacitancia específica [32,33,34,35]. Desde el punto de vista de las aplicaciones prácticas y la gran producción, es muy importante preparar el material de electrodo en polvo a través de un proceso sintético simple.
El método de solución que incluye la ruta hidrotermal / solvotermal es una de las estrategias sintéticas importantes para preparar micro / nanomateriales a gran escala. En este método, normalmente se emplea tensioactivo para controlar la velocidad de nucleación y crecimiento de cristales. Por tanto, la forma final de las nanoestructuras puede ajustarse eficazmente mediante el tensioactivo [36,37,38]. Se pueden usar varios tipos de tensioactivos, incluidos tensioactivos catiónicos, tensioactivos aniónicos, tensioactivos no iónicos, etc. para la fabricación de nanomateriales. Entre ellos, las moléculas biológicas con grupos funcionales han recibido una atención creciente debido a la benignidad ambiental de este tipo de tensioactivo. Las proteínas pueden interactuar con nanopartículas inorgánicas y luego gobernar la nucleación de materiales inorgánicos en soluciones acuosas. La albúmina de huevo, como proteína importante, puede obtenerse ampliamente de los huevos. Ha recibido mucha atención debido a sus características gelificantes, espumantes y emulsionantes. Además, la albúmina de huevo es rentable y respetuosa con el medio ambiente, y el uso de tal tensioactivo puede no resultar en peligro tanto para el medio ambiente como para la salud de los seres humanos. Por tanto, la albúmina de huevo se puede emplear para la preparación de nanomateriales con morfología controlada. Por ejemplo, Geng et al. Fe 3 monocristalino preparado O 4 nanotubos con altos rendimientos que utilizan albúmina de huevo como nanorreactor [39]. Las nanohojas de ZnS se pueden sintetizar mediante albúmina de huevo y un método asistido por microondas [40]. Además, BaCO 3 en forma de mancuerna superestructuras y SnO 2 Las galletas pueden obtenerse con la ayuda de albúmina de huevo por diferentes grupos de investigación [41, 42]. En general, los informes sobre la fabricación de nanomateriales con albúmina de huevo rara vez se han informado. En este trabajo, el Co 3 poroso O 4 Los cubos se sintetizaron con la ayuda de albúmina de huevo mediante un método hidrotermal y postcalcinación de los precursores. Estos Co 3 O 4 Los cubos porosos tenían un tamaño medio de poro de 5,58 nm y el área de superficie específica de Brunauer-Emmett-Teller (BET) se evaluó en 80,3 m 2 /gramo. Si tal Co 3 O 4 Los cubos se procesaron en un electrodo de trabajo, una alta capacitancia de 754 F g −1 se obtuvo a 1 A g −1 . Además, si se mejora la densidad de corriente a 10 A g −1 , el electrodo mostró una alta capacidad de hasta un 77%. Un rendimiento de ciclismo superior con una retención de capacitancia del 86,7% (a 5 A g −1 ) también se logró durante el proceso de carga y descarga de 4000 ciclos. Estas excelentes propiedades electroquímicas indican que el Co 3 poroso O 4 Los cubos pueden servir como un material de electrodo prometedor para supercondensadores en un futuro próximo.
Métodos
Materiales
En este trabajo, todos los reactivos eran de grado analítico puro y se utilizaron sin ninguna purificación adicional. Se adquirieron urea y acetato de cobalto (II) tetrahidratado de Sinopharm Chemical Reagent Co., Ltd., y se obtuvo albúmina de huevo de huevos frescos.
Preparación de Co 3 poroso O 4 Cubos
Para preparar el Co 3 poroso O 4 Se disolvieron cubos, 3 mL de albúmina de huevo, 2,4 g de urea y 0,3 g de acetato de cobalto (II) tetrahidratado en 37 mL de agua desionizada (DI) con agitación vigorosa. Luego se cargó la mezcla en un autoclave con 50 mL de capacidad, y se colocó el autoclave en un horno a 140 ° C. Cinco horas más tarde, los precipitados se recogieron, se aclararon y se secaron a 60ºC durante la noche. El precursor obtenido se recoció a 300 ° C durante 5 h con el fin de obtener un polvo negro. Se llevaron a cabo experimentos de control con varios tiempos hidrotermales (1, 2, 15 y 24 h) y diferentes cantidades de albúmina de huevo, respectivamente, manteniendo los mismos parámetros y procedimientos.
Fabricación de electrodo de trabajo y pruebas electroquímicas
En una estación de trabajo electroquímica CHI 660E, se realizaron tres tipos de pruebas electroquímicas, incluida la voltamperometría cíclica (CV), la cronopotenciometría (CP) y la espectroscopia de impedancia electroquímica (EIS), basándose en una configuración típica de tres electrodos, en la que el alambre de platino servía como contraelectrodo y Se utilizó electrodo de calomelanos saturado (SCE) como electrodo de referencia, respectivamente. La descripción detallada sobre la fabricación del electrodo de trabajo fue la siguiente:en primer lugar se preparó un polvo mixto que contenía material activo, negro de acetileno y fluoruro de polivinilideno (PVDF) con una relación en peso de 80:15:5, y luego se dispersó el polvo mixto en N -metil-2-pirrolidona (NMP) con ayuda de ultrasonidos. La suspensión obtenida se revistió sobre espuma de níquel previamente limpiada (1 x 1 cm 2 ) y se secó al vacío a 85 ° C; posteriormente, se realizó una presión de 10 MPa suministrada por prensa hidráulica sobre la espuma de níquel y finalmente se obtuvo el electrodo de trabajo. Todas las pruebas se realizaron en 2 M de electrolito acuoso de KOH; el potencial de las pruebas de CV varió de - 0,1 a 0,65 V, y las tasas de exploración oscilaron entre 2 y 50 mV s −1 . Para las pruebas de CP, la densidad de corriente difirió de 1 a 10 A g −1 con el potencial que varía de 0 a 0,45 V. Se adoptó un potencial de circuito abierto para la medición del EIS; la región de frecuencia era 10 −2 –10 5 Hz y la amplitud de CA fue de 5 mV. La capacitancia específica se puede obtener de la Ec. (1):
$$ {C} _s =\ frac {I \ cdot \ Delta t} {m \ cdot \ Delta V} $$ (1)donde C s (F g −1 ) representa la capacitancia específica, ∆ t (s) indica el tiempo de descarga, I (A) está descargando corriente, ∆ V (V) significa ventana potencial y m (g) es el peso del material activo.
Caracterizaciones
El patrón de difracción de rayos X (XRD) de la muestra se recogió en un difractómetro de rayos X de polvo (Bruker D8 Advance), en el que se utilizó Cu-kα como fuente de rayos X (λ =0,1548 nm) y el rango de 2θ fue de 25-100 °. Las imágenes del microscopio electrónico de emisión de campo (FESEM) estaban disponibles en un microscopio electrónico de barrido JEOL JSM7100F, y la imagen del microscopio electrónico de transmisión (TEM) se obtuvo en un equipo JEOL JEM2100F con un voltaje de funcionamiento de 200 kV. Antes de la medición TEM, el polvo debe dispersarse ultrasónicamente en etanol durante 10 minutos, luego se deja caer sobre una rejilla de cobre recubierta de carbón. El examen Raman se realizó en un espectrómetro RM 1000-Invia (Renishaw) y se eligió que la longitud de onda del láser fuera de 514 nm. La medición de espectroscopía de fotoelectrones de rayos X (XPS) se realizó en un espectrómetro ESCA 2000 y se empleó Al Kα como fuente de excitación. Según los experimentos de adsorción / desorción de nitrógeno realizados a 77 K, se obtuvo el área de superficie Brunauer-Emmet-Teller (BET). Además, la distribución del tamaño de los poros (Barrett-Joyner-Halenda, método BJH) podría obtenerse de la isoterma de desorción relacionada.
Resultados
La forma y el tamaño de la muestra preparada con 3 mL de albúmina de huevo a 140 ° C durante 5 h combinada con un proceso de post recocido a 300 ° C fueron investigados por SEM (Fig. 1a). Indicó que el producto estaba dominado por una gran cantidad de partículas en forma de cubo con un tamaño de aproximadamente 5-6 μm. La imagen SEM ampliada (Fig. 1b) demostró que algunas esquinas de cada cubo no eran perfectas, y el cubo se ensambló con estructuras en capas, como apuntaban las flechas blancas. Esta nueva estructura en capas se pudo observar claramente a partir de la imagen SEM de la Fig. 1c. La composición y la fase cristalina se investigaron mediante la técnica XRD. La Figura 1d muestra el patrón XRD típico, en el que todos los picos de difracción observados se pueden indexar como (111), (220), (400), (422), (511) y (440) planos cristalinos de Co 3 O 4 (JCPDS No. 43-1003). No se generaron picos a partir de impurezas de Co (OH) 2 y CoO, lo que sugiere una alta pureza del Co 3 O 4 muestra obtenida aquí. La imagen TEM en la Fig. 1e mostró un Co 3 representativo O 4 cubo con un tamaño de 5 μm, y el tamaño estaba de acuerdo con los datos de SEM. La Figura 1f exhibió una imagen TEM ampliada que fue tomada desde la posición enfocada en un borde del cubo. Se podía ver la estructura porosa, por lo que el Co 3 total O 4 En realidad, el cubo estaba compuesto por muchas capas basadas en nanopartículas (NP). El patrón de difracción de electrones de área seleccionada (SAED) indicó una estructura policristalina, y los anillos de difracción basados en puntos sugirieron además la gran cantidad de NP ensambladas en el Co 3 poroso. O 4 cubo. Además, el cubo era tan grueso que la caracterización TEM de alta resolución (HRTEM) era difícil de realizar.

a – c Imágenes SEM, d Patrón XRD y e , f Imágenes TEM de Co 3 poroso O 4 cuasi-cubos con el patrón SAED en el recuadro de ( f )
La información estructural detallada de Co 3 O 4 Los nanocubos se evaluaron mediante el espectro Raman que se muestra en la Fig. 2a. Cuatro bandas características ubicadas a 468, 509, 611 y 675 cm −1 se pueden observar, que corresponden a E g , \ ({\ mathrm {F}} _ {2 \ mathrm {g}} ^ 1 \), \ ({\ mathrm {F}} _ {2 \ mathrm {g}} ^ 2 \) y A 1g Modos activos de Raman, respectivamente. Dichos resultados concuerdan bien con la literatura anterior, lo que demuestra aún más la formación de Co 3 O 4 [33, 43]. La Figura 2b ilustró un espectro XPS de estudio completo representativo de Co 3 O 4 nanocubos, y no se pueden observar otros picos de impureza excepto los picos característicos de los elementos de carbono, cobalto y oxígeno. Los datos completos de la encuesta XPS sugirieron la alta pureza del Co 3 O 4 muestra. Como puede verse en la alta resolución del espectro de Co 2p que se muestra en la Fig. 2c, hay dos picos obvios centrados en 779,7 y 794,8 eV, que corresponden a Co 2p 3/2 y Co 2p 1/2 , respectivamente. Además, la separación de energía de los dos picos fue de 15,1 eV, lo que refleja la existencia de Co 3+ [14]. Además, los dos picos principales podrían separarse en dos dobletes de giro-órbita después del ajuste gaussiano; los picos con energías de unión de 779,6 y 794,6 eV estaban relacionados con Co 3+ , mientras que otros ubicados en 780.9 y 796.2 eV correspondían a Co 2+ ; Estos resultados de observación coincidieron bien con el informe anterior [44]. Se pueden observar dos picos satélites (marcados como "sat") cerca de las energías de enlace de 788,6 y 804,1 eV, y su presencia confirmó aún más la característica de las estructuras de espinela [45]. Los resultados del ajuste del espectro de O 1s (Fig. 2d) mostraron que había tres contribuciones de oxígeno (O1, O2, O3). El componente O1 situado en 529,5 eV se puede indexar al enlace típico metal-oxígeno, y el componente O2 a 531,1 eV se atribuye al grupo hidroxilo [46]. En cuanto al componente O3 con alta energía de enlace de 532,4 eV, corresponde a las moléculas de agua absorbidas en la superficie del electrodo [47].
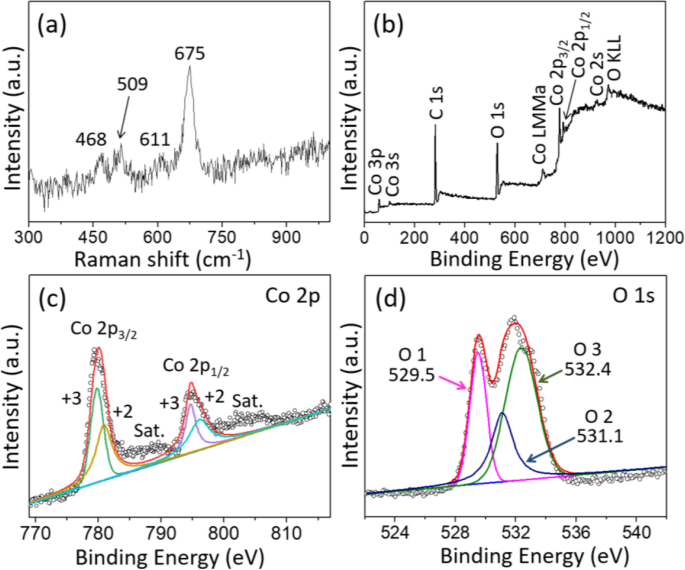
un Espectro Raman y b Espectro de levantamiento XPS de Co 3 poroso O 4 cubos y los espectros a nivel de núcleo para c Co 2p y d O 1s
La cantidad de albúmina de huevo en el sistema jugó un papel clave para formar tal Co 3 O 4 cubos. Si no se empleó albúmina de huevo, el producto estaba dominado por una gran cantidad de Co 3 O 4 nanohojas (Fig. 3a), y la estructura porosa se pudo encontrar claramente en la imagen TEM de la Fig. 3b. Tal Co 3 O 4 las nanoláminas estaban bien cristalizadas; además, los 0.287 nm de espaciado de franjas (Fig. 3c) correspondían a los (220) planos cristalinos de Co 3 O 4 . Cuando se agregaron 0.5 mL de albúmina de huevo, el Co 3 O 4 La muestra estaba compuesta por algunos cubos en capas, así como algunas hojas (Fig. 3d). Co 3 O 4 Las nanohojas desaparecieron casi por completo cuando se aumentó la dosis de albúmina de huevo a 1 ml. Bajo esta condición, Co 3 O 4 Se formaron cubos de qusi con una longitud de borde de aproximadamente 3 a 10 μm (Fig. 3e). Uniformado Co 3 O 4 se pudieron obtener cubos ya que la cantidad de albúmina de huevo se incrementó continuamente a 3 ml. Si aumentamos aún más la albúmina de huevo a 5 ml, la morfología del Co 3 O 4 los cubos estaban bien conservados sin ningún cambio, pero el tamaño se redujo a 3-4 μm (Fig. 3f). De las observaciones de SEM anteriores, el proceso de formación de Co 3 O 4 tentativamente se pueden proponer cubos con la ayuda de albúmina de huevo. Durante la reacción, Co 2+ los iones reaccionan con la albúmina de huevo para formar un complejo; la combinación de átomos de nitrógeno en las moléculas de albúmina de huevo y Co 2+ Los iones pueden promover el crecimiento agregado. Debido a las interacciones de apilamiento y la fuerza de empaquetamiento de los cristales, los agregados prefieren crecer en una estructura de escamas. Si la cantidad de albúmina de huevo es suficiente, las escamas tienden a apilarse debido a la existencia de enlaces de hidrógeno entre las moléculas, lo que lleva a la formación de estructuras de cubos en capas finales.

un Imagen SEM y b , c Imágenes TEM de Co 3 O 4 nanohojas obtenidas sin albúmina de huevo y las imágenes SEM del Co 3 O 4 muestras preparadas con albúmina de huevo de d 0.5, e 1 y f 5 ml
También se realizaron experimentos controlados con diferentes tiempos de reacción hidrotermal mientras que la dosis de albúmina de huevo se fijó en 3 mL. Si la reacción transcurrió solo 1 h, Co 3 O 4 Se produjeron NP con formas irregulares en grandes cantidades (Fig. 4a). Una pequeña cantidad de Co 3 O 4 los cubos y las NP coexistieron cuando la reacción se extendió a 2 h (Fig. 4b). Perfecto Co 3 O 4 se pudieron obtener cubos a gran escala ya que el tratamiento hidrotermal se prolongó a 5 h; después de eso, la forma y el tamaño casi no tuvieron cambios obvios y la reacción se prolongó hasta 15 ho más (Fig. 4c, d). El mecanismo de crecimiento de Co 3 O 4 cubos y la influencia de la albúmina de huevo en el Co 3 final O 4 La morfología requiere más investigaciones detalladas, y actualmente se están realizando investigaciones relacionadas.

Imágenes SEM del Co 3 O 4 muestras sintetizadas con diferentes duraciones hidrotermales: a 1, b 2, c 15 y d 24 h
La porosidad de estos Co 3 O 4 cubos se investigó mediante isotermas de adsorción-desorción de nitrógeno. Las propiedades de la estructura mesoporosa del Co 3 O 4 Los nanocubos podrían revelarse claramente por las isotermas que se muestran en la Fig. 5a, ya que tales isotermas se clasificaron como un tipo IV típico y se acompañaron con una histéresis de tipo H3. La distribución del tamaño de los poros obtenida por el método BJH demostró aún más este punto (Fig. 5b). El diámetro medio de los poros de estos Co 3 O 4 nanocubos fue de 5,58 nm, y el área de superficie específica BET se evaluó en 80,3 m 2 g −1 . Especialmente, se vio en la Fig. 5b que el tamaño de los poros se distribuyó predominantemente en 4,03 nm. Las isotermas de Co 3 O 4 Se ilustró nanohojas en la Fig. 5c, que eran similares a las isotermas de los nanocubos; sin embargo, el área de superficie específica de BET de Co 3 O 4 nanosheets fue menor que Co 3 O 4 nanocubos, solo 52,5 m 2 g −1 . Además, el diámetro medio de poro de Co 3 O 4 nanohojas obtenidas a partir de la Fig. 5d era de 4,44 nm. Es bien sabido que los materiales de electrodo con gran área superficial y porosidad son más favorables para reacciones electroquímicas rápidas porque aumenta el número de sitios electroquímicamente activos y se acelera el transporte de electrones así como de iones. Atributo de un diámetro de poro bien distribuido y una gran superficie, el Co 3 O 4 El electrodo modificado con nanocubos permite un rápido progreso de la reacción redox y una fácil penetración del electrolito dentro del electrodo, lo que conduce a una capacitancia específica favorable.
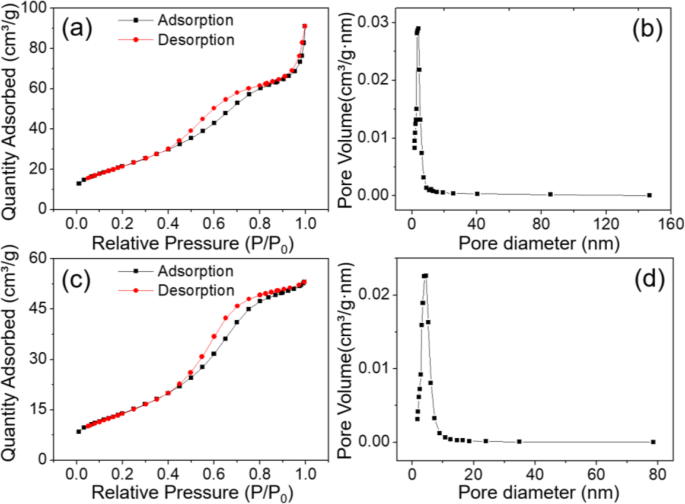
N 2 isotermas de adsorción-desorción y las correspondientes distribuciones de tamaño de poro BJH para a , b Co 3 poroso O 4 cubos y c , d Co 3 poroso O 4 nanohojas, respectivamente
El rendimiento electroquímico del Co 3 preparado O 4 Los nanocubos se evaluaron mediante mediciones de CV, CP y EIS. Todas las pruebas se realizaron en 2 M de electrolito acuoso KOH usando una configuración de tres electrodos. Con el potencial que varía de - 0,1 a 0,65 V y la velocidad de exploración cambia entre 2 y 50 mV s −1 , las curvas CV de Co 3 O 4 nanocubos y nanohojas se presentaron en la Fig. 6a, b, respectivamente. Ambas curvas CV tenían más de un par de picos de oxidación y reducción bien definidos. Tal fenómeno implicó que el almacenamiento de carga para Co 3 O 4 El electrodo de nanocubos se rige por una pseudocapacitancia en lugar de una capacitancia eléctrica de doble capa que presenta curvas CV rectangulares [48]. Según la diferencia de morfología y porosidad, las curvas CV de los dos materiales de los electrodos no son completamente similares. En términos del área integrada por curvas CV, el Co 3 O 4 El electrodo modificado con nanocubos es significativamente más grande que el electrodo modificado con nanocubos, lo que indica que el Co 3 O 4 El electrodo modificado con nanocubos puede proporcionar una mayor capacitancia específica. Como la Fig. 6a ilustra que la velocidad de exploración se aceleró, los dos picos de oxidación se mezclaron gradualmente para formar un pico de oxidación amplio. Además, los picos anódicos se desplazaron hacia una posición más positiva, mientras que los picos de reducción se desplazaron a una posición más negativa, lo que sugiere las características reversibles de las reacciones redox [29]. Los pares de picos redox en ambas curvas CV correspondían a la conversión entre diversos estados de oxidación del cobalto, y las ecuaciones se resumieron principalmente de la siguiente manera [49]:
$$ {\ mathrm {Co}} _ 3 {\ mathrm {O}} _ 4 + {\ mathrm {H}} _ 2 \ mathrm {O} + {\ mathrm {O} \ mathrm {H}} ^ {-} \ flecha izquierda 3 \ mathrm {CoOOH} + {\ mathrm {e}} ^ {-} $$ (2) $$ \ mathrm {CoOOH} + {\ mathrm {OH}} ^ {-} \ leftrightarrow {\ mathrm {CoO} } _2 + {\ mathrm {H}} _ 2 \ mathrm {O} + {\ mathrm {e}} ^ {-} $$ (3)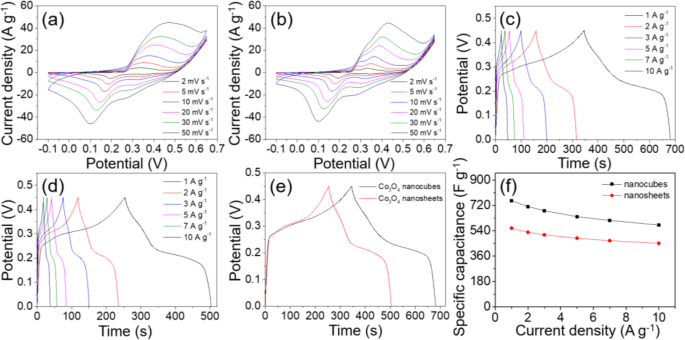
Curvas CV medidas con diferentes velocidades de escaneo para a Co 3 poroso O 4 cubos y b Co 3 poroso O 4 nanohojas, curvas de CP medidas con diferentes densidades de corriente para c Co 3 poroso O 4 cubos y d Co 3 poroso O 4 nanohojas, e Curvas CP de los dos electrodos obtenidos a 1 A g −1 y f capacitancias específicas obtenidas a varias densidades de corriente
Los comportamientos electroquímicos capacitivos del Co 3 O 4 Los nanomateriales también se investigaron mediante pruebas de CP. La Figura 6c, d exhibió las curvas CP de Co 3 O 4 nanocubos y nanoláminas con diversas densidades de corriente, que se adquirieron sobre un potencial de 0 a 0,45 V. La aparición de distintas mesetas de potencial en todas las curvas de las dos muestras demostró las características de pseudocapacitancia, lo que concuerda con las conclusiones obtenidas de las curvas CV [50 ]. Según Eq. (1), el Co 3 O 4 El electrodo modificado con nanocubos entregó capacitancias específicas de 754, 712, 683, 641, 614 y 581 F g −1 , respectivamente, a las densidades de corriente de 1, 2, 3, 5, 7, 10 A g −1 . En cuanto al Co 3 O 4 electrodo modificado con nanohojas, entregó las capacitancias específicas de 559, 530, 512, 487, 470 y 452 F g −1 en la misma condición de prueba. Según las curvas de CP de los dos tipos de electrodos a 1 A g −1 (Fig. 6e), se ve que el tiempo de descarga de Co 3 O 4 El electrodo modificado con cubos es más largo que el del Co 3 O 4 electrodo modificado con nanohojas, lo que demuestra que el Co 3 O 4 El electrodo modificado con cubos puede mostrar propiedades electroquímicas superiores. La figura 6f indica la variación de capacitancia específica a diferente densidad de corriente para los dos tipos de electrodos. Obviamente, la capacitancia específica se reduce gradualmente a medida que aumenta la densidad de corriente. Las capacidades de tasa de Co 3 O 4 nanocubos y electrodos modificados con nanoláminas de 1 a 10 A g −1 fueron 77% y 81%, respectivamente. No es difícil entender que a altas densidades de corriente, la difusión insuficiente de iones y eletrones hace imposible que el electrolito logre un contacto completo con el material del electrodo, lo que da como resultado que solo los sitios activos en la superficie exterior del material del electrodo pueden participar en el proceso. reacción quimica de óxidoreduccioón. En consecuencia, la utilización incompleta del material activo conduce directamente a una reducción de la capacitancia específica. En comparación con otras publicaciones anteriores relacionadas, el Co 3 O 4 El electrodo modificado con nanocubos sintetizado en este trabajo exhibe un desempeño electroquímico superior (Tabla 1). Cabe mencionar que los electrodos compuestos formados por la combinación de Co 3 O 4 y otros materiales tienden a exhibir un mejor rendimiento electroquímico. La conductividad mejorada del electrodo compuesto y la sinergia entre diferentes sustancias hacen una mayor contribución a la pesudocapacidad.
La estabilidad del ciclo es otro parámetro vital para medir el potencial de aplicación del Co 3 O 4 electrodo modificado con nanocubos, que se evalúa mediante 4000 pruebas continuas de CP a 5 A g −1 . La Figura 7 demuestra que la capacitancia específica tiende a disminuir gradualmente en los primeros cientos de ciclos y luego se mantiene estable mientras aumenta el número de ciclos; al final de 4000 ciclos, la capacitancia específica es 556 F g −1 y permanece alrededor del 86,7% del valor inicial. Estos resultados indican que el Co 3 O 4 El electrodo modificado con nanocubos posee una excelente durabilidad cíclica de larga duración, lo que es una garantía importante en las aplicaciones de supercondensadores. La eficiencia de Coulombic es un parámetro que puede reflejar la reversibilidad de la reacción redox, que se puede calcular mediante la siguiente ecuación:
$$ \ eta =\ frac {t_d} {t_c} \ times 100 \% $$ (4)donde η representa la eficiencia de Coulombic, t d y t c indican el tiempo de descarga y carga, respectivamente. La eficiencia Coulombic del Co 3 O 4 El electrodo modificado con nanocubos permanece casi al 100% durante todo el ciclo de prueba (Fig. 7), y sugiere que las reacciones pseudocapacitivas son notablemente reversibles.
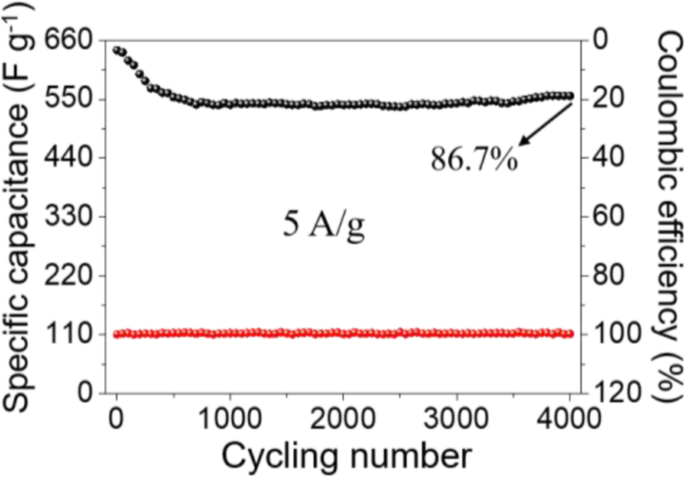
Estabilidad cíclica y eficiencia Coulombic del poroso Co 3 O 4 cubos de electrodos medidos a 5 A g −1
The ion migration and charge transfer characteristics of the Co3 O 4 nanocubes and nanosheets-modified electrodes were further investigated by EIS measurement and the results were shown in Fig. 8. As we can see that a semicircle in high-frequency region and a straight line in low-frequency region appear in the corresponding Nyquist plot. La resistencia interna ( R s ) refers to the sum of the ionic internal resistance of electrolyte, the internal resistance of active material, and the contact resistance between electrode material and electrolyte. La R s value is reflected by the intercept of the semicircle on the real axis (Z ’). The resistance of charge transfer reflected by the diameter of the semicircle, the smaller of the diameter, the better transfer of the ions between electrolyte and active material. The Warburg impedance (Z W ) can be reflected by the slope of the straight line in low frequency, and Z W is mainly caused by the diffusion of OH − ions in electrolyte. In the inset of Fig. 8 is the equivalent circuit fitted from the EIS data, from which a better understanding can be obtained. By analyzing the EIS results of the two electrodes, the R s were found to be 0.78 and 0.72 Ω for Co3 O 4 nanocubes and nanosheets-modified electrodes, respectively, which may be attributed to the fact that the thinner sheet-like structure is more favorable for ion permeation in the electrolyte than the cubic structure. Furthermore, the R ct value of the two kind of electrodes were 6.9 and 4.1 Ω, respectively, suggesting that the nanosheets-modified electrode provided higher charge transfer capability.
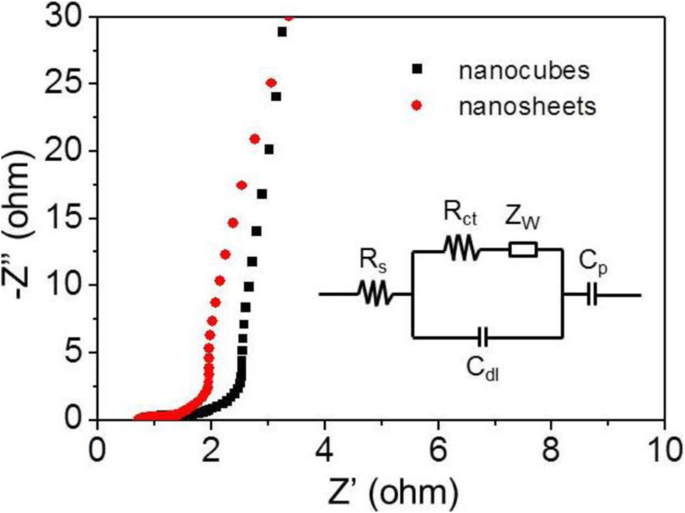
Nyquist plots of Co3 O 4 cubes and Co3 O 4 nanosheets-based electrodes in 2 M KOH solution with the fitted equivalent circuit in the inset
Conclusiones
Porous Co3 O 4 quasi-cubes were prepared through an egg albumin-assisted hydrothermal method with a subsequent high-temperature treatment of precursor in air directly. The size and shape of final Co3 O 4 samples had a close relationship with the amount of egg albumin and hydrothermal reaction time, respectively. Such Co3 O 4 cubes possessed a mesoporous characteristic with surface area of 80.3 m 2 /g, average pore size of 5.58 nm, and main pore size distribution at 4.03 nm. Once these Co3 O 4 quasi-cubes were processed into a working electrode, it delivered a high specific capacitance of 754 F g −1 at 1 A g −1 and 581 F g −1 at the current density of 10 A g −1 . After a continuous 4000 cycles at 5 A g −1 , 86.7% capacitance retention could be obtained and it demonstrated a good cycling stability. The outstanding electrochemical properties of these Co3 O 4 cubes enable them to be promising electrode materials for advanced supercapacitors. In addition, the egg albumin-assisted synthesis route is expected to be extended to prepare other oxides-based electrode materials with novel morphology and superior electrochemical performances.
Disponibilidad de datos y materiales
The datasets used and/or analyzed during the current study are obtained from the corresponding author on reasonable request.
Abreviaturas
- APUESTA:
-
Brunauer-Emmett-Teller
- CNTs:
-
Carbon nanotubes
- CP:
-
Cronopotenciometría
- Cs :
-
Specific capacitance
- CV:
-
Voltamperometría cíclica
- EDLCs:
-
Electric double-layer capacitors
- EIS:
-
Espectroscopia de impedancia electroquímica
- FESEM:
-
Field-emission electron microscope
- NMP:
-
N-methyl-2-pyrrolidone
- NP:
-
Nanoparticle
- PCs:
-
Pseudo-capacitors
- PVDF:
-
Fluoruro de polivinilideno
- Rs :
-
Internal resistance
- SAED:
-
Difracción de electrones de área seleccionada
- SCE:
-
Electrodo de calomelanos saturado
- TEM:
-
Microscopio electrónico de transmisión
- TMOs:
-
Transition metal oxides
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X
- ZW :
-
Warburg impedance
Nanomateriales
- Niobio:un material para innovaciones con gran potencial de futuro
- Nanoesferas de carbono monodispersas con estructura porosa jerárquica como material de electrodo para supercondensador
- Síntesis de material de ánodo de Li4Ti5O12 esférico recubierto de plata mediante un método hidrotermal asistido por sol-gel
- Síntesis controlada de BaYF5:Er3 +, Yb3 + con morfología diferente para la mejora de la luminiscencia de conversión ascendente
- Síntesis fácil y respetuosa con el medio ambiente de nanocables de Co3O4 y su prometedora aplicación con grafeno en baterías de iones de litio
- Sintetizado hidrotermal de microesferas de CoMoO4 como excelente material de electrodo para supercondensador
- Rendimiento energético mejorado basado en la integración con los nanolaminados de Al / PTFE
- Síntesis e investigación de nanocables de CuGeO3 como materiales anódicos para baterías avanzadas de iones de sodio
- Síntesis fácil de esferas de carbono microporoso dopado con nitrógeno para supercondensadores simétricos de alto rendimiento
- Electrodo de estaño amplifica supercondensadores
- El material de electrodo adecuado para su aplicación de soldadura por resistencia



