Nanomateriales de carbono para el tratamiento de agua contaminada con metales pesados y remediación ambiental
Resumen
La nanotecnología es un campo científico avanzado que tiene la capacidad de resolver la variedad de desafíos ambientales controlando el tamaño y la forma de los materiales a nanoescala. Los nanomateriales de carbono son únicos debido a su naturaleza no tóxica, gran área de superficie, fácil biodegradación y remediación ambiental particularmente útil. La contaminación del agua por metales pesados es un problema importante y representa un gran riesgo para la salud humana. Los nanomateriales de carbono están recibiendo cada vez más atención debido a sus propiedades fisicoquímicas superiores que pueden explotarse para el tratamiento avanzado de agua contaminada con metales pesados. Los nanomateriales de carbono, a saber, nanotubos de carbono, fullerenos, grafeno, óxido de grafeno y carbón activado, tienen un gran potencial para la eliminación de metales pesados del agua debido a su gran área de superficie, tamaño a nanoescala y disponibilidad de diferentes funcionalidades, y son más fáciles de modificar químicamente y reciclado. En este artículo, hemos revisado los avances recientes en las aplicaciones de estos nanomateriales de carbono en el tratamiento de agua contaminada con metales pesados y también hemos destacado su aplicación en la remediación ambiental. También se han debatido los aspectos toxicológicos de los nanomateriales a base de carbono.
Introducción
La contaminación se denomina como la presencia de entidades químicas indeseables que impiden el proceso natural o causan efectos adversos a los organismos vivos y al medio ambiente [1, 2, 3]. La industrialización y el inmenso aumento de la población que conduce a una creciente urbanización provocan el aumento de la contaminación a un ritmo alarmante [2, 4]. Mejorar la calidad del agua, el suelo y el aire es un inmenso desafío de la era moderna. La identificación y el tratamiento de los contaminantes ambientales y su prevención es un paso clave en la protección del medio ambiente. La ciencia de los materiales juega un papel vital en la consecución del objetivo ambiental limpio, y la tecnología de la ciencia de los materiales ha progresado exponencialmente en la última década, especialmente los nanomateriales [1, 5]. El agua pura y limpia está escaseando debido a la industrialización, y el mundo se enfrenta a una escasez de agua limpia, especialmente en el mundo en desarrollo [6]. Los contaminantes del agua pueden ser orgánicos, bacterias, virus, colorantes e iones de metales pesados como plomo, cadmio, zinc, níquel, arsénico, cromo y mercurio, cuya naturaleza no biodegradable representa un gran riesgo para la salud humana. Los iones de metales pesados pueden causar muchos efectos adversos como cáncer, daño renal, hepatitis, abortos espontáneos, anemia, encefalopatía y síndrome nefrítico [7,8,9,10]. Los iones de plomo se liberan en el medio ambiente generalmente de las industrias de extracción de metales de las baterías de plomo ácido, del papel, del vidrio y de las industrias de pulido. El cadmio se encuentra generalmente en el agua descargada por el diseño de galvanoplastia de baterías, celdas fotovoltaicas, procesos metalúrgicos y fábricas de telas [11]. Los iones de níquel pueden causar enfermedades de la piel cuando entran en contacto con joyas, cremalleras, relojes, monedas, etc. úlcera de la mucosa nasal [12]. La figura 1 muestra la adsorción de iones de metales pesados en el nanomaterial de carbono (grafeno), y la figura 2 destaca las diferentes fuentes de contaminación por metales pesados en el medio ambiente. Debido a estos efectos adversos graves, la eliminación de iones de metales pesados del agua es de primordial importancia para salvar vidas humanas de estos problemas de salud tan problemáticos. Los iones metálicos tóxicos podrían eliminarse mediante numerosos métodos, como el intercambio iónico, la ósmosis inversa, la filtración por precipitación, la biosorción, la coagulación y la extracción [13, 14]. La adsorción se considera el mejor método, ya que es rentable, altamente eficiente y fácil de operar para eliminar trazas de iones de metales pesados [15]. Se han aplicado diferentes materiales para el tratamiento del agua, como adsorbentes de plantas y materiales de naturaleza orgánica, especialmente ácido húmico, que se ha aplicado ampliamente para la desinfección del agua y para la eliminación de iones de metales pesados [8, 16, 17, 18, 19]. Wang y col. han revisado exhaustivamente el ácido húmico y su nanocompuesto en el tratamiento del agua [20].
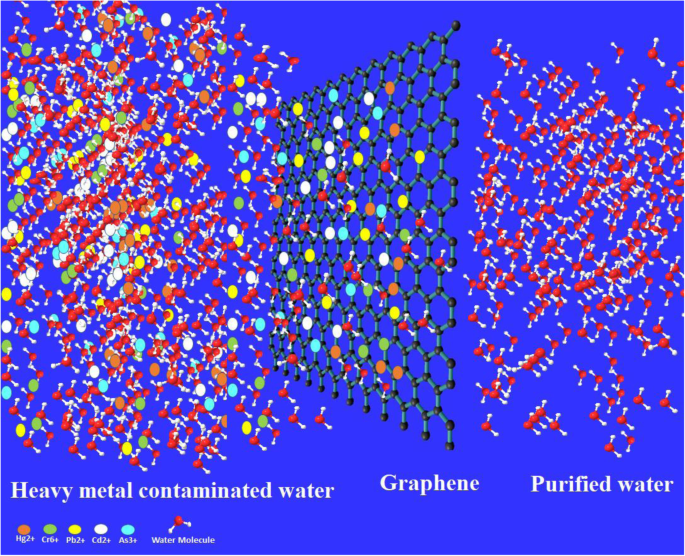
Resumen gráfico que muestra que el proceso de purificación de agua contaminada con metales pesados que utiliza grafeno y otros materiales a base de carbono también puede hacer lo mismo
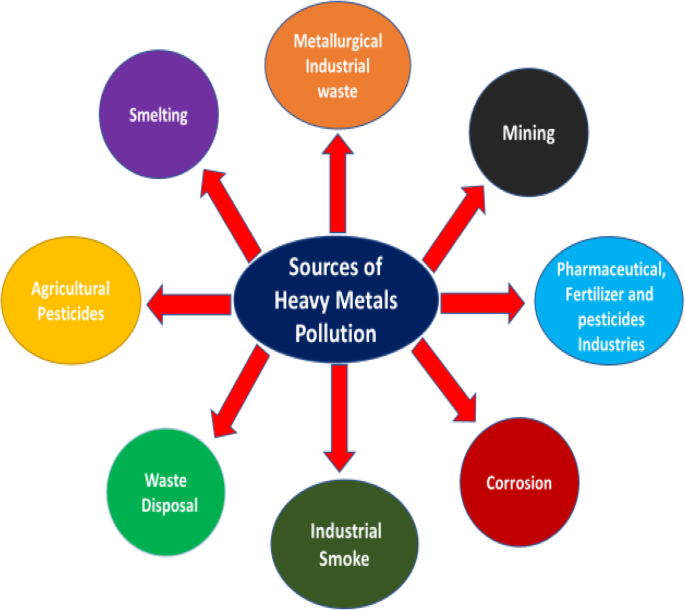
Fuentes de contaminación por metales pesados en el medio ambiente
La plataforma de nanotecnología encuentra aplicación en casi todos los campos, como ciencias ambientales, ciencias de la salud, electrónica, separación industrial, plantas portátiles de tratamiento de agua a gran y pequeña escala, catalizadores, almacenamiento de energía y generación de energía [21,22,23]. Los nanomateriales proporcionan una plataforma especial para la purificación de agua contaminada debido a la gran superficie de los nanoabsorbentes y su capacidad de modificación química y regeneración más fácil. Los nanomateriales se explotan cada vez más para la eliminación de diferentes tipos de contaminantes, a saber, orgánicos, iones metálicos, contaminantes biológicos y arsénico del agua [24, 25, 26, 27]. Los nanomateriales de carbono, a saber, grafeno, óxido de grafeno, nanotubos de carbono, fullerenos y carbones activados, se han utilizado ampliamente en almacenamiento de energía, sensores, electrónica, purificación de agua, administración de fármacos, diagnóstico de enfermedades, etc., debido a sus excepcionales propiedades químicas, mecánicas, térmicas y Características electricas. En este artículo, hemos intentado revisar los últimos avances en la aplicación de nanomateriales de carbono, a saber, fullerenos, nanotubos de carbono (CNT), grafeno, óxido de grafeno y carbón activado en la purificación de agua contaminada con iones de metales pesados.
Salud humana y toxicidad por metales pesados
Los metales pesados suelen definirse en función de sus pesos atómicos; sin embargo, el término metales pesados también se refiere a elementos tóxicos para los seres vivos [28]. Ciertos metales pesados son letales para la salud humana y otros seres vivos en sus diferentes formas y dosis (Tabla 1). Con frecuencia, los metales pesados se consideran tóxicos; sin embargo, los metales más ligeros también pueden ser letales, por ejemplo, el berilio y el litio. No todos los metales pesados son venenosos para la salud, ya que algunos son fundamentales, como el hierro y el Cr (III). Los metales tóxicos más comúnmente conocidos son Pb, Cd, Cr, Mn, Hg, As y metales radiactivos. Los metales radiactivos tienen toxicidad tanto radiológica como química. La toxicidad por metales pesados se ha convertido en una gran amenaza y existen muchos riesgos para la salud asociados con ellos. El impacto letal de estos metales es el hecho de que no tienen ningún papel biológico; sin embargo, pueden imitarse como un elemento del cuerpo e interferir con los procesos metabólicos y biológicos. Algunos metales como el aluminio pueden ser eliminados fácilmente por el sistema de excreción, mientras que ciertos metales se acumulan en la cadena alimentaria y el cuerpo. La toxicidad inducida por metales depende de la dosis, la vía de exposición y el tiempo de contacto (p. Ej., Agudo o crónico). Los detalles de la toxicidad asociada con diferentes metales pesados se dan a continuación.
Toxicidad del mercurio (Hg)
El mercurio (Hg) es un elemento del bloque d con un número atómico 80 y está en forma líquida en condiciones estándar. El mercurio se encuentra en depósitos de sulfuro de mercurio llamados cinabrio. La contaminación por mercurio es causada por las industrias farmacéuticas, la conservación de pulpa y papel, la industria de producción de sosa cáustica, la industria agrícola, etc. [47]. El mercurio es el metal pesado más tóxico en el medio ambiente, y el envenenamiento por mercurio se llama enfermedad rosa también conocida como acrodinia. El mercurio puede combinarse con compuestos orgánicos e inorgánicos. Los niveles elevados de exposición al mercurio en cualquier forma pueden dañar los riñones, el cerebro, el feto en desarrollo, etc. [48]. La agencia de protección ambiental ha declarado que el metilmercurio y el cloruro de mercurio son cancerígenos. La exposición al mercurio también puede causar daño pulmonar, erupciones cutáneas, problemas de memoria y caída del cabello. La Organización Mundial de la Salud (OMS) ha establecido el estándar para el agua potable con niveles más bajos de mercurio a 0.01 mg / l [29].
Toxicidad del plomo (Pb)
El plomo (Pb) es un elemento de número atómico 82 y se considera un metal pesado de apariencia azulada plateada que se torna gris mate por la acción del aire [30]. Existen varias fuentes de contaminación por plomo, principalmente desechos de industrias de baterías, fertilizantes y pesticidas, operaciones de enchapado y acabado de metales, gases de escape, aditivos en la gasolina, pigmentos en automóviles y fundición de minerales. Este metal pesado y tóxico se está convirtiendo en una preocupación para el medio ambiente y la salud en todo el mundo debido a su uso generalizado [31]. El plomo (Pb) es un elemento cancerígeno declarado por la Agencia de Protección Ambiental (EPA). El envenenamiento por plomo es un término utilizado por su toxicidad, y puede ser agudo o crónico. El envenenamiento por plomo puede causar retraso mental, defectos de nacimiento como autismo, alergias, dislexia, parálisis, daño cerebral y daño renal y también puede resultar en la muerte [32].
Toxicidad del arsénico (As)
El arsénico es un elemento metaloide que tiene un número atómico de 33 y se presenta en forma mineral comúnmente en combinación con azufre, algunos otros metales, sales de hierro, calcio, sodio y cobre, y también en forma elemental pura [33]. El agua está contaminada por pesticidas a base de arsénico, depósitos de minerales naturales y eliminación inadecuada de reactivos o productos químicos a base de arsénico. El arsénico en forma de arseniato y arsenito es letal para el medio ambiente y los seres vivos. El arsénico altera el protoplasma de las células al interactuar con el grupo sulfidrilo de las células, lo que provoca un mal funcionamiento de la respiración y afecta la mitosis y las enzimas celulares [34].
Toxicidad del cadmio (Cd)
El cadmio tiene un número atómico de 48 y es un metal blando de color blanco azulado que tiene propiedades químicas similares al mercurio y el zinc del grupo 12 [30]. Se producen a partir de la fundición de sus minerales, galvanoplastia, baterías, plastificantes, aleaciones, pigmentos, industria nuclear y humo de cigarrillos. Generalmente, el cadmio está presente en niveles bajos en el medio ambiente; sin embargo, los desechos industriales han aumentado considerablemente esos niveles. La toxicidad inducida por cadmio puede dañar los riñones, el sistema respiratorio y el esqueleto y es carcinógena para los seres humanos [30, 33]. El cadmio está clasificado como el séptimo metal más tóxico por la Agencia para el Registro de Sustancias Tóxicas y Enfermedades (ATSDR) [34].
Toxicidad del cromo (Cr)
El cromo (Cr) es un elemento de número atómico 24, de aspecto gris acerado [35]. El cromo se presenta en diferentes estados, por ejemplo, estados divalente, tetravalente, pentavalente y hexavalente; sin embargo, las formas trivalente y hexavalente son las más estables. El cromo (III) es un complemento nutricional esencial para humanos y animales [35]. Sin embargo, la forma de cromo (VI) es altamente tóxica y cancerígena por naturaleza [36, 37]. El cromo se produce en matrices ambientales (aire, agua y suelo) a partir de diferentes fuentes, por ejemplo, aguas residuales y aire liberado principalmente por las industrias metalúrgica y química. El cromo hexavalente Cr (VI) es un contaminante industrial establecido como carcinógeno humano [38, 39]. La concentración de Cr (VI) en las aguas subterráneas y superficiales está superando y la Organización Mundial de la Salud (OMS) ha establecido el límite de 50 μg por litro [40].
Toxicidad del zinc (Zn)
El zinc (Zn) es un elemento que tiene un número atómico 30 y se ubica en el grupo 2 de la tabla periódica. Aunque el zinc es un metal traza esencial para los seres humanos, la absorción excesiva de zinc puede suprimir la absorción de hierro. Los iones de zinc son muy tóxicos para las plantas, los peces vertebrados, los invertebrados, etc. [41,42,43].
Clasificación de nanomateriales de carbono según sus dimensiones
Los nanomateriales que tienen las tres dimensiones inferiores a 100 nm se denominan nanomateriales de dimensión cero (0-D); ejemplos son el fullereno y los puntos cuánticos [44]. Los nanomateriales que tienen solo una dimensión mayor de 100 nm y dos dimensiones menores de 100 nm se denominan nanomateriales unidimensionales (1-D), por ejemplo, nanotubos de carbono y titanio [45, 46]. Los nanomateriales cuyas dos dimensiones son superiores a 100 nm se denominan nanomateriales bidimensionales, un ejemplo famoso es el grafeno. Los materiales tridimensionales cuyas dimensiones sean mayores de 100 nm se denominan materiales tridimensionales (3-D); ejemplos son el grafito y algunos compuestos de nanomateriales [46]. La Figura 3 muestra algunos materiales de carbono de estructura famosa representativa con diferentes dimensiones, por ejemplo, fullereno 0-D, nanotubo de carbono de pared simple 1-D, grafeno 2-D y grafito 3-D.
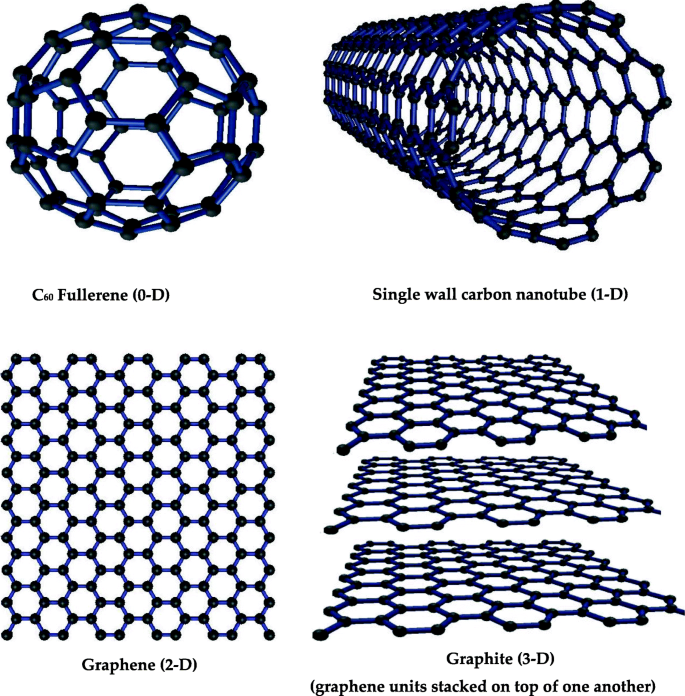
Los ejemplos de nanomaterial de carbono de diferentes dimensiones
Aplicación de fullerenos en la remediación ambiental y la purificación de agua
Los fullerenos fueron descubiertos en 1985 a partir del polvo interestelar y tienen una estructura de anillo hexagonal y pentagonal enjaulada cerrada, representada con la fórmula de C 20 + m donde m es un número entero [49]. Tienen un carácter hidrófobo, alta afinidad electrónica y alta relación superficie / volumen, y defectos superficiales. Estas propiedades fisicoquímicas únicas los convierten en un material ideal para diversas aplicaciones, como semiconductores, electrónica, ciencias biomédicas, células solares, sensores, cosméticos, fotosíntesis artificial y revestimientos de superficies [50,51,52]. Brunet y col. mostró que los fullerenos funcionalizados hidrófilos (C 60 ) también se han aplicado para matar los microorganismos patógenos en el agua mediante la utilización de un proceso fotocatalítico. Los fullerenos también son materiales ecológicos limpios ideales para el almacenamiento de hidrógeno, ya que las moléculas de fullereno se pueden convertir fácilmente en enlaces C – C en C – H debido a las energías de enlace más bajas del carbono y el hidrógeno [27]. Se ha informado que los fullerenos tienen el almacenamiento máximo de 6,1% de hidrógeno debido a su química y estructura molecular de jaula, y la estructura del fullereno puede revertirse fácilmente debido a las energías de enlace C-C más altas [3, 53, 54]. Se aplican capas conductoras de carbono sobre la superficie del electrodo de los supercondensadores, y su capacitancia depende del área de la superficie, la distribución del tamaño de los poros y la conductividad eléctrica [55, 56]. Los nanomateriales a base de carbono proporcionan una conductividad eléctrica más alta que los materiales ortodoxos disponibles debido a la mayor área de superficie [57]. Se ha informado que los materiales compuestos a base de fullereno muestran una capacitancia específica más alta de 135,36 Fg - 1 que el material de grafeno puro que no se hibridó con fullereno. Además de esto, el compuesto a base de fullereno mostró una mejor tasa de tiempo de retención del 92,35% incluso después de un círculo de carga / descarga de 1000 [58]. Los fullerenos también se han utilizado en baterías de iones de litio como ánodo y proporcionan una mejor eficiencia con el reemplazo de ánodos metálicos no degradables, demostrando así ser beneficiosos en términos de eficiencia y un material ecológico. Las propiedades fisicoquímicas de los fullerenos también los convierten en candidatos adecuados para la extracción de diferentes especies de los medios acuosos [59, 60]. Pickering y col. diseñó compuestos de fullereno solubles en agua y los aplicó con éxito como sensibilizador para producir especies reactivas de oxígeno (ROS) en el agua tras la irradiación de radiaciones visibles y ultravioleta. Los ROS pueden fotodegradar los contaminantes orgánicos en el agua y, además, los fullerenos solubles en agua (fulleroles) también actúan como antioxidantes. Lo más importante es que los fulleroles se pueden eliminar fácilmente del agua después de realizar la función de fotodegradación [53].
Se cree que los fullerenos adsorben especies por la penetración de adsorbatos en los espacios / defectos entre los nanoclusters de carbono, y además de los defectos, la menor tendencia a la agregación y la gran superficie los hacen útiles nanomateriales para ser aplicados para la adsorción de iones de metales pesados de agua [61, 62]. Alekseeva y col. realizó estudios comparativos de fullereno y película de nanocompuesto de poliestireno para la eliminación de Cu 2+ iones encontraron que los fullerenos mostraban una mejor eficiencia [60]. También han descubierto que los fullerenos siguen el modelo de adsorción de Langmuir para Cu 2+ iones [60]. Establecieron que el Cu 2+ La eficiencia de eliminación de los fullerenos es mayor en el primer caso, y la isoterma de equilibrio del Cu 2+ la adsorción en el fullereno se ajusta al modelo de Langmuir. Aunque los fullerenos tienen un gran potencial para la aplicación de adsorción de agua, su costo es demasiado alto, lo que restringe su utilización. Sin embargo, las trazas de fullerenos pueden usarse para fabricar otros materiales como carbón activado, lignina y zeolitas para aumentar su eficiencia de adsorción [63]. La fabricación de fullereno aumenta el carácter hidrófobo que hace que los materiales se apliquen mejor en la adsorción y también ayuda a facilitar el reciclaje [64]. Se ha informado que se forma material antibacteriano injertando fullereno C 60 con polivinilpirrolidona (PVP) que tiene el potencial de aplicarse en la desinfección del agua. La tecnología de membranas recibe cada vez más atención en la purificación de sales, materias orgánicas, partículas y gases del agua. El rendimiento de la membrana depende de la composición del material, ya que es responsable de la reactividad, la selectividad y la resistencia mecánica. Los fullerenos tienen un gran potencial para aplicarse en la tecnología de membranas debido a su fácil funcionalización, alta afinidad electrónica, gran resistencia, capacidad para adaptar el tamaño, etc. Los fullerenos pueden ser útiles para injertar los nanoadsorbentes para mejorar su eficiencia de adsorción.
Biocompatibilidad de fullerenos
Los nanomateriales basados en fullereno se han explotado para aplicaciones biomédicas y diferentes estudios han revelado su biocompatibilidad con organismos vivos. Se ha utilizado como biorreceptor y biosensor y también se ha explotado en ingeniería biomédica, y se ha informado que es biocompatible con sistemas vivos [65,66,67,68,69]. El fullereno es un material no tóxico que se puede explotar para filtración, adsorbentes y membranas para aplicaciones ambientales y de tratamiento de agua.
Nanotubos de carbono (CNT)
Los nanotubos de carbono fueron descubiertos por Lijima en 1999, y pueden ser de una sola pared (SWCNT), por ejemplo, grafeno enrollado en capas, o nanotubos de carbono de paredes múltiples (MWCNT), por ejemplo, grafeno enrollado multicapa [70]. Los CNT han sido el foco de la investigación en nanotecnología desde su descubrimiento debido a sus propiedades fisicoquímicas únicas. Estos alótropos de nanoestructura cilíndrica de carbono se están aplicando en electrónica, semiconductores, emisión de campo, almacenamiento de energía, catálisis, filtros biomédicos, de aire y agua, etc. Su diámetro puede ser de 1 nm a varios nanómetros con una gran superficie específica (150– 1500 m 2 / g), y poseen mesoporos que los convierten en candidatos ideales para la eliminación de iones de metales pesados por adsorción [71, 72]. Además de esto, los NTC se pueden funcionalizar fácilmente con diversas moléculas orgánicas que pueden hacerlos específicos para la selección de adsorbatos y se podría mejorar su capacidad de adsorción [73]. El mecanismo de sorción de metales pesados por los NTC se basa en la característica de la superficie, el potencial electroquímico y el proceso de intercambio iónico [11, 73].
Aplicación medioambiental de CNT / tecnología ecológica basada en CNT
Hay un inmenso aumento en la demanda mundial de energía y se realizan muchos esfuerzos para desarrollar un material simple, económico y ecológico para tecnologías confiables para materiales de recursos energéticos. La energía solar se produce mediante conversión eléctrica solar y conversión térmica solar [74]. Sin embargo, la baja eficiencia de la conversión térmica en los colectores solares es el principal obstáculo.
Los nanofluidos de carbono se están aplicando ampliamente en la conversión solar térmica debido a su buen rendimiento como absorbentes solares [75]. Las células fotovoltaicas basadas en nanotubos de carbono (PVC) recibieron mucha atención de los científicos, ya que pueden ser semiconductores de tipo p con excelente movilidad y su combinación con donantes de electrones es una idea nueva y única [76, 77]. Los dispositivos fotovoltaicos orgánicos pueden diseñarse fácilmente mediante la fabricación de CNT con polímeros [78]. Se han diseñado células solares basadas en heterouniones CNT -Si (p-n) que dan como resultado películas conductoras y transparentes excelentes. Además de esto, también se ha informado de CNT con arseniuro de galio tipo n (n-GaAs) con una mejor eficiencia del 3,8% para láser verde y lámpara de escritorio [79]. Los CNT también han sido ampliamente explotados como dispositivos de almacenamiento de energía que funcionan según los principios de los condensadores electroquímicos de doble capa (EDLC) como los ultracondensadores [80]. La incorporación de CNT en electrodos de ultracondensadores dio como resultado una gran mejora en la vida útil de más de 300.000 ciclos [81]. Además de esto, los CNT de supercondensadores también se han utilizado en diodos en lugar de transistores convencionales, ya que pueden hacer uniones p-n perfectas debido a sus excelentes propiedades mecánicas y eléctricas [58]. Los CNT también se han utilizado ampliamente en la tecnología avanzada de sensores, ya que pueden mejorar la sensibilidad, la selectividad, el tiempo de respuesta, la rentabilidad y la vida útil del químico y los biosensores [90]. Estos resultados sugieren que mejores CNT son materiales ideales con excelente movilidad y mejor eficiencia sin impacto negativo en el medio ambiente, lo cual es un gran inconveniente con los materiales de tipo p de base metálica más comúnmente aplicados.
Aplicación de CNT en fotocatálisis
La fotocatálisis es una de las tecnologías avanzadas que se están aplicando para el tratamiento de aguas residuales que utiliza semiconductores [82]. Se está aplicando una variedad de materiales semiconductores, a saber, Fe 3 O 4 , ZnO y TiO 2 ; sin embargo, la eficiencia cuántica de estos materiales no es alta y, además, su fotorespuesta ultravioleta también es lenta [83]. Los CNT son materiales avanzados prometedores para la catálisis debido a su eficiencia cuántica mejorada, tamaño nanométrico, alta estabilidad química, estructura de tubo hueco y región de adsorción de luz extendida debido a su gran área de superficie específica [84]. Gao y col. diseñado SWCNTs-TiO 2 basados en fotocatalizadores de red ultradelgados y se aplicó con éxito para la purificación de agua a partir de aceite [85]. Park y col. decoró titania en aerogel de SWCNT y se aplicó con éxito para la eliminación del azul de metileno del agua [86]. Zhao y col. MWCNTs-TiO 2 fabricados y solicitó la fotodegradación del azul de metileno [87]. Xu y col. fotocatalizadores diseñados mediante la combinación de hidroxi-MWCNT y PbO 2 ánodo nanocristalino y lo aplicó con éxito para la eliminación de piridina del agua [88].
SWCNT en la purificación de agua contaminada con metales pesados
Los SWCNT son nanomateriales de carbono unidimensionales (1-D) formados por un tubo hueco con paredes de un átomo de espesor. Este material 1-D exhibe propiedades fisicoquímicas excepcionales debido a su estructura única. Los SWCNT se están aplicando ampliamente en diferentes campos, como los semiconductores, la electrónica, las ciencias biomédicas, la química y los biosensores [44, 89,90,91,92,93]. Los SWCNT también se utilizan ampliamente para el control de la contaminación ambiental debido a su estructura porosa, área de superficie alta, funcionalización de superficie más fácil y tamaño nanométrico. Estas propiedades de los SWCNT son muy prometedoras para su aplicación en el tratamiento del agua. Alijani y col. diseñó nanocompuestos basados en SWCNT fabricándolos con sulfuro de cobalto y magnetita, y los nanocompuestos resultantes se aplicaron para la eliminación de mercurio; los resultados mostraron una alta adsorción de más del 99,56% en un período más corto de 7 min [94]. En comparación con esto, se encontró que los SWCNT por sí solos adsorben un 45,39% de mercurio [94]. Anitha y col. llevó a cabo una simulación dinámica molecular de SWCNT desnudos y sus contrapartes funcionalizadas, por ejemplo, SWCNTs-OH, SWCNTs-NH 2 y SWCNTs-COOH para las capacidades de adsorción de iones de metales pesados, por ejemplo, Cd 2+ , Cu 2+ , Pb 2+ y Hg 2+ de medios acuosos. Los resultados revelaron que los SWCNTs-COOH tienen mucha capacidad de adsorción de aproximadamente un 150–230% más en comparación con los SWCNT desnudos. Se encontró que los SWCNTs-OH y los SWCNTs-NH tenían una adsorción débil, ya que solo mostraban un 10-47% más de adsorción en comparación con los SWCNT [95]. También se ha informado de SWCNTs-COOH para la adsorción de Pb 2+ , Cu 2+ y Cd 2+ iones con capacidad de adsorción de 96,02, 77,00 y 55,89 mg / g, respectivamente. En comparación con esto, se encontró que los SWCNT no funcionalizados adsorben 33.55, 24.29 y 24.07 mg / g, para el Pb 2+, Cu 2+ y Cd 2+ iones respectivamente [96]. Zazouli y col. diseñó nanocompuestos SWCNT funcionalizándolos con l-cisteína. Aplicaron los nanocompuestos diseñados para la eliminación del mercurio del agua. Se encontró que la eficiencia de adsorción de las SWCNTs-cisteína diseñadas era del 95% [97]. Gupta y col. diseñó una membrana basada en nanocompuestos de SWCNTs-polisulfona y se aplicó para la eliminación de metales pesados. La incorporación de SWCNT dio como resultado una reducción en el tamaño de los poros de la membrana y una superficie más lisa. Se encontró que la membrana diseñada mostraba una alta capacidad de rechazo de iones metálicos y eliminó el 96,8% de Cr + 6 , 87,6% como + 3 y 94,2% Pb + 2 iones. La membrana sin SWCNT mostró solo 30,3%, 28,5% y 28,3% de rechazo para Cr + 6 , Como + 3 y Pb + 2 iones respectivamente. Estos resultados muestran la mejora en la eficiencia de la membrana debido a la incorporación de SWCNTs [98]. Dehghani y col. SWCNT aplicado para la eliminación de Cr + 6 iones del agua y evaluó el efecto de diferentes parámetros, por ejemplo, tiempo de contacto, pH inicial y Cr + 6 inicial concentración de iones en la capacidad de adsorción. Se observó que la eficiencia de la adsorción dependía del pH, la eficiencia máxima se encontró a un pH de 2,5 y la adsorción sigue el modelo de isoterma de Langmuir [99]. Estos estudios sugirieron que los nanotubos de carbono de pared simple son adecuados para el tratamiento de agua contaminada con metales pesados.
MWCNT en la purificación de agua contaminada con metales pesados
Los nanotubos de carbono que tienen múltiples capas laminadas de grafeno se denominan nanotubos de carbono de paredes múltiples (MWCNT), como se muestra en la Fig. 4. Los MWCNT exhiben propiedades únicas como alta área de superficie, alta conductividad eléctrica, térmica y alta resistencia a la tracción [100]. Debido a estas propiedades fisicoquímicas, se aplican ampliamente en electrónica, células solares, sensores y ciencias biomédicas [101,102,103]. Los MWCNT también se han aplicado ampliamente en el tratamiento de agua, y especialmente los iones de metales pesados se adsorben por interacción química con grupos funcionales de MWCNT. Se ha informado que los MWCNT oxidados tienen una alta capacidad de adsorción y eficiencia para Cr 6+ , Pb 2+ y Cd 2+ iones del agua [104, 105]. La adsorción de iones metálicos también depende del valor de pH, y esta propiedad se puede aplicar para la desorción de iones cambiando el pH, y los MWCNT se pueden reutilizar. Algunos estudios han revelado que los MWCNT oxidados con plasma tienen mejores propiedades de adsorción que los oxidados químicamente; esto puede atribuirse a un mayor número de grupos funcionales oxigenados presentes en la superficie de los nanotubos de carbono. Además, se ha informado que los MWCNT oxidados con plasma se pueden reciclar y reutilizar fácilmente [72, 106].
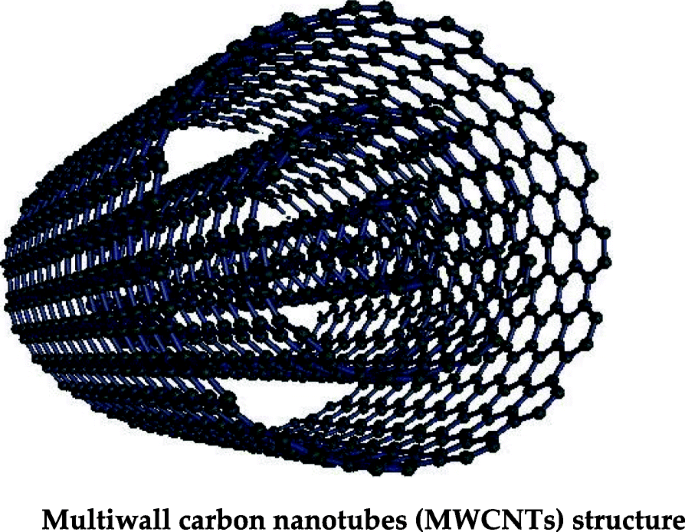
Estructura de nanotubos de carbono de paredes múltiples (MWCNT)
El material compuesto de MWCNT también se ha utilizado para la adsorción de iones de metales pesados del agua. El MWCNTs-Fe 2 O 3 , MWCNTs-ZrO 2 , MWCNTs-Fe 3 O 4 , MWCNTs-Al 2 O 3 y MWCNTs-MnO 2 -Fe 2 O 3 Se han aplicado con éxito nanocomposites para la eliminación de iones pesados de Cr 6+ , Como 3+ , Ni 2+ , Pb 2+ y Cu 2+ iones de agua [107,108,109,110]. Las condiciones experimentales de las soluciones, incluido el pH y las concentraciones de iones metálicos, pueden afectar las características de adsorción de los MWCNT, y el modelo de adsorción de Freundlich está satisfecho con sus datos experimentales [81, 111]. La eficiencia de adsorción de los MWCNT funcionalizados aumentó en comparación con otros materiales de óxidos orgánicos, y también se predice que los MWCNT funcionalizados son 20 veces más efectivos en la adsorción de iones metálicos que los MWCNT no oxidados [112]. En general, se cree que los enlaces de iones y la aparición de nanotubos de carbono en la superficie polar son el principal mecanismo de sorción [113, 114]. Los MWCNT oxidados también han demostrado una capacidad de sorción y una eficiencia excepcionalmente altas para Pb 2+ , Cd 2+ y Cr 6+ del agua. La eficacia de sorción de los MWCNT con tratamiento ácido aumenta el potencial para eliminar los iones de plomo, cromo y cadmio con un grupo funcional de oxígeno formando complejos de iones o precipitados de sales en las superficies [115]. Adsorption of MWCNTs treated with concentrated HNO3 increases significantly mainly due to oxygen functional groups created on the surface of acidified nanotubes that can react with metal ions to form complex or salt precipitates on the surface. The MWCNT composites with certain compounds like iron (III) oxide, zinc oxide, and aluminum oxide are formed by a coprecipitation method, and resulting composites are successfully applied for the removal of chromium, nickel, lead, copper, and arsenic ions. The adsorption efficiency of these nanocomposites was found to be dependent on the pH value and temperature, and the sorption process can be accomplished by changing these parameters [116, 117]. Depending on the pH and temperature, the sorption capacity of these composites varied from 10 to 31 mg/g. The adsorption process for these nanocomposites was well described by the Langmuir model [118]. The nanocomposites of oxidized multiwalled MWCNTs with manganese oxide/iron (III) oxide are reported to remove Cr 6+ ions with maximum adsorption capacity of 186.9 mg/g with the maximum removal capacity of 85% at the optimum pH 2.1 studies. Their promising adsorption was due to the surface polarity of the adsorbents. It has also been reported that plasma-oxidized MWCNTs are better in adsorption compared to chemically oxidized ones as the prior ones have more oxygenated functional groups [119]. Plasma-oxidized technique has also been reported for the formation of nanotubes with titanium oxide and manganese dioxide and utilized for the removal of lead ions from water. The results showed that these hybrid systems can act as an effective adsorbent for the lead ions in the first case; the adsorption capacity was 137 mg/g, and in the second case, it was 78.74 mg/g [120]. In a heterogeneity adsorbent surface, sites combined twice are fitted in the isotherms models of the Langmuir-Freundlich equation that was used to differentiate between two types of adsorption sites with greater and lesser energy affinities for the Ni 2+ ions [121]. It is believed that nickel ion sorption mainly occurs at the sites of energy with modified nanocomposites of MWCNTs and the nano-modification leads to a 20% increase in the adsorption capacity at small (up to 0.1 mol/l) equilibrium adsorbate concentrations. Another modification reported for MWCNTs is their functionalization with hydroxyquinoline and their application for the removal of copper, lead, cadmium, and other toxic ions [122]. The carbon nanotubes alone as well as in their oxidized and in their composite forms have tremendous ability to adsorb the heavy metal ions, and a lot of research is in progress for their applications in purification of water. Elsehly et al. applied commercial MWCNTs for the removal of the manganese and iron which could reach 71.5% and 52% respectively with a concentration in aqueous solution of 50 ppm of these metal ions [123]. In another study, CNT-based nanocomposites have been applied for the removal iron and manganese from the water [124].
Biocompatibility of CNTs
Carbon nanotubes have great potential to be applied for multidisciplinary fields like drug delivery, diagnosis, biosensors, electronics, semiconductors, and environmental remediations [125]. Different studies revealed the biocompatibility of CNTs as it has been widely exploited for biomedical applications [126, 127]. Carbon-based materials like CNTs are safe to be applied for the environmental remediation and in particularly for water treatment.
Graphene Based Material for Environmental Remediation
Graphene-based material for the adsorption of gaseous contaminants
Carbon dioxide (CO2 ) has been the environmental concern because of its immense effect in global warming [128]. Nanomaterials have been found to be promising materials as compared to conventional materials both with respect to cost and efficiency [129]. Graphene-based materials have been utilized for the adsorption of gaseous contaminants [130]. Gosh et al. showed the successful application of graphene-based nanomaterials for the capture of CO2 y H 2 . A single layer of graphene has been reported to capture 37.93% of CO2 [130]. Graphene has been reported to selectively adsorb CO2 as compared to methane (CH4 ) and nitrogen (N2 ) gases. Selectivity of graphene oxide (GO) for CO2 can be attributed to higher dipole moment of carbon dioxide which can easily interact with polar oxygenated functional groups of CO2 [74, 131]. Other studies have also been reported for tuning the graphene chemistry for the improved selectivity of the desired gaseous contaminant [75, 131].
Graphene Oxide in Removal of Organic Dyes from Water
Graphene-based nano-adsorbents are excellent advanced materials for the removal of the organic contaminants from the water because of their nano-scaled size, high surface area, ability to interact via pi-pi stacking, hydrogen bonding, and electrostatic interactions [26]. In comparative adsorption studies of GO and graphite using methylene blue and malachite green as standard organic dyes, it was found that GO showed much better adsorption than graphite [26]. GO has also been utilized for the removal of cationic dyes namely methylene blue (MB), crystal violet (CV), and rhodamine B (RhB) from water. It was found that the higher the initial dye concentration, the higher will be the adsorption with adsorption capacities of 199.2, 195.4, and 154.8 mg g −1 for MB, CV, and RhB, respectively [76]. GO has also successfully applied for the removal of anionic dyes like Acid Orange 8 (AO8) and Direct Red 23 (DR23) from aqueous solutions [77].
Graphene-Based Photocatalytic Materials for Water Decontamination
Although adsorption can remove the contaminant from water, the adsorption technique is unable to destroy/degrade the contaminants and disposal step is required [77]. Photocatalysis is a useful approach for water remediation/wastewater treatment for the complete degradation and mineralization of organic/biological contaminants [78]. Graphene-based photocatalysts have been reported for their improved activity because of their high surface area, nanosize, and more electronic movements as compared to the traditionally used materials [78, 132]. Rommozzi et al. designed reduced graphene oxide (rGO) with a greener reduction method using glucose and ammonium hydroxide and successfully designed a photocatalyst which is visible by the fabrication with TiO2 . The designed rGO-TiO2 photocatalyst was successfully applied for the refractory dye named Alizarin Red S (ARS) [133]. In other studies, graphene oxide fabricated with TiO2 and ZnO exhibited much photodegradation of methylene blue as compared to TiO2 /ZnO alone [79, 80].
Graphene and Graphene Oxide-Based Adsorbents for the Purification of Heavy Metal-Contaminated Water
Graphene is one-atom-thick-layered hexagonal lattice of carbon atoms and is known as the thinnest material with the strength of 200 times than steel. Graphene was discovered in 2004 by Sir Andre Geim and Sir Konstantin Novoselov, who were awarded a Nobel prize for their discovery in 2010. Graphene (2-D) is being used widely in almost every field such as in touch screens, mobiles, LCDs, semiconductors, computer chips, batteries, energy generation, water filters, supercapacitors, solar cells, and biomedical and environmental sciences [134,135,136,137]. These 2-D graphene-based materials are getting more and more attention in water treatment due to their unique physicochemical characteristics namely electronic properties, high surface area, thermal mobility, high mechanical strength, and tunable surface chemistry [118, 134, 138, 139]. Tabish et al. designed porous graphene and applied it as an adsorbent for the removal of heavy metal ions as well as other pollutants from water. They applied this porous graphene material for As 3+ removal from water and found 80% efficiency. The material was found to retain its water treatment properties after regeneration and recycling [138]. Guo y col. designed a nanocomposite of partially reduced graphene oxide by its fabrication with Fe3 O 4 via in situ co-precipitation method and applied it for the removal of Pb 2+ ions from water. The designed nanocomposite was found to be excellent in removing the Pb 2+ ions from aqueous solution with an adsorption capacity of 373.14 mg/g [140]. Zhang y col. functionalized the reduced graphene oxide with 4-sulfophenylazo (rGOs) and applied it for the removal of a variety of heavy metal ions from aqueous solution. The designed material showed the maximum adsorption capacity of 689, 59, 66, 267, and 191 mg/g for the Pb 2+ , Cu 2+ , Ni 2+ , Cd 2+ , and Cr 3+ respectively [141]. Diana et al. designed a graphene-based self-propelled microbot system whose structure was made up of nanosized multilayered consisting of graphene oxide, nickel, and platinum. Each layer performed a different function, e.g., graphene oxide captures the heavy metal Pb 2+ ions, the middle layer of Ni enables the control of microbots with the help of external magnetic field, and the inner layer of platinum helps the engine in self-propelling [142]. The designed system was found to remove the 80% of the Pb 2+ water solution. Figure 5 shows the schematic illustration of the working principle of microbots. Yang y col. designed hydrogen beads using graphene oxide and sodium alginate (GO-SA) and successfully applied them for the removal of Mn 2+ ions from the aqueous solution with excellent adsorption capacity of 56.49 mg/g [9]. Zheng y col. designed nanocomposites by fabrication of zinc oxide with tea polyphenol with reduced graphene oxide (TPG-ZnO). Designed material was applied for the removal of heavy metal ions with an added advantage of antibacterial properties [143]. They applied this material for the removal of Pb 2+ ions from aqueous solution with adsorption efficiency of 98.9%, and the adsorbent was found to possess antibacterial properties against Streptococcus mutans with 99% eradication [143]. Mousavi et al. designed nanocomposites of graphene oxide with iron oxide magnetite nanoparticles Fe3 O 4 and applied them for the removal of Pb 2+ ions from water and the material showed 98% removal efficiency with a capacity of 126.6 mg/g [144]. Considering functionalized graphene as an adsorbent to remove Pb 2+ ions from an aqueous medium, the highest record of Pb 2+ ion removal over graphene is 406.6 mg/g at pH of 5.0 in 40 min [145]. Graphene-hydrogel lingo sulfonate functionalized nanocomposites having oxygenated functional groups making the surface highly polar reported to increase the rate of adsorption of Pb 2+ ions with maximum efficacy of 1308 mg/g with the equilibrium reached in 40 min. Awad et al. modified graphene oxide with chloroacetic acid (GO-COOH) and ethylenediamine (GO-amino). The designed systems were applied for the removal of mercury (Hg 2+ ) from water and found that the nanocomposites (GO-COOH) and (GO-amino) have an adsorption capacity of 122 mg/g and 230 mg/g. In addition to this, designed systems retained their adsorption efficiency after the recycling process [146]. Yan y col. designed magnet graphene oxide for the rapid removal and separation of Fe (II) and Mn (II) from micropolluted water [147]. Ali et al. designed graphene-based adsorbent successfully for the removal of noxious pollutants namely Cu (II), Pb (II), Fe (II), and Mn (II) [148].
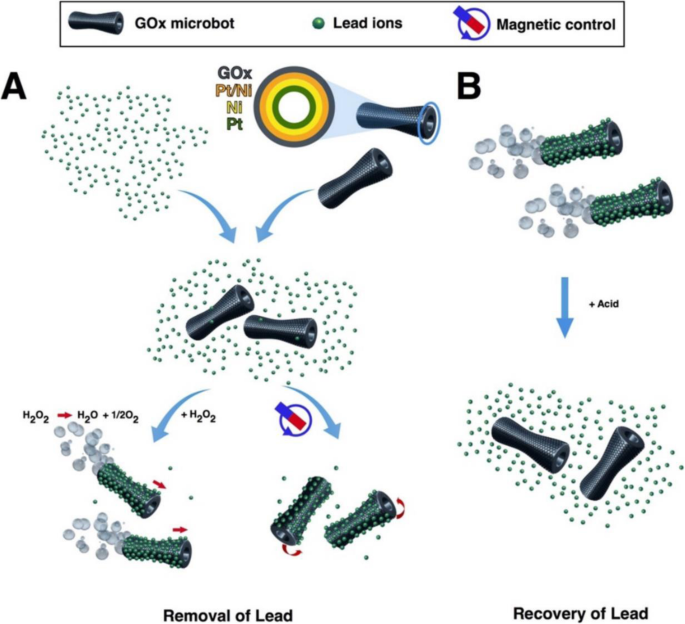
Scheme of GOx-microbot-based approach for lead decontamination and recovery. un Decontamination of polluted water using GOx-microbots fabricated by electrodeposition of nanolayers of graphene oxide (GOx), Pt/Ni layer, Ni magnetic layer, and Pt catalytic inner layer. The decontamination strategy for lead ions can be carried out by two different techniques:self-propulsion of the GOx-microbots in the presence of H2 O 2 or by using an external rotating magnetic field. b Recovery of lead ions from the GOx-microbots in the presence of acidic media [117]
Biocompatibility of Graphene-Based Nanomaterial
Graphene-based nanomaterials have been applied in different fields like electronics, chemical sensors, biosensors, drug delivery, theragnostic, and other related biomedical fields. These studies also report the cytocompatibility of graphene-based materials both by in vitro as well as in vivo animal studies [122, 133, 149,150,151,152]. These findings suggest that the graphene-based materials are safe for the environmental remediation application as they are just used for the removal and degradation of pollutants and are not consumed by humans directly.
Activated Carbon in Environmental Remediation
Activated carbon is a fabulous material because of its high surface area, highly porous structure, and ease of preparation with variety of starting materials. Because of its ideal physicochemical properties, it has wide application in environmental remediations in different industries like pharmaceutics, fertilizer plants, petroleum, cosmetics, automobiles, and textiles [153] It is also widely applied for the adsorption of gases, solvent recovery, and wastewater treatment especially for the removal of organic dyes/other pollutants; not only this, but it is also used as a catalyst in biodiesel production. It is also applied as a low-cost material for the treatment and removal of water containing COD, BOD, and TSS and stabilizing and maintaining the optimum pH for biological uses [154,155,156]. Maguana et al. prepared activated carbon from the pear seed cake and successfully applied it for the removal of methylene having an adsorption capacity of 260 mg/g [157]. Antonio et al. prepared activated carbon from the kenaf plant and applied it successfully for the treatment of the wastewater of hospitals containing paracetamol as the main pollutant [158]. The above literature suggests that the activated carbon is the pretty useful economical material which can easily be prepared and it has immense application in environmental remediations.
Activated Carbon as Adsorbents in the Purification of Heavy Metal-Contaminated Water
Activated carbon (AC) is also known as activated charcoal, and this of type carbon material is formed under some treatment protocols resulting in micro/nanopores and having the large surface area of more than 3000 m 2 [159]. The AC is produced on a large scale from coal, wood, and agricultural wastes [160]. In addition to its porous nature (as shown in Fig. 6), AC also has a high mechanical strength which enables its applications in catalyst support, capacitors, electrodes, and gas storage and most importantly used as the adsorbent for removal of metal ions, organic wastes, and gases from water [160,161,162]. The high mechanical strength of activated carbon enables its periodic cleaning, regeneration, and reutilization [160]. Abeer et al. reported the preparation of AC from apricot stone and its application in removal of Zn + 2 and Al + 3 ions with removal efficiency of 92% [163]. Ebrahim et al. designed AC from sewage sludge, applied it for the removal of Cu + 2 ions from water, and found that the designed material showed maximum adsorption capacity of above 50% [164].
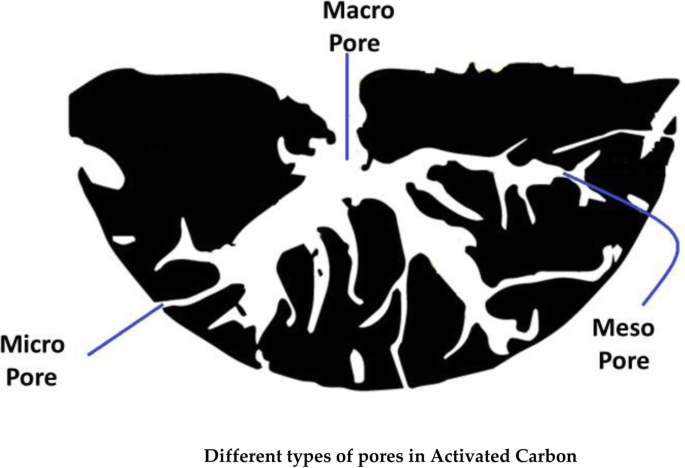
Different types of pores in activated carbon
Li y col. prepared the AC from sewage sludge produced from the wastewater treatment plant and functionalized it with sulfur [165]. They applied sulfonated AC for the removal of Pb 2+ , Cd 2+ , Cu 2+ , and Ni 2+ ions from water. The adsorption capacity of metal ions were found to be 238.1 mg/g, 96.2 mg/g, 87.7 mg/g, and 52.4 mg/g for Pb 2+ , Cd 2+ , Cu 2+ , and Ni 2+ respectively [165]. Cao y col. designed multipore activated carbon (MPAC) with a large surface area using the agricultural waste of long-root Eichhornia crassipes and applied it for removing heavy metal ions, e.g., Pb 2+ , Cd 2+ , Cu 2+ , Ni 2+ , and Zn 2+ . They found that at 30 °C adsorption capacity being 1.34 mmol/g, 1.07 mmol/g, 1.22 mmol/g, 0.97 mmol/g, and 0.93 mmol/g for Pb 2+ , Cd 2+ , Cu 2+ , and Ni 2+ respectively [166]. Dong y col. investigated the application of spent activated carbon (AC) for heavy metal ion removal from water and found high adsorption capacity of 95% and 86% for Pb 2+ and Cd 2+ ions respectively [167]. M. Bali et al. [168] applied commercial AC for the removal of heavy metal ions and found that adsorption equilibrium of Cd 2+ ion took 15 min while for Pb 2+ , Zn 2+ , and Cu 2+ it took 45 min with percentage removal of 64% for all these ions and with Cd 2+ being the highest [10]. Kongsuwan et al. prepared the activated carbon from the agricultural waste of eucalyptus bark. They applied it for the removal of Cu 2+ and Pb 2+ from water with maximum removal capacity of 0.45 and 0.53 mmol per gram of AC respectively, with adsorption being the main mechanism of ion uptake [169]. AC poultry litter has also been reported and applied for the treatment of heavy metal-contaminated water and found that for 1 kg of poultry litter AC adsorbs 404 mmol, 945 mmol, 236 mmol, and 250–300 mmol of Cu 2+ , Pb 2+, Zn 2+ , and Cd 2+ ions respectively [170]. This adsorption is significantly higher than the commercially available AC derived from coconut and bituminous. The AC of wood saw dust of rubber plant has also been reported for the removal of heavy metal ions of Cr + 6 from water with adsorption capacity of 44 mg/g [171]. AC formed from Moso and Ma bamboo was found to be highly efficient in removing the heavy metal ions, i.e., Pb 2+, Cu 2+ , Cr 3+ , and Cd 2+ with the maximum adsorption capacity of more than 90% removal [172]. Naser et al. prepared AC from rice husk and applied them for the removal of Cu 2+ from aqueous solution, and maximum capacity was found to be 33.92%. Similar results have also been reported for the removal of Cu 2+ from the AC formed from Palm shell [173]. AC of love stones has been reported for the adsorption of Cd + 2 and Ni + 2 with adsorption capacity of 1.85 mg/g and 0.67 mg/g respectively in two different studies [174, 175]. AC prepared from olive stone using the microwave method has been applied for the removal of Fe 2+, Pb 2+, Cu 2+, Zn 2+, Ni 2+ , and Cd 2+. from wastewater. Another study reported on the olive stone AC prepared via microwave to remove a group of metal ions from synthetic wastewater:Fe 2+ , Pb 2+ , Cu 2+, Zn 2+ , Ni 2+ , and Cd 2+ with removal efficiency of more than 98% [176]. Tamarind wood AC has been reported for the highest adsorption capacity of above 97% for Pb 2+ from water [177]. Activated carbon has been applied as an adsorbent for the removal of Fe (II) and Mn (II) with great efficiency [178, 179]. The activated carbon is easy to synthesize, is cheaper, and is the most promising material for the adsorption of heavy metal ions and can be prepared at a large scale from a variety of carbon sources especially form agricultural waste. In addition to easier preparation, AC can easily be functionalized. Table 2 summarizes the effect of different parameters on the process of metal ion adsorption.
Biocompatibility of the Activated Carbon
Different studies have been conducted for the biocompatibility evaluation of the activated carbon materials prepared form different carbon sources. Activated carbon has been applied for the treatment of cystitis and was found to be effective and nontoxic compared to the antibiotics being applied [180]. Biocompatibility of activated carbon can be attributed to its inertness, and it has also been functionalized and fabricated with other materials to confer on the disinfection properties [181]. The activated carbon is also given orally to human beings as a sorbent for the removal of toxins from the human body and has also been utilized in biomedical applications [182, 183]. These studies strongly suggest the biocompatibility of the activated carbon.
Conclusion
In this review, environmental and special purification of heavy metal from heavy metal contaminants by the applications of carbon nanomaterials, namely fullerene carbon nanotubes, graphene, graphene oxide, and activated carbon discussed. These carbon nanomaterials have been utilized in the purification of heavy metal-contaminated water with great success. The reason behind the successful application is due to their fascinating properties like high surface area, ease of recycling, and easiness to desorb the adsorbed metal ions; only using mineral acid solution and regenerated material can be reused with retention of adsorption capability. In addition to these properties, the carbon nanomaterials can easily be fabricated with other nanomaterials and are easy to be functionalized resulting in multifunctional nano-adsorbent. Carbon-based materials are highly biocompatible with living organisms and environment. There is also an immense effect of different parameters such as pH, contact time, and type of adsorbents on the process of metal ion adsorption. Based on this literature review, it can be concluded that carbon nanomaterials have fascinating physicochemical properties and have great potential to be exploited in the environmental remediation and water purification.
Disponibilidad de datos y materiales
Todos los datos están completamente disponibles sin restricciones.
Abreviaturas
- AC:
-
Carbón activado
- GO:
-
Óxido de grafeno
- MWCNT:
-
Multiwall carbon nanotubes
- r-GO:
-
Óxido de grafeno reducido
- SWCNT:
-
Single-wall carbon nanotubes
Nanomateriales
- La fórmula perfecta para alinear operaciones y mantenimiento
- Los pros y los contras de los anillos de fibra de carbono
- La diferencia entre fibra de carbono y fibra de vidrio
- Materiales:PP reforzado con fibra de carbono y vidrio para automoción
- Los cinco problemas y desafíos principales para 5G
- Avances y desafíos de los nanomateriales fluorescentes para síntesis y aplicaciones biomédicas
- Presentación de la estructura atómica y electrónica de las nanofibras de carbono de copa apilada
- Comprender el concepto de IoT en el tratamiento y la gestión de aguas residuales
- Linterna lunar para buscar agua en la Luna
- La plataforma correcta para las configuraciones correctas
- La importancia de un tratamiento térmico eficaz para punzones, matrices, hojas y aceros para herramientas



