Síntesis hidrotermal de nanoflakes de óxido de grafeno reducido (rGO) decoradas con plata con actividad fotocatalítica eficaz para el tratamiento de aguas residuales
Resumen
El óxido de grafeno (GO) se obtuvo mediante el método hummers modificado, y el óxido de grafeno reducido (rGO) se adquirió mediante el empleo de un tratamiento térmico. Se incorporaron diversas concentraciones (2,5, 5, 7,5 y 10% en peso) de plata (Ag) en nanohojas GO mediante la adopción de un enfoque hidrotermal. El fotocatalizador de rGO decorado con Ag sintetizado Ag / rGO se caracterizó usando difracción de rayos X (XRD) para determinar la pureza de fase y la estructura cristalina. Los patrones XRD mostraron la formación de GO a Ag / rGO. La vibración molecular y los grupos funcionales se determinaron mediante espectroscopía infrarroja por transformada de Fourier (FTIR). Las propiedades ópticas y una disminución en la banda prohibida con la inserción de Ag se confirmaron con espectrofotómetro UV-Visible (Uv-Vis) y fotoluminiscencia (PL). Las propiedades electrónicas y los trastornos en las estructuras del carbono se investigaron mediante espectroscopía Raman que reveló la existencia de bandas características (D y G). La morfología de la superficie de las muestras preparadas se examinó con un microscopio electrónico de barrido de emisión de campo (FESEM). La distribución homogénea, el tamaño y la forma esférica de los NP de Ag sobre las láminas de rGO se confirmaron aún más con la ayuda de un microscopio electrónico de transmisión de alta resolución (HR-TEM). La degradación del tinte de las muestras dopadas y no dopadas se examinó mediante espectros Uv-Vis. Los resultados experimentales indicaron que la actividad fotocatalítica de Ag @ rGO mejoró con el aumento de la relación de dopaje debido a la disminución de la recombinación de pares de electrones y huecos. Por lo tanto, se sugiere que Ag @ rGO se puede utilizar como un fotocatalizador beneficioso y superior para limpiar el medio ambiente y las aguas residuales.
Introducción
El agua en la tierra es similar a la sangre en nuestro cuerpo. Es un material de recurso clave para la supervivencia y el desarrollo de todas las especies vivientes. Aunque el 71% de la superficie terrestre está cubierta de agua, solo el 0,03% del agua total se considera agua dulce que los humanos pueden utilizar directamente a través de lagos de agua dulce, ríos y aguas subterráneas poco profundas [1]. En las últimas décadas, la disponibilidad inadecuada de agua potable se ha presentado como una preocupación mundial implacable. El rápido crecimiento de la población mundial y la industrialización ha provocado un aumento de la contaminación ambiental, de modo que alrededor de 750 millones de personas se enfrentan a la falta de acceso a agua potable [2, 3]. Los depósitos de agua se contaminan de forma recurrente por diversos contaminantes peligrosos que contienen iones de metales pesados, tintes, aceite y otros productos químicos que se liberan de diferentes curtidurías e industrias relacionadas con los textiles, el caucho, el papel, los cosméticos, el teñido, el plástico y los alimentos [4]. Según el informe del Banco Mundial, entre el 17% y el 20% de la contaminación del agua es provocada por la industria textil. Anualmente, se producen ~ 1/10 millones de tipos de tintes en numerosos procesos textiles, entre estos tintes, el azul de metileno (MB), 10-15% se libera directamente en el efluente. Estos contaminantes crean problemas de salud graves como cáncer, irascibilidades de la piel, alergias y mal funcionamiento del hígado y también son dañinos para la vida acuática [4, 5].
Para abordar estos problemas globales, se emplean ciertos enfoques de tratamiento convencionales como el intercambio iónico, la electrólisis, el filtro de carbón, la coagulación química, los métodos biológicos, la filtración por membrana y la ósmosis inversa (RO). Sin embargo, una serie de inconvenientes y limitaciones están asociados con estas técnicas, que incluyen ineptitud, procedimiento complejo, alta formación de lodos, alto costo de implementación y operación y uso de grandes cantidades de energía [4, 6, 7]. Por tanto, es necesario desarrollar tecnologías eficientes con las propiedades antes mencionadas; entre estas técnicas, la fotocatálisis supera las deficiencias máximas.
Hasta la fecha, la degradación fotocatalítica utilizando nanomateriales semiconductores inorgánicos ha mostrado una gran conveniencia e interés para los investigadores debido a sus excelentes propiedades físicas y químicas, como baja toxicidad, estabilidad electroquímica, capacidad superoxidativa, rentabilidad y viabilidad ambiental [2, 8, 9 ]. Durante el proceso fotocatalítico (PC), los nanomateriales absorben una mayor energía de luz visible que la excitación iniciada por la banda prohibida entre las bandas de valencia y conducción. A través de la separación de carga, se generan pares de huecos de electrones. Los radicales libres (OH) oxidan los compuestos orgánicos y degradan los contaminantes [8, 10].
Por otro lado, algunos factores cruciales son vitales para determinar el rendimiento de la PC, específicamente el área de superficie del fotocatalizador, ya que los contaminantes orgánicos se degradan principalmente en la superficie del semiconductor. Presencia de una robusta capacidad de absorción de luz, rápida tasa de redox interfacial, entre varias nanoestructuras; nanoestructuras bidimensionales (2D) tienden a lograr estas características de manera más eficiente [11,12,13,14]. Los nanomateriales 2D también ofrecen canales de transporte de electrones debido a uniones reducidas y límites de grano en contraste con otros nanocristales esféricos. El transporte rápido de electrones disminuye la tasa de recombinación y aumenta el rendimiento de degradación de la PC. Entonces, en esta línea, el óxido de grafeno (GO) es un candidato adecuado para respaldar la eficiencia de la PC semiconductora [15,16,17,18].
En las últimas décadas, además de los CNT y otros nanomateriales a base de carbono, el grafeno con nanohoja de espesor atómico único surgió como un candidato llamativo con una amplia gama de propiedades relevantes prometedoras que incluyen la conversión de energía, el almacenamiento y las actividades catalíticas [19, 20,21]. En estudios sobre tratamiento y destilación de agua, debido a una gran cantidad de electrones deslocalizados conjugados en sp 2 configuración de la red de carbono, el carbono grafítico enriquece el transporte de fotoelectrones y mejora significativamente la eficiencia de la fotoconversión del sistema. Además, GO exhibe una alta capacidad de absorción de materiales orgánicos en un medio acuoso [22, 23]. El GO y los óxidos de grafeno reducidos (rGO) producen la reacción de la PC y, debido a su estrecha banda prohibida, se promueven como fotocatalizadores semiconductores activos de luz visible. No obstante, existe margen de mejora, ya que se descubrió que la fotoconversión era deficiente debido a la rápida recombinación de pares de electrones y huecos en la superficie.
La eficacia de la fotoconversión de los fotocatalizadores basados en GO / rGO se puede mejorar evitando la recombinación de huecos de electrones. Para lograr este objetivo, se desarrollaron modificaciones de la superficie con iones de metales nobles, incluidos platino (Pt), paladio (Pd), plata y nanopartículas de oro (NP). La plata entre los metales nobles más estudiados se considera un candidato probable para la modificación del grafeno y sus análogos para la relevancia de la PC debido a su bajo costo, propiedades ópticas incomparables, mayor estabilidad química y naturaleza no tóxica. La mayor inmovilidad de las nanopartículas de plata decoradas en rGO se reconoce como un rendimiento mejorado, principalmente debido al aumento del área reactiva y la separación de carga superior. Las propiedades únicas de agregación y transporte de electrones de GO a través del esquema conjugado conducen a los electrones calientes a sitios reactivos y suprimen la recombinación [23]. En consecuencia, en nombre de los beneficios antes mencionados, nos propusimos sintetizar diferentes proporciones de contenido de Ag (2.5, 5, 7.5, 10)% en peso con fotocatalizador rGO a través de la ruta hidrotermal para examinar la eficiencia del fotocatalizador y también se caracterizarían muestras preparadas a través de varias técnicas para estudiar. propiedades estructurales ópticas y electrónicas.
Métodos
El estudio actual tenía como objetivo sintetizar varias concentraciones de Ag en nanohojas de rGO a través de una ruta hidrotermal para investigar la eficiencia del fotocatalizador.
Materiales
Grafito (99%) y nitrato de sodio (NaNO 3 ) El 99,9% se adquirió de "Sigma-Aldrich", mientras que el ácido sulfúrico (H 2 SO 4 , 37%) y ácido fosfórico (H 3 PO 4 ) fueron adquiridos de "Analar". Plata (Ag, 99,8%), permanganato de potasio (KMnO 4 , 99%) y ácido clorhídrico (HCL) se obtuvieron de "Merck". Todos los productos químicos se utilizaron sin purificación adicional.
Síntesis de GO
Se adoptó el método de hummers modificado para obtener GO. Grafito (5 g) y NaNO 3 (2,5 g) se mezclaron en H 2 SO 4 (108 ml) con 12 ml de H 3 PO 4 . La mezcla se agitó magnéticamente en un baño de hielo durante 10 minutos; La solución de filtrado adicional se secó en un horno de mufla a 60ºC durante 2 h para eliminar la humedad. Más tarde, KMnO 4 (15 g) se añadió lentamente a temperatura mantenida por debajo de 5ºC. La suspensión se transfirió a un baño de hielo durante 2 h después de agitar vigorosamente a 98 ° C durante 60 min mientras se añadía agua continuamente. Se añadió más agua desionizada hasta que el volumen de suspensión fue de 400 ml después de 5 centavos de H 2 O 2 (12 ml) se mezcló. Finalmente, la suspensión se centrifugó y se lavó repetidamente con agua y el producto de HCL se secó a 60 ° C y se encontró que el pH de GO era de 5,7 después del lavado como se ilustra en la Fig. 1 [24, 25].
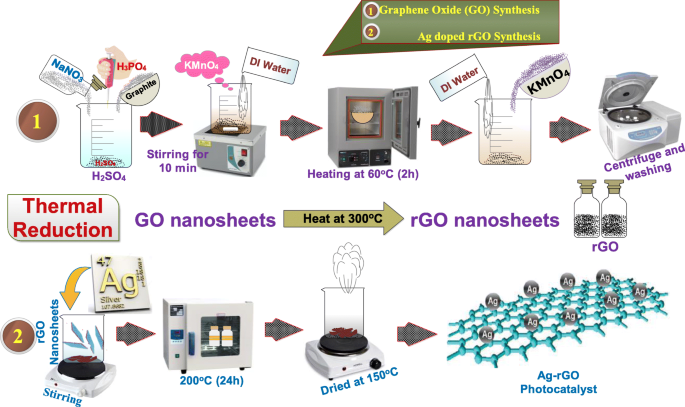
Proceso de síntesis para GO y rGO dopado con Ag
Síntesis de Ag / rGO
La rGO se extrajo de GO por reducción térmica. GO se ha reducido manteniéndola a temperatura de reducción (300 ° C) un cambio brusco de temperatura provoca la eliminación de grupos funcionales y átomos de oxígeno de los planos de carbono y se produce la exfoliación de GO para producir rGO [ 26]. El rGO puede considerarse como grafeno de origen químico, cuya estructura variaba de una capa a varias capas [27]. Se sintetizó hidrotermalmente rGO dopado con Ag con diversas relaciones de concentración, usando nanohojas de 800 mg de GO incorporadas con (25, 50, 75 y 100 mg) de Ag en 80 ml de agua desionizada con agitación vigorosa durante 20 min. Después, la solución se centrifugó (30 min) y posteriormente se transfirió a un autoclave revestido de teflón de 100 ml, se selló y se calentó a 200ºC (24 h). El producto final se secó a ~ 200 ° C como se muestra en la Fig. 1 [9].
Actividad fotocatalítica
La actividad fotocatalítica de los productos preparados se evaluó mediante la degradación del azul de metileno sintético (MB) en medio acuoso como se muestra en la Fig. 2. Se preparó tinte (5 mg / 500 ml) con 10 mg de suspensión de fotocatalizador (0.025:1, 0.050:1, 0.075:1 y 0.1:1) bajo agitación (5 min) y expuesto a la oscuridad durante 30 min para lograr una absorbancia significativa. Se transfirieron 60 ml de solución preparada con agitación vigorosa a un foto-reactor bajo una lámpara de mercurio (400 W y 400-700 nm) utilizada como fuente de luz visible. Después de la exposición a la luz durante intervalos de tiempo especificados (20 min), se recogió la suspensión (3 ml) para determinar la degradación del tinte. La concentración / absorbancia de MB se examinó con un espectrómetro UV-Vis; La eficiencia de decoloración del fotocatalizador preparado se evaluó como:
$$ \ mathrm {Degradación} \ \ left (\% \ right) =\ left [1- \ left (C / {C} _o \ right) \ right] \ times 100 $$ (1)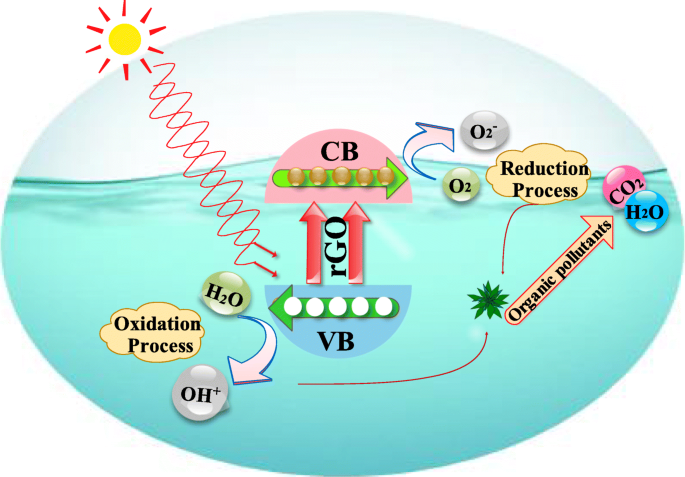
Mecanismo fotocatalítico para la degradación del tinte en presencia de Ag / rGO
donde C o es la absorbancia en t =0 y C es la absorbancia en el tiempo t (intervalo de tiempo específico) [8, 10].
El mecanismo de degradación fotocatalítica de moléculas orgánicas se aclara de la siguiente manera (Fig. 2). Cuando el fotocatalizador (Ag / rGO) se irradia con fotones de energía igual o superior a la energía de banda prohibida de PC, entonces los electrones (e - ) están excitados por la banda de valencia (VB)
$$ \ mathrm {PC} + hv \ to {e} ^ {-} \ left (\ mathrm {CB} \ right) + {h} ^ {+} \ left (\ mathrm {VB} \ right) $$ (2)Los electrones generados a través de la irradiación pueden ser atrapados fácilmente por O 2 Molécula absorbida en la superficie del fotocatalizador (PC) o O 2 disuelto para dar radicales superóxido, es decir, O 2 • -
$$ {e} ^ {-} + {\ mathrm {O}} _ 2 \ to {\ mathrm {O}} _ 2 ^ {\ bullet -} $$ (3)Por lo tanto, O 2 • - puede reaccionar con H 2 O para producir radical hidroperoxi (H 2 O • ) y radical hidroxilo (OH • ), que son agentes oxidantes influyentes que descomponen las moléculas orgánicas:
$$ {\ mathrm {O}} _ 2 ^ {\ bullet -} + {\ mathrm {H}} _ 2 \ mathrm {O} \ to {\ mathrm {H} \ mathrm {O}} _ 2 ^ {\ bullet} + \ mathrm {O} $$ (4)Al mismo tiempo, los agujeros fotogenerados podrían quedar atrapados por grupos hidroxilo de la superficie (H 2 O) en la superficie de un fotocatalizador para producir radicales hidroxilo (OH • ):
$$ {h} ^ {+} + {\ mathrm {OH}} ^ {-} \ to {} ^ {\ bullet} \ mathrm {O} {\ mathrm {H}} _ {\ mathrm {ad}} $$ (5) $$ {h} ^ {+} + {\ mathrm {H}} _ 2 \ mathrm {O} \ to {} ^ {\ bullet} \ mathrm {O} \ mathrm {H} + {\ mathrm {H}} ^ {+} $$ (6)Eventualmente, las moléculas orgánicas se oxidarán para producir CO 2 y H 2 O como sigue:
OH + moléculas orgánicas + O 2 → productos (CO 2 y H 2 O) (7)
Temporalmente, podría tener lugar una ligera recombinación del hueco positivo y el electrón, lo que podría reducir la actividad fotocatalítica del nanocatalizador preparado [28].
Caracterización de materiales
La estructura cristalina y la información de fase de GO y Ag @ rGO se investigaron a través de XRD, mediante el sistema de espectro Bruker (XRD, D2 Phaser, EE. UU.) Equipado con radiación de Cu K monocromatizada de una longitud de onda promedio de 0.154 nm (5-80 °) usando un velocidad de escaneo de 0.05 / min. Espectrómetro FTIR Perklin Elmer 3100 con un rango espectral de 4000 a 400 cm −1 con un aumento de 32 escaneos y una resolución de 0,2 cm −1 se empleó para detectar grupos funcionales y otras vibraciones moleculares de muestras preparadas. Las propiedades ópticas se registraron mediante espectrofotómetro UV-Vis (TECAN infinite M200PRO) en el rango de 200 a 700 nm. La morfología de la superficie y la distancia entre capas de las muestras sintetizadas se observaron utilizando microscopio electrónico de barrido de emisión de campo (FESEM), JSM-6460LV y microscopio electrónico de transmisión de alta resolución (HR-TEM) Philips CM30 y JEOL JEM 2100F. Para confirmar las escamas GO, Ag / rGO y los modos de vibración, se emplearon espectros Raman en Renishaw en un microscopio Raman confocal reflexivo con una longitud de onda de láser de 532 nm (6 mW). Los espectros de fotoluminiscencia de las muestras preparadas y dopadas se registraron mediante espectrofluorómetro (JASCO, FP -8300).
Resultados y discusión
Se examinaron la estructura de fase y el tamaño de cristalito de nanohojas de rGO insertadas con Ag preparadas usando análisis XRD (Fig. 3a). El difractograma de GO muestra una reflexión intensa ubicada en ~ 10,27 ° atribuida al plano (001) con un espaciado entre capas de 0,80 nm [23, 29, 30]. Tras el dopaje con Ag, el pico ancho se origina a ~ 25,4 °, que se reconoce como el pico característico del grafeno indexado como el plano (002) (JCPDS No # 04-0783) del grafito hexagonal, con un espaciado d de 0,34 nm [23, 30,31 , 32]. El pico (001) revela el polvo de grafito completamente oxidado en GO y el pico (002) respalda la eliminación de la plantilla de polihidrocarburos entre dos capas de rGO [30]. Después de la sustitución de Ag, el pico GO (001) cambió a un valor más alto a 2 θ a 25,4 ° con un menor espaciado d evidente para la reacción redox entre el óxido de grafeno y los iones de plata (Ag-rGO) y el valor de desplazamiento d después de la reducción causada por la eliminación de grupos que contienen oxígeno que se intercalan entre las capas de óxido de grafeno reducido (rGO) como se ve en el difractograma XRD [29, 32]. Tamaño medio de cristalito evaluado por la ecuación de Scherer:
$$ \ mathrm {D} =\ frac {\ mathrm {k} \ lambda} {\ beta \ cos \ uptheta} $$ (8)Se encuentra que los tamaños de cristalitos son ~ 4.85, 11.3, 11.53, 11.6 y 28.3 nm respectivamente. En Eq. (8) k =0,89, β =FWHM, λ =0,154 nm y θ =ángulo de difracción. La difracción de electrones de área seleccionada (SAED) en la Fig. 3b yc correspondiente a los patrones XRD de muestras preparadas exhibe características de anillo distintas e indica la fase hexagonal de GO y Ag / rGO manifestada en productos bien cristalizados; Además, la indexación de anillos fue consistente con los patrones de XRD.
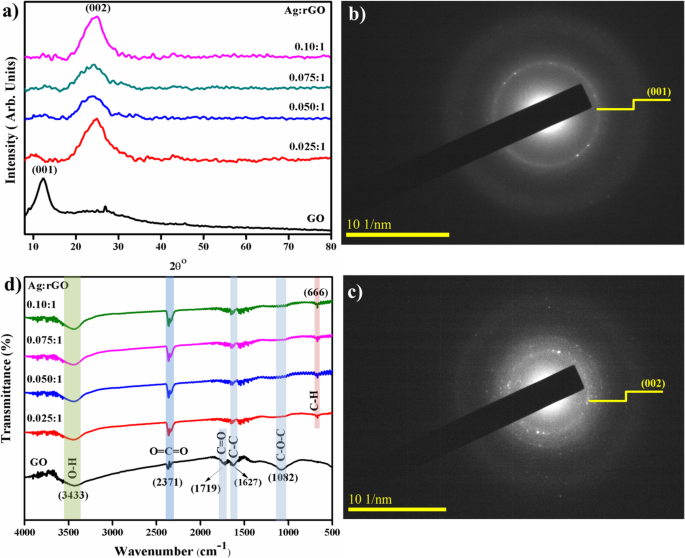
un Patrón XRD. b , c Anillos SAED de RGO preparado y dopado con Ag ( b ) 0:1 ( c ) 0,010:1. d Espectros FTIR
Los espectros de infrarrojos por transformada de Fourier (FTIR) de GO y rGO dopado con Ag se ilustran en la Fig. 3d. Pico observado ~ 3433 cm –1 corresponde a la vibración de estiramiento O-H [23]. Picos de transmitancia bajos a 1719 cm –1 asignar a C =O las vibraciones de estiramiento causadas por los grupos COOH y la banda a 1627 cm −1 asignado al estiramiento C-C aromático [10, 33]. Pico a ~ 2371 cm −1 asignado a grupos COO [34]. Pico de transmitancia (~ 650 cm −1 ) es una región de huellas dactilares de sp 2 hibridado enlace de carbono asignado como vibración de flexión C-H [35]. Banda ~ 1082 cm –1 corresponde a C – O – C de las vibraciones de estiramiento de hidroxilo, al doparse, el valor máximo de los grupos funcionales en la muestra dopada cambió ligeramente mientras que sus formas permanecen similares [23, 29, 36].
Las propiedades ópticas en términos de absorbancia y análisis de banda prohibida del fotocatalizador Ag-rGO se escrutaron a través de un espectrógrafo Uv-Vis en el rango de 200-700 nm como se muestra en la Fig. 4a. El espectro Uv-Vis de GO presenta un pico de características alrededor de 230 nm debido a π - π * la transición de enlaces C – C aromáticos indicó la restauración de un marco conjugado extenso de sp 2 Átomos de carbón. Otro pico de hombro observado a 300 nm atribuido a n - π * transiciones de enlaces C =O [19, 23, 31]. Por el contrario, estos dos picos se debilitaron en el caso de Ag / rGO correspondiente a π - π * transición de enlace C – C aromático que se encuentra desplazada al rojo a 270 nm que confirma la reducción de GO e indica que no hay restauración de la conjugación electrónica del grafeno [23, 29]. La absorción en la región visible (~ 400 nm) debido a su resonancia plasmónica de superficie de Ag NPs que es una prueba más como fotocatalizador activo de luz visible para la eliminación de cuerpos orgánicos [23, 29, 37]. Bandgap se calculó mediante la ecuación de Tauc; αhν = D ( hν - Por ejemplo ) n trazando de ( αhν ) 2 vs hν extrapolando los ajustes lineales, se calculó que la banda era 4.10 eV para GO y 3.98 a 3.50 eV para Ag / rGO, la banda prohibida disminuyó gradualmente con un mayor dopaje de Ag NP claramente observado en la Fig. 4b [38].
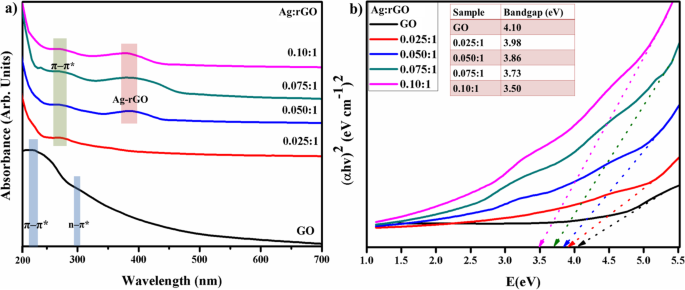
un Espectros UV-Vis de GO y Ag-rGO. b Comparación de bandgap
Las características morfológicas de las muestras de GO y Ag-rGO aclaradas a través de FESEM y HR-TEM que se muestran en la Fig. 5. Las imágenes de GO (Fig. 5a) muestran pocas capas de microestructuras con ricas arrugas y una morfología esponjosa que se asemeja a una cortina fina. Las imágenes de Ag @ rGO (Fig. 5b-d) muestran nanoláminas transparentes parcialmente dobladas y rizadas con pequeñas fluctuaciones que son esenciales para soportar la estabilidad termodinámica del grafeno, debido a su estructura de cristal 2D. Las nanoláminas exhiben estructuras extremadamente limpias, sedosas y onduladas, y esta característica puede ser importante para evitar la agregación de láminas de rGO y mantener la superficie para facilitar la fijación de NP de Ag en láminas de grafeno que pueden visualizarse en imágenes HR-TEM [36]. Las imágenes HR-TEM correspondientes (Fig. 6 a 1 -d 1 ), GO exhibe una estructura laminar y en forma de hoja con un área de superficie limpia (Fig. 6a 1 ), en la muestra Ag-rGO (Fig.5 b 1 ) pocos pliegues apilables debido a sus distorsiones de una alta fracción de sp 3 Enlaces C – O [29]. Con concentración creciente de NP de Ag (Fig. 6 c 1 , d 1 ) Las imágenes revelaron una dispersión homogénea y bien dispersa de NP de Ag de forma esférica en la superficie de las láminas de rGO con un tamaño de partícula promedio de 10-12 nm [23, 29]. En la Fig. 6 d 1 con una concentración más alta (10%) de Ag, la agregación de partículas aumentó, lo que es evidente para las especies dopadas.

( a - d , un 1 - d 1 ) Imágenes FESEM y HR-TEM de GO y Ag / rGO ( a , un 1 ) IR ( b , b 1 ) 0.050:1 ( c , c 1 ) 0.075:1 y ( d , d 1 ) 0.10:1
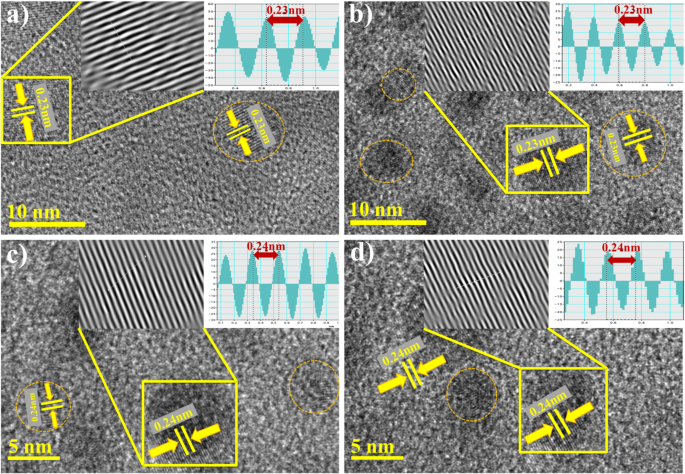
un - d espaciado d de imágenes HR-TEM de Ag-rGO ( a ) 0.025:1 ( b ) 0.050:1 ( c ) 0.075:1 ( d ) 0.10:1
Las imágenes de resolución extremadamente alta con un espaciado d de hasta 5 y 10 nm de muestras de Ag / rGO se pueden observar claramente en la Fig. 6a-d. Las áreas en círculo indican la presencia de NP de Ag con un espaciado de red de nanocristales de Ag de aproximadamente 0,235 nm [23, 29].
Se realizó un análisis de fotoluminiscencia (PL) para investigar el tiempo de vida, la transferencia y el atrapamiento del par electrón-hueco y el estudio de la interacción entre las nanoestructuras de grafeno, su influencia en la respuesta fotocatalítica ilustrada en la Fig. 7a [39, 40]. El grafito no presenta propiedades de luminiscencia debido a la banda prohibida cero. Sin embargo, al disminuir el tamaño hasta nanoescala, la banda prohibida se amplía debido al efecto de confinamiento cuántico. En nanohojas de GO y rGO, los grupos de óxidos y las vacantes de carbono alteraron el grafeno para formar cualquier nano-clúster de carbono que demuestre un comportamiento semiconductor y un fenómeno de luminiscencia que puede verse influenciado por el tamaño o fracción de cadenas y clústeres [40, 41]. En los espectros PL, los picos de luminiscencia se ubicaron a ~ 330, 565 y 608 nm, lo que se atribuye a la recombinación de pares de electrones y huecos en el estado local de sp 2 grupos de carbono incorporados con sp 3 matriz. Por lo tanto, la luminiscencia de rGO se debe a la desaparición de grupos funcionales de oxígeno que facilitan la percolación de vías entre sp 2 racimos [40]. El pico significativo a ~ 565 nm disminuyó drásticamente en el caso de rGO con reducción de los grupos funcionales de óxido de GO que están disminuidos y sp 2 los grupos de carbono se expanden simultáneamente [41].
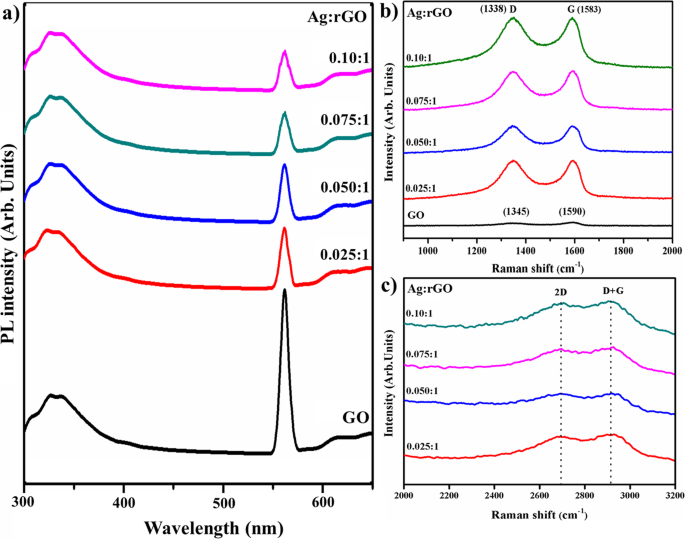
un Espectros PL. b Espectros Raman de muestras preparadas. c Área de zoom de los espectros Raman
Se implementó la espectroscopía Raman para probar las propiedades electrónicas y estructurales de la muestra de control y Ag @ rGO para distinguir las estructuras de carbono ordenadas y desordenadas, como se demuestra en la Fig. 7b, c. En el caso de GO, dos bandas están ubicadas en ~ 1340 y ~ 1590 cm −1 asignado como banda D y G, respectivamente. La banda D se asigna al modo de respiración de fonones de punto k con A 1g simetría y banda de sp 3 Átomos de carbón; La banda G sugiere un pico característico de sp 2 estructura híbrida que revela simetría y cristalizabilidad del carbono e introduce E 2g Dispersión fonónica de átomos de carbono [32, 33, 36]. Además, la banda D es evidente para los defectos de la superficie y surgen imperfecciones estructurales con grupos de funciones hidroxilo y epóxido adjuntas con planos basales de carbono [36]. La banda G es solo el modo Raman en el grafeno que se origina a partir de un proceso de dispersión Raman convencional de primer orden y corresponde al centro de la zona en el plano, modo fonónico doblemente degenerado (óptico transversal (TO) y longitudinal (LO)) con E 2g simetría [42]. En el caso del espectro Ag-rGO Raman observado a 1338 cm −1 (Banda D), 1583 cm −1 (Banda G) y 2682 cm −1 (Banda 2D) hay un pico adicional centrado en 2900 cm −1 (Banda D + G) que representa el trastorno debido a la dispersión combinada en la Fig. 7b, c [31, 35, 42,43,44,45]. Los modos D y 2D se originan a partir del proceso de resonancia doble de segundo orden entre puntos k no equivalentes en la zona de Brillouin (BZ) del grafeno, ya que la banda 2D indica el segundo orden de la banda D que alude al sobretono de la banda D con su existencia debido a dos procesos vibratorios de celosía telefónica; sin embargo, no se asocia con defectos como la banda D en la Fig. 7c [35, 41]. Las variaciones en las intensidades relativas de las bandas G y D en los espectros Raman de GO durante la reducción suelen designarse como un cambio en el estado de conjugación electrónica. Este cambio sugiere un aumento en la cantidad de sp 2 dominios atómicos tras la reducción de GO [46]. La relación de intensidad de la banda D a la G define el grado de desorden en las capas de grafito; Yo D / I G =0.87 para una muestra gratis dopada (GO), I D / I G =1,15 para muestras dopadas con Ag y un aumento en la proporción indica una disminución en el tamaño promedio de sp 2 dominios de carbono después de la síntesis de Ag @ rGO, mientras que la relación de intensidad entre la banda 2D y G (I 2D / I G ) que es 1,69, se han utilizado para sondear la concentración de electrones en rGO [31, 32, 35, 47].
Las nanopartículas agrícolas, cuando se dopan en un material semiconductor, generan una diferencia de potencial de contacto debido a sus diferentes funciones de trabajo. Esta diferencia de potencial se denomina barrera de Schottky. Como se muestra en la Fig.8, la flexión de la banda cuando se forma un contacto después de alcanzar el equilibrio depende de las energías relativas de las funciones de trabajo del metal (ϕ M ) y el semiconductor (ϕ B ) componentes. Este fenómeno puede mejorar en gran medida la eficiencia de separación de carga, una vez que puede inducir la migración direccional de electrones fotogenerados desde el semiconductor al metal. En otras palabras, puede conducir a la generación de un sitio de captura de electrones eficaz para suprimir la recombinación de los huecos de electrones [48].
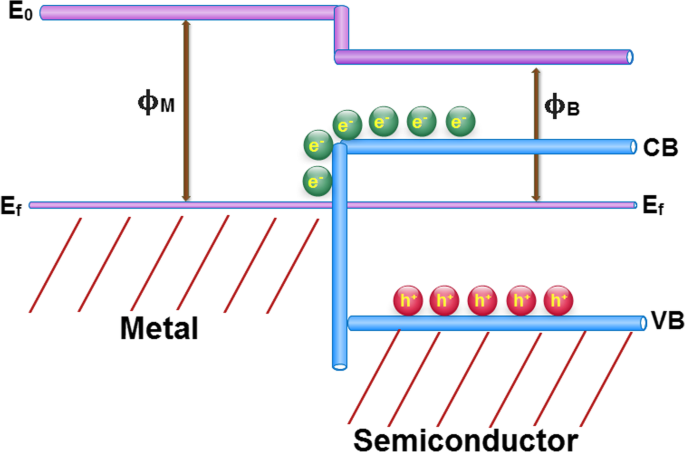
Estructura de banda electrónica cualitativa de nanohojas decoradas con Ag
La actividad fotocatalítica de las nanohojas de GO y Ag / rGO se produjo debido a su alta área de superficie y baja energía de banda prohibida. Por tanto, Ag / rGO exhibe una mejora sustancial en la fotodegradación de MB y el colorante se degrada completamente (Fig. 9b) en 120 min. La ecuación de pseudo-primer orden se puede emplear para elaborar la eficiencia fotocatalítica (Fig. 8a) de las muestras de GO y Ag / rGO explícitamente, utilizando la siguiente expresión.
$$ - \ mathit {\ ln} \ left ({C} _t / {C} _o \ right) =kt $$ (9)donde Co es la concentración inicial de tinte y C t es la concentración en el momento, k es la constante de velocidad aparente del proceso de degradación que se muestra en el gráfico de absorbancia (Fig. 9a), es decir, el valor de k para GO es de aproximadamente 0,1300 min −1 y k aumenta extraordinariamente en el caso de Ag / rGO (0,1300 min −1 a 0,7459 min −1 ). La Figura 9c revela la compresión del% de degradación con el tiempo, GO muestra un 65% de eficiencia y un aumento gradual con la concentración de dopaje. Ag / rGO (0,10:1) muestra un% de degradación máximo de hasta el 100%, lo que probablemente se deba a los efectos sinérgicos de los NP de Ag [49, 50]. Finalmente, sobre la base de estos hallazgos en el presente estudio, se puede sugerir que Ag / rGO es un producto excelente que puede usarse para la purificación de agua a partir de colorantes orgánicos.
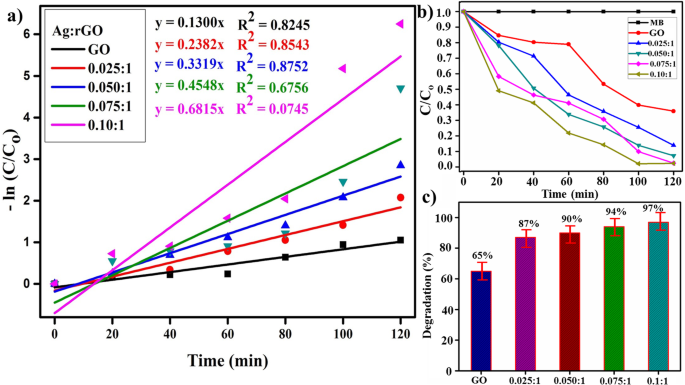
un Gráfico de -ln (Ct / C0) frente a los espectros de tiempo para la reducción del tinte. b Gráfico de la relación de concentración (C / C 0 ) versus tiempo. c Comparación de degradación (%) de todas las muestras
Conclusión
El GO se obtuvo con éxito mediante el método hummers modificado y el rGO se sintetizó a partir del tratamiento térmico durante la inserción de Ag (2,5, 5, 7,5 y 10% en peso) por vía hidrotermal. De acuerdo con el patrón XRD, el cambio de pico y la disminución en el espaciamiento d (0.34 a 0.023 nm) apuntan hacia la reacción redox de GO tras el dopaje con Ag con estructura cristalina hexagonal; Se observa un aumento medio del tamaño de cristalito (4,85 a 15,6 nm) con sustitución de Ag. Los espectros FTIR confirmaron un pico de transmitancia alrededor de 650 cm −1 que es una región de huellas dactilares de sp 2 hibridado enlace de carbono asignado como vibración de flexión C-H y revela información sobre otros grupos funcionales adjuntos. El pico característico atribuido a π - π * y n - π * vinculación y corrimiento al rojo en picos. Respalda la presencia de Ag según se aclara con espectroscopía UV-Vis, una disminución obvia en la energía de la banda prohibida (4.10 a 3.50 eV) con una mayor proporción de dopaje que se calculó con la ayuda de la ecuación de Tauc. Las características morfológicas muestran capas de apilamiento de GO y Ag / rGO con un espaciado de celosía de ~ 0.235 nm, forma esférica y tamaño (10-12 nm) de NP de Ag visualizadas a través de HR-TEM. Los átomos de carbono del estado local sp 2 clústeres incorporados con sp 3 matriz, disminución de pico significativa en el caso de rGO y sp 2 expandido El grupo de carbono tras el dopaje se confirmó con espectros PL. Un 1g simetría en sp 3 átomos de carbono en la banda D, sp 2 La estructura híbrida que revela la simetría y la cristalizabilidad del carbono e introduce la dispersión del fonón E2g de un átomo de carbono y los defectos superficiales se calcularon mediante espectros Raman. La actividad fotocatalítica responde a Ag / rGO (0,10:1) y degrada el 100% de la concentración de MB. Estos hallazgos sugieren que el nanocatalizador preparado no muestra ningún comportamiento peligroso en el tratamiento del agua y es un excelente nanocatalizador para la eliminación de contaminantes orgánicos de las aguas residuales.
Disponibilidad de datos y materiales
Todos los datos están completamente disponibles sin restricciones.
Abreviaturas
- UV-Vis:
-
Espectroscopia visible ultravioleta
- XRD:
-
Difracción de rayos X
- FTIR:
-
Espectroscopia infrarroja por transformada de Fourier
- EDS:
-
Espectroscopía de rayos X de energía dispersiva
- SEM:
-
Microscopía electrónica de barrido
- TEM:
-
Microscopía electrónica de transmisión
- JCPDS:
-
Comité conjunto sobre estándares de difracción de polvo
Nanomateriales
- Reduzca los costos operativos con programas de tratamiento de agua eficaces
- Cristalización dependiente de la temperatura de nanoflakes de MoS2 en nanohojas de grafeno para electrocatálisis
- Síntesis hidrotermal de nanopartículas de In2O3, gemelos híbridos, discos hexagonales, heteroestructuras de ZnO para mejorar las actividades fotocatalíticas y la estabilidad
- Efectos sinérgicos de nanopartículas de Ag / BiV1-xMoxO4 con actividad fotocatalítica mejorada
- Síntesis en un solo recipiente de nanoplacas de Cu2ZnSnSe4 y su actividad fotocatalítica impulsada por la luz visible
- Preparación de molienda de bolas en un solo paso de óxido de grafeno / CL-20 a nanoescala para una sensibilidad y un tamaño de partículas significativamente reducidos
- Nanocomposites a base de óxido de grafeno decorados con nanopartículas de plata como agente antibacteriano
- Tensioactivo aniónico / Líquidos iónicos Intercalado de óxido de grafeno reducido para supercondensadores de alto rendimiento
- Un enfoque fácil para la preparación de óxido de zinc de tamaño nanométrico en agua / glicerol con fuentes de zinc extremadamente concentradas
- Exfoliación con piedra de molino:una verdadera exfoliación con cizallamiento para óxido de grafeno de pocas capas de gran tamaño
- Síntesis fácil y actividad fotocatalítica de luz visible mejorada de nuevos compuestos de heterounión p-Ag3PO4 / n-BiFeO3 para la degradación del tinte



