Síntesis fácil y actividad fotocatalítica de luz visible mejorada de nuevos compuestos de heterounión p-Ag3PO4 / n-BiFeO3 para la degradación del tinte
Resumen
En este trabajo, Ag 3 PO 4 se decoraron micropartículas sobre la superficie de BiFeO 3 microcuboides mediante un método de precipitación para obtener p-Ag 3 PO 4 / n-BiFeO 3 compuestos de heterounión. Los compuestos se emplearon para la degradación de naranja ácido 7 (AO7) bajo irradiación de luz visible. Se encuentra que los compuestos exhiben una eficiencia fotocatalítica mucho mayor que BiFeO 3 desnudo . Mientras tanto, la actividad fotocatalítica intrínseca impulsada por la luz visible de Ag 3 PO 4 / BiFeO 3 compuestos se confirmó además por la degradación del fenol. Además, también se evaluó la propiedad de catálisis de tipo foto-Fenton del material compuesto. El análisis de fotocorriente indica que la combinación de BiFeO 3 con Ag 3 PO 4 conduce a la inhibición de la recombinación de electrones y huecos fotoinducidos. La mejora obvia en la actividad fotocatalítica del compuesto se atribuye principalmente a la eficiente separación de carga fotogenerada y a la migración de carga interfacial causada por la formación de Ag 3 PO 4 / BiFeO 3 heterouniones p-n.
FormalPara PACS81.05.Hd82.65. + R82.50. – m
Antecedentes
Recientemente, la fotocatálisis de semiconductores ha recibido una atención considerable como una tecnología prometedora para la conversión de energía y el tratamiento de la contaminación [1, 2, 3]. Como sabemos, el fotocatalizador TiO 2 ampliamente investigado es simplemente activo bajo la irradiación de luz ultravioleta (UV) que solo constituye alrededor del 5% de la luz solar y, por lo tanto, limita en gran medida sus aplicaciones fotocatalíticas bajo la luz solar. En consecuencia, es necesario desarrollar los fotocatalizadores impulsados por luz visible [4, 5, 6, 7, 8].
Los óxidos semiconductores a base de bismuto o ferrum generalmente poseen una energía de banda prohibida moderada (~ 2.0 eV) y se consideran una clase importante de fotocatalizadores sensibles a la luz visible [9,10,11,12,13,14,15,16, 17,18,19]. Entre ellos, BiFeO 3 con una estructura de tipo perovskita muestra un rendimiento fotocatalítico interesante para la degradación del tinte y la división del agua bajo irradiación de luz visible [20, 21, 22, 23, 24, 25]. Sin embargo, su actividad fotocatalítica no es impresionante debido a la alta tasa de recombinación de electrones fotogenerados (e - ) y agujeros (h + ). Afortunadamente, está demostrado que el acoplamiento de BiFeO 3 con un semiconductor de banda estrecha con potenciales de borde de banda emparejados para formar una heterounión es una de las estrategias más prometedoras para promover la separación de cargas fotogeneradas, lo que conduce a una actividad fotocatalítica mejorada de BiFeO 3 [26,27,28,29,30,31]. Por ejemplo, Chaiwichian et al. informó que BiFeO 3 -Bi 2 WO 6 Los nanocompuestos exhibieron una actividad mejorada en la degradación del tinte [29]. Wang y col. observó que AgCl / Ag / BiFeO 3 mostró una actividad fotocatalítica de luz visible mucho más alta que BiFeO 3 desnudo [30]. Fan y compañeros de trabajo descubrieron que la combinación de g-C 3 N 4 con BiFeO 3 obviamente puede mejorar la actividad catalítica en comparación con BiFeO 3 puro [31].
Ortofosfato de plata (Ag 3 PO 4 ), como excelente fotocatalizador impulsado por luz visible, ha atraído una atención considerable en el campo fotocatalítico [32,33,34,35,36,37]. Se ha demostrado que Ag 3 PO 4 puede lograr un rendimiento cuántico extremadamente alto (~ 90%) para la generación de oxígeno a partir de la división del agua [32, 33]. Además, posee una capacidad de fotooxidación superior para la degradación de la contaminación orgánica debido a su posición de banda de valencia altamente positiva [34]. En la mayoría de los casos, debido a la posición apropiada de la banda de energía y la banda prohibida estrecha, Ag 3 PO 4 se emplea ampliamente como cocatalizador para combinar con otros fotocatalizadores para formar compuestos, lo que conduce a una mejora obvia del comportamiento fotocatalítico, como Ag 3 PO 4 / Bi 2 WO 6 , Ag 3 PO 4 / BiPO 4 , Ag 3 PO 4 / Bi 2 O 2 CO 3 , Ag 3 PO 4 / g-C 3 N 4 , Ag 3 PO 4 / BiVO 4 , Bi 4 Ti 3 O 12 / Ag 3 PO 4 , Ag 3 PO 4 / ZnFe 2 O 4 , Ag 3 PO 4 / WO 3 , Ag 3 PO 4 / ZnO y Bi 2 MoO 6 / Ag 3 PO 4 [38,39,40,41,42,43,44,45,46,47]. Se informa que BiFeO 3 es un semiconductor de tipo n y Ag 3 PO 4 se conoce como semiconductor de tipo p [43, 48]. La construcción de Ag 3 PO 4 / BiFeO 3 Los compuestos de heterounión p-n pueden ser un método factible para obtener un fotocatalizador eficaz. Sin embargo, hasta donde sabemos, se ha dedicado poco trabajo a la investigación del rendimiento fotocatalítico de Ag 3 PO 4 / BiFeO 3 compuestos.
En este trabajo, Ag 3 PO 4 / BiFeO 3 Los compuestos de heterounión p-n se prepararon fácilmente mediante la precipitación de Ag 3 PO 4 micropartículas en BiFeO 3 microcuboides. Se seleccionaron naranja ácido 7 (AO7) y fenol como contaminante modelo para evaluar la actividad fotocatalítica de los compuestos bajo irradiación de luz visible. Además, también se investigó la actividad de catálisis de tipo foto-Fenton del material compuesto. Se discutió el mecanismo subyacente de los compuestos para la degradación de contaminantes orgánicos.
Métodos
Preparación de Ag 3 PO 4 / BiFeO 3 Compuestos
BiFeO 3 Los microcuboides se sintetizaron mediante una ruta hidrotermal. 0,005 mol de Bi (NO 3 ) 3 • 5H 2 O y 0,005 mol de Fe (NO 3 ) 3 • 9H 2 O se disolvieron en 20 ml de solución diluida de ácido nítrico (5 ml de HNO 3 + 15 mL de agua desionizada). Se añadieron sesenta mililitros de solución de KOH con una concentración de 4,5 mol / L a la solución anterior gota a gota con agitación magnética. Después de 8 min de tratamiento ultrasónico y otros 30 min de agitación magnética vigorosa, la solución de la mezcla se selló en un autoclave de acero inoxidable revestido con teflón de 100 mL de capacidad y se sometió a reacción hidrotermal a 200 ° C durante 6 h. Después de que el autoclave se enfrió naturalmente a temperatura ambiente, el precipitado se recogió por centrifugación, se lavó con agua desionizada (dos veces) y etanol absoluto (tres veces) y luego se secó a 80 ° C durante 12 h para obtener BiFeO final. 3 producto. Ag 3 PO 4 Las micropartículas se prepararon mediante un método de precipitación. Tres milimoles de AgNO 3 se disolvió en 30 ml de agua desionizada y 1 mmol de Na 3 PO 4 · 12H 2 Se añadió O a 30 ml de agua desionizada con ayuda de agitación magnética. Una vez que la solución fue homogénea, la última solución se añadió gota a gota a la primera con agitación magnética vigorosa durante 7 h. Durante la reacción, el color de la solución cambió a amarillo. Finalmente, la mezcla se centrifugó para recoger el precipitado. El precipitado obtenido se lavó varias veces con agua desionizada y luego se secó en un horno de vacío a 60 ° C durante 8 h.
Ag 3 PO 4 / BiFeO 3 los compuestos se sintetizaron de la siguiente manera:0,1 g de BiFeO 3 Los microcuboides se dispersaron en 30 ml de agua desionizada y luego se sometieron a ultrasonidos durante 2 h. Después de eso, una cierta cantidad de AgNO 3 se disolvió en la suspensión anterior. A esta mezcla se le añadió gota a gota una cierta concentración de Na 3 PO 4 solución (30 mL) bajo vigorosa agitación magnética durante 7 h. Los compuestos tal como se obtuvieron se separaron por centrifugación, se lavaron repetidamente con agua desionizada y se secaron en un horno de vacío a 60 ° C durante 8 h. Para investigar el efecto de Ag 3 PO 4 contenido en la propiedad fotocatalítica de los compuestos obtenidos, se fabricó una serie de muestras con diferentes Ag 3 PO 4 proporciones de masa de 5%, 10%, 20% y 40% y las muestras correspondientes se denominaron 5% en peso de Ag 3 PO 4 / BiFeO 3 , 10% en peso Ag 3 PO 4 / BiFeO 3 , 20% en peso Ag 3 PO 4 / BiFeO 3 y 40% en peso de Ag 3 PO 4 / BiFeO 3 , respectivamente. A modo de comparación, el compuesto denominado 20% en peso de Ag 3 PO 4 / BiFeO 3 -M también se preparó mediante mezcla mecánica directa de BiFeO 3 microcuboides y Ag 3 PO 4 micropartículas, donde Ag 3 PO 4 ocupa una fracción de masa del 20% en el compuesto.
Mediciones fotoelectroquímicas
La prueba de fotocorriente se llevó a cabo en la estación de trabajo electroquímica (CST 350) con una celda de tres electrodos como se describe en la literatura [49]. En este sistema de tres electrodos, se utilizaron una lámina de platino y un electrodo de calomelanos estándar como contraelectrodo y electrodo de referencia, respectivamente. El electrodo de trabajo se fabricó de la siguiente manera:se añadieron 15 mg de fotocatalizadores, 0,75 mg de negro de humo y 0,75 mg de fluoruro de polivinilideno (PVDF) en 1-metil-2-pirrolidiona (NMP) para producir una suspensión, que luego se revistió uniformemente sobre un 1.0 × 1,0 cm 2 Electrodo de vidrio de óxido de estaño dopado con fluoruro. Después de eso, el electrodo se secó a 60 ° C durante 5 h. Se empleó como fuente de luz visible una lámpara Xe de 300 W con un filtro de corte de 420 nm. La medición fotoelectroquímica se realizó en el 0,1-M Na 2 SO 4 solución electrolítica, y su valor de pH se midió en ~ 5.3. Las curvas de fotocorriente-tiempo (It) se midieron a un potencial de polarización fijo de 0.2 V. La prueba de espectroscopía de impedancia electroquímica (EIS) se realizó utilizando el pulso de voltaje sinusoidal con amplitud de 5 mV y en el rango de frecuencia de 10 −2 a 10 5 Hz.
Prueba de actividad fotocatalítica
Se evaluó la actividad fotocatalítica de las muestras hacia la degradación de AO7 y fenol bajo irradiación de luz visible. Normalmente, la concentración inicial de AO7 o fenol fue de 5 mg / L con una carga de catalizador de 0,5 g / L. Se midió que los valores de pH de AO7 y la solución de fenol eran ~ 6,8 y ~ 6,2, respectivamente. Antes de la iluminación, la mezcla se agitó en la oscuridad durante 0,5 h para lograr el equilibrio de adsorción-desorción de la molécula orgánica en la superficie de los catalizadores. Luego, esta solución de reacción se expuso a una lámpara de xenón de 300 W con un filtro de corte de 420 nm, y se midió la intensidad de luz correspondiente en ~ 50 mW cm -2 . Durante el experimento fotocatalítico, se recogió una pequeña cantidad de solución de reacción en los intervalos de tiempo dados y luego se centrifugó para separar los catalizadores. La concentración de AO7 o fenol se determinó detectando la absorbancia del sobrenadante a una longitud de onda determinada (λ AO7 =484 nm y λ fenol =270 nm) usando un espectrofotómetro UV-visible. Para evaluar la reutilización fotocatalítica de los fotocatalizadores, se realizó el experimento de reciclaje para la degradación de AO7. Una vez completada la primera prueba fotocatalítica, los fotocatalizadores se recogieron por centrifugación, se lavaron con agua destilada y se secaron. Los fotocatalizadores recogidos se añadieron a la solución de tinte reciente para el siguiente ciclo del experimento fotocatalítico. Para investigar la capacidad de catálisis tipo foto-Fenton de los fotocatalizadores, H 2 O 2 (5 mmol / L) se añadió a la solución de reacción. El procedimiento del experimento tipo foto-Fenton fue similar al proceso fotocatalítico anterior.
Caracterización
La pureza de fase de las muestras se investigó mediante difractómetro de rayos X (XRD, Bruker D8 Advanced) utilizando radiación Cu Kα. La morfología de las muestras se observó mediante un microscopio electrónico de barrido de emisión de campo (SEM, JEOL JSM-6701F) y un microscopio electrónico de transmisión de emisión de campo (TEM, JEOL JEM-2010). La composición de las muestras se midió mediante espectroscopía de rayos X de dispersión de energía. El estado químico del elemento se probó utilizando espectroscopía de fotoelectrones de rayos X (XPS, PHI-5702), donde la escala de energía de enlace de los datos de XPS se calibró contra el pico adventicio C 1s a la energía de enlace de 284,8 eV. Los espectros de reflectancia difusa ultravioleta-visible (UV-vis) de los productos se obtuvieron utilizando un espectrofotómetro UV-vis (PERSEE TU-1901) con BaSO 4 como una referencia. Los espectros PL de las muestras se registraron en un espectrofotómetro de fluorescencia (SHIMADZU RF-6000) con una longitud de onda de excitación de ~ 350 nm.
Resultados y discusión
Análisis XRD
La Figura 1 presenta los patrones XRD de BiFeO 3 , Ag 3 PO 4 y Ag 3 PO 4 / BiFeO 3 compuestos con diferente Ag 3 PO 4 contenido. Para BiFeO 3 desnudo muestra, todos los picos de difracción coinciden bien con la estructura romboédrica de BiFeO 3 (Tarjeta PDF n. ° 74-2016) y para Ag 3 desnudo PO 4 muestra, los picos de difracción se pueden indexar perfectamente a Ag 3 cúbicos PO 4 fase (tarjeta PDF nº 06-0505); esto indica que BiFeO 3 de alta pureza y Ag 3 PO 4 han sido preparados con éxito. En el caso de los compuestos, los patrones de XRD se pueden asignar a los picos de difracción característicos de BiFeO 3 y Ag 3 PO 4 y no aparecen picos de difracción de impurezas en los patrones. Además, se ve que al aumentar el contenido de Ag 3 PO 4 , la intensidad de los picos característicos de Ag 3 PO 4 aumenta gradualmente. Los resultados sugieren que los compuestos consisten en BiFeO 3 romboédrico y Ag 3 cúbicos PO 4 , y no se genera ninguna otra fase durante la preparación de los composites.
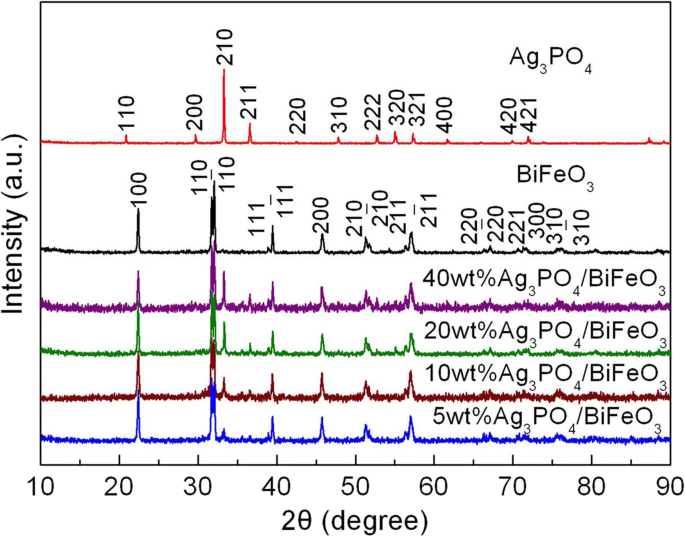
Patrones XRD de BiFeO 3 , Ag 3 PO 4 y Ag 3 PO 4 / BiFeO 3 compuestos
Observación morfológica
La morfología de las muestras se observó mediante SEM y TEM. La Figura 2a, b muestra la imagen SEM y la imagen TEM de BiFeO 3 desnudo , revelando que el BiFeO 3 preparado las partículas presentan una forma similar a un cuboide con un tamaño de 200 a 500 nm y tienen una superficie lisa. El recuadro de la Fig. 2a muestra la distribución de la relación de largo a ancho de BiFeO 3 partículas, lo que revela que la relación de largo a ancho varía de 1.1 / 1 a 2.5 / 1. Como se puede ver en la imagen TEM en la Fig. 2c, Ag 3 desnudo PO 4 consta de partículas irregulares en forma de esfera. La distribución de tamaño de Ag 3 PO 4 Las partículas se muestran en el recuadro de la Fig. 2c, lo que indica una amplia distribución de tamaño de partícula que varía de 110 a 180 nm. De la imagen TEM del 20wt% Ag 3 PO 4 / BiFeO 3 compuesto (Fig. 2d), se puede ver que las microesferas irregulares están unidas a la partícula en forma de cuboide. Las imágenes TEM de alta resolución (HRTEM) obtenidas de las diferentes partículas indican dos conjuntos distintos de franjas de celosía (recuadros en la Fig. 2d). El espaciado interplanar de ~ 0.288 nm coincide con BiFeO 3 (110) planos, mientras que la distancia interplanar de ~ 0.267 nm corresponde al Ag 3 PO 4 (210) aviones. Además, el análisis de EDX sugiere que el compuesto incluye todos los elementos de Ag 3 PO 4 y BiFeO 3 fases (Fig. 2e). Las señales de C y Cu observadas en el espectro EDX de la Fig. 2e podrían surgir de la microrred utilizada para soportar la muestra [50]. Estos resultados revelan que Ag 3 PO 4 las partículas están decoradas en la superficie de BiFeO 3 microcuboides, lo que resulta en la formación de Ag 3 PO 4 / BiFeO 3 heteroestructuras p-n.

un SEM (el recuadro es la distribución de la relación de largo a ancho de BiFeO 3 microcuboides) y b Imagen TEM de BiFeO 3 microcuboides. Imagen TEM de c Ag 3 PO 4 micropartículas (el recuadro es la distribución de tamaño de Ag 3 PO 4 micropartículas) y d 20% en peso Ag 3 PO 4 / BiFeO 3 muestra; recuadro muestra su imagen HRTEM. e Espectro EDX de 20% en peso de Ag 3 PO 4 / BiFeO 3 muestra
Análisis XPS
El análisis XPS se realizó para revelar los estados químicos de BiFeO 3 y 20% en peso de Ag 3 PO 4 / BiFeO 3 , como se muestra en la Fig. 3. La Figura 3a muestra el espectro XPS de alta resolución de Ag 3d en el compuesto. Los dos picos obvios a 373,8 y 367,7 eV se atribuyen al Ag 3d 3/2 y Ag 3d 5/2 energías de enlace de Ag + . La Figura 3b presenta el espectro XPS de alta resolución P 2p del compuesto. El pico de alrededor de 133,2 eV corresponde a la energía de enlace característica de P 5+ estado de oxidación en Ag 3 PO 4 [51]. La Figura 3c, d, muestra los espectros XPS de alta resolución de Bi 4f y Fe 2p, respectivamente. Para BiFeO 3 desnudo , el espectro de Bi 4f muestra dos picos fuertes en energías de enlace de 164,1 eV y 158,8 eV, pertenecientes al Bi 4f 5/2 y Bi 4f 7/2 , respectivamente, lo que indica que el ion Bi posee el estado de oxidación de + 3. Para el espectro de Fe 2p, el pico ubicado en 723,7 eV se asigna al Fe 2p 1/2 de Fe 3+ . Otra señal fuerte de XPS a ~ 711,6 eV se puede ajustar en dos picos a 711,7 y 709,9 eV. El pico a 709,9 eV corresponde a la energía de enlace de Fe 2p 3/2 de Fe 2+ . La energía de enlace a 711,7 eV pertenece al Fe 2p 3/2 de Fe 3+ . Además, se encuentra un pico satélite en alrededor de 718,2 eV, que se atribuye a los estados mixtos de oxidación del Fe. A partir del análisis XPS del elemento Fe, se puede ver que el Fe existe en forma de Fe 3+ y Fe 2+ en BiFeO 3 desnudo . Vale la pena señalar que las energías de unión de Bi 4f y Fe 2p en 20% en peso de Ag 3 PO 4 / BiFeO 3 exhiben un ligero cambio en comparación con BiFeO 3 , que se atribuye principalmente a la interacción entre BiFeO 3 y Ag 3 PO 4 . La Figura 3e muestra los espectros XPS de alta resolución de O 1s de BiFeO 3 y 20% en peso de Ag 3 PO 4 / BiFeO 3 . Para BiFeO 3 desnudo , la señal de O 1s se puede dividir en dos picos a 529,8 y 531,0 eV. La energía de enlace de 529,8 eV corresponde al oxígeno de la red, mientras que el pequeño pico a una energía de enlace más alta de 531,0 eV es causado por defectos superficiales y especies de oxígeno quimisorbidas. Comparado con BiFeO 3 desnudo , el pico de O 1 en el compuesto experimenta un cambio, que también se debe a la interacción entre Ag 3 PO 4 y BiFeO 3 .
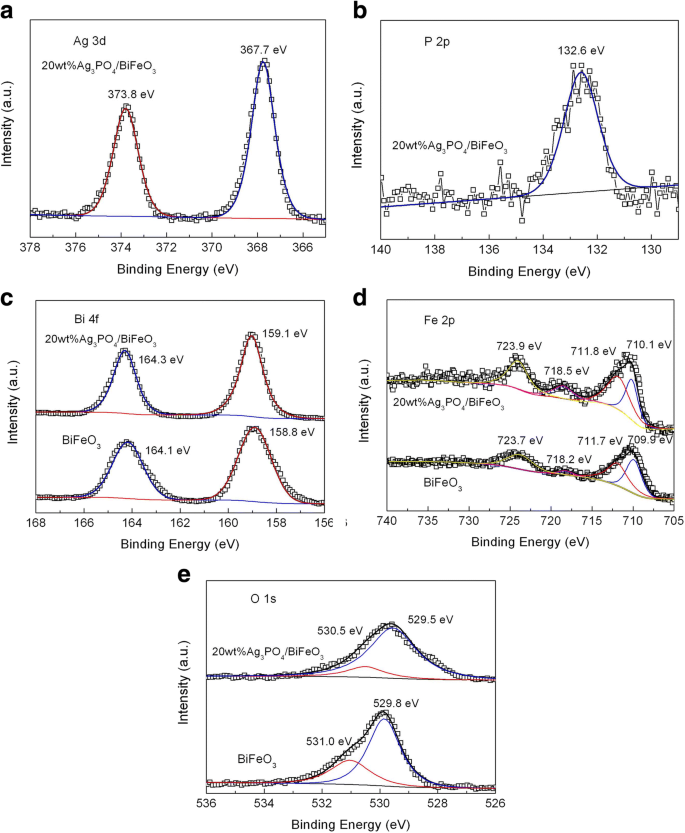
Espectros XPS de alta resolución de BiFeO 3 y 20% en peso de Ag 3 PO 4 / BiFeO 3 muestra. un Ag 3d y b P 2p de 20% en peso de Ag 3 PO 4 / BiFeO 3 muestra. c Bi 4f, d Fe 2p y e O1 de BiFeO 3 y 20% en peso de Ag 3 PO 4 / BiFeO 3 muestra
Propiedad de absorción óptica
El comportamiento de absorción óptica de las muestras se investigó midiendo sus espectros de reflectancia difusa UV-vis, como se presenta en la Fig. 4a. Los correspondientes espectros de absorción transformados a partir de los espectros de reflectancia difusa según la teoría de Kubelka-Munk (K-M) se muestran en la Fig. 4b [52]. Se ve que todas las muestras exhiben una importante absorción de luz a λ <600 nm. Para obtener el borde de absorción de las muestras, se llevó a cabo la primera derivada de la reflectancia (R) con respecto a la longitud de onda λ (es decir, dR / dλ), como se muestra en la Fig. 4c. El borde de absorción se puede determinar a partir de la longitud de onda máxima en los espectros derivados [53]. Se puede ver que el borde de absorción de luz del Ag 3 desnudo PO 4 se encuentra a ~ 527 nm, correspondiente a la energía de banda prohibida ( E g ) de ~ 2,35 eV. BiFeO desnudo 3 exhibe un borde de absorción alrededor de 567 nm, correspondiente a la E g de ~ 2,18 eV. Además del borde de absorción, se observa un pico débil a ~ 700 nm, que probablemente se atribuya a la existencia de estados de superficie en el medio de la banda prohibida de BiFeO 3 . Cuando se combina con Ag 3 PO 4 , la ventaja de absorción de BiFeO 3 no sufre cambios obvios, lo que indica que la introducción de Ag 3 PO 4 no tiene ningún efecto aparente en la estructura de banda prohibida de BiFeO 3 .
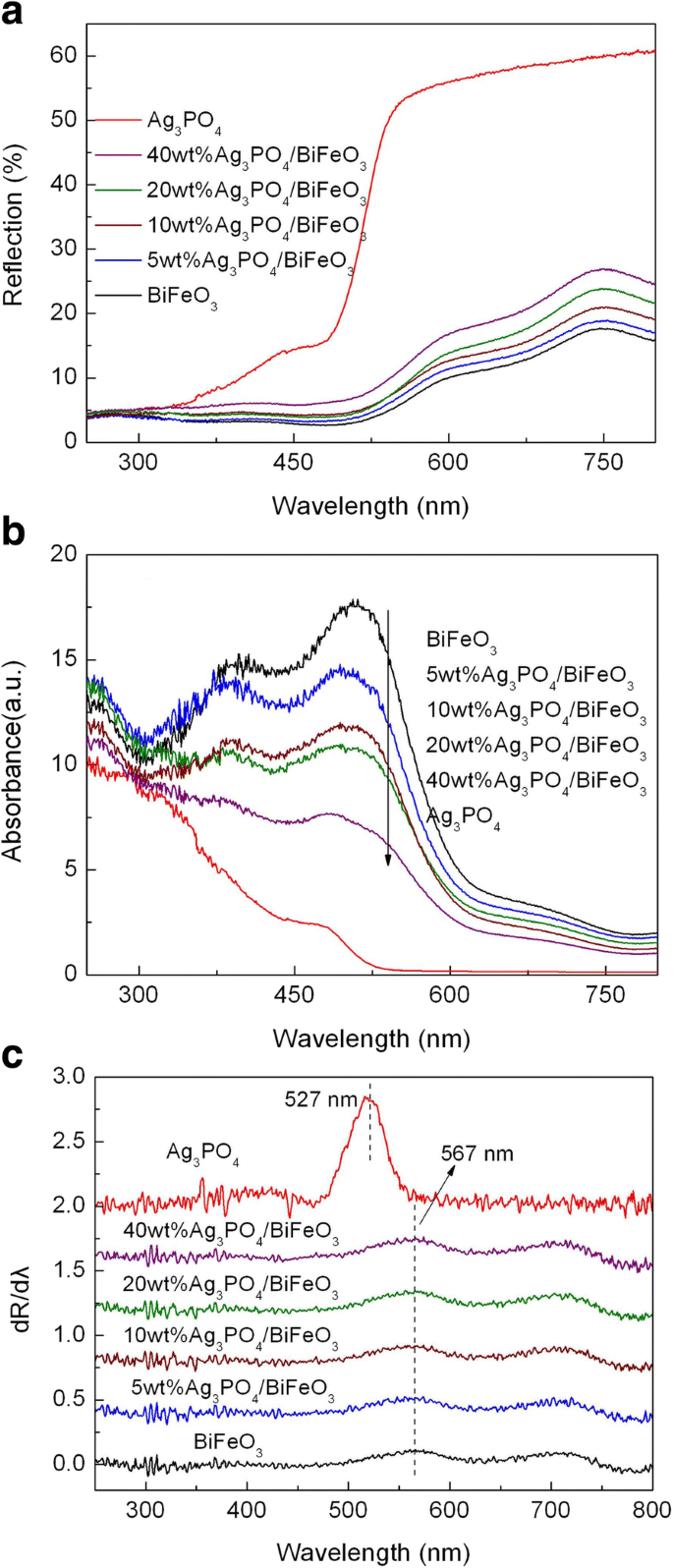
un Espectros de reflectancia difusa UV-visible de BiFeO 3 , Ag 3 PO 4 y Ag 3 PO 4 / BiFeO 3 composicion. b Los espectros de absorción correspondientes y c la correspondiente primera derivada de los espectros de reflectancia difusa
Medición de la actividad fotocatalítica
Se seleccionó AO7 como contaminante objetivo para evaluar el rendimiento fotocatalítico de las muestras. Se investigó la degradación fotocatalítica de AO7 bajo irradiación de luz visible, y el resultado se muestra en la Fig. 5. Antes de la reacción fotocatalítica, se realizaron experimentos de blanco y absorción. Se ve que no se detecta una degradación obvia del tinte bajo irradiación sin los catalizadores o en presencia de catalizadores sin irradiación, lo que sugiere que la autodegradación y absorción de AO7 durante el proceso fotocatalítico son insignificantes. BiFeO desnudo 3 tiene una actividad fotocatalítica débil y solo ~ 27% de AO7 se degrada con 120 min de irradiación. Cuando BiFeO 3 los microcuboides se combinan con Ag 3 PO 4 micropartículas, el Ag 3 formado PO 4 / BiFeO 3 los compuestos exhiben una actividad fotocatalítica superior a BiFeO 3 . Después de 120 min de exposición, el porcentaje de degradación de AO7 sobre las muestras es del orden del 40% en peso de Ag 3 PO 4 / BiFeO 3 (~ 91%)> 20% en peso de Ag 3 PO 4 / BiFeO 3 (~ 87%)> 10% en peso de Ag 3 PO 4 / BiFeO 3 (~ 69%)> 5% en peso de Ag 3 PO 4 / BiFeO 3 (~ 46%)> BiFeO 3 (~ 27%). Se encuentra que el rendimiento fotocatalítico de los compuestos exhibe una tendencia creciente con el aumento de Ag 3 PO 4 contenido. Entre estos compuestos, la eficiencia fotocatalítica de 40% en peso de Ag 3 PO 4 / BiFeO 3 está muy cerca del 20% en peso de Ag 3 PO 4 / BiFeO 3 . Por lo tanto, en el presente estudio, la proporción de masa más apropiada de Ag 3 PO 4 puede considerarse como un 20% en los composites. Además, vale la pena señalar que la muestra de mezcla mecánica 20% en peso de Ag 3 PO 4 / BiFeO 3 -M exhibe una actividad fotocatalítica mucho menor que el 20% en peso de Ag 3 PO 4 / BiFeO 3 . Esto revela que la construcción de heterounión entre BiFeO 3 y Ag 3 PO 4 es necesario para la mejora de la actividad fotocatalítica. Además, en comparación con BiFeO 3 / a-Fe 2 O 3 y BiFeO 3 -Bi 2 WO 6 compuestos [26, 29], el Ag 3 PO 4 / BiFeO 3 Los compuestos de heterounión preparados en el presente estudio manifiestan una mayor actividad fotocatalítica hacia la degradación del tinte.
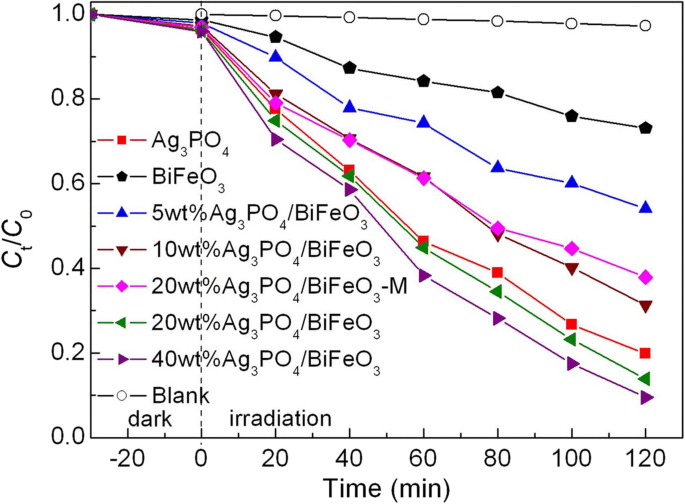
Actividades fotocatalíticas de BiFeO 3 y Ag 3 PO 4 / BiFeO 3 compuestos hacia la degradación de AO7 bajo irradiación de luz visible, junto con los resultados del experimento de absorción y el blanco
Para confirmar aún más la propiedad fotocatalítica de los compuestos, la degradación fotocatalítica del fenol incoloro sobre 20% en peso de Ag 3 PO 4 / BiFeO 3 y BiFeO 3 También se investigó bajo irradiación de luz visible. Como se muestra en la Fig. 6, la autodegradación y la absorción de fenol pueden despreciarse basándose en los resultados de los experimentos de blanco y absorción. Se puede ver que solo ~ 9% del fenol se degrada catalizado por BiFeO 3 después de 120 min de exposición. Considerando que, cuando 20% en peso de Ag 3 PO 4 / BiFeO 3 se utiliza como fotocatalizador, el porcentaje de degradación del fenol puede mejorarse obviamente en las mismas condiciones. El resultado sugiere que la degradación del tinte en el Ag 3 irradiado con luz visible PO 4 / BiFeO 3 los compuestos se atribuyen a su actividad fotocatalítica intrínseca en lugar de a la sensibilización al tinte.
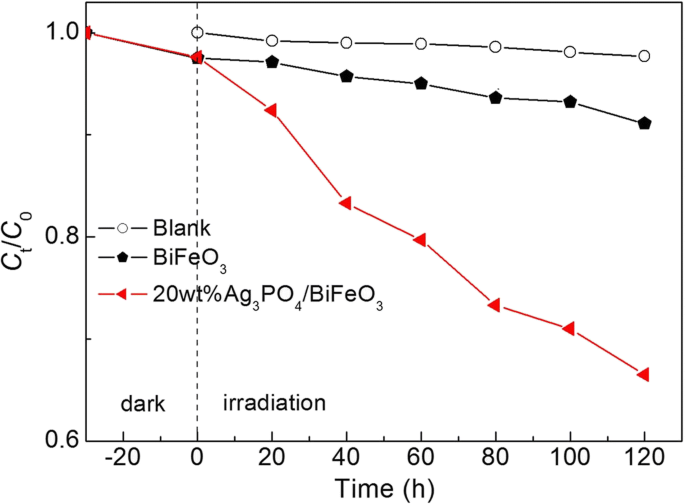
Degradación fotocatalítica de fenol sobre BiFeO 3 y 20% en peso de Ag 3 PO 4 / BiFeO 3 muestra bajo irradiación de luz visible, junto con el blanco y el resultado del experimento de absorción
Para evaluar la reutilización de los fotocatalizadores, los experimentos de degradación fotocatalítica de reciclaje de AO7 sobre 20% en peso de Ag 3 PO 4 / BiFeO 3 y Ag 3 PO 4 se llevaron a cabo en las mismas condiciones fotocatalíticas. Como se muestra en la Fig.7, después de tres ciclos de reciclaje sucesivos, el compuesto todavía exhibe una actividad fotocatalítica relativamente alta, mientras que la eficiencia de degradación sobre Ag 3 PO 4 sufre una evidente disminución. La Figura 8a, b muestra la imagen TEM y el patrón XRD del compuesto después del experimento de ciclismo, respectivamente. Está claro que Ag 3 PO 4 las micropartículas todavía están ensambladas en la superficie de BiFeO 3 microcuboides sin destrucción de las heteroestructuras, y no se observa ningún cambio evidente en la estructura cristalina. Esto sugiere que Ag 3 PO 4 / BiFeO 3 Los compuestos de heterounión p-n poseen una buena reutilización fotocatalítica.
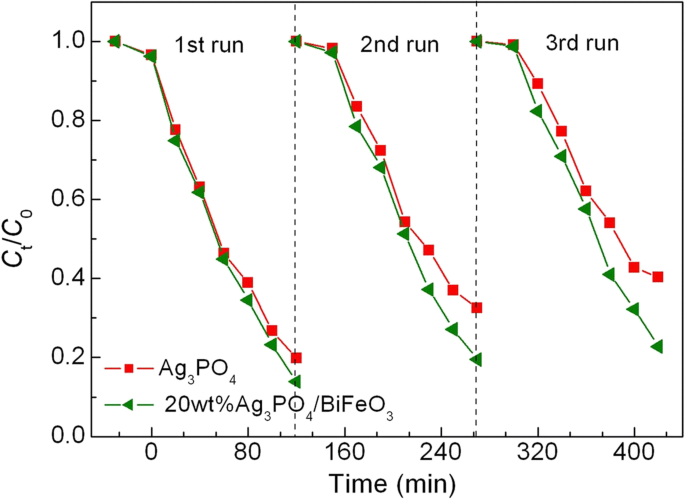
Degradación fotocatalítica de AO7 sobre Ag 3 PO 4 y 20% en peso de Ag 3 PO 4 / BiFeO 3 muestra durante tres ciclos
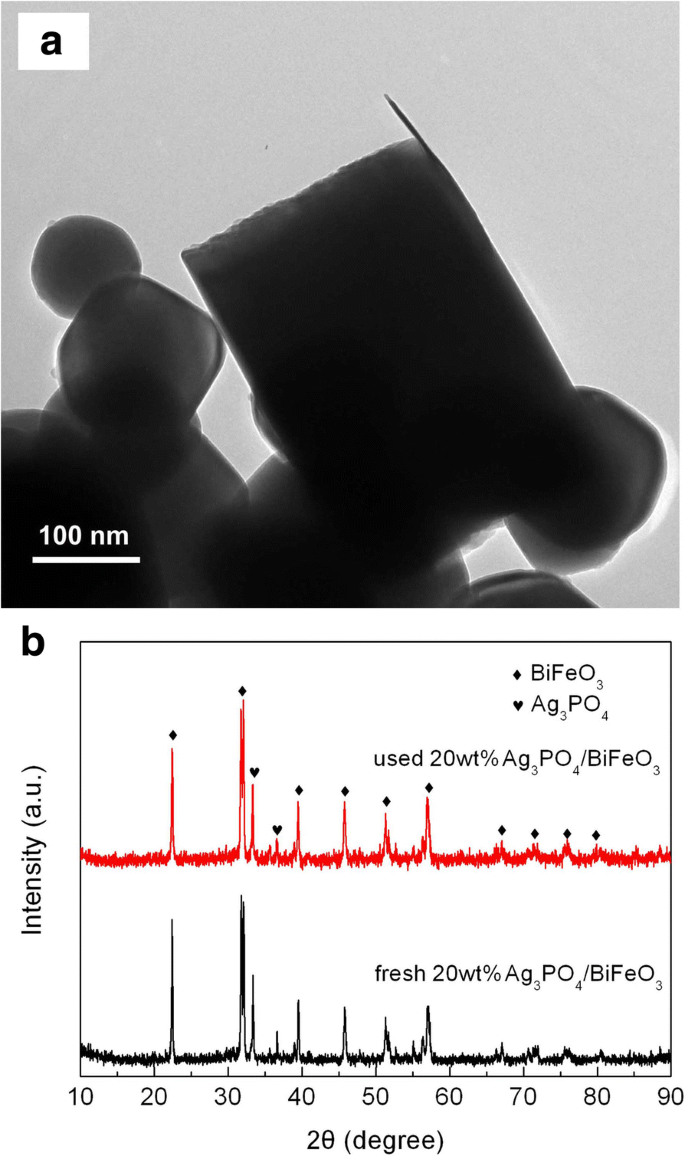
un Imagen TEM y b Patrón XRD de 20% en peso de Ag 3 PO 4 / BiFeO 3 muestra después de ciclar experimentos fotocatalíticos
Actividad catalítica tipo foto-Fenton
Aparte de su propiedad fotocatalítica, BiFeO 3 también exhibe una destacada capacidad de catálisis similar a la foto-Fenton [54,55,56]. La Figura 9 muestra la degradación similar a la foto-Fenton de AO7 sobre 20% en peso de Ag 3 PO 4 / BiFeO 3 y BiFeO 3 en presencia de H 2 O 2 . Comparado con los sistemas de reacción sin H 2 O 2 , la introducción de H 2 O 2 mejora notablemente el porcentaje de degradación del tinte. Este resultado se debe principalmente al mecanismo de reacción tipo foto-Fenton. En presencia de irradiación de luz visible y H 2 O 2 , Fe 3+ en la superficie de BiFeO 3 se puede convertir a Fe 2+ con la generación de radicales hidroxilo (• OH) (Ec. 1). En consecuencia, Fe 2+ puede reaccionar con H 2 O 2 para producir Fe 3+ y • OH (ecuación 2). Durante el ciclo de reacción anterior, se produce más • OH, que generalmente se considera una especie activa primaria para la degradación del tinte (como lo demuestra el experimento de captura de especies activas que se muestra en la Fig. 11). En el caso de BiFeO 3 desnudo , la alta tasa de recombinación de las cargas fotogeneradas limita el rendimiento de electrones fotogenerados, lo que tiende a suprimir la reducción de Fe 3+ en Fe 2+ (Ecuación 3). Esto conduce a una mejora limitada del porcentaje de degradación. Para Ag 3 PO 4 / BiFeO 3 Los compuestos, los electrones fotogenerados y los huecos se pueden separar de manera eficiente y, por lo tanto, hay más electrones fotogenerados disponibles para promover la conversión rápida de Fe 3+ en Fe 2+ (Ec. 3) [57]. Beneficiándose de esta reducción de electrones, el proceso de foto-Fenton para los compuestos es más eficiente que el de BiFeO 3 desnudo . Como resultado, Ag 3 PO 4 / BiFeO 3 Los compuestos de heterounión p-n manifiestan un rendimiento de foto-Fenton mucho mejorado.
$$ {\ mathrm {Fe}} ^ {3 +} + {\ mathrm {H}} _ 2 \ mathrm {O} + \ mathrm {h} \ upnu \ to {\ mathrm {Fe}} ^ {2+} + \ bullet \ mathrm {OH} + {\ mathrm {H}} ^ {+} $$ (1) $$ {\ mathrm {Fe}} ^ {2 +} + {\ mathrm {H}} _ 2 {\ mathrm {O}} _ 2 \ to {\ mathrm {Fe}} ^ {3 +} + \ bullet \ mathrm {OH} + {\ mathrm {O} \ mathrm {H}} ^ {-} $$ (2) $$ {\ mathrm {Fe}} ^ {3 +} + {\ mathrm {e}} ^ {-} \ to {\ mathrm {Fe}} ^ {2+} $$ (3)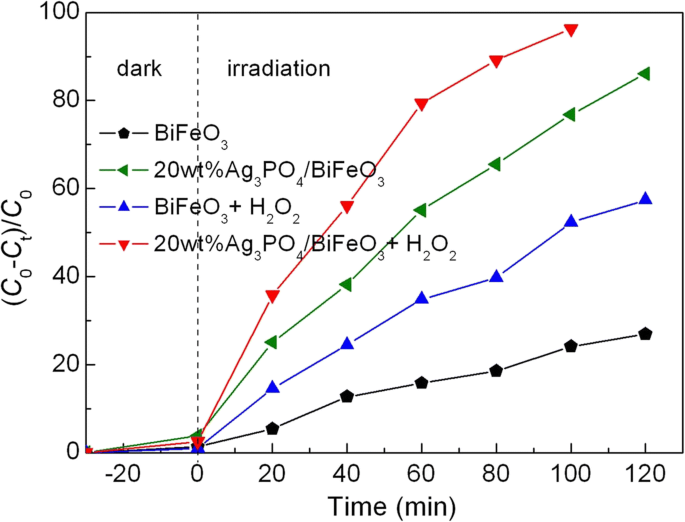
Actividades fotocatalíticas de BiFeO 3 y 20% en peso de Ag 3 PO 4 / BiFeO 3 muestra hacia la degradación de AO7 bajo irradiación de luz visible en presencia de H 2 O 2
Rendimiento de carga fotogenerado
Evaluar el comportamiento de separación de las cargas fotogeneradas de las muestras, las respuestas de fotocorriente transitoria, los espectros ESI y los espectros PL de BiFeO 3 y 20% en peso de Ag 3 PO 4 / BiFeO 3 se midieron. La Figura 10a muestra las curvas de fotocorriente-tiempo (I-t) de los fotocatalizadores bajo irradiación de luz visible intermitente con varios ciclos de encendido y apagado. Se puede ver que el valor de fotocorriente del compuesto es mucho más alto que el de BiFeO 3 desnudo. , lo que indica que la construcción de Ag 3 PO 4 / BiFeO 3 Las heterouniones p-n son beneficiosas para inhibir la recombinación de electrones y huecos fotogenerados. La Figura 10b presenta los espectros ESI de las muestras. Se puede ver que el compuesto exhibe radios de arco de impedancia más pequeños en comparación con BiFeO 3 , lo que sugiere la menor resistencia a la transferencia de carga del compuesto. Estos resultados revelan que la separación y migración de las cargas fotogeneradas se puede mejorar en el compuesto, proporcionando así más huecos fotoinducidos y electrones para la fotocatálisis. La Figura 10c muestra el gráfico de Mott-Schottky a una frecuencia de 3000 Hz para Ag 3 PO 4 . La pendiente negativa de la gráfica indica que Ag 3 PO 4 es un semiconductor de tipo p, lo que concuerda con el informe [43]. Los espectros PL de BiFeO 3 y 20% en peso de Ag 3 PO 4 / BiFeO 3 se muestran en la Fig. 10d. Las dos muestras exhiben picos de emisión obvios a ~ 522 nm, que se atribuyen principalmente a la recombinación de los pares de electrones / huecos fotogenerados. Vale la pena señalar que la intensidad PL del compuesto es mucho menor que la del BiFeO 3 desnudo. . Esto confirma además que la construcción de Ag 3 PO 4 / BiFeO 3 la heterounión promueve la separación de cargas fotoinducidas.
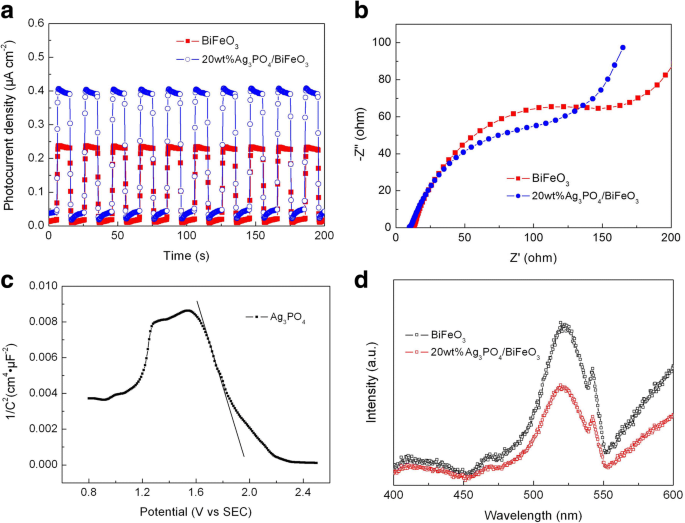
un Respuesta de fotocorriente transitoria y b Espectros EIS de BiFeO 3 y 20% en peso de Ag 3 PO 4 / BiFeO 3 muestra. c Gráfico de Mott-Schottky de Ag 3 PO 4 . d Espectros PL de BiFeO 3 y 20% en peso de Ag 3 PO 4 / BiFeO 3 muestras
Trampa de especies activas
Es bien sabido que el agujero fotogenerado (h + ), hidroxilo (• OH) y superóxido (• O 2− ) se consideran las principales especies activas responsables de la degradación fotocatalítica del tinte. Con el fin de aclarar el papel de las especies activas en el presente sistema fotocatalítico, se llevaron a cabo los experimentos de captura de especies activas, como se muestra en la Fig. 11. Se puede observar que el porcentaje de degradación de AO7 sufre una disminución obvia después de la introducción de etanol (depurador de • OH, 10% en volumen) o ácido etilendiaminotetraacético (EDTA, depurador de h + , 2 mM). Esto indica que • OH y h + son las principales especies activas implicadas en la reacción fotocatalítica. Después de la adición de benzoquinona (BQ, eliminador de • O 2− , 1 mM), se detecta una ligera disminución del porcentaje de degradación, lo que sugiere que • O 2− juega un papel relativamente menor en la degradación del tinte.
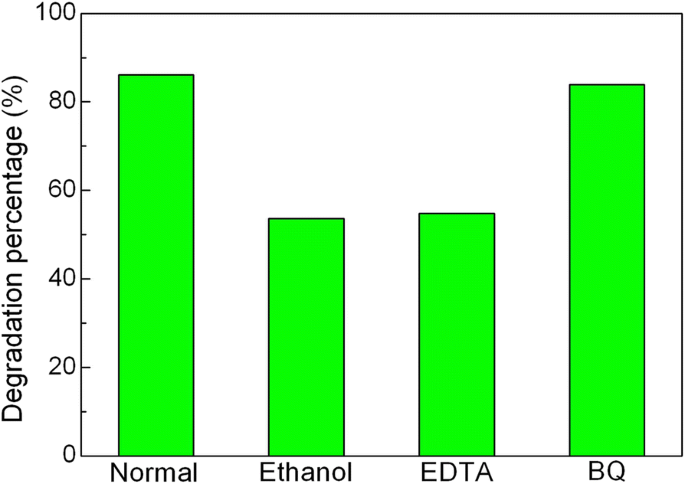
Efectos del etanol, EDTA y BQ en el porcentaje de degradación de AO7 sobre 20% en peso de Ag 3 PO 4 / BiFeO 3 compuesto
Mecanismo fotocatalítico propuesto
Es bien sabido que la capacidad redox y la migración de cargas fotogeneradas están muy relacionadas con los potenciales de banda de energía de los fotocatalizadores. La banda de valencia (VB) y la banda de conducción (CB) de BiFeO 3 y Ag 3 PO 4 se puede obtener usando la siguiente ecuación [58, 59]:
$$ {E} _ {\ mathrm {VB}} =X- {E} ^ {\ mathrm {e}} + 0.5 {E} _ {\ mathrm {g}} $$ (4) $$ {E} _ {\ mathrm {CB}} =X- {E} ^ {\ mathrm {e}} - 0.5 {E} _ {\ mathrm {g}} $$ (5)X es la electronegatividad absoluta del semiconductor (calculada como la media aritmética de la afinidad electrónica y la primera ionización de los átomos constituyentes). E e es la energía de los electrones libres en la escala del hidrógeno (~ 4,5 eV). La X valores de BiFeO 3 y Ag 3 PO 4 se estiman en 5,93 y 5,98 eV, respectivamente [43, 60]. Basado en las Ecs. (4) y (5), los potenciales CB / VB de BiFeO 3 y Ag 3 PO 4 se calculan en 0,34 / 2,52 V y 0,31 / 2,66 V frente a NHE, respectivamente. El diagrama de potencial de banda de energía de los dos fotocatalizadores se muestra en la Fig. 12a. Se informa que BiFeO 3 es un semiconductor de tipo ny su nivel de Fermi se encuentra cerca del CB [48]. Ag 3 PO 4 se demuestra que es un semiconductor de tipo p (ver Fig. 10c), cuyo nivel de energía de Fermi está cerca del VB [43]. Cuando BiFeO 3 se combina con Ag 3 PO 4 Para formar la heterounión p-n (ver Fig. 12b), la difusión de electrones y huecos entre los dos fotocatalizadores formará un campo eléctrico interno en la región de interfaz de la heterounión p-n con dirección de BiFeO 3 a Ag 3 PO 4 . Simultáneamente, el potencial de banda de energía de BiFeO 3 tiende a bajar junto con su nivel de Fermi mientras que el de Ag 3 PO 4 tiende a elevarse acompañado de su nivel de Fermi hasta que se alcanza un estado de equilibrio del nivel de Fermi de los dos fotocatalizadores. Tras la irradiación con luz visible, tanto BiFeO 3 y Ag 3 PO 4 puede excitarse para generar pares de huecos y electrones fotoinducidos. Bajo la promoción del campo eléctrico interno, los electrones fotogenerados en el CB de Ag 3 PO 4 migrará al CB de BiFeO 3 , mientras que los agujeros fotogenerados se transferirán desde el VB de BiFeO 3 al de Ag 3 PO 4 . Como resultado, la recombinación de cargas fotogeneradas se puede inhibir eficazmente, como lo demuestra el análisis de fotocorriente y PL (ver Fig. 10a, d). Por lo tanto, más electrones y huecos fotogenerados pueden participar en la reacción redox fotocatalítica, lo que conduce a la mejora de la actividad fotocatalítica del Ag 3 PO 4 / BiFeO 3 compuestos de heterounión p-n.
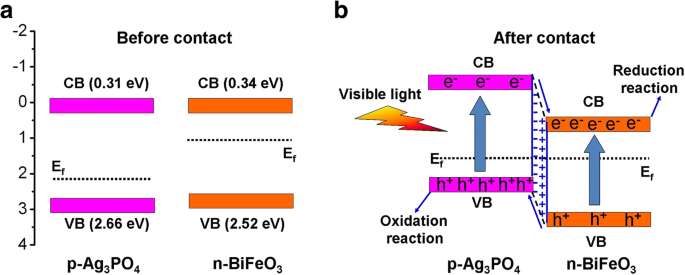
Ilustración esquemática del mecanismo fotocatalítico propuesto para Ag 3 PO 4 / BiFeO 3 compuesto. un Antes del contacto. b Después del contacto
Conclusiones
Ag 3 PO 4 / BiFeO 3 Los compuestos de heterounión p-n se sintetizaron mediante la decoración de Ag 3 PO 4 micropartículas esféricas en la superficie de BiFeO 3 microcuboides. Comparado con BiFeO 3 desnudo , los compuestos tal como se obtienen exhiben una actividad fotocatalítica de luz visible mejorada para la degradación de AO7 y fenol. Además, se ha demostrado que los materiales compuestos son excelentes catalizadores tipo foto-Fenton. La actividad fotocatalítica mejorada de los compuestos se atribuye principalmente a la separación eficiente de electrones y huecos fotogenerados debido a la formación de la heterounión p-n entre BiFeO 3 y Ag 3 PO 4.
Abreviaturas
- AO7:
-
Naranja ácida 7
- CB:
-
Banda de conducción
- DRS:
-
Espectros de reflectancia difusa UV-vis
- EDX:
-
Rayos X de energía dispersiva
- E g :
-
Energía Bandgap
- I-t:
-
Fotocorriente-tiempo
- NMP:
-
1-metil-2-pirrolidiona
- PVDF:
-
Fluoruro de polivinilideno
- R:
-
Reflectancia
- SEM:
-
Microscopio electrónico de barrido
- TEM:
-
Microscopio electrónico de transmisión
- VB:
-
Banda de valencia
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difractómetro de rayos X
Nanomateriales
- Nanofibras y filamentos para una mejor administración de fármacos
- Avances y desafíos de los nanomateriales fluorescentes para síntesis y aplicaciones biomédicas
- Síntesis hidrotermal de nanopartículas de In2O3, gemelos híbridos, discos hexagonales, heteroestructuras de ZnO para mejorar las actividades fotocatalíticas y la estabilidad
- Un nuevo fotocatalizador de heterounión Bi4Ti3O12 / Ag3PO4 con rendimiento fotocatalítico mejorado
- Síntesis fácil de óxido de estaño mesoporoso similar a un agujero de gusano a través del autoensamblaje inducido por evaporación y las propiedades mejoradas de detección de gas
- Síntesis en un solo recipiente de nanoplacas de Cu2ZnSnSe4 y su actividad fotocatalítica impulsada por la luz visible
- Síntesis sonoquímica de un solo paso y propiedades fotocatalíticas fáciles de compuestos de puntos cuánticos de grafeno / Ag3PO4
- Actividad fotocatalítica de nanocompuesto ternario de atapulgita-TiO2-Ag3PO4 para la degradación de rodamina B bajo irradiación solar simulada
- Fabricación y propiedad fotocatalítica de nuevos nanocompuestos SrTiO3 / Bi5O7I
- Un método sencillo para la preparación de heterounión Cu2O-TiO2 NTA con actividad fotocatalítica visible
- Influencia del dopaje de Mg en nanopartículas de ZnO para una evaluación fotocatalítica mejorada y análisis antibacteriano



