Fabricación y propiedad fotocatalítica de nuevos nanocompuestos SrTiO3 / Bi5O7I
Resumen
La novela SrTiO 3 / Bi 5 O 7 Los nanocompuestos se fabricaron con éxito mediante un enfoque de descomposición térmica. Las muestras preparadas se caracterizaron por espectros XRD, XPS, SEM, EDS, FTIR, DRS y PL. Los resultados muestran que el SrTiO 3 / Bi 5 O 7 Los nanocompuestos están compuestos de perovskita SrTiO 3 nanopartículas y Bi 5 tetragonal O 7 Yo nanorods. El SrTiO 3 / Bi 5 O 7 Los nanocompuestos I exhiben un excelente rendimiento fotocatalítico para la degradación de la solución de RhB bajo irradiación de luz solar simulada, que es superior al de Bi 5 prístino O 7 Yo y SrTiO 3 . En particular, el 30% en peso de SrTiO 3 / Bi 5 O 7 I nanocomposite se encuentra como los composites óptimos, sobre los cuales la degradación del tinte alcanza el 89,6% durante 150 min de fotocatálisis. La tasa de degradación fotocatalítica del 30% en peso de SrTiO 3 / Bi 5 O 7 Se encontró que el nanocompuesto es 3.97 veces y 12.5 veces más alto que el de Bi 5 desnudo O 7 Yo y SrTiO 3 , respectivamente. Los experimentos de captura de especies reactivas sugieren que \ (\ bullet {\ mathrm {O}} _ 2 ^ {-} \) y los huecos son las principales especies activas responsables de la degradación de RhB. Además, los espectros PL aclaran la separación efectiva de pares de electrones-huecos fotoinducidos. Además, el posible mecanismo fotocatalítico del SrTiO 3 / Bi 5 O 7 I nanocomposites también se dilucida en base a las evidencias experimentales.
Antecedentes
Los tintes de las industrias textil o de tintes han suscitado mucha preocupación por el impacto en la calidad de los recursos hídricos y los productos de degradación tóxicos y cancerígenos [1]. Por lo tanto, se necesitan técnicas de tratamiento más competentes para la eliminación completa de los tintes de las aguas residuales. Se han aplicado varios métodos convencionales que involucran métodos físicos, químicos y biológicos para la remediación del tinte de las aguas residuales [2]. Estos métodos pueden eliminar los tintes de las aguas residuales, pero a menudo son costosos, ineficaces y producen productos de desecho secundarios [3, 4]. Entre las diversas tecnologías de tratamiento de aguas residuales con tintes, la fotocatálisis basada en semiconductores ha recibido un gran interés y ha atraído la atención mundial [5, 6, 7]. Esto se debe a que utiliza la energía solar para la descomposición de los colorantes contaminantes, cuya fuente de energía es abundante, inagotable, no contaminante y gratuita [8, 9]. En la actualidad, TiO 2 es el fotocatalizador semiconductor más utilizado debido a su alta fotoactividad, bajo costo, estabilidad química y fotoquímica, no toxicidad y características ecológicas. Sin embargo, mostró una actividad fotocatalítica muy baja bajo irradiación de luz visible debido a su amplia banda prohibida de 3,2 eV y la rápida recombinación de portadores fotogenerados [10]. Para resolver eficazmente los problemas mencionados anteriormente, se ha dedicado mucho trabajo a la modificación de la superficie o la combinación de fotocatalizadores semiconductores [11]. Sin embargo, el desarrollo de fotocatalizadores novedosos y altamente eficientes sigue siendo un desafío importante [12].
Bi 5 O 7 I es un semiconductor de tipo p recién descubierto, que muestra un nivel de banda de valencia (VB) relativamente más positivo que otros oxiyoduros de bismuto al proporcionar más agujeros fotoexcitados y posteriormente facilita la separación de portadores fotogenerados [13]. Por lo tanto, el Bi 5 O 7 I fotocatalizador exhibe una alta actividad para la fotodegradación de rodamina B (RhB) en agua y acetaldehído bajo irradiación de luz visible [14]. Desafortunadamente, la aplicación práctica de Bi 5 O 7 El fotocatalizador en la descontaminación ambiental es todavía limitado, lo que se atribuye a su baja eficiencia de transferencia causada por la recombinación de electrones y huecos fotogenerados [15]. Con el fin de mejorar aún más la fotoactividad de Bi 5 O 7 Yo, se han realizado muchos intentos como el dopaje con metales o no metales [16], o el acoplamiento con otros semiconductores. Por ejemplo, Huang et al. g-C sintetizado 3 N 4 / Bi 5 O 7 I heterounión a través de un método de co-cristalización, y el compuesto exhibió una tasa de degradación 2,9 veces mayor que la de Bi 5 puro O 7 Yo [17]; Cheng y col. Bi 5 fabricado O 7 I / Bi 2 O 3 composite mediante el método de grabado químico, que mostró una alta actividad fotocatalítica en la descomposición del verde de malaquita [18]; Hu y col. informó que un compuesto que comprende Sr de tipo n 2 TiO 4 y Bi 5 de tipo p O 7 Mostré una fotoactividad mejorada debido a la inhibición de la recombinación de agujeros de electrones [19]; Cui y col. fabricado AgI / Bi 5 O 7 Híbrido mediante una simple reacción iónica de un solo paso y el AgI / Bi 5 O 7 El compuesto mejoró la actividad fotocatalítica [20], y así sucesivamente. Estos resultados mostraron que Bi 5 O 7 Los compuestos basados en I exhibieron un rendimiento fotocatalítico mejorado bajo irradiación de luz visible. Por lo tanto, podemos fabricar Bi 5 O 7 Compuestos basados en I mediante el acoplamiento a otro semiconductor con una banda de conducción adecuada (CB) y posiciones VB como un fotocatalizador de luz visible prometedor. Entre varios candidatos, el titanato de estroncio (SrTiO 3 ) es un material semiconductor de tipo n, que ha sido ampliamente estudiado debido a sus muchas propiedades excelentes, por ejemplo, estabilidad térmica, buena resistencia al calor, corrosión y resistencia [21, 22, 23]. Pure SrTiO 3 solo absorbe la luz ultravioleta debido a su amplia banda prohibida de 3,1 ~ 3,4 eV [24]. Afortunadamente, el VB de SrTiO 3 se coloca entre CB y VB de Bi 5 O 7 I, mientras que su CB se posiciona sobre el CB de Bi 5 O 7 I. Considerando los méritos estructurales de Bi 5 O 7 Yo, combinación de SrTiO 3 con Bi 5 O 7 I para formar el SrTiO 3 / Bi 5 O 7 El composite puede ser una forma viable y aconsejable de realizar la alta actividad fotocatalítica.
En este trabajo, una serie de SrTiO 3 / Bi 5 O 7 Los fotocatalizadores nanocompuestos fueron sintetizados por primera vez. Su fase cristalina, microestructura y propiedades ópticas se investigaron mediante una serie de técnicas. El SrTiO 3 / Bi 5 O 7 Los nanocompuestos mostraron un rendimiento fotocatalítico mejorado en la degradación de la solución de rodamina B (RhB) bajo irradiación de luz solar simulada. Además, el posible mecanismo fotocatalítico del SrTiO 3 / Bi 5 O 7 I nanocomposites también se dilucidó sobre la base de las evidencias experimentales.
Métodos
Preparación de SrTiO 3 / Bi 5 O 7 Yo composites
SrTiO 3 nanopartículas y SrTiO 3 / Los compuestos BiOI se sintetizaron en primer lugar mediante un método sol-gel como se describe en la bibliografía [25, 26]. SrTiO 3 / Bi 5 O 7 Luego, los compuestos se sintetizaron mediante una ruta de descomposición térmica. Todos los reactivos químicos se utilizaron directamente para los experimentos sin ninguna purificación adicional. Durante la descomposición térmica, el SrTiO 3 preparado / Los compuestos BiOI se colocaron en un horno de tubo y el programa de calentamiento se estableció de la siguiente manera:rampa a 5 ° C min - 1 a 500 ° C continuamente y manteniéndose a 500 ° C durante 3 h. Luego, el horno se enfrió naturalmente a temperatura ambiente para obtener 10% en peso de SrTiO 3 / Bi 5 O 7 Yo nanocompuesto. Otro SrTiO 3 / Bi 5 O 7 I materiales nanocompuestos con diferentes SrTiO 3 el contenido fue fabricado por un método similar.
Caracterización de la muestra
Las estructuras cristalinas de las muestras sintetizadas se caracterizaron mediante difracción de rayos X (XRD) con Cu K α radiación (D / max-2500, Rigaku). La morfología de las muestras se investigó mediante un microscopio electrónico de barrido de emisión de campo de ultra alta resolución (FE-SEM; SUAPR55, Alemania Zeiss) con espectroscopia de rayos X de dispersión de energía (EDS). El componente elemental de la superficie y el estado químico de las muestras se analizaron mediante espectroscopia de fotoelectrones de rayos X (XPS; Axis Ultra DLD, Kratos Analytical, Reino Unido) con un Al K α monocromatizado. Fuente de rayos X (hν =1486,6 eV). Los espectros de reflectancia difusa (DRS) ultravioleta-visible (UV-vis) se obtuvieron usando un espectrofotómetro UV-vis (UV-2450, Shimadzu). Los grupos funcionales en la superficie de las muestras se investigaron en una espectroscopia infrarroja de transformada de Fourier Nicolet iS50 (FTIR; Thermo Fisher Scientific, EE. UU.). Los espectros de emisión de fotoluminiscencia (PL) se midieron en un espectrómetro de fluorescencia de estado estable LH110911.
Estudios de evaluación fotocatalítica
La actividad fotocatalítica de los materiales se evaluó mediante la descomposición de RhB bajo irradiación de luz solar simulada (luz UV) en un aparato de fotorreacción. Después de 30 min de adsorción en la oscuridad, la adsorción-desorción está en equilibrio entre el fotocatalizador y las moléculas de RhB. Se utilizó una lámpara de xenón de 500 W como fuente de luz solar simulada (lámpara UV). Se dispersaron completamente cien miligramos de fotocatalizador en 100 ml de solución de RhB (20 mg / L). Durante cada experimento fotocatalítico, se pipetearon 3 ml de la suspensión cada 30 min y se centrifugaron para eliminar las partículas de catalizador. La concentración de RhB se midió usando un espectrofotómetro UV-vis.
Resultados y discusión
Análisis XRD
Los patrones de XRD de polvo proporcionan la estructura cristalina y la información de fase de las muestras sintetizadas, como se muestra en la Fig. 1. El SrTiO 3 la muestra está altamente cristalizada con una estructura de perovskita (JCPDS no. 35-0734). Los picos de difracción en el 2 θ los valores de 22,75 °, 32,39 °, 39,95 °, 46,47 °, 52,34 °, 57,78 °, 67,82 ° y 77,18 ° se pueden indexar a (100), (110), (111), (200), (210), Planos de cristal (211), (220) y (310), respectivamente [27]. No se detecta ningún otro pico de difracción específico. Del patrón XRD de Bi 5 puro O 7 I, se puede ver que los picos de difracción principal a 7.71 °, 13.31 °, 15.38 °, 23.19 °, 28.08 °, 31.09 °, 33.43 °, 46.28 °, 47.69 °, 53.45 °, 56.51 ° y 58.02 ° son conformes al (001), (201), (002), (401), (312), (004), (020), (024), (224), (714), (332) y (624) planos del Bi 5 O 7 I (JCPDS Nº 10-0548), respectivamente [28]. El pico más fuerte corresponde al plano cristalino (312) de Bi 5 O 7 I. Del patrón XRD del 30% en peso de SrTiO 3 / Bi 5 O 7 I nanocompuesto, se puede encontrar que todos los picos de difracción prominentes surgen de Bi 5 tetragonal O 7 Yo y perovskita SrTiO 3 . No se observan otros picos obvios de impureza, lo que indica que el Bi 5 O 7 Yo y SrTiO 3 las fases coexisten en el compuesto.
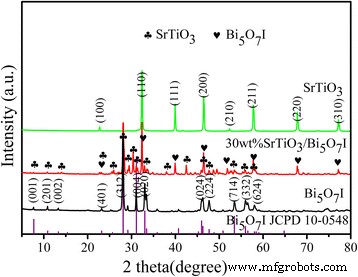
Patrones XRD de Bi 5 puro O 7 Yo, SrTiO 3 y 30% en peso de SrTiO 3 / Bi 5 O 7 Yo nanocompuesto
Análisis XPS
Las mediciones de XPS proporcionan más información para la evaluación de la composición elemental de la superficie y la pureza del 30% en peso de SrTiO 3 / Bi 5 O 7 Yo nanocompuesto. La energía de enlace obtenida en el análisis XPS se corrigió para la carga de la muestra haciendo referencia a C 1 sa 284,65 eV, y los resultados se muestran en la Fig.2. existencia de elementos Ti, Sr, Bi, I y O en el compuesto. Los dos picos fuertes a 159,02 y 164,25 eV se asignan respectivamente a Bi 4f 5/2 y Bi 4f 7/2 picos de Bi 3+ en el SrTiO 3 / Bi 5 O 7 I nanocomposites como se muestra en la Fig. 2b [29]. En los espectros XPS de I 3d que se muestran en la figura 2c, los dos picos fuertes a 617,88 y 630,22 eV, correspondientes a I 3d 5/2 y yo 3d 3/2 , respectivamente, sugieren el estado de oxidación -1 del yodo [30]. Como se muestra en la Fig. 2d, las energías de enlace de Ti 2p 3/2 y Ti 2p 1/2 corresponden a los picos a 457,90 y 463,80 eV en el espectro de Ti 2p, respectivamente. La separación máxima entre el Ti 2p 3/2 y Ti 2p 1/2 es 5,90 eV, lo que indica un estado de oxidación + 4 de Ti en SrTiO3 / Bi 5 O 7 Yo composites [31]. En la figura 2e, los picos a 132,50 y 134,25 eV corresponden a las energías de enlace de Sr 3d 5/2 y Sr 3d 3/2 , respectivamente, indicando su existencia en el Sr 2+ estado [32]. En la figura 2f, los picos de 529,65 y 531,25 eV se atribuyen a O 1 s. El pico a 529,65 eV se atribuye al oxígeno reticulado de SrTiO 3 / Bi 5 O 7 I nanocompuestos, y el pico de 531,25 eV se atribuye generalmente al oxígeno quimisorbido causado por las vacantes de oxígeno [33]. El resultado de XPS confirma aún más la formación de SrTiO 3 / Bi 5 O 7 I nanocomposites, y se ha logrado una integración íntima, lo que concuerda bien con los resultados de XRD.
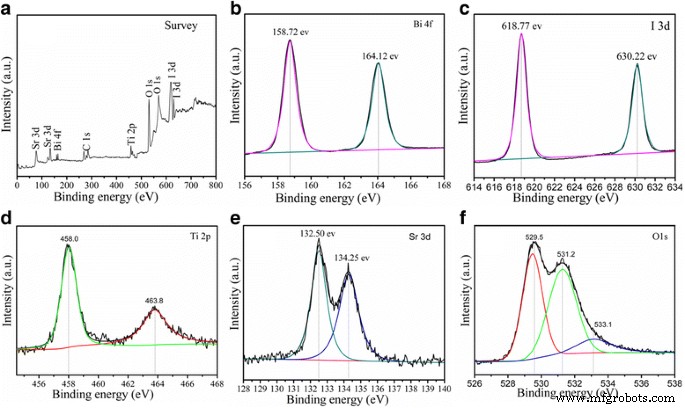
Patrones XPS del 30% en peso de SrTiO 3 / Bi 5 O 7 Yo nanocomposites: a encuesta, b Bi 4f, c Yo 3d, d Ti 2p, e Sr 3d y f O1s
Análisis SEM y EDS
Las composiciones y morfologías de la superficie de SrTiO 3 puro tal como se preparó , Bi 5 O 7 Yo y 30% en peso de SrTiO 3 / Bi 5 O 7 Se observaron nanocompuestos mediante FE-SEM. Como se ve en la Fig. 3a, SrTiO 3 puro está compuesto por partículas esferoidales o esféricas con diámetros en el rango de 50 ~ 300 nm. El SrTiO 3 de menor tamaño las partículas, obviamente, se agregan juntas hasta cierto punto. En la Fig. 3b, para Bi 5 O 7 En nanohojas, tienen un tamaño promedio de alrededor de 1 μm y un grosor en el rango de 80 ~ 100 nm, que es similar al reportado anteriormente [13]. Por el contrario, después de la combinación Bi 5 O 7 I no es de nanohojas sino de morfología de nanobarras, que está construida por muchas nanovarillas, como se muestra en la Fig. 3c. Para el Bi 5 O 7 En nanobarras, la longitud está en el rango de 100 ~ 300 nm y el diámetro promedio es de aproximadamente 80 nm. Puede verse claramente que SrTiO 3 las partículas están firmemente adheridas a la superficie de Bi 5 O 7 I nanovarillas, y se cree que es favorable para el rendimiento fotocatalítico. Además, se utilizó EDS para analizar la composición química del 30% en peso de SrTiO 3 / Bi 5 O 7 Yo nanocompuesto. Como se muestra en la Fig. 3d, la señal C observada se puede derivar del adhesivo conductor que se usa para fijar la muestra. Cabe señalar que el EDS se utiliza adecuadamente para la determinación cuantitativa del contenido de elementos pesados (por ejemplo, Bi, Ti, I y Sr), pero no para los elementos ligeros (por ejemplo, P y O) [34]. La relación atómica de Bi a I se obtiene como 11/63 del espectro EDS, que concuerda bien con la relación atómica Bi / I de Bi 5 O 7 Yo fase. La relación atómica de Sr / Bi está muy cerca de 1 / 12.5, lo que implica que SrTiO 3 fase representa aproximadamente el 30% del contenido molar total del compuesto.
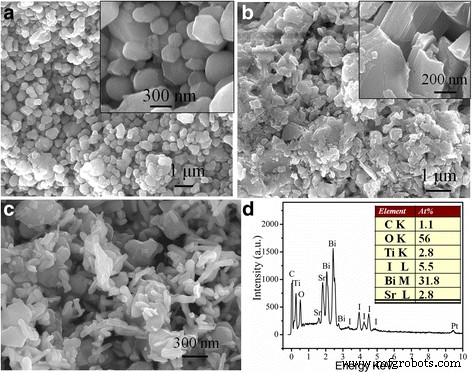
Imágenes SEM de a SrTiO puro 3 , b puro Bi 5 O 7 Yo, c 30% en peso de SrTiO 3 / Bi 5 O 7 Yo nanocompuesto y d Espectro EDS de 30% en peso de SrTiO 3 / Bi 5 O 7 Yo nanocompuesto
Análisis de propiedades ópticas
Los espectros UV-vis DRS de los diferentes catalizadores se muestran en la Fig. 4a. El SrTiO 3 puro exhibe un borde de la banda de absorción a 380 nm en la región UV, lo que podría atribuirse a la energía de la banda prohibida amplia [35, 36]. El Bi 5 O 7 I muestra un borde de absorción mucho más largo de 520 nm, que puede responder a la luz visible. El borde de absorción del SrTiO 3 / Bi 5 O 7 Los nanocompuestos miden 480 ~ 520 nm. Comparado con SrTiO 3 puro , después de acoplarse con Bi 5 O 7 I nanohojas, la intensidad máxima de absorción del SrTiO 3 / Bi 5 O 7 I nanocomposites mejorado significativamente.
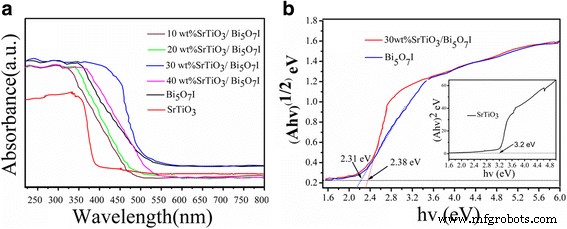
un Espectros DRS de SrTiO 3 / Bi 5 O 7 Yo nanocomposites y b la trama Tauc de (Ahν) 1/2 versus hν el Bi 5 puro O 7 Yo y 30% en peso de SrTiO 3 / Bi 5 O 7 I nanocompuesto, el diagrama de Tauc de (Ahν) 2 versus hν el puro SrTiO 3 imagen insertada de b
Según los espectros de absorción, el E g del semiconductor se puede calcular a partir de Aһν =A ( һν - E g ) n / 2 ecuación [37]. Los valores de n para SrTiO 3 y Bi 5 O 7 Tengo 4 y 1, respectivamente. La energía de banda prohibida del SrTiO 3 se puede estimar a partir de la gráfica (Aһν) 2 versus energía ploton (һν), y la energía de banda prohibida de Bi 5 O 7 Se puede estimar a partir de la trama (Aһν) 1/2 versus һν. La intersección de la tangente a la X El eje da una aproximación de la energía de la banda prohibida de las muestras como se muestra en la Fig. 4b. Los valores de la energía de la banda prohibida de Bi 5 puro O 7 Yo, 30% en peso de SrTiO 3 / Bi 5 O 7 Yo nanocompuesto y SrTiO puro 3 son aproximadamente 2,31, 2,38 y 3,2 eV, respectivamente, que son consistentes con los valores informados en la literatura relevante [38, 39].
Análisis de espectroscopia FTIR
El Bi 5 O 7 Yo y SrTiO 3 / Bi 5 O 7 Los nanocompuestos se caracterizaron aún más utilizando espectroscopía FTIR para analizar su enlace químico. Como se muestra en la Fig. 5. Se puede ver que en casi todas las muestras las bandas de adsorción de 3445.5 y 1621.9 cm −1 se debieron a la vibración de estiramiento O – H y la vibración de deformación de las moléculas de agua quimisorbidas [40]. La banda a 2906,5 cm −1 se atribuye a la vibración de estiramiento Ti – O [41]. Los otros picos en el rango de 1471,6 a 500 cm −1 corresponden a los modos de estiramiento y deformación involucrados en enlaces Bi – O [42].
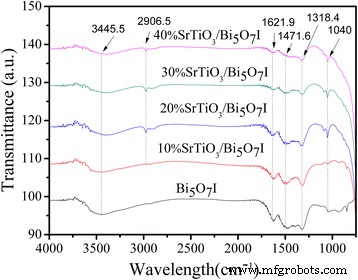
Espectros FTIR del Bi 5 puro O 7 Yo y SrTiO 3 / Bi 5 O 7 Yo nanocomposites
Actividad fotocatalítica
Como Bi 5 O 7 Yo y SrTiO 3 tienen una fotoabsorción muy distinta y SrTiO 3 responde principalmente a la luz ultravioleta, la luz solar simulada y la luz ultravioleta en las mismas condiciones se emplean por separado como fuente de luz para explorar el rendimiento fotocatalítico de Bi 5 O 7 Yo, SrTiO 3 y SrTiO 3 / Bi 5 O 7 Yo nanocomposites. La Figura 6a muestra las curvas de degradación de RhB bajo irradiación de luz solar simulada. Se observa que RhB es estable y difícilmente se descompone sin el catalizador bajo irradiación solar simulada durante 150 min. El SrTiO 3 puro muestra una actividad catalítica moderada, y solo se logró una reducción de RhB del 18% después de 150 min de irradiación. Se atribuye a la baja absorción de luz de SrTiO 3 en la región de luz visible o sus grandes energías de banda prohibida. Pure Bi 5 O 7 Muestro una actividad muy distinta que degrada más del 52% de RhB en 150 min. Comparado con SrTiO 3 puro y Bi 5 O 7 Yo, el SrTiO 3 / Bi 5 O 7 Los nanocompuestos muestran una actividad fotocatalítica significativamente mejorada en las mismas condiciones. Con el aumento de SrTiO 3 contenido de 10 a 40%, la actividad fotocatalítica de los compuestos aumenta primero y luego disminuye, y la actividad fotocatalítica más alta se observa para el 30% en peso de SrTiO 3 / Bi 5 O 7 Yo nanocompuesto. Para este compuesto óptimo, la degradación del tinte alcanza aproximadamente el 89,6% bajo irradiación de luz solar simulada durante 150 min. Una actividad tan alta se puede atribuir a los electrones fotogenerados que tienen una movilidad y separación más rápidas.
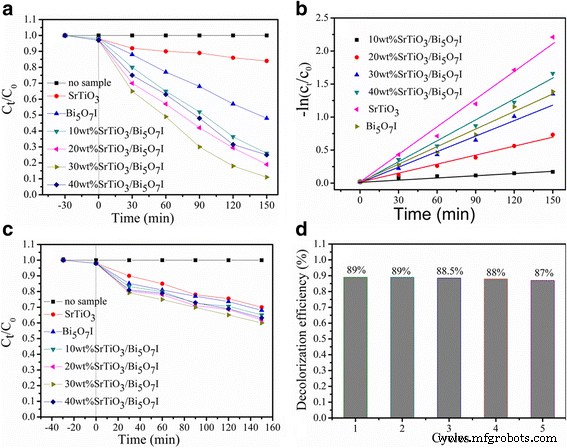
un Degradación fotocatalítica de la solución de RhB para todas las muestras bajo irradiación de luz solar simulada. b Gráficas de -ln (C t / C 0 ) frente al tiempo para todas las muestras. c Degradación fotocatalítica de la solución RhB para todas las muestras bajo iluminación con luz ultravioleta. d Eficiencia cíclica de degradación de RhB sobre SrTiO 3 / Bi 5 O 7 Yo nanocomposites
Para comprender mejor la cinética de reacción de la degradación fotocatalítica de RhB para diferentes fotocatalizadores, se calculó la eficiencia de la degradación fotocatalítica mediante la siguiente ecuación:ln ( C 0 / C t ) = K aplicación t , donde C 0 , C t y K aplicación son representativos de la concentración inicial, la concentración en el tiempo t y la constante de velocidad de pseudoprimer orden aparente, respectivamente [43]. El -ln (C t / C 0 ) muestra una buena relación lineal con el tiempo de irradiación y la reacción fotocatalítica pertenece a la reacción de pseudoprimer orden como se muestra en la Fig. 6b. El k aplicación valores obtenidos para Bi 5 O 7 Yo, SrTiO 3 , 10% en peso de SrTiO 3 / Bi 5 O 7 Yo, 20% en peso de SrTiO 3 / Bi 5 O 7 Yo, 30% en peso de SrTiO 3 / Bi 5 O 7 I, y 40% en peso de SrTiO 3 / Bi 5 O 7 Los nanocompuestos miden 1,16 × 10 −3 , 4,88 × 10 −3 , 9 × 10 −3 , 1,06 × 10 −2 , 1,45 × 10 −2 y 9,24 × 10 −3 min −1 , respectivamente. Es evidente que el 30% en peso de SrTiO 3 / Bi 5 O 7 I nanocomposite manifiesta la máxima constante de velocidad de reacción fotocatalítica, que es aproximadamente 2,97 veces mayor que la del Bi 5 desnudo O 7 I, y 12,5 veces mayor que el de SrTiO 3 puro .
Las curvas de degradación de RhB sobre todas las muestras bajo irradiación con luz ultravioleta se muestran además en la Fig. 6c. Puede verse claramente que el fenómeno es similar al de la Fig. 6a. Sin embargo, todas las muestras presentan una eficacia fotocatalítica muy baja debido a la poca absorción de luz ultravioleta, y la sensibilización del colorante tiene un efecto sobre la actividad fotocatalítica. Como se muestra en la Fig. 6a, el 30% en peso de SrTiO 3 / Bi 5 O 7 I nanocomposite sigue mostrando la mejor actividad; sin embargo, la fotodegradación de RhB es solo del 40% en 150 min. Estos resultados demuestran que el SrTiO 3 / Bi 5 O 7 Los nanocompuestos poseen una actividad fotocatalítica más eficiente bajo irradiación de luz solar simulada.
La estabilidad y reutilización del 30% en peso de SrTiO 3 / Bi 5 O 7 El nanocompuesto se realizó repitiendo las pruebas de degradación del RhB. Después de cada ciclo, el SrTiO 3 / Bi 5 O 7 Los nanocompuestos se reutilizaron en el siguiente ciclo antes de ser recolectados por centrifugación, se lavaron varias veces con agua desionizada y alcohol etílico y finalmente se secaron a 80 ° C durante 3 h. Como se muestra en la Fig. 6d, la actividad fotocatalítica del compuesto no disminuye obviamente incluso después del quinto reciclado bajo irradiación solar simulada, lo que sugiere una buena estabilidad para reciclar el 30% en peso de SrTiO 3 / Bi 5 O 7 Yo nanocompuesto.
Discusión sobre el mecanismo fotocatalítico
Para obtener una idea de las especies activas involucradas en la fotodegradación de SrTiO 3 / Bi 5 O 7 En nanocomposites, llevamos a cabo experimentos de captura de especies reactivas sobre el 30% en peso de SrTiO 3 / Bi 5 O 7 I nanocompuesto para conocer las principales especies activas en la reacción fotocatalítica. Como se muestra en la Fig. 7, la adición de isopropanol (IPA) casi no tiene ningún efecto sobre la degradación de RhB sobre el SrTiO 3 / Bi 5 O 7 I nanocomposites, lo que indica que no se generan radicales • OH. Por el contrario, se observa una disminución significativa en la degradación del tinte después de la adición de benzoquinona (BQ) o sal disódica del ácido etilendiaminotetraacético (EDTA-2Na), lo que implica que \ (\ bullet {\ mathrm {O}} _ 2 ^ {- } \) y los agujeros son las principales sustancias reactivas para la fotodegradación del RhB.
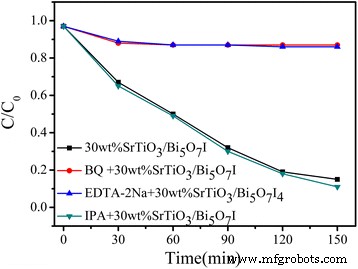
La constante de eficiencia de degradación de RhB sobre el 30% en peso de SrTiO 3 / Bi 5 O 7 Realizo nanocompuestos en presencia de varios carroñeros
Para investigar la separación de carga de los fotocatalizadores preparados, se introdujo además la espectroscopia PL. La Figura 8 muestra la comparación de los espectros PL entre Bi 5 O 7 Yo y 30% en peso de SrTiO 3 / Bi 5 O 7 Yo nanocompuesto bajo la excitación a 320 nm. Los espectros PL de ambas muestras se caracterizan por un pico a 497 nm, que se atribuye a la emisión de energía de transición de banda prohibida de Bi 5 O 7 I. Sin embargo, hay una fuerte disminución en la intensidad del 30% en peso de SrTiO 3 / Bi 5 O 7 Yo nanocompuesto. Este fenómeno demuestra una separación eficiente de los portadores fotogenerados dentro del compuesto entre SrTiO 3 y Bi 5 O 7 I.
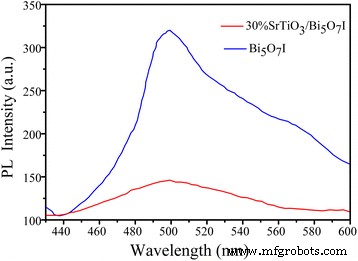
Espectros PL de Bi 5 puro O 7 I nanohojas y 30% en peso de SrTiO 3 / Bi 5 O 7 Yo nanocompuesto
Para comprender mejor el mecanismo de la actividad fotocatalítica mejorada de SrTiO 3 / Bi 5 O 7 I nanocomposites bajo irradiación de luz solar simulada, las posiciones CB y VB correspondientes para SrTiO 3 y Bi 5 O 7 Teóricamente se calcula de acuerdo con \ ({E} _ {VB} =\ chi - {E} _0 + \ frac {1} {2} {E} _g \) y E CB = E VB - E g , donde E VB es el potencial VB, E CB es el potencial CB, E 0 es la energía de los electrones libres en la escala del hidrógeno (aprox. 4,5 eV), E g es la energía de la banda prohibida, y χ se calcula como la media geométrica de las electronegatividades de Mulliken de los componentes del semiconductor [44]. Por lo tanto, la E VB y E CB de Bi 5 O 7 Se calculó que era 2,92 y 0,56 eV, mientras que las energías de SrTiO 3 fueron alrededor de 2,03 y -1,15 eV, respectivamente. Estos dos semiconductores tienen potenciales de banda adecuados y, por lo tanto, pueden construir una estructura compuesta.
De acuerdo con los resultados anteriores, una ilustración esquemática de las bandas de energía que coinciden entre SrTiO 3 y Bi 5 O 7 I y las posibles formas de transferencia de cargas se muestran en la Fig. 9. Ambos SrTiO 3 y Bi 5 O 7 Estoy excitado bajo luz solar simulada (luz ultravioleta) y los electrones en el VB de ambos SrTiO 3 y Bi 5 O 7 Estaría emocionado con el CB, los agujeros permanecieron en su VB. Como el potencial CB de SrTiO 3 (- 1,15 eV) es más negativo que el de Bi 5 O 7 I (+ 0.56 eV), los electrones de SrTiO 3 se inyectan fácilmente en el CB de Bi 5 O 7 I. Los electrones fotogenerados podrían reaccionar con O 2 para producir el radical superóxido de especies de oxígeno activo (\ (\ bullet {\ mathrm {O}} _ 2 ^ {-} \)), que luego induce la degradación del RhB [45]. Por otro lado, los agujeros en el VB de Bi 5 O 7 Migro al VB de SrTiO 3 , lo que resulta en una separación efectiva de los electrones y huecos fotoinducidos. De esta forma, los electrones y huecos fotogenerados se separan de forma eficaz en el SrTiO 3 / Bi 5 O 7 Yo nanocomposites. El VB de SrTiO 3 es 2,23 eV, menor que el potencial redox de • OH / H 2 O (+ 2,27 eV). Según los informes pertinentes [46, 47], el VB de SrTiO 3 es insuficiente para oxidar H 2 O en • OH. Indica que \ (\ bullet {\ mathrm {O}} _ 2 ^ {-} \) y los agujeros son las principales especies activas de oxígeno para SrTiO 3 / Bi 5 O 7 I nanocomposites en la decoloración RhB, bajo irradiación de luz solar simulada. Por lo tanto, el SrTiO 3 sintetizado / Bi 5 O 7 I fotocatalizador nanocompuesto exhibe un rendimiento fotocatalítico mucho mayor que el de SrTiO 3 y Bi 5 O 7 I.
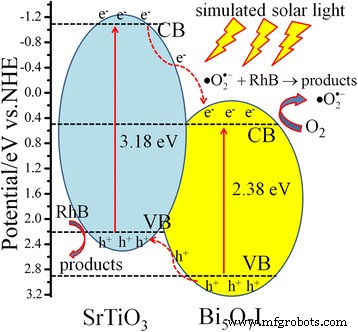
El diagrama esquemático de bandas de energía y el posible proceso fotocatalítico de SrTiO 3 / Bi 5 O 7 Yo nanocomposites
Conclusiones
En resumen, la novela SrTiO 3 / Bi 5 O 7 Los fotocatalizadores de nanocomposites han sido diseñados y fabricados mediante un enfoque solvotermal junto con la descomposición térmica. Las mediciones de XRD, XPS y EDS ilustran que los productos son realmente SrTiO 3 / Bi 5 O 7 Yo nanocomposites. El análisis UV-vis DRS muestra que el SrTiO 3 / Bi 5 O 7 Los nanocompuestos tienen un buen rendimiento de absorción de luz. The results of PL spectra show that the recombination of photoinduced electron-hole pairs is obviously inhibited in SrTiO3 /Bi5 O 7 I nanocomposites. The obtained nanocomposites show a good stability and a recycling capacity in the photocatalytic process. The as-synthesized SrTiO3 /Bi5 O 7 I photocatalysts exhibit a highly efficient photocatalytic property for the degradation of RhB under simulated solar light irradiation, which is superior to that of SrTiO3 and Bi5 O 7 I. The outstanding photocatalytic activity of the photocatalysts is ascribed to the efficient separation and migration of photogenerated charge carriers. The \( \bullet {\mathrm{O}}_2^{-} \) and holes are the main oxygen-active species causing the dye degradation. This work could provide insights into the design and development of other excellent photocatalytic materials for environmental and energy applications.
Abreviaturas
- BQ:
-
Benzoquinone
- CB:
-
Conduction band
- DRS:
-
Diffuse reflectance spectra
- EDS:
-
Energy-disperse X-ray spectroscopy
- EDTA-2Na:
-
Ethylenediaminetetraacetic acid disodium salt
- FE-SEM:
-
Field-emission scanning electron microscope
- FTIR:
-
Fourier-transform infrared spectroscopy
- IPA:
-
Isopropanol
- PL:
-
Photoluminescence
- RhB:
-
Rhodamine B
- UV-vis:
-
Ultraviolet-visible
- VB:
-
Valence band
- XPS:
-
X-ray photoelectron spectroscopy
- XRD:
-
Difracción de rayos X
Nanomateriales
- Rendimiento fotocatalítico de luz visible de nanocompuestos de ZnO / g-C3N4 dopado con N
- Preparación y rendimiento fotocatalítico de fotocatalizadores LiNb3O8 de estructura hueca
- Un nuevo fotocatalizador de heterounión Bi4Ti3O12 / Ag3PO4 con rendimiento fotocatalítico mejorado
- Fabricación de películas delgadas de SrGe2 en sustratos Ge (100), (110) y (111)
- Síntesis en un solo recipiente de nanoplacas de Cu2ZnSnSe4 y su actividad fotocatalítica impulsada por la luz visible
- La fabricación y el rendimiento de absorción de ondas electromagnéticas de alta eficiencia de los nanocompuestos estructurados CoFe / C Core-Shell
- Fabricación y caracterización de nanoclips de ZnO mediante el proceso mediado por poliol
- Fabricación de nanofibras helicoidales CA / TPU y análisis de su mecanismo
- Modulación de la morfología y propiedad óptica de nanoestructuras de aleación de PdAuAg y PdAg multimetálicas
- Fabricación de heteroestructuras jerárquicas de núcleo-capa de ZnO @ NiO para un rendimiento fotocatalítico mejorado
- Síntesis fácil y actividad fotocatalítica de luz visible mejorada de nuevos compuestos de heterounión p-Ag3PO4 / n-BiFeO3 para la degradación del tinte



