Síntesis en un solo recipiente de nanoplacas de Cu2ZnSnSe4 y su actividad fotocatalítica impulsada por la luz visible
Resumen
A SeO 2 La solución de etanol como precursor fácil se ha utilizado para la preparación de Cu 2 cuaternario ZnSnSe 4 (CZTSe) nanoplacas. Las nanoplacas CZTSe monodispersas monofásicas se han preparado con éxito mediante un sencillo método químico térmico de un solo recipiente. Las nanoplacas CZTSe preparadas muestran una morfología uniforme con un intervalo de banda de ~ 1,4 eV. Como prueba de concepto, las nanoplacas CZTSe se han utilizado como fotocatalizador impulsado por luz visible para la degradación del colorante rodamina B y muestran una alta actividad fotocatalítica y estabilidad. La excelente eliminación de tinte se atribuye principalmente a la utilización eficiente de la luz de las nanoplacas CZTSe.
Antecedentes
Los contaminantes químicos en el agua natural han despertado una gran atención debido a su grave daño al medio ambiente, y la técnica de degradación fotocatalítica basada en semiconductores mediante el empleo de energía solar se ha considerado una solución prometedora a este problema [1]. Sin embargo, los fotocatalizadores típicos, como TiO 2 y ZnO, solo puede absorber luz ultravioleta (UV). De hecho, alrededor del 50% de la energía solar se concentra principalmente en la región de la luz visible, mientras que la luz ultravioleta representa menos del 4% del espectro solar [2]. Para utilizar la luz visible y mejorar la actividad fotocatalítica, se han explorado y aplicado varios fotocatalizadores eficientes en la degradación de pigmentos orgánicos, la división del agua y los absorbentes de células solares [3]. Entre varios fotocatalizadores, semiconductores de calcogenuro cuaternarios y ternarios a base de cobre, como Cu 2 SnS 3 , CuIn x Ga 1-x Se 2 y Cu 2 ZnSnS 4 , han sido de gran interés debido a sus excelentes propiedades optoelectrónicas con un gran coeficiente de absorción (> 10 4 cm −1 ), buena estabilidad y energía de banda prohibida adecuada (1.0–1.5 eV) [4,5,6,7,8,9].
Cu 2 ZnSnSe 4 (CZTSe) nanocristales y películas delgadas con elementos constituyentes económicos, no tóxicos y abundantes en la tierra se han investigado ampliamente en los últimos años [8, 10,11,12,13,14,15]; sin embargo, hay algunos informes relacionados con el estudio de la morfología de las nanoplacas [16, 17]. El método químico térmico de inyección en caliente y en un recipiente se aplica generalmente a la síntesis de nanoestructuras CZTSe [18,19,20,21]. Sin embargo, los precursores de Se usados en estos métodos son costosos, tóxicos o inestables. Aquí, un precursor fácil de Se que disuelve SeO 2 polvo en etanol se desarrolla en este estudio.
Aquí, presentamos un método químico térmico de un solo recipiente de síntesis de nanoplacas CZTSe utilizando un precursor fácil de Se. Se investigó la actividad fotocatalítica impulsada por la luz visible y el rendimiento de reciclaje de las nanoplacas CZTSe. Las nanoplacas CZTSe tienen potencial en el tratamiento de aguas residuales.
Métodos / Experimental
Síntesis de nanoplacas CZTSe
Todos los productos químicos utilizados en este trabajo se compraron a Aladdin y se utilizaron directamente. Normalmente, 1,0 mmol Cu (acac) 2 , 0,5 mmol Zn (OAc) 2 · 2H 2 O, 0,5 mmol de SnCl 2 · 2H 2 O y 2,0 mmol de SeO 2 disueltos en 4 ml de etanol se añadieron a 20 ml de oleilamina (OLA) en un matraz de tres bocas de 100 ml. La mezcla se desgasificó a 130 ° C durante 1 h, se purgó con Ar durante 30 min y luego se calentó a 280 ° C durante 1 h. Las nanoplacas se lavaron con hexano y etanol tres veces mediante centrifugación a 8000 rpm durante 5 min. El polvo negro se recogió y se secó a 60 ° C al vacío. Antes de la reacción fotocatalítica, las nanoplacas se trataron hidrófilas con Na 2 S para eliminar los ligandos OLA de cadena larga [8].
Caracterizaciones
Se aplicaron difracción de rayos X en polvo (XRD, D / max 2200, Rigaku, Japón) utilizando radiación Cu Kα (40 kV, 100 mA) y un espectrómetro Raman (Inviareflex, Renishaw, Reino Unido) acoplado con un láser de 514 nm para analizar la fase de las muestras. Se realizaron mediciones de microscopía electrónica de transmisión (TEM, JEM-2100F, JEOL., Japón) y microscopía electrónica de barrido (SEM, Quatan 250FEG, FEI, EE. UU.) Para caracterizar las morfologías de las muestras. Los espectros de absorción UV-vis del polvo de nanoplaca CZTSe y la solución acuosa de rodamina B (RhB) se registraron en un espectrómetro UV / vis utilizando la esfera integradora y la cubeta, respectivamente (Lambda, Perkin Elmer, EE. UU.).
Medidas de actividad fotocatalítica
La actividad fotocatalítica impulsada por luz visible de las nanoplacas CZTSe se evaluó mediante la fotodegradación de la solución acuosa de RhB (10 mg / L) a temperatura ambiente. Se utilizó una lámpara Xe de 300 W equipada con un filtro de corte de 420 nm como fuente de luz visible. Normalmente, se añadieron 50 mg de fotocatalizador a 100 ml de solución acuosa de RhB. La solución se agitó continuamente en la oscuridad durante 12 h para asegurar el equilibrio de adsorción-desorción antes de la irradiación. La concentración del RhB residual se controló en una secuencia de intervalos de tiempo mediante el espectrómetro UV-vis a 554 nm para calcular la tasa de degradación según la Ley de Beer-Lambert.
Resultados y discusión
En la Fig. 1a, todos los picos de difracción de la muestra de CZTSe preparada en el patrón XRD se pueden atribuir claramente a la estructura de kesterita tetragonal de Cu 2 ZnSnSe 4 (JCPDS No. 70-8930). Los picos de difracción a 27,1 °, 45,1 °, 53,5 °, 65,8 ° y 72,5 ° se pueden indexar a (112), (204), (312) / (116), (400) / (008) y (332 ) de CZTSe, respectivamente. Se aplicó además la dispersión Raman para confirmar la fase pura, como se muestra en la Fig. 1b. Tres picos en el espectro Raman también verifican la fase pura de las nanoplacas CZTSe y ninguna otra fase binaria de Cu x Se y ZnSe (picos principales a 262 y 252 cm −1 , respectivamente) y la fase ternaria de Cu 2 SnSe 3 (pico principal a 180 cm −1 ) son observados. Por lo tanto, ni el resultado XRD ni el Raman revelan ninguna fase secundaria, lo que sugiere la fase cuaternaria pura de las nanoplacas CZTSe.
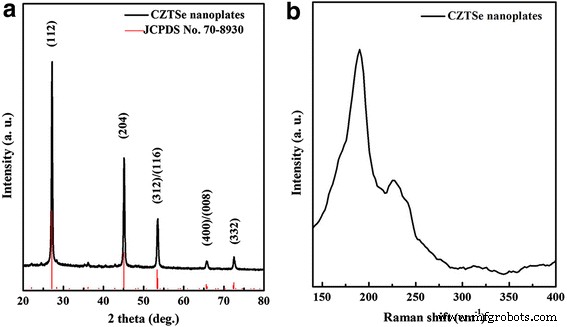
un Patrón XRD y b Espectro Raman de nanoplacas CZTSe
La Figura 2 muestra las imágenes SEM, TEM y TEM de alta resolución (HRTEM) de las nanoplacas CZTSe sintetizadas. Se puede observar en la Fig. 2a que las muestras de CZTSe tienen una morfología uniforme y en forma de placa. El tamaño medio de las nanoplacas CZTSe calculado a partir de la Fig. 2b es ~ 210 nm, lo que coincide bien con la observación SEM. El patrón de difracción de electrones de área seleccionada (SAED) que se muestra en el recuadro de la Fig. 2b indica una alta cristalización de las nanoplacas. La Figura 2c muestra la imagen HRTEM de una nanoplaca, mostrando su estructura cristalina principalmente ordenada y un espaciado d interplanar de 0,33 nm indexado al (112) de CZTSe.

un Imagen SEM. b Imagen TEM (recuadro:patrón SAED). c Imagen HRTEM de nanoplacas CZTSe
El espectro de absorción UV-vis revela la propiedad óptica de las nanoplacas CZTSe. Puede verse en la Fig. 3a que las nanoplacas CZTSe tienen un rendimiento de absorción de la región de luz visible completa. La banda prohibida se puede calcular a partir de la ecuación: αhν = A ( hν − E g ) 1/2 , donde A , α , h , v y E g son una constante, el coeficiente de absorción, la constante del tablón, la frecuencia de la luz y la banda prohibida, respectivamente. La banda prohibida de las nanoplacas CZTSe obtenidas de la Fig. 3b es ~ 1,4 eV, que es un poco más grande que la del volumen CZTSe debido al efecto de confinamiento cuántico [9].
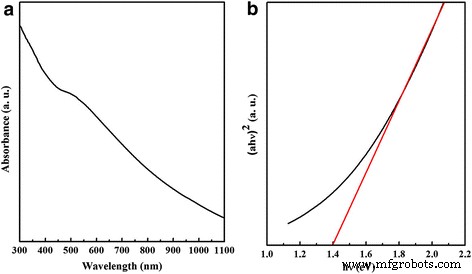
un Espectro de absorción UV-vis y b banda prohibida de nanoplacas CZTSe
La actividad fotocatalítica de las nanoplacas de CZTSe preparadas se evalúa con la fotodegradación de la solución acuosa de RhB en la región de luz visible. Puede verse en la Fig. 4a que ~ 90% de RhB se fotodegrada en 120 min. La estabilidad y la reutilización del fotocatalizador juegan un papel clave en la aplicación de contaminantes ecológicos que se desintegran. Por tanto, se llevaron a cabo experimentos de cinco ciclos y los resultados se muestran en la Fig. 4b. Las nanoplacas CZTSe mantienen una alta actividad de fotodescomposición en las pruebas de ciclo, lo que indica su alta estabilidad en la reacción fotocatalítica. Es bien sabido que el proceso de fotooxidación podría estar relacionado principalmente con varias especies activas, como radicales hidroxilo (• OH), radicales superóxido (• O 2 - ) y agujero (h + ). Porque tanto el E CB y E VB de CZTSe son más negativos que los potenciales redox estándar de E θ (O 2 / • O 2 - ) y E θ (H 2 O / • OH), el • O 2 - en lugar de • OH se puede generar en el proceso fotocatalítico. Para verificar aún más las principales especies activas, se aplicaron argón (Ar), oxalato de amonio (AO), terc-butanol (TBA) y benzoquinona (BQ) para la eliminación de O 2 , h + , • OH y • O 2 - , respectivamente. El sistema de reacción con los extintores correspondientes (0,1 mmol) se iluminó durante 120 min y los resultados se muestran en la Fig. 4c. Se puede confirmar que el O 2 es la necesidad en el proceso de fotooxidación, rara vez se produce • OH, y tanto el • O 2 - y h + son especies activas. El • O 2 - juega un papel más importante que h + por su eficiencia de degradación más aguda, disminuyen después de la captura. La figura 4d muestra el posible mecanismo del proceso de reacción fotocatalítica. Los electrones se excitan desde la banda de valencia (VB) a la banda de conducción (CB) bajo iluminación. Los electrones fotogenerados son capturados por O 2 en la solución acuosa para formar • O 2 - , que es altamente oxidativo y puede degradar el RhB en productos inorgánicos. Simultáneamente, los agujeros funcionan directamente como oxidantes. Por lo tanto, la actividad fotocatalítica impulsada por la luz visible se logra mediante el uso completo de la luz visible de las nanoplacas CZTSe.
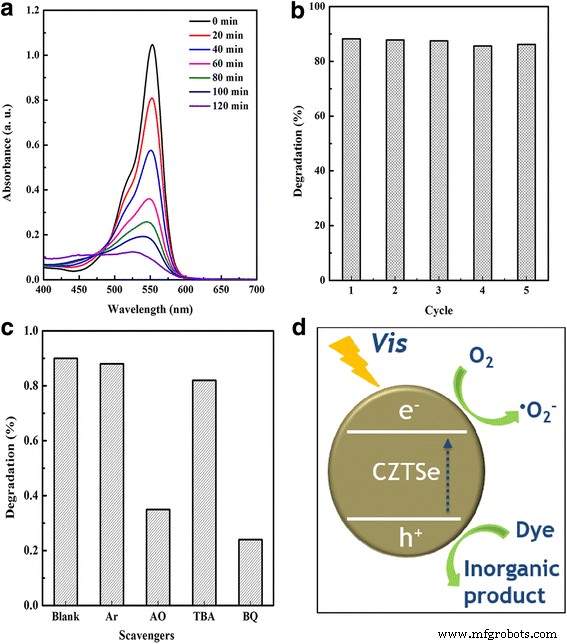
un Degradación de RhB. b Prueba de ciclo. c Efectos de varios extintores sobre la eficiencia de degradación de RhB. d Esquema del proceso de degradación fotocatalítica
Conclusiones
A SeO 2 La solución de etanol como precursor fácil se ha utilizado para la preparación de nanoplacas de CZTSe cuaternarias. Las nanoplacas CZTSe monodispersas se han preparado con éxito mediante un sencillo método químico térmico de un solo recipiente. Como prueba de concepto, las nanoplacas CZTSe se han utilizado como fotocatalizador de respuesta a la luz visible para la degradación del colorante RhB. La eliminación eficiente del tinte se atribuye principalmente a la utilización eficiente de la luz de las nanoplacas CZTSe.
Nanomateriales
- Síntesis verde en un recipiente de microesferas de SnO2 decoradas con Ag:un catalizador eficiente y reutilizable para la reducción de 4-nitrofenol
- Síntesis hidrotermal de nanopartículas de In2O3, gemelos híbridos, discos hexagonales, heteroestructuras de ZnO para mejorar las actividades fotocatalíticas y la estabilidad
- Síntesis y actividad de oxidación del CO de óxido binario mixto 1D CeO2-LaO x catalizadores de oro soportados
- Síntesis de puntos cuánticos de sulfuro de antimonio solubles en agua y sus propiedades fotoeléctricas
- Síntesis fácil y respetuosa con el medio ambiente de nanocables de Co3O4 y su prometedora aplicación con grafeno en baterías de iones de litio
- Síntesis sonoquímica de un solo paso y propiedades fotocatalíticas fáciles de compuestos de puntos cuánticos de grafeno / Ag3PO4
- Síntesis y caracterización de BiOCl modificado y su aplicación en la adsorción de tintes de baja concentración a partir de una solución acuosa
- Síntesis verde de nanopartículas de metal y óxido de metal y su efecto sobre el alga unicelular Chlamydomonas reinhardtii
- Fabricación y propiedad fotocatalítica de nuevos nanocompuestos SrTiO3 / Bi5O7I
- Propiedades de las nanopartículas de óxido de zinc y su actividad contra los microbios
- Síntesis fácil de nanopartículas de iridio sin ligando y su biocompatibilidad in vitro



