Síntesis y actividad de oxidación del CO de óxido binario mixto 1D CeO2-LaO x catalizadores de oro soportados
Resumen
Se sintetizaron nanovarillas de Ce-La unidimensionales (1D) con diferentes contenidos de La (Ce y La en la relación molar de 1:0, 3:1, 1:1, 1:3 y 0:1) mediante un proceso hidrotermal. Los catalizadores de nanovarillas de Au / Ce-La se obtuvieron mediante un método modificado de deposición-precipitación. Las muestras se caracterizaron por N 2 adsorción-desorción (BET), ICP, difracción de rayos X (XRD), SEM, TEM, EDX, espectroscopía de fotoelectrones de rayos X (XPS), espectroscopía de reflectancia difusa UV-vis (UV-vis DRS) y reducción programada por temperatura (H 2 -TPR). Reveló que La existía como LaO x en las nanovarillas 1D. Los resultados de la catálisis demostraron que los óxidos de nanovarillas de Ce-La binarios mixtos podrían ser un buen soporte para los catalizadores de oro. El contenido de La tuvo una influencia importante en el rendimiento catalítico de los catalizadores de nanovarillas de Au / Ce-La. Entre los catalizadores, cuando la relación molar Ce / La era 3:1, el 1.0% Au / Ce 0.75 -La 0.25 Las nanovarillas pretratadas a 300 ° C mostraron la mejor actividad entre los catalizadores para la oxidación del CO, que podría convertir el CO por completo a 30 ° C. Los catalizadores también presentaron resistencia a altas temperaturas y buena estabilidad para la oxidación del CO a las temperaturas de reacción de 40, 70 y 200 ° C.
Antecedentes
Como gas muy dañino, el CO puede unirse fuertemente al átomo de hierro en la hemoglobina sanguínea evitando la liberación de oxígeno. Por tanto, su presencia en interiores puede llegar incluso a provocar la muerte de seres humanos y animales en poco tiempo. Se ha convertido en un problema cada vez más grave de contaminación del aire. La oxidación catalítica de CO ha sido una de las soluciones más eficaces para la eliminación de CO para resolver un problema medioambiental tan grave [1, 2, 3, 4, 5, 6, 7, 8]. También ha recibido una gran atención recientemente por parte de la comunidad científica en los campos de los dispositivos de control de la contaminación para la purificación de gases de escape de los vehículos, la limpieza del aire interior y los sensores de CO de baja temperatura [6,7,8,9,10]. En muchos casos, el precioso Au se dispersa sobre óxidos metálicos específicos con alta capacidad de almacenamiento de oxígeno como CeO 2 , TiO 2 y Fe 2 O 3 son candidatos muy eficaces para la oxidación del CO [11,12,13]. Durante las últimas décadas, los estudios sobre los catalizadores de oro soportados para la oxidación del CO a bajas temperaturas han dado lugar a observaciones inesperadas. En general, se acepta que las actividades catalíticas de los catalizadores de Au dependen en gran medida de la naturaleza de las nanopartículas de Au y de las propiedades de los soportes, como el tamaño de las partículas de oro, la interacción metal-soporte de Au y la reducibilidad del soporte [14,15,16 , 17, 18].
Como uno de los óxidos de tierras raras más importantes, CeO 2 ha sido ampliamente utilizado en catalizadores de tres vías como un soporte de catalizador eficiente debido a sus propiedades físicas y químicas únicas [6, 8, 15, 17]. Director ejecutivo 2 tiene una excelente capacidad de almacenamiento y liberación de oxígeno debido a la capacidad de cambiar Ce 4+ / Ce 3+ , lo que convierte a CeO 2 convertirse en un componente de óxido activo de varios catalizadores de oxidación utilizados en diversas reacciones catalíticas redox [17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32]. Las áreas de superficie, las estructuras mesoporosas, los defectos de la red y los efectos sinérgicos con otros dopantes pueden promover las propiedades catalíticas de los nanomateriales de ceria [3, 22]. Para mejorar aún más el rendimiento de Au-CeO 2 catalizadores para la reacción de oxidación de CO, se han probado muchas estrategias, como métodos de preparación que incluyen deposición-precipitación, coprecipitación y coprecipitación de urea-gelificación, que se han utilizado para controlar y optimizar la interacción de la estructura de Au-O-Ce, así como como el tamaño y la forma de la ceria [33,34,35]. También se ha intentado modificar la superficie del soporte [4, 5, 22, 24, 26, 36,37,38]. Se ha encontrado que el uso de óxidos mixtos binarios como soporte podría proporcionar una buena solución para la estabilización de nanopartículas de oro. Además, la promoción por metales nobles o de transición mejora la reducibilidad de la ceria y facilita la formación de vacantes de oxígeno en la superficie. Mientras tanto, el dopaje con cationes de metales de transición ha demostrado ser un método eficaz para promover las propiedades fisicoquímicas de nanomateriales nanoestructurados unidimensionales (1D), como la actividad catalítica [38,39,40]. Wang y col. [5] modificó la superficie de Au / CeO 2 con CoO x muy disperso y demostró una excelente actividad catalítica en la oxidación de CO a baja temperatura. Ma et al. [37] informó que CaO, NiO, ZnO, Ga 2 O 3 , Y 2 O 3 , ZrO 2 , y los aditivos de tierras raras para el catalizador de oro-titania son beneficiosos para la oxidación del CO, y los catalizadores dopados podrían mostrar una actividad significativa a temperatura ambiente después de un envejecimiento a 500 ° C. Park y col. [38] informó que el director ejecutivo x TiO 2 modificado El soporte es un buen catalizador para la reacción de cambio de gas de agua. Se han realizado muchos estudios sobre óxidos metálicos mixtos para la oxidación catalítica de CO. Estos iones metálicos dopados se depositan sobre la superficie del soporte en forma de partículas de óxido o en la red del soporte, que no podría formar una fase de óxido separada. El objetivo de esta investigación es preparar nanovarillas de Ce-La binarias 1D, que no sean perovskita ni óxido mixto tipo solución sólida. Es decir, en la estructura de nanobarra 1D, los dos óxidos metálicos coexisten combinando los méritos de las dos composiciones para maximizar el efecto sinérgico. Debido a las posibles aplicaciones tecnológicas, muchos nanomateriales 1D, incluidos nanobarras, nanocables y nanotubos, se han investigado exhaustivamente durante los últimos años [2, 4, 41, 42]. Estos materiales nanoestructurados 1D, especialmente los materiales nanobarras 1D, se han estudiado como importantes soportes o componentes activos en el campo de la catálisis, la óptica y la electroquímica, como los nanocables de silicio bien controlados utilizados en las células solares [42]. Se ha descubierto que las propiedades de los materiales de estructura 1D, como la actividad catalítica, a menudo están estrechamente relacionadas con su estructura y forma cristalinas. Como consecuencia, el desarrollo de materiales de nanovarillas 1D para adaptar sus propiedades electrónicas y catalíticas resulta intrigante y valioso.
En este documento, informamos una estrategia solvotermal simple para preparar una serie de compuestos mixtos de nanovarillas Ce-La. En el proceso de síntesis, LaO x y director ejecutivo 2 podrían crecer juntos en una varilla. La morfología de los productos finales no se vio afectada. Los resultados de XRD y TEM muestran que las Lacaciones han existido en forma de LaO x . Se encontró que el dopante de LaO x mostró un efecto positivo sobre la actividad de los catalizadores de oro-ceria. Au / Ce 0,25 -La 0,75 nanobarras exhibieron una excelente actividad catalítica para la oxidación del CO.
Experimental
Todos los productos químicos de este documento eran de grado analítico y se utilizaron tal como se recibieron sin ninguna purificación.
Preparación de asistencia
Las nanovarillas de Ce-La se sintetizaron mediante un método hidrotermal convencional. En una síntesis típica, las soluciones de NaOH (9 mol / L) y Ln (NO 3 ) 3 (Ln =Ce, La, 0,8 mol / L) se mezclaron y se mantuvieron en vigorosa agitación durante 30 min a temperatura ambiente. La suspensión resultante se vertió en un autoclave de acero inoxidable revestido con teflón. El autoclave se selló y se mantuvo a 110 ° C durante 14 hy luego se enfrió al aire a temperatura ambiente. Los productos resultantes se filtraron, se lavaron con agua desionizada y alcohol absoluto, se secaron a 80 ° C durante 12 h, y luego se calcinaron a 400 ° C en aire con una velocidad de calentamiento de 5 ° C min -1 antes de soportar nanopartículas de oro. Los productos finales con diferentes contenidos de La (Ce y La en la relación molar de 1:0, 3:1, 1:1, 1:3 y 0:1) se denominaron nanovarillas de Ce, Ce 0,75 -La 0.25 nanovarillas, Ce 0.50 -La 0.50 nanovarillas, Ce 0.25 -La 0,75 nanovarillas y La nanovarillas.
Preparación del catalizador
Se llevó a cabo un proceso de deposición-precipitación para preparar catalizadores de nanovarillas de Au / Ce-La. Brevemente, la cantidad requerida de nanovarillas de Ce-La se dispersó en 100 ml de agua desionizada y luego se mezcló con una cierta cantidad 0.01 mol / L de HAuCl 4 solución. Como el pH del HAuCl 4 final La solución era aproximadamente 7, que estaba relacionada con la basicidad del soporte y la acidez de HAuCl 4 , el pH de la solución no se ajustará. La suspensión se mantuvo en agitación durante 12 horas y se mantuvo a reflujo a 100ºC durante 4 horas. Después del procedimiento de deposición-precipitación, el precipitado se centrifugó, se lavó con agua para eliminar el Cl - iones y se secaron a 80 ° C al aire durante 12 h. Las concentraciones de oro se expresaron como porcentaje del contenido de masa.
Técnicas de caracterización
Las cargas de oro de los catalizadores de nanovarillas de Au / Ce-La se determinaron mediante espectroscopía de emisión atómica de plasma acoplada inductivamente (ICP-9000, USA Thermo Jarrell – Ash Corp). Las áreas de superficie Brunauer-Emmett-Teller (BET) de las muestras de nanobarras de Ce-La se midieron mediante adsorción de nitrógeno a - 196 ° C utilizando un aparato Micromeritics Tristar II 3020. El estudio XRD se llevó a cabo en un difractómetro de rayos X Rigaku D / Max-2500 ( Kα λ =0.154 nm) en el 2 θ rango de 3 a 80 °. Se recogieron DRS UV-visible de los catalizadores en un espectrofotómetro UV-vis NIR (JASCO Corp V-570). Las observaciones de TEM y el análisis de rayos X de dispersión de energía (EDX) se obtuvieron con un microscopio electrónico de transmisión JEM-2100 que funcionaba a 200 kV. Los datos SEM y las imágenes de mapeo de elementos se obtuvieron con un microscopio electrónico de barrido JSM-7500F que funcionaba a 15 kV. Se registraron XPS para identificar la composición química y el estado de oxidación de los catalizadores en un espectrómetro de fotoelectrones de rayos X Kratos Axis Ultra DLD utilizando un Al Kα monocromático fuente operada a 150 W. Las energías de enlace se calibraron utilizando el C 1 s pico ubicado en 284,6 eV. Reducción de temperatura programada (H 2 –TPR) se realizó en un aparato PX200 para medir H 2 consumo. Antes de H 2 -Análisis de TPR, las muestras se pretrataron en flujo de He a 300 ° C durante 1 h. Después de enfriar a 50 ° C, el catalizador se redujo con 10% en volumen de H 2 / Flujo de gas Ar calentando hasta 900 ° C a una velocidad de 10 ° C / min.
Prueba de actividad catalítica
La evaluación de la actividad catalítica se realizó en un milireactor de flujo de lecho fijo con un diámetro interno de 8 mm. Antes de la reacción, se diluyeron 200 mg de catalizador con 17,6 g de arena de cuarzo químicamente inerte. Posteriormente, se introdujo en el reactor una mezcla de CO al 10% balanceada con aire a un caudal total de 36,3 mL min −1 . Después de mantener la temperatura de reacción durante 30 minutos, los productos gaseosos se analizaron en línea mediante CO x analizador (cromatografía de gases GC-508A). La conversión de CO se calculó de acuerdo con la siguiente ecuación:
$$ \ mathrm {CO} \ kern0.5em \ mathrm {conversión} =\ frac {\ left [\ mathrm {CO} \ 2 \ right]} {\ left [\ mathrm {CO} \ right] + \ left [ \ mathrm {CO} \ 2 \ right]} \ times 100 \% $$donde [CO] y [CO 2 ] representan la salida CO y CO 2 concentración, respectivamente. La dependencia de la temperatura de la actividad catalítica de la muestra se registró en el rango de 30-200 ° C con una velocidad de rampa de 10 ° C min −1 .
Resultados y discusión
Caracterización de catalizadores Au / Ce-La Nanorod
ICP
Las cantidades de oro presentes en los catalizadores de nanovarillas de Au / Ce-La se determinaron mediante ICP-AES. Los resultados mostrados en la Tabla 1 revelaron que la cantidad real de oro en todos los catalizadores era menor que la nominal. Según el procedimiento de preparación, el oro debe perderse durante el proceso de precipitación y deposición.
APUESTA
N 2 Las mediciones de absorción se utilizaron para medir el área de superficie BET y el diámetro promedio en ambos CeO 2 nanorods y nanocomposites Ce-La. Como se muestra en la Fig. 1, las isotermas de adsorción para las nanovarillas de Ce-La eran de tipo IV y presentaban características de bucles de histéresis H3. Todas las muestras muestran un aumento muy fuerte de N 2 -volumen adsorbido a una presión relativa superior a 0,85, que es una característica de la presencia de una cantidad apreciable de mesoporosa, [2, 22] indicando nanocompuestos Ce-La compuestos por agregados (ensamblajes sueltos) que forman poros en forma de rendijas. Con el dopante de La, los bucles de histéresis cambiaron a una presión relativa de aproximadamente 0,95, lo que significaba que el tamaño de los poros se haría más pequeño, lo que corresponde a la disminución de los compuestos Ce-La. Como se presenta en la Tabla 2, el área de superficie específica de CeO 2 nanorods es 99,7 m 2 / g, que disminuye a 74,1 m 2 / g cuando La está dopada con la relación molar Ce / La de 3:1. Con el aumento del contenido de La, el área de superficie de los nanocompuestos de Ce-La disminuyó continuamente. Esto se debe principalmente al contenido de La, que no se incrustaría en el entramado de CeO 2 y existir como aislado LaO x lo que lleva a una pequeña diferencia en la morfología de los nanocompuestos de Ce-La. Se pudo observar que todas las nanovarillas tienen superficies similares de 80 a 100 m 2 /gramo. Volumen de poro de Ce 0,75 -La 0.25 nanorods es de 0,23 cm 3 / g, que era similar a la de las nanovarillas Ce, y más grande que otras nanovarillas Ce-La. Los diámetros de poro estimados a partir del análisis de BJH confirmaron la naturaleza mesoporosa de los nanocompuestos de Ce-La. Puede ser una ventaja para la oxidación catalítica del CO.
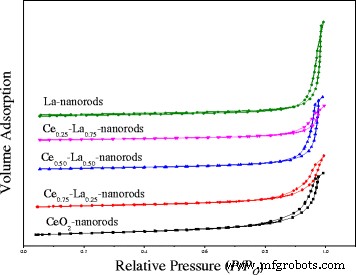
Isotermas de adsorción-desorción de nitrógeno de nanobarras de Ce-La con diferente contenido de La
XRD
Las muestras sintetizadas se sometieron a análisis de difracción de rayos X en polvo y posteriormente se analizaron sus atributos estructurales. Los picos de cristalinidad para el óxido de cerio (Fig.2a) se observaron en 2θ =28.6 °, 33.1 °, 47.6 ° y 56.3 ° correspondientes a los planos de difracción (111), (200), (220) y (311) y corroborar con la estructura cúbica de fluorita de CeO 2 cristal (JCPDS no. 34-0394). Cuando el contenido de La era 0,25 at.%, Los picos de difracción de los compuestos La-Ce se ensanchan. Los picos centrados en 2θ =30.0 °, 46.0 °, 52.0 ° y 53.6 ° corresponden a planos de difracción de La 2 aislada O 3 . No hay picos asignados a La (OH) 3 podría ser detectado. Pero debido al bajo contenido y a la posición de difracción aproximada, no es fácil identificar la existencia de LaO x . Con el aumento del contenido de La, se observan algunos picos prominentes para La 2 O 3 o La (OH) 3 en el nanocompuesto. Los principales picos de difracción de La 2 O 3 están presentes en 2θ =30.0 ° (101), 39.6 ° (220), 46.2 ° (110) y 66.8 ° (112), que se pueden asignar a la fase hexagonal (tarjeta JCPDS 05-0602). Los principales picos de difracción de La (OH) 3 están presentes en 2θ =15,7 ° (100), 27,3 ° (110), 27,9 ° (101) y 39,4 ° (201), que se pueden asignar a la fase hexagonal (tarjeta JCPDS 36-1481). Los resultados demuestran que La podría existir como La 2 aislada O 3 o La (OH) 3 en el compuesto. Después de la deposición de oro, no hubo pico de difracción que pudiera indexarse a la estructura cristalina pura centrada en la cara del oro (Fig. 2b). Esto podría deberse al bajo contenido y / o al tamaño de partícula pequeño de las nanopartículas de oro.
Patrones de XRD de nanobarras de 1% Au / Ce-La con diferentes contenidos de La (0–100 at.%) ( a ) y Au / Ce 0,75 -La 0.25 nanovarillas con diferentes cargas de Au calcinadas a 300 ° C durante 2 h ( b )
SEM y TEM
La Figura 3a – e muestra las fotografías SEM del CeO 2 y nanocompuestos Ce-La obtenidos en diferentes concentraciones de La 3+ iones. Se ve que todos los nanocompuestos de Ce-La exhibieron una estructura en forma de varilla. Obviamente, muchas varillas se apilan en paquetes de Ce-La, lo que lleva a la formación de poros en forma de rendijas con diferentes tamaños. Los resultados coincidieron con los N 2 isotermas de adsorción-desorción. Como se muestra en la Fig. 2a, el producto consiste principalmente en nanobarras con un diámetro de 5 a 10 nm y una longitud de 100 a 300 nm. En la Fig. 3e, se vio claramente una gran cantidad de nanobarras con un diámetro de aproximadamente 12,5 nm, y también había una pequeña cantidad de nanovarillas cortas con un diámetro medio de aproximadamente 8,0 nm. En la Fig. 3b – d, al aumentar la concentración de dopaje de La 3+ , las muestras siempre presentan morfología de nanobarras. Sin embargo, aunque la concentración de dopaje fue del 25% en moles, las muestras obtenidas mostraron las nanovarillas más uniformes con un diámetro de 5 a 20 nm y una longitud de 100 a 300 nm entre todas las muestras. La Figura 3f muestra imágenes TEM de las nanovarillas Ce-La individuales obtenidas. Se pudo ver que hay muchos poros en el soporte, como lo revelan las isotermas de adsorción-desorción de nitrógeno. La imagen HRTEM de las nanovarillas Ce-La reveló que son estructuralmente uniformes y de naturaleza monocristalina. Las franjas de celosía insertadas en la Fig. 3f ilustran dos valores de espaciado interplanar, es decir, 0.31 y 0.34 nm, que son consistentes con los planos (111), (110) del CeO 2 y La 2 O 3 , respectivamente [3, 15, 43]. Reveló que La 3+ iones se han generado de manera efectiva en La 2 O 3 , que es consistente con el espectro XRD.

Imágenes SEM de nanobarras de Ce-La con diferentes contenidos de La:0 ( a ), 25 en.% ( b ), 50 en.% ( c ), 75 en.% ( d ), 100 en.% ( e ); Imagen TEM de Ce 0.50 -La 0.50 nanorods ( f ); y el recuadro muestra la imagen HRTEM correspondiente
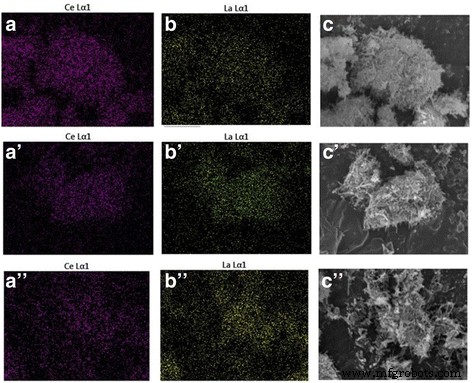
Se empleó el mapeo de elementos y el análisis EDS para determinar la composición química de las muestras de Ce-La (Fig. 4 y Tabla 3). Los resultados mostraron relaciones molares La / Ce uniformes en buen acuerdo con los valores esperados de la síntesis. Las imágenes TEM de Au / Ce 0,75 -La 0.25 las muestras calcinadas a 300 ° C (Fig. 5a) y 400 ° C (Fig. 5c) mostraron claramente que las formas de los nanocristales de Ce-La permanecieron esencialmente sin cambios después de la adición de oro. No se observaron partículas de oro por TEM en las nanovarillas Ce-La. La presencia de grupos de oro muy dispersos ( d <1 nm) se ha evidenciado mediante el mapeo de elementos y el análisis EDX (recuadro en la Fig. 5b, eyf). De acuerdo, el análisis XRD realizado en esta muestra (Fig. 2) no reveló ningún pico relacionado con el oro debido al hecho de que las partículas de oro son demasiado pequeñas para ser detectadas. Esto indica que las superficies de nanovarillas de Ce-La pueden dispersar y estabilizar los átomos de oro como agrupaciones subnanométricas (TEM invisible). Esto está de acuerdo con las literaturas [2, 44,45,46]. Sin embargo, algunos grandes aglomerados de partículas de oro (promedio d ~ 7 nm) se han observado en Au / Ce 0,75 -La 0.25 nanobarras calcinadas a 400 ° C debido a que las franjas con un espaciado de 0,236 nm se asignan al plano (11 1) del Au metálico (Fig. 5c en la que se muestra un aglomerado de partículas de oro). Se pudo ver que junto con la alta temperatura de calcinación, las partículas de oro obviamente crecieron, lo que condujo correspondientemente a la pérdida de actividad catalítica.

Las imágenes de mapeo de elementos de Ce y La, imágenes SEM de las muestras mixtas para nanobarras Ce-La con contenido de La de 25 at.% ( a - c ), 50 en.% ( a ′ - c ′), 75% at. ( a ′ ′ - c ″)
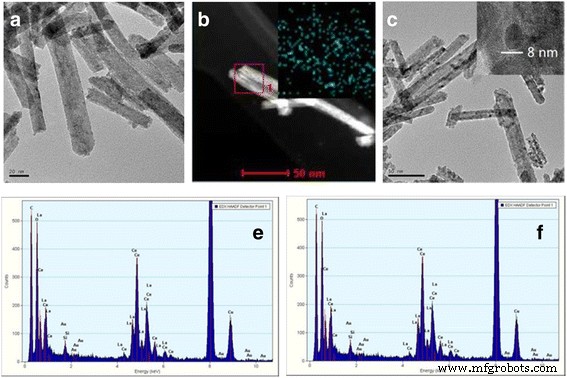
Imágenes TEM y STEM de 0,5% Au / Ce 0,75 -La 0.25 nanobarras calcinadas a 300 ° C ( a - b ) y 400 ° C ( c ), Análisis EDX ( e - f ) de las imágenes de ( a - b ) que indica la presencia de señal de Au
XPS
Los espectros XPS en la Fig.6 se realizan para investigar el compuesto químico y los estados en 1% Au / Ce 0,75 -La 0.25 muestras de nanobarras calcinadas a 300 ° C durante 2 h. El espectro XPS de Ce 3 d muestra los distintos picos de 3 d 3/2 estados de órbita giratoria y 3 d 5/2 estados de órbita de giro en la Fig. 6a. Como se sabe, los picos se encuentran a una energía de enlace de aproximadamente 899, 903 y 916 eV, que normalmente se utiliza como marcador espectroscópico para detectar la presencia de Ce 4+ Expresar. En nuestro caso, Ce 3 d Los niveles centrales muestran tres dobletes orbitales de espín, que son los picos característicos de los estados tetravalentes de Ce 4+ . Los picos ubicados alrededor de 882,8, 888,1 y 898,4 eV se asignan al Ce 3 d 5/2 , y aquellos en alrededor de 901.3, 907.0 y 916.7 eV se asignan al Ce 3 d 3/2 , correspondiente a dobletes divididos en órbita de espín de compuestos de Ce (IV). Los resultados observados se comparan con la literatura publicada en general [19, 28, 29, 32]. Es obvio que las muestras están en el estado Ce 4+ sin ninguna impureza del Ce 3+ Expresar. La Figura 6b muestra los espectros XPS de La 3 d región de 1% Au / Ce 0,75 -La 0.25 muestras de nanovarillas. Tanto el giro-órbita dividido 3 d 5/2 y 3 d 3/2 los niveles mostraron estructuras de doble pico. La órbita de giro dividida entre los 3 d 3/2 y 3 d 5/2 los niveles fueron de aproximadamente 17.0 eV, y la separación entre el satélite y el pico principal fue de 4.1 eV, lo que coincidió con los valores reportados para La 3+ compuestos [11, 47]. Como era de esperar, La sale en el estado de oxidación + 3 y puede tener una influencia importante sobre la actividad catalítica. Los O 1 s El espectro XPS (Fig. 6c) es asimétrico y deconvolucionado en 529,3, 531,6 y 527,6 eV, respectivamente. El pico de 529,3 eV se asigna al oxígeno de la red y el de alrededor de 531,9 eV se asigna a grupos hidroxilo en la superficie del soporte [27, 28, 32]. El pequeño pico del hombro a 527,6 eV se atribuye a La-O, que también podría revelar la presencia de LaO x en los catalizadores [11, 48]. Claramente, hay un gran número de grupos hidroxilo en la superficie del soporte de acuerdo con la alta intensidad del pico. Los espectros XPS en Au 4 f La región de los catalizadores calcinados a 300 y 400 ° C se muestra en la Fig. 6d. En la Fig. 6d, los catalizadores calcinados a 300 ° C mostraron el Au 4 f 2/7 señales de energías de enlace a 84,6 eV. Las señales eran características del Au + catiónico especies [14, 15, 31]. En comparación, después de que los catalizadores se calcinaran a 400 ° C, el Au 4 f 2/7 el pico se ubicó en una energía de enlace de 83,6 eV y Au 4 f 5/2 se ubicó en una energía de enlace de 87,7 eV. La presencia de Au 0 metálico se observa claramente. También se detectaron los pequeños picos ubicados alrededor de 85.0 y 88.2 eV, correspondientes a especies de oro oxidado. Es evidente que los catalizadores calcinados a 300 ° C mostraron prácticamente principalmente Au + catiónico especies (> 90% de Au + especies). Por el contrario, las muestras calcinadas a 400 ° C tienen un 90% de Au 0 y 10% de Au δ + . La transferencia de densidad electrónica del Au metálico hacia el soporte dio como resultado la oxidación parcial del Au y una fuerte interacción entre el oro y el soporte. La presencia de Au δ + es responsable de la reducción parcial de la superficie de apoyo. En consecuencia, Au δ + se considera más activo que Au 0 para la oxidación del CO [11, 21]. En nuestro caso, los catalizadores calcinados a 300 ° C tenían más Au δ + que el calcinado a 400 ° C, por lo que no es difícil deducir que los catalizadores calcinados a 300 ° C fueron más activos que los catalizadores calcinados a 400 ° C, lo cual fue consistente con los resultados de la actividad.
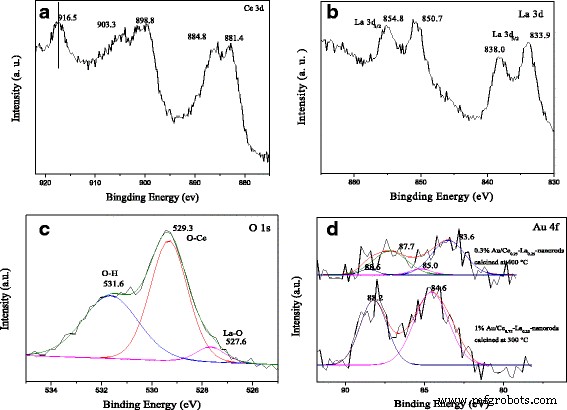
Espectros XPS de 1% Au / Ce 0,75 -La 0.25 nanovarillas calcinadas a 300 ° C durante 2 h:Ce 3 d picos ( a ), La 3 d picos ( b ) y O 1 s picos ( c ). Au 4 f picos ( d ) de Au / Ce 0,75 -La 0.25 nanobarras calcinadas a 300 y 400 ° C durante 2 h
Visible a la luz ultravioleta
El espectro de reflectancia difusa UV-vis del Ce 0,75 -La 0.25 nanovarillas y 0.5% Au / Ce 0.75 -La 0.25 Las nanovarillas calcinadas a diferentes temperaturas se presentan en la Fig. 7. Como se ve en esta figura, en comparación con los espectros del soporte, los espectros de los catalizadores calcinados a diferentes temperaturas exhibieron una banda de absorción débil y ancha entre 500 y 600 nm que se caracterizó para la resonancia de plasmón de superficie (SPR) de nanopartículas de oro metálico [21, 24, 49]. El SPR podría atribuirse a las oscilaciones colectivas de electrones en respuesta a la excitación óptica, lo que daría como resultado la absorción de luz en la región Uv-vis. La ubicación de la resonancia del plasmón superficial se vio afectada por el tamaño de la partícula de oro disperso, la forma de la partícula y las propiedades dieléctricas del material circundante. En el presente estudio, el pretratamiento de calcinación provocó un gran desplazamiento hacia el rojo de las bandas de absorción, y las posiciones de las bandas de absorción (500-600 nm) se desplazaron hacia el rojo al aumentar la temperatura de calcinación. Los rangos de cambio son los siguientes:80 ° C → 200 ° C → 300 ° C. Con un aumento adicional de la temperatura de calcinación a 400 ° C, las bandas de absorción se movieron a la longitud de onda corta. Hubo varios informes sobre la explicación del cambio de posición del pico [24, 50,51,52,53]. Si bien el diámetro de la partícula de oro es <2 nm, la posición del pico de desplazamiento ensanchado se debió principalmente a la amortiguación dependiente del tamaño de la función dieléctrica del metal. También se produjo una reducción de la densidad de electrones en las partículas de oro debido a interacciones químicas con los óxidos metálicos circundantes, lo que podría explicar el mecanismo que conduce a un desplazamiento hacia el rojo aún más [52]. Un aumento en el tamaño de las partículas de oro causaría un desplazamiento hacia el azul en el pico de absorción (diámetro medio menor de 25 nm), y para partículas grandes (diámetro medio mayor de 25 nm), se observó el efecto contrario [53]. Según los datos de TEM, el tamaño de las partículas de oro en el catalizador era <1 nm para el catalizador calcinado a 300 ° C. Sin embargo, con un aumento adicional de la temperatura de calcinación a 400 ° C, las partículas de oro crecieron y el tamaño promedio fue de aproximadamente 7 nm. Como se mencionó anteriormente, la posición de la banda de plasmón dependía en gran medida de la forma y el tamaño de las partículas de oro. En el presente caso, este gran cambio podría explicarse en términos de la diferencia en el tamaño de las partículas de oro. Los datos fueron consistentes con los resultados de la prueba de actividad catalítica. También indicó que las nanopartículas de oro se dispersaron bien en la superficie de los soportes.
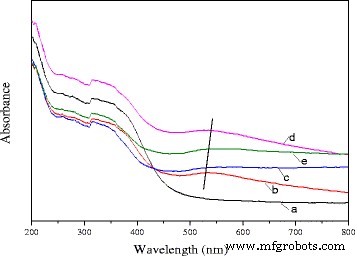
DRS UV-vis de Ce puro 0,75 -La 0.25 soporte nanorod (a) y 0,3% Au / Ce 0,75 -La 0.25 nanobarras calcinadas a 80 ° C (b), 200 ° C (c), 300 ° C (d) y 400 ° C (e)
H 2 -TPR
La Figura 8a muestra el perfil de TPR para muestras de óxidos puros y mixtos. Para CeO puro 2 nanovarillas, el pico de reducción centrado a una temperatura baja (410 ° C) y una temperatura alta (620 ° C) podría atribuirse a la reducción de la superficie y las especies de oxígeno a granel de CeO 2 , respectivamente [1, 32]. Para las nanovarillas de La puras, se podrían detectar picos de reducción obvios a ~ 700 ° C asignados a la reducción de La 2 a granel O 3 . Fue interesante encontrar que aparecieron los picos de reducción a ~ 500 ° C de nanobarras de Ce-La. El pico de reducción de las tres muestras con 25, 50 y 75% de dopaje at.% La muestra un cambio a una temperatura más alta en aproximadamente 20 ° C tras el dopaje La. Cuando el contenido de La es del 25% at., Se observó una fuerte reducción de la temperatura máxima de 520 ° C. Es una nueva temperatura de reducción y notablemente relativa a la del CeO 2 puro nanorods. En comparación con la referencia, debido a la interacción sinérgica entre La – O y Ce – O, la temperatura de reducción de las nanovarillas de Ce-La fue más alta que la CeO pura 2 [31, 54]. Se pudo encontrar que los óxidos binarios deberían tener CeO 2 independiente y LaO x . Como se muestra en la Fig. 8b, después de la deposición de oro, aparece un nuevo pico de reducción a muy baja temperatura (100-200 ° C) para Au / CeO 2 y nanobarras de Au / La-Ce. Aquí, debido a los resultados de XPS, después de que los catalizadores se calcinaron a 300 ° C, Au fue principalmente Au δ + , por lo que los picos de reducción a ~ 200 ° C se atribuyen a la reducción de especies de Au en valencia alta [21]. El pequeño pico centrado en ~ 350 ° C se puede asociar con la reducción de nanobarras Ce-La. Además, para 1% Au / Ce 0,75 -La 0.25 nanovarillas, otro pico de reducción a alrededor de 230 ° C se puede atribuir a la reducción promovida por el oro de CeO 2 . Uno por ciento de Au / Ce 0,75 -La 0.25 nanorods tiene la temperatura de reducción más baja entre los catalizadores, lo que podría ayudar a que sea el catalizador más activo para la oxidación del CO. Esto estuvo de acuerdo con los resultados de la actividad. Since the surface reduction peaks for all oxide supports are significantly decreased after gold deposition, it indicates that most available oxygen is reduced at this lower temperature and suggests that H2 dissociation on gold and spill-over onto the adjacent oxide surface are more likely to be responsible for the strong low-temperature reduction peak [31]. TEM and XPS data indicated that the cationic gold particles with small size highly dispersed on the surface of the supports. The presence of LaO x could also help stabilize cationic Au. This is beneficial for the strength of gold-support interaction [11]. The strong interaction between gold and support promoted the reduction of Au/Ce-La nanorods shifted to low temperature. The results indicated that the reducibility of Ce-La nanorods is strongly affected by the gold deposition.
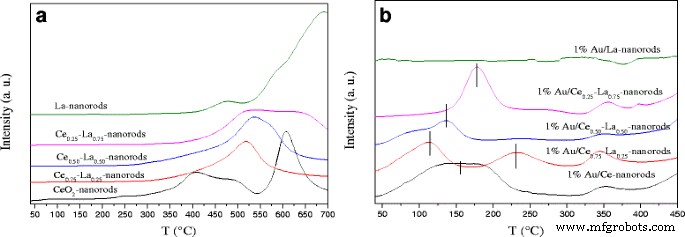
H 2 -TPR profiles of a La-Ce nanorods with different La content (0–100 at.%) and b 1% Au/La-Ce nanorods with different La content calcined at 300 °C
Catalytic Activity
Effect of La Content
As shown in Fig. 9, catalytic activity results for Au/Ce-La nanorod samples ranging from pure CeO2 to 100 at.% La-content nanorod supports. The most striking feature in the figure is the high activity of the Au/Ce0.75 -La0.25 nanorod catalyst with the 100% conversion at temperature as low as 30 °C. In contrast, the other Au/La-Ce catalysts showed lower activity compared to Au/Ce0.75 -La0.25 nanorods catalysts under the same reaction conditions. The results indicated that La doping has very much impact on this high CO conversion activity with a La content of 25 at.%, while a further increase results in a significant drop in activity. This again closely mirrors the trends seen in the reducibility of the samples, where an increase of La content from 25 at.% results in a strong loss of reducibility.
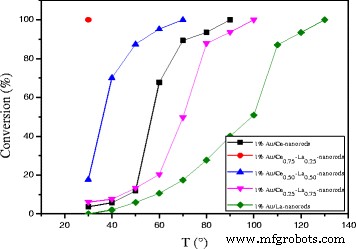
Catalytic activities of 1% Au/ La-Ce nanorods with different La content calcined at 300 °C for 2 h
In consideration of the preparation methods, gold loadings, gold particle size and distribution on different Ce-La nanorods supports, XRD, TEM and XPS data showed that all the catalysts should have the same number and type of active Au sites. So this high activity of the Au/Ce0.75 -La0.25 nanorods catalysts correlates well with the reducibility data discussed above. H 2 -TPR results indicated that Au/Ce0.75 -La0.25 nanorods has the lowest reducibility temperature and highest reducibility in the region of 50–400 °C, especially in the region of 50–150 °C, which could exactly approach the region of reaction temperature. In the process of reaction, the Ce0.75 -La0.25 nanorod support served as oxygen carrier. The reducibility of Ce0.75 -La0.25 nanorods could promote the formation of active oxygen. That is to say high reducibility of the catalyst, good activity the catalyst has. Au/Ce0.75 -La0.25 nanorod catalyst subsequently has the best activity.
Effect of Gold Content
The catalytic activities for CO oxidation were measured from low conversion to 100% conversion for the Au/Ce0.75 -La0.25 nanorod catalysts calcined at 300 °C for 2 h with a series of low gold contents. As shown in Fig. 10, all of the catalysts showed high catalytic activities. The CO conversion increased greatly with increasing gold content. The complete CO conversion could be attained at 50 °C over 0.5% Au/Ce0.75 -La0.25 nanorod catalyst. The size and chemical states of gold nanoparticles are generally thought to be vital for the performance of supported gold catalysts. It has been reported that its gold nanoparticles with the diameter of < 5 nm would be suitable for the supported gold catalysts in the catalytic CO oxidation [27, 28]. The XPS data proved that gold in Au/Ce0.75 -La0.25 nanorod catalyst exists in the form of cationic Au + . TEM images of the samples were also shown to investigate the diameter of gold nanoparticles in the catalysts. Consequently, the gold particles of Au/Ce0.75 -La0.25 nanorods were detected as sub-nanometer. Taking into account the particle size, mass content, and chemical states of the gold nanoparticles, gold particles with small diameter highly dispersed on the surface of Ce0.75 -La0.25 nanorods and interacted strongly with the support [17, 21, 23]. The strong interaction between gold particles and the support would help improve CO adsorption and accelerate active oxygen spillover to gold particles from the support, so 0.5% Au/Ce0.75 -La0.25 nanorods which had relatively high content of gold should exhibit the best CO oxidation activity. In fact, 0.5% Au/Ce0.75 -La0.25 nanorods indeed present high performance. The results demonstrated the activity of supported gold catalysts is strongly dependent on the gold nanoparticle size, chemical states, and the quantity of the active species, an increase of which implied an increase of the catalytic activity. In the case of Au/Ce0.75 -La0.25 nanorod catalyst, catalysts with low gold content could also exhibits high activity at low temperature, which would promote the progress of supported gold catalyst. The results indicated that supported gold catalysts prepared by deposition-precipitation with pH value of 6–10 for HAuCl4 solution could have high catalytic activity due to small diameter of gold nanoparticles, corresponding with the references [8,9,10].
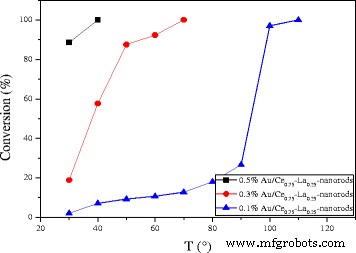
Catalytic activities of Au/Ce0.75 -La0.25 nanorods with different gold goadings calcined at 300 °C for 2 h
Effect of Calcination Temperature
The effect of calcination temperature on the catalytic activity of 0.5%Au/Ce0.75 -La0.25 nanorods is also shown in Fig. 11. The results indicated an increase in the activity of catalyst with the calcination temperature from 80 to 300 °C. The 0.5% Au/Ce0.75 -La0.25 nanorod catalyst calcined at 200 °C could convert CO to CO2 completely at 80 °C. While for 0.5% Au/Ce0.75 -La0.25 nanorod catalyst calcined at 80 °C, the temperature increased to 100 °C. The results showed that CO conversion increased with increasing calcinations temperature. Then, for the sample calcined at 400 °C, about 90% CO can be converted to CO2 at 100 °C and CO could be converted to CO2 completely at 120 °C. The sample calcined at 300 °C possessed the best catalytic activity. The catalytic performance of supported gold catalysts strongly depends on gold nanoparticle size and metal-support interaction due to “synergic effect” at the gold-support interface [10, 13, 15, 18]. The gold-support interaction largely depended on calcination temperature of catalysts. The electron could transfer from gold to the support [10]. Thus, with increasing calcination temperature, the charges on gold particles became increasingly positive, which is good for the enhancement of catalytic activity for CO oxidation. Here, as shown in the Fig. 5, size of gold particles in the catalysts calcined at 300 °C was small. The XPS data also indicated that gold was main Au δ+ after calcination at 300 °C. Thus, the stronger metal-support interaction could account for the relative good catalytic performance for catalysts calcined at 300 °C. From 80 to 300 °C, the higher the calcination temperature is, the stronger interaction exists between gold particles and support. As a consequence, from 80 to 300 °C, the activity of catalysts increased. However, after the 0.5% Au/Ce0.75 -La0.25 nanorod catalyst calcined at 400 °C, complete conversion temperature increased. The main reason might be that the high-temperature treatment led to increased mobility and growth of gold nanoparticles, which correspondingly led to the loss of catalytic activity. The XPS also suggested that the catalysts calcined at 400 °C, Au was mainly Au 0 . It could be concluded that the activities of supported gold nanoparticles were influenced by both the oxidation state and the size of gold nanoparticles, and the appropriate calcination temperature was 300 °C.
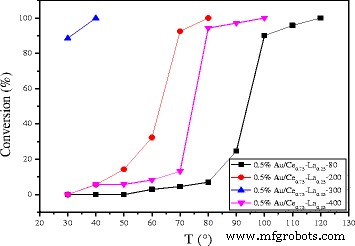
Catalytic activities of 0.5% Au/Ce0.75 -La0.25 nanorods calcined at different temperatures
Stability Observations
The stability of the 0.3% Au/Ce0.75 -La0.25 nanorod catalyst during CO oxidation at different reaction temperatures was measured, as shown in Fig. 12a. When the reaction was carried out at 70 °C, the initial CO conversion over 0.3% Au/Ce-La catalyst can reach 100% and has almost no change with continuously increasing reaction time. 0.3% Au/Ce-La catalyst with 60% CO conversion rate at 40 °C is also attained even after 10-h running period, and no obvious decline in CO conversion is observed. Although the catalytic activity of 0.3% Au/Ce0.75 -La0.25 nanorod catalyst at 40 °C was lower than that of 0.3% Au/Ce0.75 -La0.25 nanorod catalyst at 70 °C, the conversion of CO over the catalysts at both temperatures still seemed to be stable over 10 h on stream. It is thought that the catalyst was of good durability. It was clear that the activity over 0.3% Au/Ce0.75 -La0.25 nanorod catalyst did not strongly depend on the reaction temperature. As the reaction temperature decrease the activation rate barely becomes little slower and then finally reaching a steady state in which the CO conversion was still around 90%. For comparison, the stability of 0.5% Au/Ce0.75 -La0.25 nanorod catalyst at the reaction temperature of 40 °C with initial conversion of 100% was also provided in Fig. 12b. It was obvious that in 10 h, no decrease of CO conversion for 0.5% Au/Ce0.75 -La0.25 nanorods was detected. The results depicted that with the change of gold content, Au/Ce0.75 -La0.25 nanorods could still perform good stability.
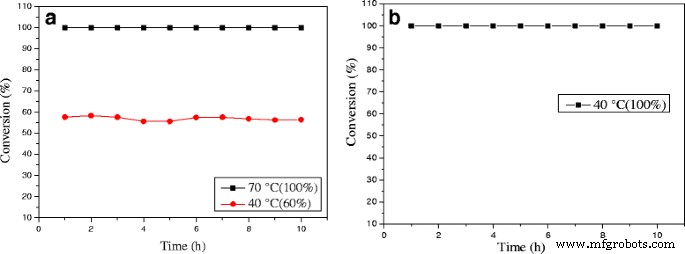
The stability of 0.3% Au/Ce0.75 -La0.25 nanorods, reaction temperature:40 and 70 °C (a ) and 0.5% Au/Ce0.75 -La0.25 nanorods, reaction temperature:40 °C (b ) for the CO oxidation
As engine efficiency increases and automotive exhaust temperatures decrease, traditional supported gold catalysts would be insufficient to meet emission regulations. And there are also a number of industrial catalytic processes which (e. g., the catalytic oxidation of CO in automotive exhaust gas) are sometimes carried out at high temperatures. Thus, the development of new catalysts that are active at lower temperature, yet still stable at periodic high temperatures, will be vital. In the two regards, catalysts with good activity at low temperature that are stable at high reaction temperatures are desirable. It is necessary to investigate their catalytic performance for CO oxidation at a certain high temperature which is a very stringent test for the stability of gold nanocatalysts against sintering. In the present work, the stability of 0.3% Au/Ce0.75 -La0.25 nanorod catalyst was also measured at 200 °C (100%) for high-temperature treatment. As shown in Fig. 13, no decline of catalytic activity was observed within 50 h indicates that the catalyst keeps good stability within 50 h. Remarkably, very few serious gold sintering occurred during the reaction. It indicated that 0.3% Au/Ce-La catalyst can exhibit good catalytic stability at both low and high reaction temperatures.
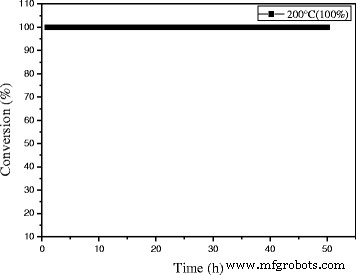
The stability of 0.3% Au/Ce0.75 -La0.25 nanorods at the reaction temperature of 200 °C for CO oxidation
Reaction Mechanism Speculate
Combined with H2 -TPR and XPS experiments, it suggested that CO oxidation over LaO x -doped CeO2 -supported Au catalysts might follow the Langmuir–Hinshelwood + Redox mechanism [1, 20, 26, 30, 32]. The XPS results suggest that there are Ce 3+ and Ce 4+ on the surface of the catalyst. H 2 -TPR data also proved that reducibility of this binary Ce-La nanorod oxides could be promoted by Au deposition. The reducibility of Au/Ce-La nanorods was much higher than pure Au/CeO2 or Au/LaO x catalysts. This would help the produce of oxygen vacancies. The oxygen vacancy is a very lively activity center. The active center can promote the activation of O2 . Thus, the CO oxidation reaction could become more easily. There are also amount of adsorbed oxygen species on the surface of catalyst. Usually adsorbed oxygen species play an important role in the oxidation of CO. The O2 of the reaction will form the chemisorbed oxygen, and the oxygen vacancy would be replenished by O2 of reaction gas to form new active lattice oxygen. XPS data also proved that gold in the catalysts was mainly Au δ+ species, which would accelerate the adsorption of CO. The possible reaction mechanisms of Au/Ce-La nanorod catalyst could be described as follows. Firstly, CO and O2 were chemisorbed on the surface of the catalysts. Then, the chemisorbed oxygen directly reacts with CO, or the active lattice oxygen of the catalyst reacts with CO, and the catalyst produced the oxygen vacancy with oxygen from gas-phase O2 . At last, CO was oxidized into CO2 (shown in Fig. 14).
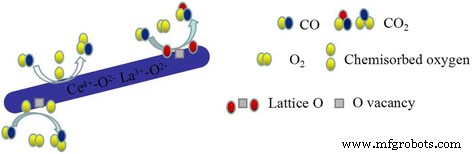
Proposed CO reaction pathways over the catalysts, Au/Ce-La nanorods
Conclusions
In summary, a series of mixed Ce-La nanorods with various amounts of La was prepared via a simple hydrothermal reaction at high concentration of NaOH and without surfactant. Gold was loaded by deposition-precipitation. After La doping, the composite could retain the initial rod morphology. As a result, Ce-La nanorods with 25 at.% La maintained the optimal nanorods with the length of 0.6 um and the diameter of 3–5 nm. Gold particles were dispersed well on the support. The reducibility of Ce-La nanorods could be affected significantly by LaO x doping. The deposition of gold had important influence on the reducibility of catalyst. Thus, the CO oxidation activity of Au/Ce-La nanorods was essentially changed in comparison with pure Au/CeO2 and Au/La nanorods. One percent Au/Ce0.75 -La0.25 nanorods could convert CO to CO2 completely at 30 °C. Further increase in La content results in decreased activity due to the decrease in reducible oxygen sites. The Au/Ce0.75 -La0.25 nanorod catalyst with low gold concentration also showed high activity. With the increase of gold content, there is an increase in the activity. The stability test of 0.3% Au/Ce0.75 -La0.25 nanorods indicated that the catalyst not only kept 100% conversion after continuous operation for 10 h under 70 °C but also showed no deactivation after 10 h on stream at 40 °C. As expected, the activity of 0.3% Au/Ce0.75 -La0.25 nanorods also retained a 100% CO conversion during 50 h at 200 °C. The results revealed that LaO x as the dopant could grow together with CeO2 in one rod. The 1D binary mixed Ce-La nanorods could be a good support for precious metal group catalysts with low content of gold.
Nanomateriales
- Avances y desafíos de los nanomateriales fluorescentes para síntesis y aplicaciones biomédicas
- Síntesis biogénica, caracterización y evaluación del potencial antibacteriano de nanopartículas de óxido de cobre contra Escherichia coli
- Síntesis de compuesto de nanopartículas de oro / nanofibras de sílice conductoras eléctricas mediante pulsos de láser y técnica de pulverización
- Bioseguridad y capacidad antibacteriana del grafeno y el óxido de grafeno in vitro e in vivo
- Síntesis de nanocristales de ZnO y aplicación en células solares de polímero invertido
- Síntesis de calentamiento de estado sólido de compuesto de poli (3,4-etilendioxitiofeno) / oro / grafeno y su aplicación para la determinación amperométrica de nitrito y yodato
- Síntesis fácil de óxido de estaño mesoporoso similar a un agujero de gusano a través del autoensamblaje inducido por evaporación y las propiedades mejoradas de detección de gas
- Síntesis en un solo recipiente de nanoplacas de Cu2ZnSnSe4 y su actividad fotocatalítica impulsada por la luz visible
- Saponinas Platycodon de Platycodi Radix (Platycodon grandiflorum) para la síntesis verde de nanopartículas de oro y plata
- Síntesis verde de nanopartículas de metal y óxido de metal y su efecto sobre el alga unicelular Chlamydomonas reinhardtii
- Propiedades de las nanopartículas de óxido de zinc y su actividad contra los microbios



