Síntesis biogénica, caracterización y evaluación del potencial antibacteriano de nanopartículas de óxido de cobre contra Escherichia coli
Resumen
El desarrollo de resistencia a los antibióticos utilizados para tratar infecciones bacterianas junto con la prevalencia de residuos de medicamentos presenta importantes problemas de salud pública a nivel mundial. Los gérmenes resistentes a los antibióticos provocan infecciones que son difíciles o imposibles de tratar. La disminución de la eficacia de los antibióticos requiere un rápido desarrollo de antimicrobianos alternativos. En este sentido, las nanopartículas (NP) de óxido de cobre (CuO) manifiestan una nanoestructura inorgánica latente y flexible con notable impacto antimicrobiano. En el presente estudio se realizó la síntesis verde de NP de CuO, que luego se dopó con cantidades variables de jengibre ( Zingiber officinale , ZO) y ajo ( Allium sativum , AS) extractos. En dosis bajas y altas, el compuesto sintetizado se utilizó para medir la eficacia antimicrobiana contra Escherichia coli patógena. . La presente investigación demostró con éxito una técnica de síntesis renovable y ecológica con materiales naturales que es igualmente aplicable a otros NP de óxidos metálicos verdes.
Introducción
Las plantas autóctonas a base de hierbas y especias incluyen valiosas propiedades antioxidantes y antibacterianas que se emplean en tratamientos humanos y veterinarios [1]. Entre las plantas medicinales que contienen propiedades antimicrobianas se encuentran el ajo, el jengibre, el neem, la cúrcuma, el tulsi, etc. y entre estos, el ajo y el jengibre son famosos por su uso medicinal [2]. Zingiber officinale comúnmente conocido como jengibre es una raíz de planta indígena perteneciente a la familia Zingiberaceae. Contiene gingerol, shogaol, curcumina y paradol como importantes fitoquímicos [3]. La actividad antimicrobiana contra una amplia gama de microbios se ha manifestado por extractos acuosos de jengibre, debido a su contenido fenólico de naturaleza terapéutica [4]. Allium sativum comúnmente conocido como ajo contiene compuestos fenólicos que exhiben una actividad antibacteriana de amplio espectro incluso contra bacterias MDR [5]. Allium sativum ha exhibido una actividad antibacteriana de amplio espectro contra varias bacterias Gram positivas y Gram negativas [6].
La explotación del conocimiento de la nanotecnología a nivel molecular y atómico sirve como base para aplicar un enfoque integrador para desarrollar compuestos novedosos con características únicas para su uso en aplicaciones de amplio espectro [7]. Las aplicaciones medicinales, agrícolas, conservantes de alimentos y cosméticas de las nanopartículas debido a sus propiedades inherentes incomparables han llevado a una mayor exploración por parte de los investigadores [8, 9]. Se han demostrado con éxito varias aplicaciones biológicas de las nanopartículas de óxido de cobre, incluidos posibles antimicrobianos, compuestos terapéuticos eficaces, portadores de administración de fármacos, fotocatalizadores, detección de gases, estabilidad fotovoltaica, efecto de confinamiento cuántico y sondas biológicas [10,11,12,13,14]. La generación de especies reactivas de oxígeno (ROS) es desencadenada por nanopartículas debido a su naturaleza semiconductora, que traen transformaciones oxidativas y degenerativas a nivel celular que resultan en la destrucción de las paredes celulares bacterianas y la liberación de contenido celular [15]. Se han practicado muchos métodos para la síntesis de nanopartículas, es decir, síntesis química, física y biológica [16]. La reducción de compuestos metálicos da como resultado la producción de nanopartículas utilizando cualquier bioquímico o microorganismo, plantas o sus extractos [17].
Escherichia coli ( E. coli ), un habitante natural del intestino y parte de la flora intestinal, tiene una posición distintiva en el mundo microbiológico debido a sus potenciales propiedades virulentas [18]. La existencia de virulencia depende del número de genes en E. coli También se han revelado aislamientos y, en algunos casos, la transferencia horizontal de genes de resistencia [19, 20] que pueden crear un problema de salud en los seres humanos y los animales [21] y un desafío para la seguridad alimentaria [22]. E. coli es el agente causante de mastitis en vacas lecheras y búfalos y se encontró responsable de una disminución importante en la producción de leche y las consiguientes pérdidas económicas [23, 24], que desarrollaron genes de resistencia, es decir, β-lactamasas de espectro extendido (BLEE) o sobre- expresaron cefalosporinasas (AmpCs) [25]. Fracaso del tratamiento asociado con E. coli Las infecciones se consideran una amenaza latente que conduce a la resistencia a múltiples fármacos tanto en medicamentos humanos como veterinarios [26].
Las nanopartículas con sus características antimicrobianas tienen el potencial de matar alrededor de 600 células en contraste con la capacidad de los antibióticos para tratar solo unas pocas enfermedades de origen infeccioso [27]. El presente estudio tiene como objetivo explorar, evaluar y comparar el posible potencial antimicrobiano de nanopartículas de CuO verdes y sintetizadas químicamente y extractos de raíces de hierbas comunes de Allium sativum (AS) y Zingiber officinale (ZO), contra E. coli como alternativas a los antibióticos para superar los desafíos emergentes de resistencia.
Métodos
El presente estudio tuvo como objetivo investigar la acción bactericida de NP de CuO reducidas fitoquímicamente contra raíces de hierbas de Allium sativum (AS) y Zingiber officinale (ZO), un aislado de mastitis bovina.
Materiales
Las nanopartículas de CuO fabricadas químicamente se adquirieron de Sigma-Aldrich, mientras que las raíces de ZO y AS se adquirieron en el mercado local de frutas y verduras de Lahore, Pakistán. Las raíces de ZO y AS se secaron a la sombra para lograr un peso uniforme. Medios de crecimiento para E. coli y los productos químicos de grado analítico se utilizaron sin modificaciones.
Extracción acuosa de raíces ZO y AS
Las raíces secas de ZO y AS se trituraron ultrafinas hasta obtener polvos finos que luego se almacenaron en frascos herméticos. Se llevó a cabo una fuerte agitación de 30 min a 70 ° C para mezclar raíces en polvo fino con agua destilada-DIW en una proporción de 1:10. La filtración de las soluciones preparadas se realizó usando papel de filtro Whatman No. 1 después de enfriar las soluciones y el almacenamiento del filtrado se llevó a cabo a 4 ° C para el siguiente experimento [28] como se muestra en la Fig. 1a.
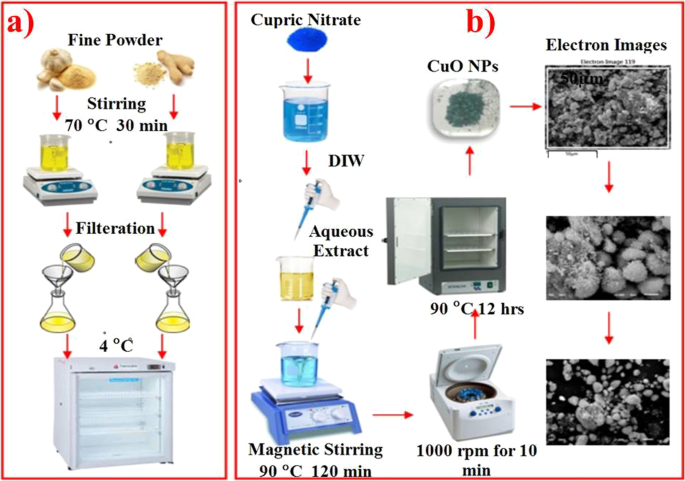
Descripción general de a extracción acuosa de Zingiber officinale y Allium sativum raíces, b síntesis verde de CuO NP
Síntesis verde de CuO
Se mezcló nitrato cúprico tetrahidratado (0,1 M) con diferentes concentraciones, es decir, 3 ml, 6 ml y 12 ml de extractos de ZO y AS con agitación continua. Se usó NaOH (2 M) para mantener el pH 12 de la solución agitada durante 2 ha 90ºC para la formación de precipitados. La centrifugación de los precipitados se llevó a cabo a 10.000 rpm durante 20 min, seguido de lavado con agua desionizada y secado durante la noche en un horno de aire caliente a 90 ° C [29] como se muestra en la Fig. 1b.
Caracterización
Se utilizó el espectrofotómetro GENESYS-10S UV-visible para comprobar los espectros de absorción de nanopartículas de CuO y extractos acuosos de ZO y AS en un rango de longitudes de onda de 200 a 500 nm [30]. El análisis estructural y de fase de CuO NP se realizó mediante difracción de rayos X (XRD) BRUKER D2 Phaser con 2 θ =(10 ° –80 °) equipado con radiación Cu Kα de λ =1,540 Å [31]. Se realizó espectroscopia infrarroja por transformada de Fourier (ATR-FTIR) para el análisis de grupos funcionales en NP de CuO y extractos acuosos de ZO y AS [31]. Se llevó a cabo una microscopía electrónica de barrido (JSM-6610LV SEM) junto con un detector EDS para la observación de la constitución elemental y morfológica de las NP de CuO. Se tomaron imágenes TEM de alta resolución y patrones SAED utilizando el microscopio JEOL JEM-2100F [32].
E. coli Aislamiento e identificación
Colección de muestras
Se rastrearon e identificaron vacas y búfalos que padecían mastitis clínica en varias explotaciones ganaderas para la recolección de muestras de leche.
E. coli Aislamiento
Se usó agar MacConkey para sembrar y cultivar leche por triplicado para el aislamiento de colonias purificadas de E. coli [33]. Difusiones en disco de colonias distintivas de E. coli fueron evaluados para verificar la susceptibilidad frente a antibióticos específicos siguiendo las pautas del Comité Nacional de Estándares de Laboratorio Clínico (NCCLS) para aislar E. coli .
Identificación de E. coli
Identificación y confirmación de E. coli las colonias se llevaron a cabo en base a la tinción de Gram; distinguir caracteres morfológicos y pruebas bioquímicas, es decir, pruebas de rojo de metilo y catalasa con perspectiva al Manual de Bacteriología Sistemática de Bergey. El cultivo de aislados en agar con azul de metileno eosina (EMB) se realizó para E. coli distinción y ratificación de mastitógenos Gram-negativos relacionados.
Evaluación del potencial antibacteriano in vitro de NP de CuO contra E. coli
Se realizaron varios experimentos para evaluar in vitro Potencial antibacteriano del extracto de CuO NP dopado contra E. coli . In vitro Los ensayos se realizaron utilizando 10 E. patógenos representativos. coli aislamientos para la evaluación del potencial antibacteriano de CuO NP. Se utilizó la evaluación del método de difusión en disco para evaluar in vitro potencial antimicrobiano. Se limpiaron placas de Petri con el crecimiento activado de E. coli 1,5 × 108 UFC / ml (0,5 Mcfarland estándar) en agar MacConkey [34]. Se utilizó un barrenador de corcho estéril para preparar pocillos de 6 mm de diámetro en las placas de Petri. Extractos acuosos de ZO y AS , junto con extractos dopados en verde y nanopartículas de óxido de cobre sintetizadas químicamente en diferentes concentraciones, se aplicaron en los pozos. El potencial antimicrobiano de los extractos acuosos de ZO y AS junto con los extractos dopados con verde y las nanopartículas de óxido de cobre sintetizadas químicamente se evaluó incubando aeróbicamente las placas de Petri a 37 ° C durante la noche midiendo las zonas de inhibición (mm) usando un calibre Vernier. El análisis estadístico de las zonas de inhibición (mm) se realizó utilizando ANOVA unidireccional y visualizando ( p <0.05).
Resultados y discusión
Se realizó espectroscopía UV-Vis de NP de CuO dopadas y extractos acuosos de ZO y AS para investigar el comportamiento óptico como se muestra en la Fig. 2a, b. Para la formación posterior de NP de CuO, se observó un cambio gradual de color del vino al negro carbón mientras se realizaba la optimización de los NP sintetizados mediante extractos acústicos abovedados. Se observaron picos de absorción de extractos acuosos ZO y AS a 275 y 280 nm. Los resultados se muestran λ máx para CuO dopado con ZO y AS a 250 nm que representa una relación de 6 ml:1 con corrimientos al rojo y al azul característicos, respectivamente [35]. Los picos anchos especificaron grupos de partículas y la transición de electrones a las bandas de conducción desde la fase de valencia con extractos concentrados en CuO según lo divulgado por las bandas de absorción fuerte [36]. En las NP de CuO sintetizadas en verde, se observó una absorción reducida al aumentar o reducir el volumen del extracto además del valor optimizado (6 ml:1).
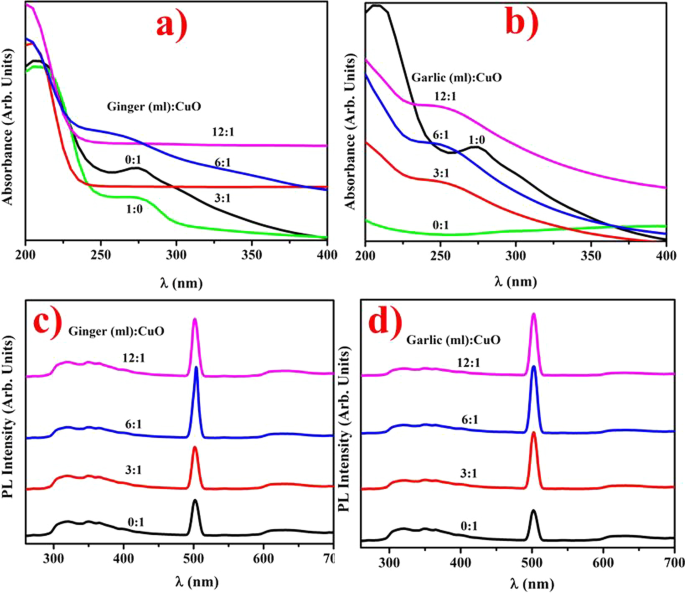
Espectros de absorción de NP de CuO dopadas con a ZO b Extracto de AS y espectro de PL CuO NP con c ZO y d AS extractos, respectivamente
Además, fue notable observar que las estructuras semiconductoras confirmaron sus características físicas a los efectos de tamaño cuántico nanométrico existentes. Los espectros PL de CuO NP dopados con ZO y AS con una excitante longitud de onda UV de 300 nm se presentan en la Fig. 2c, d. Los tres picos de emisión a 418, 561 y 664 nm se representaron en cada gráfico PL puro y dopado de CuO (región UV) [37]. Una banda de luz violeta-azul que se encuentra a 418 nm es un pico de emisión de CuO estándar en el borde cercano de la banda [38, 39]. A 430 nm, el borde del hombro puede deberse a vacantes de CuO, que es un semiconductor de tipo p. El borde verde amarillento es responsable de los defectos de profundidad a bajas temperaturas a 561 nm. Los picos de emisión de rojo a 664 nm son responsables de las diferentes condiciones del cobre o de la presencia de vacantes individuales de oxígeno ionizado [40, 41]. La diversa existencia de emisiones visibles en el espectro violeta-azul, amarillo-verde y rojo indica que las partículas de CuO estudiadas tienen una alta relación volumen-superficie y una multitud de condiciones superficie-volumen y defectos (vacantes o intersticiales) que producen rangos de trampa a emisión [40, 42].
Se realizó una XRD para evaluar la estructura cristalina, la composición y la escala de CuO NP como se presenta en la Fig. 3a, d dopado con ZO y AS, respectivamente. El aumento de cristalinidad se demostró mediante picos detectados a 2 θ =38,7 °, 48,6 °, 53,5 °, 58,3 °, 61,7 ° y 66,2 ° con los correspondientes planos cristalinos (111), (-202), (020), (202), (-113) y (022), respectivamente. Los picos detectados aseguraron la presencia de fase monoclínica de CuO sincronizada con la tarjeta JCPDS nº:00–002–1040 [43]. El tamaño de cristalito característico medido usando D =0,9 λ / β porque θ se encontró que era 24,7 y 47,6 nm para CuO dopado con ZO y AS, respectivamente, y el tamaño de cristalito de la muestra prístina era 27,4 nm. Se han identificado varios productos naturales como agentes de protección y reducción del tamaño medio de cristalito en extractos de AS y ZO [44].
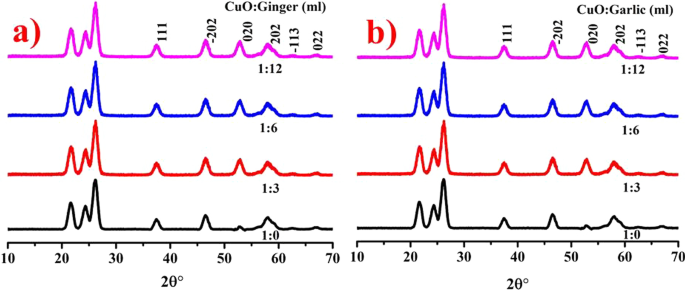
Patrones XRD de CuO NP sin y con dopaje de a AS b ZO
Los grupos funcionales de NP de CuO dopados con extracto de AS y ZO se examinaron con FTIR como se ilustra en la Fig. 4a, b, correspondientemente. El pico ancho a 3314 cm −1 ratificó la presencia de grupos hidroxilo y la amplitud del pico representa C =O directo con (N – H) aminas [45]. El pico intenso a 1638 cm −1 correspondía a CH 2 –OCH 3 grupo existente en 6-snogal y 6-gingerol de ZO ya que encontró una reducción sustancial de CuO. Los enlaces simples típicos de Cu – O observados a 478,8 cm −1 en la forma de torsión se debían a fuertes modos de vibración [46]. Todos los picos sugieren que los grupos alcohol, amina y cetona dieron como resultado quelación y recubrimiento de flavonoides, sustancias químicas vegetales y proteínas [47].
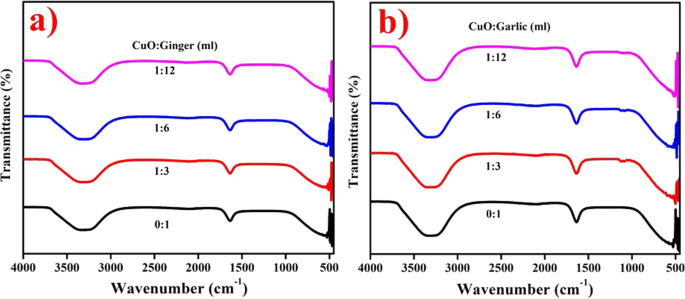
Espectros FTIR de a AS b NP CuO dopadas con ZO
Se utilizó FE-SEM para estudiar las características de la superficie y la escala de NP de CuO dopadas con extracto de ZO y AS, como se muestra en la Fig. 5a – d ′. Las imágenes FE-SEM muestran que las NP de CuO están extremadamente aglomeradas en morfología esférica. La interferencia magnética y la conformidad de los polímeros entre partículas pueden mostrar aglomeración entre partículas [48]. El dopaje de ZO y AS con CuO fue evidente por las imágenes que muestran la formación de grupos y el tamaño de las partículas parece <1 μm, como se ilustra en la Fig. 5b – d ′.

Imágenes CuO NP tomadas con FESEM a CuO, b - d CuO y b ′ dopados con ZO - d ′ NP de CuO dopadas con AS, respectivamente
La espectroscopia de rayos X de dispersión de energía (EDS) ilustró la composición química con una investigación elemental de una muestra prístina y NP de CuO dopado con extractos de raíz de ZO y AS mediante fases de CuO inveterado, como se muestra en la Fig. 6a – d ′. Tres picos correspondientes a la alta pureza de Cu confirmada por EDS de las muestras ensayadas en comparación con el oxígeno precursor entre 1 y 10 keV. La resonancia de plasmón superficial (SPR) de CuO NP dio lugar a picos de absorción [49]. 83,7%, 15,2% y 0,6% se observaron para el peso atómico a través de espectros de Cu, O y Ca, respectivamente, para la muestra de control, mientras que 82,8%, 14,8% y 2,4% para la muestra optimizada y dopada con ZO (6 mL:1) observado a través de espectros de Cu, O y Zn, respectivamente. Asimismo, se encontraron 65,3, 29,6 y 4,6 para Cu, O y S con dopaje AS, respectivamente. Los compuestos atómicos suplementarios que aparecen en EDS respondieron al soporte de muestra SEM utilizado durante el análisis [50].
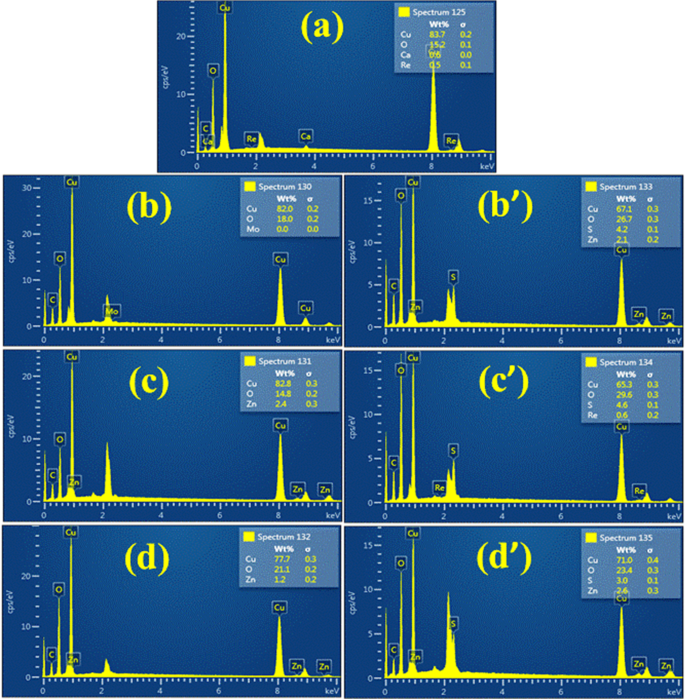
Espectros EDS de CuO NPs a CuO puro b - d CuO y b ′ dopados con ZO - d ′ NP de CuO dopadas con AS, respectivamente
La estructura exclusiva y característica de CuO NP se evaluó adicionalmente utilizando HR-TEM a 50 nm como se muestra en la Fig. 7a-l. Las imágenes HR-TEM revelaron nanopartículas adornadas similares a las imágenes FE-SEM, junto con una mayor aglomeración mientras que el tamaño medía menos de 50 nm. La presencia de fitoquímicos en NP de CuO dopadas con ZO y AS también se confirmó con imágenes HR-TEM [51]. No se observaron imperfecciones ni deformidades en la estructura reticular integral de los NP de CuO dopados con ZO y AS [52]. Se presentaron micrografías filtradas mediante los resultados de HR-TEM junto con la transformada rápida de Fourier [FFT] del área especificada representada por un cuadrado amarillo en la Fig. 7b, d, f, h, j, l presentando características estructurales y atómicas de alta resolución. Las dimensiones medias de partículas de HR-TEM se corresponden con precisión con los tamaños de cristalitos observados durante el análisis de XRD y SEM [53].
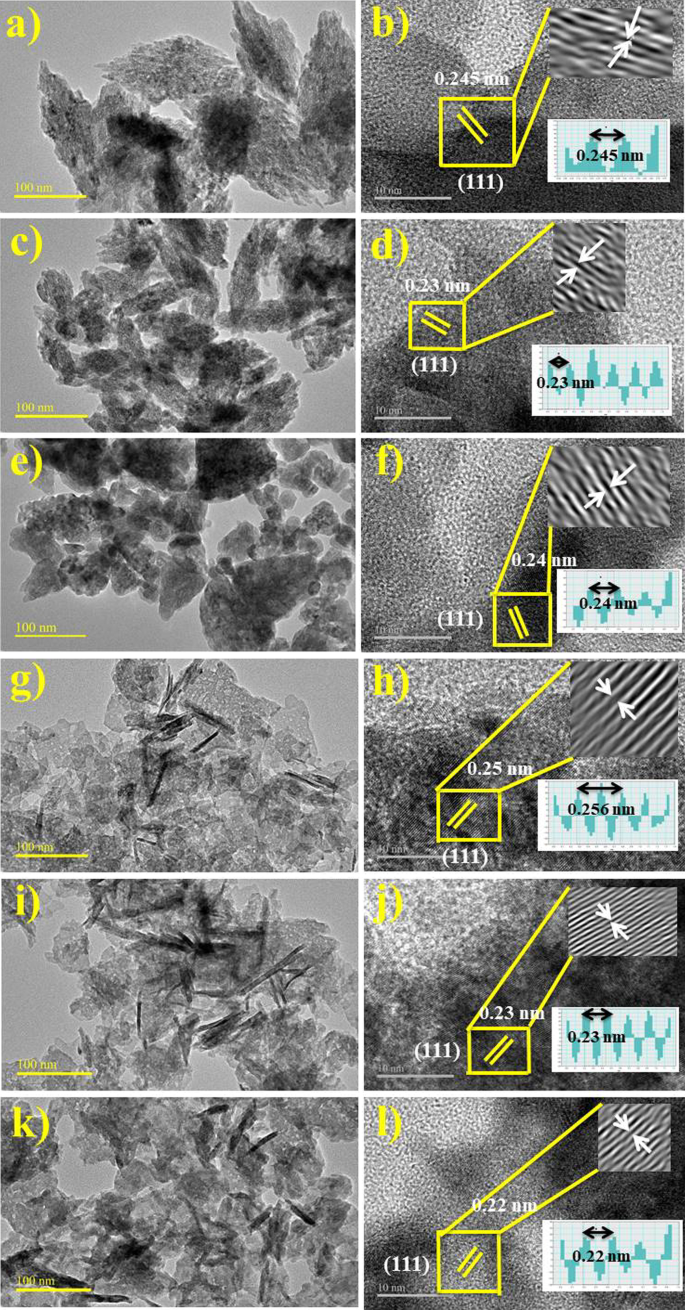
un , b HR-TEM, a - f franjas de celosía de 3 mL, 6 mL y 12 mL CuO dopado con ZO g - l franjas de celosía de NP de CuO dopadas con AS de 3 ml, 6 ml y 12 ml, respectivamente
El análisis XPS de CuO dopado con Gi y Ga CAE que representa C 1 s y Cu 2 p El espectro se muestra en la Fig. 8a, b. El C1 s rango indica la presencia de cuatro picos distintos Fig. 8a con grupos funcionales distintivos como C (H, C) (284.39 eV), C (N) (285.6 eV), C (O, =N) (287.0 eV) y C – O –C (288,75 eV) [54,55,56]. Principalmente, la Fig. 8b muestra Cu 2 p patrón de CuO dopado con picos en energías de unión de 933,3 y 953,3 eV correspondientes a Cu 2 p 3/2 y Cu 2 p 1/2 La órbita de giro indica el estado de oxidación divalente de la muestra preparada. Los picos relevantes a 942,2 y 962 eV se refieren a picos de satélite de Cu 2 p 3/2 y Cu 2 p 1/2 que parecía deberse principalmente a 3 d parcialmente llenos 9 orbital en estado de oxidación divalente [57].
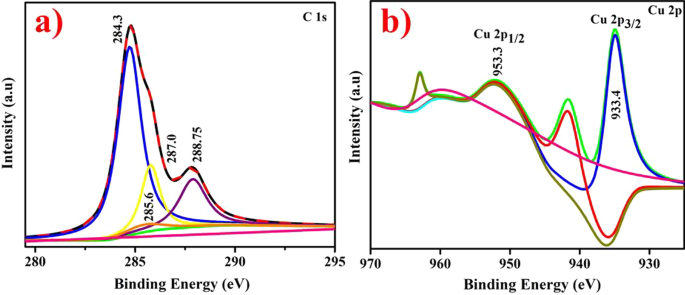
un , b Análisis XPS de NP de CuO dopadas a C1s b Cu 2p
Se aplicó el método de difusión de pozos para la evaluación del potencial bactericida de los extractos acuosos de ZO y AS y se sintetizaron NP de CuO midiendo las áreas de inhibición después de incubar las placas de Petri durante 24 h, como se muestra en la Fig. 9a – d, archivo adicional 1:Fig. S1 y tabulados en la Tabla 1. Los hallazgos revelaron que la concentración de NP y las zonas inhibidoras respondieron sinérgicamente. Las zonas de inhibición significativas encontradas para la muestra 1 (3 mL:1), la muestra 2 (6 mL:1) y la muestra 3 (12 mL:1) fueron (1.05–1.85 mm) y (1.85–2.30 mm) usando disminuciones (↓) y concentraciones aumentadas (↑), respectivamente, para nanopartículas de CuO dopadas con ZO ( p <0,05), figura 9a. De manera similar, los NP dopados con AS exhibieron zonas de inhibición (0,65-1,00 mm) solo a la concentración máxima, figura 9b. Los NP dopados con AS demostraron una eficacia nula contra E. coli a concentraciones mínimas. El extracto de ZO mostró un efecto a una concentración disminuida (↓) en comparación con una concentración aumentada (↑) que muestra una zona de 1,55 mm, de manera similar, no se encontró ningún efecto antibacteriano de los extractos de AS tanto en concentraciones disminuidas (↓) como aumentadas (↑). El control positivo tratado con ciprofloxacino mostró una zona de 4,25 mm mientras que el control negativo tratado con DIW mostró 0 mm. El% de edad de eficacia bactericida se elevó del 24,7 al 43,5% y del 43,5 al 54,1% para los NP dopados con ZO a concentraciones mínima y máxima, respectivamente (Fig. 9c). De manera similar, la eficacia del 15,3 al 23,5% resultó en la concentración máxima sólo para NP dopadas con AS (Fig. 9d). En resumen, el CuO dopado con extracto de ZO y optimizado a 6 ml:1 manifestó un mayor potencial bactericida frente a la E. coli de origen mastitis bovina ( p <0.05) como se muestra en la Fig. 9a, b.
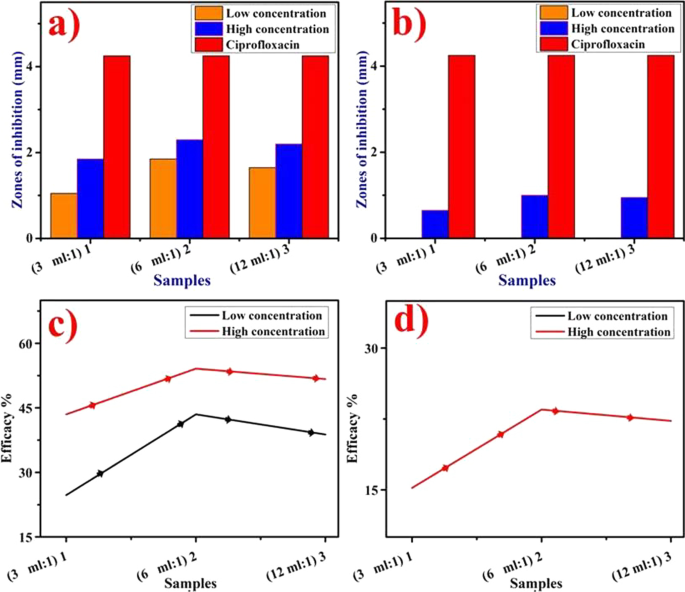
un - d Actividad antibacteriana in vitro de CuO NP a dopado con ZO a ↓ y ↑ dosis, b dopado con AS en ↓ y ↑ dosis, respectivamente, c eficacia% edad dopada con ZO y d eficacia% edad dopada con AS
El potencial bactericida de las nanopartículas depende del tamaño de las NP, la estructura morfológica y la relación superficie-masa. Se cree que las especies reactivas de oxígeno (ROS) son responsables de la formación de zonas de inhibición por nanopartículas de CuO [58, 59]. La desnaturalización de la proteína celular resultó de la generación de especies reactivas de oxígeno (ROS) perjudiciales [60]. Algunas especies reactivas exhibieron papeles trascendentales en la fotocatálisis, como radicales hidroxilo y superóxido y huecos [61]. La síntesis de especies reactivas de oxígeno (ROS) y la liberación de iones metálicos son las principales características que manifiestan los cambios estructurales de las enzimas y proteínas, lo que resulta en un daño irreparable del ADN y la posterior muerte bacteriana [62]. De manera similar, el estrés oxidativo producido por especies reactivas de oxígeno (ROS) se considera el principal contribuyente a la fotocatálisis [63]. La producción de ROS es inversamente proporcional al tamaño de las nanopartículas, es decir, cuanto menor es el tamaño de las NP, mayor es la producción de ROS que, en consecuencia, daña la membrana bacteriana, lo que da como resultado la extrusión del contenido citoplásmico y la degradación del ADN que conduce a la explosión bacteriana, como se muestra en la Fig.10. Al mismo tiempo, el Cu cargado positivamente interactúa electrostáticamente con la membrana bacteriana cargada negativamente dando como resultado la desintegración celular y finalmente la destrucción bacteriana [58, 64, 65]. Se han propuesto dos respuestas como posibles para el mecanismo bactericida de las nanoestructuras. Uno implica un mejor enlace entre los cationes Cu 2+ y células bacterianas, lo que lleva a la formación de secciones negativizadas y finalmente al colapso. El otro implica la excitación electrónica de la superficie de la banda de cenefa de CuO mediante excitación. Además, el O 2 eléctrico la reacción produce O 2− radicales, que conducen a la formación de H 2 O 2 . El O 2− generado Las especies son esenciales para la descomposición de las moléculas de lípidos o proteínas en la membrana celular exterior de las bacterias [58, 66].
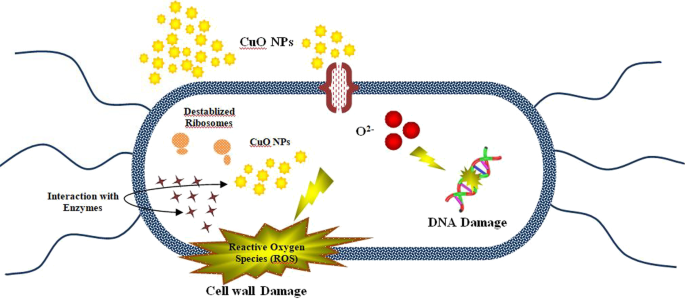
Ilustración de la acción bactericida de CuO NP
Conclusiones
Potencial bactericida de los NP de CuO dopados con Zingiber officinale y Allium sativum extractos contra E. coli fue evaluado en este estudio, elaborado con el objetivo de antimicrobianos alternativos, económicos y efectivos. El papel significativo de los ingredientes fitoquímicos de los extractos de ZO y AS se reveló en la síntesis biogénica de NP de CuO, mientras que se descubrió que los efectos sinérgicos de los flavonoides con CuO dependen de la concentración y explotan el potencial bactericida contra E. coli . Se realizó FTIR para confirmar el dopaje de extractos de ZO y AS y los picos de XRD confirmaron la fase monoclínica y la estructura esférica con tamaños medios de 24,7 nm (dopado con ZO) y 47,6 nm (dopado con AS). La morfología esférica se confirmó con imágenes FESEM junto con una exorbitante conglomeración de NP de CuO. Las nanopartículas adornadas revelaron una mayor aglomeración en imágenes TEM con un tamaño de menos de 50 nm. Para las muestras dopadas con extractos de raíces, se encontró que el espaciado entre capas de nanopartículas de CuO medido como 0,23 nm era compatible con los patrones de XRD. Los resultados de este estudio sugieren que se puede anticipar el potencial antibacteriano de las NP de CuO sintetizadas en verde como agentes bactericidas alternativos para corregir las preocupaciones relacionadas con la resistencia y los residuos de los antibióticos. Se puede concluir que los NP de CuO dopados con hierbas autóctonas son agentes antibacterianos económicos, eficaces y respetuosos con la naturaleza.
Disponibilidad de datos y materiales
Todos los datos están completamente disponibles sin restricciones.
Abreviaturas
- EDS:
-
Espectroscopia de rayos X de dispersión de energía
- fcc:
-
Cúbico centrado en la cara
- FTIR:
-
Espectroscopía infrarroja por transformada de Fourier
- G + ve:
-
Gram positivo
- G −ve:
-
Gram negativo
- JCPDS:
-
Comité conjunto sobre estándares de difracción de polvo
- CuO:
-
Óxido de cobre
- nm:
-
Nanómetro
Nanomateriales
- Eliminación por adsorción de iones de cobre (II) de una solución acuosa utilizando un nano-adsorbente de magnetita de residuos de cascarilla de molino:síntesis, caracterización, adsorción y mode…
- Síntesis fácil y propiedades ópticas de nanocristales y nanovarillas de selenio pequeños
- Síntesis fácil de compuesto de CuSCN coloreado y conductor recubierto con nanopartículas de CuS
- Bioseguridad y capacidad antibacteriana del grafeno y el óxido de grafeno in vitro e in vivo
- Propiedades de síntesis y luminiscencia de nanopartículas de α-NaGdF4 / β-NaYF4:Yb, Er Core-Shell solubles en agua
- Síntesis y actividad de oxidación del CO de óxido binario mixto 1D CeO2-LaO x catalizadores de oro soportados
- Aptitud ecológica en la síntesis y estabilización de nanopartículas de cobre:actividades catalíticas, antibacterianas, citotóxicas y antioxidantes
- Síntesis y caracterización de nanoestructuras de cobre puro utilizando la arquitectura inherente de la madera como plantilla natural
- Las nanopartículas de oxohidróxido de cobre dopado con ligando son antimicrobianos eficaces
- Un escrutinio comparativo in vivo de nanopartículas de óxido de zinc y cobre biosintetizadas por vías de administración intraperitoneal e intravenosa en ratas
- Síntesis verde de nanopartículas de metal y óxido de metal y su efecto sobre el alga unicelular Chlamydomonas reinhardtii



