Aptitud ecológica en la síntesis y estabilización de nanopartículas de cobre:actividades catalíticas, antibacterianas, citotóxicas y antioxidantes
Resumen
Las nanopartículas de cobre (CuNPs) son de gran interés por sus extraordinarias propiedades como alta relación superficie-volumen, alto límite elástico, ductilidad, dureza, flexibilidad y rigidez. Las CuNP muestran actividades catalíticas, antibacterianas, antioxidantes y antifúngicas junto con propiedades citotoxicológicas y anticancerígenas en muchas aplicaciones diferentes. Se han utilizado muchos métodos físicos y químicos para sintetizar nanopartículas que incluyen ablación láser, proceso asistido por microondas, sol-gel, coprecipitación, descarga de alambre pulsado, deposición de vapor al vacío, irradiación de alta energía, litografía, molienda mecánica, reducción fotoquímica, electroquímica , síntesis por electropulverización, reacción hidrotermal, microemulsión y reducción química. La fitosíntesis de nanopartículas se ha sugerido como una alternativa valiosa a los métodos físicos y químicos debido a su baja citotoxicidad, perspectivas económicas, biocompatibilidad mejorada y respetuosa con el medio ambiente y alta actividad antioxidante y antimicrobiana. La revisión explica las técnicas de caracterización, su función principal, las limitaciones y la sensibilidad utilizadas en la preparación de CuNP. Una descripción general de las técnicas utilizadas en la síntesis de CuNP, el procedimiento de síntesis, los parámetros de reacción que afectan las propiedades de los CuNP sintetizados y un análisis de detección que se utiliza para identificar fitoquímicos en diferentes plantas se presenta a partir de la literatura publicada recientemente que ha sido revisada y resumida. . Se dan los mecanismos hipotéticos de reducción del ión cobre por quercetina, estabilización de nanopartículas de cobre por santina, actividad antimicrobiana y reducción de 4-nitrofenol con ilustraciones esquemáticas. El objetivo principal de esta revisión fue resumir los datos de las plantas utilizadas para la síntesis de CuNP y abrir una nueva vía para que los investigadores investiguen aquellas plantas que no se han utilizado en el pasado.
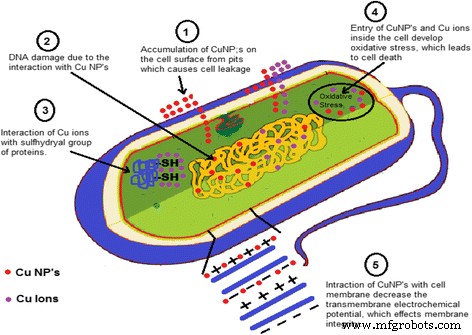
Mecanismo propuesto para la actividad antibacteriana de las nanopartículas de cobre.
Antecedentes
Las nanopartículas (NP) tienen una serie de aplicaciones interesantes en el campo industrial, como la tecnología espacial, el magnetismo, la optoelectrónica y electrónica, la cosmética y las aplicaciones catalíticas, farmacéuticas, biomédicas, medioambientales y energéticas [1, 2]. Las propiedades extraordinarias de los NP como ductilidad, alto límite elástico, dureza, flexibilidad, rigidez, alta relación superficie-volumen, efecto de túnel macrocuántico y tamaño cuántico son atribuibles en comparación con las propiedades de los materiales a granel que tienen la misma composición química [3 ]. De hecho, las propiedades de las NP, que pueden diferir considerablemente de las observadas para las partículas finas, son una mayor superficie específica, propiedades ópticas específicas, puntos de fusión más bajos, magnetizaciones específicas, resistencia mecánica y numerosas aplicaciones industriales [4]. Las nanopartículas de cobre (CuNP) son de gran interés debido a su fácil disponibilidad, bajo costo y propiedades similares a las de los metales nobles [5,6,7,8,9]. Los CuNP también se pueden utilizar en sensores, sistemas de transferencia de calor [10,11,12] y electrónica (pila de combustible y pila solar), como catalizadores en muchas reacciones y como agentes bactericidas y antimicrobianos utilizados para revestir equipos hospitalarios [13,14, 15, 16, 17, 18, 19].
Numerosos métodos físicos y químicos, incluida la ablación con láser [20], el proceso asistido por microondas, el sol-gel [21], la coprecipitación [22], la descarga de alambre pulsado [23], la deposición de vapor al vacío [24], la irradiación de alta energía [ 25], litografía [26], fresado mecánico [27], reducción fotoquímica, electroquímica [28,29,30,31,32], síntesis por electropulverización [33], reacción hidrotermal [34], microemulsión [35] y reducción química se utilizan para sintetizar nanopartículas. Aunque los métodos físicos y químicos producen nanopartículas puras y bien definidas, estos métodos no son rentables ni ecológicos debido al uso de productos químicos tóxicos. Uno de los criterios más importantes de la nanotecnología es el desarrollo de procedimientos químicos ecológicos, no tóxicos y limpios [36]. Por lo tanto, la biosíntesis de nanopartículas contiene un método basado en la química verde que emplea diferentes cuerpos biológicos como plantas [37, 38], actinomicetos [39, 40], hongos [41,42,43,44], bacterias [45,46, 47,48,49], levadura [50,51,52] y virus [53, 54]. Las entidades biológicas ofrecen un enfoque no tóxico, limpio y respetuoso con el medio ambiente para sintetizar los NP con una amplia gama de tamaños, propiedades fisicoquímicas, formas y composiciones [55].
Las nanopartículas de cobre se sintetizaron y estabilizaron en la literatura utilizando diferentes plantas como Euphorbia esula [56], Punica granatum [57], Ocimum sanctum [58], Ginkgo biloba [59], Calotropis procera [60], Lawsonia inermis [61], Citrus medicalinn [62], Camellia sinensis [63], Datura innoxia [64], Syzygium aromaticum [65], Sesamum indicum [66], Citrus limon , curcumina de cúrcuma [67], Gloriosa superba L. [68], Ficus carica [69], Aegle marmelos [70], Caesalpinia pulcherrima [71], Cassia fístula [72], Leucas aspera , Leucas chinensis [73], Delonix elata [74], Aloe barbadensis Miller [75], Thymus vulgaris [76], Phyllanthus emblica [77], Magnolia kobus [78], Eucalipto [79], Artabotrys odoratissimus [80], Capparis zeylanica [81], Vitis vinifera [82], Hibiscus rosa-sinensis [83], Zingiber officinale [84], Datura metel [85], Zea mays [86], Urtica , Matricaria chamomilla , Glycyrrhiza glabra , Schisandra chinensis , Inula helenium , Cinnamomum [87], Dodonaea viscosa [88], Cassia auriculata [89], Azadirachta indica , cámara Lantana , Tridax procumbens [90], Allium sativum [91], Asparagus adscendens , Bacopa monnieri , Ocimum bacilicum , Withania somnifera [92], Smithia sensitiva , Colocasia esculenta [93], Nerium oleander [94] y Psidium guajava [95]; mediante el uso de diferentes algas / hongos como Phaeophyceae [96], Stereum hirsutum [97] y Hypocrea lixii [98]; y mediante el uso de algunos microorganismos como Pseudomonas fluorescens [99] y Enterococcus faecalis [100] culturas.
Biosíntesis de nanopartículas de cobre
Partes de la planta utilizadas para el extracto
Se utilizan diferentes partes de las plantas para la preparación de extractos de plantas como hojas, semillas, cortezas, frutos, piel, bonote, raíces y goma de mascar. Las hojas y las raíces se utilizan de dos formas. En primer lugar, se utilizan hojas y raíces frescas para la preparación de extractos de plantas y, en segundo lugar, se utilizan hojas y raíces secas en forma de polvo.
Procedimiento para la síntesis de CuNP
Para la síntesis de CuNP, se preparó extracto vegetal utilizando diferentes partes de diferentes plantas. Para la síntesis de la parte del extracto de la planta de interés, se recogen las hojas y se lavan con agua del grifo y luego con agua destilada para eliminar las partículas de polvo. Las hojas lavadas se utilizan además de dos formas. Primero, estas hojas se secan al sol durante 1 a 2 h para eliminar la humedad residual. Los pesos conocidos de estas hojas secadas al sol se dividen en pequeñas partes y se sumergen en agua desionizada o en una solución de etanol. Esta mezcla se agita durante 24 ha temperatura ambiente usando un agitador magnético y luego se filtra para su uso posterior. En segundo lugar, estas hojas se secan al sol durante 4 a 7 días o se secan en un horno a 50 ° C durante 1 día y se pulverizan con una licuadora doméstica. El peso conocido de polvo vegetal se mezcla en agua o solución de etanol y luego se agita y filtra.
Para la síntesis de CuNP, se mezcla una solución acuosa de sales precursoras como sulfato de cobre, cloruro de cobre, acetato de cobre y nitrato de cobre con diferentes concentraciones con extracto vegetal. También se prepara una solución acuosa de hidróxido de sodio y se agrega a la mezcla de reacción para controlar el pH del medio. La mezcla de reacción se agita fuertemente durante diferentes intervalos de tiempo en un agitador eléctrico y se calienta en un horno a diferentes intervalos de tiempo y a diferentes temperaturas. La formación de CuNP también puede tener lugar a temperatura ambiente y se confirma cambiando el color de la mezcla de reacción. Al final, las nanopartículas se centrifugaron y secaron a diferentes temperaturas. Las optimizaciones de la reacción tienen lugar cambiando el pH de la mezcla, la concentración de la sal precursora, el tiempo de calentamiento y la temperatura de la mezcla de reacción. En la literatura, se han utilizado diferentes plantas para la formación de nanopartículas de cobre mediante el uso de diferentes sales precursoras con diferentes condiciones de reacción, como se muestra en la Tabla 1. De la tabla, se puede ver que las diferentes condiciones de reacción afectan la forma y el tamaño del cobre. nanopartículas.
Efecto de los parámetros de reacción en las propiedades de los NP
La concentración de extracto vegetal juega un papel principal en la reducción y estabilización de CuNP. Se ha informado de que al aumentar la concentración de extracto vegetal, aumenta el número de partículas [88]. Al aumentar la concentración de extracto vegetal, aumentó la concentración de fitoquímicos y también aumentó la reducción de la sal de cobre. Debido a la rápida reducción de la sal metálica, el tamaño de las nanopartículas también disminuyó [101].
El tamaño y la estructura de los CuNP se ven muy afectados por la sal de cobre. La morfología de las nanopartículas cambia cuando la sal (p. Ej., Cloruro de cobre, acetato de cobre, nitrato de cobre o sulfato de cobre) se usa en presencia de hidróxido de sodio. Se informó que la forma era triangular y tetraedro en el caso del cloruro de cobre, de barra en el caso del acetato de cobre y esférica en el caso del sulfato de cobre [102]. Al aumentar la concentración de la sal precursora, también aumentó el tamaño de los CuNP.
La síntesis de CuNP da mejores resultados al variar el pH del medio de reacción dentro del rango preferido. El tamaño de las nanopartículas se controló cambiando el valor de pH de la mezcla de reacción. A pH más alto, se obtuvieron nanopartículas de menor tamaño en comparación con las obtenidas a un valor de pH bajo. Esta diferencia se puede atribuir a la diferencia en la tasa de reducción de las sales metálicas por extracto vegetal. La relación inversa entre el valor de pH y el tamaño de la nanopartícula mostró que un aumento en el valor de pH nos permite obtener nanopartículas esféricas de pequeño tamaño, mientras que una disminución en el valor de pH da nanopartículas de gran tamaño (en forma de barra y triangulares). El efecto sobre los espectros de absorción de diferentes valores de pH (4, 6, 8, 10 y 12) se representa en la Fig. 1 [36]. Se informó que la adición de extracto vegetal a CuCl 2 no condujo a la formación de CuNP sino que, en cambio, los CuNP se obtuvieron cambiando el pH de la mezcla de reacción a medio básico. Wu y Chen observaron el mismo comportamiento, y se concluyó que el pH juega un papel importante en la síntesis de CuNP [103].
Partes de la planta utilizadas para la preparación de extracto vegetal
Mecanismo de fitosíntesis de nanopartículas de cobre
Detección fitoquímica:un análisis cualitativo
El análisis de cribado fitoquímico es un análisis químico que se lleva a cabo para la detección de fitoquímicos en diferentes plantas. Para este análisis se utiliza extracto de planta fresca con productos químicos o reactivos químicos [77], como se muestra en la Tabla 2.
Fitoquímicos para la reducción de metales y estabilización de NP
La síntesis verde de CuNP mediante el uso de fitoquímicos ofrece un control más flexible sobre la forma y el tamaño de los NP (es decir, al cambiar la temperatura de reacción, la concentración de extracto vegetal, la concentración de sal metálica, el tiempo de reacción y el pH de la mezcla de reacción). El cambio de color del medio de reacción indica la reducción del ión metálico y la formación de NP. La reducción verde de las sales de cobre comienza instantáneamente y la formación de nanopartículas de cobre está indicada por el cambio de color de la mezcla de reacción. Los fitoquímicos tienen un papel principal al reducir primero los iones metálicos y luego estabilizar los núcleos del metal en forma de nanopartículas, como se muestra en la Fig. 2. La interacción de los fitoquímicos con los iones metálicos y la concentración de estos fitoquímicos controlan la forma y el tamaño de los CuNP.
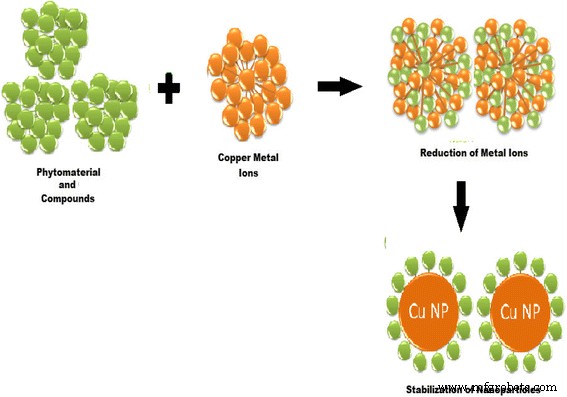
Un protocolo para reducir los iones metálicos y luego estabilizar los núcleos del metal
Los flavonoides contienen compuestos polifenólicos, por ejemplo, quercetina, catequinas, flavanonas, isoflavonas, santina, penduletina, alizarina, pinocembrina, antocianinas, flavonas, taninos y saponinas, que están presentes en diferentes plantas como Ginkgo biloba [59], Citrus medicalinn [62], Phyllanthus emblica [77], Hibiscus rosa-sinensis [83] y Dodonaea viscosa [93]. Estos compuestos juegan un papel principal en la reducción y quelación del metal. Varios grupos funcionales presentes en los flavonoides son responsables de la reducción del ion cobre. Se ha supuesto que un átomo de hidrógeno reactivo en los flavonoides puede liberarse durante las alteraciones tautoméricas de la forma enol a la forma ceto, lo que puede reducir los iones de cobre para formar núcleos de cobre o CuNP. Por ejemplo, se supone que en el caso de Ginkgo biloba extractos de plantas, es la transformación de la quercetina (flavonoide) la que juega un papel principal en la reducción de iones metálicos de cobre en núcleos de cobre o CuNP debido al cambio de forma enol a ceto como se muestra en la Fig. 3.
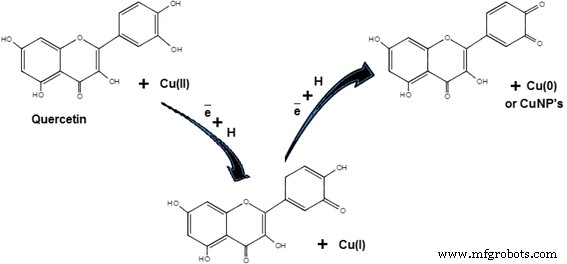
Reducción de iones de cobre por quercetina
Durante el proceso de síntesis de CuNP, los iones metálicos con estados de oxidación monovalente o divalente se convierten en núcleos de cobre de oxidación cero y estos núcleos se fusionan para obtener diferentes formas. Durante la nucleación, los núcleos se agregan para formar diferentes formas, como alambres, esferas, cubos, varillas, triángulos, pentágonos y hexágonos. Algunos flavonoides tienen la capacidad de quelar los CuNP con su π electrones y grupos carbonilo. La quercetina y la santina son flavonoides con fuerte actividad quelante debido a la presencia de dos grupos funcionales que involucran a los hidroxilos y carbonilos. Estos grupos se quelan con nanopartículas de cobre siguiendo el mecanismo anterior y también explican la capacidad de adsorción de santina (flavonoide) en la superficie de CuNP como se muestra en la Fig. 4.
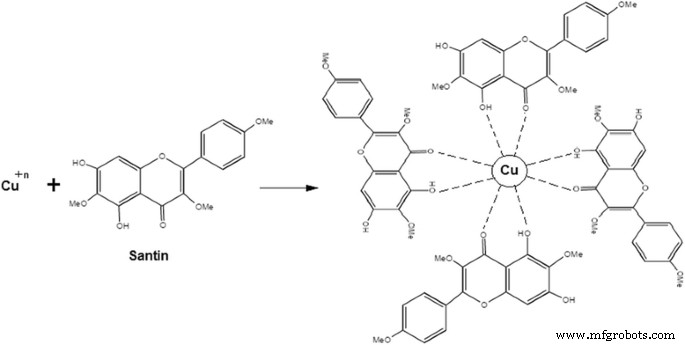
Estabilización de nanopartículas de cobre por santin
Se asumió que las moléculas de proteína (superóxido dismutasa, catalasa, glutatión) en diferentes plantas como Hibiscus rosa-sinensis [83] y Camellia sinensis [104] muestran una alta actividad reductora para la formación de nanopartículas a partir de iones metálicos, pero su actividad quelante no es excesiva. Azúcares como monosacáridos (glucosa), disacáridos (maltosa y lactosa) y polisacáridos en Camellia sinensis La planta [63] puede actuar como agentes reductores o antioxidantes y tener una serie de transformaciones tautoméricas de cetona a aldehído.
Otros fitoquímicos como los polifenoles (p. Ej., Ácido elágico y ácido gálico) que están presentes en Hibiscus rosa-sinensis [40], fenilpropanoides (fenilalanina, tirosina) en Aegle marmelos [70], terpenoides en Ocimum sanctum y Asparagus adscendens [58, 92], cisteína proteasas en Calotropis procera [60], curcumina anilineazometina en curcumina de cúrcuma [67], ácido ascórbico en Citrus medicalinn [62], eugenol en Syzygium aromaticum [65] y alcaloides en Aegle marmelos [70] desempeñan el mismo papel de reducir los iones de cobre y estabilizar las nanopartículas de cobre. Carbohidratos, antraquinona, quinona y antocianósido en Phyllanthus emblica [77]; ligninas y xantonas en Hibiscus rosa-sinensis [83]; y glucósido cardíaco, triterponoide, glucósido carotenoide y glucósido de antraquinona en Colocasia esculenta plant [93] son también fitoquímicos que están presentes en extractos de diferentes plantas y actúan como agentes reductores y estabilizantes. En la Fig. 5 se muestran ejemplos de ciertos fitoquímicos con estructuras.
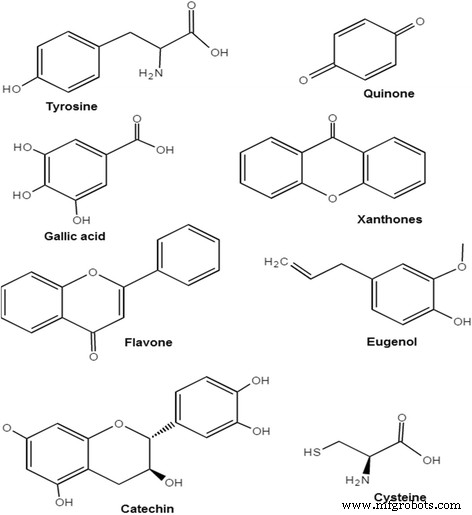
Fitoquímicos con sus estructuras
Técnicas de caracterización
Para la caracterización de nanopartículas sintetizadas se utilizaron diferentes técnicas como espectroscopia ultravioleta-visible (UV-vis), microscopía electrónica de transmisión (TEM), dispersión de rayos X de ángulo pequeño (SAXS), espectroscopía infrarroja por transformada de Fourier (FTIR), X- espectroscopía de fluorescencia de rayos (XRF), difracción de rayos X (XRD), espectroscopía de fotoelectrones de rayos X (XPS), microscopía electrónica de barrido (SEM), microscopía electrónica de barrido por emisión de campo (FESEM), análisis del tamaño de partículas (PSA), Malvern Zetasizer ( MZS), espectroscopia de rayos X de dispersión de energía (EDX / EDS), análisis de seguimiento de nanopartículas (NTA), reflectometría de rayos X (XRR), análisis Brunauer-Emmett-Teller (BET), difracción de electrones de área seleccionada (SAED) y microscopía de fuerza atómica (AFM) (Tabla 3).
Aplicaciones de nanopartículas de cobre
Debido a sus excelentes propiedades químicas y físicas, gran relación superficie-volumen, superficie constantemente renovable, bajo costo y preparación no tóxica, los CuNP han sido de gran interés para aplicaciones en diferentes campos. Las nanopartículas de cobre presentan actividad catalítica, actividad antibacteriana, citotoxicidad o actividad anticancerígena, actividad antioxidante y actividad antifúngica en diferentes aplicaciones. En la actividad catalítica, las nanopartículas de cobre se utilizan para la cicloadición Huisgen [3 + 2] de alquinos y azidas en muchos disolventes en condiciones libres de ligando [59], 1-metil-3-fenoxibenceno, 3,3-oxibis (metilbenceno) [94], síntesis de 1 H sustituido en 1 -1,2,3,4-tetrazol [76], adsorción de dióxido de nitrógeno y adsorción de dióxido de azufre [66]. En la mayoría de los metales de transición catalizados, los ligandos de reacción de acoplamiento de Ullmann, como las fosfinas, se describen en la bibliografía y la mayoría de los ligandos son costosos, difíciles de preparar y sensibles a la humedad. Para este trabajo, se utilizan nanopartículas de cobre sintetizadas para el acoplamiento de Ullmann sin ligando de difeniléter. Los diferentes colorantes y compuestos orgánicos tóxicos y pesticidas presentes en los desechos industriales son muy dañinos para el medio ambiente y los organismos vivos. Las nanopartículas de cobre se utilizan para la degradación de diferentes tintes como el azul de metileno [73], la degradación de la atrazina [86] y la reducción del 4-nitrofenol [76].
Entre los agentes antimicrobianos, los compuestos de cobre se han utilizado comúnmente en la agricultura como herbicidas [105], algicidas [106], fungicidas [107] y plaguicidas, así como en la cría de animales como desinfectante [108] (que se muestra en la Tabla 4). Las nanopartículas de cobre biogénicas mostraron una poderosa actividad antibacteriana contra patógenos grampositivos y gramnegativos como Pseudomonas aeruginosa (MTCC 424), Micrococcus luteus (MTCC 1809), Enterobacter aerogenes (MTCC 2832) [57], Salmonella enterica (MTCC 1253), Rhizoctonia solani , Xanthomonas axonopodis pv. citri , Xanthomonas axonopodis pv. punicea [58], Escherichia coli (ATCC 14948) [62], Staphylococcus aureus (ATCC 25923), Bacillus subtilis (ATCC 6633), Pediococcus acidilactici [69] y Klebsiella pneumoniae (MTCC 4030). En la actividad antifúngica, las nanopartículas de cobre se utilizan contra Alterneria carthami , Colletotrichum gloeosporioides , Colletotrichum lindemuthianum , Drechslera sorghicola , Fusarium oxysporum f.sp. carthami , Rhizopus stolonifer , Fusarium oxysporum f.sp. ciceris , Macrophomina phaseolina , Fusarium oxysporum f.sp. udum , Rhizoctonia bataticola [58], Candida albicans , Curvularia , Aspergillus niger y Trichophyton simii [67]. En citotoxicidad, las nanopartículas de cobre se utilizan para un estudio en líneas celulares HeLa, A549, MCF7, MOLT4 y BHK21 (tumores cancerosos) [60, 104].
Mecanismo hipotético de actividad antimicrobiana
Se observó que las CuNP tienen una excelente actividad antimicrobiana y solo informes limitados presentaron el mecanismo de la actividad antibacteriana de las nanopartículas de cobre en la literatura, pero estos mecanismos eran hipotéticos. Se observó que las bacterias y las enzimas / proteínas se destruyeron debido a la interacción de CuNP con el grupo –SH (sulfhidrilo) [109, 110]. También se informó que la estructura helicoidal de las moléculas de ADN se ve alterada por la interacción de CuNPs [111]. La interacción de CuNP con la membrana celular de las bacterias disminuyó el potencial electroquímico transmembrana y, debido a la disminución del potencial electroquímico transmembrana, afectó la integridad de la membrana [112]. Se asumió que los NP metálicos liberan sus respectivos iones metálicos. Las nanopartículas de cobre y los iones de cobre se acumulan en la superficie celular de las bacterias y forman hoyos en la membrana, provocando la fuga del componente celular desde la célula y dentro de la célula, provocando estrés oxidativo que conduce a la muerte celular [112,113,114]. En la Fig. 6 se muestra un mecanismo hipotético de actividad antibacteriana que representa las posibilidades anteriores.
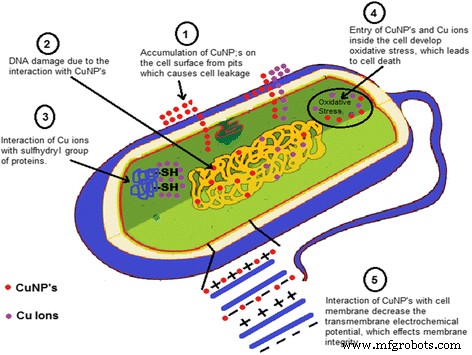
Mecanismo de actividad antibacteriana de nanopartículas de cobre
Actividad catalítica para la reducción de 4-nitrofenol
El 4-nitrofenol (4-NP), que generalmente se encuentra en las aguas residuales agrícolas y en los productos industriales, es peligroso y no es amigable con el medio ambiente. La hidrogenación o reducción de 4-NP, que se convierte en 4-aminofenol (4-AP), tiene lugar en presencia de CuNP. Los CuNP pueden catalizar la reacción para superar la barrera cinética al ayudar a la transferencia de electrones desde los iones de borohidrato donantes al aceptor 4-NP.
Se ha estudiado la actividad catalítica de los CuNP sintetizados en la reducción de 4-nitrofenol en medio acuoso a temperatura ambiente en presencia de una solución acuosa de borohidruro de sodio [56]. La reducción de 4-NP mediante el uso de CuNP es un proceso sencillo y respetuoso con el medio ambiente. La eficacia catalítica de CuNP para la reducción de 4-NP se examinó utilizando un espectrómetro UV-vis. Se observó que el pico de absorción máximo para 4-NP en medio acuoso estaba a 317 nm y el pico de adsorción se desplazó a 403 nm mediante la adición de borohidruro de sodio debido a la formación de iones 4-nitrofenolato. Un pico a 403 nm no se vio afectado incluso después de 2 días, lo que indicó que la reducción de 4-NP no puede tener lugar en ausencia de un catalizador. Después de agregar los CuNP, el pico de absorción de la solución se desplazó a 300 nm y el pico a 403 nm desapareció por completo, lo que indicó la reducción de 4-NP a 4-AP sin ningún producto secundario. En la figura 7 se muestra un mecanismo hipotético para la reducción de 4-NP. En el mecanismo, 4-NP y borohidruro de sodio están presentes en la solución en forma de iones. Los protones del ion borohidruro se adsorben en la superficie de las nanopartículas de cobre y BO 2 producido. Los iones 4-nitrofenolato también se adsorben en la superficie de los CuNP. Debido a la adsorción tanto de protones como del ión 4-nitrofenolato, los CuNP superan la barrera cinética de los reactivos y el ión 4-nitrofenolato se convierte en el ión 4-aminofenolato. Después de la conversión, tiene lugar la desorción del ion 4-aminofenolato y se convierte en 4-aminofenol.
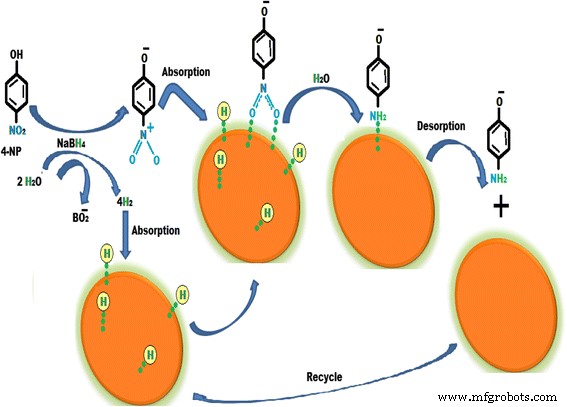
Mecanismo de reducción de 4-nitrofenol
Conclusiones
Este artículo ha revisado y resumido información reciente de métodos biológicos utilizados para la síntesis de nanopartículas de cobre (CuNP) utilizando diferentes plantas. La síntesis verde de CuNP se ha propuesto como una alternativa valiosa a los métodos físicos y químicos con baja citotoxicidad, perspectivas económicas, respetuosa con el medio ambiente, biocompatibilidad mejorada, viabilidad y alta actividad antioxidante y alta actividad antimicrobiana de CuNP. El mecanismo de biosíntesis de las NP aún se desconoce, y es necesario realizar más investigaciones sobre el mecanismo de formación de nanopartículas y la comprensión del papel de los fitoquímicos en la formación de las NP. Esta revisión proporciona datos de plantas utilizadas en la síntesis de nanopartículas de cobre, el procedimiento de síntesis y los parámetros de reacción que afectan las propiedades de los CuNP sintetizados. Un análisis de cribado fitoquímico es un análisis químico que se utiliza para identificar los fitoquímicos como la detección de carbohidratos, taninos, saponinas, flavonoides, alcaloides, antraquinonas y antocianósidos en diferentes plantas. En este artículo se describe el mecanismo de reducción de iones de cobre por quercetina y estabilización de nanopartículas de cobre por santina. Las técnicas de caracterización utilizadas en la literatura para nanopartículas de cobre son UV-vis, FTIR, XRD, SEM, FESEM, TEM, PSA, MZS, EDX, NTA, SAXS, XRR, XRF, XPS, BET, SAED y AFM. Las nanopartículas de cobre presentan actividad catalítica, actividad antibacteriana, citotoxicidad o actividad anticancerígena, actividad antioxidante y actividad antifúngica en diferentes aplicaciones. En este artículo se muestran los mecanismos hipotéticos de la actividad antimicrobiana y la reducción del 4-nitrofenol con diagramas.
Los CuNP con diferentes propiedades estructurales y efectos biológicos efectivos se pueden fabricar utilizando nuevos protocolos ecológicos en los próximos días. El control sobre el tamaño de las partículas y, a su vez, las propiedades dependientes del tamaño de los CuNP abrirán las nuevas puertas de sus aplicaciones. Este estudio proporciona una descripción general de la síntesis de CuNP mediante el uso de extractos de plantas, extractos microbianos y biomoléculas naturales. Aunque todos estos protocolos verdes para la síntesis de CuNP tienen sus propias ventajas y limitaciones, el uso de extracto vegetal como reductor es más beneficioso en comparación con el uso de extracto microbiano debido a la rápida tasa de producción de nanopartículas con el ex reductor verde.
Nanomateriales
- Síntesis biogénica, caracterización y evaluación del potencial antibacteriano de nanopartículas de óxido de cobre contra Escherichia coli
- Síntesis fácil y propiedades ópticas de nanocristales y nanovarillas de selenio pequeños
- Preparación y actividad de hidrogenación catalítica mejorada de nanopartículas de Sb / Palygorskita (PAL)
- Síntesis verde en un recipiente de microesferas de SnO2 decoradas con Ag:un catalizador eficiente y reutilizable para la reducción de 4-nitrofenol
- Síntesis fácil de compuesto de CuSCN coloreado y conductor recubierto con nanopartículas de CuS
- Síntesis hidrotermal de nanopartículas de In2O3, gemelos híbridos, discos hexagonales, heteroestructuras de ZnO para mejorar las actividades fotocatalíticas y la estabilidad
- Método de postratamiento para la síntesis de nanopartículas de FePt-Fe3O4 binarias monodispersas
- Saponinas Platycodon de Platycodi Radix (Platycodon grandiflorum) para la síntesis verde de nanopartículas de oro y plata
- Síntesis verde de nanopartículas de metal y óxido de metal y su efecto sobre el alga unicelular Chlamydomonas reinhardtii
- Síntesis fácil de nanopartículas de iridio sin ligando y su biocompatibilidad in vitro
- Síntesis en un solo recipiente de nanopartículas de núcleo-capa de CoFe2O4 @ Ag monodispersas y su caracterización



