Síntesis en un solo recipiente de nanopartículas de núcleo-capa de CoFe2O4 @ Ag monodispersas y su caracterización
Resumen
En los últimos años, se esperan nanopartículas magnéticas monodispersas con una estructura de núcleo / capa para sus amplias aplicaciones, incluido el fluido magnético, los catalizadores recuperables y el análisis biológico. Sin embargo, su método de síntesis necesita numerosos procesos, como la sustitución de disolventes, el intercambio de agentes protectores y la centrifugación. Un método simple y rápido para la síntesis de nanopartículas núcleo-capa monodispersas permite acelerar sus aplicaciones posteriores. Este documento describe una síntesis de núcleo simple y rápida en un solo recipiente (CoFe 2 O 4 ) nanopartículas de caparazón (Ag) con alta monodispersidad. Las nanopartículas sintetizadas mostraron absorción de luz plasmónica debido a la capa de Ag. Además, la propiedad magnética de las nanopartículas tuvo un comportamiento magnético suave a temperatura ambiente y un comportamiento magnético duro a 5 K. Además, las nanopartículas mostraron una alta monodispersidad con un índice de polidispersidad (PDI) bajo de 0.083 en hexano.
Antecedentes
Durante la última década, las nanopartículas magnéticas con una estructura de núcleo / capa han ganado mucha atención en una amplia gama de campos, desde la ingeniería hasta las ciencias médicas debido a las aplicaciones de los fluidos magnéticos [1, 2], la separación magnética [1,2, 3], catalizadores recuperables [1, 2, 4, 5, 6, 7], sistema de administración de fármacos [1, 8, 9, 10] y agentes de contraste mejorados para imágenes por resonancia magnética (IRM) [7, 9, 10, 11].
Entre las nanopartículas magnéticas, una nanopartícula de ferrita de espinela se ha empleado con frecuencia como núcleo magnético debido a sus excelentes propiedades magnéticas y eléctricas [12]. En particular, la ferrita de cobalto (CoFe 2 O 4 ) las nanopartículas tienen un gran campo coercitivo máximo ( H c ), incluso con un tamaño pequeño, así como una notable estabilidad química y una dureza mecánica [13,14,15,16,17]. Aunque se han desarrollado muchos métodos químicos diferentes para fabricar nanopartículas de CoFe2O4, el método de descomposición térmica se ha empleado recientemente como uno de los procedimientos más prometedores para obtener nanopartículas altamente controladas estructural y morfológicamente con una alta cristalinidad [13, 17, 18].
Las nanopartículas magnéticas con una estructura de núcleo / capa han atraído una gran atención debido a su multifuncionalidad, incluidas las propiedades ópticas, electrónicas y magnéticas [6, 8, 10, 19]. En particular, las nanopartículas magnéticas recubiertas de capa de Au se han estudiado ampliamente para proporcionar no solo las propiedades del plasmón superficial, sino también una superficie reactiva para una fuerte unión a compuestos orgánicos que contienen grupos tiol [3, 20]. Por lo general, un enfoque de proceso combinado de descomposición térmica de dos pasos puede sintetizar continuamente desde núcleos hasta capas, lo que da como resultado la formación de nanopartículas magnéticas recubiertas de Au con una alta monodispersidad [20]. Por otro lado, las nanopartículas magnéticas recubiertas con caparazón de Ag no han sido sintetizadas por este enfoque a pesar de sus excelentes propiedades plasmónicas, un coeficiente de extinción más alto, una banda de extinción más aguda, un efecto de dispersión de luz hasta la extinción más alto y fuertes campos electromagnéticos locales. de proyectiles Ag.
En este estudio, logramos sintetizar CoFe 2 recubierto de capa de Ag O 4 nanopartículas por un método simple y rápido de un solo recipiente que involucra dos procesos de descomposición térmica. Se confirmó que nuestras nanopartículas sintetizadas formaban una estructura núcleo-capa precisa, en comparación con las sintetizadas en un artículo anterior [21, 22]. Además, demostramos que el CoFe 2 O 4 @Ag mostró que la resonancia de plasmón de superficie localizada (LSPR) se originó a partir de los caparazones de Ag. En la investigación de la propiedad magnética, esta nanopartícula de núcleo-capa reveló un comportamiento magnético suave con H c de 70 Oe a 300 ky comportamiento magnético duro con 11 k Oe a 5 K.
Método / Experimental
Material
Fe (acac) 3 y Co (acac) 2 fueron adquiridos de Tokyo Chemical Industry. El éter difenílico, la oleilamina (OAm) y el acetato de plata (I) se adquirieron de Wako. El ácido oleico (OA) se adquirió de Kanto Chemical.
Síntesis de CoFe2O4 @ Ag
El CoFe2O4 @ Ag se sintetizó mediante el método de alta descomposición térmica de dos pasos (esquema 1). Fe (acac) 3 (0,353 g, 1 mmol), Co (acac) 2 (0,129 g, 0,5 mmol) y OA (3,39 g, 12 mmol) se disolvieron en 30 ml de difenil éter, que se pretrató calentando a 180ºC durante 30 min. Se calentó una mezcla a 180 ° C durante 16 h con agitación vigorosa. El color de la solución cambió gradualmente de rojo oscuro a negro fino. Después de enfriar a temperatura ambiente, se añadió a la mezcla una mezcla de OA (1,48 g, 5,2 mmol), OAm (8,13 g, 30,4 mmol) y acetato de plata (0,61 g, 3,6 mmol) disuelto en 100 ml de difenil éter. seguido de calentamiento a 180 ° C durante 1,5 h. El color de la mezcla se volvió más púrpura oscuro metálico durante el calentamiento. Después de enfriar, se agregaron 400 mL de metanol como un pobre solvente a la solución de la mezcla, seguido de centrifugación (5000 rpm, 5 min) y la redispersión en 60 mL de hexano. Aunque las nanopartículas dispersas en la solución podrían separarse magnéticamente, lleva tiempo recuperarse. El proceso de centrifugación se repitió varias veces para eliminar los precursores que no reaccionaron. Finalmente, centrifugando la solución coloidal de hexano (14.000 rpm, 20 min), se eliminaron los precipitados resultantes. El peso neto de las nanopartículas por este método es de aproximadamente 60 mg como 1 mg / ml de la solución coloidal de hexano. El CoFe 2 O 4 Las nanopartículas como referencia se prepararon realizando solo el paso 1 en el Esquema 1.
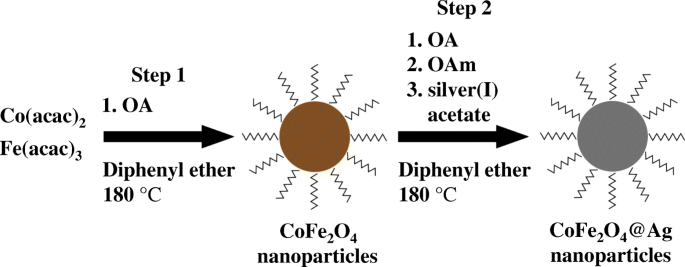
Procedimiento para sintetizar CoFe 2 O 4 @Ag nanopartículas
Caracterización y cálculo
La morfología de las nanopartículas se observó mediante microscopía electrónica de transmisión de emisión de campo (TEM) (Hitachi, Ltd., FE 2000). Las estructuras cristalinas se midieron con difracción de rayos X (XRD) (PANalytical, X’Pert PRO MPD) en el rango de 2 θ =20 ° a 80 ° utilizando el rayo α de CuK. La composición de elementos de las nanopartículas se analizó mediante espectroscopia de fotoelectrones de rayos X (XPS) (KARATOS ESCA 3400). La operación de grabado se realizó con pistola de iones Ar. Las medidas de magnetización se realizaron mediante un dispositivo superconductor de interferencia cuántica (SQUID) (Cryogenic, S700X-R). Las propiedades ópticas se midieron en un espectrofotómetro UV-visible (Jasco, V-670). La dispersión de luz dinámica (DLS) (Malvern, zetasizer-nano-zs) se midió con una línea láser de 633 nm. Para las propiedades ópticas de nuestras nanopartículas núcleo-capa sintetizadas, los datos experimentales están respaldados por cálculos de dispersión de Mie que fueron llevados a cabo por la solución de Bohren y Huffman [23] usando el código MATLAB escrito por Mätzler [24]. Las funciones dieléctricas para el Ag se tomaron de la Referencia [25].
Resultados y discusión
La Figura 1 muestra las imágenes TEM de CoFe 2 O 4 nanopartículas y CoFe 2 O 4 @Ag nanopartículas núcleo-caparazón. Como se muestra en los recuadros de la Fig. 1, las distribuciones de tamaño de ambas nanopartículas son estrechas. Los tamaños medios (media ± SD) de ellos son 3,5 ± 0,76 y 5,5 ± 0,77 nm, respectivamente. A partir de estos resultados, se estimó que el espesor de la capa de Ag era de aprox. 1 nm. Agregación de CoFe 2 O 4 se produjeron partículas pero no para CoFe 2 O 4 @Ag nanopartículas. Esto posiblemente se deba a una mayor energía superficial de las nanopartículas de CoFe2O4 que la de CoFe 2 O 4 @Ag nanopartículas debido a una mayor proporción de superficie a volumen de CoFe 2 O 4 nanopartículas [26]. Además, CoFe 2 residual O 4 No se pudieron observar nanopartículas (núcleos) en la muestra de CoFe 2 O 4 @Ag. Este resultado sugiere que casi todos los núcleos están recubiertos uniformemente con el caparazón de plata Ag.
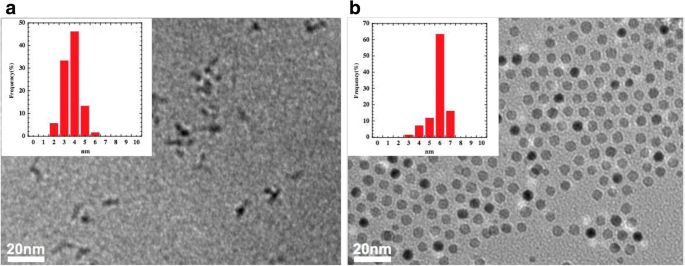
Imágenes TEM e histogramas de tamaño de partículas para nanopartículas de a CoFe 2 O 4 y b CoFe 2 O 4 @Ag
La Figura 2 presenta los patrones XRD para CoFe 2 O 4 y el CoFe 2 O 4 @Ag nanopartículas. Los picos de difracción de CoFe 2 O 4 nanopartículas a 2 θ =30,50 °, 35,75 °, 43,50 °, 53,8 °, 57,5 °, 63,0 ° y 74,4 ° muestran la formación de una sola fase cristalográfica, que puede indexarse como la estructura cúbica de los óxidos de espinela [17]. Por otro lado, los picos de difracción de CoFe 2 O 4 @Ag a las 2 θ =38,42 °, 44,50 °, 64,91 °, 77,75 ° y 81,83 ° corresponden a los de la fase cúbica estándar centrada en las caras (fcc) de Ag [10]. La intensidad de los picos de difracción de CoFe 2 O 4 son relativamente débiles y su pico principal se superpone con Ag; por tanto, todos emergen en los de Ag. El tamaño del cristalito se calculó a partir del ancho completo a la mitad del máximo (FWHM) del pico de difracción de mayor intensidad, que se basa en la ecuación de Debye-Scherrer,
$$ t =0.9l / b \ \ cos \ y $$ (1)donde t es el tamaño del cristalito, l es la longitud de onda de la radiación Cu-Ka, b es el FWHM, y y es el ángulo de difracción del pico más fuerte. Los tamaños de cristal evaluados a partir de los patrones de difracción fueron 7,1 y 3,6 nm para CoFe 2 O 4 nanopartículas y CoFe 2 O 4 @Ag nanopartículas, respectivamente. El tamaño del cristal de CoFe 2 O 4 Se observó que las nanopartículas eran más grandes que el tamaño de TEM debido al residuo de CoFe 2 O 4 nanopartículas fuera de distribución de tamaño, que no pudieron eliminarse mediante centrifugación en hexano. Por otro lado, el tamaño del cristal de XRD mostró un acuerdo en las nanopartículas de CoFe2O4 @ Ag considerando que el tamaño del cristal de la capa de Ag tiene que ser más pequeño que el tamaño de TEM. El tamaño del coloide después de la reacción de recubrimiento de plata permite seleccionar mediante centrifugación debido a su gran peso en hexano.
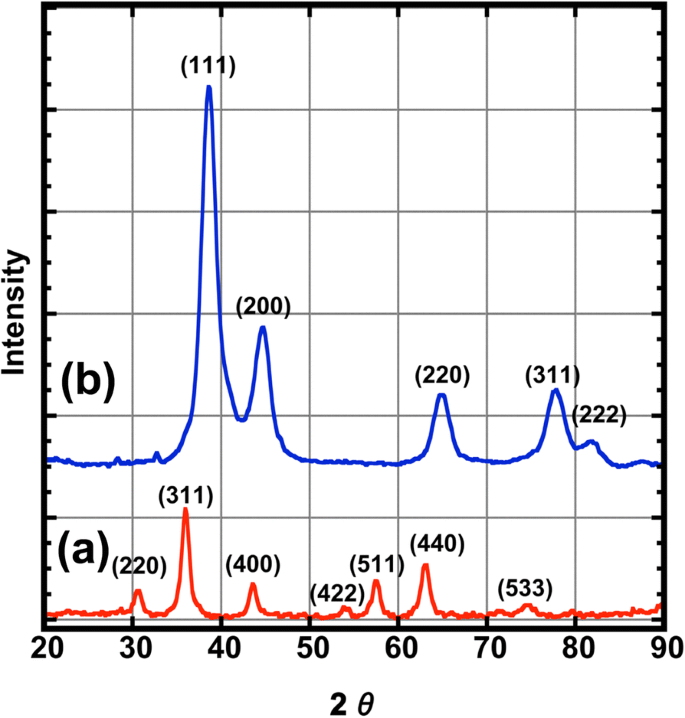
Patrón XRD de nanopartículas, ( a ) CoFe 2 O 4 (línea roja) y ( b ) CoFe 2 O 4 @Ag (línea azul)
Para evaluar la composición interna de las nanopartículas obtenidas con una estructura de núcleo-capa, se grabaron las superficies de las nanopartículas utilizando una pistola de iones de Ar en la cámara [27]. Según los estudios anteriores, cuando las partículas tenían una estructura núcleo-capa precisa, la intensidad máxima del elemento contenido en el núcleo debería incrementarse a medida que avanza el grabado. Como se muestra en la Fig. 3a – d, para determinar la composición de la superficie de CoFe 2 O 4 @Ag nanopartículas, medimos los espectros XPS antes del grabado con iones de Ar. En las superficies iniciales, los peek C (1 s) se observaron fácilmente en las nanopartículas debido a la presencia del agente protector en la superficie de las nanopartículas (Fig. 3a). Se descompuso el espectro de C (1 s) y se observó un pico derivado de C-O-C, que se deriva del ácido oleico modificado en la superficie. Si bien se observaron los picos de Ag (3d), no se pudieron observar los de Fe (2p) y Co (2p), lo que indica que el núcleo estaba completamente cubierto con las capas de Ag (Fig. 3b – d). Por otro lado, los picos de Fe (2p) y Co (2p) se observaron en las nanopartículas después de la operación de grabado con ion argón (Fig. 3f, g). Los picos de Fe (2p) y Co (2p) se descomponen y se pueden asignar a Fe 2+ , Fe 3+ , Co 2+ y Co 3+ , respectivamente. La formación de ambos tipos de portadores de carga resulta de la pérdida de oxígeno durante el proceso de reacción a alta temperatura [28, 29]. Para la compensación de carga, una parte de Fe3 + se convierte en Fe2 + y una parte de Co2 + se convierte en Co3 +. Además, cada uno de los picos de Ag (3d) después del grabado se puede descomponer en dos picos (Fig. 3h), debido a la diferencia en el estado electrónico entre las superficies de las nanopartículas y el interior de las carcasas. Estos resultados indican que se forma la estructura precisa de núcleo y capa.
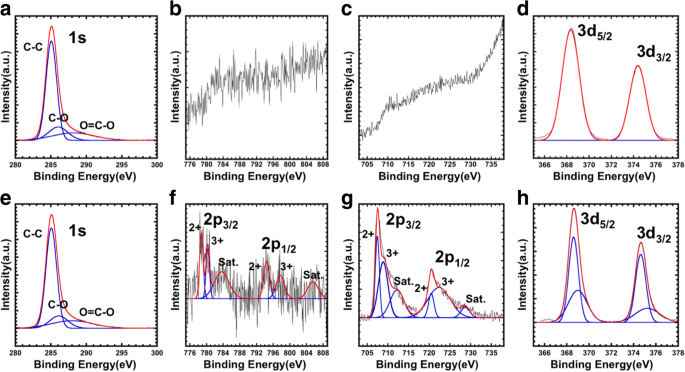
Espectros XPS de CoFe 2 O 4 @Ag por grabado con iones de argón antes ( a - d ) y después ( e - h ). un , e C 1 s. b , f Co 2p. c , g Fe 2p. d , h Ag 3d
Los bucles de histéresis magnética de las películas compuestas por CoFe 2 O 4 y el CoFe 2 O 4 Las nanopartículas de @Ag se midieron a 300 y 5 K, como se muestra en la Fig. 4. Estos bucles de histéresis se normalizaron como la susceptibilidad magnética por unidad de peso de cobalto. Debido al análisis de la fase cristalográfica usando XRD (Fig.2), las densidades cristalinas de CoFe 2 O 4 y CoFe 2 O 4 Se estimó que las nanopartículas de @Ag eran de 5,3 y 10,5 g / cm 3 , respectivamente. Además, los volúmenes de CoFe 2 O 4 y CoFe 2 O 4 Las nanopartículas de @Ag se calcularon utilizando los resultados de la observación TEM (Fig. 1). CoFe 2 O 4 Las nanopartículas mostraron un comportamiento superparamagnético a temperatura ambiente (Fig. 4a). Como lo mencionan López-Ortega et al. [17], el CoFe 2 O 4 las nanopartículas con un tamaño inferior a 20 nm mostraron el comportamiento superparamagnético a temperatura ambiente. Las propiedades magnéticas de cada muestra a las dos temperaturas se resumen en la Tabla 1. Saturación magnética ( M s ) del CoFe 2 O 4 nanopartículas era 11 (emu / g CoFe 2 O 4 ), que es inferior a los resultados anteriores [17, 30, 31]. Esto posiblemente se deba al tamaño de partícula más pequeño obtenido en este estudio. Por otro lado, el M s del CoFe 2 O 4 @Ag fue incluso menor con un valor de 3.3 (emu / g, CoFe 2 O 4 ). Como se menciona en la literatura anterior para Fe 3 O 4 @Ag nanopartículas [8,9,10, 32,33,34], el M s de CoFe 2 O 4 @Ag disminuye posiblemente debido a la contribución diamagnética de la capa de Ag. Además, CoFe 2 O 4 @Ag mostró 77 Oe, que es alto H c valor a 300 k. El H c del CoFe 2 O 4 @Ag también es diferente al de CoFe 2 O 4 bajo la temperatura baja (Fig. 4b). Ambas nanopartículas exhibieron ferromagnetismo a 5 K a pesar de sus tamaños relativamente pequeños. Sobre la base de los datos de magnetización cercana a cero, el valor de H c aumentos para CoFe 2 O 4 @Ag nanopartículas (7 k Oe para CoFe 2 O 4 y 11 k Oe para CoFe 2 O 4 @Ag). Este interesante comportamiento también se ha observado en otras nanopartículas núcleo-capa como Fe @ Ag [10] y Fe 3 O 4 @Au nanopartículas [5]. Teniendo en cuenta estos hechos, el aumento de la H c del CoFe 2 O 4 Las nanopartículas de @Ag pueden derivarse de un acoplamiento menos eficaz del momento dipolar magnético [5, 20].
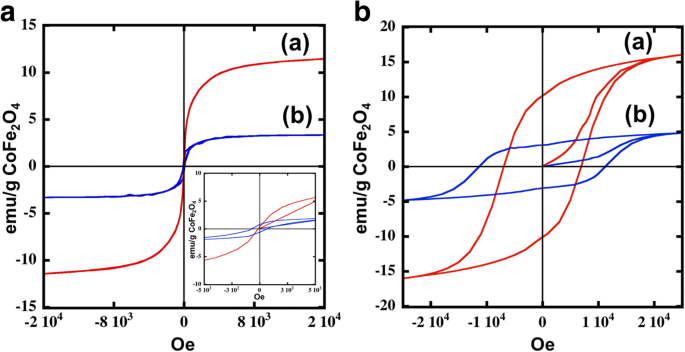
Bucles de histéresis para nanopartículas:( a ) y ( b ) son para CoFe 2 O 4 nanopartículas (línea roja) y CoFe 2 O 4 @Ag nanopartículas (línea azul), respectivamente, en a 300 K y b a 5 K
A continuación, propiedades ópticas del CoFe 2 O 4 Las nanopartículas se investigaron mediante mediciones espectrales UV-visibles. Se sabe que las nanopartículas de Ag muestran una extinción significativa de la luz en la región visible debido a la excitación de la resonancia de plasmón de superficie localizada (LSPR) por el acoplamiento de la luz irradiada con la oscilación coherente de los electrones de superficie dentro de las nanopartículas de Ag. Aunque el CoFe 2 O 4 Las nanopartículas no mostraron banda de extinción LSPR en la región visible (Fig.5), la solución coloidal de nuestro tipo de núcleo-capa CoFe 2 O 4 Las nanopartículas de @Ag mostraron un pico de extinción agudo a 416 nm. Esto se puede atribuir a la absorción de plasmón (modo dipolo) de la capa de Ag, que teóricamente está respaldada por la teoría de Mie (consulte el archivo adicional 1). Este interesante comportamiento se ha observado para nanopartículas de Fe @ Ag [10] y nanopartículas de Co @ Ag [7]. Además, las propiedades espectroscópicas del CoFe 2 O 4 Las nanopartículas de @Ag no se cambiaron durante 1 mes, lo que indica la estabilidad superior de las nanopartículas en el aire.
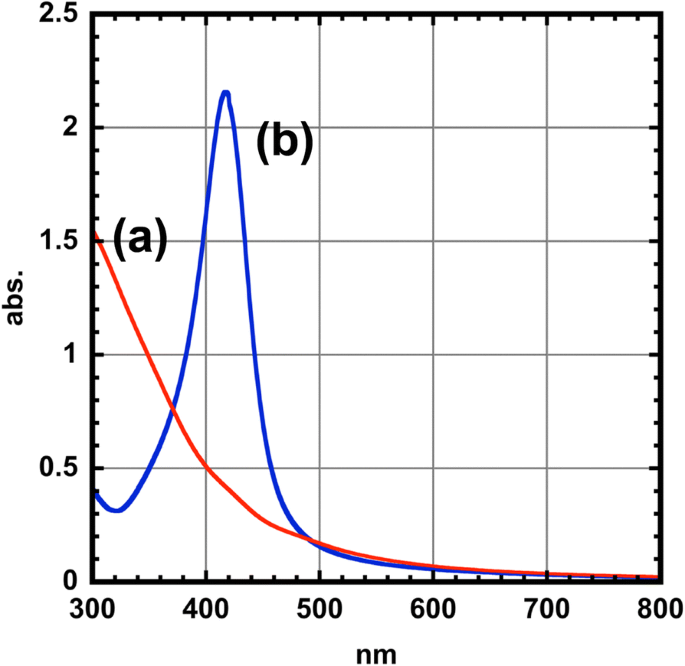
Espectros UV-vis para ( a ) CoFe 2 O 4 nanopartículas (línea roja) y ( b ) CoFe 2 O 4 @Ag nanopartículas (línea azul)
La estabilidad coloidal del CoFe 2 O 4 y el CoFe 2 O 4 Las nanopartículas de @Ag se evaluaron midiendo las distribuciones de tamaño de las nanopartículas en hexano usando DLS (Fig. 6). Los tamaños medios de CoFe 2 O 4 y CoFe 2 O 4 Se midió que las nanopartículas de @Ag eran 19,67 y 9,27 nm, respectivamente. Los tamaños de estas nanopartículas obtenidas de las mediciones de TEM, XRD y DLS se resumen en la Tabla 2. La principal diferencia en los tamaños medidos por estas dos técnicas se debe a la presencia de una capa de adsorción que consta de OA y OAm en la superficie del partículas [35]. Los compuestos orgánicos como OA y OAm no aparecieron en las imágenes TEM debido a la permeabilidad de los electrones (Fig. 1). Dado que las longitudes de cadena de OA y OAm son aproximadamente 2 nm [36, 37], el tamaño de CoFe 2 O 4 El @Ag estimado por el TEM es ligeramente (aproximadamente 4 nm) más grande que el del DLS. Por otro lado, es razonable que el tamaño de CoFe 2 O 4 por el DLS es mucho mayor que el estimado a partir de este supuesto. Estos resultados sugieren que las nanopartículas de CoFe2O4 están aglomeradas en hexano. Este factor incluye no solo el efecto de tamaño de las partículas descritas anteriormente, sino también la baja afinidad entre CoFe 2 O 4 superficies y agentes protectores. La tendencia a la aglomeración del CoFe 2 O 4 puede no solo debido al efecto de tamaño de las partículas descrito anteriormente, sino también debido a la baja afinidad entre el CoFe 2 O 4 superficies y agentes protectores. Precipitación de CoFe 2 O 4 Se observaron nanopartículas con mucha más frecuencia que CoFe 2 O 4 @Ag nanopartículas en proceso de redispersión aumentando el número de lavados con metanol. La alta monodispersidad de CoFe 2 O 4 @Ag está fuertemente respaldado por el bajo índice de polidispersidad (PDI) obtenido por las mediciones DLS [38]. Estos resultados indican que el recubrimiento con Ag agrega no solo una función óptica sino también la estabilidad en solución al CoFe 2 O 4 nanopartículas.
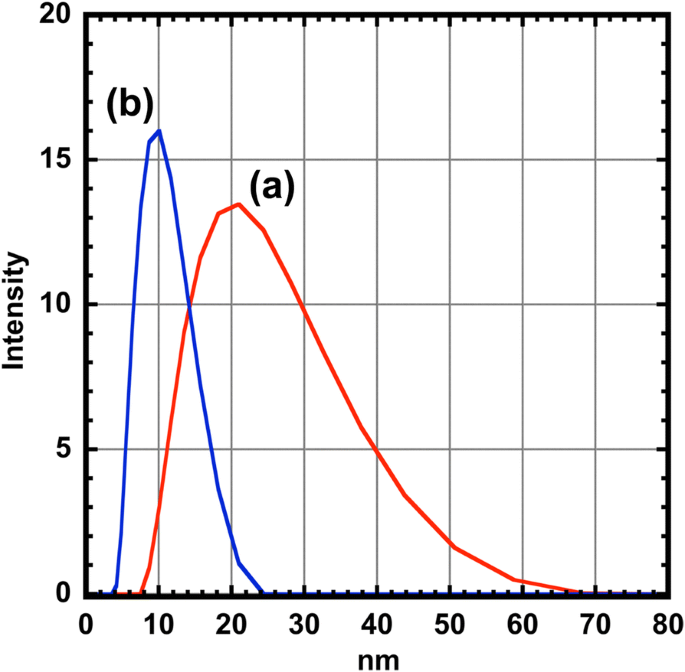
Distribución de tamaño ( a ) del CoFe 2 O 4 (línea roja) y ( b ) el CoFe 2 O 4 @Ag nanopartículas (línea azul) medidas por DLS
Conclusiones
El CoFe 2 O 4 Se descubrió que las nanopartículas de @Ag sintetizadas mediante un proceso de un solo recipiente simple y rápido se formaban al tener una estructura de núcleo-capa uniforme con una distribución de tamaño estrecha a partir de imágenes TEM (Fig. 6). Además, estas nanopartículas mostraron una multifuncionalidad consistente en la propiedad de extinción de la luz plasmónica y un comportamiento superparamagnético a temperatura ambiente. Además, las nanopartículas de núcleo-capa mostraban una H más alta c que CoFe 2 O 4 nanopartículas a 5 K y 300 k. Además, estas nanopartículas mantuvieron una alta monodispersidad en un disolvente orgánico. Las nanopartículas uniformes sintetizadas por el proceso simple tienen un gran potencial en varios campos debido a la multifuncionalidad y estabilidad.
Abreviaturas
- DLS:
-
Dispersión de luz dinámica
- fcc:
-
Cúbico centrado en la cara
- H c :
-
Campo coercitivo
- M s :
-
Saturación magnética
- OA:
-
Ácido oleico
- OAm:
-
Oleilamina
- PDI:
-
Índice de polidispersidad bajo
- SQUID:
-
Dispositivo superconductor de interferencia cuántica
- TEM:
-
Microscopía electrónica de transmisión por emisión de campo
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X
Nanomateriales
- Nanopartículas de oro multifuncionales para aplicaciones terapéuticas y diagnósticas mejoradas:una revisión
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- Síntesis biogénica, caracterización y evaluación del potencial antibacteriano de nanopartículas de óxido de cobre contra Escherichia coli
- Síntesis fácil y propiedades ópticas de nanocristales y nanovarillas de selenio pequeños
- Síntesis fácil de compuesto de CuSCN coloreado y conductor recubierto con nanopartículas de CuS
- El efecto del plasma de no equilibrio por contacto sobre las propiedades estructurales y magnéticas de Mn Х Fe3 - X О4 Espinelas
- Propiedades de síntesis y luminiscencia de nanopartículas de α-NaGdF4 / β-NaYF4:Yb, Er Core-Shell solubles en agua
- Método de postratamiento para la síntesis de nanopartículas de FePt-Fe3O4 binarias monodispersas
- Síntesis de puntos cuánticos de sulfuro de antimonio solubles en agua y sus propiedades fotoeléctricas
- Efecto del método de síntesis de nanopartículas de manganita La1 - xSr x MnO3 en sus propiedades
- Síntesis en un solo recipiente de nanoplacas de Cu2ZnSnSe4 y su actividad fotocatalítica impulsada por la luz visible



