El efecto del plasma de no equilibrio por contacto sobre las propiedades estructurales y magnéticas de Mn Х Fe3 - X О4 Espinelas
Resumen
Ferritas de manganeso de tamaño nanométrico Mn х Fe 3 - х О 4 ( х =0-1,3) se prepararon utilizando plasma de no equilibrio de contacto (CNP) en dos pH diferentes (11,5 y 12,5). Se investigó la influencia de las condiciones de síntesis (p. Ej., Relación de cationes y pH inicial) en la composición de la fase, el tamaño del cristalito y las propiedades magnéticas empleando difracción de rayos X (XRD), análisis térmico diferencial (DTA), infrarrojo por transformada de Fourier (FTIR), barrido microscopía electrónica (SEM), microscopía electrónica de transmisión (TEM) y técnicas de medición magnética. La formación de partículas de ferrita facetadas monodispersas en х =0-0,8 se mostró. Los espectros FTIR revelaron una reflexión en la región 1200-1700 cm −1 causado por la presencia de agua adsorbida en la superficie de Fe 3 - x Mn x O 4 microgránulos o incrustados en su red cristalina. La mayor sensibilidad de los espectros de reflexión a los cambios de composición tiene lugar dentro de 400-1200 cm −1 rango, típico de las vibraciones de estiramiento de Fe (Mn) –O (hasta 700 cm −1 ), Fe (Mn) –OH y Fe (Mn) –OH 2 enlaces (más de 700 cm −1 ). Los resultados de XRD mostraron que el Mn nanocristalino х Fe 3 - х О 4 (0 < x <1.0) tenían una estructura cristalina de espinela cúbica con un tamaño de cristalito promedio de 48-49 A. La disminución del tamaño cristalino con el x también se observó un aumento.
Antecedentes
La capacidad de las espinelas nanodispersivas con metales polivalentes para formar una serie de soluciones y compuestos sólidos ofrece posibilidades ilimitadas para controlar las propiedades tecnológicas de los compuestos de espinela. Durante mucho tiempo, muchos investigadores se ha prestado gran atención a las investigaciones de ferritas de manganeso (Fe 3 O 4 - Mn 3 O 4 sistema) debido a su amplia aplicación en la industria. Se utilizan ampliamente en hornos microondas y dispositivos de almacenamiento magnético, así como catalizadores altamente activos en la producción de hidrógeno a través de la deshidrogenación de metano en etileno o acetileno, adsorbentes [1,2,3,4,5,6].
La síntesis de espinela de ferrita de manganeso es tecnológicamente compleja. Actualmente, existen pocos métodos para la síntesis de partículas de ferrita de manganeso, tales como cerámica [7], coprecipitación [8,9,10,11,12], método hidrotermal [13], micela inversa [14, 15], sol- gel [16], método de combustión [17], mecanosíntesis [18,19,20], tecnologías de alta energía [21, 22] y dopaje mecánico [23, 24]. Los métodos de hidrofase permiten regular la composición, cristalinidad y morfología de las partículas.
Dichos métodos han sido estudiados por muchos investigadores y se aplican con éxito para la síntesis de ferritas [9, 25, 26] con un tamaño de partícula de 30–50 nm a 50–150 ° С, que es significativamente más bajo que para la tecnología cerámica. Los métodos de hidrofase, por regla general, incluyen varias etapas:la primera, deposición, la segunda, síntesis directa de ferrita, llevada a cabo debido a oxidación, envejecimiento, etc. Los métodos para el inicio de la segunda etapa principal de síntesis de ferrita mediante tratamiento por ultrasonidos, microondas Influencia, ultravioleta y diversas descargas [27,28,29] se han utilizado recientemente. Durante el tratamiento de soluciones con descarga de CNP, se produce un complejo complejo de reacciones químicas que involucran partículas de radicales y electrones libres. Los principales productos de tales interacciones son el oxígeno, el hidrógeno y el peróxido de hidrógeno. La actividad oxidativa de las soluciones "activadas" plasmoquímicamente se puede utilizar para la síntesis de compuestos de óxidos complejos.
El espectro de emisión [30,31,32] ha demostrado que las principales contribuciones al espectro de emisión del plasma de vapor de agua son el OH, el hidrógeno atómico y el radical oxígeno. En el caso del modo burbuja, cuando las serpentinas llenan toda la burbuja, se produce una emisión significativa del segundo sistema positivo de nitrógeno y del ion nitrógeno (primer sistema negativo). La descarga opera en dos modos diferentes. Para pequeñas conductividades del líquido, la descarga es una descarga directa de serpentina de líquido (modo líquido). Este modo es similar a las típicas descargas de corona en el agua. Para conductividades superiores a los 45 μS cm −1 se forma una gran burbuja de vapor. En el modo burbuja, las serpentinas están ubicadas en la interfaz burbuja-líquido. La eficiencia de formación de peróxido de hidrógeno depende de la potencia con un máximo para las potencias intermedias. La eficiencia de formación de peróxido de hidrógeno es significativamente menor en el modo de burbuja que en el modo líquido. En el trabajo [33] se han estimado los parámetros cinéticos de los electrones para la descarga de la barrera dieléctrica con un electrodo líquido a presión atmosférica. Así, podemos suponer que el CNP poseerá actividad química con respecto a su aplicación en la realización de los diferentes procesos oxidativo-reductores.
Nuestros estudios preliminares de tratamiento con plasma de soluciones han demostrado que la composición de la solución oxidante sintetizada depende de una amplia gama de factores [29]. El uso de CNP garantiza un alto grado de homogeneidad en la distribución de los componentes tanto en la solución inicial como en el producto formado durante la oxidación, lo que estimula la interacción efectiva entre ellos con formación de ferritas con estructura y composición homogénea.
El objetivo del trabajo es estudiar la posibilidad de obtener Mn de tamaño nanométrico Х Fe 3 - Х О 4 espinela a partir de soluciones acuosas utilizando plasma de no equilibrio de contacto. Dado que las ferritas son soluciones sólidas, es importante establecer el grado de homogeneidad estructural y de concentración en las condiciones de síntesis seleccionadas. El método experimental consistió en la comparación de ferrospinel obtenido a partir de sulfatos de manganeso y hierro en diferentes proporciones de cationes.
Dicha investigación comparativa de las muestras permite establecer la influencia de la composición química de la solución inicial y las condiciones de síntesis sobre el estado de la fase estructural de los compuestos preparados mediante tratamiento con CNP.
Métodos
Para la síntesis de ferrita de manganeso, los autores han utilizado soluciones acuosas de FeSO 4 · 7H 2 O, MnSO 4 · 5H 2 O, y se utilizó una solución acuosa de NaOH como precipitante. Usamos soluciones de 0,5 M de sales de hierro y manganeso. Todos los productos químicos y disolventes empleados para la síntesis eran de calidad analítica y se utilizaron tal como se recibieron sin purificación adicional. Se utilizó agua desionizada como disolvente en todo el procedimiento.
Los estudios preliminares [25] mostraron que a pH <11 se formaban óxidos y oxihidróxidos no magnéticos, por lo que se prepararon dos conjuntos de muestras. El primer conjunto en рН inicial =11,5 y el segundo en 12,5. Los compuestos coprecipitados se prepararon vertiendo con agitación continua la correspondiente mezcla de soluciones de sulfato con la proporción de cationes necesaria. El tratamiento adicional se llevó a cabo utilizando CNP.
El tratamiento se realizó en un reactor cilíndrico con un diámetro interior de 45 mm y una altura de 85 mm. La mezcla de reacción se enfrió mediante la circulación continua de agua fría en la camisa exterior. Uno de los electrodos de acero inoxidable (diámetro 4 mm) se ubicó en la parte inferior del reactor, y el otro (diámetro 2,4 mm) se ubicó 10 mm por encima de la superficie de la solución. El voltaje inicial se entregó al transformador elevador. La corriente alterna de la bobina secundaria se entregó al puente rectificador y luego, ahora voltaje pulsante, se entregó a través de una resistencia de lastre a los electrodos del reactor. La unidad de encendido se conectó adicionalmente al ánodo. Esta unidad formó pulsos con amplitud de hasta 15 kV con un ancho de 1,5 ms. Los pulsos estaban estrictamente sincronizados con la fase del voltaje pulsante. En el instante en que se formó el pulso de encendido, hubo una ruptura entre los electrodos del reactor en el espacio de vacío creado por la rarefacción a 0.06-0.08 MPa. La resistencia cayó bruscamente y una corriente de ánodo comenzó a fluir creando así una descarga. El voltaje de combustión de descarga permaneció casi sin cambios en 750-900 V. La corriente en el espacio de descarga fue determinada por la resistencia del plasma y el voltaje aplicado al sistema formado por la descarga de plasma y el controlador de balasto. El voltaje se controlaba mediante el principio del método de fase, es decir, el voltaje de ánodo promedio aplicado al reactor dependía de la fase del voltaje pulsante en el ánodo y del instante en el que se entregó un pulso de encendido.
El plasma apareció en el instante de encendido y se extinguió cuando terminaron las pulsaciones de voltaje del ánodo (Fig. 1). La frecuencia de repetición del proceso fue de 100 Hz. La corriente de descarga se controló cambiando el instante de encendido en relación con la fase de las pulsaciones de voltaje del ánodo con un dispositivo de sincronización. La duración del tratamiento con plasma varió de 10 a 40 min. Todos los precipitados se lavaron hasta que reaccionó negativamente en el ion sulfato. Los precipitados lavados y filtrados se secaron a 150ºC. Propiedades magnéticas relativas (de magnetización de saturación I S (emu 2 / g), fuerza coercitiva Нс (Oe)) fueron evaluados por magnetómetro [29].

El pilar de plasma de no equilibrio de contacto entre el electrodo en la fase gaseosa y la superficie del líquido
La concentración de Mn 2+ en las muestras obtenidas se determinó complexométricamente. La concentración de hierro se determinó mediante métodos de permanganato y bicromato. Para controlar el proceso de reacción, el reactor se equipó con un sistema de electrodos. El [Fe 2+ ] / [Mn 2+ ] relación en Mn х Fe 3 - х О 4 El compuesto se calculó de acuerdo con la fórmula:
$$ \ frac {C _ {\ mathrm {Mn}}} {C _ {\ mathrm {Fe}}} =\ frac {x} {3-x} $$y los valores eran iguales a х =0; Se eligieron 0,2, 0,4, 0,6, 0,8, 0,9, 1, 1,1, 1,2 y 1,3. Espectros de reflexión infrarroja por transformada de Fourier de ferritas de manganeso Mn x Fe 3 - x O 4 ( x =0.0, 0.2, 0.4, 0.6, 0.8, 0.9, 1.0, 1.1, 1.2, 1.3) se midieron dentro de una distancia de 400 a 4000 cm −1 rango mediante el empleo de un espectrómetro de infrarrojos por transformada de Fourier (FTIR) Nicolet iS10. Para estudiar las transformaciones que ocurren al calentar los polvos obtenidos, utilizamos análisis térmico diferencial (DTA) y análisis termogravimétrico diferencial (DTG). Las curvas de DTA, TG de pérdida de masa y DTG de tasa de pérdida de masa se registraron en el Derivatograph Q-1500D (F. Paulik, J. Paulik y L. Erdey). La temperatura se varió en un rango de 20 a 1000 ° C a una velocidad de calentamiento de 10 ° / min. γ-Al 2 O 3 se utilizó como referencia. La masa de cada muestra fue de 200 mg. La morfología de los polvos de ferrita y el tamaño de partícula se estudiaron mediante microscopía electrónica de barrido. La composición de fase (XRD) y la estructura de las muestras de ferrita se estudiaron utilizando un difractómetro de rayos X DRON-2 en C®-K monocromatizado α radiación. El tamaño de cristalito y el grado de microesfuerzos se calcularon usando el método de aproximación. El tamaño y la forma de las partículas se determinaron utilizando un microscopio electrónico “Jem 1010” (JEOL) a una tensión de valor de trabajo de 200 kV. Se realizó microscopía electrónica de barrido con microanálisis de rayos X utilizando REMMA-102 (SELMI, Ucrania).
Resultados y discusión
Las propiedades de los materiales magnéticos a base de ferritas de manganeso dependen de su estado estructural y de fase. La síntesis de tales ferritas requiere la preparación de un producto monofásico con estructura de espinela que no tiene óxido de hierro residual u otras fases, que son productos intermedios de formación de ferrita a partir de óxidos. A la par con la composición de las fases, las propiedades magnéticas están significativamente influenciadas por la oxidación de los cationes de hierro y manganeso y el carácter de su ubicación en el sitio de la red cristalina de espinela. Se sabe que los cationes divalentes (Zn 2+ , Mn 2+ ) se encuentran principalmente en posiciones tetraédricas y trivalentes (Fe 3+ ) —En posiciones octaédricas de la red cristalina de espinela. Según la teoría de la relajación de Néel, tal disposición proporciona el valor máximo de magnetización del material. Durante la preparación de ferritas, oxidación de Mn 2+ a Mn 3+ es posible, que puede ir acompañado de una reducción de Fe 3+ a Fe 2+ y reordenamiento de cationes en subredes, con transferencia parcial de Fe 2+ en tetraédrico y Mn 3+ —En los nodos octaédricos de la red cristalina, que impacta negativamente en las propiedades magnéticas de las ferritas. Oxidación de Mn 2+ ocurre a la tasa más alta a 900–1000 ° С, y la condición óptima para la sinterización de ferritas de manganeso para tecnología cerámica:1000–1200 ° С. Los datos disponibles en diversas fuentes bibliográficas sobre la discusión de la estructura magnética y las propiedades de las ferritas de manganeso son contradictorios, lo que probablemente esté relacionado con la variación en la disposición de los iones de hierro y manganeso y su polivalencia. Los datos de la dependencia del parámetro de celosía del valor de х en el caso de varias tecnologías, es posible asumir el carácter de disposición catiónica en la red.
Los resultados de la evaluación de las muestras preparadas se pueden formular de la siguiente manera:todas las muestras incluyen agua unida químicamente en varias cantidades. En ambos conjuntos, el contenido de agua más alto se encuentra en muestras con х =0,4, 1,1… 1,3. El primer conjunto mostró propiedades magnéticas débiles (Figuras 2 y 3), por lo que no se consideró en detalle.
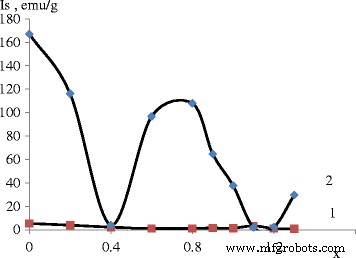
Dependencia de la magnetización de saturación de la relación molar de cationes a diferentes рН:1 — рН =11,5 y 2 — рН =12,5
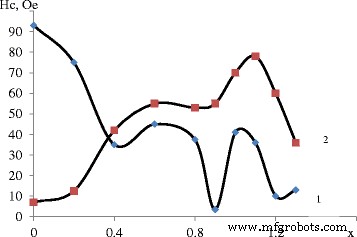
Dependencia de la fuerza coercitiva de la ración molar catiónica a diferentes рН:1 — рН =11,5 y 2 — рН =12,5
Como puede verse en la Fig. 1, existen algunas diferencias en la magnetización de saturación de ambos conjuntos. El valor más alto para el conjunto 1 corresponde a la relación 1,1 Mn 1.0 Fe 0.9 Mn 0.1 О 4 . El valor más alto se alcanza con рН =12,5 y una proporción de х =0.8 (Mn 0.8 Fe 0.2 Fe 2 О 4 ). Esta relación es diferente de la ferrita de manganeso estequiométrica.
Al evaluar la magnetización de saturación, se puede decir que los números de muestra. 1, 2, 3 y 8 tienen valores más bajos debido a su estructura amorfa y presencia de fases no magnéticas.
La Figura 4 muestra los patrones XRD de las muestras del segundo conjunto. Los patrones de XRD se pueden dividir en dos categorías:las primeras muestras 6–10 que tienen una estructura cristalina monofásica correspondiente a la ferrita en fase de espinela (JCPDS 10-0467). Se pueden observar líneas relativamente nítidas e intensas de ferritas en fase espinela en los patrones XRD de las muestras. Las líneas relacionadas con las fases de óxido de Fe 2 O 3 y MnO x están ausentes en los patrones XRD (Fig. 4).
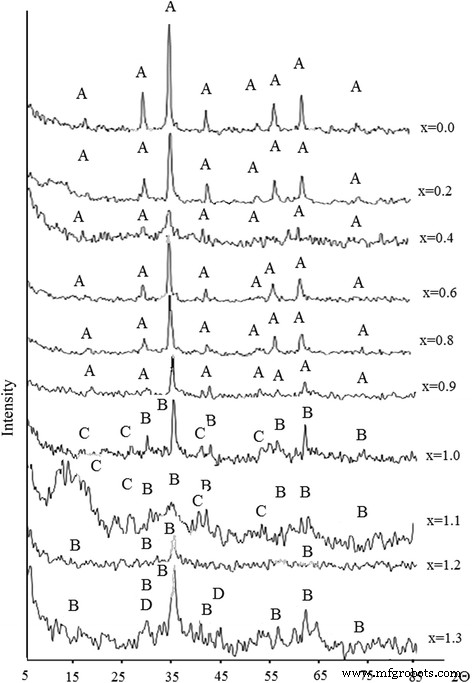
Patrones XRD de ferrita obtenidos en diferentes proporciones de componentes (Tabla 1):A — Fe 3 O 4 , B — MnFe 2 O 4 , C — Mn 3 O 4 y D — β-MnO 2
El segundo conjunto tiene menos cristalino con pocas fases presentes. En los patrones XRD de las muestras, preparadas con mayor contenido de manganeso, las líneas se ensanchan ligeramente, lo que puede indicar cambios en su estructura en comparación con la muestra estequiométrica. La presencia de otras fases en caso de mayor contenido de manganeso se encontró mediante el método XRD. Los picos anchos se pueden observar en los patrones de XRD, que se pueden indexar como (311) de la fase de espinela de ferrita (JCPDS 74-2403). En la región de ángulos correspondientes a las líneas de mayor intensidad para Fe 3 O 4 y Mn 3 O 4 , se observa un halo de baja intensidad, que puede indicar la presencia de estos óxidos en las muestras. Existe una clara correlación entre las características magnéticas y el grado de cristalinidad y homogeneidad del producto.
Teniendo en cuenta que Mn 2+ cationes son los más grandes de todos, se podría suponer que como el valor de x aumenta, es posible aumentar el parámetro de celosía. El análisis de los patrones de XRD (Fig.5) muestra que el parámetro de la red cristalina а =8.4196 А (para ferrita de manganeso tetragonal estequiométrica MnFe 2 O 4 a =8.51 А). Un valor notablemente más pequeño del parámetro de red se puede explicar con la formación de ferrita de manganeso en рН =12,5 siguiendo el mecanismo de formación de magnetita. Tras la oxidación de Mn 2+ :
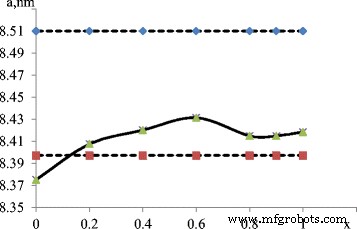
Dependencia del parámetro de la red cristalina en la proporción de cationes х
3Mn 2+ → 2Mn 3+ + □
Se forman vacantes, que facilitan la reducción de parámetros de celosía. La magnetita se forma en el segundo conjunto, y la sustitución gradual de los cationes de hierro por cationes de manganeso conduce a la reducción de las propiedades magnéticas a una proporción de 0.4 (el primer pico) después de 1-1,1, correspondiente a la ferrita de manganeso estequiométrica. Análisis de las Figs. 2 y 3 permite establecer que la formación de compuestos en el segundo conjunto ocurre según el mecanismo de formación de maghemita.
Como se indica en la Tabla 1, ferrita Mn Х Fe 3 - X О 4 se obtuvo en el nanorango. El tamaño medio de cristalito de nanopartículas Mn Х Fe 3 - X О 4 tenían un rango de 5 a 8 nm y alcanzaron un máximo en x =0. El Mn Х calculado Fe 3 - X О 4 El tamaño cristalino excedió el tamaño del cristalito de ferrita en la imagen TEM en cuatro veces debido a la agregación de nanopartículas.
Además, la Tabla 1 muestra la variación de la temperatura de Curie, parámetro de celosía con relación x en FeMn 2 - x O 4 . La temperatura de Curie disminuye a medida que aumenta el contenido de cationes manganeso. Como se puede saber, la temperatura de Curie está determinada principalmente por la interacción de superintercambio más fuerte en las ferritas. Los factores que disminuyen esta interacción conducen a una disminución de la temperatura de Curie. Con un aumento en el contenido de manganeso, el parámetro de la red aumenta (Tabla 1). Esto conduce a un aumento de las distancias iónicas, así como a una disminución de la temperatura de Curie.
El presente supuesto requiere un estudio adicional. El análisis de los patrones de derivatografía indica la formación de ferrita de manganeso en las muestras nos. 4 y 5 e isomorfismo de propiedades para las muestras 5–10 (Fig. 6). Los compuestos de diversa composición se forman en las muestras 1 a 5. Las pérdidas de masa más bajas también se observan para las composiciones estequiométricas. Las primeras regiones de los patrones de derivatografía demuestran varios efectos endotérmicos y exotérmicos correspondientes a la oxidación de los cationes de manganeso y hierro. La región de alta temperatura corresponde a la reordenación de la red cristalina (efectos endo sin cambiar la masa).
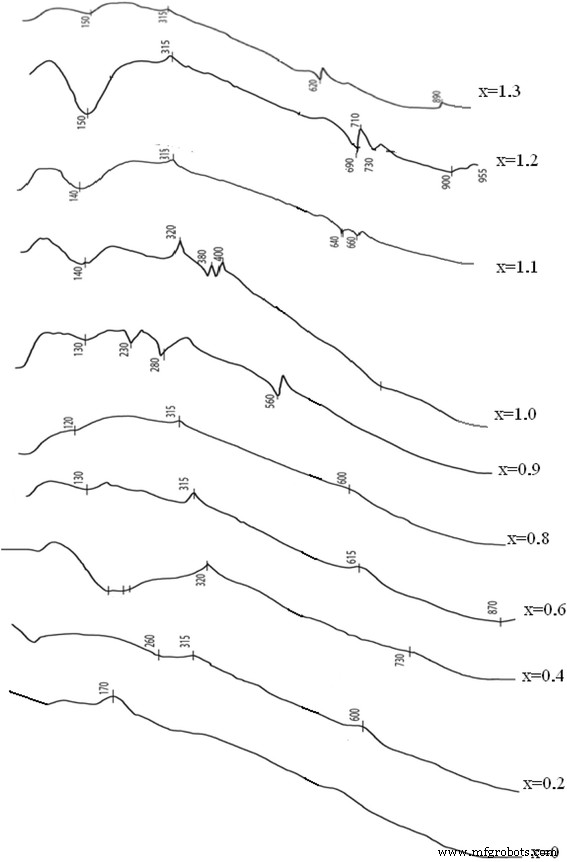
Patrones de derivatografía de muestras sintetizadas en рН =12.5
Las curvas DTG demuestran que para todas las composiciones la principal pérdida de masa corresponde a la pérdida de agua libre a 100 ° С y unida a 160 ° С. Para la composición 4, correspondiente a la ferrita estequiométrica, se observan picos exotérmicos, que corresponden a la oxidación del catión manganeso a varios estados de oxidación. En el trabajo [34], los autores han presentado el siguiente conjunto de reacciones que ocurren a varias temperaturas.
- 1.
3 Fe 2+ → 2Fe 3+ + □ temperatura 280 ° C
- 2.
4 Mn 3+ → 3Mn 4+ + □ temperatura 330 ° C
- 3.
3 Mn 2+ → 2Mn 3+ + □ temperatura 360 ° C
- 4.
3Mn 4+ + □ → 4Mn 3+ temperatura 420 ° C
- 5.
2Mn 2+ → Mn 3+ temperatura 600 ° C
Al calentar a 450–500 ° С, una estructura de γ-Fe 2 O 3 se forma el tipo.
Se puede suponer que los picos a 600 ° C corresponden a la oxidación y reducción de los cationes de hierro y manganeso. La oxidación adicional va acompañada de la transición de una red cúbica a una romboédrica, en la que todos los cationes son trivalentes. La formación de α-Fe 2 O 3 y α-Mn 2 O 3 ocurre en el rango de 600 a 1000 ° С. El análisis XRD de los productos obtenidos después de calentarlos a 1000 ° C indica la presencia de una fase magnética de ferrita de manganeso romboédrica para las muestras con una relación estequiométrica de hierro y manganeso formada a partir de óxidos de hierro y manganeso.
Además, en las muestras de encabezado 1–10 a 1000 ° С (Tabla 1), la formación de óxido de manganeso y hierro complejo se produce a través de un mecanismo similar. Los compuestos formados tienen picos similares independientemente de la composición inicial. Esto está relacionado con la estructura romboédrica, en la que todos los cationes son trivalentes. Dado que la hematita y la hausmannita tienen una estructura similar, todos los patrones XRD tienen un carácter similar.
Según los resultados de TEM, todas las muestras sintetizadas mediante el método CNP están compuestas por partículas con forma facetada regular, con un tamaño que varía de 50 a 100 nm (Fig. 7). El producto es monodisperso con un tamaño de partícula promedio de 70 a 80 nm. Las partículas facetadas observadas son policristalinas. Los datos adquiridos mediante SEM confirman que las partículas de ferrita grandes están compuestas por partículas primarias muy pequeñas y su tamaño no concuerda con los valores calculados utilizando el tamaño de cristalito (Tabla 1).

Imagen TEM ( a ) e imagen SEM ( b ) de muestra no. 4 conjunto 2
Se sabe a partir de fuentes bibliográficas que en los patrones de IR de γ-Fe 2 O 3 y Fe 3 O 4 , hay dos grupos principales de líneas características que permiten juzgar intrincadas diferencias estructurales. Estas son líneas relacionadas con las vibraciones de los enlaces М – О y М – О – Н. Introducción de diferentes iones metálicos en el óxido de hierro, lo que provoca la distorsión de la simetría del entorno de coordinación de Fe 3+ o cambios en la constante del enlace Fe-O, pueden conducir a la división o desplazamiento de las líneas características de las vibraciones del enlace Fe-O. En el caso de una distribución homogénea de iones de diferente naturaleza en la red cristalina de la estructura de la espinela, normalmente solo podemos observar el desplazamiento de los máximos de las oscilaciones características de la línea de absorción.
La figura 8 muestra los espectros de IR de las muestras estudiadas. La distribución espectral sobre 1200 cm −1 es bastante independiente de la composición de la muestra (Fig. 8).
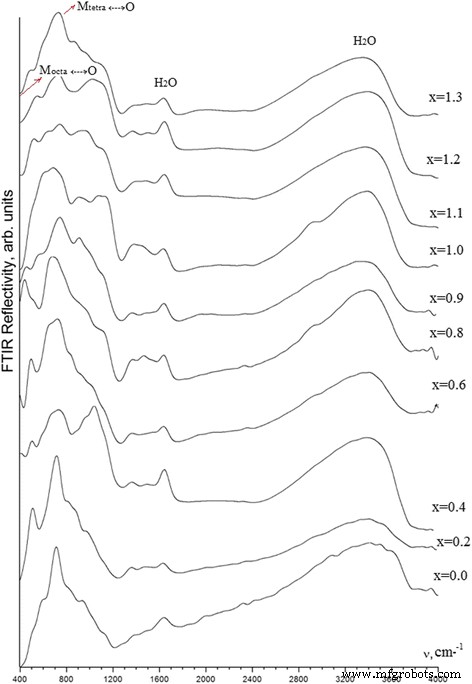
Espectros de reflexión de infrarrojos de muestras con рН =12,5 sintetizados a diferentes proporciones de cationes
La reflexión en esta región es causada por la presencia de agua que se adsorbe en la superficie de Fe 3 - x Mn x O 4 microgránulos o incrustados en su red cristalina. Las bandas dentro de 1200-1700 cm −1 El rango está relacionado con las vibraciones de flexión H – O – H, y aquellas dentro de un rango de 2400–3700 cm −1 el rango se debe a las vibraciones de estiramiento de los enlaces O – H.
La mayor sensibilidad de los espectros de reflexión a los cambios de composición tiene lugar dentro de 400-1200 cm −1 rango, típico de las vibraciones de estiramiento de Fe (Mn) –O (hasta 700 cm −1 ), Fe (Mn) –OH y Fe (Mn) –OH 2 enlaces (más de 700 cm −1 ). La posición espectral de la banda más intensa se varía con x cambiando. Su mayor desplazamiento, de 715 cm −1 en el Fe 3 O 4 espectro ( x =0.0) hasta 688 cm −1 , ocurre para la muestra con x =0,8. La ampliación de esta banda con la x también se observa un aumento (Fig. 8). Además, una nueva banda a 445 cm −1 se detecta con seguridad en los espectros de muestras con x =0,8 y 0,9. Además de estas características, debemos mencionar una redistribución espectral significativa en el x =0.4 espectro, como resultado del aumento de 1039 cm −1 banda de reflexión relativa a la banda a 715 cm −1 en el x =0.0 espectro.
De acuerdo con los datos cristalográficos, los iones metálicos (Mn, Fe) pueden ocupar posiciones con oxígeno tetraédrico y octaédrico vecino [35]. Las posiciones más probables para los iones de manganeso a una concentración de x <1.3 son las posiciones tetraédricas correspondientes al Mn 2+ estado de carga. Se detecta la aparición de iones manganeso octaédricos coordinados con el mismo estado de carga para los valores de x dentro de un rango de 0,8 a 1,2. El llenado de posiciones octaédricas con Mn 3+ iones comienza en x =1.0, y la parte de ellos en x =1,3 no es más del 23% de la cantidad total de iones manganeso [35].
Esta es la razón para explicar los cambios observados en el x =0.8 espectro iniciando el llenado de posiciones octaédricas con Mn 2+ iones.
La elevación de los 1039 cm −1 banda en la x =0.4 El espectro puede estar relacionado con las variaciones estructurales en los iones de metal (Mn, Fe) vecinos, lo que resulta en un cambio de impulso dipolar.
Desafortunadamente, un análisis más detallado se complica por la superposición esencial de bandas ensanchadas que es típico de las soluciones sólidas que contienen complejos tetraédricos y octaédricos con átomos centrales cuyas masas están próximas entre sí.
Conclusiones
En el presente trabajo, hemos encontrado una nueva ruta para la síntesis de ferrita de manganeso ultrafina de tipo Mn Х Fe 3 - X О 4 en un ancho Mn 2+ rango de sustitución de x por coprecipitación con tratamiento con CNP. La coprecipitación seguida de un tratamiento con CNP es un método eficaz para la preparación de polvo de ferrita de manganeso. Las propiedades magnéticas de Mn Х Fe 3 - X О 4 las muestras se incrementaron al aumentar los valores de pH. El proceso de ferritización fue eficaz solo a pH =12,5. La formación de compuestos a pH =11,5 se produce por el mecanismo de formación de maghemita. Las altas propiedades magnéticas exhibieron ferrita nanodispersa obtenida a pH =12.5, x =0,6-0,8. El tamaño medio de los cristalitos osciló entre 50 y 80 A. Las ferritas nanodispersas tenían una forma facetada y partículas uniformes. El patrón XRD indica los nanocristales de fase de espinela simple con estructura de espinela cúbica a 0 < x <0,8.
La espectroscopía FTIR confirmó los resultados de las mediciones magnéticas. La disminución del valor de la saturación magnética que comienza con x =1.0 se debe al llenado de posiciones octaédricas con Mn 2+ iones.
Abreviaturas
- CNP:
-
Contacto con plasma no equilibrado
- DTA:
-
Análisis térmico diferencial
- DTG:
-
Análisis termogravimétrico diferencial
- FTIR:
-
Infrarrojos por transformada de Fourier
- I S :
-
Magnetización de saturación
- SEM:
-
Microscopía electrónica de barrido
- T C :
-
Temperatura
- TG:
-
Pérdida masiva
- XRD:
-
Difracción de rayos X
- Нс:
-
Fuerza coercitiva (Oe)
Nanomateriales
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- Síntesis fácil y propiedades ópticas de nanocristales y nanovarillas de selenio pequeños
- Nanocompuestos magnéticos de poli (N-isopropilacrilamida):efecto del método de preparación sobre las propiedades antibacterianas
- Síntesis de puntos cuánticos de sulfuro de antimonio solubles en agua y sus propiedades fotoeléctricas
- Síntesis fácil de óxido de estaño mesoporoso similar a un agujero de gusano a través del autoensamblaje inducido por evaporación y las propiedades mejoradas de detección de gas
- Efecto del método de síntesis de nanopartículas de manganita La1 - xSr x MnO3 en sus propiedades
- Prueba de las propiedades estructurales, electrónicas y magnéticas de Ag n V (n =1–12) Clusters
- Influencia del parámetro de ajuste de pH para la modificación sol-gel en las propiedades estructurales, microestructura y magnéticas de la ferrita de estroncio nanocristalina
- Síntesis verde de nanopartículas de metal y óxido de metal y su efecto sobre el alga unicelular Chlamydomonas reinhardtii
- Síntesis y propiedades de puntos cuánticos de CdTe de aleación de Mn emisor de azul soluble en agua
- Efecto de la morfología y la estructura cristalina en la conductividad térmica de los nanotubos de titania



