Fabricación y actividad fotocatalítica de heteroestructuras Ag3PO4 / T-ZnOw
Resumen
El Ag 3 PO 4 / Se prepararon heteroestructuras de bigotes de ZnO de tipo tetrápodo (T-ZnOw) mediante un método de precipitación simple. Las heteroestructuras obtenidas se caracterizaron por difracción de rayos X, microscopía electrónica de barrido, microscopía electrónica de transmisión, microscopía electrónica de transmisión de alta resolución, espectroscopía fotoelectrónica de rayos X y espectroscopía de reflectancia difusa UV-Vis. La actividad de fotodegradación de Ag 3 PO 4 / T-ZnOw se evaluó mediante la degradación de rodamina B (RhB) bajo irradiación de luz visible. Cuando la relación molar de Ag 3 PO 4 a T-ZnOw fue del 10% (Ag 3 PO 4 / T-ZnOw-2), la mayor eficiencia de degradación (92,9%) podría lograrse entre las heteroestructuras. La constante de velocidad de fotodegradación de Ag 3 PO 4 / T-ZnOw-2 (0,05179 min −1 ) fue 3,59 veces mayor que el de T-ZnOw (0,01444 min −1 ). Además, el Ag 3 PO 4 El fotocatalizador / T-ZnOw-2 todavía poseía una eficiencia de degradación del 77,8% después de cuatro ciclos sucesivos. El Ag 3 PO 4 / El catalizador T-ZnOw-2 tenía una actividad fotocatalítica mucho más alta que el T-ZnOw puro y una mejor estabilidad y capacidad de reutilización que el Ag 3 puro PO 4 . Se investigó el efecto de diferentes depuradores sobre la eficiencia de degradación y el posible mecanismo fotocatalítico del Ag 3 PO 4 / También se presentó el fotocatalizador T-ZnOw.
Introducción
La contaminación por tintes de las aguas residuales de las industrias textiles ha sido un problema ambiental importante en las últimas décadas debido a la no biodegradabilidad y la potencial carcinogenicidad. Actualmente, los investigadores han explorado varias técnicas para manejar los contaminantes en las aguas residuales. La tecnología de fotocatálisis de semiconductores se ha considerado una forma eficaz de purificar el agua contaminada [1, 2, 3, 4, 5, 6]. El óxido de zinc (ZnO), un material fotocatalítico ecológico, ha sido ampliamente estudiado debido a sus características de bajo costo, alta controlabilidad y estabilidad térmica y química [7,8,9,10,11]. Desafortunadamente, el ancho de banda prohibida (3.37 eV) de ZnO restringe sus aplicaciones prácticas a gran escala en luz visible [12]. Además, la baja tasa de separación de los pares de electrones y huecos fotogenerados también limita el rendimiento fotocatalítico del ZnO. Para la modificación de los fotocatalizadores de ZnO, una estrategia eficaz es cambiar la banda de absorción del rango de luz ultravioleta a visible, permitiendo la absorción de más energía de la irradiación solar y mejorando la utilización de la luz solar [13]. En general, se sabe que el acoplamiento de ZnO con semiconductores de banda prohibida estrecha puede ser una forma eficaz de absorber más energía de la irradiación solar y mejorar la actividad fotocatalítica. Además, la formación de heteroestructuras con una brecha de energía adecuada también puede mejorar la separación de los portadores de carga en los fotocatalizadores. Por ejemplo, AgBr / ZnO [14], ZnO / BiOI [15], ZnO / AgI [16], Ag 3 Voz 4 / ZnO [17], Ag 2 CO 3 / ZnO [18], Ag 2 O / ZnO [19] y BiVO 4 / ZnO [20].
Recientemente, el ortofosfato de plata (Ag 3 PO 4 ) ha atraído una atención considerable como material de acoplamiento prometedor debido a una banda prohibida estrecha (aproximadamente 2,4 eV) [21], que mostró una alta eficiencia de fotodegradación de contaminaciones orgánicas en solución acuosa bajo luz visible [22,23,24,25]. Sin embargo, el Ag 3 PO 4 se puede reducir a Ag 0 durante el proceso fotocatalítico debido a la fotocorrosión de los electrones fotogenerados bajo irradiación de luz visible, lo que puede disminuir la estabilidad estructural y la reutilización, y limitar fuertemente la aplicación a largo plazo para el tratamiento del agua [23, 26,27,28]. Además, el uso de una gran cantidad de material caro que contiene plata en el sistema fotocatalítico aumentó considerablemente los costes operativos. Como se informó anteriormente, la estabilidad de Ag 3 PO 4 se puede mejorar mediante la preparación de compuestos sobre un material de soporte de estructura electrónica combinada y los compuestos mostraron un excelente rendimiento fotocatalítico al mismo tiempo [27, 29, 30, 31].
En este trabajo, depositamos Ag 3 PO 4 partículas en las superficies de T-ZnOw mediante un método de deposición in situ fácil a temperatura ambiente. En el Ag 3 PO 4 / T-ZnOw, T-ZnOw funciona como un sustrato, que tiene una forma y estructura únicas, baja densidad de defectos nativos y grandes superficies específicas [32,33,34,35]. Las actividades fotocatalíticas del Ag 3 PO 4 Los compuestos de / T-ZnOw se investigaron descomponiendo RhB bajo la irradiación de luz visible, y también se determinó la estabilidad. Además, también se discutió en detalle el posible mecanismo fotocatalítico.
Métodos
Materiales
T-ZnOw se obtuvo de Chengdu Crystrealm Co. Ltd. (Chengdu, China). Nitrato de plata (AgNO 3 ,> 99,8%) se adquirió de Tianjin Fengchuan Chemical Reagent Co. Ltd. (Tianjin, China). Fosfato de sodio dibásico dodecahidrato (Na 2 HPO 4 · 12H 2 O, 99,0%) y benzoquinona (BQ) se adquirieron de Aladdin Reagents Company (Shanghai, China). RhB fue proporcionado por Macklin Biochemical Company (Shanghai, China). El alcohol isopropílico (IPA) se obtuvo de Tianjin Kemiou Chemical Co. Ltd. (Tianjin, China). La sal disódica del ácido etilendiaminotetraacético (EDTA-2Na) se adquirió de Tianjin Shentai Chemical Industry Co. Ltd. (Tianjin, China). El etanol absoluto se obtuvo de Sinopharm Chemical Reagent Co. Ltd. (Shanghai, China). En todos los casos se utilizó agua desionizada con resistividad de 18,2 MΩ cm procedente de un sistema de purificación de agua ULUPURE (Chengdu, China).
Preparación de fotocatalizadores
Se empleó un método de precipitación in situ para preparar Ag 3 PO 4 / T-ZnOw compuestos y las proporciones molares de Ag 3 PO 4 a T-ZnOw fueron 5%, 10% y 15%, respectivamente. Los productos se marcaron como Ag 3 PO 4 / T-ZnOw-1, Ag 3 PO 4 / T-ZnOw-2 y Ag 3 PO 4 / T-ZnOw-3, respectivamente. Por ejemplo, para Ag 3 PO 4 / Muestra de T-ZnOw-2, 0,1 g de T-ZnOw y 0,0440 g de Na 2 HPO 4 · 12H 2 O se dispersaron en 100 ml de agua desionizada mediante ultrasonidos y luego se agitaron magnéticamente. A continuación, 0,0626 g de AgNO 3 disuelto en 50 ml de agua desionizada se añadió lentamente a la suspensión anterior mediante una jeringa fijada en la bomba de inyección con agitación magnética. Posteriormente, el sistema de reacción se mantuvo en agitación durante 3 h. El Ag 3 PO 4 El precipitado de / T-ZnOw se recogió por centrifugación, se lavó minuciosamente con agua desionizada y etanol absoluto y posteriormente se secó en un horno a 60 ° C. A modo de comparación, Ag 3 puro PO 4 se preparó de acuerdo con el mismo proceso en ausencia de T-ZnOw.
Caracterización
Las mediciones de difracción de rayos X (XRD) se llevaron a cabo en un difractómetro Rigaku SmartLab utilizando Cu K-α como radiación con una velocidad de exploración de 10 ° / min. La morfología de los compuestos se estudió mediante microscopía electrónica de barrido (SEM, JSM-7200F, JEOL, Japón). Se utilizó espectroscopia de rayos X de dispersión de energía (EDS) adjunta al instrumento SEM para determinar la composición química del producto. Se obtuvieron imágenes de microscopía electrónica de transmisión (TEM) y microscopía electrónica de transmisión de alta resolución (HRTEM) con un microscopio electrónico de transmisión JEM-2100F. Las mediciones de espectroscopía de fotoelectrones de rayos X (XPS) se registraron en Thermo ESCALAB 250XI, y las energías de unión (BE) se calibraron con respecto al pico de C1s a 284,6 eV. Las mediciones de espectros de reflectancia difusa (DRS) de UV-Vis se obtuvieron usando un espectrofotómetro UV-Vis-NIR (Cary5000, Agilent Technologies, EE.UU.) con politetrafluoroetileno como referencia. Los espectros de emisión de fotoluminiscencia (PL) de las muestras se midieron con un espectrofotómetro de fluorescencia F-7000 (Hitachi, Japón) con una longitud de onda de excitación de 355 nm.
Experimentos de fotocatálisis
Los experimentos de fotocatálisis se probaron mediante la fotodegradación de RhB bajo luz visible. Los experimentos se llevaron a cabo en un vaso de precipitados de vidrio con camisa de 250 ml con agua de refrigeración para mantener constante la temperatura del sistema a temperatura ambiente. Una lámpara de xenón de 300 W con un filtro de corte de 420 nm proporcionó la luz visible. Cuarenta miligramos de Ag 3 PO 4 Se añadió compuesto / T-ZnOw a 100 ml de solución de RhB 10 mg / L. Antes de encender la lámpara de xenón, las suspensiones se agitaron en la oscuridad durante 30 minutos para alcanzar un equilibrio de adsorción-desorción. La distancia entre la fuente de luz y la superficie de las suspensiones fue de 15 cm. Cada 10 minutos, se recogieron 3 ml de suspensión y se centrifugaron para obtener un líquido transparente y luego se analizaron en un espectrofotómetro TU-1901 UV-Vis (Puxi, China) a 554 nm. La eficiencia de degradación fotocatalítica se calculó mediante la siguiente fórmula:
$$ \ eta =\ left (1-C / {C} _0 \ right) \ times 100 \% $$donde C 0 es la concentración inicial de RhB y C es la concentración de RhB después de la iluminación en el momento t , que varía con el tiempo de reacción.
Resultados y discusión
La Figura 1 muestra los patrones XRD del Ag 3 PO 4 / T-ZnOw compuestos con diferentes proporciones molares de Ag 3 PO 4 , junto con los de T-ZnOw y Ag 3 PO 4 . Los patrones mostraron que T-ZnOw era consistente con el patrón estándar de ZnO de la fase de wurtzita hexagonal (JCPDS no. 36-1451) (Fig. 1 (a)), mientras que Ag 3 PO 4 era un cristal de fase cúbica (JCPDS nº 06-0505) (Fig. 1 (e)). El Ag 3 PO 4 / T-ZnOw compuestos (Fig. 1 (b) - (d)) exhibieron una coexistencia de ambos Ag 3 PO 4 y T-ZnOw. Con las proporciones molares de Ag 3 PO 4 aumentando, las intensidades de los picos de Ag 3 PO 4 mejorado notablemente, mientras que los de T-ZnOw disminuyeron al mismo tiempo. Los picos del Ag 3 PO 4 / Los compuestos T-ZnOw obviamente estaban relacionados con T-ZnOw y Ag 3 PO 4 , y no se encontraron otras fases cristalinas nuevas, lo que demuestra que la carga de Ag 3 PO 4 no había cambiado la fase cristalina de T-ZnOw. Estos resultados revelaron que Ag 3 PO 4 Las partículas se depositaron con éxito en las superficies T-ZnOw, y Ag 3 PO 4 Se obtuvieron heteroestructuras de / T-ZnOw.
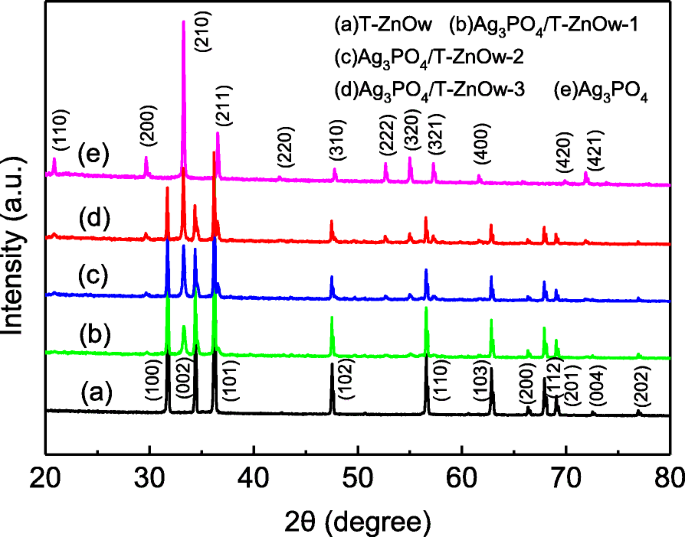
Patrones XRD de (a) T-ZnOw, (b) Ag 3 PO 4 / T-ZnOw-1, (c) Ag 3 PO 4 / T-ZnOw-2, (d) Ag 3 PO 4 / T-ZnOw-3 y (e) Ag 3 PO 4
La Figura 2 mostró las imágenes SEM de T-ZnOw, Ag 3 PO 4 y el Ag 3 PO 4 / T-ZnOw heteroestructuras, junto con la imagen TEM y la imagen HRTEM de Ag 3 PO 4 / T-ZnOw-2. T-ZnOw con una superficie bastante lisa tenía cuatro patas que crecían desde un núcleo común y se extendían hacia el espacio circundante. Esta extensión facilitó el ensamblaje en una buena red con resistencia mecánica al conectar las patas entre sí. Pure Ag 3 PO 4 exhibió una forma esférica irregular con un diámetro de 150 a 500 nm. El tamaño de T-ZnOw estaba a nivel de micras, mientras que el tamaño de Ag 3 PO 4 estaba a nivel de nanoescala. La Figura 2c – e muestra las imágenes SEM de Ag 3 PO 4 / T-ZnOw heteroestructuras. Se pudo encontrar que Ag 3 de tamaño nanométrico PO 4 las partículas se depositaron sobre la estructura de soporte tridimensional (3D) de T-ZnOw. La cantidad y el tamaño de Ag 3 PO 4 partículas aumentadas con las proporciones molares de Ag 3 PO 4 creciente. Cuando la relación molar de Ag 3 PO 4 era del 10%, el diámetro medio de Ag 3 PO 4 partículas era de aproximadamente 150 nm, mientras que aumentaba aún más la cantidad de Ag 3 PO 4 resultó en la agregación de Ag 3 PO 4 partículas en la superficie de T-ZnOw (Fig. 2e). La Figura 2f era la imagen TEM de la interfaz de contacto del Ag 3 PO 4 / T-ZnOw-2. El Ag 3 de tamaño nanométrico PO 4 las partículas se unieron a la superficie de T-ZnOw con un buen contacto. El recuadro mostraba la imagen HRTEM de la región del rectángulo rojo de Ag 3 PO 4 / T-ZnOw-2, y el espaciado de la red de 0.240 nm corresponde al plano cristalino (211) de Ag 3 PO 4 . El recuadro de la Fig. 2d mostró el espectro EDS correspondiente a la región rectangular de la imagen SEM del Ag 3 PO 4 / Muestra de T-ZnOw-2. La muestra constaba de cuatro elementos, Zn, Ag, O y P, lo que coincidía con los resultados de XPS.

Imágenes SEM de a T-ZnOw, b Ag 3 PO 4 , c Ag 3 PO 4 / T-ZnOw-1, d Ag 3 PO 4 / T-ZnOw-2 (el recuadro mostraba el espectro EDS del área seleccionada), e Ag 3 PO 4 / T-ZnOw-3 y f Imagen TEM de Ag 3 PO 4 / T-ZnOw-2 (el recuadro mostraba la imagen HRTEM de la región del rectángulo rojo)
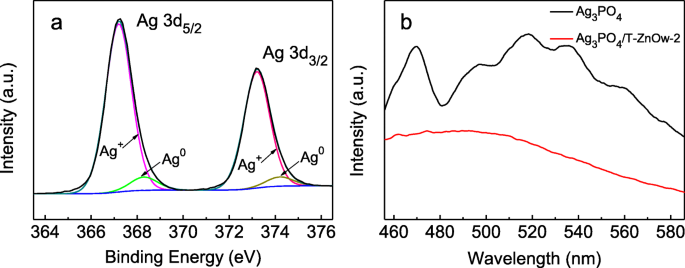
Se llevaron a cabo mediciones de XPS para investigar la composición elemental y los estados químicos del Ag 3 PO 4 / Muestra de T-ZnOw-2. La Figura 3a mostró el espectro XPS de la encuesta e indicó la existencia de Zn, Ag, O y P. La Figura 3b mostró el espectro XPS de alta resolución del Zn 2p, y dos picos de energía de enlace a 1021.5 y 1044.6 eV podrían asignarse a Zn 2p 3/2 y Zn 2p 1/2 de T-ZnOw, respectivamente [36]. Dos picos ubicados en 367.2 y 373.2 eV podrían atribuirse a Ag 3d 5/2 y Ag 3d 3/2 en el espectro XPS del orbital Ag 3d (Fig. 3c), que era una característica de Ag + [11]. Como se ve en el espectro XPS de O 1s en la Fig. 3d, había tres picos en 529,9, 531,2 y 532,5 eV, que podrían atribuirse a las redes de oxígeno en T-ZnOw [33], Ag 3 PO 4 [37], y adsorbieron grupos –OH en la superficie de Ag 3 PO 4 / T-ZnOw-2, respectivamente. Una banda ancha y débil centrada en 132,3 eV en la Fig. 3 e podría atribuirse a la característica P 2p de Ag 3 PO 4 [38]. Los resultados de XPS demostraron además que Ag 3 PO 4 y T-ZnOw se había compuesto.
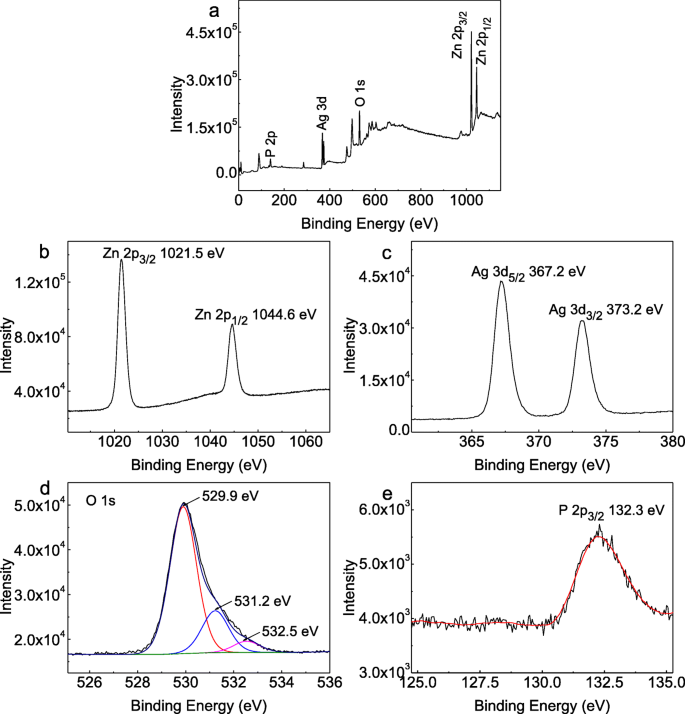
Espectros XPS de Ag 3 PO 4 / T-ZnOw-2: a escaneo de la encuesta, b Zn 2p, c Ag 3d, d O1s y e P 2p
Se midieron los espectros de reflectancia difusa (DRS) de UV-Vis para estudiar las propiedades de absorción óptica del Ag 3 PO 4 / T-ZnOw heteroestructuras, junto con las de T-ZnOw y Ag 3 PO 4 (Figura 4a). Se pudo observar que el borde de absorción de T-ZnOw y Ag 3 PO 4 se dijo que era de aproximadamente 400 y 510 nm, respectivamente. En comparación con T-ZnOw, el Ag 3 PO 4 / T-ZnOw heteroestructuras exhibieron intensidades de absorción crecientes en la región de luz visible con las proporciones molares de Ag 3 PO 4 creciente. El rango de absorción ampliado y la absorbancia mejorada del Ag 3 PO 4 / T-ZnOw heteroestructuras en la región de luz visible se beneficiaron de la introducción de la banda prohibida más estrecha de Ag 3 PO 4 . Los resultados anteriores indicaron que el Ag 3 PO 4 Las heteroestructuras de / T-ZnOw eran fotocatalizadores potenciales impulsados por luz visible. Además, la energía de banda prohibida de T-ZnOw y Ag 3 PO 4 fue evaluado por la función de Kubelka-Munk [39]. Según la trama de ( ahv ) 2 versus energía, como se muestra en la Fig. 4b, el valor de banda prohibida de T-ZnOw y Ag 3 PO 4 fue de aproximadamente 3,16 y 2,42 eV, respectivamente.
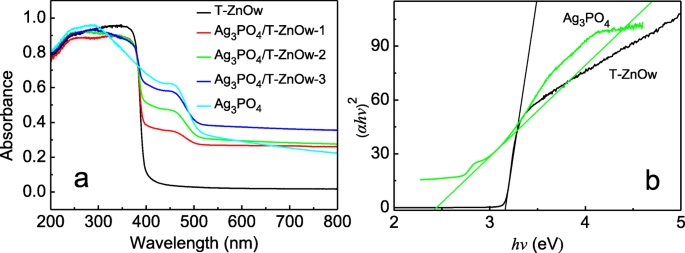
un UV-Vis DRS de T-ZnOw, Ag 3 PO 4 / T-ZnOw-1, Ag 3 PO 4 / T-ZnOw-2, Ag 3 PO 4 / T-ZnOw-3 y Ag 3 PO 4 . b Gráficas de ( αhv ) 2 versus energía ( hv )
La fotodegradación de RhB se utilizó para evaluar la actividad fotocatalítica de T-ZnOw, Ag 3 PO 4 / T-ZnOw-1, Ag 3 PO 4 / T-ZnOw-2, Ag 3 PO 4 / T-ZnOw-3, Ag 3 PO 4 y una mezcla de T-ZnOw (26,41 mg) y Ag 3 PO 4 (13,59 mg) bajo luz visible. La Figura 5a mostró la actividad fotocatalítica de diferentes muestras para la degradación de RhB. Después de la irradiación durante 50 min, la eficiencia de degradación de T-ZnOw, Ag 3 PO 4 / T-ZnOw-1, Ag 3 PO 4 / T-ZnOw-2, Ag 3 PO 4 / T-ZnOw-3, Ag 3 PO 4 y la mezcla era 52,5%, 85,3%, 92,9%, 79,9%, 96,9% y 62,9%, respectivamente. La mezcla física de T-ZnOw y Ag 3 PO 4 que tenía la misma proporción de composición con Ag 3 PO 4 / T-ZnOw-2 mostró una menor eficiencia de degradación de RhB que la de Ag 3 PO 4 / T-ZnOw-2, lo que implica que Ag 3 PO 4 Se formaron heteroestructuras / T-ZnOw. Con las proporciones molares de Ag 3 PO 4 aumentando, la eficiencia de degradación de RhB primero aumentó y luego disminuyó, y Ag 3 PO 4 / T-ZnOw-2 mostró la mayor eficiencia de degradación entre las heteroestructuras, que era muy cercana a la de Ag 3 PO 4 . El Ag 3 aglomerado PO 4 partículas en el Ag 3 PO 4 / La muestra de T-ZnOw-3 afectó el tamaño y la dispersión de Ag 3 PO 4 . Es bien sabido que un tamaño de partícula más pequeño disminuye la posibilidad de recombinación de huecos de electrones, mejorando así el rendimiento fotocatalítico del material. Además, el gran tamaño de Ag 3 PO 4 partículas en el Ag 3 PO 4 / La muestra de T-ZnOw-3 puede debilitar la fuerza de anclaje entre T-ZnOw y Ag 3 PO 4 y destruir la estructura de heterounión, lo que limitaría la actividad fotocatalítica. La fotodegradación de RhB siguió a la reacción de pseudoprimer orden, como se muestra en la Fig. 5b. La Figura 5c muestra las constantes de la tasa de degradación de diferentes fotocatalizadores, y la tendencia es la misma que la eficiencia de degradación. La constante de velocidad de fotodegradación de Ag 3 PO 4 / T-ZnOw-2 (0,05179 min −1 ) fue 3,59 veces mayor que el de T-ZnOw (0,01444 min −1 ). Los resultados anteriores indicaron claramente que la actividad fotocatalítica de T-ZnOw aumentó con Ag 3 PO 4 modificación. La actividad fotocatalítica mejorada de Ag 3 PO 4 / T-ZnOw heteroestructuras se benefició de la mayor intensidad de absorbancia de luz visible al cargar Ag 3 PO 4 en la superficie de T-ZnOw, lo que permitiría que Ag 3 PO 4 / T-ZnOw heteroestructuras para producir portadores fotogenerados para la fotodegradación de RhB bajo luz visible. Cabe señalar que Ag 3 PO 4 parecía tener la mejor actividad fotocatalítica entre las muestras preparadas. Sin embargo, Ag 3 PO 4 exhibió menor estabilidad en comparación con Ag 3 PO 4 / T-ZnOw que se muestra en la siguiente discusión, que afectó sus usos a largo plazo.
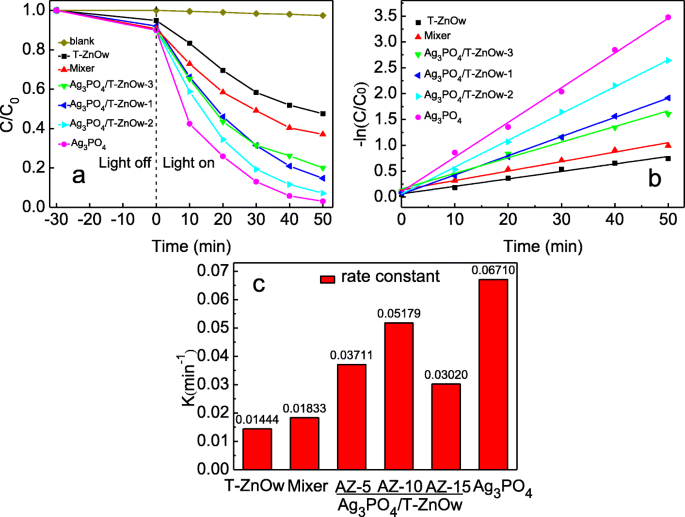
un Fotodegradación de RhB con diferentes fotocatalizadores. b Las curvas de simulación cinética. c Constantes de velocidad aparentes
Las dosis adecuadas de fotocatalizador en el sistema de fotodegradación pueden reducir el costo desde el punto de vista económico. La Figura 6a mostró la influencia de las dosis de alimento de Ag 3 PO 4 / T-ZnOw-2 sobre la eficiencia de degradación. La eficacia de degradación aumentó obviamente con el aumento de la dosis de 0,2 a 0,4 g / L y disminuyó posteriormente. Con el aumento de las dosis de catalizador, se incrementó la turbidez de la solución y al mismo tiempo se redujo la penetración de luz en el sistema de reacción. La menor absorción de luz visible del fotocatalizador podría disminuir la eficiencia de degradación a una dosis mayor del fotocatalizador [40, 41].
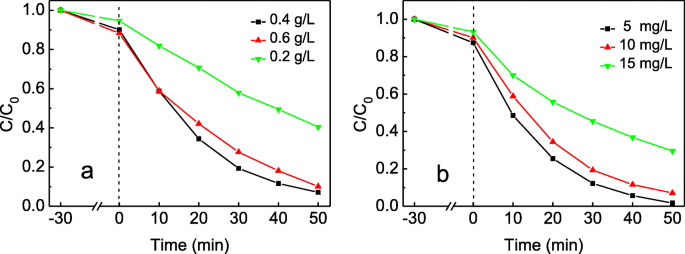
un Efecto de diferentes Ag 3 PO 4 / Dosis de T-ZnOw-2 sobre la fotodegradación de RhB. b Efecto de diferentes concentraciones iniciales de RhB sobre la actividad fotocatalítica de Ag 3 PO 4 / T-ZnOw-2
El efecto de diferentes concentraciones iniciales de RhB sobre la actividad fotocatalítica de Ag 3 PO 4 Se estudió / T-ZnOw-2 y se muestra en la Fig. 6b. Cuando las concentraciones iniciales fueron de 5 mg / L, 10 mg / L y 15 mg / L, la eficiencia de degradación de RhB fue del 98,2%, 92,9% y 70,4%, respectivamente. La disminución de la eficiencia de degradación puede deberse a la disminución de los fotones absorbidos por el catalizador como resultado del aumento en la longitud de la trayectoria de los fotones que entran en la solución con concentraciones iniciales más altas. Otra razón puede ser que se formen más intermedios con las concentraciones iniciales más altas de RhB, lo que podría formar una competencia de adsorción con los reactivos iniciales [42, 43]. Sin embargo, una concentración inicial demasiado baja no puede mostrar completamente la capacidad de fotodegradación del catalizador. Por lo tanto, la concentración inicial de la solución de RhB en el experimento fue preferiblemente de 10 mg / L.
La estabilidad y reutilización de un fotocatalizador son cruciales para medir su aplicación práctica [44]. Es bien sabido que el Ag 3 PO 4 El fotocatalizador se puede reducir fácilmente a Ag mediante fotocorrosión, lo que limita su aplicación práctica a largo plazo. La Figura 7 muestra los experimentos de reciclaje para la degradación de RhB sobre Ag 3 PO 4 / T-ZnOw-2 y Ag 3 PO 4 . Después de cuatro ciclos sucesivos, la eficiencia de degradación de Ag 3 PO 4 era obviamente más bajo que el de Ag 3 PO 4 / T-ZnOw-2. Los resultados presentados anteriormente demostraron que mientras que Ag 3 PO 4 El fotocatalizador mostró una actividad fotocatalítica algo mayor en el primer uso, el Ag 3 PO 4 Las heteroestructuras de / T-ZnOw parecían ser potenciales para aplicaciones a largo plazo debido a la estabilidad mejorada. Pure Ag 3 PO 4 El fotocatalizador es inestable si no se añade ningún reactivo de sacrificio en el proceso fotocatalítico [45]. La solubilidad del Ag 3 puro PO 4 en solución acuosa es relativamente alto, lo que da como resultado una disminución de su estabilidad durante el proceso fotocatalítico [25]. Ag 3 PO 4 se puede reducir a Ag metálico por los electrones fotogenerados, y una cierta cantidad de Ag puede formar la estructura de Ag / Ag 3 PO 4 / T-ZnOw. La fotocorrosión adicional de Ag 3 PO 4 en Ag / Ag 3 PO 4 / El compuesto T-ZnOw puede inhibirse mediante la transferencia de electrones desde la banda de conducción de Ag 3 PO 4 a Ag metálico [46]. Después de Ag 3 PO 4 Las partículas se anclaron en las superficies de T-ZnOw, Ag 3 PO 4 Las partículas y T-ZnOw tenían un contacto íntimo entre sí, y las superficies lisas de T-ZnOw sirvieron como un refugio ideal para Ag 3 PO 4 y producir menos cantidad de Ag 3 PO 4 decapado en solución acuosa, que era similar al Ag 3 informado PO 4 / BiVO 4 heterounión [47]. Por lo tanto, Ag 3 PO 4 / La heteroestructura de T-ZnOw-2 mostró una buena estabilidad fotocatalítica y poseía una eficiencia de degradación del 77,8% después de los experimentos de reciclaje.
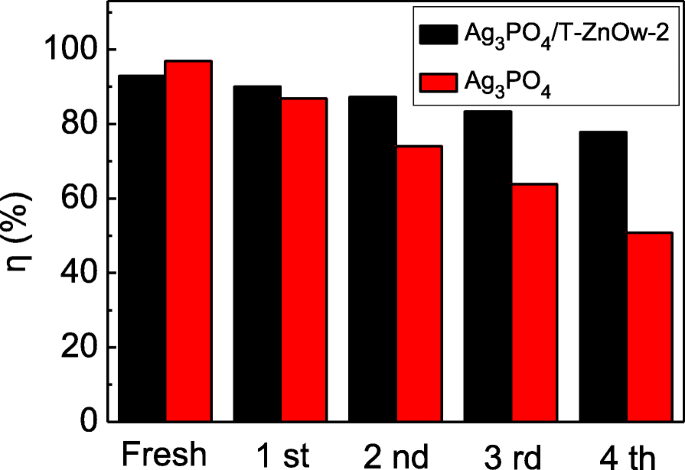
Cuatro ciclos sucesivos para la degradación de RhB sobre Ag 3 PO 4 / T-ZnOw-2 y Ag 3 PO 4
El efecto de diferentes eliminadores sobre la eficiencia de degradación de RhB por Ag 3 PO 4 / T-ZnOw-2 se muestra en la Fig. 8 después de la irradiación durante 50 min. Después de la adición de IPA, BQ y EDTA-2Na, la eficiencia de degradación disminuyó a 38,8%, 65,6% y 82,6%, respectivamente, lo que indica que los radicales hidroxilo (∙ OH) y los radicales superóxido (∙ O 2 - ) fueron las especies principalmente activas, y los agujeros (h + ) jugó parcialmente en la decoloración fotocatalítica. La posición de la banda de Ag 3 PO 4 y T-ZnOw se calculó mediante la siguiente ecuación [18]:
$$ {\ Displaystyle \ begin {array} {l} {E} _ {\ mathrm {VB}} =X- {E} ^ 0 + 0.5 {E} _ {\ mathrm {g}} \\ {} { E} _ {\ mathrm {CB}} ={E} _ {\ mathrm {VB}} - {E} _ {\ mathrm {g}} \ end {matriz}} $$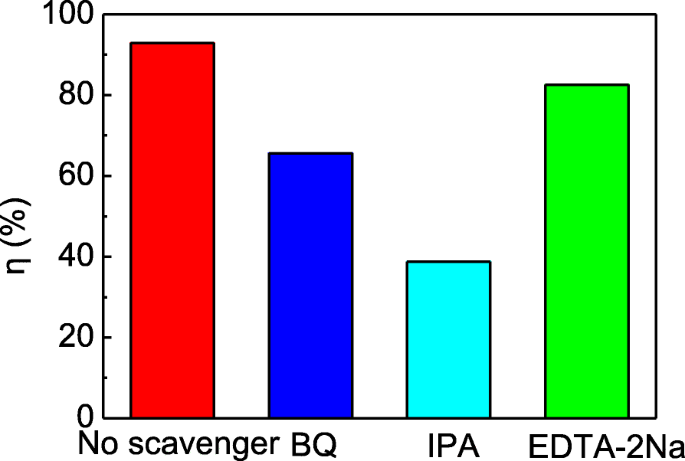
La influencia en la eficiencia de degradación de RhB por Ag 3 PO 4 / T-ZnOw-2 con diferentes eliminadores (dosis de eliminación =0,2 mmol / L)
donde X es la electronegatividad absoluta del semiconductor y E g es la energía de la banda prohibida. La X valor para Ag 3 PO 4 y ZnO son 6,16 [48] y 5,76 eV [49], respectivamente. De acuerdo con la banda prohibida lograda en la Fig.4, el E VB de Ag 3 PO 4 y T-ZnOw se calculó en 2,87 y 2,84 eV, y sus homólogos E CB fue de 0,45 y - 0,32 eV, respectivamente.
El posible mecanismo para la degradación fotocatalítica de RhB podría proponerse basándose en los resultados anteriores, como se muestra en el Esquema 1. El potencial de la banda de conducción (CB - 0.32 eV) y el potencial de la banda de cenefa (VB 2.84 eV) de T-ZnOw fueron más negativos que los de Ag 3 PO 4 (CB 0,45 eV; VB 2,87 eV). El emocionado Ag 3 PO 4 podría producir pares de agujeros de electrones bajo iluminación de luz visible. Por lo tanto, los agujeros fotogenerados podrían cambiar del VB de Ag 3 PO 4 en el VB vacío de T-ZnOw, lo que facilitó la separación efectiva de electrones y huecos fotogenerados. Una parte de los agujeros fotogenerados reaccionaría con el H 2 adsorbido. O para formar ∙ OH como principal especie activa, y la otra parte de los agujeros adsorbidos en la superficie de la heteroestructura podría participar directamente en la fotodegradación de RhB. Sin embargo, el potencial CB de Ag 3 PO 4 fue de 0,45 eV, que era superior al potencial de reducción de O 2 / ∙ O 2 - (-0,33 eV) [29]. Los electrones fotogenerados en la banda de conducción de Ag 3 PO 4 no pudo reaccionar con oxígeno disuelto para formar ∙ O 2 - . Una pequeña cantidad de Ag metálico podría formarse por la reacción entre Ag + de Ag 3 PO 4 y electrones fotogenerados por iluminación de luz visible, lo que podría ser probado por el espectro XPS de Ag 3 PO 4 / T-ZnOw-2 después de la iluminación durante 50 min en reacción fotocatalítica. La Figura 9a mostró el espectro Ag3d XPS de Ag 3 PO 4 / T-ZnOw-2 después de fotocatálisis durante 50 min. El pico de 367,2 y 373,2 eV podría atribuirse a Ag + iones, y el pico de 368,3 y 374,2 eV se asignó al Ag metálico [11]. Luego, electrones fotogenerados en la banda de conducción de Ag 3 PO 4 podría transferirse a Ag metálico, inhibiendo así la recombinación de pares de agujeros de electrones. Además, los electrones fotogenerados podrían ser capturados por oxígeno disuelto para formar ∙ O 2 - , que jugó uno de los papeles principales en la fotodegradación de RhB. Todas estas especies reactivas fotogeneradas (∙ OH, ∙ O 2 - y h + ) podría reaccionar con RhB para formar CO 2 y H 2 O y, finalmente, mejorar el rendimiento fotocatalítico para la degradación de RhB. La Figura 9b presentó los espectros PL de Ag 3 PO 4 y Ag 3 PO 4 / T-ZnOw-2 con la longitud de onda de excitación de 355 nm. Comparado con Ag 3 puro PO 4 , la intensidad de Ag 3 PO 4 / T-ZnOw-2 reveló una disminución en la fluorescencia, que se atribuyó principalmente a la transferencia eficiente del portador de carga entre Ag 3 PO 4 y T-ZnOw. Los resultados de PL fueron consistentes con el mecanismo fotocatalítico propuesto.
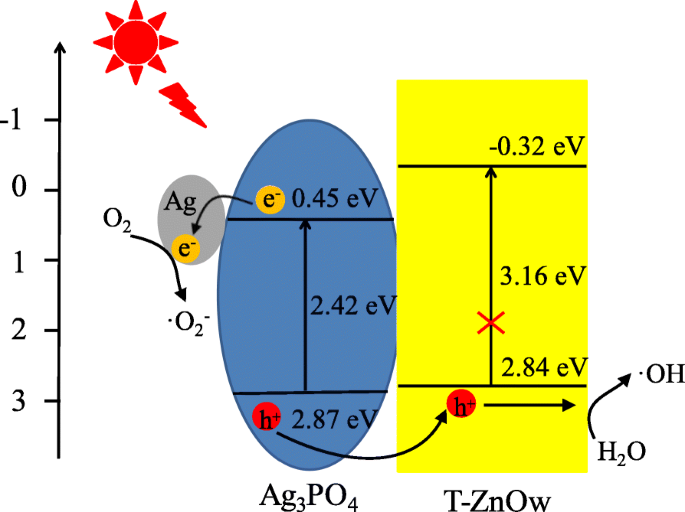
Diagrama esquemático del posible mecanismo fotocatalítico de Ag 3 PO 4 / T-ZnOw
un Espectro Ag 3d XPS de Ag 3 PO 4 / Muestra de T-ZnOw-2 después de fotocatálisis. b Espectros PL de Ag 3 PO 4 y Ag 3 PO 4 / T-ZnOw-2
Conclusiones
En resumen, Ag 3 PO 4 Las heteroestructuras de / T-ZnOw se fabricaron con éxito mediante un sencillo método de precipitación in situ. El Ag 3 PO 4 / El catalizador T-ZnOw-2 exhibió una actividad fotocatalítica superior para la degradación de RhB que el T-ZnOw puro y poseía una mejor estabilidad y capacidad de reutilización en comparación con Ag 3 puro PO 4 . En condiciones óptimas, Ag 3 PO 4 / T-ZnOw-2 mostró la mayor eficiencia fotocatalítica entre las heteroestructuras y aún poseía una eficiencia de degradación del 77,8% después de cuatro ciclos sucesivos. El rendimiento fotocatalítico eficiente de Ag 3 PO 4 El fotocatalizador / T-ZnOw podría atribuirse a la respuesta mejorada a la luz visible. El Ag 3 PO 4 El fotocatalizador / T-ZnOw-2 también mostró una buena estabilidad. La investigación del efecto de diferentes eliminadores sobre la eficiencia de degradación de RhB demostró que ∙ OH y ∙ O 2 - fueron las especies principalmente activas. Se propuso un posible mecanismo de la vía de fotodegradación de RhB. Ag 3 PO 4 / T-ZnOw puede ser uno de los fotocatalizadores potenciales para su uso en el tratamiento de contaminantes del agua.
Disponibilidad de datos y materiales
Todos los datos generados o analizados durante este estudio se incluyen en este artículo publicado.
Abreviaturas
- T-ZnOw:
-
Bigote de ZnO similar a un tetrapodo
- RhB:
-
Rodamina B
- BQ:
-
Benzoquinona
- IPA:
-
Alcohol isopropílico
- EDTA-2Na:
-
Sal disódica del ácido etilendiaminotetraacético
- XRD:
-
Difracción de rayos X
- SEM:
-
Microscopía electrónica de barrido
- EDS:
-
Espectroscopía de rayos X de energía dispersiva
- TEM:
-
Microscopía electrónica de transmisión
- HRTEM:
-
Microscopía electrónica de transmisión de alta resolución
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- BE:
-
Vinculando energías
- DRS:
-
Espectros de reflectancia difusa UV-Vis
- PL:
-
Fotoluminiscencia
Nanomateriales
- Preparación y actividad de hidrogenación catalítica mejorada de nanopartículas de Sb / Palygorskita (PAL)
- Síntesis hidrotermal de nanopartículas de In2O3, gemelos híbridos, discos hexagonales, heteroestructuras de ZnO para mejorar las actividades fotocatalíticas y la estabilidad
- Preparación y rendimiento fotocatalítico de fotocatalizadores LiNb3O8 de estructura hueca
- Un nuevo fotocatalizador de heterounión Bi4Ti3O12 / Ag3PO4 con rendimiento fotocatalítico mejorado
- Efectos sinérgicos de nanopartículas de Ag / BiV1-xMoxO4 con actividad fotocatalítica mejorada
- Síntesis en un solo recipiente de nanoplacas de Cu2ZnSnSe4 y su actividad fotocatalítica impulsada por la luz visible
- Fabricación, caracterización y actividad biológica de sistemas de nanoportación de avermectina con diferentes tamaños de partículas
- Síntesis sonoquímica de un solo paso y propiedades fotocatalíticas fáciles de compuestos de puntos cuánticos de grafeno / Ag3PO4
- Fabricación y caracterización de nanoclips de ZnO mediante el proceso mediado por poliol
- Fabricación y propiedad fotocatalítica de nuevos nanocompuestos SrTiO3 / Bi5O7I
- Propiedades de las nanopartículas de óxido de zinc y su actividad contra los microbios



