Fabricación y caracterización de óxido de grafeno funcionalizado con taurina con 5-fluorouracilo como sistemas de administración de fármacos contra el cáncer
Resumen
Recientemente, los sistemas de nanoportadores para medicamentos contra el cáncer, especialmente los sistemas de administración de medicamentos basados en GO, se han convertido en una bendición para los pacientes con cáncer. En este estudio, elegimos Tau para funcionalizar la superficie GO para mejorar su biocompatibilidad. En primer lugar, el GO a nanoescala se sintetizó mediante el método Hummer modificado y el método de extracción ultrasónica. El portador de óxido de grafeno modificado con taurina (Tau-GO) se sintetizó por método químico para obtener Tau-GO que tiene una buena dispersabilidad y estabilidad en agua, con un potencial zeta de -38,8 mV y un tamaño de partícula de 242 nm. Con base en los criterios de evaluación de la eficiencia de encapsulación, se determinó la formulación óptima para combinar Tau-GO y 5-FU mediante enlace no covalente. El 5-FU-Tau-GO fue más estable en un ambiente neutro que en un ambiente ácido, y con una cierta respuesta de PH y un efecto de liberación sostenida. In vivo, comparamos las administraciones oral e intravenosa de 5-FU y 5-FU-Tau-GO, respectivamente, utilizando pruebas farmacocinéticas y parámetros relacionados y demostramos que la administración oral o intravenosa de 5-FU-Tau-GO prolonga el tiempo de acción de 5 -FU en el organismo y mejora su biodisponibilidad. Además, la inhibición de las células HepG2 que se midió mediante el ensayo MTT, mostró que el IC 50 valor de 5-FU fue 196 ± 8,73 μg / ml, y el IC 50 El valor de 5-FU-Tau-GO fue de 65,2 ± 0,7 μg / ml, lo que indica que 5- FU-Tau-GO es más potente contra las células HepG2 y tiene un efecto inhibidor más fuerte sobre las células cancerosas. El efecto sobre la morfología celular que se midió usando la tinción AO / EB también mostró que el 5-FU-Tau-GO no solo alteraba las células, sino que también inducía significativamente la apoptosis en comparación con el 5-FU. También verificamos mediante un diseño asistido por computadora que Tau-GO puede unirse mejor al 5-FU que al GO sin modificar, y que el sistema 5-FU-Tau-GO formado es más estable y propicio para la transferencia y liberación de 5- FU in vivo.
Introducción
La quimioterapia sigue siendo un método común que se utiliza en el tratamiento de varios cánceres [1]. Un obstáculo importante de la mayoría de los agentes quimioterapéuticos es su incapacidad para penetrar en los tejidos tumorales, a concentraciones eficaces, o sus efectos secundarios no deseados en los tejidos normales [2]. Por lo tanto, los científicos han concentrado sus esfuerzos en desarrollar un potente sistema de administración de fármacos que pueda lograr la tasa controlada de liberación de fármacos en los tejidos tumorales para garantizar una administración y una terapia efectivas.
Se han desarrollado muchos materiales nanométricos, incluidos liposomas [3], polímeros [4], nanopartículas [5], dendrímeros [6], micelas [7] y óxido de grafeno [8, 9] para la administración de diversos fármacos. Entre estos nanomateriales, el óxido de grafeno (GO) es un nuevo nanomaterial de carbono que se exfolia químicamente a partir del grafito oxidado y exhibe varias propiedades físicas y químicas fascinantes, como abundantes grupos funcionales, gran área de superficie específica, alta cantidad de carga de fármaco y excelente dispersión. capacidad en agua [10,11,12]. Además, la mayoría de los resultados experimentales in vitro mostraron que una concentración baja de GO podría usarse como sustrato para el crecimiento celular y para activar las células inmunes. Por lo tanto, GO se ha utilizado ampliamente en el diagnóstico de enfermedades [13], la obtención de imágenes y el seguimiento de células cancerosas [14], la terapia fototérmica del cáncer [15], la ingeniería de tejidos [16], la administración de fármacos dirigida [17] y, especialmente, como un anti portador de fármacos tumorales [18, 19]. Sin embargo, varios grupos de investigación han informado que una concentración alta de GO tiene efectos citotóxicos obvios en estudios preclínicos y clínicos. El mecanismo por el cual la GO produce efectos tóxicos in vivo es a través del estrés oxidativo y la sobreproducción de especies reactivas de oxígeno intracelulares, que inducen la apoptosis celular y provocan inflamación grave, edema pulmonar y formación de granulomas [20]. Por lo tanto, es de vital importancia resolver el problema de la toxicidad del GO.
Según se informa, la funcionalización de enlaces covalentes o no covalentes puede reducir la fuerte interacción hidrofóbica entre GO y las células. Así lo demostraron varios estudios que demostraron que la funcionalización de GO mejora su biocompatibilidad y casi elimina su toxicidad in vivo e in vitro. Yang et al. estudiaron, por primera vez, la biodistribución a largo plazo de PEG-GO conjugado covalentemente en ratones utilizando un método de radiomarcaje, y los resultados mostraron que PEG-GO podría excretarse gradualmente de los ratones, probablemente en orina y heces [21]. Zhang y col. comparó el GO funcionalizado con DEX con el GO y descubrió que el GO-DEX podía reducir notablemente la toxicidad celular y eliminarse principalmente de los ratones en una semana [22]. Además, la unión no covalente de GO a pluronic F127 da como resultado una solubilidad benigna y estabilidad en condiciones fisiológicas, y una baja toxicidad [23]. Aunque se han utilizado varios polímeros o moléculas para funcionalizar GO, se han logrado resultados significativos en este campo. Sin embargo, aún se necesitan esfuerzos para desarrollar métodos simples para construir un buen portador de medicamentos biocompatibles basados en GO.
La taurina (Tau) es un aminoácido semi-esencial con buena estabilidad y solubilidad en agua. Tau puede prevenir enfermedades cardiovasculares y cerebrovasculares, mantener la función visual, proteger las células y regular la inmunidad. Numerosos estudios han propuesto que Tau tiene propiedades antitumorales a través de su regulación positiva o negativa de los factores de expresión que juegan un papel importante en varios cánceres, incluidos los de pulmón, estómago, colorrectal y mama [24]. Por tanto, el GO funcionalizado con Tau puede ejercer un papel superior como portador de fármacos antitumorales. En este artículo, utilizamos, por primera vez, GO funcionalizado con Tau covalente como nanoportador y evaluamos su citotoxicidad in vitro. Además, se utilizó 5-fluorouracilo (5-FU) como fármaco contra el cáncer que se cargó de forma no covalente en la superficie de Tau-GO para construir un sistema de administración de fármacos. El 5-FU-Tau-GO no solo podría reducir los efectos secundarios en los tejidos normales, sino también mejorar la biodisponibilidad del fármaco. En consecuencia, Tau-GO se desarrolló con éxito como un nanomaterial novedoso basado en GO que puede tener importantes aplicaciones biomédicas en el futuro.
Experimentos y métodos
Materiales
El polvo de grafito, la solución salina tamponada con fosfato (PBS) y el dimetilsulfóxido (DMSO) se adquirieron de Tianjin Laibo Chemical Co., Ltd .; Carbodiimida (EDC), N-hidroxisuccinimida (NHS), ácido clorhídrico (HCl) y peróxido de hidrógeno (H 2 O 2 30%) se adquirieron de Shandong Yuwang Industrial Co., Ltd .; Se adquirieron taurina (Tau), 5-fluorouracilo (5-FU), células de hepatoma humano (HepG2), solución de penicilina-estreptomicina y suero bovino fetal (FBS) de Dalian Meilun Biotechnology Co., Ltd .; ácido sulfúrico (H 2 SO 4 98%) y permanganato de potasio (KMnO 4 ) se adquirieron de Nanjing Chemical Reagent Co., Ltd .; nitrato de sodio (NaNO 3 ) y dodecilsulfato de sodio (SDS-Na) se adquirieron de Shanghai Jinjinle Industrial Co., Ltd .; El MTT se adquirió de Sigma-Aldrich, Inc; DMEM se adquirió de HyClone, Inc; Las ratas se compraron en el Centro de Animales Experimentales de Benxi Changsheng. Todos los demás reactivos y productos químicos eran analíticamente puros y estaban disponibles comercialmente.
Síntesis de GO
El GO se preparó a partir de polvo de grafito según el método de Hummer modificado. En primer lugar, se agregaron 168 mL de ácido sulfúrico al 98% a lo largo de la pared del matraz de un matraz de tres bocas que se colocó en un baño de hielo con termómetro, y se agregaron 5 g de grafito y 4 g de nitrato de sodio cuando la temperatura alcanzó los 5 ° C. Luego, se agregaron lentamente 22,5 g de permanganato de potasio en lotes durante 1 hora y la temperatura se mantuvo por debajo de 5 ° C. Después de eso, el matraz de tres bocas se transfirió a un baño de aceite y la mezcla obtenida se hizo reaccionar a 35 ° C durante 30 min, luego se aumentó la temperatura a 65 ° C y la reacción se agitó durante 30 min. Después de este paso, la temperatura se aumentó a 85 ° C y la mezcla se hizo reaccionar adicionalmente durante 1 h para obtener una pasta de color marrón púrpura. Esta mezcla se dejó reposar a temperatura ambiente durante 1 semana, se transfirió a un vaso de precipitados con 700 ml de agua caliente y se añadió gota a gota el peróxido de hidrógeno al 30% hasta que se volvió marrón amarillento. La mezcla se centrifugó a 10.000 rpm, se lavó con agua caliente y este proceso se repitió varias veces hasta que el pH del sobrenadante fue de 7,0. Finalmente, el producto se secó en un liofilizador al vacío y se obtuvo el nano GO.
Síntesis de Tau-GO
Se disolvieron 50 mg de GO pesados con precisión en 50 ml de agua destilada y se añadieron 150 mg de EDC y 100 mg de NHS para activar el GO mediante ultrasonidos en un baño de agua helada durante 20 min. A continuación, se añadieron lentamente (gota a gota) 10 ml de solución acuosa de Tau (0,1 g / ml) a la solución acuosa de GO preparada, y el pH se ajustó a 6–7 con HCl y se agitó continuamente durante 24 h en la habitación en la oscuridad. El producto se recogió por centrifugación a 5000 rpm durante 10 min y se lavó 3 veces con agua destilada. El Tau-GO se recogió después de la liofilización.
Carga de 5-FU
Se sometió a ultrasonidos una cantidad de 20 ml de solución de Tau-GO durante 2 h. Se disolvió una cantidad pesada con precisión de 5-FU en una cantidad apropiada de agua destilada y se añadió lentamente gota a gota a la solución de Tau-GO preparada con agitación a temperatura ambiente, luego se sonicó a 30 ° C en la oscuridad durante 1,5 h. Los productos se centrifugaron a 5000 rpm durante 10 min a 4 ° C. El sedimento inferior se lavó con 20 mL de agua destilada y se centrifugó (5000 rpm durante 10 min a 4 ° C) y el proceso se repitió 3 veces. La capa inferior se liofilizó, el sobrenadante se colocó en un vaso de precipitados, se pesó el volumen y se determinó la concentración de 5-FU mediante una HPLC 1200 (Agilent, EE. UU.). Las condiciones de detección fueron las siguientes:columna cromatográfica:C18 (4,6 x 250 nm, 5 µm); temperatura de la columna:25 ° C; fase móvil:0,1% KH 2 PO 4 solución con pH 5,5; caudal:1,0 ml / min; volumen de inyección:20μL; y longitud de onda de medición:265 nm. La relación de encapsulación (EE) y la eficiencia de carga de fármaco (LE) se obtuvieron mediante la siguiente fórmula:
$$ \ begin {alineado} {\ text {EE}} \ left (\% \ right) &=\ frac {{M_ {1} - C_ {1} \ times L_ {1}}} {{M_ {1 }}} \ times 100 \% \\ {\ text {LE}} \ left (\% \ right) &=\ frac {{M_ {1} - C_ {1} \ times L_ {1}}} {{ 20C_ {0} + M_ {1} - C_ {1} \ times L_ {1}}} \ times 100 \% \\ \ end {alineado} $$La dosis total de 5-FU se registró como M 1 , la concentración y el volumen de 5-FU libre se registraron como C 1 y L 1 , y la concentración de portador se registró como C 0 .
Caracterización
Para caracterizar el nanocompuesto preparado, se escanearon espectros infrarrojos por transformada de Fourier (FT-IR) de 4000 a 400 cm −1 en el espectrómetro IRAffinity-1 (Shimadzu, Japón) para confirmar las interacciones. Los espectros de absorción UV-vis se registraron en un espectrofotómetro de barrido UV-3600 (Shimadzu, Japón). Las muestras se disolvieron en agua destilada y los tamaños de partícula, los potenciales zeta y los valores de PDI se obtuvieron en un instrumento Nano-ZS 90 Nano (Malvern, Reino Unido). Las morfologías de las muestras se analizaron utilizando un microscopio electrónico de transmisión (TEM) JEM-2100 (JEOL, Japón). Los análisis termogravimétricos (TGA) se llevaron a cabo usando un analizador termogravimétrico (NETZSCH, Alemania) a una velocidad de calentamiento de 10 ° C / min de 0 a 800 ° C bajo una atmósfera de nitrógeno. La medición de XRD de las muestras se llevó a cabo mediante un difractómetro de rayos X (Bruker, Alemania) con una radiación de cobre CuKα ( λ =1.5406 Å) en un gran angular con un ángulo de 2θ. Las mediciones de XPS se realizaron utilizando una sonda Omicron ESCA con una radiación de Al monocromática (Thermo, América).
Liberación de fármacos in vitro
La liberación del fármaco in vitro se llevó a cabo a pH 1,2 (entornos gástricos simulados), pH 6,5 (entorno celular de cáncer de hígado simulado) y pH 7,4 (entorno fisiológico simulado) a 37 ° C (temperatura corporal simulada), respectivamente. En resumen, se colocaron 15 mg de 5-FU-Tau-GO en una membrana de diálisis, se sumergieron en 50 ml de soluciones tampón que contenían SDS-Na al 0,1% con pH de 1,2, 6,5 y 7,4. Todas las muestras se colocaron en un baño de agua con agitación continua a una velocidad de 100 rpm y a una temperatura de 37 ° C. En puntos de tiempo predeterminados (0 min, 5 min, 10 min, 20 min, 30 min, 1 h, 1,5 h, 2 h, 2,5 h, 3 h, 4 h, 8 h, 12 h, 24 h, 48 hy 72 h), se tomó 1 mL de cada muestra y se reemplazó con 1 mL de solución tampón fresca que contenía SDS-Na al 0,1% para mantener el mismo volumen de medio de liberación. El medio liberado se centrifugó y analizó usando 1200 HPLC.
Estudios de citotoxicidad in vitro
Ensayo MTT
El ensayo MTT se utilizó para evaluar la citotoxicidad de 5-FU, Tau-GO y 5-FU-Tau-GO. Brevemente, las células HepG2 de hepatoma humano se cultivaron en medio DEME, complementado con FBS al 10% y antibióticos al 1% (solución de penicilina-estreptomicina) a 37 ° C en una atmósfera humidificada de CO 2 al 5%. . Las células se sembraron en una placa de 96 pocillos a una densidad de 5 × 10 3 células por pocillo que contienen 100 μL de medio DEME, suplementado con FBS y antibióticos. La placa se colocó durante 24 h en una cámara humidificada a 37 ° C que contenía 5% de CO 2 . Después de eso, el medio de crecimiento se retiró y se volvió a llenar con 100 μL de medio fresco que contenía varias concentraciones (5, 10, 20, 40, 60, 80 y 100 μg / ml) de 5-FU, Tau-GO, 5-FU- Tau-GO, respectivamente. Después de 24 h de incubación, las células se trataron con 20 μL de solución de MTT y se incubaron durante 4 h. A continuación, se aspiró el medio y se disolvieron los cristales de formazán en 150 µl de DMSO. Finalmente, las placas de pocillos se agitaron a 37 ° C durante 15 min en un oscilador de temperatura constante. La densidad óptica (DO) de cada muestra se midió a 570 nm usando un lector de microplacas. Los experimentos se realizaron por triplicado. La tasa de inhibición celular se calculó a partir de los resultados utilizando la siguiente fórmula:
$$ {\ text {Cell}} \; {\ text {inhibition}} \; {\ text {rate}} =\ frac {{{\ text {OD}} _ {{{\ text {control}}} } - {\ text {OD}} _ {{{\ text {tratado}}}}}} {{{\ text {OD}} _ {{{\ text {control}}}}}} \ veces 100 \ % $$donde OD control es la absorbancia obtenida por las células de control no tratadas, DO tratadas es la absorbancia obtenida por las células tratadas.
Ensayo de tinción AO / EB
Se utilizó doble tinción AO / EB para evaluar los cambios morfológicos de las células que se trataron con 5-FU, Tau-GO y 5-FU-Tau-GO. Brevemente, las células HepG2 en una fase de crecimiento logarítmica se sembraron en una placa de 6 pocillos a una densidad de 10.000 células por pocillo y se cultivaron en una incubadora a 37 ° C y bajo un 5% de CO 2 atmósfera. Después de 24 h, las células se trataron con una concentración fija de 5-FU, Tau-GO o 5-FU-Tau-GO, y se incubaron adicionalmente durante 24 h. Se eliminó el medio de cada pocillo y las células se lavaron dos veces con PBS. A continuación, se añadió 1 mL de PBS suplementado con 40 μL de tintes fluorescentes (se mezclaron 1 mg / mL de AO y 1 mg / mL de EB en una proporción de 1:1) a cada pocillo y se incubaron durante 10 min sin luz. Las células teñidas se observaron bajo un microscopio de fluorescencia y las imágenes se tomaron al azar.
Estudio farmacocinético
Todos los experimentos con animales se realizaron de acuerdo con las políticas y principios formulados por el Comité de Protección y Ética Animal. Un total de 24 ratas SD macho, con pesos corporales de 230-270 g, se mantuvieron en ayunas durante 12 horas y se dividieron al azar en 4 grupos antes de la administración del fármaco. Los grupos A y B se inyectaron por vía intravenosa con soluciones de 5-FU y 5-FU-Tau-GO, y los grupos C y D recibieron soluciones orales de 5-FU y 5-FU-Tau-GO, respectivamente. Todos los grupos recibieron una dosis de 20 mg / kg. Después de la administración del fármaco, se recogieron muestras de sangre (aproximadamente 0,5 ml) en tubos de anticoagulación en momentos determinados (15 min, 1 h, 2 h, 4 h, 6 h, 8 h, 12 h, 16 h, 24 hy 48 h). h). Las muestras de plasma se separaron por centrifugación a 7500 rpm y a 4 ° C durante 10 min. Luego, 200 μL de plasma y 50 mg (NH 4 ) 2 SO 4 se combinaron en un tubo (10 μL de 40 μg / mL de solución estándar interna de 5-BrU, se secaron con nitrógeno en un baño de agua a 40 ° C, se agitaron con vórtex durante 5 min y se centrifugaron a 10800 rpm durante 3 min. A continuación, se se adicionó con 900 μL de solución de acetato de etilo / isopropanol (85:15, v / v), se agitó con vórtex durante 3 min y se centrifugó a 10800 rpm durante 15 min. El sobrenadante se retiró y se secó con nitrógeno, se agregaron 100 μL de fase móvil y se El tubo se agitó durante 1 min. Finalmente, la solución resultante recogida del sobrenadante se midió mediante 1200 HPLC.
Simulación de dinámica molecular
La simulación de dinámica molecular se utiliza principalmente para analizar la fuerza de interacción entre el fármaco y el portador y el comportamiento de difusión del fármaco. La estructura química del 5-FU se construyó usando Chemdraw of chem office 2014, y las estructuras de Tau-GO y GO se llevaron a cabo en el módulo Polymer and Molecule Builders utilizando el software de simulación molecular Materials Studio (versión 7.0, Accelrys Inc. , EE.UU). Todos los compuestos construidos se optimizaron geométricamente bajo el campo de fuerza COMPASS II, y se seleccionó la conformación con la energía más baja como la conformación estable. Se realizó un equilibrado NVT de 10 ps para cada sistema. La simulación se realizó con 100 ps MD para obtener una estructura equilibrada a 298 K y 101,325 kPa con un tamaño de paso de 1 fs. Finalmente, se obtuvo el desplazamiento cuadrático medio (MSD) y la densidad de energía cohesiva (CED) para cada sistema, y el coeficiente de difusión (D) se dio mediante la siguiente fórmula:
$$ D =\ frac {1} {2d} \ mathop {\ lim} \ limits _ {\ tau \ to \ infty} \ frac {{\ text {d}}} {{{\ text {d}} \ tau }}\izquierda izquierda. {r \ overrightarrow {\ left (t \ right)} - r \ overrightarrow {\ left (0 \ right)}} \ right]} \ right. ^ {2} $$donde el d es la dimensión del sistema, \ (r \ overrightarrow {\ left (t \ right)} \) y \ (r \ overrightarrow {\ left (0 \ right)} \) son el vector de posición de la molécula del fármaco en el tiempo t y 0, respectivamente, \ (\ left [{\ left. {r \ overrightarrow {\ left (t \ right)} - r \ overrightarrow {\ left (0 \ right)}} \ right]} \ right. ^ { 2} \) son las siglas de MSD.
Resultados y discusión
Caracterización
El conjugado Tau-GO se fabricó mediante un enlace amida de GO y Tau. La síntesis exitosa del nanocompuesto fue validada por espectros FT-IR (Fig. 1). La presencia de las funcionalidades de oxígeno en GO fue confirmada por los picos de absorbancia en –OH (~ 3405 cm −1 ), C =O (1723 cm −1 ), C =C (1628 cm −1 ) y C – OH (1391 cm −1 ). Estos resultados demostraron que la preparación de GO fue exitosa (Fig. 1a) [25]. Además de algunos picos característicos de GO, los nuevos picos a 1638 cm −1 y 3427 cm −1 correspondía al grupo amida, y los 1164 cm −1 y 1085 cm −1 correspondió a –SO. El espectro Tau-GO indicó claramente que Tau se ha funcionalizado en la superficie GO (Fig. 1b). En la Fig. 2b, el pico característico de –SO 3 a 1164 cm −1 fue inundado por la acción de los enlaces de hidrógeno y no era visible en los espectros FT-IR. Por lo tanto, 5-FU se cargó con éxito en el Tau-GO.
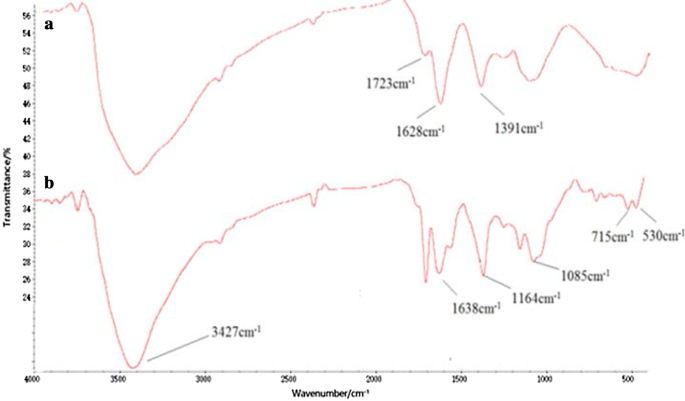
Espectros FT-IR de GO ( a ) y Tau-GO ( b )
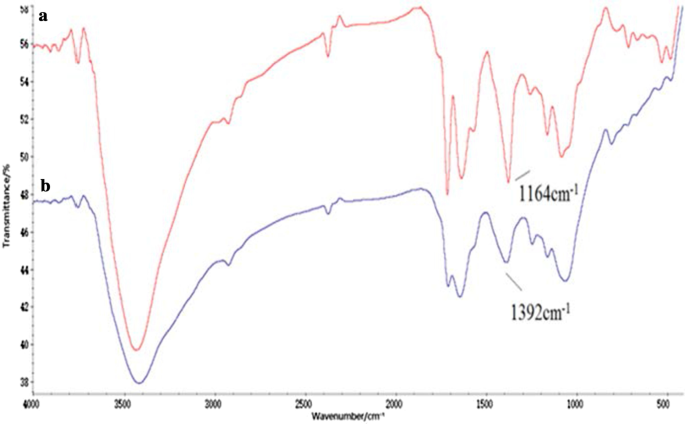
Espectros FT-IR de Tau-GO ( a ) y 5-FU-Tau-GO ( b )
Los espectros de absorción GO UV-Vis se muestran en la Fig. 3. El pico de absorción obvio a 234 nm se atribuyó a la transición π – π * de los enlaces de grafeno C =C. Además, el pico del hombro de 300 nm se atribuyó a la transición n-π * de los enlaces C =O del óxido de grafeno en el grupo carboxilo o carbonilo. Se demostró que los dos picos de absorción característicos eran preparaciones satisfactorias de GO.
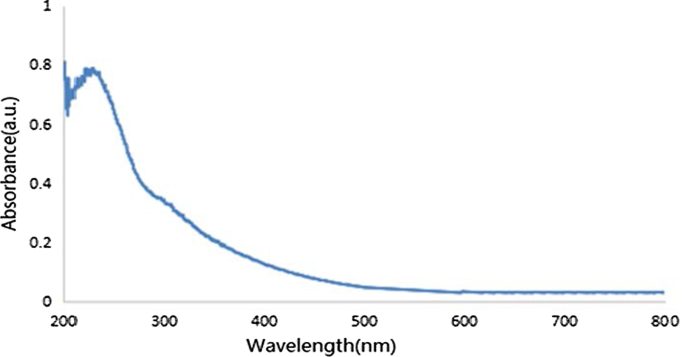
Espectros UV de GO
El tamaño de GO, Tau-GO y 5-FU-Tau-GO se muestran en la Fig. 4. El potencial zeta de GO, Tau-GO y 5-FU-Tau-GO se muestran en la Fig. 5. El tamaño de las hojas de GO eran de aproximadamente 221 nm y el valor de PDI era de aproximadamente 0,188, lo que indica que el GO preparado tiene una distribución uniforme y una buena estabilidad. El potencial zeta fue de aproximadamente -33,3 mV, lo que indica que la carga negativa se debe principalmente a la presencia de muchos grupos que contienen oxígeno en la superficie. Cuando el GO se modificó con Tau a través de un enlace amida, los grupos amino reemplazaron algunos de los grupos carboxilo y el –SO 3 tenía una capacidad de ionización más fuerte en solución, el potencial zeta disminuyó y se convirtió en - 38,8 mV. El tamaño y los valores de PDI de Tau-GO fueron aproximadamente 242 nm y 0,190. A continuación, se cargó 5-FU en Tau-GO mediante un enlace no covalente. El potencial zeta fue de aproximadamente - 26,7 mV y el valor absoluto fue superior a 20 mV. Además, el tamaño y los valores de PDI de 5-FU-Tau-GO fueron aproximadamente 264 nm y 0.182, esto indica que la repulsión electrostática entre partículas es grande, lo que no es fácil de causar agregación o precipitación, y que Tau tiene buena solubilidad en agua. , GO también tiene buena solubilidad en agua porque su superficie está modificada por grupos funcionales que contienen oxígeno. El uso del portador Tau-GO para cargar 5-FU mejora significativamente la solubilidad en agua del 5-FU, de modo que el 5-FU-Tau-GO se puede dispersar de manera estable en una solución acuosa.
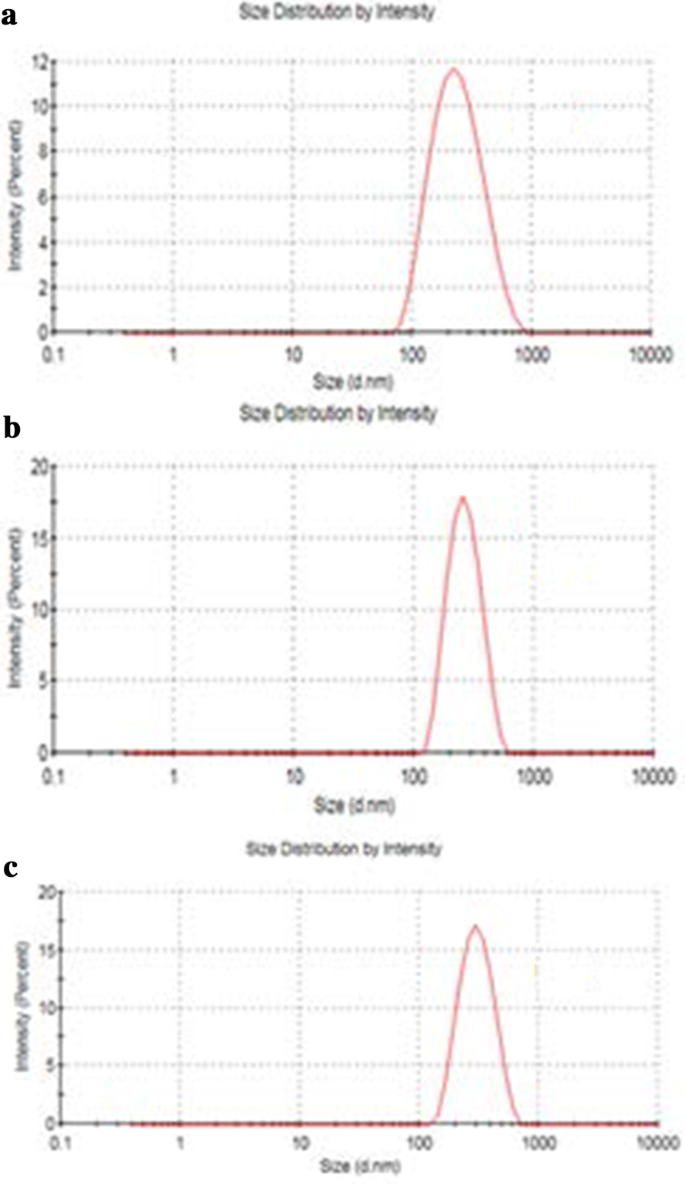
Tamaño de partícula de GO ( a ), Tau-GO ( b ) y 5-FU-Tau-GO ( c )
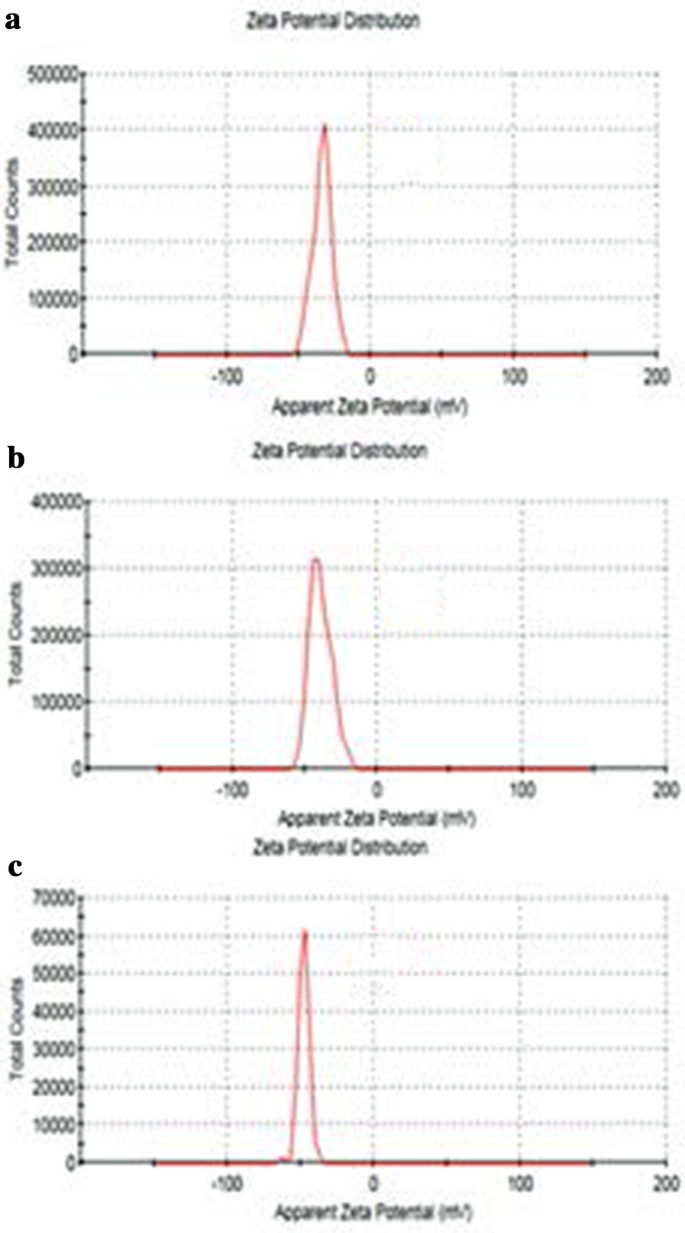
Potenciales Zeta de GO ( a ), Tau-GO ( b ) y 5-FU-Tau-GO ( c )
Las morfologías de GO, Tau-GO y 5-FU-Tau-GO se caracterizaron por TEM (Fig. 6). El GO es una estructura plana con arrugas en la superficie, lo que ilustra que es una estructura bidimensional plana (Fig. 6a). En comparación con GO, el tamaño de Tau-GO aumentó ligeramente, pero aún mostraba una estructura laminar (Fig. 6b). La imagen de 5-FU-Tau-GO mostró que los materiales no se agregaron ni cambiaron con la estructura laminar inicial de GO permaneciendo intacta (Fig. 6c). En consecuencia, Tau-GO y 5-FU-Tau-GO tuvieron una buena estabilidad.

TEM de GO ( a ), Tau-GO ( b ) y 5-FU-Tau-GO ( c )
Se utilizó análisis termogravimétrico para cuantificar las composiciones de los composites. Las curvas de TGA de GO y Tau-GO se muestran en la Fig. 7. GO y Tau-GO tienen masas remanentes de 39,73% y 34,22% en una atmósfera de nitrógeno de 800 ° C. Por lo tanto, al comparar los valores de cambio de peso, se determinó que el contenido de Tau en Tau-GO era aproximadamente del 13%.
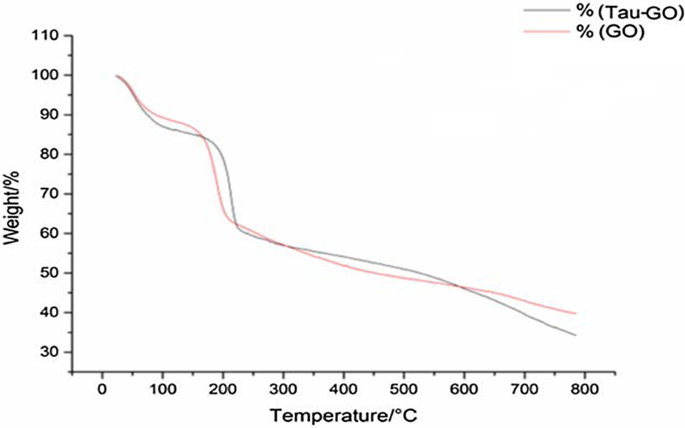
ETIQUETA de GO y Tau-GO
Los patrones XRD de Tau, GO y Tau-GO se muestran en la Fig. 8. El pico característico de GO se puede observar a 10.7 ° del valor 2θ, lo que confirma la formación de GO con oxidación completa para un fuerte proceso de oxidación química y exfoliación. . Después de funcionalizado con Tau en la superficie GO, el patrón de difracción del pico disminuyó ligeramente a un valor de 2θ 8,2. Esto significa que Tau ha funcionalizado con éxito GO.
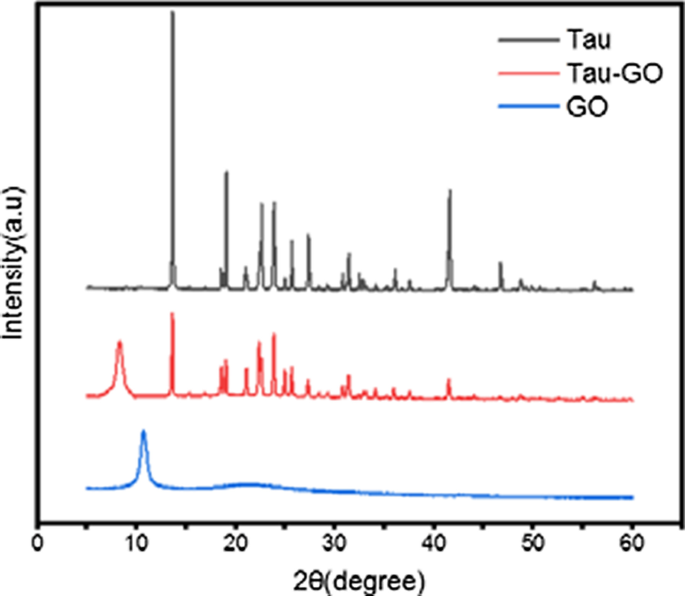
Patrones XRD de Tau, Tau-GO y GO
Los espectros C1s XPS de GO y Tau-GO se muestran en la Fig. 9. Los espectros C1s XPS de GO indican que hay un grado considerable de oxidación, con la presencia de cuatro átomos de carbono correspondientes a diferentes grupos funcionales. Los espectros C1s XPS de Tau-GO también exhiben estos mismos átomos de carbono. Además, la aparición de picos de componentes relacionados con el enlace C-N se atribuyó a los grupos amino, grupos amida. Estos resultados también indican que Tau funcionalizó con éxito GO.
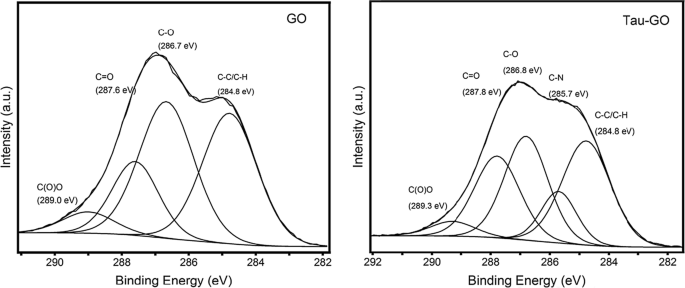
Patrones C1s XPS de GO y Tau-GO
Comportamientos de carga y liberación de medicamentos
El 5-FU se adsorbió en el nanoportador Tau-GO mediante interacciones no covalentes. La curva de calibración de 5-FU fue y =62,135 x + 21.873 ( r =0,9999), y el intervalo fue de 6,5 ~ 250 µg / ml. La relación de encapsulación (EE) y la eficiencia de carga de fármaco (LE) se determinaron mediante concentraciones de fármaco no unido para evaluar el rendimiento de carga de fármaco. Los resultados mostraron que EE aumentó con el aumento en la concentración de fármaco y que el valor más alto de EE fue 83,2%. Según la fórmula, el LE fue del 33,7%, es decir, 508,52 μg de 5-FU pueden adsorberse en 1 mg de Tau-GO. Por lo tanto, Tau-GO es un portador de fármacos prometedor que puede lograr una gran carga de fármacos. Los posibles mecanismos de la alta capacidad de carga del 5-FU sobre el Tau-GO se pueden resumir con las siguientes explicaciones:en primer lugar, Tau se utiliza para funcionalizar el GO e introducir grupos funcionales activos (–SO 3 ). –SO 3 tiene una fuerte capacidad de ionización en la solución, lo que reduce la aglomeración entre GO y facilita la carga de 5-FU en Tau-GO. En segundo lugar, el potencial Zeta de 5-FU-Tau-GO es 12,1 mV diferente al de Tau-GO, lo que indica que 5-FU se carga en la superficie de Tau-GO, y la interacción electrostática juega un papel importante en la carga de 5-FU. Por último, existen muchas formas de enlaces de hidrógeno entre el 5-FU y el portador Tau-GO, incluidos –COOH en Tau-GO y –NH– en 5-FU, –COOH en Tau-GO y-en 5-FU C =O , –OH en Tau-GO y –NH– en 5-FU, –OH en Tau-GO y –C =O en 5-FU, –COOH y 5-FU en Tau-GO –F en Tau-GO, - COOH en Tau-GO y –F en 5-FU, estos enlaces de hidrógeno hacen que 5-FU-Tau-GO sea estable en solución.
La liberación acumulada in vitro de 5-FU del 5-FU-Tau-GO, a una temperatura de 37 ° C en una solución de PBS de pH 1,2, 6,5 y 7,4 (simula el entorno gástrico, el entorno de las células de cáncer de hígado y el entorno fisiológico, respectivamente) se muestra en la Fig. 10. Se encuentra que el comportamiento de liberación de 5-FU se vio afectado por el valor de pH del medio ambiente. En un tampón de pH 7,4, la liberación del fármaco fue lenta y continua, y la cantidad total liberada de fármaco fue aproximadamente del 70,84% después de 72 h. Por el contrario, la cantidad liberada de fármaco a pH 7,4 fue significativamente menor que a pH 1,2 y pH 6,5 en el mismo momento. La carga total de fármaco que se liberó del 5-FU-Tau-GO se pudo lograr a aproximadamente 90,29% y 85,75% ya pH 1,2 y pH 6,5, respectivamente. Se puede atribuir a las interacciones π-π y los enlaces de hidrógeno entre 5-FU y Tau-GO. Cuanto menor sea el valor de pH, mayor será el grado de protonación del enlace de hidrógeno. Por lo tanto, la fuerza del enlace de hidrógeno se controló mediante el valor del pH, lo que condujo a la liberación de 5-FU. Este sistema de administración de fármacos sensible al pH juega un papel importante en los fármacos antitumorales y puede lograr la liberación de los fármacos en la célula tumoral.
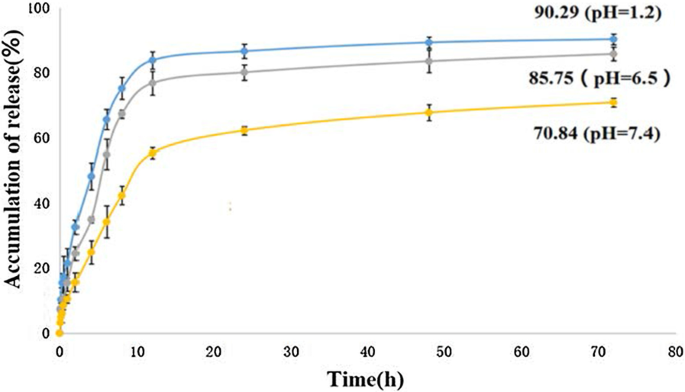
Curvas de liberación in vitro de 5-FU-Tau-GO en solución salina de fosfato a 37 ° C
Estudios de citotoxicidad in vitro
Para evaluar la toxicidad potencial y la eficacia de la terapia tumoral del nanoportador, se llevó a cabo la viabilidad celular in vitro en células HepG2 usando ensayos MTT (Fig. 11). El Tau-GO no mostró citotoxicidad significativa a diferentes concentraciones. Después de la carga de 5-FU, el 5-FU-Tau-GO mostró un efecto de inhibición obvio, y de manera dependiente de la dosis, por lo tanto, el nanoportador tenía la capacidad de administrar fármacos antitumorales. El IC 50 El valor de 5-FU-Tau-GO fue de 65,2 ± 0,7 μg / mL, que fue más tóxico que el 5-FU libre (196 ± 8,73 μg / mL). Esto puede deberse a la capacidad de la taurina para inducir la apoptosis en las células tumorales, mejorando así indirectamente el efecto inhibidor del 5-FU en las células. Además, se pudo ver en el experimento de liberación in vitro que el 5-FU cargado en el Tau-GO podría liberarse gradualmente en las células. Por lo tanto, el tiempo efectivo de 5-FU-Tau-GO en las células fue mayor que el del 5-FU libre y, por lo tanto, produjo una mejor inhibición.
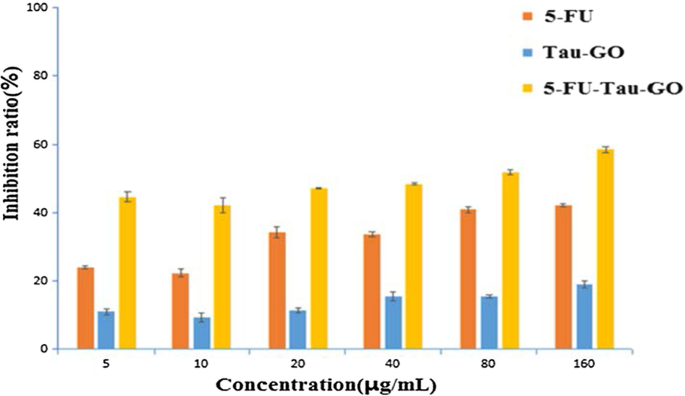
The viability of different concentrations of 5-FU, Tau-GO, and 5-FU-Tau-GO
AO fluorescent agent could emit green fluorescence when it passed through intact cell membranes and stained nuclei, while EB only marked the nucleus of damaged cells that emitted a red/orange fluorescence. The cells with early and late apoptosis presented greenish yellow or orange nuclei with the AO/EB stain, respectively. Therefore, AO/EB staining was performed to investigate whether the cells death was associated with apoptosis using characteristics of cell morphological changes. The results obtained from the AO/EB staining are presented in Fig. 12. Control cells were in spindle shape and with green nuclei. In the cell group that was cultured with Tau-GO alone, small parts of the nuclei were invaginated and with dark green or orange-red staining. Significant orange or red apoptotic cells with chromatin fragments and apoptotic bodies were observed in the 5-FU alone group. Compared with 5-FU, 5-FU-Tau-GO caused more damage to HepG2 cell morphology, which not only broke the cells, but also caused a large amount of apoptosis in cancer cells. As can be seen from the pictures, almost all the cells that were treated with 5-FU-Tau-GO, had morphological changes, a large number of cell debris and apoptotic bodies, indicating that the 5-FU-Tau-GO nano drug delivery system had a good killing effect on HepG2 cells.
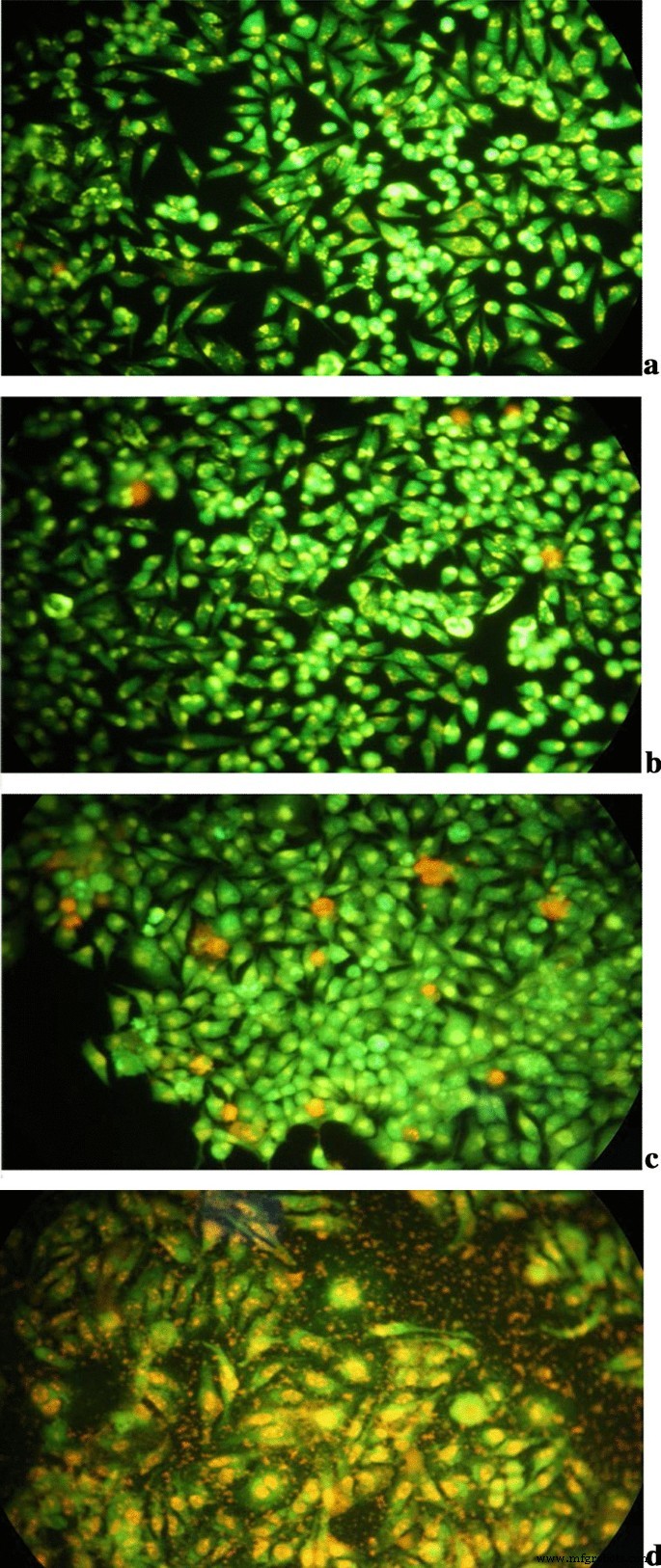
The AO/EB of control (a ), Tau-GO (b ), 5-FU (c ), and 5-FU-Tau-GO (d )
Pharmacokinetic Studies
The pharmacokinetic studies of 5-FU and 5-FU-Tau-GO were performed in SD rats. The profiles of 5-FU concentration in plasma vs. time, following oral administration, are presented in Fig. 13a. We found that the tendency of the two curves was similar, but the 5-FU plasma concentration from the 5-FU-Tau-GO nanocarrier was higher than that from the 5-FU alone and this was observed at each measured time point. Figure 13b shows the 5-FU in vivo release profiles via tail vein. The 5-FU-Tau-GO could achieve sustained drug release over 24 h, and the drug concentration gradually decreased in the first few hours, indicating that 5-FU was slowly released.
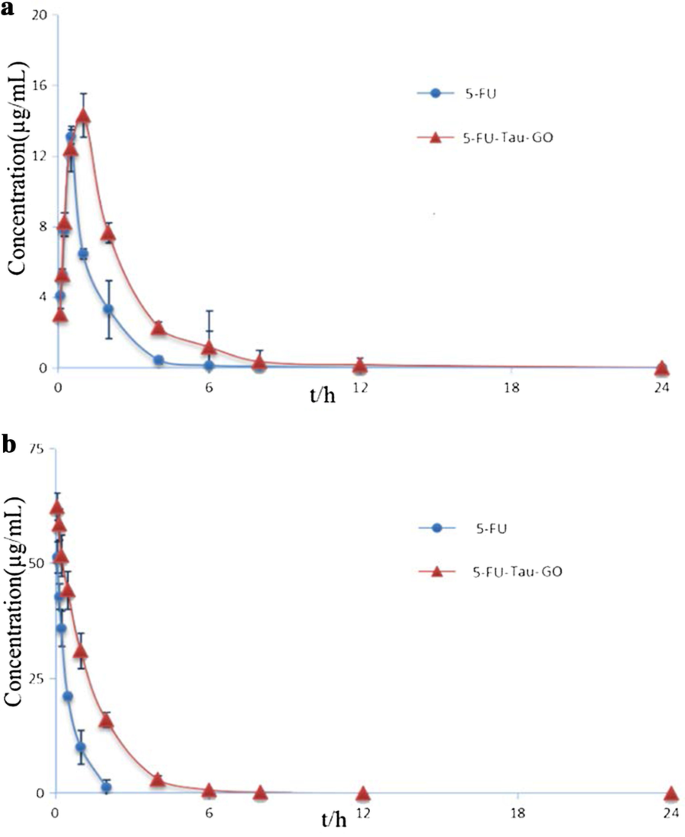
In vivo pharmacokinetic standard curves of 5-FU and 5-FU-Tau-GO through oral administration (a ). In vivo pharmacokinetic standard curve of 5-FU and 5-FU-Tau-GO through intravenous injection (b )
The two-compartment model was used to analyze the pharmacokinetic parameters of oral or intravenous administration in rats. The pharmacokinetic parameters are presented in Table 1. Compared with the 5-FU, the 5-FU-Tau-GO showed higher T1/2β that were 2.3 times by oral administration, and 3.0 times by intravenous injection, respectively. Moreover, the area under the concentration time curve (AUC0−t ) of 5-FU-Tau-GO nanocomplexes was roughy 2.1-fold higher through the oral administration, and 2.8-fold higher through intravenous injection when compared to that of the 5-FU solution, respectively. Therefore, we concluded that 5-FU-Tau-GO could significantly extend 5-FU retention time in vivo and improve bioavailability. In addition, the T1/2β of the 5-FU-Tau-GO nanocomplexes that were orally administered (1.67 ± 1.15 h), was longer than that of the intravenous injection (1.33 ± 0.64 h); however, the AUC0−t of oral administration (36.02 ± 1.83 mg/L*h) was lower than that of intravenous injection (96.50 ± 8.70 mg/L*h). These results might be due to two aspects:on the one hand, when administered by intravenous injection, the drug directly enters the blood system for circulation and without passing through the gastrointestinal barrier for redistribution; on the other hand, because 5-FU easily causes a certain damage to the gastrointestinal system, it may also affect the effective use of drugs in the body.
MD Simulations
The docking and molecular dynamics of unmodified GO, Tau-GO and 5-FU were simulated by molecular docking and molecular dynamics simulation. The molecular docking results of GO, Tau-GO and 5-FU are shown in Fig. 14, where it can be seen that the bond lengths of 5-FU and GO and Tau-GO are 3.66 Å and 2. 602 Å, respectively. Moreover, from the calculation results, the binding energies of 5-FU to GO and Tau-GO were 47.69 kcal/mol and 25.04 kcal/mol, respectively. These indicated that the binding force of Tau-GO and 5-FU was stronger than that of GO and 5-FU. This is due to Tau polar atoms, such as S and N, forming a stronger non-covalent bond with 5-FU, that makes the force between Tau-GO and 5-FU stronger.
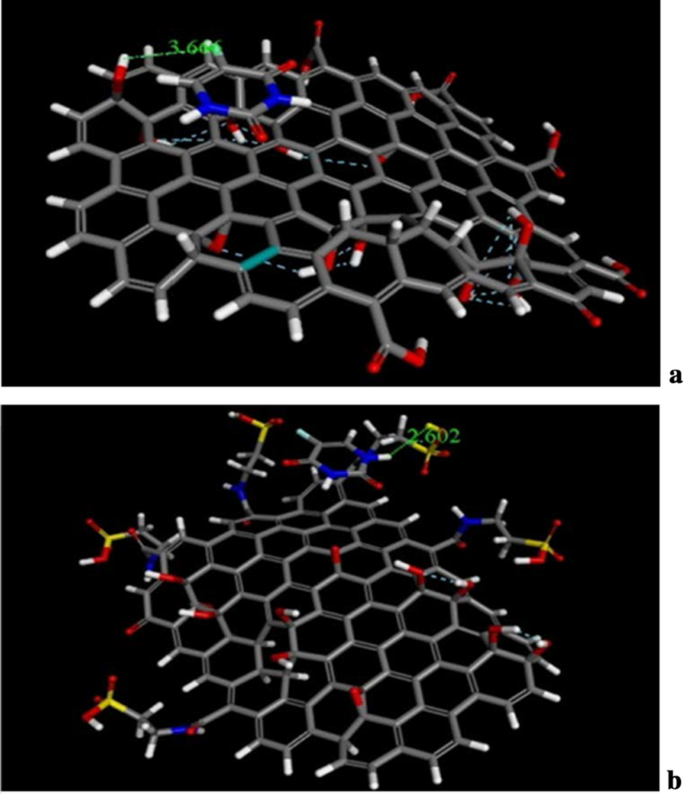
The Molecular docking of GO sheets with 5-FU (a ). The molecular docking of Tau-GO with 5-FU (b )
The diagrams of the molecular dynamics simulation of GO, Tau-GO and 5-FU were shown in Fig. 15. According to the calculation results, the CED of 5-FU-GO and 5-FU-Tau-GO were 2.67*10 8 and 2.83*10 8 , respectivamente. These results showed a stronger interaction between the drug and the Tau-GO. The graphs between MSD and time were plotted (Fig. 16) to obtain the diffusion coefficient via MSD. The drug diffusion coefficients were obtained by the slope divided by 6 as follows:0.094m 2 /s and 0.058 m 2 /s. These show that the force between Tau-GO and 5-FU is stronger, which is consistent with the results of the molecular docking. Therefore, the functionalized GO makes the entire carrier more abundant in atoms and groups; Therefore, making the non-covalent bond with 5-FU stronger, and the entire system more stable.
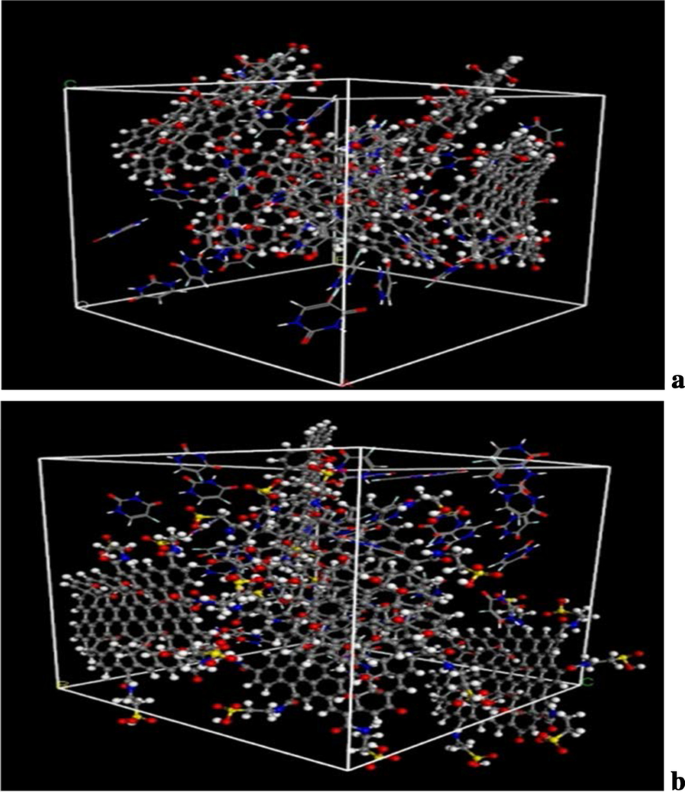
Snapshots of the GO and 5-FU at the end of the MD (a ). Snapshots of the Tau-GO and 5-FU at the end of the MD (b )
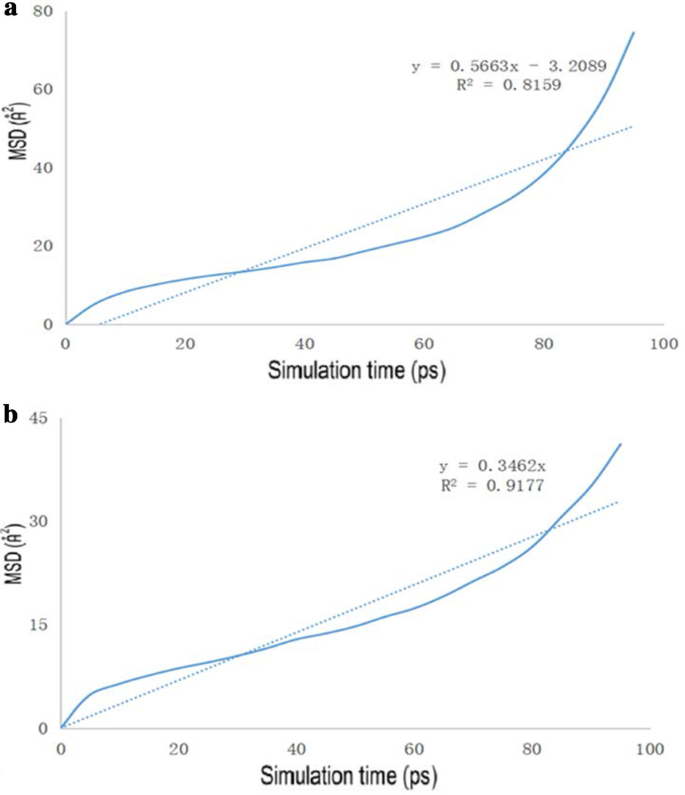
The drug MSD profiles of the GO and 5-FU (a ), Tau-GO and 5-FU (b )
Conclusiones
In summary, we successfully prepared a Tau-GO nanocomposite through a simple chemical method. GO functionalization with Tau has a good stability and improves its biocompatibility. The unique structure and brilliant properties of Tau-GO nanocarriers offer great opportunities for the loading and delivery of 5-FU. The 5-FU-Tau-GO has a potential anti-tumor ability and an excellent circulation time of drugs. Therefore, we believe that the modification of GO by the carrier Tau for 5-FU loading, is an effective and applicable tool for constructing a 5-FU-Tau-GO nano drug delivery system for the delivery of anticancer drugs and anti-tumor therapy.
Disponibilidad de datos y materiales
Los conjuntos de datos utilizados y / o analizados durante el estudio actual están disponibles del autor correspondiente a solicitud razonable.
Abreviaturas
- GO:
-
Óxido de grafeno
- Tau:
-
Taurine
- 5-FU:
-
5-Fluorouracil
- 5-FU-Tau-GO:
-
Taurine functionalized graphene oxide loading 5-fluorouracil
- EE:
-
Encapsulation ratio
- LE:
-
Drug-loading efficiency
- FT-IR:
-
Infrarrojos por transformada de Fourier
- TEM:
-
Microscopía electrónica de transmisión
- TGA:
-
Thermogravimetric analyses
- MSD:
-
Mean square displacement
- CED:
-
Cohesive energy density
Nanomateriales
- Nanofibras y filamentos para una mejor administración de fármacos
- Nanopartículas de FePO4 biocompatibles:administración de fármacos, estabilización de ARN y actividad funcional
- Nanotubos de titanato Nanocompuestos de óxido de grafeno decorados:preparación, retardo de llama y fotodegradación
- Bioseguridad y capacidad antibacteriana del grafeno y el óxido de grafeno in vitro e in vivo
- RGO y redes de grafeno tridimensionales co-modificadas TIM con alto rendimiento
- Mecanismo de conducción y resistencia mejorada en RRAM basado en HfO2 con tratamiento de nitruración
- Fabricación, caracterización y actividad biológica de sistemas de nanoportación de avermectina con diferentes tamaños de partículas
- Evaluación de estructuras de grafeno / WO3 y grafeno / ceO x como electrodos para aplicaciones de supercondensadores
- Aerogel de grafeno / polianilina con superelasticidad y alta capacitancia como electrodo supercondensador altamente tolerante a la compresión
- Fabricación y caracterización de nanoclips de ZnO mediante el proceso mediado por poliol
- Reducción de óxido de grafeno a baja temperatura:Conductancia eléctrica y microscopía de fuerza de sonda Kelvin de barrido



