Nanopartículas de FePO4 biocompatibles:administración de fármacos, estabilización de ARN y actividad funcional
Resumen
FePO 4 Los NP son de especial interés en la fortificación de alimentos y la obtención de imágenes biomédicas debido a su biocompatibilidad, alta biodisponibilidad, propiedad magnética y desempeño sensorial superior que no causa efectos organolépticos adversos. Estas características también son deseables en la administración de fármacos. Aquí, exploramos el FePO 4 nanopartículas como vehículo de administración del fármaco contra el cáncer, doxorrubicina, con una carga de fármaco óptima de 26,81% ± 1,0%. Esta carga refuerza aún más la formación de Fe 3+ complejo de doxorrubicina que da como resultado la formación de FePO 4 -Nanopartículas DOX. FePO 4 -Nanopartículas DOX mostraron una buena homogeneidad de tamaño y biocompatibilidad dependiente de la concentración, con una biocompatibilidad superior al 70% hasta una concentración de 80 µg / mL. Es importante destacar que el análisis de citotoxicidad mostró que el Fe 3+ complejación con DOX en FePO 4 -Los NP de DOX mejoraron la citotoxicidad alrededor de 10 veces que los DOX libres y mejoraron la selectividad hacia las células cancerosas. Además, FePO 4 Los NP estabilizan la temperatura del ARN y apoyan la actividad de traducción del ARNm, lo que muestra promesas para los agentes estabilizadores de ARN. Los resultados muestran la biocompatibilidad de las nanopartículas inorgánicas a base de hierro, su actividad de carga, estabilización y administración de ARN y fármacos, con posibles ramificaciones para la fortificación de alimentos y la administración de fármacos / ARN.
Introducción
Entre varias nanopartículas inorgánicas como oro, sílice y puntos cuánticos, las nanopartículas a base de hierro (Fe-NP) se exploran ampliamente para aplicaciones biomédicas como agentes de contraste, vehículos de administración de fármacos y terapias de base térmica [1, 2, 3]. Debido a la propiedad magnética, la alta bioadaptabilidad y el metabolismo endógeno conocido del hierro, los Fe-NP son candidatos deseables para aplicaciones biomédicas. Como tal, los Fe-NP producen la mayoría de la nanomedicina inorgánica aprobada por la FDA [1, 2]. Estos incluyen INFeD, DexFerrum, Ferrlecit, Venofer, Feraheme e Injectafer que están disponibles comercialmente para su aplicación en la anemia por deficiencia de hierro y la deficiencia de hierro en la enfermedad renal crónica [1]. De manera similar, la administración intravenosa del gluconato de hierro quelato es una intervención bien tolerada para la anemia [4]. La anemia es una de las deficiencias nutricionales más prevalentes en el mundo y nanopartículas a base de Fe como FePO 4 y FeSO 4 se ha utilizado en la fortificación de alimentos para prevenir la anemia. La fortificación de alimentos es el proceso de agregar micronutrientes a los alimentos con el objetivo de superar la deficiencia nutricional en una población [5]. FePO 4 Los NP son de especial interés en la fortificación de alimentos debido a su biocompatibilidad, alta biodisponibilidad y rendimiento sensorial superior que no causan efectos organolépticos adversos [6,7,8,9]. Perfecto y col. han demostrado el FePO 4 La internalización de las NP en las células intestinales humanas se produce principalmente a través del transportador de metales divalentes 1 (DMT-1) y, por tanto, pueden absorberse fácilmente [9, 10]. Feridex® y Revosit® a base de hierro son agentes de contraste de resonancia magnética (IRM) ampliamente utilizados para IRM mejoradas con contraste [11,12,13,14,15,16]. A la luz de estos informes sobresalientes, FePO 4 Los NP se presentan a sí mismos como un buen vehículo de reparto. Aquí, exploramos FePO 4 como vehículo de administración de fármacos mediante la carga de un fármaco contra el cáncer, Doxorrubicina (DOX). Ión férrico (Fe 3+ ) puede formar un complejo con la molécula de DOX facilitada por la interacción electrostática entre el Fe deficiente en electrones en FePO 4 y grupo –OH rico en electrones en DOX para formar FePO 4 cargado con DOX NP:FePO 4 -NP DOX. Evaluamos las propiedades fisicoquímicas de FePO 4 y FePO 4 -DOX NP y evaluaron su biocompatibilidad y perfil de citotoxicidad, respectivamente, en el osteosarcoma de ratón K7M2 y la línea celular de fibroblastos NIH / 3T3.
Junto con eso, la nanopartícula inorgánica ha mostrado promesas en la estabilización y liberación de ácidos nucleicos [17, 18, 19]. En este sentido, la nanopartícula de oro ha sido ampliamente estudiada debido a su capacidad para inmovilizar oligonucleótidos en su superficie, lo que resulta en la prevención de la agregación y degradación molecular [17, 20]. Sin embargo, el oro no es un elemento endógeno y, por lo tanto, puede limitar su aplicación de traslación. Aquí, nanopartículas a base de Fe como FePO 4 Las nanopartículas pueden ser de gran interés para el estudio de estabilización de ARN debido a su naturaleza endógena y perfil de biocompatibilidad establecido. Hay dos mecanismos propuestos de interacción del ácido nucleico (ARN / ADN) con Fe-NP para la estabilización:(1) la formación de enlaces de hidrógeno y la interacción electrostática entre el grupo fosfato de la columna vertebral del ácido nucleico y las Fe-NP que resultan en la adsorción de nucleicos. ácido en Fe-NP, y (2) el ácido nucleico puede adsorberse en la superficie de Fe-NP a través de la interacción de pares de bases de nucleótidos [19, 21, 22]. Un estudio ha demostrado el potencial de las nanopartículas de fosfato de calcio para la estabilización y administración de vacunas de ADN [23]. En este sentido, aquí hemos explorado la estabilización del ARN y la actividad funcional de otra nanopartícula a base de fosfato, FePO 4 , para investigar el potencial multifuncional de FePO 4 nanopartículas basadas en la entrega y estabilización de carga.
Con la rápida aprobación de la vacuna de ARNm contra COVID19, las nanopartículas de la vacuna de ARNm son de gran interés, ya que el ARN está sujeto a una rápida hidrólisis y pérdida de expresión funcional, corresponde a la nanopartícula mejorar estas características críticas. Aquí mostramos FePO 4 Los NP estabilizan el ARN y apoyan la traducción funcional del ARNm. Dadas estas excelentes características, FePO 4 Los NP pueden merecer una consideración para la fortificación de alimentos, la administración de fármacos y ARN, lo que abre interesantes aplicaciones biomédicas.
Resultados y discusión
FePO 4 Análisis de síntesis, caracterización y biocompatibilidad de NP
Una simple reacción química de un paso entre (NH 4 ) 3 PO 4 y Fe (NO 3 ) 3 da FePO 4 como precipitado que se dispersa en un tensioactivo lipídico-PEG biocompatible que ayuda a estabilizar el FePO 4 nanopartículas y previenen la agregación. FePO 4 Las NP mostraron un tamaño hidrodinámico de 175 ± 5 nm con un índice de polidispersidad (PDI) de 0,150 ± 0,01, lo que sugiere una buena homogeneidad de partículas y una distribución de tamaño estrecha. El análisis de potencial Zeta mostró una carga superficial negativa de FePO 4 NP con - 19,1 ± 8 mV de potencial zeta. La carga superficial negativa ayuda además a estabilizar las partículas en los coloides, evitando así la opsonización de las proteínas, un mecanismo que evita la focalización celular y altera la farmacocinética [24, 25, 26]. FePO 4 se caracterizó además por FTIR. La figura 1c muestra la característica espectral de FePO 4 nanopartículas y su precursor:Fe (NO 3 ) 3 y (NH 4 ) 3 PO 4 . FePO 4 los espectros muestran un pico nítido distinto en 1030 cm −1 que se puede atribuir a la banda de estiramiento P – O, un pequeño pico a 520 cm −1 corresponde a la flexión antisimétrica O – P – O, y un amplio rango de 3000 a 3500 cm −1 representa las vibraciones de flexión y estiramiento del agua de las moléculas de agua adsorbidas [27, 28]. El FePO 4 los espectros mostraron la presencia de PO 4 3− grupo y son similares al pico FTIR informado por otros estudios, lo que confirma la formación de FePO 4 nanopartículas [27,28,29]. Fe (NO 3 ) 3 los espectros mostraron picos característicos para las bandas de estiramiento N – O a 1326 y 813 cm −1 [30]. El pico en 1625 se puede atribuir a la vibración de flexión –OH y un pico ancho alrededor de 3000 cm −1 puede atribuirse a las vibraciones de flexión y estiramiento del agua [30]. Asimismo, (NH 4 ) 3 PO 4 mostró picos característicos para el grupo del amonio alrededor de 1500 cm −1 y grupo fosfato alrededor de 1000 cm −1 [31]. La ausencia de picos de nitrato y amonio en FePO 4 Las nanopartículas sugieren que el producto está libre de posibles subproductos y confirma la pureza de la síntesis.
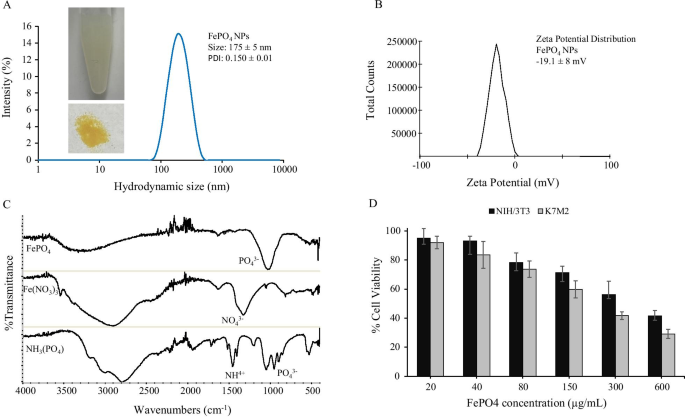
Caracterización y biocompatibilidad de FePO 4 nanopartículas. un Distribución de tamaño hidrodinámico de FePO 4 NP, b medición del potencial zeta de FePO 4 NP que muestran la carga superficial, c FTIR de FePO 4 NP y su precursor-Fe (NO 3 ) 3 y (NH 4 ) 3 PO 4 y d biocompatibilidad de FePO 4 NP en el osteosarcoma de ratón K7M2 y la línea celular NIH / 3T3 de fibroblastos de ratón. Las NP se trataron a diversas concentraciones durante 48 h ( a, b los datos representan la media ± desviación estándar; n =3 réplicas. d representa la media ± s.d., n =6 réplicas).
Con la garantía de una síntesis exitosa, pureza, homogeneidad de buen tamaño y carga superficial estable de FePO 4 NP, pasamos a analizar la biocompatibilidad de FePO 4 NP. Para este propósito, usamos células cancerosas y no cancerosas:osteosarcoma de ratón K7M2 y fibroblasto de ratón NIH / 3T3 y analizamos la biocompatibilidad de NP a una concentración variable en términos de viabilidad celular utilizando el ensayo MTT. FePO 4 Los NP mostraron biocompatibilidad dependiente de la concentración en ambas líneas celulares, K7M2 y NIH / 3T3, en el rango de concentración de 20 a 600 µg / mL (Fig. 1d). FePO 4 Los NP mostraron una buena biocompatibilidad hasta una concentración de 80 µg / mL con una viabilidad celular superior al 70%. La biocompatibilidad fue relativamente mayor en las células no cancerosas NIH / 3T3 en comparación con las células cancerosas K7M2.
Carga de doxorrubicina en FePO 4 y citotoxicidad de FePO 4 -DOX
La doxorrubicina se carga en FePO 4 mediante el método de co-incubación-precipitación en el que la solución de doxorrubicina se mezcla con el precursor de FePO 4 que da como resultado la formación de FePO 4 cargado con DOX . Se emplean tres formulaciones diferentes para cargar DOX como se describe en los métodos. La formulación 1 mostró la mejor eficiencia de carga de 26,81% ± 1 mientras que la formulación 2 mostró una eficiencia de carga de 8,83% ± 2 y la formulación 3 no mostró ninguna carga (Fig. 2a). Para la carga, agregamos solución de DOX al precursor Fe (NO 3 ) 3 en la formulación 1 y para (NH 4 ) 3 PO 4 en la formulación 2, mientras que, en la formulación 3, agregamos solución DOX a FePO 4 NP directamente. Los datos de carga mostraron claramente que agregar DOX al FePO 4 Los NP no retienen el DOX mientras que agregan DOX a cualquiera de los precursores:Fe (NO 3 ) 3 y (NH 4 ) 3 PO 4 La solución ayuda en la carga y retención de DOX. Esto puede explicarse por el hecho de que Fe 3+ de Fe (NO 3 ) 3 puede formar un complejo con el grupo de oxígeno rico en electrones presente en la doxorrubicina [32, 33]. El Fe 3+ -El complejo DOX se precipita luego mediante la adición de (NH 4 ) 3 PO 4 resultando en FePO 4 -DOX, que se caracteriza por un cambio de color de amarillo pálido a marrón pálido (Fig. 2b). A pesar del cambio de color, no hubo cambios en los espectros de emisión de FePO 4 -DOX que mostró máximos de emisión a 590 nm similares a los de DOX libre, cuando se excitó a 480 nm (Fig. 2c). FePO 4 -DOX NPs mostró un tamaño hidrodinámico de 187 ± 7 nm y PDI de 0.143 ± 0.02, similar al de FePO 4 (Figura 2d). Sin embargo, hubo una diferencia significativa en la carga superficial de FePO 4 -DOX NP (-8,89 ± 5 mV), en comparación con FePO 4 NP (-19,1 ± 8 mV) (figura 2e). El cambio en el potencial zeta sugiere cambios funcionales en las propiedades superficiales de las nanopartículas. Aquí, la reducción del potencial zeta de - 19,1 a - 8,89 mV se puede atribuir a la complejación de DOX que agrega propiedad catiónica en el complejo.
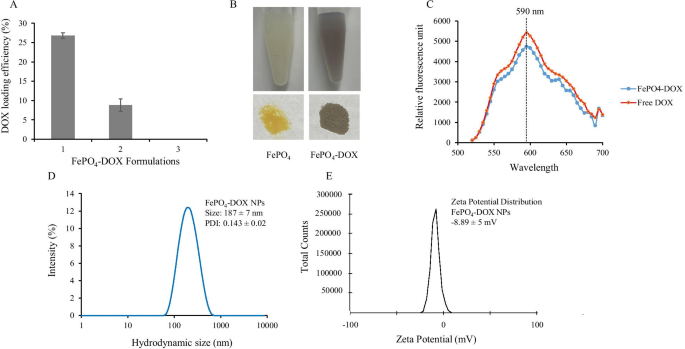
Carga de doxorrubicina (DOX) en FePO 4 NP y caracterización de FePO 4 -DOX. un Eficiencia de carga de DOX en tres formulaciones diferentes de FePO 4 NP y DOX, b Representación pictórica del cambio de color de amarillo a marrón después de la carga de DOX en FePO 4 para formular FePO 4 -DOX, c Caracterización de espectros de emisión de FePO 4 cargado con DOX NP (FePO 4 -DOX) después de la excitación a 480 nm, d distribución de tamaño hidrodinámico de FePO 4 -DOX NP y e Caracterización del potencial zeta de FePO 4 -NP de DOX que muestran la carga superficial (los datos representan la media ± desviación estándar; n =3 réplicas)
Tras la caracterización fisicoquímica, la citotoxicidad de FePO 4 -DOX se analizó en células K7M2 y NIH / 3T3 y se comparó con DOX libre (Fig. 3). FePO 4 -DOX mostró una mayor citotoxicidad en comparación con el DOX libre a una concentración de DOX equivalente en ambas líneas celulares. El valor de IC50 mostró una reducción de alrededor de 10 veces con FePO 4 -Tratamiento con DOX, de 2,61 a 0,248 µM en NIH / 3T3 y de 1,01 a 0,107 µM en células K7M2. Esta drástica reducción en el valor de IC50 en ambas líneas celulares sugiere un perfil de citotoxicidad mejorado de FePO 4 -NP DOX. El FePO 4 equivalente concentración en el rango de concentración IC50 de FePO 4 -DOX es 40 µg / mL (0,107 µM en células K7M2) y 100 µg / mL (0,248 µM en células NIH / 3T3), ambos dentro del rango biocompatible de FePO 4 concentración, con más del 70% de viabilidad celular. Por lo tanto, la elevación de FePO 4 -La citotoxicidad de DOX se puede atribuir al Fe 3+ -Formación del complejo DOX y no a la contribución individual de FePO 4 y DOX. La literatura ha demostrado el elevado efecto citotóxico de la antraciclina como la doxorrubicina en presencia de hierro [34,35,36,37]. Estos informes están respaldados además por el alivio de la citotoxicidad del Fe-DOX mediante el uso de quelantes de hierro [35,36,37]. Un mecanismo propuesto es el complejo Fe-DOX que potencia la toxicidad de las especies reactivas de oxígeno (ROS) derivadas de DOX transformando ROS relativamente seguros (O 2 · - y H 2 O 2 ) en ROS mucho más tóxicos que conducen a un daño elevado del ADN y muerte celular [34, 36]. Otro mecanismo propuesto es la interacción de la DOX con la función de las proteínas reguladoras del hierro y la ferritina en presencia de un exceso de Fe, lo que afecta la homeostasis del hierro y conduce a un daño dependiente e independiente de ROS y a la muerte celular apoptótica [36, 38].
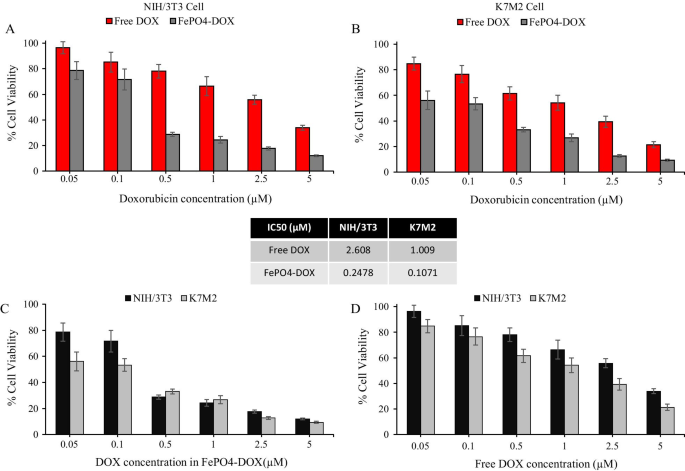
Citotoxicidad de FePO 4 -NP DOX. a, b Citotoxicidad de la doxorrubicina libre (DOX) y FePO 4 -DOX NP en fibroblasto de ratón NIH / 3T3 y línea celular de osteosarcoma K7M2, respectivamente, a diversas concentraciones de DOX equivalente. La citotoxicidad se analizó en porcentaje de viabilidad celular después del tratamiento con partículas durante 48 h. c, d Una comparación en el porcentaje de viabilidad celular de FePO 4 -DOX NP y DOX libre en líneas celulares NIH / 3T3 y K7M2, respectivamente, a una concentración equivalente de DOX. El recuadro en el medio representa los valores IC-50 de DOX libre y FePO 4 -NP DOX en celdas NIH / 3T3 y K7M2 (los datos representan la media ± desviación estándar; n =6 repeticiones)
Junto con la citotoxicidad elevada, FePO 4 -DOX mostró selectividad hacia células cancerosas con un comportamiento de citotoxicidad superior similar al de DOX libre. La Figura 3c muestra FePO 4 equivalente a 0,1 µM de DOX -DOX mostró un 53% de viabilidad celular para la célula cancerosa K7M2 en comparación con el 72% de viabilidad celular para NIH / 3T3 no cancerosos. Asimismo, el DOX libre también mostró un mayor comportamiento de citotoxicidad hacia las células cancerosas, con un 54% de viabilidad celular en las células K7M2 en comparación con el 66% en NIH / 3T3. Sin embargo, las diferencias han aumentado en el caso de FePO 4 -DOX, con un 19% de diferencias en la viabilidad celular entre células cancerosas y no cancerosas en comparación con el 12% en DOX libre. El análisis de citotoxicidad ha demostrado que la complejación de Fe con DOX en FePO 4 -DOX NPs ha mejorado significativamente la citotoxicidad y mejorado la selectividad hacia las células cancerosas.
Internalización celular de FePO 4 -NP DOX
El comportamiento de internalización de FePO 4 Los NP-DOX se analizaron mediante microscopía confocal después de un estudio de internalización dependiente del tiempo (Fig. 4). Se utilizó DOX libre como control positivo. Ambos FePO 4 -DOX NP y DOX libre no mostraron una internalización significativa en los puntos de tiempo de incubación iniciales de 0,5 y 1 h. Sin embargo, a las 3 h de incubación, ambos mostraron internalización como se muestra por la fluorescencia roja de DOX en la imagen confocal. El color azul proviene de la tinción del núcleo por DAPI. El análisis muestra que en 3 h, FePO 4 -Los NP de DOX se internalizan en las células siguiendo un comportamiento de internalización similar al del DOX libre. Es importante señalar que, debido al cambio de color de FePO 4 -DOX, que es marrón en comparación con el color rojo del DOX libre, no podemos comparar cuantitativamente el perfil de internalización relativo de FePO 4 -DOX. No obstante, el ensayo de internalización confirmó que FePO 4 -La DOX es absorbida por las células en 3 h. Dado el mecanismo bien entendido de manejo del hierro por nuestro cuerpo, los NP propuestos podrían ser prometedores en el desarrollo de terapias contra el cáncer a base de hierro con la capacidad de monitorear la respuesta terapéutica en una sola sesión de terapia.
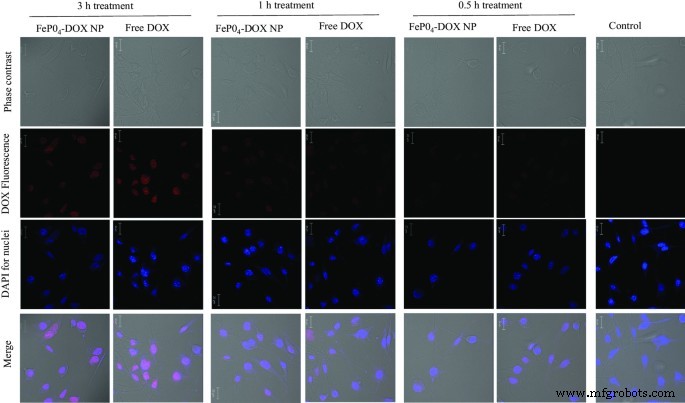
Estudio de internalización celular. Internalización celular de FePO 4 -NP de DOX y DOX libre en células K7M2 después de 3 h, 1 hy 0,5 h de tratamiento. Las células se trataron con 200 µl de 5 µg / ml de concentración de DOX. El color rojo observado en la línea celular tratada con nanopartículas significa una internalización exitosa de las nanopartículas. El color rojo se debe a la característica de fluorescencia de DOX. No se observa señal roja en la celda de control sin tratar
Estabilización de ARN y expresión de ARNm
Como se puede ver en la Fig. 5a, mientras que las nanopartículas de cobre (Cu NP) y los nanotubos de carbono (CNT) aceleran la degradación hidrolítica del ARN (menor intensidad de banda que el control), el FePO 4 y las nanopartículas de plata (Ag) de control estabilizan el ARN como se muestra por una intensidad de banda relativamente fuerte en la electroforesis en gel de agarosa de ARN (RAGE). El FePO 4 y la nanopartícula de óxido de zinc de control (ZnO NP) también imparte cierta resistencia a la degradación en el suero, como se muestra por la intensidad de la banda que es ligeramente más alta que los controles (Fig. 5b). Es importante destacar que la actividad funcional, la expresión de ARNm es más alta que los controles sin nanopartículas, mientras que la Cu NP que degrada el ARN causa pérdida en la expresión de ARNm medida por unidades de luz relativas (Fig. 5c). Estos resultados muestran que FePO 4 Las NP ayudan a estabilizar el ARN y se pueden usar como agente de administración estabilizante para la administración de ARN terapéutico. Los experimentos preliminares anteriores habían indicado un rango de trabajo normal de traducción. Se muestran dos experimentos independientes para las muestras de control no tratadas con nanopartículas que muestran 2393 y 2630 RLU / pocillo, lo que es representativo. Un aumento doble consistente con los datos anteriores sugiere que FePO44 NP apoya la traducción mientras que consistente con la desnaturalización / degradación del ARN anterior, Cu NP suprime la traducción. Se ha aprovechado una variedad de sistemas de nanopartículas inorgánicas para la estabilización y administración de ARN terapéuticos, que incluyen; oro, plata, cobre, óxido de hierro, nanopartículas de sílice mesoporosa (MSN), polímeros a base de carbono, compuestos y otros [39-45]. Por ejemplo, nuestro grupo había informado que la complejación de nanopartículas con ARN macromolecular puede hacer que resista la degradación por la ARNasa o las nucleasas presentes en el suero y los tejidos. La vacuna de ARNm de COVID-19 ha renovado el interés en tales terapias de ARN macromolecular que se extienden más allá de las vacunas, donde incumbe a la nanopartícula no solo proteger al ARN de la hidrólisis y la digestión mediada por nucleasas, sino que la complejación del NP debe preservar la función del ARN, por ejemplo , expresión de ARNm. Anteriormente, habíamos visto que el ARN macromolecular de complejación de nanopartículas de cobre provoca la desnaturalización del ARN [46]. Por lo tanto, investigamos los efectos de la complejación de NP con ARN macromolecular utilizando ARN de levadura Torula (TY-ARN) o un ARNm de construcción informadora que expresa Luciferasa.

Hidrólisis de ARN. un Se utilizó un modelo de ARN que hemos utilizado en varias de nuestras publicaciones, similar en tamaño y composición de secuencia a la mayoría de los ARNm de la levadura torula (TY-RNA). El ARN se incubó en agua bidestilada a lo largo del tiempo en presencia o ausencia de nanopartículas de cobre (Cu NP), fosfato de hierro (FePO4), plata (Ag NP) o nanotubos de carbono (CNT) a 37 grados centígrados y las muestras se retiraron a en el mismo momento y analizado mediante electroforesis en gel de agarosa de ARN (RAGE). La pérdida de intensidad de tinción de la banda indica degradación del ARN, mientras que el mantenimiento de la intensidad de tinción de la banda de ARN indica estabilización. b De manera similar a lo anterior, el ARN se incubó en FBS al 10% / DMEM a temperatura ambiente en presencia de óxido de zinc (ZnO) NP o FePO 4 NP versus control que era ARN solo en ausencia de nanopartículas. De nuevo, las muestras se retiraron con el tiempo y se analizaron mediante RAGE; la presencia de la banda de ARN teñida a lo largo del tiempo indica nuevamente la estabilidad y resistencia de la degradación de nucleasa o ARNasa del suero. c El ARNm que codifica la luciferasa se tradujo in vitro a partir de reticulocitos de conejo estándar y la luminiscencia relativa se estandarizó a ARN en presencia o ausencia de fosfato de hierro (FePO 4 ) o nanopartículas de cobre (Cu)
Conclusión
FePO 4 Las nanopartículas se sintetizaron con éxito siguiendo una técnica simple de co-incubación-precipitación que dio como resultado la formación de partículas de tamaño homogéneo de 175 ± 5 nm. El análisis FTIR confirmó la presencia de grupo fosfato y la ausencia de impurezas precursoras en la nanopartícula. El análisis de biocompatibilidad reveló una biocompatibilidad dependiente de la concentración con más del 70% de viabilidad celular hasta 80 µg / mL. Además, DOX se cargó de manera efectiva en FePO 4 resultando en FePO 4 -NP de DOX que mostraron propiedades fisicoquímicas similares a las de FePO 4 . El análisis de citotoxicidad reveló que la complejación de Fe con DOX en FePO 4 -Los NP de DOX mejoraron la citotoxicidad, con una mejora de alrededor de 10 veces en la IC50, y mejoraron la selectividad hacia las células cancerosas. Además, el ensayo de internalización mostró FePO 4 Los NP-DOX se internalizaron de manera eficiente en las células en un punto de tiempo de incubación de 3 h. El estudio de estabilización de ARN mostró que FePO 4 Las nanopartículas estabilizan eficazmente el ARN, previenen la degradación rápida y mantienen la actividad funcional, lo que demuestra las promesas para la entrega de ARN terapéutico. Dada la buena homogeneidad de tamaño, rango de biocompatibilidad, eficiencia de carga del fármaco, perfil de citotoxicidad mejorado, propiedad estabilizadora del ARN y absorción celular eficiente, FePO 4 Los NP mostraron características deseables para los vehículos de administración de fármacos y ARN. Además, los resultados han mostrado perspectivas prometedoras de utilizar FePO 4 -Pn de medicamentos en fortificaciones de alimentos para el desarrollo de una plataforma de medicamentos basada en alimentos.
Métodos
Síntesis y caracterización de FePO 4 Nanopartículas
FePO 4 Las nanopartículas se sintetizaron mediante el protocolo de optimización de la técnica de precipitación química de Sokolova et al. [47]. Brevemente, fosfato de amonio ((NH 4 ) 3 PO 4, 16 mg / mL) y nitrato de hierro (Fe (NO 3 ) 3, Se preparó una solución de 8 mg / ml). Al 1 mL de Fe (NO 3 ) 3 , 1 mL de (NH 4 ) 3 PO 4 se añadió gota a gota con agitación constante dando como resultado la precipitación de fosfatos de hierro (FePO 4 ). Exceso de (NH 4 ) 3 PO 4 se utilizó para que todo el Fe de Fe (NO 3 ) 3 precipitar como FePO 4. La solución de fosfatos de hierro así formada se lavó con agua 3 veces para eliminar los subproductos mediante centrifugación a 300 g durante 2 min. Finalmente, FePO 4 El precipitado se dispersó con una solución de DSPE-PEG-COOH (10% p / p) en agua para formular FePO 4 nanopartículas. FePO 4 Las NP se caracterizaron por tamaño y propiedades de la superficie usando dispersión dinámica de luz (DLS) y características espectrales usando espectroscopía infrarroja por transformada de Fourier (FTIR).
Carga de doxorrubicina (DOX) en FePO 4 Nanopartículas
La doxorrubicina se cargó en FePO 4 nanopartículas por el método de co-incubación-precipitación. Tres DOX-FePO 4 diferentes Se exploraron las formulaciones de NP para optimizar la mejor eficiencia de carga. En la primera formulación, DOX-FePO 4 Las NP se formularon agregando 100 µg de DOX en 1 ml de Fe (NO 3 ) 3 (8 mg / mL) seguido de la adición de 1 mL de (NH 4 ) 3 PO 4 (16 mg / mL) gota a gota con agitación constante. En las segundas formulaciones, primero se agregaron 100 µg de DOX a 1 ml de (NH 4 ) 3 PO 4 (16 mg / mL) seguido de la adición de 1 mL de Fe (NO 3 ) 3 (8 mg / mL) gota a gota con agitación constante. En las terceras formulaciones, se agregaron 100 µg de DOX al FePO 4 Solución NP. FePO 4 así formulado -Las NP de DOX se lavaron tres veces con agua y la cantidad de doxorrubicina en FePO 4 -DOX se cuantificó espectrofluorimétricamente midiendo la excitación y emisión de DOX a 490 nm y 595 nm.
La eficiencia de carga de DOX se calculó mediante la siguiente ecuación:
$$ \% \; {\ text {Cargando}} \; {\ text {eficiencia:}} \; \ left ({{\ text {DOX}} \; {\ text {presente}} \; {\ text {in}} \; {\ text {FePO}} _ {{4}} - {\ text {DOX}} \; {\ text {NP / Initial}} \; {\ text {input}} \; { \ text {of}} \; {\ text {DOX}}} \ right) \ times {1} 00 $$Biocompatibilidad de FePO 4 NP y citotoxicidad de FePO 4 -NP DOX
Biocompatibilidad de FePO 4 NP y citotoxicidad de FePO 4 -DOX NPs se analizaron en osteosarcoma de ratón K7M2 y fibroblasto de ratón NIH / 3T3 utilizando el ensayo MTT siguiendo el protocolo establecido [48, 49]. Brevemente, se sembraron 10.000 células en placas de 96 pocillos y se incubaron durante 24 h en una atmósfera de CO 2 al 5% a 37 ° C incubadora. Luego, se eliminó el medio y se trataron las células con medios frescos con concentraciones variables de nanopartículas y se dejaron incubar durante 48 h. Las células de control se mantuvieron solo con medio. FePO 4 La concentración de NP varía de 20 a 600 µg / mL y la concentración de DOX varía de 0,05 a 5 µM. Después de la incubación NP, se eliminó el medio y las células se incubaron con solución de MTT (0,5 mg / ml) en medio sin suero durante 2 h para permitir la formación de cristales de formazán. Se eliminó la solución de MTT y se disolvió el cristal de formazán en DMSO y se dejó durante 15 min a temperatura ambiente para una mezcla adecuada. Luego, se midió la absorbancia de la solución de DMSO a 550 nm usando un lector de microplacas (BioTek, Synergy H1 Hybrid Reader) y se calculó el porcentaje de viabilidad celular.
Internalización celular mediante microscopía confocal
Internalización celular de FePO 4 -DOX NP se analizó en células de osteosarcoma K7M2 de ratón utilizando microscopía confocal [49, 50, 51]. Brevemente, se sembraron 12.000 células en placas de 8 pocillos y se incubaron durante 24 h en 37 ° C 5% CO 2 incubadora. Luego, se trataron 200 µl de 5 µg / ml de concentración de DOX en el medio durante 3 h, y las células se fijaron con paraformaldehído al 4% para la obtención de imágenes. El núcleo se tiñó con DAPI y las células se observaron con un microscopio de barrido láser confocal (Carl Zeiss, LSM-700). Aquí, el máximo de emisión de DOX a 560 nm se puede aprovechar para rastrear su internalización, lo que da un color rojo en microscopía confocal. Utilizando el mismo protocolo, se realizó un ensayo de internalización dependiente del tiempo incubando FePO 4 -DOX NP y DOX libre durante 0,5, 1 y 3 h respectivamente.
Estabilidad y expresión del ARN
Se disolvió ARN de levadura Torula (Sigma-Aldrich) a 1 mg / ml en agua desionizada estéril y alícuotas de 2 µg se expusieron a nanopartículas de 20 ug / ml (CNT, Cu, Ag, ZnO NP o FePO 4 ) incubados a 37 ° C y analizados a lo largo del tiempo mediante electroforesis en gel de agarosa de ARN como hemos informado anteriormente [42, 52]. El punto de tiempo que se muestra en la Fig. 5 es durante la noche. De manera similar, el ARN con / sin nanopartículas se expuso a FBS al 10% / DMEM y se analizó nuevamente mediante RAGE como anteriormente. El mRNA fLuc se obtuvo de Trilink Biotechnologies, se incubaron 2 µl en reticuloisado de conejo suplementado con metinina, cisteína y leucina (ProMega Corp) durante 30 grados durante 1,5 h con o sin nanopartículas a 20 µg / ml, se añadió reactivo luciferina estándar y se midió la luminiscencia tomado en un lector de placas Biotek Synergy H1 en condiciones estándar.
Análisis estadístico
Todos los datos representan al menos tres réplicas independientes y se expresan como media ± desviación estándar. cuando sea posible. Cell viability data includes six replicates.
Availability of Data and Materials
The datasets used and/or analyzed during the current study are available from the corresponding author on reasonable request.
Nanomateriales
- Nanofibras y filamentos para una mejor administración de fármacos
- Nanopartículas de lípidos de PLGA trazadas con 131I como portadores de administración de fármacos para el tratamiento quimioterapéutico dirigido del melanoma
- Preparación y actividad de hidrogenación catalítica mejorada de nanopartículas de Sb / Palygorskita (PAL)
- Nanotecnología:del sistema de imágenes in vivo a la administración controlada de fármacos
- Nuevas nanopartículas de Au Nanostars @ PEG biocompatibles para la obtención de imágenes de TC in vivo y las propiedades de depuración renal
- Poliglicerol hiperramificado modificado como dispersante para el control del tamaño y la estabilización de nanopartículas de oro en hidrocarburos
- Determinación de la actividad catalítica de nanopartículas de TiO2 dopado con metal de transición mediante análisis espectroscópico de superficie
- Síntesis y rendimiento in vitro de nanopartículas de hierro-platino recubiertas de polipirrol para terapia fototérmica e imágenes fotoacústicas
- Aptitud ecológica en la síntesis y estabilización de nanopartículas de cobre:actividades catalíticas, antibacterianas, citotóxicas y antioxidantes
- Actividad antibacteriana de la solución de nanopartículas de plata / quitosano preparada in situ contra cepas de Staphylococcus aureus resistentes a la meticilina
- Síntesis verde de nanopartículas de metal y óxido de metal y su efecto sobre el alga unicelular Chlamydomonas reinhardtii



