Nanorods de oro recubiertos con BSA para la terapia fototérmica NIR-II
Resumen
La segunda ventana del infrarrojo cercano se considera la ventana óptica óptima para la obtención de imágenes médicas y la terapia por su capacidad de penetración profunda en los tejidos. La preparación de nanobarras de oro con absorción de longitud de onda larga y baja citotoxicidad sigue siendo un desafío. Se ha sintetizado una serie de nanobarras de oro con una gran relación de aspecto. Se pudo observar una fuerte absorción de plasma en la segunda ventana del infrarrojo cercano de 1000 a 1300 nm. La biocompatibilidad de las nanovarillas de oro sintetizadas se mejora drásticamente mediante el recubrimiento con albúmina de suero bovino (BSA), mientras que se mantienen las propiedades ópticas. El ratón portador de tumores de cáncer de mama podría tratarse bien con las nanovarillas de oro preparadas con una intensidad de luz NIR-II tan baja como 0,75 W / cm 2 . En resumen, estos resultados demuestran la viabilidad de utilizar una dosis de iluminación baja para tratar el tumor en la región NIR-II a través de las nanopartículas de gould de gran relación de aspecto.
Introducción
Las nanopartículas de oro han atraído un gran interés en las investigaciones biomédicas como la brillante biocompatibilidad y la baja citotoxicidad. Por ejemplo, las nanopartículas de oro con alta eficiencia de atenuación de rayos X resultaron prometedoras para el diagnóstico de tumores basado en tomografía computarizada (TC) [1, 2]. Además, las nanopartículas de oro exhiben excelentes propiedades ópticas, lo que se conoce como efecto de resonancia de plasmón superficial (SPR). Las nanopartículas de oro podrían convertir eficientemente la energía de los fotones en energía térmica para la terapia del cáncer en presencia de luz de resonancia de plasmón en la superficie [3, 4]. Por lo tanto, se han desarrollado varias nanopartículas de oro con tamaño y morfología ajustables para la ablación fototérmica de tumores, por ejemplo, nanobarras de oro, nanocapas de oro y nanocajas de oro [5,6,7]. En particular, las nanovarillas de oro (AuNR) con forma y tamaño anisotrópicos ajustables han sido ampliamente estudiadas debido a su excelente estabilidad fototérmica, biocompatibilidad y fuerte absorción en la región NIR [8]. Es bien sabido que la luz del infrarrojo cercano podría penetrar en los tejidos biológicos con mayor eficacia que la luz visible, ya que cuanto mayor es la longitud de onda de la luz, menor es la pérdida por dispersión de la luz [9]. Además, se ha encontrado que las nanopartículas en forma de varilla tienen una permeabilidad tumoral dramáticamente mejorada y un tiempo de circulación sanguínea más prolongado, lo que resulta en una mayor acumulación de tumores [10, 11]. Sin embargo, el inconveniente importante de la aplicación de nanobarras de oro a la terapia fototérmica (PTT) es la irradiación láser de alta potencia, que induciría un gran daño al tejido normal (exposición máxima a la intensidad de luz permitida) [12]. Se ha demostrado que el PTT en la segunda ventana del infrarrojo cercano (NIR-II, 1000-1700 nm) tiene una profundidad de penetración tisular mucho mayor que la de NIR-I (700-1000 nm), ya que la dispersión de luz mucho más baja en NIR -II [13,14,15,16,17]. Por lo tanto, se espera que la nanoplataforma PTT en el NIR-II logre un tratamiento PTT más eficaz del tumor y tenga un gran potencial de aplicación clínica para terapias tumorales más complejas. Sin embargo, la preparación de nanobarras de oro con absorción de longitud de onda larga y baja citotoxicidad sigue siendo un gran desafío. Aquí, informamos la síntesis de nanobarras de oro por el método sin semillas con picos de absorción en la segunda ventana de la ventana del infrarrojo cercano (1000-1300 nm). La modificación de la superficie se introdujo mediante recubrimiento con BSA para reducir la citotoxicidad. La relación de aspecto de nanobarras de oro preparadas (AuNR @ BSA) se caracterizó mediante microscopio electrónico de transmisión (TEM) y dispersión dinámica de luz (DLS). El modelo de ratón portador de tumores de cáncer de mama se utilizó para probar el efecto terapéutico fototérmico de AuNR @ BSA. Descubrimos que el tumor podría tratarse bien con una intensidad de luz tan baja como 0,75 w / cm 2 .
Materiales y métodos
Materiales
Trihidrato de cloruro de oro (HAuCl 4 · 3H 2 O) (99,9%), bromuro de hexadecil trimetilamonio (CTAB) (99%), ácido nítrico (GR, 65-68%) y solución de peróxido de hidrógeno (GR, 30%) se recibieron de Shanghai Aladdin Biological Technology Co.Ltd. . Borohidruro de sodio (NaBH 4 ) (97%) y nitrato de plata (AgNO 3 ) (99,8%) se recibieron de Shanghai Lingfeng Chemical Reagent Co. Ltd. Se recibió ácido clorhídrico (HCl) (38%) de Dongguan Dongjiang Chemical Reagent Co. Ltd. Se recibió hidroquinona (99%) de Energy Chemical. La albúmina de suero bovino (98%) se obtuvo de Sigma-Aldrich. Se recibió hidróxido de sodio (AR, 96%) de Greagent.
El medio RPMI 1640 y la penicilina-estreptomicina se adquirieron de HyClone. La solución tamponada con fosfato (PBS) se adquirió de Corning. La pancreatina se compró a Coolaber. El suero fetal bovino (FBS) se adquirió de Gibco. Las células 4T1 fueron proporcionadas por el Centro de Investigación de Óptica Biomédica e Imágenes Moleculares del Instituto de Tecnología Avanzada de Shenzhen, Academia de Ciencias de China. Dojindo Chemical Technology (Shanghai) Co., Ltd suministró el kit de recuento celular 8 (CCK-8) para la prueba de proliferación celular y toxicidad. El agua ultrapura Millipore se utilizó durante todo el experimento.
Preparación de nanopartículas AuNR @ CTAB
La síntesis de nanovarillas de oro se realiza de la siguiente manera:0,4 mL de HAuCl 4 (aq) (10 mM) y 10 mL de CTAB (aq) (0.1 M) se agregaron a 23-33 µL de AgNO 3 (ac) (100 mM). Luego, se agregaron 10-30 µL de HCl (1.2 M) y 525 µL de hidroquinona acuosa (0.1 M) a la solución de crecimiento bajo mezcla suave. El color de la solución de crecimiento cambió de naranja a amarillo muy claro. Después de 15 minutos de agitación, de 10 a 40 µL de NaBH 4 helado recién preparado Se inyectó una solución (ac) (10 mM) en la solución de crecimiento. La mezcla se agitó durante 30 sy se dejó reposar durante 18 ha temperatura ambiente. Luego, el AuNR @ CTAB se lavó dos veces con PBS.
Preparación de AuNR @ BSA
Primero, agregamos una cierta cantidad de CTAB para ajustar su concentración en la solución AuNR @ CTAB a 1 mM, y luego el ultrasonido disuelve completamente el CTAB. Se añaden lentamente 3 ml de AuNR @ CTAB a 3 ml de solución de BSA (10 mg / ml) y la solución mezclada se sonica durante 30 min. Después de la centrifugación a 9500 × r durante 40 min, el sobrenadante se reemplazó con 6 ml de solución de BSA (5 mg / ml), y luego, el pH se ajustó a 11-12 con hidróxido de sodio (2 M), se agitó durante al menos 18 h. Después de eso, el AuNR @ BSA sintetizado se centrifugó a 9500 × r durante 40 min, luego se lavó dos veces con PBS y se disolvió en PBS para su uso posterior.
Caracterizaciones de nanopartículas AuNR @ CTAB y AuNR @ BSA
El análisis morfológico de nanobarras de oro fue obtenido por Beijing Zhongke Baice Co., Ltd. a través del microscopio electrónico Talos F200X para obtener imágenes TEM. Se utilizó Zetasizer Nano ZS (Malvern, Reino Unido) para estudiar la distribución de tamaño y el potencial zeta de varias nanopartículas mediante DLS. El espectro de absorción UV-Vis se determinó con un espectrofotómetro ultravioleta-visible UV-2700 (SHIMADZU, Japón).
Para la caracterización morfológica de AuNR @ BSA dentro del tumor, se inyectaron 100 µL de AuNR @ BSA (DO =25 a 1064 nm) en los sitios del tumor con irradiación de aproximadamente 10 minutos, después de que se recogieron los tumores tratados. El tumor no tratado se recogió como control. Los tumores recogidos se incubaron en una solución de glutaraldehído al 2,5% (Coolaber.co., Beijing, China) para microscopía electrónica de transmisión (Beijing Zhongke Baice Co., Ltd). El patrón de espectroscopia infrarroja por transformada de Fourier (FT-IR) y los patrones de difracción de rayos X (XRD) de muestras de AuNR fueron obtenidos por Beijing Zhongke Baice Co., Ltd.
Medición del rendimiento fototérmico de AuNR @ CTAB y AuNR @ BSA
La solución de nanovarillas de oro se diluyó a diferentes DO a 1064 nm (0,5, 1, 1,5 y 2) y se usó el PBS como control en blanco. Las nanovarillas de oro (500 µL) se irradiaron con un láser de 1064 nm (Haoliangtech, Shanghai, China) a una intensidad de potencia de 0,35–1 W / cm 2 durante 30 min. La temperatura se registró con una cámara termográfica infrarroja (FLUKE TI25).
Fotoestabilidad de AuNR @ BSA
Para probar la fotoestabilidad, se midieron los espectros de absorción de AuNR @ BSA en función del tiempo de irradiación. Los AuNR @ BSA (OD =1) se irradiaron con láser NIR (1064 nm, 0,5 w / cm 2 ). De 0 a 10 min, el espectro se registró cada minuto. La prueba del ciclo fototérmico también se llevó a cabo como la solución AuNR @ BSA (0.5 mL) irradiada con irradiaciones láser cada 10 min encendidas y apagadas (1064 nm, 0.5 W / cm 2 ) y se registró el cambio de temperatura.
Cultivo celular
La línea celular de cáncer de mama murino (células 4T1) se cultivó en RPMI 1640 que contenía FBS al 10% y 100 U / ml de penicilina o 100 µg / ml de estreptomicina. El ambiente de cultivo es 37 ° C y la condición de humidificación es 5% CO 2 .
In Vitro Evaluación de citotoxicidad de nanopartículas de oro
El ensayo CCK-8 se utilizó para identificar la citotoxicidad de las nanovarillas de oro. Las células 4T1 se sembraron previamente en placas de 96 pocillos (5 × 10 3 por pocillo) y se incubó durante 24 h. Posteriormente, se agregaron 10 μL de diversas concentraciones de AuNR @ CTAB y AuNR @ BSA y se incubaron durante otras 24 h. Después de lavar con PBS dos veces, se agregaron 10 μl de solución de CCK-8 a cada pocillo y se incubaron durante 40 minutos, seguido de la medición de la absorbancia a 450 nm con un lector de microplacas.
Para la fototoxicidad, las células 4T1 se sembraron previamente en una placa de 96 pocillos (5 × 10 3 por pocillo) y se incubaron durante 24 h, luego las células se irradiaron con láser NIR (1064 nm, 0,75 W / cm 2 , 10 min) y se incubó adicionalmente durante 24 h. Después de eso, se agregaron 10 μL de solución de CCK-8 en cada pocillo y se incubaron durante 40 min más a 37 ° C. Luego, se utilizó un lector de microplacas para detectar la absorbancia de cada pocillo a 450 nm.
Modelo de ratón portador de tumores
Todos los ratones BALB / c se compraron en Beijing Vital River Laboratory Animal Technology Co. Ltd. Todos los procedimientos de experimentos con animales se llevaron a cabo siguiendo los procedimientos estándar aprobados por el Comité de Tecnología Avanzada del Instituto de Shenzhen de la Academia China de Ciencias. El modelo tumoral se estableció mediante la inyección subcutánea de células 4T1 (2 × 10 6 ) en la espalda de los ratones. Los estudios en animales se realizaron cuando el volumen del tumor alcanza aproximadamente 100 mm 3 .
In Vivo Circulación y biodistribución de sangre
Para medir el tiempo de circulación, primero se inyectaron por vía intravenosa 200 μL de AuNR @ BSA en la vena de la cola de ratones BALB / c, y luego se recolectaron 20 μL de sangre a 0.25, 2, 4, 6, 8, 12, 36 y 48 h, y se diluyó con 30 μL de PBS para obtener 50 μL de muestra de sangre. Aproximadamente 400 μL de HNO 3 concentrado (calidad cromatográfica), se apretó la tapa y se digirió a 90 ° C durante 2 h. Después de enfriar a temperatura ambiente, 150 μL de H 2 O 2 (grado cromatográfico) se vertió lentamente y luego se calentó a 90 ° C durante 1 h sin cubrir. Al final, la solución se diluyó a 5 mL con agua ultrapura. La concentración de ion Au se midió mediante espectroscopia de emisión óptica de plasma acoplado inductivamente (ICP-OES) después de pasar a través de un filtro de jeringa de nailon de 0,44 mm.
Para medir la biodistribución, se inyectaron por vía intravenosa aproximadamente 200 μL de AuNR @ BSA en la vena de la cola de ratones BALB / c. Después de 24 h, se sacrificó el ratón y se extrajeron el corazón, el hígado, el bazo, el pulmón y el riñón y se secaron en un horno a 80 ° C. Antes de la digestión, se pesó cada órgano, 800 μL concentrado de HNO 3 Se añadió (GR) y se calentó a 90ºC durante 2 h. Después de enfriar a temperatura ambiente, 200 μL de H 2 O 2 (GR) se añadió lentamente gota a gota, se calentó a 90ºC durante 1 h, y luego, la solución se diluyó a 10 ml con agua ultrapura. Finalmente, la concentración de ion Au se midió mediante ICP-OES después de pasar a través de un filtro de jeringa de nailon de 0,44 mm.
Eficiencia del tratamiento fototérmico
Para evaluar el efecto terapéutico térmico de AuNR @ BSA, los ratones portadores de tumores con tumores 4T1 se dividieron aleatoriamente en cuatro grupos con un volumen tumoral de aproximadamente 100 mm 3 :(1) AuNR @ BSA, (2) AuNR @ BSA + láser; (3) Solo láser (4) Control en blanco. Se utilizó una cámara termográfica infrarroja para registrar la imagen térmica infrarroja del sitio del tumor. El volumen del tumor y el peso corporal de los ratones se registraron antes y después del tratamiento, respectivamente. El volumen del tumor se puede calcular de acuerdo con la ecuación normal (volumen =ancho 2 × longitud / 2). Dos semanas después, se sacrificó a los ratones y se aislaron los tumores.
Análisis de datos
Para el análisis de los datos se utilizó el software estadístico SPSS 16.0. Los datos de medición se expresaron como media ± d, la comparación entre grupos se realizó mediante análisis de varianza y la comparación de los datos de recuento se realizó mediante la prueba de Chi-cuadrado. P <0,05 se consideró estadísticamente significativo.
Resultados y discusión
Síntesis y caracterización de AuNR @ CTAB
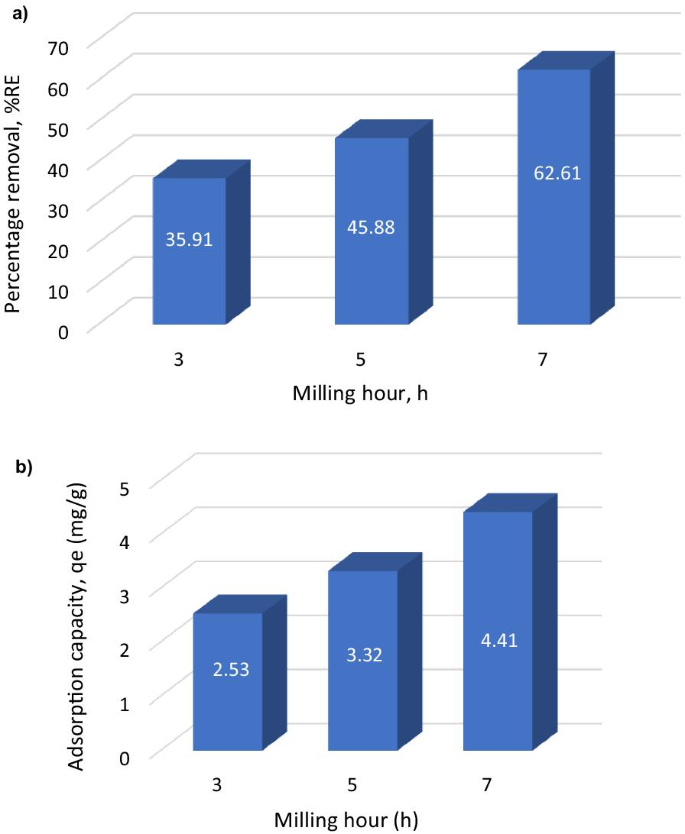
Se encontró que las nanovarillas de oro más pequeñas, mejor farmacocinética y menor citotoxicidad [18]. Sin embargo, el pico de absorción de SPR de las nanovarillas de oro está muy relacionado con la relación de aspecto, cuanto mayor es la relación de aspecto, menor energía del pico de SPR. Para sintetizar AuNR con una relación de aspecto grande, mientras tanto, mantener el tamaño lo más pequeño posible, se optimizaron los parámetros de síntesis, como la concentración de tensioactivo, el pH de la solución de crecimiento y la concentración del agente reductor. El NaBH 4 (aq) es un tipo de agente reductor fuerte que forma el núcleo de Au a través de la nucleación en ráfaga de LaMer, seguida de una rápida unión aleatoria de iones de Au y una maduración intrapartícula [19]. Como la cantidad molar de NaBH 4 aumentando, el pico de absorción máximo de nanobarras de oro sufre un cambio azul de 1223 a 865 nm (Fig. 1C). El pH de la solución de crecimiento también es un parámetro clave para controlar el crecimiento de nanobarras de oro, y se ajusta mediante la cantidad de ácido clorhídrico [20]. Se encontró que el pico de absorción máximo de las nanovarillas de oro se desplazaba gradualmente hacia el rojo de 871 a 1070 nm mientras aumentaba la cantidad de ácido clorhídrico (Fig. 1D). Además, Ag + se considera que puede controlar la dirección de crecimiento de las nanovarillas de oro, y cuanto menor sea el valor de Ag + concentración, podría obtenerse la longitud de onda de absorción más larga del pico SPR (Fig. 1E). Al final, las nanovarillas de oro sintetizadas son de color rojo vino, como se muestra en la Fig. 1B. Por lo tanto, considerando la eficiencia de síntesis de las nanovarillas de oro y la disponibilidad de una fuente de luz láser, elegimos nanovarillas de oro con un pico de absorción máximo a 1064 nm para el tratamiento fototérmico de tumores.
Las fotopropiedades de AuNR @ CTAB en diferentes condiciones de síntesis. un La preparación de AuNR @ CTAB. b La imagen de nanobarras de oro revestidas con CTAB (AuNR @ CTAB), c Espectros UV-vis de AuNR @ CTAB preparado con NaBH 4 variable concentración, d Espectros UV – vis de AuNR @ CTAB preparado con concentración variable de HCl e Espectros UV-vis de AuNR @ CTAB preparado con AgNO 3 variable concentración
Síntesis y caracterización de AuNR @ BSA
El bromuro de cetiltrimetilamonio (CTAB) es el compuesto más utilizado para la síntesis de nanobarras de oro con longitudes y proporciones precisas. Sin embargo, CTAB tiene una citotoxicidad significativa cuando la concentración es superior a 1 a 10 μM. La aplicación de las nanovarillas de oro revestidas con CTAB (AuNR @ CTAB) en biomedicina se ha restringido considerablemente [21]. Además, la estabilidad coloidal de las nanovarillas de oro revestidas con CTAB en solución acuosa se ve drásticamente afectada por la temperatura, que es fácil de cristalizar a bajas temperaturas [22]. Dada la reducción de la citotoxicidad de CTAB y la mejora de su estabilidad, se han propuesto varios enfoques para reemplazar CTAB durante el proceso de síntesis de nanobarras de oro o para funcionalizar las nanovarillas de oro recubiertas de CTAB. Utilizando polímeros, péptidos, tensioactivos y lípidos para modificar la superficie de las nanopartículas, la mayoría de estas estrategias utilizan moléculas tioladas o fuerzas de interacción electrostática para unirse a la superficie del oro [23]. Las proteínas son las opciones más prometedoras como las ventajas de la estabilidad coloidal, la biocompatibilidad y una mayor funcionalización. [26]
Las nanovarillas de oro envueltas con CTAB y BSA se muestran en la Fig. 2A. El pico de absorción máximo de AuNR @ BSA es de alrededor de 1064 nm, que es aproximadamente 30 nm desplazado al rojo en comparación con el de AuNR @ CTAB (Fig. 2B). El potencial zeta de las nanovarillas de oro cambió de positivo a negativo mediante la sustitución del recubrimiento CTAB por BSA (archivo adicional 1:Fig. S1). A partir de los espectros FTIR de AuNR @ BSA y AuNR @ CTAB (archivo adicional 1:Fig. S2), pudimos encontrar que dos picos característicos de a 1649 cm −1 y 1539 cm −1 en el caso de AuNR @ BSA, que se atribuyeron a las bandas vibratorias amida I y amida II de BSA. La dispersión dinámica de luz (DLS) también se aplicó para analizar el tamaño hidrodinámico de AuNR @ CTAB y AuNR @ BSA; Además, la morfología de AuNR @ BSA y AuNR @ CTAB se caracterizó por microscopía electrónica de transmisión (TEM) como se muestra en la Fig.2C, D. Se pudieron encontrar claramente dos picos a partir de la medición de la intensidad de dispersión de DLS, uno con un tamaño hidrodinámico de aproximadamente 3.10 ( ± 0.85) nm y el otro alrededor de 57.45 (± 24.22) nm para AuNR @ CTAB. Sin embargo, en el caso de AuNR @ BSA, los picos se desplazan a 8,64 (± 3,80) nm y 89,24 (± 42,24) nm. Pudimos encontrar que la forma de AuNR permanece similar después del recubrimiento con BSA, excepto que los extremos se vuelven ligeramente redondeados (Fig. 2C, D). Para aplicaciones de terapia in vivo, el tamaño crítico de las nanopartículas se limita a menos de 100 nm [25]. Más allá de este tamaño, la capacidad de las nanopartículas para penetrar en los tumores será limitada; por lo tanto, las nanovarillas de oro presentadas serían un candidato ideal para la terapia tumoral [24]. Como se muestra en el archivo adicional 1:Fig. S3, los picos característicos de Au se pueden observar claramente en el patrón XRD, desde los planos (111), (200), (220) y (311) de nanopartículas de Au.
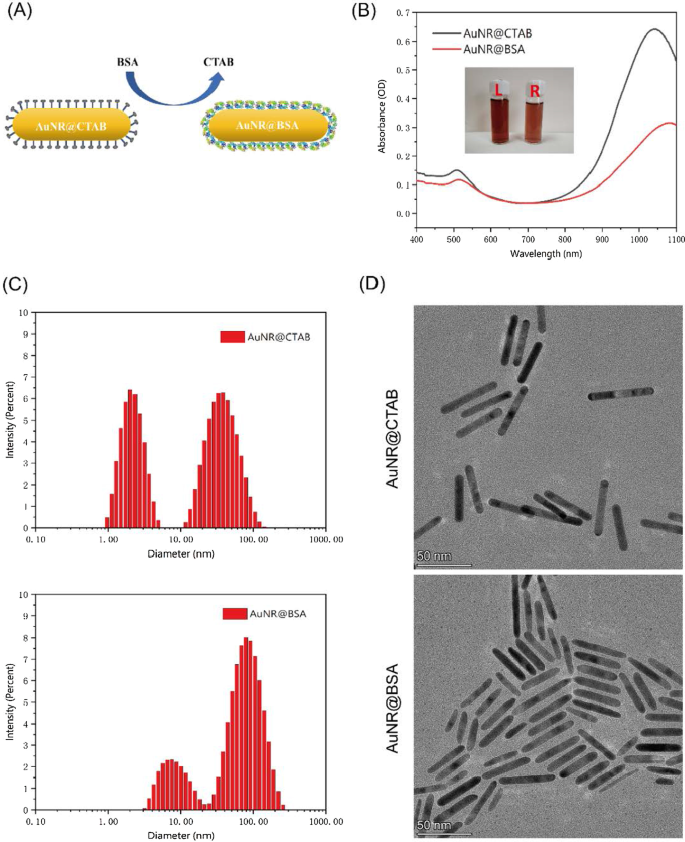
Caracterización de AuNR @ BSA y AuNR @ CTAB. un Elaboración de AuNR @ BSA. b Espectros UV-Vis de AuNR @ CTAB (L) y AuNR @ BSA (R). c La medición de intensidad DLS de AuNR @ CTAB y AuNR @ BSA. d Las imágenes TEM de AuNR @ CTAB y AuNR @ BSA
In Vitro Efecto fototérmico de nanobarras de oro
El láser de diodo de 1064 nm como la fuente de luz NIR-II más económica se considera la longitud de onda óptima para la terapia fototérmica. Por lo tanto, se considera que la nanoplataforma de oro NIR-II ideal para una terapia fototérmica eficiente se caracteriza por una fuerte absorción de SPR a 1064 nm, alta eficiencia fototérmica y excelente estabilidad fototérmica. Para investigar el efecto fototérmico del AuNR @ BSA preparado, se excitaron PBS y diferentes DO (=0,5, 1, 1,5, 2) de AuNR @ BSA a 1064 nm con una intensidad de luz de 0,35 a 1 W / cm 2 durante 30 min. Se utilizó un generador de imágenes de temperatura para registrar los cambios de temperatura cada 5 min, como se muestra en la Fig. 3A. El efecto fototérmico de AuNR @ BSA y AuNR @ CTAB con la misma absorbancia (DO =1) es significativamente mayor que el de PBS. Pudimos encontrar que la temperatura se elevó rápidamente en los primeros 5 minutos y luego se mantuvo en aproximadamente 80 ° C durante el resto del tiempo, como se ilustra en la Fig. 3A. El aumento de temperatura inducido por fototermia para PBS causado principalmente por la absorción de matices de agua a 1064 nm. La temperatura máxima en función de la intensidad de la luz se ilustra en la Fig. 3B. Se encontró que la temperatura térmica fotoinducida de AuNR @ CTAB y AuNR @ BSA a una absorbancia de aproximadamente 1 es proporcional a la intensidad de la luz. El aumento de temperatura es mucho más rápido para AuNR @ CTAB y AuNR @ BSA que para PBS a medida que aumenta la intensidad del láser. Además, la Fig. 3C muestra que en las mismas condiciones de irradiación (1064 nm, 0,75 W / cm 2 ), la temperatura fototérmica máxima aumenta drásticamente a medida que aumenta la absorbancia de ambos AuNR. Las propiedades fototérmicas del AuNR recubierto con BSA son un poco mejores que las del recubierto con CTAB. No hay ningún cambio significativo en la temperatura fototérmica máxima de AuNR @ BSA (OD =1, 61,1 ° C) dentro de tres ciclos de irradiación (0,5 W / cm 2 , 10 min), lo que indica la excelente estabilidad fototérmica del AuNR @ BSA preparado (Fig. 3D). La Figura 3E representa la imagen de temperatura fototérmica de AuNR @ CTAB (OD =1), AuNR @ BSA (OD =1) y PBS bajo irradiación láser durante 10 min. La temperatura máxima de PBS es de 44,5 ° C, mientras que la temperatura máxima de AuNR llega a los 85,5 ° C. Los resultados anteriores demostraron que el AuNR @ BSA sintetizado posee características de absorción apropiadas, eficiencia de conversión fototérmica y fotoestabilidad en el rango NIR-II como un excelente agente terapéutico fototérmico.
Evaluación in vitro del efecto fototérmico de AuNR @ BSA. un La temperatura fototérmica de AuNR @ BSA y AuNR @ CTAB en función del tiempo de irradiación del láser (absorbancia de SPR aproximadamente 1, 1064 nm, 1 W / cm 2 ). b Aumento de temperatura provocado por NIR de PBS, AuNR @ CTAB (OD =1) y AuNR @ BSA (OD =1) en función de la intensidad de la irradiación láser (1064 nm, 0,35 a 1 W / cm 2 ). c Aumento de temperatura activado por NIR de AuNR @ BSA y AuNR @ CTAB con diferente absorbancia para una irradiación láser de 10 minutos (1064 nm, 1 W / cm 2 ). d Conversión fototérmica de AuNR @ BSA (OD =1) bajo tres ciclos de irradiación (1064 nm, 0,5 W / cm 2 ). e Imagen térmica de PBS, AuNR @ CTAB (OD =1), AuNR @ BSA (OD =1) bajo irradiación con láser NIR (1064 nm, 1 W / cm 2 ) en un intervalo de tiempo de 5 y 10 min. (media ± DE, n =3)
Citotoxicidad y toxicidad fototérmica in vitro de nanovarillas de oro
El análisis CCK-8 se realizó para cuantificar la citotoxicidad de AuNR @ CTAB y AuNR @ BSA en células 4T1 a diferentes concentraciones. Incluso sin irradiación con láser, el AuNR @ CTAB ya exhibe una citotoxicidad significativa a una concentración muy baja (absorbancia de aproximadamente 0,05), por lo que su aplicación biológica está muy restringida. Sin embargo, AuNR @ BSA demuestra excelentes perspectivas de aplicación biológica, por ejemplo, la viabilidad celular todavía está en el rango aceptable cuando la absorbancia de AuNR @ BSA alcanza aproximadamente 1 (Fig. 4A). Alentada por la estabilidad prometedora y la alta eficiencia de conversión fototérmica de AuNR @ BSA, la toxicidad fototérmica se realizó en células tumorales 4T1 in vitro con una intensidad de luz de aproximadamente 0,75 W / cm 2 durante 10 min. Se encontró una toxicidad fototérmica significativa a una absorbancia de alrededor de 1 con una tasa de supervivencia celular de alrededor del 20%; sin embargo, se encontró aproximadamente el 100% de supervivencia celular para experimentos sin radiación (Fig. 4B, archivo adicional 1:Fig. S4). Estos resultados in vitro indican que el tratamiento fototérmico AuNR @ BSA en la región NIR-II podría matar eficazmente las células cancerosas a una intensidad de radiación relativamente.
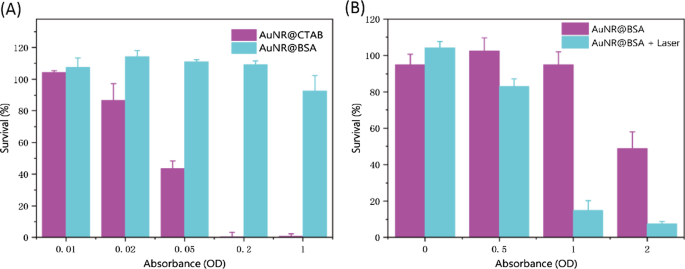
Citotoxicidad in vitro y toxicidad fototérmica de nanobarras de oro. un Viabilidad celular de células 4T1 incubadas con diversas concentraciones de AuNR @ CTAB y AuNR @ BSA. b Viabilidad celular de células 4T1 incubadas con diversas concentraciones de AuNR @ BSA sin y con irradiación láser NIR (1064 nm, 0,75 W / cm 2 , 10 minutos). (media ± DE, n =3)
In Vivo Estudios de biodistribución
El tiempo de circulación sanguínea es esencial para la administración satisfactoria de los fármacos basados en nanopartículas [24]. El tiempo de circulación sanguínea de AuNR @ BSA se controló mediante la concentración de Au mediante ICP-OES y se encontró que era de aproximadamente 1,5 h (vida media) (Fig. 5A). La biodistribución in vivo de AuNR @ BSA también se midió mediante la concentración de Au en diferentes órganos (archivo adicional 1:Fig. S5). Como se muestra en la Fig. 5B, AuNR @ BSA se acumularon en gran medida en el hígado y el bazo después de una inyección intravenosa de 24 h debido a su fuerte fagocitosis como un órgano del sistema reticuloendotelial (RES) [27, 28]. Estos resultados muestran que AuNR @ BSA puede acumularse eficazmente en el hígado y el bazo. AuNR @ BSA tiene aplicaciones potenciales en enfermedades relacionadas con el hígado y el bazo.
La biodistribución de AuNR @ BSA en sangre y órganos. un La concentración de Au en sangre en función del tiempo mediante inyección intravenosa de AuNR @ BSA. b La biodistribución de AuNR @ BSA en varios órganos
In Vivo Tratamiento fototérmico de infrarrojo cercano de nanobarras de oro
El excelente rendimiento fototérmico de AuNR @ BSA nos anima a seguir la terapia fototérmica in vivo en ratones BALB / c con tumores. AuNR @ BSA se inyectó in situ en el tumor y, a continuación, se introdujo la luz para la terapia fototérmica 10 minutos más tarde (1064 nm, 0,75 W / cm 2 ). La variación de temperatura in vivo se controló mediante una cámara termográfica de temperatura. Los cambios de temperatura antes y después del tratamiento se muestran en la Fig. 6D. La temperatura del sitio del tumor fue de aproximadamente 63,9 ° C dentro de los 10 min de la irradiación y mantuvo poca fluctuación a esta temperatura (Fig. 6D). Por el contrario, no hay ningún cambio de temperatura observable para el grupo de control en la misma condición de irradiación (grupo AuNR @ BSA, grupo PBS, grupo láser). Después de la terapia fototérmica, se controló el volumen del tumor y el peso corporal de los ratones cada dos días durante 14 días. Como se presenta en la Fig.6A, B, el tumor del grupo AuNR @ BSA_laser se inhibió por completo y se dejó como costras quemadas en la ubicación del sitio del tumor original, mientras que el de los grupos de control creció relativamente rápido y fuera de control (AuNR @ BSA group, Grupo PBS, grupo láser). Las costras son la piel quemada, lo que demuestra directamente que el proceso de PPT podría provocar un exceso de calor local en el sitio del tumor con AuNR @ BSA inyectado. El efecto fototérmico es muy eficiente, ya que observamos que los tumores sólidos en el grupo láser AuNR @ BSA + disminuyen rápidamente dos días después del tratamiento. Para capturar aún más los cambios tumorales después del tratamiento, al final de la observación de los 14 días, se sacrificaron los ratones y se aislaron los tumores. Como se muestra en la Fig. 6C, el tamaño del tumor del grupo de tratamiento AuNR @ BSA_laser se suprimió totalmente, mientras que se encontró que todos los demás grupos tenían un crecimiento descontrolado. Las imágenes de ratones del grupo (láser AuNR @ BSA +) mostraron que los tumores no continuaron creciendo después del tratamiento de 14 días (Fig. 6E). Por lo tanto, considerando la capacidad terapéutica ideal y la ausencia de citotoxicidad obvia, AuNR @ BSA para la terapia de irradiación con láser de segunda ventana en el infrarrojo cercano es un candidato ideal para el PTT activado por luz in vivo. Esto muestra claramente que la hipertermia simple utilizando la terapia NR-II actual puede inhibir eficazmente el crecimiento tumoral (archivo adicional 1).
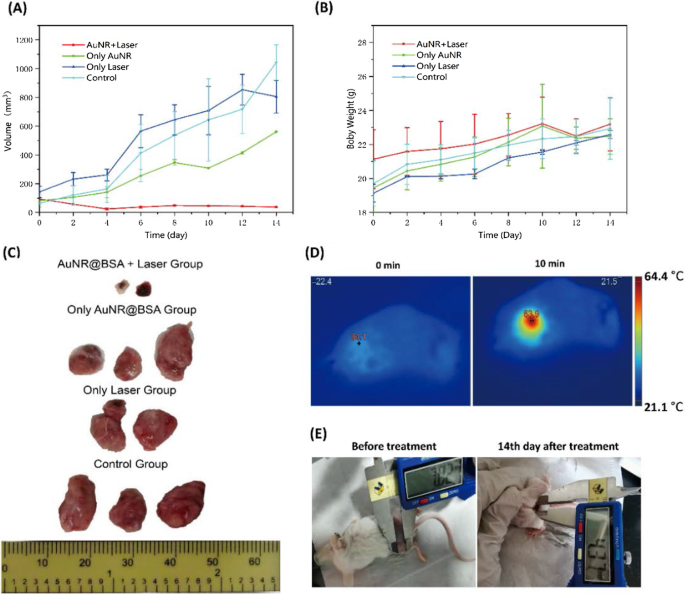
Tratamiento fototérmico de ratones portadores de tumores. un Volumen tumoral en función del tiempo en diferentes condiciones de tratamiento. b Cambios en el peso corporal de los ratones portadores de tumores en función del tiempo, después del tratamiento. c Fotografías de tejidos tumorales en diferentes grupos después de un tratamiento de 14 días. d Imágenes termográficas infrarrojas de ratones portadores de tumores expuestos a un láser de 1064 nm (0,75 W / cm 2 , 10 min) a los 10 min después de la inyección intratumoral de AuNR @ BSA. e Imágenes de ratones del grupo AuNR @ BSA_laser después del tratamiento. (media ± DE, n =2)
Además, se tomó TEM para el tumor aislado después del tratamiento fototérmico y el tumor no tratado. La AuNR se pudo observar en el tejido tumoral después del tratamiento fototérmico. Proporcionó evidencia adicional de que las nanovarillas de oro todavía tienen una excelente fotoestabilidad en el entorno del tejido tumoral (Fig. 7).
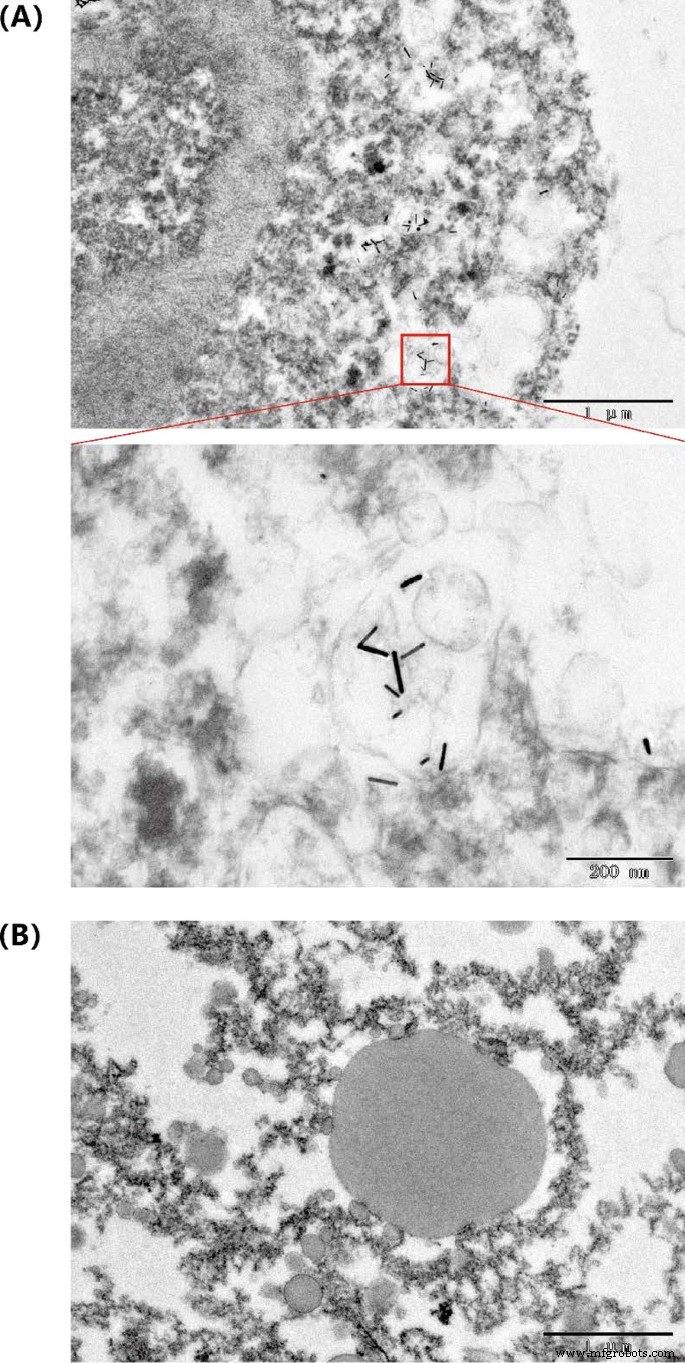
Micrografía electrónica de transmisión de AuNR @ BSA en tejido tumoral a Tumor tratado. b Tumor no tratado
Conclusión
Aquí, sintetizamos el AuNR @ BSA con el máximo de absorción SPR en la segunda ventana del infrarrojo cercano para la terapia fototérmica, como sus excelentes propiedades fototérmicas y biocompatibilidad. La biocompatibilidad del AuNR informado mejoró significativamente al recubrir con albúmina de suero bovino, y las propiedades fototérmicas no se vieron afectadas. The biodistribution of the intravenously injected AuNR@BSA indicates that large amounts of AuNR accumulated in the liver and spleen. The TEM image of AuNR@BSA inside tumor reveals that the high in vivo photostability of the AuNR and suggests that once upon injection, several phototreatment might be applied to reach the desired therapy outcomes. The excellent photothermal conversion of the reported AuNR was able to sufficiently inhibit tumor growth even under low light irradiation. The PTT of AuNR@BSA combined with other treatment strategies, such as immunotherapy and chemotherapy, would be promising for developing a useful tool for personalized, safe, and effective tumor treatment.
Availability of data and materials
The data set used and/or analyzed in this study can be obtained from the corresponding author upon reasonable request. All data generated or analyzed during this study is included in this published article.
Nanomateriales
- Nanopartículas plasmónicas
- Nanopartículas de oro para sensores de quimioterapia
- TPE de grado médico utilizado para la pelota de terapia ganadora de premios
- Nanopartículas de oro multifuncionales para aplicaciones terapéuticas y diagnósticas mejoradas:una revisión
- Nanopartículas para la terapia del cáncer:avances y desafíos actuales
- Marcos metal-orgánicos sensibles al medio ambiente como sistema de administración de fármacos para la terapia tumoral
- Síntesis y rendimiento in vitro de nanopartículas de hierro-platino recubiertas de polipirrol para terapia fototérmica e imágenes fotoacústicas
- Nanoconjuntos de ácido 5-aminolevulínico-escualeno para fotodetección y terapia de tumores:estudios in vitro
- Vesículas etosomales biocompatibles cargadas con nanopartículas de ácido 5-aminolevulínico / Au para terapia fotodinámica / fototérmica sinérgica transdérmica in vitro de cicatrices hipertróf…
- Nanorods de oro modificados con sílice conjugada con anticuerpo para el diagnóstico y la terapia fototérmica de Cryptococcus neoformans:un experimento in vitro
- Plataforma para tecnologías cuánticas usando oro



