Nanoconjuntos de ácido 5-aminolevulínico-escualeno para fotodetección y terapia de tumores:estudios in vitro
Resumen
La protoporfirina IX (PpIX) como fotosensibilizador natural derivado de la administración de ácido 5-aminolevulínico (5-ALA) ha encontrado uso clínico para el fotodiagnóstico y la terapia fotodinámica de varios cánceres. Sin embargo, el uso más amplio de 5-ALA en oncología se ve obstaculizado por su carga y polaridad que resultan en su capacidad reducida para atravesar barreras biológicas y alcanzar el tejido tumoral. Se necesitan plataformas avanzadas de administración de fármacos para mejorar la biodistribución de 5-ALA. Aquí, informamos sobre un nuevo enfoque para la entrega de 5-ALA. La estrategia de escualenoilación se utilizó para conjugar covalentemente 5-ALA con escualeno, un precursor natural del colesterol. Los nanoconjuntos 5-ALA-SQ se formaron por autoensamblaje en agua. Los nanoconjuntos fueron monodispersos con tamaño promedio de 70 nm, índice de polidispersidad de 0.12 y potencial ζ de + 36 mV. Mostraron una buena estabilidad durante varias semanas. La carga de fármaco de 5-ALA fue muy alta en un 26%. En células de cáncer de próstata humano PC3 y células de glioblastoma humano U87MG, se controló la producción de PpIX in vitro tras la incubación con nanoconjuntos. Fueron más eficientes en la generación de fluorescencia inducida por PpIX en células cancerosas en comparación con 5-ALA-Hex de 1,0 a 3,3 mM en tiempos de incubación cortos y largos. En comparación con el 5-ALA, mostraron un rendimiento de fluorescencia superior a las 4 h, que disminuyó a las 24 h. 5-ALA-SQ presenta una nueva plataforma de nano-entrega con gran potencial para la administración sistémica de 5-ALA.
Antecedentes
La nanotecnología médica ha introducido nuevas y prometedoras plataformas de administración de fármacos. Se componen de nanomateriales biocompatibles y biodegradables que ayudan a mejorar la estabilidad química y el perfil farmacocinético de compuestos farmacológicamente activos mientras proporcionan una entrega controlada en el sitio de acción [1, 2, 3]. Sin embargo, hasta ahora solo han llegado al mercado unos pocos sistemas de nanopartículas. Los principales inconvenientes de las nanopartículas (NP) existentes son principalmente su mala carga de fármaco (normalmente menos del 5%) y el "efecto de liberación explosiva" que provoca una liberación prematura de una parte significativa del fármaco antes de llegar al sitio objetivo. Esto provoca efectos secundarios adversos y puede provocar toxicidad y pérdida de actividad farmacológica [4].
El escualeno (SQ) es un triterpeno lineal con la fórmula química C 30 H 50 y un precursor del colesterol y otros esteroides [5]. En el cuerpo humano, el escualeno se sintetiza en el hígado y la piel y es transportado por lipoproteínas de baja densidad (LDL) y lipoproteínas de muy baja densidad (VLDL) en la sangre [6]. En el contexto de la terapia tumoral, el escualeno mostró un fuerte efecto de potenciación sobre ciertos agentes quimioterapéuticos [7]. Debido a que se encuentra ampliamente en la naturaleza y es seguro, el escualeno ha encontrado aplicaciones en la tecnología farmacéutica como excipiente en la preparación de emulsiones lipídicas para la administración de vacunas, diversos compuestos activos y genes [6, 8, 9]. Se ha encontrado que el escualeno es adecuado para la conjugación covalente con diferentes fármacos. Los nanosistemas avanzados creados de esta manera incorporan escualeno conjugado con agentes quimioterapéuticos como gemcitabina [10,11,12], paclitaxel [13], cisplatino [14] o doxorrubicina [15]. Este enfoque se denomina "escualenoilación" e implica una estrategia de profármacos con la formación de sistemas nano-coloidales donde el principio activo se une covalentemente [16, 17]. Los nanoconjuntos basados en escualeno (NA) se forman mediante el autoensamblaje de componentes funcionales en medios acuosos y se caracterizan por una alta carga de fármaco inherente [18]. Se ha descubierto que la escualenoilación mejora la estabilidad del fármaco y aumenta la solubilidad de los fármacos poco solubles en agua, lo que mejora la biodisponibilidad y prolonga la vida media del fármaco en la circulación sistémica [14, 16]. En la mayoría de los casos, estos AN autoensamblados muestran una mejor actividad farmacológica que el fármaco original [16, 19]. Además, la escualenoilación proporciona un medio para construir NA que contienen una modalidad tanto terapéutica como de imagen [20]. Couvreur y colaboradores han informado de NA teranósticas similares mediante la incorporación de un agente de resonancia magnética en nanoconjuntos de escualenoil-gemcitabina (SQgem) [14]. Estos tipos de sistemas multifuncionales pueden ser de gran importancia en el desarrollo de nuevos agentes teranósticos para la medicina personalizada.
En el contexto de la terapia del cáncer, la administración de una pequeña molécula de ácido 5-aminolevulínico (5-ALA) (Fig. 1) ha llevado al uso clínico de 5-ALA para la terapia fotodinámica (TFD) [21,22,23]. , fotodiagnóstico (DP) [24] y resección tumoral guiada por fluorescencia en pacientes con glioma de cáncer de cerebro [25,26,27]. La teranología se logra mediante el metabolismo del 5-ALA y la acumulación selectiva de protoporfirina IX (PpIX) dentro del tejido canceroso como consecuencia de la inhibición por retroalimentación omitida del ciclo del hemo [22]. Sin embargo, la eficacia de 5-ALA PD y PDT se ve seriamente obstaculizada por su naturaleza bipolar a pH neutro que se encuentra en el torrente sanguíneo. Se han realizado diferentes intentos para mejorar la estabilidad y el perfil farmacocinético del 5-ALA. Tanto el extremo amino como el carboxílico del 5-ALA se han modificado mediante varios enfoques [28]. La esterificación del grupo carboxilo del 5-ALA ha dado lugar al éster metílico del 5-ALA (Metvix®) [29] y se utiliza en el tratamiento tópico de la queratosis actínica, el carcinoma de células basales y el acné agudo. El éster hexílico de 5-ALA (5-ALA-Hex) (Hexvix®) ha obtenido la autorización de comercialización para el fotodiagnóstico (EP) del cáncer de vejiga [30, 31] y se explota experimentalmente para el tratamiento del cáncer de cuello uterino y el acné severo [32 , 33, 34].
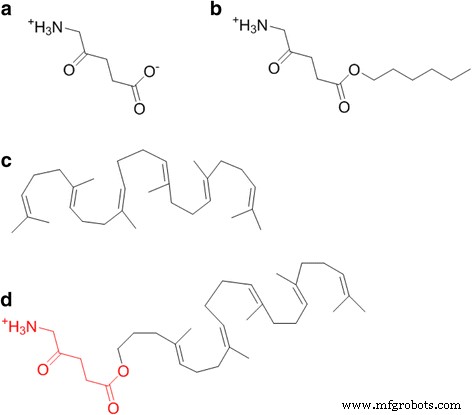
Estructuras químicas de elementos básicos de NA. 5-ALA ( a ), 5-ALA-Hex ( b ), escualeno ( c ) y 5-ALA-SQ ( d )
Sin embargo, con la excepción de Gliolan ™, el uso clínico de 5-ALA y sus derivados se limita principalmente a la administración tópica. Esto limita su uso en tipos de cáncer más importantes, como el de mama, colorrectal, de pulmón y de próstata. Los intentos de ampliar el uso de 5-ALA tienen derivados de 5-ALA sensibles a la fosfatasa modificados en el extremo amino que han mostrado una actividad muy prometedora recientemente [35, 36]. Además, se han realizado intentos para encapsular 5-ALA en diferentes nanosistemas, incluidos los NA poliméricos [37,38,39] o los liposomas [40,41,42,43] y su conjugación en dendrímeros [44, 45] o NP de oro [46 , 47]. Aunque algunas de estas soluciones han ayudado a mejorar la estabilidad del 5-ALA y su perfil farmacocinético, ninguno de los intentos antes mencionados ha resultado en un candidato clínico exitoso en el campo de la nanomedicina del cáncer.
El objetivo de este trabajo fue el diseño y síntesis del bloque de construcción conjugado de 5-ALA-escualeno (5-ALA-SQ) (Fig.1d) que se autoensambla en medio acuoso y contiene una alta carga de fármaco de 5-ALA, un requisito previo para la actividad farmacológica en cánceres. Los NA se probaron en dos líneas de células cancerosas diferentes para determinar sus capacidades de fluorescencia de PD. Combinado con informes recientes de NA basados en escualeno que explotan las lipoproteínas plasmáticas para lograr un direccionamiento indirecto contra el cáncer [48], este enfoque de nanotecnología 5-ALA amplía el uso de 5-ALA para la EP y la TFD de diferentes cánceres, como el cáncer de próstata utilizado en este estudio. .
Resultados y discusión
Síntesis de bloques de construcción 5-ALA-SQ
Se utilizó una estrategia química convergente eficiente para sintetizar el bloque de construcción 5-ALA-SQ a partir de escualeno y 5-ALA (Fig. 2). El 5-ALA se protegió primero en el extremo amino con N -Grupo protector Boc en condiciones estándar. Alcohol de escualeno inductor de nanoensamblaje ( 3 ) se sintetizó a partir de escualeno en cuatro pasos sintéticos de acuerdo con los procedimientos descritos en la literatura [49]. Boc-5-ALA ( 2 ) y alcohol de escualeno ( 3 ) luego se acoplaron en presencia de EDC y DMAP para producir el derivado de éster protegido ( 4 ) con buen rendimiento. La desprotección final de Boc tuvo que realizarse en condiciones ácidas suaves para evitar la adición electrofílica sobre el armazón de escualeno. El producto final se purificó mediante HPLC de fase inversa para producir el bloque de construcción de NA con buen rendimiento.
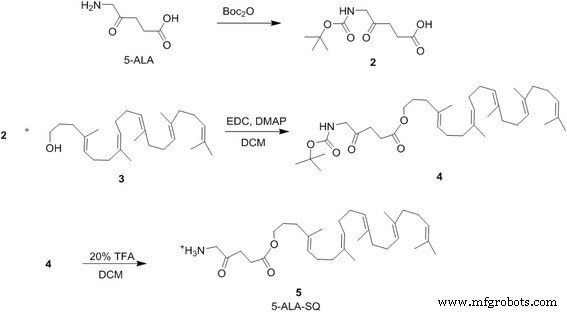
Síntesis de bloques de construcción 5-ALA-SQ. 5-ALA-SQ se sintetizó en cuatro pasos sintéticos utilizando síntesis convergente de 5-ALA y SQ
Nanoensamblajes 5-ALA-SQ
Para lograr una entrega eficiente de un compuesto activo por nanopartículas (NP) a su sitio de acción, parámetros como el tamaño, la forma y la carga superficial de las nanopartículas juegan un papel importante y gobiernan la farmacocinética de los sistemas de nanopartículas en el cuerpo [ 50]. En particular, el tamaño de partícula rige varios fenómenos farmacocinéticos como la vida media de NP en la circulación sistémica, el secuestro por macrófagos y la extravasación a través de la vasculatura con fugas en el sitio de acción [51]. La forma y el tamaño de las nanopartículas regulan su capacidad de extravasarse a través de las fenestraciones que se encuentran en la vasculatura [50, 51]. El tamaño y la forma también son muy importantes para la focalización activa y la absorción en las células, ya que los NP más pequeños y las formas esféricas tienen un área de superficie más pequeña, por lo que los puntos de contacto son mucho más limitados en comparación con los sistemas de nanopartículas no esféricas más grandes [51].
El autoensamblaje del bloque de construcción 5-ALA-SQ se produjo espontáneamente en medios acuosos. Los NA se formaron por nanoprecipitación. El conjugado de 5-ALA-SQ se disolvió en disolventes orgánicos y se añadió gota a gota en agua. La evaporación total de los disolventes orgánicos produjo una solución acuosa de NA. Los NA de 5-ALA-SQ fueron monodispersos con un índice de polidispersidad bajo de 0,12. Las mediciones de movilidad electroforética dieron un potencial ζ de 36 mV, y la dispersión dinámica de la luz (DLS) reveló una distribución monodispersa de NA con un tamaño promedio de 70 nm (Fig. 3). El rango de tamaño de NA ofrece un buen potencial para una circulación prolongada en el torrente sanguíneo [50]. No obstante, los NA de 5-ALA-SQ son significativamente más pequeños que los compuestos SQ informados anteriormente, que oscilan entre 100 y 300 nm, lo que indica una disposición supramolecular diferente [19].
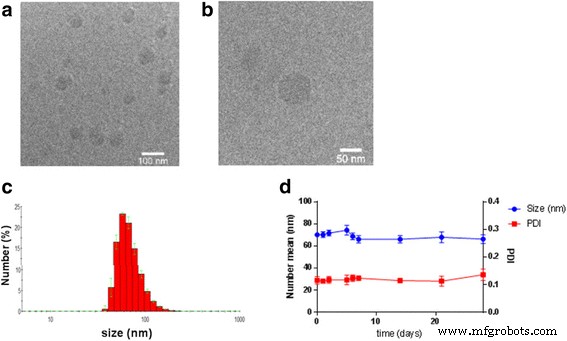
Caracterización de NA 5-ALA-SQ. Bajo ( a ) y alto ( b ) aumento de imágenes crio-TEM, análisis DLS ( c ) y estabilidad a 4 ° C ( d )
El tamaño más pequeño podría deberse a grupos amino cargados positivamente y a una molécula de 5-ALA relativamente pequeña en comparación con el resto SQ. Se ha demostrado que la variación de pequeñas moléculas unidas al escualeno introduce cambios en el autoensamblaje y el empaquetamiento de conjugados compuesto-escualeno, alterando consecuentemente la forma y el tamaño de los NA [16]. Es posible que el grupo amino altamente cargado positivamente del 5-ALA se oriente hacia la masa de agua mientras que las cadenas lipofílicas ocupan el interior de estos NA; sin embargo, queda por dilucidar la estructura supramolecular exacta. A pesar del tamaño significativamente más pequeño en comparación con otros nanocompuestos de escualeno, los NA muestran una excelente estabilidad en almacenamiento y el tamaño y el PDI permanecen constantes durante varias semanas.
Otro aspecto importante de los nuevos NA 5-ALA-SQ es que logran una carga de fármaco del 26%, que es alta en comparación con otros sistemas de nanopartículas de 5-ALA reportados donde la carga era mucho menos eficiente [37, 38, 41]. La carga de fármaco es muy importante en la administración de NP porque en NP con poca carga de fármaco, la dosis administrada puede no ser suficiente para alcanzar una concentración farmacológicamente activa en los tejidos diana [4]. La carga podría determinarse mediante un cálculo simple teniendo en cuenta los pesos moleculares de 5-ALA y 5-ALA-SQ, ya que el 5-ALA está unido covalentemente al armazón de escualeno en una proporción molar de 1:1.
Mediciones cinéticas de fluorescencia de PpIX en células cancerosas
Se evaluó la formación de PpIX dependiente del tiempo en células de cáncer de próstata humano PC3 y glioblastoma U87MG incubados con 5-ALA-SQ NA y 5-ALA-Hex como referencia. La Figura 4 presenta la formación de PpIX en células de cáncer de próstata humano PC3 expuestas a concentraciones crecientes de 5-ALA-SQ NA o 5-ALA-Hex durante 24 h.
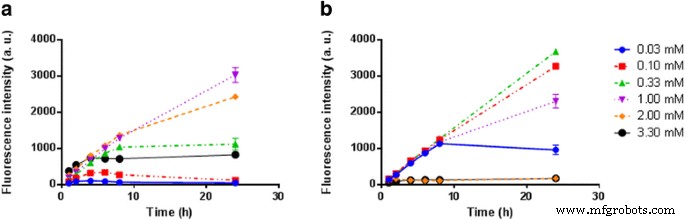
Medidas de fluorescencia cinética de la acumulación de PpIX en células PC3. Las células se incubaron con concentraciones crecientes de 5-ALA-SQ NA ( a ) o 5-ALA-Hex ( b )
Se observaron perfiles de fluorescencia de PpIX dependientes de la concentración para NA de 5-ALA-SQ. A 1,0 y 2,0 mM, la fluorescencia de PpIX aumentó de manera constante durante 24 h mientras alcanzaba una meseta después de 8 h de incubación para concentraciones más bajas. Por otro lado, 5-ALA-Hex indujo la mayor acumulación de PpIX en un rango de concentración más bajo entre 0,10 y 0,30 mM como se informó anteriormente [35, 52]. Sin embargo, se descubrió que el 5-ALA-Hex en concentraciones superiores a 1 mM es tóxico para las células, lo que reduce la fluorescencia general observada e impide su uso [36].
A continuación, se realizó la acumulación de PpIX dependiente de la dosis en células de cáncer de glioblastoma humano PC3 y U87MG con el objetivo de estimar la dosificación óptima de NA. La intensidad de la fluorescencia a las 4 y 24 h de incubación con 5-ALA-SQ NA y 5-ALA-Hex se muestra en la Fig. 5. Muy importante, 5-ALA-SQ NA indujo la producción de PpIX en ambas líneas celulares. Además, los niveles máximos de fluorescencia son comparables con el control ALA-Hex en ambas líneas celulares. También puede observarse que en las células PC3, las concentraciones de 1,0 y 2,0 mM de NA de 5-ALA-SQ fueron óptimas para inducir la mayor acumulación de PpIX. En las células U87MG, no hubo diferencias significativas entre las diferentes concentraciones de NA de 5-ALA-SQ para tiempos de incubación cortos (Fig. 5c). A las 24 h, se encontró que la acumulación de PpIX dependía de la concentración de 5-ALA-SQ NA o 5-ALA-Hex similar a las células PC3. Se encontró una disminución en la inducción de PpIX algo similar a ALA-Hex después de un período más largo de incubación a concentraciones más altas de NA de 5-ALA-SQ que eran más sensibles a la presencia de NA.
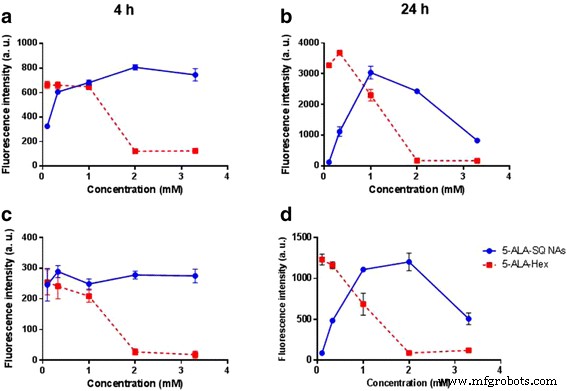
Curvas dosis-respuesta. Acumulación de PpIX dependiente de la concentración con 5-ALA-SQ NA (azul) y 5-ALA-Hex (rojo) en PC3 ( a , b ) y U87MG ( c , d ) células después de 4 h (izquierda) y 24 h (derecha) de incubación
La Figura 5 demuestra que a las 24 h, las curvas de producción de PpIX tienen forma de campana en las células PC3 y U87MG. Mientras que la concentración 1 mM de 5-ALA-SQ NA indujo la mayor acumulación de PpIX en las células PC3, las células U87MG toleraron concentraciones más altas y se observó un aumento en la fluorescencia de PpIX hasta 2 mM de 5-ALA-SQ NA. En general, se necesitaban concentraciones más altas de 5-ALA-SQ NA para inducir eficazmente la biosíntesis de PpIX en comparación con 5-ALA-Hex, presumiblemente debido a las diferentes tasas de escisión del enlace éster dentro de las células cancerosas. Se observó una disminución en la producción de PpIX cuando se utilizaron concentraciones superiores a 1 mM de 5-ALA-Hex debido a la toxicidad no específica de 5-ALA-Hex. Este efecto fue mucho menos pronunciado para el 5-ALA-SQ donde la fluorescencia los niveles comenzaron a descender sólo a la concentración más alta probada (3,3 mM) y tiempos de incubación prolongados (Fig. 5b, d). Sin embargo, los niveles de fluorescencia fueron similares para ambos compuestos sin ningún retraso de fluorescencia observado para los NA.
Los NA también se analizaron en el glioblastoma U87MG frente al control de 5-ALA que se comercializa para la EP del glioblastoma durante la resección quirúrgica. La Figura 6 presenta la fluorescencia de la célula U87MG después de 4 y 24 h. Los NA de 5-ALA-SQ indujeron una fluorescencia significativamente mayor después de 4 h en comparación con el 5-ALA, que es muy relevante en un entorno clínico. A las 24 h, el perfil de fluorescencia se desplaza a favor del 5-ALA a concentraciones más bajas, ya que la captación lenta y activa de 5-ALA proporciona cantidades suficientes de 5-ALA dentro de las células. Los NA todavía muestran niveles de fluorescencia similares a los del 5-ALA a concentraciones óptimas de 1,0 y 2,0 mM de NA (Fig. 6b).
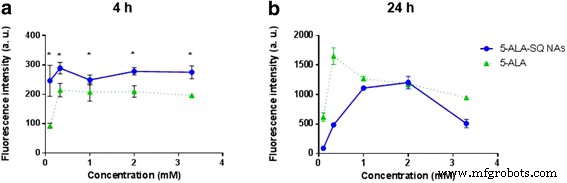
Curvas dosis-respuesta. Acumulación de PpIX dependiente de la concentración en células U87MG después de 4 h ( a ) y 24 h ( b ) incubación con 5-ALA-SQ NA (azul) y 5-ALA (verde)
En la práctica clínica, el 5-ALA se administra por vía tópica u oral, pero debido a su naturaleza cargada, solo una pequeña porción de la dosis inicial ingresa a las células diana a través de transportadores de péptidos endógenos como los transportadores PEPT1, PEPT2 o BETA, según el tipo de célula. [40, 53]. Estudios recientes sobre NA de un derivado de SQgem indican que la entrada celular se rige por la difusión potenciada por la albúmina de bloques de construcción de una sola molécula y se encontró que es altamente dependiente de la presencia de proteínas extracelulares [54, 55]. Además, los NA fluorescentes de color rojo lejano que informamos recientemente también demostraron una rápida internalización, y los experimentos cinéticos de fluorescencia de 5-ALA-SQ y las curvas de dosis-respuesta corroboran la internalización de bloques de construcción de una sola molécula y el metabolismo posterior eficiente para producir PpIX fluorescente.
Conclusiones
En este estudio de prueba de concepto in vitro, se utilizó una estrategia química convergente para sintetizar el bloque de construcción 5-ALA-SQ a partir de escualeno y 5-ALA. Los NA de 5-ALA-SQ se prepararon mediante nanoprecipitación espontánea en agua. Los NA eran monodispersos y estables con un tamaño promedio de 70 nm, índice de polidispersidad de 0,12, potencial ζ positivo de 36 mV y alta carga de 5-ALA del 26%. La producción de PpIX se evaluó in vitro en dos líneas de células cancerosas midiendo el aumento de fluorescencia a lo largo del tiempo y se comparó con 5-ALA y 5-ALA-Hex. Los resultados mostraron que los NA SQ-ALA son muy eficientes para inducir la producción de PpIX en los tipos de células cancerosas PC3 y U87MG. Superan al 5-ALA-Hex en la inducción de fluorescencia a concentraciones más altas en tiempos de incubación de 4 y 24 h in vitro; sin embargo, en comparación con el 5-ALA, muestran una inducción de fluorescencia superior en tiempos de incubación más cortos. Dentro del alcance de estos hallazgos, podemos concluir que los NA 5-ALA-SQ presentan una solución nanotecnológica atractiva para superar los inconvenientes farmacocinéticos del 5-ALA. Además, los experimentos in vivo evaluarán su potencial para la administración sistémica de 5-ALA para la terapia de tumores con PD por fluorescencia y TFD.
Métodos / Experimental
Los reactivos se adquirieron de proveedores comerciales Sigma-Aldrich (Bucks, Suiza) y Acros Organics (Basilea, Suiza) y se usaron sin purificación adicional. Los disolventes de RMN deuterados se obtuvieron de Cambridge Isotope Laboratories (Tewksbury, EE. UU.). Tetrahidrofurano (THF) y diclorometano (CH 2 Cl 2 ) se obtuvieron a partir de un sistema de secado basado en columna de alúmina de ingeniería anhidra. Todos los demás disolventes utilizados fueron de calidad HPLC. N, N-dimetilformamida (DMF), metanol (CH 3 OH), éter dietílico (Et 2 O) y acetona se adquirieron de Sigma-Aldrich (Buchs, Suiza). Se adquirió acetato de etilo (AcOEt) de Biosolve (Dieuze, Francia); acetonitrilo (CH 3 CN) fue suministrado por Carlo Erba Reagents (Balerna, Suiza). Se adquirió hexano ≥ 95% de n-hexano de Fisher Chemical (Basilea, Suiza). El agua utilizada para las preparaciones se desionizó mediante un sistema de agua de laboratorio Milli-Q (Millipore, Molsheim, Francia). Las reacciones químicas se realizaron utilizando septos de jeringa estándar con presión positiva de argón para asegurar condiciones anhidras.
La cromatografía en capa fina (TLC) se realizó con placas de sílice con respaldo de aluminio (Merck-Keiselgel 60 F254) con una fase móvil adecuada y se visualizó utilizando una lámpara de fluorescencia UV (254 y 366 nm) y / o desarrollada con ninhidrina, sulfúrico al 20%. ácido o ácido fosfomolíbdico (PMA). La cromatografía ultrarrápida se realizó en una máquina PuriFlash® 4100 automatizada de Interchim (Montlucon, Francia) utilizando columnas de sílice Interchim puriFlash® HP 30 μm equipadas con un detector PDA (200-800 nm) y un recolector de fracciones automático. El perfil de elución se controló utilizando el software Flash Interchim versión 5.0x. La columna de HPLC semipreparativa se realizó en una columna C8 Waters Symmetry 300TM - 5 μm (19 x 150 mm) (Baden-Dättwil, Suiza). La UPLC analítica se realizó usando una columna Macherey-Nagel EC50 / 2 Nucleodur Gravity de 1,8 μm (50 x 2,1 mm) montada en un sistema de agua equipado con un detector Waters PDA (Baden-Dättwil, Suiza). Tampón A =CH 3 CN + ácido fórmico al 0,1%) y tampón B =H 2 O + 0,1% de ácido fórmico. Velocidad de flujo =400,0 μL / min a 25 ° C. 1 H y 13 Los espectros de RMN C se registraron en espectrómetros Varian Gemini 300 MHz, Varian Innova 500 MHz o Bruker Avance III Cryo 600 MHz a 298 K. Los cambios químicos (δ) se expresan en partes por millón (ppm) y las constantes de acoplamiento (J) en hercios (Hz). s para singlete, d para doblete, dd para doblete de dobletes, t para triplete, q para cuarteto ym para multiplete. Los picos de disolvente residual se utilizaron como referencia interna para los desplazamientos químicos de protones y carbono. Los espectros de RMN se procesaron con el paquete de software Mnova versión 10.0.2. La espectrometría de masas de baja resolución (LRMS) se llevó a cabo en un instrumento HTS PAL-LC10A - API 150Ex en ESI (modo positivo). La espectrometría de masas de alta resolución (HRMS) se llevó a cabo en un instrumento QSTAR Pulsar (AB / MDS Sciex) en ESI (modo positivo). Las estructuras químicas se dibujaron y nombraron de acuerdo con la nomenclatura IUPAC usando el paquete de software ChemBioDraw Ultra versión 14.0.0.117. El pH se midió en un medidor de pH Metrohm 691 usando un electrodo de punta de lanza (Zofingue, Suiza), calibrado con tampones Metrohm. Los análisis estadísticos se realizaron utilizando el software GraphPad Prism 6, 2016, (GraphPad Software). P valor <0,05 se consideró estadísticamente significativo.
Síntesis del Building Block SQ-ALA
Ácido 5- (terc-butoxicarbonilamino) -4-oxopentanoico (2)
Se sintetizó Boc-5-ALA de acuerdo con el procedimiento publicado. Los datos espectroscópicos son idénticos a los de la bibliografía [56]. 1 H RMN (600 MHz, DMSO-d6) δ 12,12 (s, 1 H), 7,06 (t, J =5,9 Hz, 1 H), 3,76 (d, J =5,9 Hz, 2 H), 2,61 (t, J =6,6 Hz , 2 H), 2,40 (t, J =6,5 Hz, 2 H), 1,38 (s, 9 H). 13 C NMR (151 MHz, DMSO) δ 206,62, 174,07, 156,21, 78,54, 49,97, 40,38, 40,24, 40,11, 39,97, 39,83, 39,69, 39,55, 34,22, 28,64. [M + H] + 232.1, encontrado 232.7.
(4E, 8E, 12E, 16E) -4,8,13,17,21-pentametildocosa-4,8 , 12,16,20-pentaen-1-ol (3)
Alcohol de escualeno 3 se sintetizó a partir de escualeno en cuatro etapas sintéticas con un rendimiento del 23,7% como aceite incoloro de acuerdo con los procedimientos descritos [49]. 1 H RMN (300 MHz, CDCl 3 ) δ 5,17-5,06 (m, 5H, CH), 3,62 (q, J =6,3 Hz, 2H, CH 2 -OH), 2,17 - 1,92 (m, 18H, CH 2 ), 1,67 (s, 3H, CH 3 ), 1,59 (m, 17 H, CH 3 y CH 2 ). 13 C NMR (75 MHz, CDCl 3 ) δ 135,35, 135,17, 135,14, 134,81, 131,49, 125,05, 124,64, 124,60, 124,47, 63,07, 39,98, 39,95, 39,89, 36,24, 30,92, 28,48, 26,98, 26,88, 26,78, 25,94, 17,92, 16,28, 16,23, 16,08. LRMS (ESI):m / z calculado para [M + NH 4 ] + 404.4, encontrado 404.8.
(4E, 8E, 12E, 16E) -4,8,13,17,21-pentametildocosa-4,8 , 12,16,20-pentaen-1-ilo 5 - ((terc-butoxicarbonil) amino) -4-oxopentanoato (4)
Alcohol de escualeno ( 3 ) (100 mg, 0,26 mmol), EDC (74 mg, 0,38 mmol) y DMAP (94 mg, 0,78 mmol) y ácido 5- (terc-butoxicarbonilamino) -4-oxopentanoico (2) (77 mg, 0,34 mmol) se disolvieron en DCM (15 ml). Después de agitar durante la noche a temperatura ambiente, el disolvente se evaporó a presión reducida y el producto bruto se purificó por cromatografía ultrarrápida usando gradiente de DCM / acetato de etilo (EA) dando un aceite incoloro (108 mg, 0,18 mmol, 70%). 1 H RMN (300 MHz, CDCl 3 ) δ 5,31 - 5,20 (ancho s, 1H), 5,13 - 5,07 (m, 5H), 4,09 - 3,95 (m, 4H), 2,75 - 2,53 (m, 4H), 2,02 - 1,95 (m, 20H), 1,64 ( s, 3 H), 1,63 - 1,50 (m, 19 H), 1,41 (s, 9 H). 13 C NMR (75 MHz, CDCl3) δ 204.46, 172.65, 135.30, 135.16, 135.09, 133.75, 131.43, 125.34, 124.60, 124.57, 124.48, 124.45, 64.81, 50.53, 39.96, 39.93, 39.87, 35.92, 34.56, 28.52, 28.47 , 28.43, 28.24, 28.02, 26.97, 26.86, 25.92, 23.11, 17.90, 16.25, 16.21, 16.06. LRMS (ESI):m / z calculado para [M + NH 4 ] + 617.5, encontrado 617.8.
Sal de ácido trifluoroacético de 5-amino - (((4E, 8E, 12E, 16E) -4,8,13 , 17,21-pentametildocosa-4,8,12,16,20-pentaen-1-il) oxi) -4-oxopentanoato (5)
Compuesto 4 (34 mg, 57 mmol) se disolvió en DCM (2,0 ml). Se añadió ácido trifluoroacético (TFA) (200 µl) y la mezcla de reacción se agitó a temperatura ambiente. Después de 10 min, los disolventes se evaporaron al vacío a baja temperatura y las trazas de TFA se eliminaron por coevaporación con EA (3 x 10 ml). El producto crudo se purificó por RP-HPLC usando H 2 completo Gradiente de O / AcN (TFA al 0,025%) que produce un aceite incoloro (25 mg, 74%). %). 1 H RMN (300 MHz, CDCl 3 ) δ 5,31 - 5,20 (ancho s, 1H), 5,13 - 5,07 (m, 5H), 4,09 - 3,95 (m, 4H), 2,75 - 2,53 (m, 4H), 2,02 - 1,95 (m, 20H), 1,64 ( s, 3 H), 1,63 - 1,50 (m, 19 H). LRMS (ESI):m / z calculado para [M + H] + 500,4, encontrado 500,6.
Preparación de nanoconjuntos
Los NA se prepararon mediante nanoprecipitación que se describe en detalle en otro lugar [20]. Brevemente, componente básico 5 (1,2 mg, 2,0 μmol) se disolvió en un 50/50 V / V mezcla acetona / etanol (500 μL). Luego, la fase orgánica se agregó gota a gota usando una micro-jeringa en agua MilliQ (1.25 mL) a 100 μL / min con agitación magnética. Después de 5 min con agitación, se retiró la barra de agitación magnética y se eliminaron los disolventes orgánicos y el exceso de agua usando un evaporador rotatorio a 30 ° C. La concentración final de nanoconjuntos fue de 2,00 mM.
Caracterización de 5-ALA-SQ NAs
La carga de 5-ALA de 5-ALA.SQ NA se calculó a partir de las contribuciones respectivas de los pesos moleculares de 5-ALA y del conjugado 5-ALA-SQ de la siguiente manera [19]:
$$ \ mathrm {Cargando} \ \ left (\% \ right) =\ frac {\ mathrm {MW} \ \ left (5- \ mathrm {ALA} \ right)} {\ mathrm {MW} \ left (5 - \ mathrm {ALA} - \ mathrm {SQ} \ right)} \ times 100 $$El diámetro hidrodinámico de los NA se midió mediante dispersión de luz dinámica (DLS) utilizando un instrumento NANO ZS de Malvern (Worcestershire, Reino Unido) con el software ZetaSizer 7.01. Los análisis se realizaron con láser He-Ne de 4 mW (633 nm) a un ángulo de dispersión de 173 ° a 25 ° C en una microcubeta de poliestireno (PS) de Brand (Wertheim, Alemania). El potencial zeta (ZP) se determinó usando el mismo instrumento Nano ZS de Malvern en células capilares plegadas DTS 1070 de Malvern. La distribución de tamaño y el diámetro medio de tamaño se calcularon a partir de los datos. La estabilidad de los NA almacenados a 4 ° C fue analizada por DLS en puntos de tiempo regulares durante un período de 1 mes.
La morfología de los NA se evaluó mediante microscopio electrónico de transmisión criogénica (cryo-TEM) utilizando TECNAI® G 2 Microscopio esférico (FEI, Thermo Fisher Scientific) equipado con una cámara digital TCL de alta resolución de 2000 por 2000 píxeles (Gräfelfing, Alemania). Las muestras de hielo vitrificado se prepararon utilizando el crio-émbolo Virtobot (FEI, Thermo Fisher Scientific). Se aplicaron NA (2,0 μL, 2,0 mM) a rejillas Quantifoil Cu / Rh 200 mesh R3.5 / 1 (SPI, West Chester, EE. UU.) Y se vitrificaron con etano líquido.
Cultivo celular
Se cultivaron células de cáncer de próstata humano PC3 (ATTC® CRL-1435 ™) y células de glioblastoma humano U87MG (ATTC® HTB-14 ™) y se mantuvieron mediante pases en serie en una mezcla de nutrientes F-12K (21127-022, Thermo Fisher Scientific) o como mínimo Essential Media (31095-029, Thermo Fisher Scientific), respectivamente. Los medios celulares se complementaron con suero de ternero fetal (10%, CVFSVF00-01, Eurobio), estreptomicina (100 μL / mL) y penicilina (100 UI / mL, 15140-122, Thermo Fisher Scientific). Las células se cultivaron a 37 ° C en una atmósfera humidificada que contenía 95% de aire y 5% de CO 2.
Mediciones cinéticas de fluorescencia in vitro PpIX
Se sembraron células de cáncer de próstata humano PC3 (12.000 células / pocillo) y células de glioblastoma U87MG (10.000 células / pocillo) en placas de 96 pocillos (placa negra de fondo transparente, 3603, Corning). Al día siguiente, las células se expusieron a concentraciones crecientes de 5-ALA-SQ NA, 5-ALA-Hex y 5-ALA en medios sin suero. La fluorescencia de PpIX se registró con un lector de placas (Safire, Tecan, Suiza) en diferentes momentos. La longitud de onda de excitación se fijó en 405 nm y la longitud de onda de emisión en 630 nm. Valores medios y d.e. para cada concentración en cada punto de tiempo por placa se restaron con el valor de referencia (sin tratamiento) y se trazaron para cada línea celular.
Nanomateriales
- Nanofibras y filamentos para una mejor administración de fármacos
- Nanopartículas para la terapia del cáncer:avances y desafíos actuales
- Marcos metal-orgánicos sensibles al medio ambiente como sistema de administración de fármacos para la terapia tumoral
- Nanopartículas de albúmina cargadas con resveratrol con circulación sanguínea prolongada y biocompatibilidad mejorada para una terapia de tumores pancreáticos dirigida altamente eficaz
- Síntesis y rendimiento in vitro de nanopartículas de hierro-platino recubiertas de polipirrol para terapia fototérmica e imágenes fotoacústicas
- Vesículas etosomales biocompatibles cargadas con nanopartículas de ácido 5-aminolevulínico / Au para terapia fotodinámica / fototérmica sinérgica transdérmica in vitro de cicatrices hipertróf…
- Anticuerpo monoclonal de heparanasa marcada con nanopartículas de oro magnético y su aplicación posterior para la obtención de imágenes por resonancia magnética tumoral
- Nanorods de oro modificados con sílice conjugada con anticuerpo para el diagnóstico y la terapia fototérmica de Cryptococcus neoformans:un experimento in vitro
- Liposoma paramagnético de enfoque dual de integrina αvβ 3 y NRP-1 para la detección temprana de tumores en imágenes de resonancia magnética
- Sistema de administración de fármacos de doble respuesta fototérmica / pH de rGO modificado con HBP terminado en amino y la terapia quimio-fototérmica en células tumorales
- Nanogeles activados por estímulos duales en respuesta a cambios de temperatura y pH para la liberación controlada de fármacos



