Síntesis de puntos cuánticos de tipo II / tipo I de ZnSe / CdS / ZnS con supresión de reabsorción y su aplicación para el ensayo inmunoabsorbente
Resumen
Divulgamos un método de un solo recipiente libre de fosfina para sintetizar puntos cuánticos (QD) de núcleo-capa de ZnSe / CdS / ZnS con estructuras compuestas de tipo II / tipo I y las consiguientes propiedades de supresión de la reabsorción. Los QD sintetizados poseen una emisión roja de alta eficiencia (con un rendimiento cuántico del 82%) y una alta estabilidad óptica. En comparación con los QD de tipo I, los QD de ZnSe / CdS / ZnS muestran un desplazamiento de Stokes más grande y una menor reabsorción, lo que puede reducir la pérdida de emisión y mejorar el nivel de salida de fluorescencia. Los QD de ZnSe / CdS / ZnS se utilizan como etiquetas fluorescentes para aprovechar su aplicación en el ensayo de inmunoabsorción ligado a fluorescencia (FLISA) por primera vez en la detección de proteína C reactiva (CRP) con un límite de detección (LOD) de 0,85. ng / mL, que es más sensible que el FLISA basado en CdSe / ZnS tipo I QD (1,00 ng / mL). Los resultados indican que los QD de ZnSe / CdS / ZnS tipo II / tipo I pueden ser buenos candidatos para aplicaciones en la detección de información biomédica.
Antecedentes
Los puntos cuánticos (QD) semiconductores de núcleo / capa fluorescente se caracterizan por las excelentes propiedades ópticas, como un rango de emisión más amplio, mayores rendimientos cuánticos (QY) de fotoluminiscencia (PL) y una mayor estabilidad óptica y química que los tintes orgánicos tradicionales. Estas ventajas abren oportunidades para avances revolucionarios en etiquetas fluorescentes para diagnóstico biomédico, imágenes moleculares y campo fotoeléctrico [1, 2, 3, 4, 5, 6, 7]. De acuerdo con la alineación de la banda entre los materiales del núcleo y la carcasa, las QD de núcleo / carcasa se pueden clasificar como estructuras de tipo I, tipo I inverso y tipo II. QD de tipo I caracterizados por la estructura de alineación de banda "anidada", que puede confinar tanto los electrones como los huecos a la región del núcleo para mejorar la recombinación radiativa y separar físicamente la superficie del núcleo óptico activo de su medio circundante, y así mejorar la intensidad de PL y estabilidad óptica [6,7,8,9]. A pesar de estas propiedades favorables, un pequeño desplazamiento de Stokes (solo una docena de nanómetros), conocido como la diferencia entre los espectros de absorción y PL, genera una reabsorción grave, que conduce a una pérdida general de emisiones y limita su aplicación en la determinación cuantitativa [10, 11]. Por el contrario, los QD de tipo II con alineación de banda prohibida escalonada promueven la separación espacial de electrones y huecos en diferentes regiones de la estructura de núcleo / capa. La energía de transición de recombinación e-h del borde de banda subsiguiente es más pequeña que la banda prohibida de cualquiera de los componentes del material constituyente, lo que conduce a una emisión significativa desplazada al rojo, que no está disponible con ninguno de los materiales monocomponentes. La fuerza del oscilador de la primera característica de absorción de excitones de las QD de tipo II disminuye drásticamente en comparación con la de las QD centrales [12, 13]. La emisión en gran parte desplazada al rojo y el primer pico de absorción de excitón plano reducen la superposición de los espectros de absorción y emisión, lo que suprime la reabsorción y beneficia la detección cuantitativa biológica. Los QD típicos de ZnSe / CdS de tipo II tienen una emisión sintonizable desde el violeta azulado al rango rojo y la reabsorción suprimida [13]. Sin embargo, los electrones deslocalizados en la capa de CdS son vulnerables a la trampa de los defectos de la superficie o el medio circundante, lo que conduce a un bajo rendimiento cuántico de fluorescencia. Una solución factible es recubrir los QD de ZnSe / CdS con la capa más externa de ZnS, no solo para pasivar la superficie y aumentar el rendimiento cuántico y la estabilidad óptica, sino también para restringir la fuga del elemento Cd tóxico, reduciendo la biotoxicidad. Hasta ahora, la mayoría de las investigaciones se han centrado en las QD de tipo I, y solo unas pocas se han llevado a cabo en las QD de ZnSe / CdS / ZnS tipo II / tipo I [12,13,14,15]. Además, todos los estudios sobre el proceso de síntesis de QD de ZnSe / CdS / ZnS utilizaron una preparación de dos pasos mediante la purificación previa de QD de núcleo de ZnSe en bruto y utilizaron fosfinas tóxicas y caras. Además, ninguno de ellos implicó la aplicación de QD de ZnSe / CdS / ZnS en la detección biológica.
Aquí, presentamos un método de un solo recipiente sin fosfina para sintetizar las QD de núcleo / capa de ZnSe / CdS / ZnS de alta calidad de emisión roja de ZnSe / CdS / ZnS tipo II / tipo I con la característica de supresión de reabsorción y el primer uso de las QD para fabricar un ensayo inmunoabsorbente ligado a fluorescencia (FLISA). Usamos un precursor de Se altamente reactivo y poco tóxico (ODE-Se) y oleato de zinc para sintetizar QD de núcleo de ZnSe de alta calidad, y luego logramos un crecimiento de múltiples capas sin purificación de los puntos cuánticos del núcleo. Esto muestra una gran promesa para la síntesis a gran escala de puntos cuánticos de núcleo / capa. El rendimiento cuántico de los QD de ZnSe / CdS / ZnS tipo II / tipo I emisores de rojo tal como se preparan puede alcanzar hasta el 82% con un contenido de cadmio tóxico más bajo, lo que es particularmente importante para reducir la biotoxicidad en el campo biomédico. Además, los QD tienen un gran desplazamiento de Stokes, así como un primer pico de absorción plano, lo que conduce a una baja superposición de PL y espectros de absorción y un efecto de reabsorción suprimido.
La proteína C reactiva (PCR), como proteína de fase aguda de las células hepáticas, se ha considerado un indicador temprano de infección y trastornos autoinmunes. Estas enfermedades a menudo comienzan con niveles de PCR muy bajos. Por lo tanto, el análisis de inmunoensayo cuantitativo sensible de los niveles de PCR en muestras biológicas es de importancia crítica para el diagnóstico y el seguimiento de la evolución de las enfermedades [16]. En comparación con el ensayo inmunoabsorbente ligado a enzimas (ELISA) tradicional, FLISA ahorra tiempo sin reacción enzimática y es menos sensible a las condiciones ambientales derivadas de la calidad óptica de las QD fluorescentes [17]. Por lo tanto, FLISA se ha convertido en un nuevo foco de investigación del inmunoensayo cuantitativo [2, 18, 19, 20, 21]. Aquí, en primer lugar demostramos el inmunoensayo cuantitativo de FLISA utilizando QD de núcleo / capa de ZnSe / CdS / ZnS soluble en agua tipo II / tipo I como sonda fluorescente. El límite de detección (LOD) para la detección cuantitativa de la proteína CRP alcanzó 0,85 ng / ml, que fue un 15% más sensible que el FLISA basado en CdSe / ZnS tipo I QD en experimentos de control. Los QY altos, la excelente estabilidad óptica y el efecto de reabsorción bajo pueden promover la aplicación de QD de ZnSe / CdS / ZnS tipo II / tipo I en biomedicina y campo fotoeléctrico.
Métodos
Productos químicos
Óxido de cadmio (CdO, 99,99%), óxido de zinc (ZnO, 99,9%, polvo), selenio (Se, 99,9%, polvo), 1-octadeceno (ODE, 90%), 1-octanetiol (OT, 98%), ácido oleico (OA, 90%) El poli (anhídrido maleico-alt-1-octadeceno) (PMAO) y el ácido 2- (N-morfolino) etanosulfónico (MES) se adquirieron de Aldrich. El aceite de parafina (grado analítico), acetona (grado analítico), hexanos (grado analítico) y metanol (grado analítico) se obtuvieron de Beijing Chemical Reagent Co., Ltd, China. NaOH, HCl, Na 2 CO 3 , NaHCO 3 , KH 2 PO 4 , Na 2 HPO 4 , H 3 BO 3 , Na 2 B 4 O 7 · 10H 2 O, y Tween-20 se adquirieron de Shanghai Sangon Co., Ltd, China. La albúmina de suero bovino (BSA) y el suero de ternera se adquirieron de Sigma. La 1-etil-3- (3- (dimetilamino) propil) carbodiimida (EDC), N-hidroxisulfosuccinimida (sulfo-NHS) y las microplacas se adquirieron de Thermo Fisher Scientific (EE. UU.). El anticuerpo monoclonal de la proteína de reacción C de ratón y el antígeno CRP se obtuvieron de Abcam (EE. UU.). Todos los productos químicos y disolventes se utilizaron tal como se recibieron sin purificación adicional.
Solución madre para el precursor de Se (0,1 M)
Se cargaron Se (6 mmol) y ODE (60 mL) en un matraz de tres bocas de 100 mL y luego se calentaron a 220 ° C durante 180 min bajo nitrógeno para obtener una solución transparente amarilla.
Solución madre para el precursor de Zn (0,4 M) y el precursor de Cd (0,2 M)
Se cargaron ZnO (30 mmol), ácido oleico (30 ml) y 45 ml de ODE en un matraz de tres bocas de 100 ml y se calentaron a 310ºC bajo nitrógeno para obtener una solución transparente. Se dejó enfriar la solución resultante a 140 ° C para inyección. El proceso de preparación del precursor de Cd fue el mismo que el del precursor de Zn, excepto que la concentración se ajustó a 0,2 M y la temperatura de reacción se ajustó a 240 ° C.
Síntesis típica de QD de ZnSe / CdS / ZnS Tipo II / Tipo I
Como procedimiento sintético típico, se colocaron 4 ml de precursor de Se y ODE (15 ml) en un matraz redondo de 100 ml. La mezcla se calentó a 310 ° C. A esta temperatura, se inyectaron rápidamente 2 ml de precursor de Zn en el matraz de reacción. Se extrajeron alícuotas en diferentes intervalos de tiempo para controlar la evolución de la posición PL que se coordina con el tamaño de partícula de QD. Cuando los nanocristales del núcleo alcanzaron la dimensión deseada, la temperatura de reacción se redujo a 230 ° C para el crecimiento de la capa de CdS. Sin ningún paso de purificación, ya que la mezcla de precursor de Cd y 1-octanetiol (el radio molar de OT y catión es 1:1.2) comenzó a agregarse gota a gota con una bomba de jeringa a una velocidad de 3 mL / h, mientras la temperatura era elevado a 310 ° C. Se aplicó el mismo proceso al crecimiento de la cáscara de ZnS. Se tomaron alícuotas de QD durante la reacción para analizar el desarrollo de QD de núcleo / capa de ZnSe / CdS / ZnS. Los QD de núcleo / cáscara tal como se prepararon se purificaron agregando acetona y luego se redispersaron en cloroformo.
Síntesis típica de QD de CdSe / ZnS Tipo-I
CdSe / ZnS QD se sintetizaron como se describe en nuestros informes anteriores [7]. Posteriormente, el proceso de transferencia de fase, QDs-sondas de detección de anticuerpos y la preparación de FLISA fueron los mismos que los de ZnSe / CdS / ZnS QDs, que se describirían a continuación.
Transferencia de fase de ZnSe / CdS / ZnS QD para aplicaciones biológicas
Poli (anhídrido maleico-alt-1-octadeceno) (PMAO), un oligómero anfifílico cuyos extremos hidrofóbicos se entrelazan con el recubrimiento orgánico de los QD y los grupos terminales hidrofílicos están libres para interactuar con el tampón circundante, se ha utilizado para transferir QD hidrofóbicos a puros. agua. Los QD de ZnSe / CdS / ZnS y PMAO se mezclaron y disolvieron en cloroformo con sonicación (la relación molar de QD / PMAO fue 1:7). Después de eso, se eliminó el cloroformo mediante evaporación rotatoria a 45 ° C. Luego, un volumen igual de 0.1 M NaHCO 3 Se añadió una solución acuosa (pH =8,5) para disolver el QDs-PMAO. Los QD de ZnSe / CdS / ZnS tipo II / tipo I encapsulados en PMAO no muestran pérdida de fluorescencia y tienen una alta estabilidad en solución acuosa en una amplia gama de entornos de pH.
Preparación de sondas de detección de anticuerpos QDs
El procedimiento ha sido ampliamente informado en la literatura anterior [1, 2, 3]. Los QDs-PMAO se conjugaron en primer lugar con el anticuerpo monoclonal CRP mediante la activación de estos grupos -COOH por EDC y sulfo-NHS. A continuación, se añadió una cierta cantidad de anticuerpos CRP monoclonales a las QD y se disolvieron en tampón BS y luego se bloquearon con BSA. Finalmente, el producto se lavó con tampón BS 5 mM (pH =8,0) bajo centrifugación. El QDs-mAb se almacenó en 50 μL de tampón BS (5 mM, pH =8,0).
Preparación de microplaca de fluorescencia recubierta de anticuerpo
El anticuerpo primario (la concentración de anticuerpo monoclonal CRP fue de 1,8 mg / ml) se diluyó con un tampón de carbonato-bicarbonato (50 mM pH =9,6, tampón CB) en cada pocillo de la microplaca. Posteriormente, la microplaca se cubrió con una película selladora y se incubó a 4 ° C durante 24 h. Para eliminar el anticuerpo de recubrimiento adicional, la microplaca se lavó tres veces con un tampón de lavado (Tween-20 al 0,05% en PBS 10 mM, pH =7,4). Luego, los sitios de unión en exceso se bloquearon con BSA al 0,5% (p / v) en PBS 10 mM (pH =7,4) para incubar durante la noche a 4ºC. Este proceso aseguró que se cubrieran todos los lados de unión disponibles y restantes de los pocillos de la microplaca. La microplaca se secó en una cámara con temperatura y humedad constantes durante 24 h, luego se almacenó a 4 ° C para uso futuro.
Detección cuantitativa de PCR mediante inmunoensayo ligado a fluorescencia
En cada pocillo de una microplaca de 96 pocillos, se añadió el anticuerpo de recubrimiento contenido 100 μl del antígeno estándar y se diluyó a una serie de concentraciones con el tampón de muestra. Las placas se incubaron a 37 ° C durante 30 min y luego se lavaron cinco veces con un tampón de lavado. A continuación, se diluyeron 100 μL de las sondas QDs-mAb con el tampón de sonda (suero de ternera al 10% (v / v) en PBS 0,1 M) en cada pocillo y se lavaron igual que en el proceso mencionado anteriormente.
Caracterización
La absorción de UV-vis a temperatura ambiente y los espectros PL se midieron con un espectrofotómetro Ocean Optics (modo PC2000-ISA). Los rendimientos cuánticos de PL (QY) se determinaron mediante la comparación de la intensidad de fluorescencia integrada de las muestras QD en solución con la del estándar de QY conocidos (solución de etanol de rodamina 101 (R101) (HCl al 0,01%, QY =100%) como estándar) . Los estudios de microscopía electrónica de transmisión (TEM) se realizaron utilizando un microscopio electrónico JEOL JEM-2010 que opera a 200 kV. La determinación de fase de los productos se llevó a cabo en un difractómetro de rayos X (D8-ADVANCE) utilizando radiación Cu-Ka (longitud de onda =1,54 Å). Los tamaños de QD y de la sonda de anticuerpo QD se registraron utilizando dispersión de luz dinámica (Nano-ZS 90, Malvern Instruments, Reino Unido).
Resultados y discusión
La absorción UV-vis y los espectros PL del proceso de crecimiento de la cáscara se muestran en la Fig. 1. El desplazamiento de Stokes del núcleo de ZnSe es de solo 8 nm con el primer pico de absorción a 420 nm y el pico de emisión a 428 nm, y el ancho total de emisión a la mitad máximo (FWHM) de 17 nm. Sin embargo, cuando solo una monocapa (ML) de caparazón de CdS creció en el núcleo de ZnSe, el cambio de Stokes aumentó significativamente a 54 nm con el primer pico de absorción a 497 nm y el pico de emisión a 551 nm, con la emisión de ancho completo a la mitad del máximo (FWHM) de 38 nm. Debido a la deslocalización de la función de onda del electrón, la emisión PL de ZnSe / CdS QD (629 nm) se desplaza al rojo con respecto a las QD del núcleo de ZnSe (428 nm), y la FWHM se amplía a 52 nm con la deposición de la capa de CdS. El PL FWHM ampliado se originó a partir de un aumento de la interacción excitón-fonón similar a Frölich [22, 23]. Es más, la fuerza del oscilador del primer pico de absorción se debilitó rápidamente debido a la transición de tipo II espacialmente indirecta desde la banda de valencia del ZnSe a la banda de conducción del CdS. El fenómeno es común en las QD de tipo II [24, 25, 26]. Mientras que el aumento espectacular de la absorción en la región espectral azul (<500 nm) se asignó a la banda prohibida del material CdS a granel (2,42 eV). En consecuencia, la emisión roja, el primer pico de absorción de excitón plano y la absorción robusta en la región de longitud de onda corta (<500 nm) de las QD de ZnSe / CdS tipo II dieron como resultado un gran desplazamiento de Stokes y una reabsorción suprimida. Con el crecimiento secuencial de la capa de ZnS, el PL se cambió a una longitud de onda corta y el FWHM se redujo de 52 nm a 43 nm. Este fenómeno se atribuyó al hecho de que los átomos de Zn se difunden en las regiones ricas en Cd para formar una capa de gradiente a alta temperatura, aumentando así el desplazamiento de banda de la capa. Los QY podrían aumentar del 20 al 82% durante el proceso de crecimiento de la capa de CdS y ZnS en los núcleos de ZnSe.
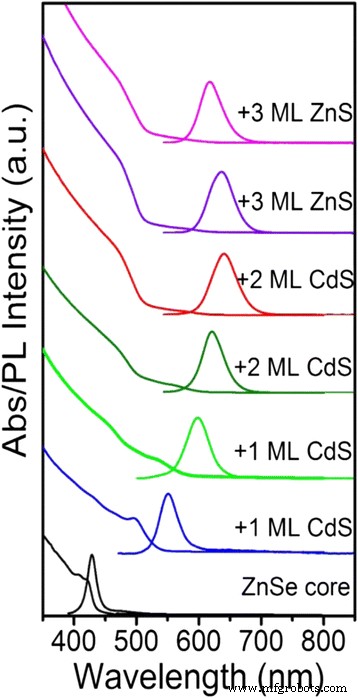
Evolución de los espectros de absorción UV-vis y PL tras el crecimiento consecutivo de QD de núcleo / capa de ZnSe / CdS / ZnS
Cabe señalar que el exceso de precursor de Zn-OA en relación con el precursor de Se en la solución de núcleo era necesario para obtener QD de núcleo de ZnSe monodispersos y de alta calidad. Como resultado, la cáscara de aleación de ZnCdSeS se formaría inevitablemente durante la adición del precursor de cáscara de Cd-OT en la etapa inicial, ya que la alta temperatura (> 200 ° C) promovió el intercambio catiónico y la difusión entre Zn 2 + y Cd 2+ , y el octanetiol rico en el precursor de Cd-OT también podría reaccionar con el exceso de Zn-OA [7, 12, 27, 28]. La carcasa de aleación no solo puede reducir la tensión interfacial y el defecto para aumentar los QY, sino que también genera una barrera de energía para los agujeros. El borde de la banda de conducción del material de la carcasa de aleación de ZnCdSeS estaba ubicado entre el de ZnSe y CdS, mientras que el borde de la banda de valencia era más profundo que el CdS. Esto formó un canal de potencial más grande en el borde de la banda de valencia como una capa de bloqueo adicional para los agujeros (Esquema 1) [12]. Esta estructura de banda de energía puede reducir aún más la superposición de electrones y huecos para disminuir la fuerza del primer pico de absorción de excitones y suprimir la reabsorción.
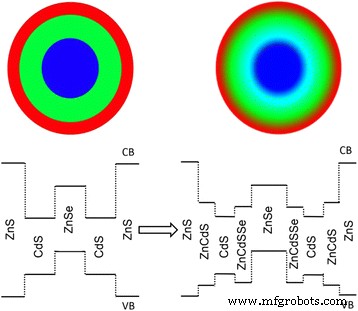
La estructura esquemática ( arriba ) y la alineación de la banda ( inferior ) para ZnSe / CdS / ZnS tipo II / tipo I QD basados en las correspondientes interfaces abruptas y aleadas, respectivamente
La información sobre la estructura de la banda de núcleo / capa y la evolución de PL y la absorbancia durante el crecimiento de la capa se puede verificar aún más mediante la comparación de XRD, TEM y HRTEM de nanocristales de núcleo y núcleo / capa. Los patrones de XRD de polvo del núcleo de ZnSe, ZnSe / CdS y el núcleo / capa de ZnSe / CdS / ZnS (la imagen de la izquierda de la Fig.2) muestran que los picos de difracción se vuelven nítidos y cambian a posiciones correspondientes a la wurtzita a granel (WZ) CdS o estructuras cristalinas de ZnS. Este resultado es coherente con los valores predichos para el mayor volumen de caparazón de CdS o ZnS en comparación con el núcleo de ZnSe en los QD de núcleo / caparazón final y atestigua el crecimiento de múltiples capas. Además, se ha producido una transformación de núcleos de ZnSe tipo mezcla de zinc (ZB) a núcleo / carcasa de tipo WZ con el revestimiento de CdS y ZnS. Este fenómeno se ha informado en sistemas QD de núcleo / carcasa CdSe / CdS [29, 30]. Las imágenes TEM de los QD del núcleo y varios QD del núcleo / capa se muestran en la Fig.2a - 2 F.Todas las imágenes TEM muestran QD esféricos casi monodispersos con diámetros promedio gradualmente crecientes desde el núcleo ZnSe original (3,90 nm) hasta el tipo ZnSe / 6CdS- II QD (7,98 nm) y ZnSe / 6CdS / 6ZnS tipo II / tipo I QD (11,92 nm). Como se muestra en la imagen HRTEM de los QD del núcleo de ZnSe (recuadro de la Fig. 2a), el espaciado de la red de los planos (111) es de 0,32 nm, y los QD poseen buena cristalinidad y monodispersidad. Con el crecimiento de las conchas, el parámetro de la red mostró el cambio correspondiente (0,35 nm para CdS y 0,31 nm para ZnS) de acuerdo con los datos XRD. Los resultados han sugerido claramente el crecimiento controlable de CdS y los subsiguientes materiales de la cáscara de ZnS.
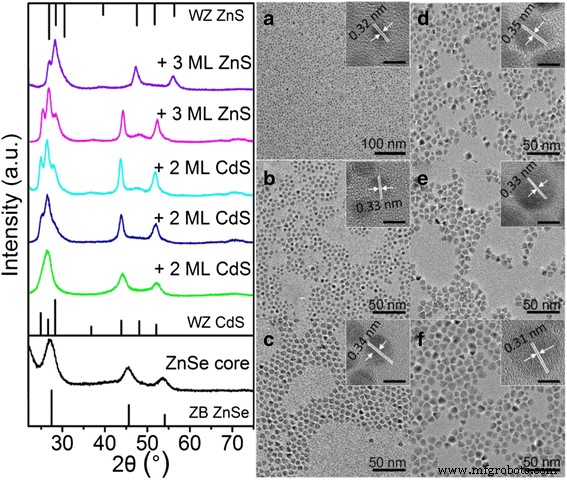
Izquierda :Patrones XRD de QD de ZnSe / CdS / ZnS tipo II / tipo I con diferentes etapas de crecimiento de la cáscara. Las líneas de difracción para la mezcla de zinc (ZB) ZnSe (abajo), WZ CdS ( medio ) y WZ ZnS ( arriba ) están indexados. Derecha :el TEM y HRTEM correspondientes ( recuadro , barra de 5 nm) imágenes del núcleo de ZnSe ( a ), QD de ZnSe / CdS tipo II con 2 ML ( b ), 4 ML ( c ) y 6 ML ( d ) CdS shell, respectivamente, y QD de ZnSe / CdS / ZnS tipo II / tipo I con 3 ML (E) y 6 ML (F), respectivamente
Mientras tanto, para confirmar la evolución de la composición durante el crecimiento de multicapa, se ha tomado el análisis de espectroscopía de rayos X de dispersión de energía (EDS) para las diferentes etapas del crecimiento del núcleo / capa, como se muestra en el archivo adicional 1:Tabla S1. Los datos de EDS muestran que los cambios correspondientes de contenido de Cd, Se, Zn y S están de acuerdo con la etapa de crecimiento de la cáscara. Pero vale la pena señalar que la relación molar Cd / (Zn + Cd) en las QD de ZnSe / CdS resultantes es mayor que la relación de alimentación Cd / (Zn + Cd) debido al intercambio de cationes entre Zn 2 + y Cd 2+ durante el proceso de recubrimiento de la carcasa de CdS sobre el núcleo de ZnSe a más de 200 ° C. En comparación con la literatura publicada sobre las QD típicas de CdSe / CdS / ZnS de tipo I (relación molar de Cd ~ 40%) [31], las QD de ZnSe / CdS / ZnS de tipo II / tipo I contenían mucho menos elemento Cd (~ 13%).
En el archivo adicional 1:Figura S1 (A) se muestra una comparación visual de las QD hidrofóbicas en cloroformo y las QD cubiertas con PMAO en agua bajo la luz del sol y la luz ultravioleta. Parece que ambas soluciones QD no se alteran y no hay agregación de nanopartículas. Ambos QD emitieron la misma luz roja cuando fueron iluminados con una lámpara UV de mano (365 nm). Archivo adicional 1:La Figura S1 (B) muestra la absorción UV-visible y los espectros PL de QD antes y después de la transferencia de fase. En comparación con las QD hidrófobas en cloroformo, el espectro PL de las QD cubiertas con PMAO tiene un cambio insignificante, lo que indica que no hay cambios obvios en el tamaño de partícula y las propiedades de PL. Archivo adicional 1:la Figura S1 (C) y (D) presentan las imágenes TEM de los QD antes y después de la transferencia de fase, lo que determina aún más la morfología y el estado de los QD con límite de PMAO. Parece que las QD cubiertas con PMAO están bien aisladas y rara vez se observan como agregados.
Con el fin de confirmar la formación de QD encapsulados en PMAO durante el proceso de transferencia de fase, se utilizó la espectroscopia FTIR para caracterizar los grupos funcionales en la superficie de los QD (que se muestra en el archivo adicional 1:Figura S2). La disminución del pico a 1777 cm −1 (comparado con PMAO con QDs-PMAO) y el aumento del pico a 1715 cm −1 (compararon las tres muestras) se atribuyeron a la descomposición de anhídrido y la formación de -COOH. Los resultados de FTIR indicaron que el polímero anfifílico PMAO se recubrió con éxito en la superficie de los QD de ZnSe / CdS / ZnS.
La estabilidad de las QD preparadas es muy importante para el tratamiento posterior. La Figura 3a muestra la evolución de la estabilidad relativa de PL de las QD hidrófobas de ZnSe / CdS / ZnS tras las etapas de purificación. La intensidad de PL de los QD de núcleo / capa de ZnSe / CdS / ZnS podría mantenerse en un 85% tras muchos ciclos de purificación en hexanos. Como se muestra en la Fig. 3b, la estabilidad coloidal de QDs-PMAO en tampón BS (pH =7,2) se estimó en función del tiempo a 25ºC. La intensidad de PL casi se mantuvo constante y la solución era clara incluso después de 400 h. Esto indica que el QDs-PMAO es estable en la solución BS sin ningún daño. La Figura 3c muestra la variación en la intensidad de PL de QDs-PMAO que se sumergieron en una solución de pH ácido a básico (pH =1-14, ajustado por HCl o NaOH) durante 30 min. La intensidad de PL de los QD hidrófilos podría retener más del 85% excepto cuando el PH =14. La Figura 3d muestra el efecto del parámetro de temperatura sobre la intensidad de fluorescencia relativa de QDs-PMAO. La intensidad de la fluorescencia disminuyó gradualmente con el aumento de temperatura, pero aún se mantuvo en un 76% a 90 ° C, mientras que los picos de PL se desplazaron gradualmente a una longitud de onda más larga debido a la expansión térmica y al efecto de acoplamiento electrón-fonón. Toda la evaluación de estabilidad indica que los QD y QD-PMAO de ZnSe / CdS / ZnS tipo II / tipo I eran muy estables y, por lo tanto, adecuados para aplicaciones biológicas.
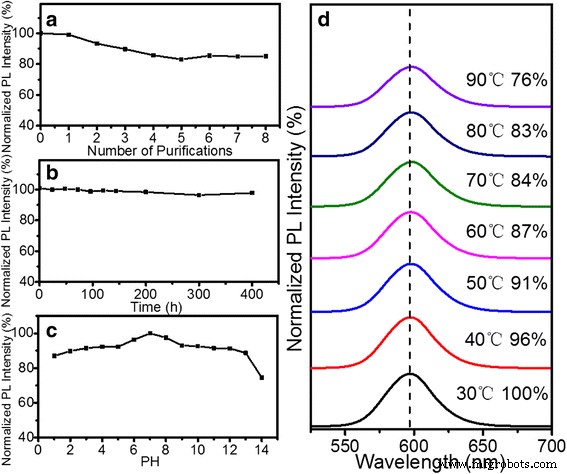
Prueba de estabilidad de QD hidrófobos sobre ( a ) pasos repetidos del proceso de purificación; prueba de estabilidad de QDs-PMAO sobre ( b ) Búfer BS, ( c ) PH y ( d ) temperatura
La PCR es una proteína de fase aguda de las células hepáticas y su nivel se considera un indicador temprano de infección y trastornos autoinmunes. Aquí, los QD de ZnSe / CdS / ZnS rematados con PMAO sintetizados se acoplan con CRP para demostrar la posibilidad de aplicación en inmunoensayos cuantitativos. El diagrama de comparación de los espectros de fluorescencia de las QD acuosas de ZnSe / CdS / ZnS y el QDs-mAb se muestra en la Fig. 4a. Claramente, la forma del pico PL de ambas muestras es aproximadamente idéntica excepto que la intensidad de fluorescencia disminuye al 60% después de la reacción de acoplamiento debido a la inevitable pérdida de muestra durante el proceso de separación por centrifugación. Demuestra la excelente estabilidad óptica de las QD de ZnSe / CdS / ZnS tipo II / tipo I incluso después del proceso de acoplamiento de la proteína del anticuerpo.
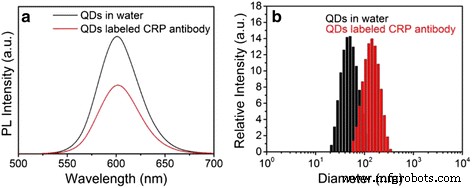
Espectros de fluorescencia ( a ) y dispersión dinámica de la luz ( b ) de QDs-PMAO y QDs-mAb en tampón
Para investigar más a fondo el efecto de la conjugación sobre el tamaño de los QD, los QD acuosos y los QD-mAb se caracterizan por la dispersión dinámica de la luz (DLS). Los resultados de DLS (Fig. 4b) muestran claramente que ambas muestras tienen una distribución de tamaño estrecha con buena monodispersidad y mantienen una forma discreta sin agregación, mientras que el tamaño hidrodinámico aumenta de 46 a 120 nm después del proceso de acoplamiento. Esto demuestra el éxito en la conjugación con anticuerpos CRP.
Además, utilizamos los puntos cuánticos compuestos de ZnSe / CdS / ZnS tipo II / tipo I en lugar de los QD de CdSe / ZnS tipo I como sonda fluorescente para establecer un FLISA para la detección cuantitativa de CRP. El proceso de ensamblaje se muestra en el archivo adicional 1:Esquema S1. La Figura 5a muestra la intensidad de fluorescencia relativa del marcador de fluorescencia QD para inmunoensayo en la detección de diversas concentraciones de antígenos de CRP (el antígeno de CRP estándar se diluye a 0, 1, 5, 10, 50, 100, 200, 400 ng / ml). Obviamente, la intensidad de PL aumenta gradualmente con el aumento de concentración de CRP. La Figura 5b muestra que la correlación entre la intensidad de fluorescencia y las concentraciones de CRP objetivo obedecen a una ecuación de curva de regresión cuadrática de y =44230 + 8121.1x-10.3x 2 con un coeficiente de correlación de 0,9991, que cuanto más cerca de 1 mejor. Las concentraciones de trabajo oscilan entre 0 y 400 ng / mL. El LOD es uno de los parámetros clave para el inmunoensayo para FLISA. Al utilizar los QD compuestos de ZnSe / CdS / ZnS tipo II / tipo I como sonda fluorescente, la sensibilidad de la detección cuantitativa de PCR es de 0,85 ng / ml, que es un 15% más sensible que la de FLISA basada en el tipo de CdSe / ZnS -I QD (1,00 ng / ml) (en el archivo adicional 1:Figura S3).
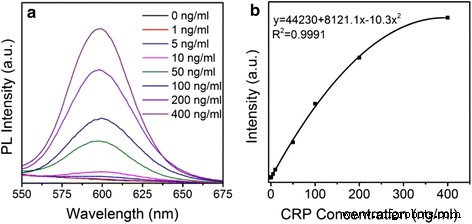
Espectros de fotoluminiscencia de FLISA para la determinación de diferentes concentraciones de antígeno de CRP ( a ) y las curvas estándar ( b )
Además, se utilizaron experimentos de recuperación para evaluar el efecto de la matriz de FLISA con una serie de antígenos de CRP estándar conocidos para su análisis, y las concentraciones finales cubrieron los niveles de riesgo bajo, medio y alto. Como se muestra en la Tabla 1, todas las tasas de recuperación están dentro del rango de 83,61-105,9%. Estos resultados indican que el FLISA basado en QD de ZnSe / CdS / ZnS tipo II / tipo I con propiedad de supresión de la reabsorción tiene una alta precisión y es de grandes ventajas en la detección de inmunoensayos cuantitativos.
Conclusiones
Presentamos un método de un solo recipiente sin fosfina para sintetizar ZnSe / CdS / ZnS tipo II / tipo I de núcleo / capa con supresión de reabsorción QD con un gran desplazamiento de Stokes y un primer pico de absorción plano. Estas características reducen la reabsorción y mejoran el nivel de salida de fluorescencia. Los QD sintetizados tienen un QY alto (82%) y una alta estabilidad frente a diversas condiciones de prueba. Luego, primero usamos ZnSe / CdS / ZnS QDs como sonda de fluorescencia en FLISA para la detección cuantitativa de proteína CRP con alta sensibilidad (LOD de 0.85 ng / mL). Indica que las QD de núcleo / capa de ZnSe / CdS / ZnS de tipo II / tipo I con supresión de reabsorción tienen un potencial prometedor para su aplicación en campos de biomedicina y fotoeléctricos.
Abreviaturas
- BSA:
-
Albúmina de suero bovino
- CRP:
-
Proteína C reactiva
- DLS:
-
Dispersión de luz dinámica
- EDC:
-
1-etil-3- (3- (dimetilamino) propil) carbodiimida
- EDS:
-
Espectroscopia de rayos X de dispersión de energía
- ELISA:
-
Ensayo inmunoabsorbente ligado a enzimas
- FLISA:
-
Ensayo inmunoabsorbente ligado a fluorescencia
- FWHM:
-
Ancho completo a la mitad del máximo
- LOD:
-
Límite de detección
- MES:
-
Ácido 2- (N-morfolino) etanosulfónico
- OT:
-
1-octanetiol
- PMAO:
-
Poli (anhídrido maleico-alt-1-octadeceno)
- QD:
-
Puntos cuánticos
- QY:
-
Rendimientos cuánticos
- sulfo-NHS:
-
N-Hydroxysulfosuccinimide
Nanomateriales
- Avances y desafíos de los nanomateriales fluorescentes para síntesis y aplicaciones biomédicas
- Síntesis de puntos cuánticos de carbono codopados N, S ricos en piridínicos como imitadores enzimáticos eficaces
- Síntesis ecológica de puntos cuánticos de núcleo / carcasa de InP / ZnS para su aplicación en diodos emisores de luz sin metales pesados
- Síntesis de nanocristales de ZnO y aplicación en células solares de polímero invertido
- Síntesis de calentamiento de estado sólido de compuesto de poli (3,4-etilendioxitiofeno) / oro / grafeno y su aplicación para la determinación amperométrica de nitrito y yodato
- Síntesis de puntos cuánticos de sulfuro de antimonio solubles en agua y sus propiedades fotoeléctricas
- Control electroquímico reversible sobre la luminiscencia fotoexcitada de la película de puntos cuánticos de núcleo / carcasa CdSe / ZnS
- Síntesis fácil y respetuosa con el medio ambiente de nanocables de Co3O4 y su prometedora aplicación con grafeno en baterías de iones de litio
- Síntesis sonoquímica de un solo paso y propiedades fotocatalíticas fáciles de compuestos de puntos cuánticos de grafeno / Ag3PO4
- Síntesis y caracterización de BiOCl modificado y su aplicación en la adsorción de tintes de baja concentración a partir de una solución acuosa
- Dependencia del espesor de la cáscara de la transferencia de energía entre partículas en el dopaje de puntos cuánticos de ZnSe / ZnSe Core-Shell con europio



