Ferromagnetismo a temperatura ambiente inducido por grafeno en nanopartículas de cobalto Nanohíbrido de grafeno decorado
Resumen
El control de las interacciones magnéticas en las nanopartículas magnéticas (MNP) es un tema crucial para el futuro desarrollo de aplicaciones “espintrónicas” integradas de tamaño nanométrico. Aquí, hemos desarrollado una estructura nanohíbrida para lograr ferromagnetismo a temperatura ambiente, a través de un método de síntesis solvotermal fácil, eficaz y reproducible. El plan se ha puesto en cobalto (Co) NP, donde el crecimiento de Co NP en la superficie de nanoplacas de óxido de grafeno reducido (rGO) cambia las interacciones magnéticas de superparamagnéticas a ferromagnéticas a temperatura ambiente. El ferromagnetismo de activación en este nanohíbrido puede deberse a la hibridación entre 2p z insaturados orbitales de grafeno y orbitales 3d de Co, que promueve el ordenamiento ferromagnético de largo alcance. El comportamiento ferromagnético del nanohíbrido Co-rGO lo convierte en un material excelente en el campo de la espintrónica, la catálisis y la resonancia magnética.
Introducción
En la última década, las nanopartículas magnéticas (MNP) han atraído un interés considerable de científicos debido a sus aplicaciones potenciales en espintrónica, catálisis y biología [1, 2]. En varios NP de metales (Fe, Co, Ni), los NP de Co se han estudiado exhaustivamente debido a sus posibles aplicaciones industriales. En la actualidad, se ha encontrado que las NP de Co son una excelente alternativa a las NP de hierro debido a su gran anisotropía y mayor relajación de protones [3]. Estas interesantes propiedades de Co NPs las convierten en un candidato ideal para aplicaciones en catálisis, resonancia magnética (MRI), administración de fármacos y terapéutica [4, 5, 6].
En materiales de carbono 2D, el grafeno se ha encontrado como un material de soporte perfecto para nanopartículas de óxido metálico y semiconductores debido a su gran área de superficie, peso ligero, menor toxicidad y naturaleza hidrófila [7]. Las excelentes y únicas propiedades del grafeno 2D surgen de sus átomos de carbono compactos que forman un sp 2 -Red híbrida en celosía alveolar. En el híbrido de NP de metal y grafeno, las NP se unen a la superficie de la hoja de grafeno a través de un enlace covalente fuerte que evita aún más la evaporación y migración de las NP. Además, el grafeno tiene p z insaturado orbital y zero bandgaps, ambas propiedades son útiles para la interacción electrónica con el orbital 3d de NP de metales de transición [8]. Además, el material híbrido resultante puede tener propiedades únicas del grafeno, tales como largos tiempos y longitudes de coherencia de espín debido a las limitadas interacciones finas y al pequeño acoplamiento espín-órbita [8]. Por lo tanto, el grafeno es un material prometedor para alternar la estructura de banda electrónica de los NP magnéticos de manera eficiente y puede promover las interacciones ferromagnéticas a temperatura ambiente.
Para la síntesis de nanocompuestos de MNPs-grafeno, el investigador ha explorado varios métodos, incluido el método sol-gel, la deposición electroquímica, el método de síntesis verde, el método de ensamblaje in situ y el método solvotermal [9,10,11,12,13] . Dependiendo de las aplicaciones requeridas, se puede seleccionar una forma adecuada para sintetizar nanocompuestos de grafeno-MNP, ya que los métodos descritos anteriormente tienen sus ventajas e inconvenientes. En un estudio reciente, Xu et al . [14] han sintetizado el nanocompuesto de Co-rGO mediante el método solvotermal de un solo paso y han descubierto que este compuesto es un excelente catalizador para la reducción de Cr (VI) a Cr (III). Athinarayanan y otros . [12] han preparado Co 3 O 4 -Nanocompuesto rGO utilizando jarabe de fruta de palmera datilera y evaluó sus propiedades biológicas en células madre mesenquimales humanas.
En este trabajo, hemos diseñado el nanohíbrido Co-rGO mediante un método de síntesis solvotermal simple y eficaz. En el nanohíbrido Co-rGO, el grafeno se utilizó como material de soporte que proporciona una amplia superficie, monodispersidad para Co NP y también evita que se oxiden y agreguen. Los resultados experimentales microestructurales detallados revelan la formación exitosa del nanohíbrido Co-rGO. Además, las propiedades magnéticas de Co NP y Co-rGO nanohíbrido se examinaron mediante la técnica del magnetómetro de muestra vibrante, donde la curva M-H a temperatura ambiente muestra un comportamiento superparamagnético para Co NP. Además, mediante la decoración de Co NP en la superficie del grafeno, hemos observado un comportamiento ferromagnético a temperatura ambiente.
Métodos
Materiales
Acetilacetonato de cobalto (III) (99,99%, Sigma Aldrich), oleilamina (> 50,0% (GC), TCI), etanol (99,9%, Merc). Etilenglicol (Fisher Scientific), acetato de sodio anhidro (98,5%, Fisher Scientific), etilendiamina (99%, Merc), agua bidestilada (99%, Merc). Ácido sulfúrico (H 2 SO 4 , Fisher Scientific), ácido nítrico (HNO 3 , Fisher Scientific), ácido clorhídrico (HCl, Fisher Scientific), clorato de potasio (KClO 3 , Fisher Scientific).
Síntesis de óxido de grafito
El óxido de grafito se preparó utilizando el método de Staudenmaier con una ligera modificación [13, 15, 16]. En un vaso de precipitados de 500 ml se añaden 180 ml de ácido sulfúrico y 90 ml de ácido nítrico bajo un baño de hielo. Además, se añadieron 5 g de polvo de grafito a la mezcla y se dejó mezclar mediante agitación magnética. Luego, se añadieron 55 g de clorato de potasio a las mezclas de reacción en 2 h. Después de eso, se retiró el baño de hielo y se dejó que la mezcla de reacción se agitara durante 5 días. Finalmente, la solución se lavó bien con HCl y solución de agua destilada (10 veces), y el producto obtenido se secó en horno de vacío a 80 ° C.
Síntesis de nanopartículas de cobalto
La síntesis de Co NP se llevó a cabo mediante el método solvotermal de un solo paso [17]. Brevemente, se añadieron 1,8 mmol (641,26 mg) de acetilacetonato de cobalto (III) a los 75 ml de oleilamina en un vaso de precipitados. La mezcla de reacción se calentó a 100ºC con agitación magnética durante aproximadamente 1 h. Además, la mezcla se transfirió a un autoclave de 100 ml y se calentó a 220ºC durante 20 h. Finalmente, la solución se purificó con etanol y el precipitado obtenido se secó en un horno de vacío a 60 ° C.
Síntesis del nanohíbrido Co-rGO
El nanohíbrido Co-rGO se sintetizó mediante un método de síntesis solvotermal simple, tal como lo describió nuestro grupo en el estudio anterior [13, 15, 16]. En un protocolo de síntesis típico, 80 ml de etilenglicol, 15 ml de etilendiamina, 6 g de acetato de sodio, 200 mg de óxido de grafito y 50 mg de nanopartículas de cobalto sintetizadas se han sometido a ultrasonidos en un vaso de precipitados durante 3 h. Además, la solución dispersada se transfirió a un autoclave de 100 ml y se calentó a una temperatura de 200ºC durante 12 h. Finalmente, la mezcla de reacción se dejó enfriar a temperatura ambiente, se purificó con etanol varias veces y el producto obtenido se secó en un horno de vacío a 60 ° C.
Difractómetro de rayos X de mesa (XRD) Rigaku MiniFlex con Cu Kα ( λ =1,54 Å) para obtener el patrón XRD de las muestras de polvo sintetizadas. El tamaño y la forma de las muestras preparadas se obtuvieron de un microscopio electrónico JEOL-2100F. Para esta caracterización, el voltaje de aceleración se usó como 120 kV y las muestras se prepararon mediante el cálculo del costo por caída de la muestra dispersa en una rejilla de cobre recubierta de carbón de 300 mallas. Las morfologías de la superficie y el mapeo elemental de las muestras sintetizadas se determinaron a partir del microscopio SEM, Zeiss EVO 40, donde el voltaje de funcionamiento era de 20 kV. La espectroscopía Raman se llevó a cabo mediante un espectrómetro raman Wi-tech alpha 300 RA que tenía un láser de argón de longitud de onda de 532 nm. Las propiedades magnéticas de Co NPs, rGO y Co-rGO composite se obtuvieron mediante la técnica del magnetómetro de muestra vibrante (VSM) unida con PPMS cryogenics limited, EE. UU.
Resultados y discusión
La Figura 1 ilustra el mecanismo de síntesis del nanohíbrido Co-rGO. Como se muestra en la figura, primero se tomaron óxido de grafito (GO), Co NP, etilendiamina (EDA), etilenglicol (EG) y acetato de sodio (NaAc) en un vaso de precipitados y se sometieron a ultrasonidos dentro de un sonicador para una dispersión adecuada de la mezcla. Aquí, se utilizó NaAc como estabilizador electrostático que puede detener la aglomeración de partículas; EDA y EG actúan como medios solventes para la dispersión adecuada de Co NP. Después de la dispersión adecuada, la mezcla se transfirió a un horno a 200 ° C durante 12 h. En esta reacción solvotermal, EDA juega un papel importante en la evolución del nanohíbrido Co-rGO, y EG actúa como un agente reductor que contribuye a la reducción de GO en rGO [15, 16].
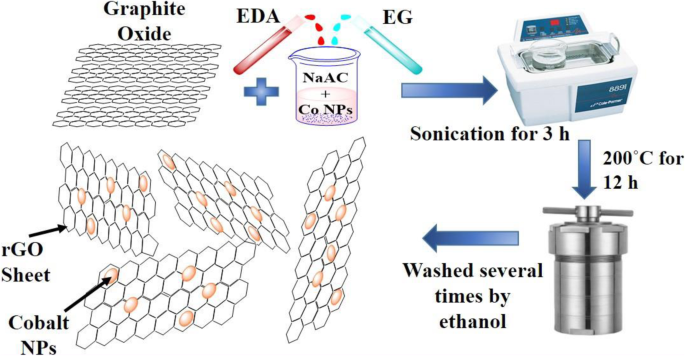
Diagrama esquemático que ilustra el mecanismo de síntesis del nanohíbrido Co-rGO
El tamaño, la forma y la disparidad de las Co NP preparadas se han investigado mediante microscopio electrónico de transmisión (TEM). Como puede verse en la Fig. 2a, la mayoría de los Co NP tienen una forma casi esférica con un tamaño promedio de 15 a 20 nm. La Figura 2b es la imagen TEM de las nanohojas rGO, que muestra que la hoja rGO es casi transparente con una superficie arrugada similar al papel. Además, la Fig. 2 cyd son, respectivamente, imágenes TEM y HRTEM del nanohíbrido Co-rGO. Está bien representado que los Co NP se decoran con éxito sobre la superficie de la hoja rGO. Se encontró que el diámetro promedio de Co NP en la superficie de la hoja rGO es de 5-8 nm, que es menor que el valor observado en el caso de Co NP. Este cambio se observa debido al grafeno y al etilenglicol, que limitan el tamaño de las NP de Co en la reacción solvotermal [14]. Además, a partir de la imagen HRTEM (Fig. 2d), el espaciado interplanar se calculó como 0,36 y 0,22 nm para rGO y Co NP, respectivamente, lo que corresponde al plano (002) de ambos materiales. La morfología de la superficie del nanohíbrido de rGO y Co-rGO sintetizados se investigó mediante microscopio electrónico de barrido (SEM). La Figura 2 e es una imagen SEM típica de nanohojas rGO. Ilustra que rGO tiene una morfología esponjosa con una estructura laminar. La imagen SEM del nanohíbrido Co-rGO se muestra en la Fig. 2f. Las manchas blanquecinas sobre la lámina de rGO son una clara indicación de la buena dispersión de Co NP. También indica una fuerte unión covalente entre Co NP y la hoja rGO a través de la interacción electrónica. Por lo tanto, rGO juega un papel vital en el nanohíbrido Co-rGO al aumentar el área de superficie específica y promover la disparidad de NP de Co, que mejoran sinérgicamente la actividad catalítica [14].

un - d Imágenes TEM a Co NP, b nanohojas rGO, c y d Nanohíbrido Co-rGO. e - f Imágenes SEM e nanohojas rGO y f Nanohíbrido co-rGO
Se utilizó el análisis de rayos X de dispersión de energía (EDX) para investigar la información de los elementos localizados dentro del nanocompuesto Co-rGO. La Figura 3 muestra el análisis elemental del nanohíbrido Co-rGO, que muestra claramente la existencia de elementos C, O y Co dentro de la muestra. La imagen insertada de la Fig. 3 demuestra el porcentaje atómico (en%) de los elementos constituyentes en el nanohíbrido Co-rGO. Se encontró que los porcentajes atómicos de Co, C y O eran 27.05, 67.77 y 5.18, respectivamente en el nanohíbrido.
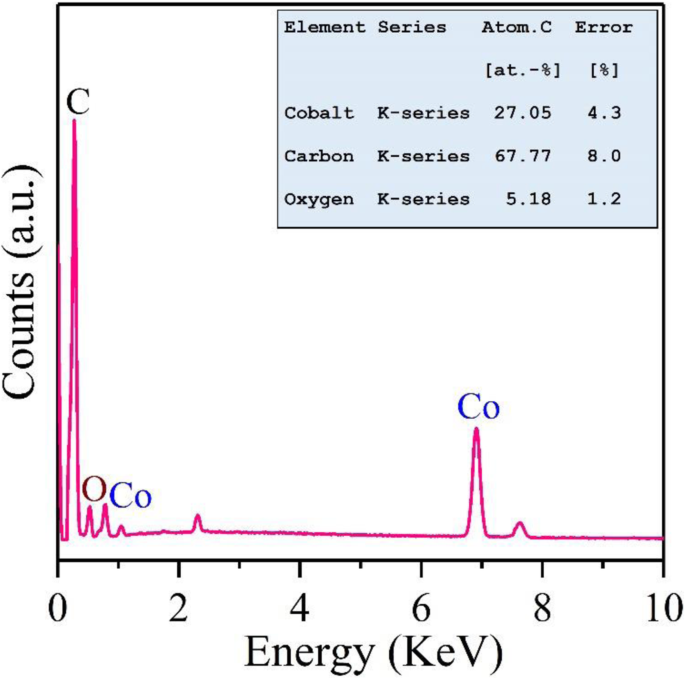
Espectro EDX del nanohíbrido Co-rGO. La imagen insertada muestra los resultados de mapeo elemental obtenidos de la muestra Co-rGO
La Figura 4a muestra el patrón XRD de las nanohojas rGO. Describe la exfoliación exitosa de GO en rGO ya que contiene la reflexión de los planos (002) y (100) a 24,83 ° y 43 °, respectivamente [15]. Patrón XRD de Co NP indexadas con éxito con planos (100), (002), (101) y (110) a 41,63 °, 44,24 °, 47,37 ° y 75,80 °, respectivamente de Co (Fig. 4Ab) [14] . Estos planos de reflexión son muy consistentes con la estructura hcp de Co NPs (JCPDS No. 05-0727). Esta fase de excitación se observó debido a la conversión de acetilacetonato de cobalto [Co (acac) 3 ] en cobalto metálico por la reacción solvotermal. Además, la Fig. 4Ac muestra el patrón XRD del nanohíbrido Co-rGO. Además de los planos de reflexión observados en rGO {(002), (100) a 24,83 ° y 43 °, respectivamente}, el patrón XRD contiene todos los planos de reflexión como se encuentra en el caso de Co NP. Este resultado indica una formación de fase adecuada de Co NP en la superficie de las nanohojas de rGO. También se observa en la Fig. 4Ac que la intensidad relativa de los picos de Co aumentó con la formación del nanohíbrido de Co-rGO. Esto podría atribuirse a la mejora en la cristalinidad y orientación de Co NP debido a rGO. Xu y col. observaron características similares en el caso del nanocompuesto de Co-rGO [14].
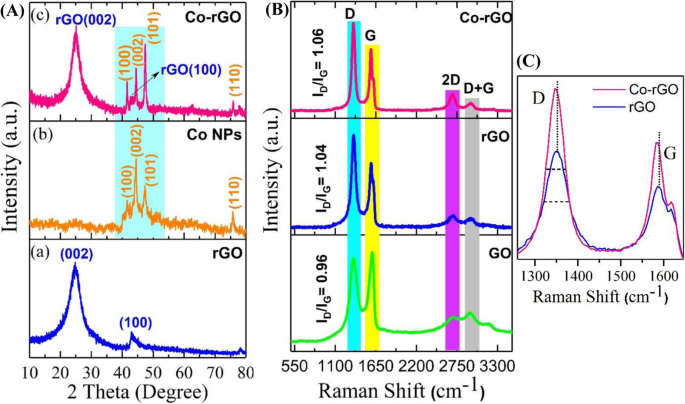
( A ) Patrones XRD a nanohojas rGO, b Co NP y c Nanohíbrido Co-rGO (B) Espectros Raman de nanohíbrido GO, rGO y Co-rGO (de abajo hacia arriba). (C) Espectros Raman de rGO y Co-rGO, que muestran cambios en los picos D y G
La Figura 4b muestra los espectros Raman del nanohíbrido GO, rGO y Co-rGO. Los tres materiales contienen cuatro bandas, a saber, D, G, 2D y D + G, con un ligero cambio en su número de onda. La banda G del nanohíbrido rGO y Co-rGO aparece a 1586 cm −1 y 1585 cm −1 respectivamente, mientras que la banda G de GO se observa a 1600 cm −1 [15, 16]. En comparación con GO, la banda G de rGO y Co-rGO se desplaza hacia un número de onda más bajo, lo que indica la reducción de GO a rGO [15]. En general, el origen de la banda D se considera un desorden de los átomos de carbono, así como un defecto en la estructura grafítica, mientras que la banda G se conoce como sp 2 hibridación de átomos de carbono ordenados en E 2g modo de vibración [18, 19]. Además, la relación de intensidad de la banda D y G (I D / I G ) calcula aproximadamente la extensión del defecto y el grado de grafitización de los átomos de carbono. La I D / I G Se encontró que los valores de rGO y Co-rGO eran 1.04 y 1.06, respectivamente, que son más altos que I D / I G valor de GO (0,96). Además, se observa en la Fig. 4c que las bandas D y G del híbrido se desplazaron hacia un número de onda más bajo (desplazamiento al rojo), y sus medios máximos de ancho completo también se cambiaron en comparación con rGO. Estos resultados indican la hibridación de los orbitales rGO y Co y confirman una fuerte interacción electrónica entre rGO y Co en la estructura híbrida [8, 20] La división en la banda G del híbrido rGO y Co-rGO (Fig. 4c) estableció que el Las láminas rGO no tienen más de tres capas de grafeno [21].
La Figura 5a demuestra la curva de magnetización dependiente del campo a temperatura ambiente (M-H) para rGO, Co NP y Co-rGO nanohíbrido. Revela que la nanoplaca rGO tiene una respuesta no magnética, como se esperaba. Por otro lado, los Co NP representan un comportamiento superparamagnético (coercitividad mínima, H C 115 Oe) [22, 23]. Este comportamiento se observó debido al menor tamaño de las NP de Co (por debajo de 20 nm) [24]. En esta condición, la energía térmica se vuelve comparable con la energía magnética anisotrópica y conduce a la inversión de los espines en un corto período de tiempo (Fig. 6 panel izquierdo). La energía de anisotropía magnética E ( ϴ ) por partícula se define como "la energía necesaria para mantener el momento magnético en una dirección particular" y se puede expresar como
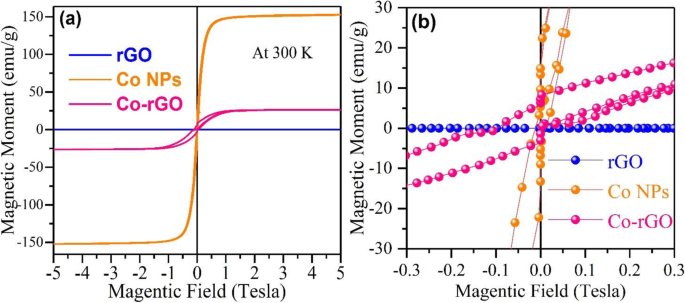
un Gráfico M-H de temperatura ambiente de rGO, Co NP y Co-rGO nanohíbrido. b Gráfico M-H en la región del campo inferior (- 0,3 T a + 0,3 T).
E ( ϴ ) = K ef V Sin 2 ϴ
Aquí, K ef es la constante de anisotropía, V es el volumen de la partícula, y ϴ es el ángulo entre la magnetización y el eje fácil [22]. La barrera de energía anisotrópica magnética que separa los dos giros, es decir, el estado de giro hacia arriba y hacia abajo, es proporcional a K ef V . Cuando el tamaño del NC disminuye lo suficiente, la barrera de energía se vuelve más pequeña que la energía térmica (K B T), lo que resulta en el cambio de giros. Este comportamiento se llama superparamagnético y el material se llama super-paramagnet. Dicho material tiene un momento magnético masivo en un pequeño campo magnético sin histéresis en absoluto. Desde el bucle M-H, el valor calculado de coercitividad (H C ), magnetización remanente (M R ) y magnetización de saturación (M S ) para Co NP y Co-rGO nanohíbrido se enumeran en la Tabla 1.
Además, la curva M-H del nanohíbrido CO-rGO, como se muestra en la Fig.5, ilustra el comportamiento ferromagnético desde su magnetización casi saturada con H C alto y M R valores 650 Oe y 5,90 emu / g, respectivamente. Sin embargo, la M S valor del nanohíbrido Co-rGO reducido significativamente a 26 emu / g en comparación con su volumen M S valor (168 emu / g) [24]. Esto se debe a las nanohojas de rGO no magnéticas y al tamaño más pequeño de las NP de Co. Se cree que el origen del ferromagnetismo (FM) en el nanohíbrido Co-rGO es el resultado de la hibridación de p z -orbital de rGO con d-orbital de Co NPs (Fig. 6 panel derecho). Esto da como resultado una transferencia parcial de electrones de rGO a Co d-orbital, que modificó aún más los estados electrónicos del nanohíbrido y promovió la interacción ferromagnética. Como se discutió anteriormente, el espectro Raman de híbrido representa una fuerte interacción electrónica entre Co y rGO, confirmó la transferencia de carga entre Co y rGO. Sun y otros . observaron características similares en el caso de puntos cuánticos de ZnO (Co:ZnO) codopados con rGO [8]. Han propuesto que rGO puede formar Co 2+ -V O complejo en el Co:ZnO debido a la transferencia de carga de rGO a Co:ZnO. Esto conduce a cambios en el nivel de fermi y da como resultado la observación de ferromagnetismo a temperatura ambiente en la estructura híbrida.
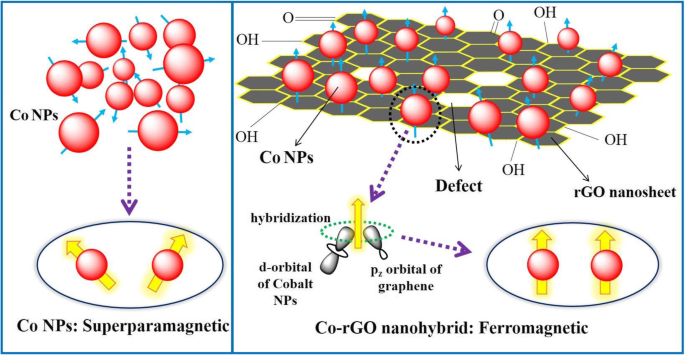
Modelo esquemático para el comportamiento de SPM y FM en Co NP y Co-rGO nanohíbrido, respectivamente
Así, con la formación del híbrido Co-rGO, la interacción superparamagnética entre Co NP se transformó en interacción ferromagnética de largo alcance. Los otros parámetros microestructurales, como la morfología, la tensión interna y los defectos de orientación, también pueden mejorar el valor de coercitividad [25, 26]. Los resultados de magnetización del presente trabajo se han comparado con algunos nanocompuestos MNPs-rGO y se enumeran en la Tabla 2.
Conclusiones
Hemos utilizado un método solvotermal de un solo paso para preparar nanopartículas de cobalto y óxido de grafeno reducido y su derivado que forma el nanohíbrido Co-rGO. Se utilizaron técnicas de caracterización XRD, TEM, SEM y EDX para confirmar la formación adecuada del nanohíbrido Co-rGO. Los cambios significativos en el espectro Raman del nanohíbrido Co-rGO indican una interacción electrónica intensiva entre rGO y Co en el nanohíbrido. La observación del ferromagnetismo a temperatura ambiente en el nanohíbrido Co-rGO podría ser el resultado de la interacción electrónica entre rGO y Co NP, lo que promueve aún más la interacción magnética a través del ordenamiento de largo alcance. Por lo tanto, este estudio abre la posibilidad de sintetizar nanohíbridos ferromagnéticos de Co-rGO, lo que podría ser beneficioso para futuras aplicaciones de espintrónica, catálisis y resonancia magnética.
Disponibilidad de datos y materiales
Las hojas de datos y los materiales utilizados están disponibles del autor correspondiente a solicitud razonable.
Abreviaturas
- NP:
-
Nanopartículas
- MNP:
-
Nanopartículas magnéticas
- Co:
-
Cobalto
- Fe:
-
Hierro
- Ni:
-
Níquel
- GO:
-
Óxido de grafito
- rGO:
-
Óxido de grafeno reducido
- IRM:
-
Imágenes por resonancia magnética
- 2D:
-
Dos dimensiones
- M-H:
-
Magnetización dependiente del campo
- XRD:
-
Difractómetro de rayos X
- SEM:
-
Microscopio electrónico de barrido
- EDX:
-
Rayos X de energía dispersiva
- TEM:
-
Microscopio electrónico de transmisión
- HRTEM:
-
TEM de alta resolución
- VSM:
-
Magnetómetro de muestra vibrante
- en%:
-
Porcentaje atómico
- SPM:
-
Superparamagnetismo
- FM:
-
Ferromagnetismo
- Oe:
-
Oersted
- T:
-
Tesla
- M S :
-
Magnetización de saturación
- M R :
-
Magnetización remanente
- H C :
-
Coercitividad
Nanomateriales
- El primer transistor de temperatura ambiente ultrarrápido totalmente óptico del mundo
- Nanopartículas de FePO4 biocompatibles:administración de fármacos, estabilización de ARN y actividad funcional
- Nanofibras poliméricas electrohiladas decoradas con nanopartículas de metales nobles para detección química
- Nanotubos de titanato Nanocompuestos de óxido de grafeno decorados:preparación, retardo de llama y fotodegradación
- Un nuevo sensor inteligente de dispersión Raman mejorado en la superficie basado en nanopartículas de ag con tapa de poliacriloilhidrazina que responden al pH
- Poliglicerol hiperramificado modificado como dispersante para el control del tamaño y la estabilización de nanopartículas de oro en hidrocarburos
- Evaluación de estructuras de grafeno / WO3 y grafeno / ceO x como electrodos para aplicaciones de supercondensadores
- Dependencia de la temperatura de fonones E2g en el plano con actividad Raman en grafeno en capas y escamas de h-BN
- Nanocomposites a base de óxido de grafeno decorados con nanopartículas de plata como agente antibacteriano
- El poli (ácido γ-glutámico) promueve la decloración mejorada de p-clorofenol mediante nanopartículas de Fe-Pd
- Síntesis selectiva de fase de nanopartículas CIGS con fases metaestables a través de la composición del disolvente de sintonización



