Un nuevo sensor inteligente de dispersión Raman mejorado en la superficie basado en nanopartículas de ag con tapa de poliacriloilhidrazina que responden al pH
Resumen
Se preparó por primera vez una nueva nanopartícula de hidrazida de poliacriloil Ag @ poliacriloilo (Ag @ PAH) sensible al pH como sustrato de dispersión Raman mejorada en la superficie (SERS) sin agente reductor ni reactivo de protección terminal. Las nanopartículas de Ag @ PAH exhibieron un excelente rendimiento de detección sintonizable en el rango de pH =4 a pH =9. Esto se explica que el comportamiento de hinchamiento-contracción del PAH sensible puede controlar la distancia entre los NP de Ag y las moléculas objetivo bajo estímulos de pH externos, dando como resultado el LSPR sintonizable y el SERS más controlado. Además, las nanopartículas de Ag @ PAH poseían una capacidad de detección ultrasensible y el límite de detección de rodamina 6G se redujo a 10 −12 M. Estas ventajas calificaron a Ag @ PAH NP como un sustrato inteligente y prometedor de SERS en el campo del análisis de trazas y sensores.
Antecedentes
La dispersión Raman mejorada en la superficie (SERS) es una poderosa herramienta espectroscópica para identificar la estructura de la molécula mediante la información vibratoria de las moléculas objetivo [1]. Debido a su conveniencia y análisis ultrasensible, SERS ha sido reconocido como un enfoque ideal para detectar moléculas biológicas, incluyendo ADN, ARN y células cancerosas [2]. En general, se acepta que la técnica SERS se puede ilustrar con el electromagnético mejorado (EM) [3]. Entre las influencias de EM, la resonancia de plasmón de superficie localizada (LSPR) juega un papel clave y dominante [4]. Cuando las moléculas objetivo residen en los espacios entre las nanopartículas metálicas vecinas (los denominados "puntos calientes"), bajo la irradiación de la luz incidente, la nanopartícula metálica genera LSPR y su campo electromagnético de superficie aumenta, lo que da como resultado la señal mejorada de SERS [5 , 6,7]. La enorme mejora asegura la alta sensibilidad de SERS, lo que significa que la huella dactilar característica de las moléculas diana se puede adquirir incluso a bajas concentraciones [8,9,10].
Hasta la fecha, se han dedicado esfuerzos considerables para mejorar la sensibilidad de SERS para desarrollar la técnica de análisis de SERS. Las estrategias exitosas para SERS ultrasensibles se han realizado mediante sustratos de nanopartículas metálicas con diferentes formas y dimensiones [11]. Sin embargo, hasta donde sabemos, no existen informes correspondientes sobre la detección controlable de SERS [12,13,14,15]. Por lo tanto, el desarrollo de SERS sintonizables se convertirá en uno de los mayores desafíos asociados con los SERS y biosensores de alta sensibilidad. La poliacriloilhidrazida (PAH) es un polímero sensible al pH, que se ha aplicado a varios campos biomédicos [16]. Debido a los abundantes grupos funcionales hidrazida en los PAH, los PAH pueden servir no solo como reactivo de protección terminal, sino también como agente reductor de los precursores de iones metálicos para preparar fácilmente nanopartículas de Ag (NP) [17]. El comportamiento de hinchamiento-contracción del PAH sensible puede controlar la distancia entre los NP de Ag y las moléculas objetivo bajo estímulos de pH externos, lo que da como resultado el LSPR sintonizable y el SERS más controlado.
En este trabajo, al combinar polímero PAH sensible al pH y NP de Ag, preparamos con éxito NP de Ag @ PAH sin otros reactivos. Rodamina 6G (R6G) como molécula diana, los NP de Ag @ PAH se utilizaron para la detección de SERS por primera vez. Debido a la respuesta del polímero PAH en la superficie de las NP de Ag, se puede lograr un efecto SERS controlable de las NP de R6G / Ag @ PAH ajustando el valor de pH. Además, los NP Ag @ PAH exhiben una alta sensibilidad y reproducibilidad, lo que les permite ser explorados en busca de peligros biológicos o análisis de reactivos químicos en aplicaciones de campo.
Métodos
La ilustración del proceso preparado de Ag @ PAH NP se muestra en la Fig. 1. Brevemente, 250 μL de AgNO 3 Se añadió una solución acuosa (0,2 mol / L) a 25 ml de solución acuosa de PAH (ESI † para más detalles) (2% w / v ). La mezcla se agitó en condiciones suaves durante 30 min a 30ºC. La solución de color marrón rojizo resultante se purificó mediante diálisis frente a agua desionizada durante 24 h, se recogió mediante centrifugación y se dispersó en agua desionizada. Luego, los diferentes valores de pH de las soluciones de Ag @ PAH NP se ajustaron mediante una solución de HCl 0,1 mol / L o una solución de NaOH 0,1 mol / L.
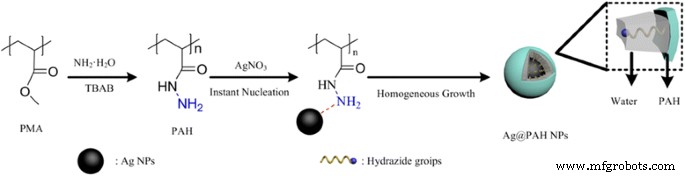
Ilustración esquemática del proceso preparado de Ag @ PAH NPs
Resultados y discusión
El polímero PAH poseía grupos hidrazida en cada unidad repetitiva, que sirvió como un agente reductor eficaz para la preparación de NP de metal [18]. Ag + sustitución electrofílica, el nitrógeno al final de los grupos hidrazida, formado -CO-NH-NH- y Ag NPs, en el proceso de preparación de Ag @ PAH NPs. Por microscopía electrónica de transmisión de alta resolución, encontramos que las NP de Ag estaban completamente encapsuladas por el polímero PAH con la estructura completa de núcleo-capa. Además, estimamos que el tamaño medio de las NP de Ag era de aproximadamente 90 nm en la Fig. 2a. El diámetro hidrodinámico de las NP de Ag @ PAH fue de 192,6 nm a pH =9 y disminuyó a 103,3 nm cuando el valor de pH era 4 en la Fig. 2b. Además, calculamos el espesor de la capa de PAH restando el diámetro de NP de Ag del total de NP de Ag @ PAH que era 102,6 nm a pH =9 y 13,3 nm a pH =4. La razón debe atribuirse al hinchamiento y encogimiento de la PAH. El hinchamiento y la contracción de los PAH se atribuyen a un efecto sinérgico de los siguientes factores, el cambio de protonación-desprotonación, la repulsión de carga y la capacidad de formación de enlaces de hidrógeno del polímero de PAH. Además, las NP de Ag @ PAH mostraron un pico de absorción similar (a aproximadamente 423 nm) en los espectros UV-vis y solo la intensidad de absorción disminuyó en el rango de pH de 4 a 9 en la Fig. 2c. Esto indicó que el creciente grosor de la capa de la cubierta de polímero dificultaría la propagación de la resonancia del plasmón de superficie localizada sin cambiar la propiedad óptica de los NP de Ag.
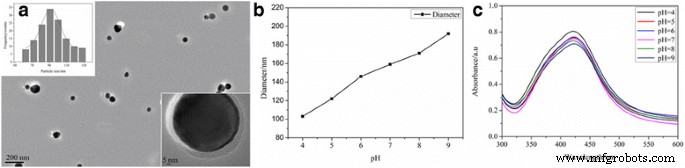
un Imágenes HRTEM y distribución del tamaño de partícula de NP de Ag @ PAH. b Dependencia del pH del diámetro hidrodinámico de las NP de Ag @ PAH. c Dependencia del pH de los espectros de absorción UV-vis de Ag @ PAH NPs
El rendimiento de SERS de los NP de Ag @ PAH se evaluó con R6G como analito objetivo del modelo. Para comprender el origen de los NP de Ag @ PAH que mejoran las señales de R6G Raman, se realizaron experimentos comparados para distinguir la influencia de la capa de polímero de PAH. Comparamos las señales Raman de la solución de R6G pura, la solución de PAH pura, las NP de Ag individuales y las NP de Ag @ PAH, todas las cuales tenían la misma concentración en la Fig. 3a. Es bien sabido que la señal de la solución R6G pura (10 −6 M) es bastante débil. Después de agregar NP de Ag o NP de Ag @ PAH como sustratos, la característica principal alcanza su punto máximo en 1311, 1363, 1509 y 1651 cm −1 , que coincidían perfectamente con los espectros de Ramam de R6G, obviamente se mejoraron. Esto demuestra que una SERS notable señales de moléculas R6G presentes en la superficie de NP de Ag y NP de Ag @ PAH. Por el contrario, en ausencia de NP de Ag, se observaron señales de SERS insignificantes del polímero de PAH individual, lo que sugiere que la presencia de polímero de PAH no tuvo ningún efecto sobre el efecto de SERS para las moléculas de R6G.
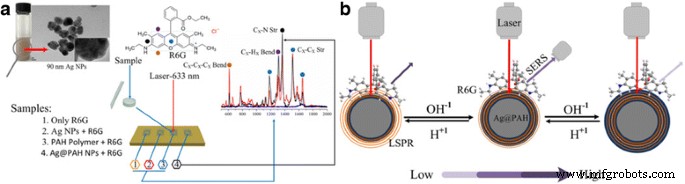
un Ilustración esquemática del proceso de fabricación SERS de R6G en sustratos Ag @ PAH NPs. b Ilustración esquemática del mecanismo SERS sintonizable de R6G con NP de Ag @ PAH a diferentes valores de pH
La mejora de SERS de la celda de metal / capa de polímero fue muy sensible al grosor de la capa de polímero, lo cual ha sido probado por estudios teóricos y experimentales. Investigamos el efecto entre diferentes valores de pH y señales mejoradas con SERS como se expresa en la Fig. 4a. En comparación con la señal original de R6G, las señales de SERS se amplificaron en presencia de NP de Ag @ PAH en diferentes condiciones de pH. Además, la intensidad relativa de SERS de los espectros disminuyó a medida que aumentaba el valor del pH. Esto se explica que el efecto SERS de Ag @ PAH NPs fue sensible al grosor de la capa de PAH. La capa de cubierta de PAH se contrajo a un valor de pH bajo, lo que resultó en una mayor intensidad del campo electromagnético que a un valor de pH alto en la misma concentración de NP de Ag @ PAH, como se muestra en la Fig. 3b. Por lo tanto, las NP de Ag @ PAH a pH bajo indujeron señales Raman extremadamente mejoradas, lo que aseguró la sintonización de las NP de Ag @ PAH como sustratos de SERS. Este fenómeno se cuantificó calculando los factores de mejora Raman (EF) de 1509 cm −1 pico para NP de Ag @ PAH (Eq. S1, ESI †). Se estimó que los FE de los NP de Ag @ PAH a diferentes valores de pH eran 0,8 × 10 6 , 1,1 × 10 6 , 1,5 × 10 6 , 2,2 × 10 6 , 3,3 × 10 6 y 4,3 × 10 6 , respectivamente, en la Fig. 4b (ESI † para detalles). Los FE de los NP de Ag @ PAH a diferentes valores de pH fueron todos altos, hasta 10 6 que reveló que Ag @ PAH NP podría usarse como un sustrato SERS eficaz e inteligente en la detección de trazas.
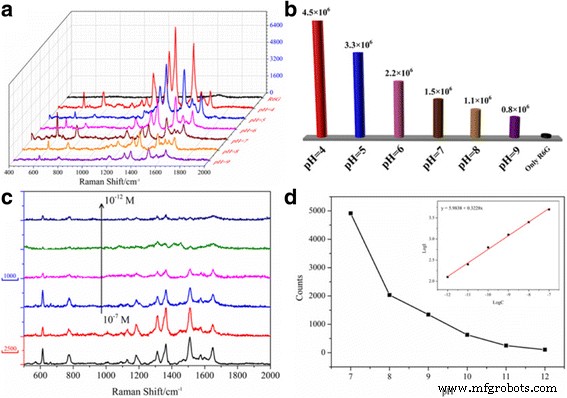
un Espectros SERS de R6G adsorbidos con diferentes valores de pH. b EF de R6G en NP de Ag @ PAH en función de los valores de pH a 1509 cm −1 . c Espectros SERS de R6G con diferentes concentraciones adsorbidas en NP de Ag @ PAH. d Relación de las intensidades máximas a 1509 cm −1 y concentraciones de R6G (el recuadro es la relación lineal entre las intensidades logarítmicas y las concentraciones de R6G.)
Además, los NP de Ag @ PAH a un valor de pH bajo indujeron señales Raman extremadamente mejoradas, lo que aseguró la ultrasensibilidad de los NP de Ag @ PAH como sustratos de SERS. Por lo tanto, una serie de espectros SERS de R6G a diferentes concentraciones (10 −7 –10 −12 M) se midieron adicionalmente a pH =4 añadiendo NP de Ag @ PAH a la misma concentración. Comparando las señales de estas curvas, las intensidades de SERS disminuyeron diluyendo las concentraciones de la molécula diana en la Fig. 4c. Las bandas características de R6G se identifican claramente incluso a una concentración tan baja como 10 −12 M, lo que demuestra que los NP de Ag @ PAH poseen una alta sensibilidad detectada para R6G. Además, se encuentra una dependencia lineal entre las concentraciones logarítmicas de R6G y las intensidades del pico de la huella dactilar (1509 cm −1 ) en la Fig. 4d. Cuando en el rango de concentración de R6G varió de 10 −7 a 10 −12 M, la ecuación de regresión lineal fue y =5.9838 + 0.3228 log (x), y el coeficiente de correlación fue 0.9971 ( n =6). Obviamente, en la región de baja concentración, la intensidad de SERS disminuyó con la disminución de la concentración de prueba. Estos resultados confirmaron que los NP Ag @ PAH se convertirán en un candidato prometedor en una detección inteligente de ultratrazas de peligros biológicos o reactivos químicos.
Conclusiones
En resumen, utilizamos NP de Ag @ PAH sensibles al pH como sustratos deseados para las aplicaciones de SERS por primera vez. La introducción de polímero PAH sensible al pH como capa de caparazón puede dotar a los Ag NP de una resonancia de plasmón de superficie localizada controlable ajustando el espesor de capa bajo estímulos de pH, lo que da como resultado efectos SERS sintonizables. Los resultados demostraron que los NP de Ag @ PAH poseían un excelente rendimiento SERS sensible al pH controlable y ultrasensible que el límite de detección de R6G redujo a 10 −12 Los NP de M. Ag @ PAH son prometedores para la aplicación inteligente de SERS en la detección de ultratrazas de peligros biológicos o reactivos químicos.
Contenido asociado
Información de soporte. Materiales, instrumentación, preparación de PAH y método de cálculo de EF. Figura S1. 1 Espectro de H RMN de PMA en CDCl 3 y PAH en D 2 O (archivo adicional 1).
Abreviaturas
- EF:
-
Factores de mejora
- EM:
-
Electromagnético mejorado
- LSPR:
-
Resonancia de plasmón de superficie localizada
- NP:
-
Nanopartículas
- PAH:
-
Poliacriloilhidrazida
- SERS:
-
Dispersión Raman mejorada en superficie
Nanomateriales
- Monitoreo de la calidad del aire de ciudades inteligentes basado en LoRa
- Nanopartículas de FePO4 biocompatibles:administración de fármacos, estabilización de ARN y actividad funcional
- Monocapa de nanocables de plata grabada químicamente y alineada como sustratos de dispersión Raman mejorados en la superficie
- Sensor plasmónico basado en nanoprismas dieléctricos
- Sensor de deformación ultrasensible basado en una película piezoeléctrica de poli (fluoruro de vinilideno) flexible
- El poli (ácido γ-glutámico) promueve la decloración mejorada de p-clorofenol mediante nanopartículas de Fe-Pd
- Información sobre la absorción celular y el tráfico intracelular de nanopartículas
- Un sensor de campo magnético flexible basado en AgNWs y MNs-PDMS
- Adaptación de las perturbaciones morfomecánicas de la célula mediante nanopartículas de óxido metálico
- Técnicas Raman:Fundamentos y fronteras
- Preparación de nanopartículas de ZnO con alta dispersibilidad basada en el proceso de fijación orientada (OA)



