Evolución mejorada del hidrógeno fotocatalítico mediante la carga de Cd0.5Zn0.5S QD en nanohojas porosas de Ni2P
Resumen
Ni 2 P se ha decorado en nanocables o nanovarillas de CdS para obtener un H 2 fotocatalítico eficiente producción, mientras que la superficie específica sigue siendo limitada debido al gran tamaño. Aquí, los compuestos de Cd 0.5 Zn 0.5 S puntos cuánticos (QD) en Ni 2 delgados Se construyeron nanohojas porosas P con un área de superficie específica alta para el H 2 fotocatalítico libre de metales nobles Generacion. El Ni 2 poroso Nanohojas P, que se formaron mediante la interconexión de Ni 2 de 15 a 30 nm de tamaño Nanopartículas de P, permitieron la carga uniforme de Cd 0.5 de tamaño 7 nm Zn 0.5 S QD y la densidad de carga controlable. Ajustando el contenido de Ni 2 P, H 2 tasas de generación de 43,3 μM h - 1 (Fotocatalizador de 1 mg) y 700 μM h - 1 (Fotocatalizador de 100 mg) y una eficiencia solar a hidrógeno del 1,5% para el Ni 2 P-Cd 0.5 Zn 0.5 S compuestos. El efecto de Ni 2 Se estudió sistemáticamente el contenido de P sobre la absorción de luz, la fotoluminiscencia y las propiedades electroquímicas del material compuesto. Junto con el cálculo de la estructura de bandas basado en la teoría funcional de la densidad, la promoción de Ni 2 Se revelaron P en la transferencia de carga y la actividad HER junto con el efecto de sombreado sobre la absorción de luz. Esta estrategia se puede aplicar a otros fotocatalizadores hacia una generación de hidrógeno solar eficiente.
Antecedentes
Como estrategia eficiente para producir H 2 Al utilizar energía solar, la producción de hidrógeno fotocatalítico ha atraído una gran atención desde TiO 2 se informó como fotocatalizador en 1972 [1]. Comparado con TiO 2 , Cd x Zn 1 − x S muestra una excelente actividad catalítica impulsada por la luz visible debido a la brecha de banda más estrecha y la buena estabilidad fotoquímica. A H 2 tasa de producción de hasta 1097 μM h - 1 g - 1 se ha logrado mediante el uso de Cd 0.5 Zn 0.5 S como fotocatalizador [2], cuya composición ha demostrado ser la óptima para la propiedad fotocatalítica. Para disminuir la recombinación del portador y la rápida separación del portador para la reacción de desprendimiento de hidrógeno (HER), se han utilizado metales nobles como Pt, Co-Pt, Ru, Au y Pd como cocatalizadores [3,4,5,6,7, 8]. Por ejemplo, cuando se co-cataliza con Co-Pt, el H 2 fotocatalítico tasa de generación de Cd 0.5 Zn 0.5 Los puntos cuánticos (QD) S podrían incrementarse en 4,7 veces [4]. A H 2 producción tan alta como ~ 6,3 mM h - 1 mg - 1 se logró cuando CdZnS se combinó con Au [9]. Sin embargo, el alto costo de los metales nobles limita en gran medida la aplicación futura a gran escala, lo que hace que los cocatalizadores no preciosos sean buenos candidatos de los preciosos para el H 2 fotocatalítico. generación.
Entre los diversos cocatalizadores no nobles que incluyen la familia del carbono (grafeno, nanotubos de carbono, óxido de grafema reducido, nanotubos de carbono) [10,11,12,13,14,15], fosfuros [16,17,18,19,20 , 21, 22] y TiO 2 [23, 24] y sulfuros [25,26,27,28,29,30,31,32], Ni 2 P y CoP se han combinado ampliamente con nanocables y / o nanovarillas de CdS para lograr un H 2 fotocatalítico eficiente producción [16,17,18, 33,34,35,36]. En estos compuestos, el CdS unidimensional (1D) siempre estaba decorado con nanopartículas de fosfuros más pequeñas o nanohojas con actividad HER, y las recombinaciones de portadores se pueden reducir en gran medida debido a la larga longitud de difusión del portador de la estructura 1D y su heterogeneidad bien definida. interfaz con los cocatalizadores. Teniendo en cuenta las ventajas de los QD, como su alta eficiencia de conversión de energía solar a combustible, los bajos costos de fabricación [37, 38], y el HER ocurre principalmente en la interfaz cocatalizador / electrolito, es racional construir hetero-nanoestructuras con mucha superficie específica área de sitios activos sin dejar de mantener una rápida separación de portadores. En este caso, se informó de una estructura inversa con fotocatalizadores cargados en cocatalizadores para un H 2 fotocatalítico eficiente generación [10, 13]. Por ejemplo, tasas de generación de hidrógeno de 2,08 y ~ 33,4 mM h - 1 mg - 1 se establecieron cargando Cd 0.5 Zn 0.5 S QD sobre carbono similar a la cebolla y nitruro de carbono grafítico 2D (g-C 3 N 4 ) microcintas, respectivamente. Estos lo hacen muy esperado para fotocatalíticos H 2 generación si las nanoestructuras de fosfuro estuvieran decoradas con Cd 0.5 Zn 0.5 S QDs. Sin embargo, hasta ahora rara vez se ha informado de una estructura inversa de este tipo.
Aquí, una estructura inversa de Cd 0.5 Zn 0.5 S QD en Ni 2 Las matrices de nanohojas P se sintetizaron mediante el método de solución térmica para mejorar el H 2 fotocatalítico Generacion. Una tasa de generación de hidrógeno de 700 μM h - 1 (con 100 mg de catalizador de alimentación) y una eficiencia solar a hidrógeno (STH) del 1,5% se lograron al 1,5% en peso de Ni 2 P. El efecto de Ni 2 P en el H 2 Se estudió sistemáticamente la tasa de generación, las propiedades ópticas y electroquímicas del material compuesto. Además, la estructura de bandas de Ni 2 P se calculó en base a la teoría funcional de la densidad, junto con la propiedad fotoelectroquímica, el papel detallado del Ni 2 P para el H 2 generación fue revelada.
Métodos / experimental
Síntesis de cocatalizador
En primer lugar, se transfirieron 20 ml de agua desionizada que contenía 2,61 g de nitrato de níquel y 2,52 g de hexametilentetramina a un autoclave de teflón y se calentó a 120ºC durante 10 h para la formación de NiOOH. Después de enfriar a temperatura ambiente, el producto de NiOOH se lavó con alcohol y agua desionizada mediante centrifugación a 2000 rpm tres veces y cada vez durante 5 min. Luego, se puso una mezcla de 0,22 g de NiOOH y 0,44 g de hipofosfito de sodio en un horno tubular y se calentó a 500ºC durante 2 h para fosforizar. Cuando se enfrió naturalmente a temperatura ambiente, Ni 2 negro Se obtuvo y se recogió polvo de P.
Síntesis de Ni 2 P-Cd 0.5 Zn 0.5 S Nanocomposites
Para preparar Ni 2 P-Cd 0.5 Zn 0.5 S compuesto, 100 mg Ni 2 El polvo de P se dispersó en 20 ml de etanol mediante procesamiento ultrasónico durante 1 h. Entonces x mL ( x =0.48, 0.96, 1.4, 3, 5) Ni 2 bien disperso Se añadió una solución de P a una solución de etilenglicol de 20 ml que contenía 272,6 mg de ZnCl 2 y 456,7 mg de CdCl 2 ∙ 2.5H 2 O, y se calentó a 170 ° C con agitación continua bajo protección de nitrógeno. Después de la adición de 20 ml de solución de etilenglicol disolviendo 960,7 mg de Na 2 S ∙ 9H 2 O, la solución se calentó a 180 ° C y se mantuvo durante 1 h para el crecimiento de Cd 0.5 Zn 0.5 S en Ni 2 P. Finalmente, las muestras se lavaron con alcohol y agua desionizada respectivamente tres veces. Pesando el xNi 2 final P-Cd 0.5 Zn 0.5 S compuestos, se determinó que los porcentajes en peso (% en peso) eran 0,5 ( x =0,48), 1 ( x =0,96), 1,5 ( x =1.4), 3 ( x =3), 5 ( x =5). Como comparación, puro Cd 0.5 Zn 0.5 Los S QD se sintetizaron mediante un método similar, excepto por la adición de Ni 2 P.
Caracterización de morfología, estructura y propiedades ópticas
La morfología, microestructura y composición se caracterizaron por microscopía electrónica de barrido de emisión de campo (FESEM, JSM-7100F, JEOL) y microscopía electrónica de transmisión (TEM, FEI Tecnai 20) equipada con microscopía electrónica de barrido de transmisión (STEM) y rayos X de energía dispersiva. espectroscopia (EDX). Los patrones de difracción de rayos X en polvo (XRD) se registraron en un difractómetro de rayos X Bruker AXS D8 con Cu Kα (λ =1,54056 Å). La composición elemental, los estados químicos y de valencia se estudiaron mediante (banda de valencia) mediciones de espectroscopía de fotoelectrones de rayos X (XPS) (XPS, Escalab 250Xi) con radiación Al Kα. La absorción de UV-Vis se investigó mediante un espectrofotómetro de UV-Vis (UV-3600, Shimadzu) equipado con un dispositivo de esfera integradora, y la relación peso / volumen de la muestra con respecto al agua desionizada se mantuvo en 1 mg / 10 ml. Las mediciones de fotoluminiscencia (PL) se llevaron a cabo en un espectrofotómetro 7000 FL (Hitachi, F7000) con una longitud de onda de excitación de 400 nm. Antes de las mediciones de PL, puro Cd 0.5 Zn 0.5 Los S QD y los compuestos estaban bien dispersos en etanol y la concentración de Cd 0.5 Zn 0.5 S se mantuvo en 0,5 mg / ml para todas las muestras.
Mediciones de voltamperometría de barrido lineal (LSV) y espectros de impedancia electroquímica (EIS)
Las mediciones de LSV se realizaron en un electrolito de NaOH 1 M (pH =14) en una estación de trabajo electroquímica (CHI 760E, CH Instruments) con una configuración típica de tres electrodos. Se utilizaron una lámina de Pt y un Ag / AgCl saturado como electrodo contador y de referencia, respectivamente. Los potenciales se convirtieron a esos frente al electrodo de hidrógeno reversible (RHE) mediante la ecuación E (frente a RHE) =E (frente a Ag / AgCl) + E Ag / AgCl (ref) + 0.0591 V × pH, donde (E Ag / AgCl (ref) =0,1976 V frente a NHE (electrodo de hidrógeno normal) a 25 ° C) [39]. Las mediciones de espectros de impedancia electroquímica (EIS) se llevaron a cabo en la oscuridad a 0,5 V frente a RHE con una amplitud de 5 mV y el electrolito de 0,35 M Na 2 SO 3 y 0,25 M de Na 2 S solución acuosa usando un sistema similar de tres electrodos. El electrodo de trabajo se hizo esparciendo ~ 2 mg de producto (dispersado en 5 ml de etanol) sobre 4 cm 2 área del sustrato FTO y se secó a 70 ° C durante 5 h. El rango de frecuencia se mantuvo dentro de 0,1 Hz ~ 100 kHz, y los espectros fueron analizados por el programa Z-View (Scribner Associates Inc.).
Fotocatalítico (PC) H 2 Generación
Antes de H 2 producción, los fotocatalizadores con diferente masa (1, 5 y 10 mg) se dispersaron en un reactor de cuarzo sellado (volumen 40 mL, 5 cm x 5 cm x 1,6 cm) con 15 mL 0,75 M Na 2 S y 1,05 M Na 2 SO 3 solución acuosa. Después de desgasificar durante 30 min con nitrógeno, el experimento fotocatalítico se realizó bajo la irradiación de una lámpara de 300 W Xe (PLS-SXE300 / 300UV, Perfect Light) con un filtro de corte de 420 nm y una potencia incidente de 300 mW / cm 2 . La solución catalítica se mantuvo en agitación continua durante todo el experimento de PC. En cada hora, se recogió y analizó la producción de gas de 1 ml mediante un cromatógrafo de gases (GC-2018, Shimadzu, Japón, TCD). Se realizó un experimento de estabilidad cíclica adicional en las mismas condiciones. Se realizaron experimentos paralelos con la dosificación de alimentación de fotocalysts de 15 a 100 mg en 100 mL de electrolito de Na 2 S y Na 2 SO 3 en un reactor más grande (volumen 150 mL) bajo la misma iluminación. La eficiencia solar a hidrógeno (STH) se calculó mediante la ecuación de flujo:
$$ {\ Displaystyle \ begin {array} {l} \ mathrm {STH} \ \ left (\% \ right) =\ kern0.5em \ frac {\ mathrm {energía} \ \ mathrm {of} \ \ mathrm { generado} \ {\ mathrm {H}} _ 2} {\ mathrm {ligero} \ \ mathrm {energía} \ \ mathrm {sobre} \ \ mathrm {la} \ \ mathrm {superficie} \ \ mathrm {de} \ \ mathrm {solución}} \ times 100 \% \\ {} \ kern6.5em =\ frac {237 \ mathrm {KJ} / \ mathrm {mole} \ kern0.5em \ times \ mathrm {moles} \ \ mathrm {de } \ {\ mathrm {H}} _ 2 \ \ mathrm {producida}} {\ mathrm {área} \ \ mathrm {de} \ \ mathrm {solución} \ \ mathrm {estado} \ \ mathrm {irradiado} \ veces 300 \ mathrm {mW} / {\ mathrm {cm}} ^ 2} \ times 100 \% \ end {matriz}} $$Métodos computacionales
Las propiedades energéticas y electrónicas del Ni 2 a granel P se calcularon utilizando el método de la teoría funcional de la densidad (DFT). El Paquete de Simulación Ab-initio de Viena (VASP) [40] se adoptó durante los cálculos con los pseudopotenciales de onda aumentada del proyector (PAW) [41] y la aproximación de gradiente generalizada (GGA) del tipo Perdew-Burke-Ernzerhof (PBE) [42 ] métodos funcionales de intercambio-correlacional. Una zona de Brillouin con una cuadrícula de Γpuntos Monkhorst − Pack de 9 × 9 × 9 [43], una energía cinética cortada con 450 eV y un criterio de energía de 10 - 6 Se aplicaron eV para la optimización geométrica hasta que las fuerzas residuales convergieron a menos de 0.01 eV / Å. El modelo a granel de Ni 2 hexagonal Se tuvo en cuenta P con simetría P-62M. Después de una estructura optimizada por completo, el parámetro de red de Ni 2 P ( a = b =5.86918 Å y c =3.37027 Å), lo cual es muy consistente con los valores reportados [44].
Resultados y discusión
Las figuras 1a, b muestran la morfología de Ni 2 P antes y después de la composición con Cd 0.5 Zn 0.5 S QD (Ni 2 P% en peso:1,5%). Ni 2 puro P tiene una morfología similar a una flor que se compone de muchas nanoláminas cruzadas con un grosor inferior a 20 nm y un tamaño plano de varias decenas de nanómetros a micrómetros. Del patrón XRD de Ni 2 puro P en la figura 1c, los picos de difracción de los planos (111), (201), (210) y (300) se pueden observar claramente a 40,7 °, 44,6 °, 47,4 ° y 54,2 °, respectivamente, que corresponden a hexagonales Ni 2 P (JCPDF núm. 89-2742). Después de cargar con Cd 0.5 Zn 0.5 S QD, la superficie de las nanoláminas se vuelve bastante rugosa y se pueden distinguir muchas nanopartículas con un tamaño inferior a 10 nm en el prístino Ni 2 P esqueleto. Al mismo tiempo, los picos de refracción XRD de Cd 0.5 Zn 0.5 Los planos S (JCPDF n. ° 89-2943) (100), (002), (101) y (110) se pueden encontrar claramente en 26,0 °, 27,8 °, 29,6 ° y 45,9 °, respectivamente [6, 45] , mientras que la señal de difracción de Ni 2 P está muy deprimido debido a la baja relación en peso (1,5% en peso) de Ni 2 P a Cd 0.5 Zn 0.5 S. La convivencia de Cd 0.5 Zn 0.5 S y Ni 2 P se demostró mediante el espectrómetro de fotoelectrones de rayos X (XPS) fino y los espectros de levantamiento en la Fig. 1d-f. Excepto las señales de oxígeno y carbono que surgen de la absorción del aire, solo se pueden detectar Ni, P, Cd, Zn y S, lo que descarta la posibilidad de otras impurezas. Los picos a 855,5 y 873,9 eV se pueden asignar a Ni 2p 3/2 y 2p 1/2 , respectivamente, y el pico de P 2p 3/2 se puede encontrar en 133,6 eV [16, 46]. Al mismo tiempo, los picos de doblete de Zn 2p, Cd 3d y S 2p sugieren el Zn bivalente 2+ , Cd 2+ y S 2− desde Cd 0.5 Zn 0.5 S QD [3, 34, 47]. En resumen, el crecimiento de Cd 0.5 Zn 0.5 S en Ni 2 Se han establecido nanohojas P para la formación de Ni 2 P-Cd 0.5 Zn 0.5 S nanocomposites.
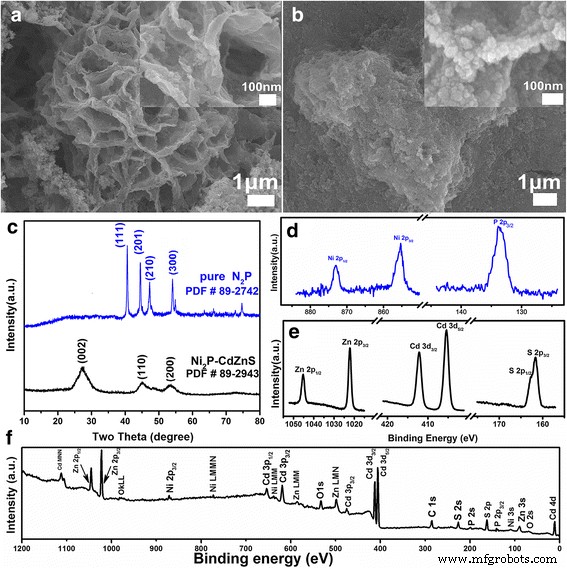
Morfología, propiedad cristalina y estados químicos del Ni 2 P-Cd 0.5 Zn 0.5 Compuestos S (1,5% en peso de Ni 2 PAGS). a – b Imágenes SEM de aumento bajo y alto (recuadro) de Ni 2 P antes y después de la carga de Cd 0.5 Zn 0.5 S, c Patrón XRD de Ni 2 P y Ni 2 P-Cd 0.5 Zn 0.5 S, d – f Espectros finos y de levantamiento XPS de Ni 2 P-Cd 0.5 Zn 0.5 S compuesto
La microestructura y la composición elemental de las muestras se investigaron más a fondo mediante técnicas relacionadas con TEM. De las imágenes TEM de diferentes aumentos de Ni 2 puro P (Fig. 2a, b), las nanoláminas son porosas y están compuestas por nanopartículas irregulares reticuladas con un tamaño de ~ 15-30 nm. El patrón de difracción de electrones de área seleccionada (SAED) en la Fig. 2c muestra el anillo de difracción de Ni 2 Planos P (111), (201), (210) y (300). Las señales difractivas de planos de índice alto como (222), (402) y (420) también pueden detectarse debido a la fuerte dispersión múltiple de los electrones de alta energía. Después de componer con Cd 0.5 Zn 0.5 S, el Ni 2 entrecruzado Las nanohojas P estaban cubiertas por muchas nanopartículas más pequeñas con un tamaño de ~ 7 nm (Fig. 2d). El espectro EDX (recuadro, Fig. 2f) muestra claramente la señal de Ni, P, Cd, Zn y S, indicativa de la coexistencia de Ni 2 P y Cd 0.5 Zn 0.5 S. Del patrón SAED (Fig. 2f), fuertes anillos difractivos de Cd 0.5 Zn 0.5 Los planos S (002), (110) y (200) (indicados por líneas de trazos amarillos) se pueden distinguir claramente junto con las señales débiles de Ni 2 P (300), (402) y (420) (marcados con líneas discontinuas blancas), lo que sugiere la buena composición de Ni 2 P con QD. Es notable que Ni 2 El anillo P (300) se superpone con Cd 0.5 Zn 0.5 Aviones S (110) y (200), lo que dificulta su distinción. La imagen TEM de alta resolución de Ni 2 P-Cd 0.5 Zn 0.5 La muestra S en la Fig. 2e muestra además las franjas de celosía con un espaciado de 0.34 y 0.22 nm, que corresponde al Cd 0.5 Zn 0.5 S (002) y Ni 2 Planos de cristal P (111), respectivamente. Las asignaciones de EDX elementales (Fig. 2h – l) tomadas de la región mostrada por la imagen de campo oscuro anular de ángulo alto (HAADF) (Fig. 2g) muestran que Ni, P, Cd, Zn y S se distribuyen uniformemente entre los muestra, lo que demuestra aún más la composición exitosa de Cd 0.5 Zn 0.5 S QD con el poroso Ni 2 P nanohojas.

Microestructura de Ni 2 P y Ni 2 P-Cd 0.5 Zn 0.5 S compuesto. a – c y d – f Imágenes TEM con diferentes aumentos y patrón SAED de Ni 2 P y Ni 2 P-Cd 0.5 Zn 0.5 S, el recuadro f es el espectro EDX, donde las líneas discontinuas amarillas y blancas denotan Cd 0.5 Zn 0.5 S y Ni 2 P, respectivamente. g Imagen del sistema de campo oscuro anular de ángulo alto (HAADF) y h – l las correspondientes asignaciones EDX de Ni 2 P-Cd 0.5 Zn 0.5 S compuesto
La Figura 3a muestra el H 2 tasa de evolución de Ni 2 P-Cd 0.5 Zn 0.5 S nanocomposites varió con el contenido de Ni 2 P a la dosis de alimentación de 1 mg en un reactor de 40 mL. Pure Cd 0.5 Zn 0.5 S muestra un fotocatalítico H 2 tasa de evolución de 12,6 μM h - 1 mg - 1 y Ni 2 puro P muestra una generación de hidrógeno insignificante. Con la adición de Ni 2 P, la actividad fotocatalítica del Ni 2 P-Cd 0.5 Zn 0.5 Los compuestos S obviamente se han mejorado y alcanzan el valor más alto de 43,3 μM h - 1 mg - 1 al 1,5% en peso de Ni 2 P, casi 3.4 veces más alto que el Cd puro 0.5 Zn 0.5 S. Adición adicional de Ni 2 P (≥ 3% en peso) dará como resultado una rápida degradación de la propiedad, y el H 2 La tasa de evolución es menor que el Cd puro 0.5 Zn 0.5 S cuando Ni 2 P aumenta al 5% en peso. Tal comportamiento no lineal sugiere que existe un óptimo Ni 2 Contenido de P, es decir, una densidad de carga adecuada de Cd 0.5 Zn 0.5 S en Ni 2 P para la propiedad fotocatalítica. Al mismo tiempo, la estabilidad del 1,5% en peso de Ni 2 P-Cd 0.5 Zn 0.5 S se estudió mediante la prueba de ciclismo (Fig. 3b). Durante cuatro ciclos sucesivos que duraron un total de 16 h, el H 2 La generación se mantuvo relativamente estable con una degradación insignificante, lo que indica la buena estabilidad fotocatalítica del compuesto.
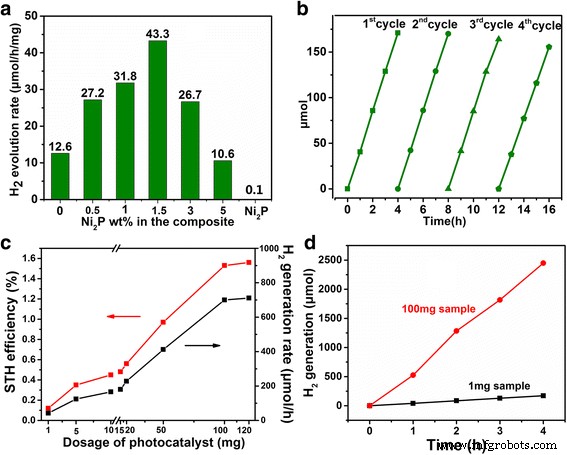
Propiedad fotocatalítica de Ni 2 P-Cd 0.5 Zn 0.5 S compuestos. un Generación de hidrógeno fotocatalítico a diferentes% en peso de Ni 2 P y b la prueba cíclica del compuesto con 1,5% en peso de Ni 2 P probado en un reactor pequeño (40 ml, 1,0 mg de fotocatalizador). c Tasa de producción de hidrógeno y eficiencia solar a hidrógeno (STH) en diversas cantidades de fotocatalizador. Las pruebas para el fotocatalizador de dosificación de 15 a 100 mg se realizaron en un reactor de 150 mL y las de dosificación de 1 a 10 mg en un reactor de 40 mL. d La tasa de generación de hidrógeno para muestras compuestas de 1 y 100 mg (1,5% en peso de Ni 2 P)
El efecto de la cantidad de catalizador en la eficiencia de STH y H 2 La generación se estudió sistemáticamente (Fig. 3c-d) para 1,5% en peso de Ni 2 P-Cd 0.5 Zn 0.5 Muestra S. Se adoptaron dos reactores típicos con un volumen de 40 y 150 ml con la misma densidad de potencia de iluminación. Cuando se prueba en el reactor más pequeño (40 ml), aunque tanto el STH como el H 2 aumento de la tasa de generación con la dosis del catalizador de 1 a 10 mg, el paso aumentado es mucho menor que el de la dosis. El STH y H 2 la tasa de generación es de solo 0.45% y 166 μM h - 1 cuando la dosis del catalizador aumentó a 10 mg, casi 3,8 veces la muestra de 1 mg. Para el reactor más grande (150 ml), aumento marcado en STH y H 2 La generación se puede encontrar con la dosis aumentada de 15 a 100 mg, y una STH de 1.53% y una h de 700 μM - 1 de H 2 La generación se puede lograr con una dosis de 100 mg, casi 3,1 veces el catalizador de 15 mg. Teniendo en cuenta que la luz incidente tiene una trayectoria más larga cuando pasa a través de un reactor más profundo, tal resultado muestra que un reactor más grande será más beneficioso para la utilización de la luz incidente. Sin embargo, la eficacia de STH se saturará una vez que la dosis se incremente a aproximadamente 100 mg, lo que sugiere que existe una dosis óptima para la utilización de la luz. El H 2 óptimo la tasa de generación es superior a CdZnS QDs-2D g-C 3 N 4 microcintas (H 2 tasa de generación 33,4 mM h - 1 g - 1 ) [10], Cd 0.1 Zn 0.9 S nanopartículas-nanotubos de carbono (velocidad:1563 μM h - 1 g - 1 ) [11], un C 3 con estructura de sándwich N 4 / Au / CdZnS fotocatalizador (velocidad 6,15 mM h - 1 g - 1 ) [9], y Zn 1 − x sensibilizado con CdS QDs Cd x S soluciones sólidas (tasa 2128 μM h - 1 g - 1 ) [48].
Revelar el mecanismo de la propiedad fotocatalítica mejorada y el papel detallado de Ni 2 P, la propiedad tanto óptica como electroquímica del Ni 2 puro P, Cd 0.5 Zn 0.5 S, y los compuestos fueron estudiados por la Fig. 4. A partir de los espectros de absorción (Fig. 4a), Cd puro 0.5 Zn 0.5 S exhibe un borde de absorción a 506 nm, correspondiente a la banda prohibida de 2,45 eV [13, 49]. Para Ni 2 puro P (el recuadro), se puede encontrar una amplia absorción en todo el rango visible. Después de la composición, además de la absorción en el rango <506 nm, se pueden encontrar colas obvias sobre la longitud de onda visible> 506 nm, que se pueden atribuir al aporte de Ni 2 P. A medida que aumenta la absorción visible en longitudes de onda más largas con Ni 2 P, el composite muestra una absorción reducida de Cd 0.5 Zn 0.5 S (<506 nm). Al mismo tiempo, los espectros de fotoluminiscencia (Fig. 4b) muestran que el Cd puro 0.5 Zn 0.5 S tiene luminiscencia de borde de banda intensiva a ~ 620 nm cuando se excita a la longitud de onda de 400 nm. Después de la composición, se degradará gradualmente con la adición de Ni 2 P. Considerando que un mayor contenido de Ni 2 P inducirá más Ni 2 P / Cd 0.5 Zn 0.5 S que ayudan a mejorar la transferencia de carga y suprimen la recombinación de carga, la disminución de la intensidad de PL puede entenderse por la recombinación de portadora reducida y la transferencia de carga mejorada en el Ni 2 P / Cd 0.5 Zn 0.5 Interfaz S.
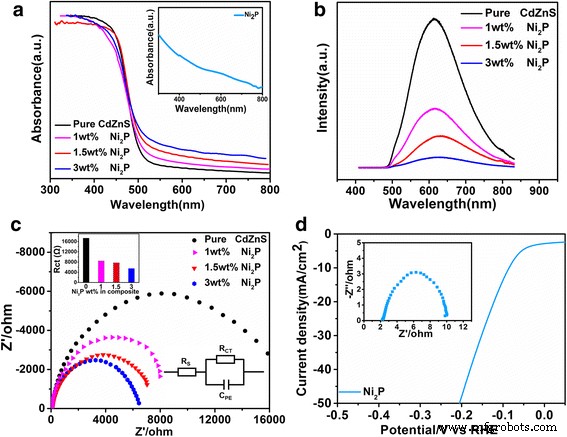
El efecto de Ni 2 Contenido de P en las propiedades ópticas y electroquímicas del Ni 2 P-Cd 0.5 Zn 0.5 S compuesto. un Espectros de absorción UV-Vis (insertado Ni 2 puro P), b espectros de fotoluminiscencia y c Espectros EIS. d Curva LSV y espectro EIS (recuadro) de Ni 2 puro P
El papel eficaz de Ni 2 P en la solicitud de transferencia de carga también puede reflejarse en los espectros EIS dependiendo de Ni 2 Contenido de P (Fig. 4c). Como se muestra en el circuito equivalente (recuadro, Fig. 4c), la resistencia de transferencia de carga (Rct) en la interfaz catalizador / electrolito se puede evaluar mediante el radio de semicírculo de los gráficos de Nyquist basados en el circuito equivalente R-C. La resistencia en serie equivalente (ESR) se puede obtener a partir de la intersección de la curva y la resistencia real ( Z ’), Mientras que la resistencia de transferencia de carga (Rct) corresponde al ancho del semicírculo trazado a frecuencias más altas. El R CT de Cd puro 0.5 Zn 0.5 S es 17.320 Ω, indicativo de su naturaleza semiconductora. Después de la composición con 1, 1,5 y 3% en peso de Ni 2 P, R CT disminuye gradualmente a 8432, 7721 y 5473 Ω, respectivamente, lo que sugiere la mejora de Ni 2 P en la conductividad eléctrica. De hecho, Ni 2 P se ha considerado como un buen electrocatalizador para HER [44, 50, 51]. De la curva LSV de Ni 2 puro P en la espuma de Ni que se muestra en la Fig. 4d, el Ni 2 P tiene buena actividad HER con sobrepotenciales de 84 mV y 201 mV para conectar la densidad de corriente de 10 y 50 mA / cm 2 (sin corrección de iR), respectivamente. El espectro EIS (recuadro Fig. 4d) muestra que Ni 2 P tiene un R CT muy bajo (~ 7,3 Ω), que indica el carácter metálico de Ni 2 P. Por lo tanto, Ni 2 P no solo puede aumentar la conductividad eléctrica en Cd 0.5 Zn 0.5 S / Ni 2 P, pero también proporciona sitios activos efectivos para HER, lo que conduce a una propiedad fotocatalítica mejorada del compuesto.
Considerando que la adición de Ni 2 P disminuyó la absorción a una longitud de onda <506 nm, es necesario demostrar si la absorción de luz de Ni 2 P se puede utilizar para generar hidrógeno. La estructura de bandas de Ni 2 A continuación, se estudió P mediante el cálculo de DFT. La Figura 5a, b presenta el modelo de bola y palo de Ni 2 a granel P y la estructura de bandas calculada. De la Fig. 5b, no se puede detectar ninguna banda prohibida, lo que sugiere la característica metálica de Ni 2 P, que concuerda bien con el resultado de EIS anterior. Esto indica que los fotoelectrones se atribuyen principalmente a la fotoexcitación de Cd 0.5 Zn 0.5 S en lugar de Ni 2 P. Además, el nivel de Fermi de Ni 2 P (obtenido del archivo de nuestro auto) se ubica en 1.03 V frente a NHE, mucho más bajo que el nivel mínimo de banda conductora (CBM) (- 1.04 V frente a NHE) de Cd 0.5 Zn 0.5 S QD [13].
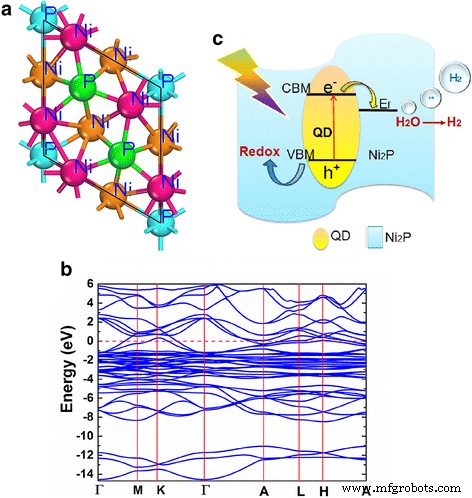
El diagrama de bandas y el mecanismo de separación y transferencia de carga para el fotocatalítico H 2 evolución. un Vistas superiores del modelo de bola y palo de (001) Ni 2 a granel terminado en superficie P. b Estructura de banda calculada de Ni 2 P donde la línea punteada roja representa el nivel de Fermi. c Mecanismo esquemático que ilustra la separación y transferencia de carga para el fotocatalítico H 2 generación
En consecuencia, se demostró el mecanismo esquemático para el fotocatalítico H 2 evolución del composite de la Fig. 5c. La ubicación del nivel de Fermi de Ni 2 P lo hace energéticamente favorable para la transferencia de electrones fotogenerados desde Cd 0.5 Zn 0.5 S a Ni 2 P, luego provoca la separación de electrones fotoexcitados y huecos en la interfaz, lo que resulta en la depresión de la recombinación de carga. Al mismo tiempo, H 2 evolucionará de manera eficiente en los sitios activos de Ni 2 P debido a la buena actividad HER y la gran superficie específica de los composites. Los roles positivos de Ni 2 La transferencia de carga de P y la actividad de HER dominarán en el contenido más bajo de Ni 2 P (≤ 1,5% en peso). Cuando el contenido supera el 1,5% en peso, el efecto de sombreado de Ni 2 El P en la absorción de luz superará el aspecto positivo, lo que conducirá a la degradación del H 2 Generacion. Se logrará una propiedad fotocatalítica óptima al 1,5% en peso de Ni 2 P cuando los dos efectos alcanzan un equilibrio.
Conclusiones
Una estructura inversa de Cd 0.5 Zn 0.5 S QD en Ni 2 Se fabricaron nanohojas porosas P para obtener H 2 fotocatalítico eficiente producción. El Ni 2 Las nanohojas porosas P estaban compuestas por nanopartículas de tamaño de 15 a 30 nm que permiten la carga efectiva de Cd 0.5 de tamaño 7 nm Zn 0.5 S QDs. Como la propiedad de transferencia y separación de carga se mejora con la adición de Ni 2 P de 0 a 5% en peso, un efecto de sombreado competitivo que no es beneficioso para la absorción de luz de Cd 0.5 Zn 0.5 S está inducido. Un H 2 fotocatalítico óptimo generación de 43,3 μM h - 1 (dosis de 1 mg) se logrará al 1,5% en peso de Ni 2 P. Basado en el contenido óptimo, la dependencia fotocatalítica de la dosis de alimentación de catalizador muestra que la eficiencia de STH alcanzará el valor más alto de 1.5% a la dosis de 100 mg. The high HER activity and band structure of Ni2 P were revealed, confirming the effective role of Ni2 P in prompting photocatalytic H2 evolution dynamics from both experimental and theoretical aspects. The heterostructure of Cn0.5 Zn0.5 S QDs-Ni2 P porous nanosheets can not only help to prompt the photo-excited charge separation and transfer, but also speed up the dynamics of hydrogen evolution reaction via the co-catalytic role of Ni2 P, thus enhances the photocatalytic hydrogen generation property. Such a method can be applied to other catalysts toward efficient photocatalytic property.
Abreviaturas
- CBM:
-
Conductive band minimum
- DFT:
-
Teoría funcional de la densidad
- EDX:
-
Espectroscopía de rayos X de energía dispersiva
- EIS:
-
Electrochemical impedance spectra
- FESEM:
-
Field emission scanning electron microscopy
- FTO:
-
Fluorine-doped tin oxide
- GGA:
-
Aproximación de gradiente generalizada
- ELLA:
-
Hydrogen evolution reaction
- LSV:
-
Linear sweep voltammetry
- NHE:
-
Normal hydrogen electrode
- PBE:
-
Perdew-Burke-Ernzerhof type
- PC:
-
Photocatalytic
- PL:
-
Fotoluminiscencia
- QD:
-
Puntos cuánticos
- RHE:
-
Electrodo de hidrógeno reversible
- STEM:
-
Microscopía electrónica de barrido de transmisión
- STH:
-
Solar to hydrogen
- TEM:
-
Microscopía electrónica de transmisión
- VASP:
-
Vienna Ab-initio Simulation Package
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X
Nanomateriales
- MoS2 con espesor controlado para evolución electrocatalítica de hidrógeno
- S, N Co-Doped Graphene Quantum Dot / TiO2 Composites para la generación eficiente de hidrógeno fotocatalítico
- Desentrañar la evolución morfológica y la cinética de grabado de nanocables de silicio poroso durante el grabado químico asistido por metales
- Actividades fotocatalíticas mejoradas por nanopartículas au-plasmónicas en un fotoelectrodo de nanotubos de TiO2 recubierto con MoO3
- Heteroestructura jerárquica de esferas huecas de ZnO @ TiO2 para una evolución fotocatalítica de hidrógeno altamente eficiente
- Un nuevo fotocatalizador de heterounión Bi4Ti3O12 / Ag3PO4 con rendimiento fotocatalítico mejorado
- Efectos sinérgicos de nanopartículas de Ag / BiV1-xMoxO4 con actividad fotocatalítica mejorada
- Modificación del cocatalizador de aleación de PtNi del híbrido g-C3N4 / GO sensibilizado con eosina Y para una evolución eficiente del hidrógeno fotocatalítico de luz visible
- Síntesis fácil y actividad fotocatalítica de luz visible mejorada de nuevos compuestos de heterounión p-Ag3PO4 / n-BiFeO3 para la degradación del tinte
- Influencia del dopaje de Mg en nanopartículas de ZnO para una evaluación fotocatalítica mejorada y análisis antibacteriano
- Propiedades fotocatalíticas sensibles a la luz visible mejoradas de los compuestos de nanohojas Ag / BiPbO2Cl



