Actividades fotocatalíticas mejoradas por nanopartículas au-plasmónicas en un fotoelectrodo de nanotubos de TiO2 recubierto con MoO3
Resumen
Aunque TiO 2 Anteriormente era un material común para las reacciones de fotocatálisis, su banda prohibida amplia (3.2 eV) da como resultado que solo absorba la luz ultravioleta, que representa solo el 4% de la luz solar total. Modificación de TiO 2 se ha convertido en un foco de investigación de reacciones de fotocatálisis, y la combinación de dos semiconductores de óxido metálico es el método más común en el proceso de mejora fotocatalítica. Cuando MoO 3 y TiO 2 entran en contacto para formar una interfaz heterogénea, los agujeros fotogenerados excitados de la banda de valencia de MoO 3 debe transferirse a la banda de valencia de TiO 2 para reducir eficazmente la recombinación de carga de pares electrón-hueco fotogenerados. Esto puede separar eficientemente los pares y promover la eficiencia de la fotocatálisis. Además, la mejora de la fotocorriente se atribuye a los fuertes efectos de campo cercano y de dispersión de la luz de las nanopartículas de Ag plasmónicas. En este trabajo, fabricamos MoO 3 -revestido de TiO 2 heteroestructuras de nanotubos con una configuración jerárquica 3D mediante oxidación anódica en dos pasos y un método hidrotermal fácil. Esta estructura jerárquica 3D consta de un TiO 2 núcleo de nanotubos y un MoO 3 shell (denominado TNTs @ MoO 3 ), caracterizado por microscopía electrónica de barrido por emisión de campo y espectroscopía fotoelectrónica de rayos X.
Antecedentes
El rápido desarrollo tecnológico ha ido acompañado de una mayor demanda de energía. En consecuencia, la investigación sobre fuentes de energía alternativas se ha vuelto popular durante la última década, con muchos científicos enfocados en fuentes de energía renovable con bajas emisiones de carbono y mínimo impacto ambiental. Estos incluyen energía solar [1, 2], calor geotérmico [3, 4], mareas [5] y diversas formas de biomasa [6, 7]. La división fotocatalítica del agua, como método más directo para lograr el objetivo de la energía limpia y renovable [8], es también el método más investigado para convertir directamente la energía solar en energía química. Algunos medios comunes de promover la eficiencia de conversión de energía incluyen aumentar el área de reacción, la deposición del catalizador y la composición con materiales secundarios; por ejemplo, sintetizar microestructuras específicas [9,10,11], depositar Pt como catalizador [12, 13] y combinar dos óxidos metálicos diferentes [14,15,16].
TiO 2 Los arreglos de nanotubos (TNT) han recibido una atención considerable por su gran área de superficie, su robusta actividad fotocatalítica y sus propiedades vectoriales de transferencia de carga [17, 18, 19]. Sin embargo, la aplicación práctica de TiO 2 está restringido por su amplia banda prohibida (3,2 eV). Esto da como resultado que se absorba solo la luz ultravioleta, que representa el 4% de la luz solar total, lo que limita en gran medida su actividad fotocatalítica en la región de la luz visible. Además, la alta tasa de recombinación de TiO 2 reduce la eficacia de la actividad fotocatalítica. Para resolver estos problemas, muchos estudios se han centrado en extender el borde de absorción del TiO 2 en la región de la luz visible, incluido el dopaje con nitrógeno u otros no metales [20, 21], la modificación de la superficie con metales nobles [22, 23] y el acoplamiento con semiconductores de banda estrecha [14,15,16].
Trióxido de molibdeno (MoO 3 ) es un semiconductor de óxido metálico de tipo p con una alta función de trabajo y una excelente conductividad del orificio; por lo tanto, se usa ampliamente en células solares orgánicas y diodos emisores de luz orgánicos [24, 25]. MoO 3 tiene una banda prohibida de aproximadamente 2,8 eV, con un 20-30% de carácter iónico y la capacidad de absorber tanto la luz UV como la visible [26]. Las posiciones de las bandas de conducción y valencia de MoO 3 son ambos más bajos que los de TiO 2 . Por lo tanto, una heterounión entre TiO 2 y MoO 3 podría mejorar la actividad fotocatalítica al disminuir la recombinación de carga y promover el proceso de transferencia de carga [27]. Bajo irradiación de luz visible, los agujeros excitados de la banda de valencia de MoO 3 debe transferirse a la banda de valencia de TiO 2 , para reducir la recombinación de carga de pares electrón-hueco fotogenerados.
La fotocatálisis plasmónica ha facilitado recientemente la rápida mejora de la eficacia fotocatalítica bajo irradiación de luz visible [28, 29]. Un plasmón de superficie es una onda electromagnética de superficie en la interfaz metal-dieléctrico, ampliamente utilizada en detección óptica, química y biológica debido a la alta sensibilidad de sus ondas resonantes. El efecto de resonancia del plasmón superficial se limita a la superficie del metal para formar un campo eléctrico altamente mejorado [30]. Cuando la frecuencia de resonancia particular de las nanopartículas de metal plasmónico coincide con la del fotón incidente, se forma un campo eléctrico fuerte cerca de la superficie del metal. Además, las interacciones sintonizables entre la luz visible incidente y las nanopartículas plasmónicas excitadas se logran controlando sus tamaños y formas, así como la constante dieléctrica del entorno circundante [31,32,33].
En el presente trabajo, primero sintetizamos MoS 2 Recubrimiento en la superficie de TNTs a través de un método hidrotermal. MoS 2 luego se oxidó a MoO 3 mediante un sencillo proceso de recocido (esquema 1). Este proceso permitió una alta cobertura de MoO 3 partículas a nanoescala con una estructura muy ordenada. Para mejorar aún más el rendimiento fotocatalítico de división del agua, introdujimos un efecto de resonancia de plasmón superficial (SPR).
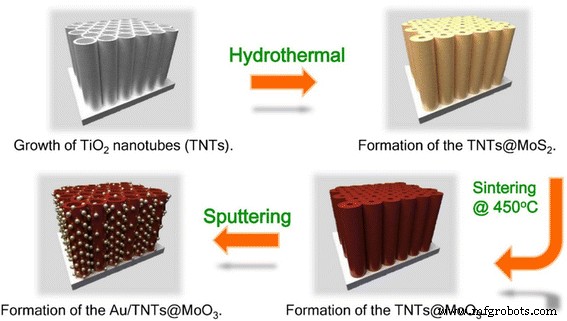
Separación de carga en la interfaz del TiO 2 –MoO 3 compuesto
Métodos
Fabricación del TiO 2 Nanotubos
Los TNT se fabricaron mediante un método de oxidación anódica de dos pasos. Antes del proceso de oxidación anódica, la hoja de titanio se cortó a la medida y se colocó en acetona, luego en etanol, luego en agua desionizada (DI) y luego se sometió a vibración ultrasónica durante 5 min. La oxidación anódica se llevó a cabo utilizando un sistema convencional de dos electrodos con la hoja de Ti como ánodo y una varilla de carbono como cátodo. Todos los electrolitos consistían en un 0,3% en peso de fluoruro de amonio (NH 4 F) en etilenglicol (C 2 H 6 O 2 , EG) solución con 5% en volumen de agua. Todos los procesos se llevaron a cabo a temperatura ambiente.
En el primer paso de oxidación anódica, la hoja de Ti se anodizó a 60 V durante 30 min; los nanotubos recién desarrollados se eliminaron posteriormente en HCl 1 M mediante vibración ultrasónica. A continuación, la misma hoja de Ti se sometió a un segundo proceso de oxidación anódica a 60 V durante 30 min. Una vez completados ambos pasos, los TNT preparados se lavaron con etanol y agua desionizada. Los TNT se recocieron en aire a 450 ° C durante 4 horas a una velocidad de calentamiento de 2 ° C / min para formar los TNT anatasa.
Síntesis de TNTs @ MoO 3 Estructura núcleo-carcasa
Los TNTs @ MoO 3 La estructura núcleo-capa se sintetizó con un método hidrotermal y un proceso de recocido simple. MoS 2 Las nanohojas se sintetizaron mediante los siguientes procedimientos:0,12 g de molibdato de sodio (Na 2 MoO 4 · 2H 2 O) y 0,24 g de tioacetamida (TAA) se disolvieron en 80 ml de agua desionizada con agitación vigorosa durante 15 min. Posteriormente, la solución transparente y los TNT crecidos se transfirieron a un autoclave de acero inoxidable revestido con teflón de 100 ml, que se selló y se calentó a 200 ° C a una velocidad de calentamiento de 3 ° C / min y se mantuvo durante 24 h. Después de que el autoclave se enfrió a temperatura ambiente, los TNT preparados @ MoS 2 se lavaron con agua desionizada. Los TNTs @ MoS 2 se recocieron en aire a 450 ° C durante 4 h con una velocidad de calentamiento de 2 ° C / min para formar los TNT @ MoO 3 estructura núcleo-caparazón.
Deposición de nanopartículas de Au
Los fotoelectrodos del cocatalizador plasmónico (Au / TNTs @ MoO 3 ) se fabricaron con los TNT preparados @ MoO 3 estructura cocatalítica núcleo-capa a través del método hidrotermal, seguido de la deposición catódica estándar de nanopartículas de Au.
Análisis característico y mediciones de fotocorriente
Las microestructuras y morfologías de las muestras se examinaron mediante microscopía electrónica de barrido por emisión de campo (FE-SEM) y espectroscopía de rayos X de dispersión de energía (EDS). Para confirmar la energía de unión del TiO 2 desarrollado , MoS 2 y MoO 3 fotoelectrodos, se empleó espectroscopia de fotoelectrones de rayos X (XPS). Finalmente, la reacción fotocatalítica se midió en una solución de NaOH 1 M operando tres potenciostatos terminales a temperatura ambiente bajo irradiación láser de 532 nm con un tamaño de punto de 1 mm de diámetro.
Resultados y discusión
La Figura 1 muestra las imágenes SEM y el mapeo EDS de las muestras preparadas. La Figura 1a – c muestra las imágenes SEM de los TNT, TNTs @ MoS 2, y TNTs @ MoO 3 . La imagen SEM de TNT obtenida por oxidación anódica en dos pasos de lámina de Ti en 0,3% en peso de NH 4 El F contenido en la solución de etilenglicol (Fig. 1a) exhibió un tamaño de poro uniforme (100-120 nm). Después de que se formó la estructura núcleo-capa con MoS 2 cubierto mediante el método hidrotermal, la estructura porosa de los TNT no se bloqueó para reducir los sitios de reacción activos (Fig. 1b). Posteriormente, los TNTs @ MoO 3 La estructura núcleo-carcasa se formó mediante un proceso de recocido simple en el horno de tubo (Fig. 1c). La Figura 1d muestra la imagen SEM y el mapeo EDS de Au / TNTs @ MoO 3 , proporcionando información clara sobre Ti, O, Mo y Au. La deposición uniforme de nanopartículas de Au en forma de isla, observable en la parte superior de los TNT @ MoO 3 , facilitó la generación del efecto SPR.

Imágenes SEM de a TNT, b TNTs @ MoS 2 , c TNTs @ MoO 3 y d Au / TNTs @ MoO 3 (izquierda), así como el mapeo EDS (derecha)
Se utilizó XPS para investigar los estados químicos de los TNT @ MoO 3 después de la conversión de TNTs @ MoS 2 mediante un sencillo proceso de recocido (Fig. 2). En la Fig. 2a, b se pueden observar tres picos característicos de Ti y O. Las energías de enlace en los picos de Ti2p1, Ti2p3 y O1s son 464,6, 458,9 y 530,4 eV, respectivamente. En la Fig. 2c, se puede identificar un pico de Mo3d3 a 231,6 eV y un pico de Mo3d5 a 228,9 eV, lo que indica la composición química de MoS 2 en los TNTs @ MoS 2 . Además, un pico débil que aparece a aproximadamente 226 eV es el pico de señal de S2s. Los picos de Mo3d3 y Mo3d5 en la Fig. 2d con energías de enlace de 235,6 y 232,6 eV se atribuyen a Mo 6+ en MoO 3 . Por lo tanto, las investigaciones de XPS confirman que el desplazamiento hacia el rojo del espectro refleja la conversión de la valencia del elemento Mo de tetravalente a hexavalente.
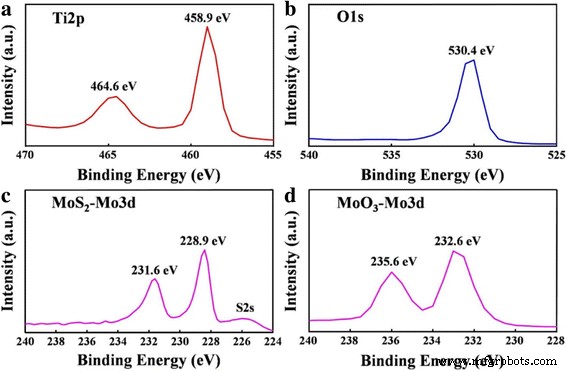
Análisis XPS de a Ti2p, b O1s, c Mo3d de MoS 2 y d Mo3d de MoO 3
El rendimiento fotocatalítico de separación de agua de los fotoelectrodos preparados se midió con irradiación láser de 532 nm. La Figura 3a, b muestra la respuesta de fotocorriente (curvas I – V) de TNTs @ MoO 3 y Au / TNTs @ MoO 3 . Según los resultados, TiO 2 @MoO 3 exhibe una fotocorriente más alta debido a la tasa de separación de carga mejorada en el TiO 2 @MoO 3 interfaz heterogénea (mostrada en la Fig. 3a). Además, con la integración de nanopartículas de Au, Au / TNTs @ MoO 3 presentó una respuesta de fotocorriente aproximadamente 1,5 veces mayor que los TNT @ MoO 3 a la tensión de polarización de −1 V. La figura 3c muestra las curvas I – T de los TNT, TNT @ MoO 3 y Au / TNT @ MoO 3 con el voltaje de polarización de 0 V. Como se muestra en la Fig. 3c, la respuesta de la fotocorriente fue mayor nuevamente en los Au / TNTs @ MoO 3 estructura en comparación con los TNTs @ MoO 3 fotoelectrodo sin la aplicación de voltaje de polarización. La respuesta de fotocorriente de Au / TNTs @ MoO 3 podría mejorarse mediante el simple efecto SPR.
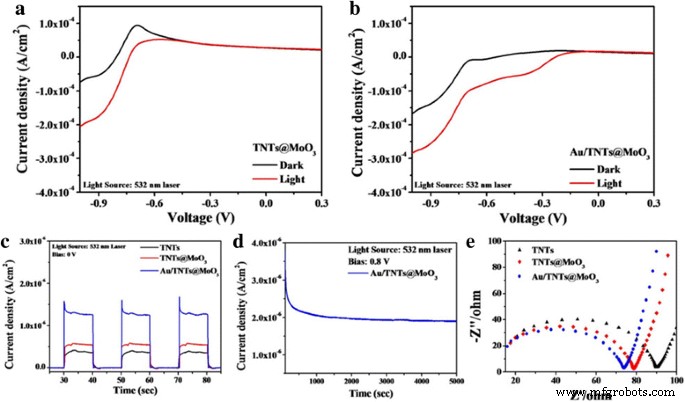
Curvas de barrido lineal de fotoelectrodos a sin y b con irradiación de luz y respuestas de fotocorriente en c 0 V (fuente de luz:láser de 532 nm). d Mediciones de fotocorriente prolongadas bajo irradiación láser de 532 nm. e Gráficos de Nyquist de varios fotoelectrodos
Para investigar más a fondo la actividad fotocatalítica de los fotoelectrodos preparados, también examinamos las respuestas de fotocorriente extendida y la espectroscopia de impedancia electroquímica para comprender la estabilidad de la fotocorriente y la transferencia de carga en las interfaces fotoelectrodo-electrolito (Fig. 3d, e). La estabilidad extendida del fotoelectrodo con el rendimiento óptimo, Au / TNTs @ MoO 3 , se examinó bajo irradiación láser de 532 nm durante aproximadamente 1,5 h (Fig. 3d). A la tensión aplicada de 0,8 V, la fotocorriente se mantuvo al 57% de su valor inicial. La Figura 3e muestra los gráficos de Nyquist de los tres fotoelectrodos probados bajo irradiación láser de 532 nm registrados a un potencial de CC de 1,23 V frente a RHE y un rango de frecuencia de potencial de CA de 10 6 –1 Hz con una amplitud de 1 V bajo irradiación láser de 532 nm. Según los resultados, se pueden observar diámetros de semicírculo más pequeños en los Au / TNTs @ MoO 3 muestra, lo que indica una impedancia de transporte más baja para los portadores de carga. La formación de una interfaz heterogénea entre TiO 2 y MoO 3 se ha confirmado que facilita la transferencia de carga y mejora la actividad fotocatalítica a través de las excelentes propiedades de conducción de portadores de las nanopartículas de Au.
Conclusiones
Información de respaldo
En la información de apoyo (archivo adicional 1) realizamos el análisis de espectros Raman de MoS 2 capa, el grosor relacionado y el tamaño de poro medio de las imágenes SEM de TNT, y el mecanismo de mejora del sistema.
En este estudio, fabricamos con éxito un TNTs @ MoS 2 heteroestructura núcleo-capa mediante un proceso de oxidación anódica de dos pasos y un método hidrotermal fácil para formar TNTs @ MoO 3 estructura núcleo-capa a través de un sencillo proceso de recocido. Según los resultados, un MoO 3 El revestimiento de un fotoelectrodo puede mejorar su utilización de fotones en la región visible. Además, con la integración de nanopartículas plasmónicas de Au, se observó una mejora significativa en la fotocorriente de división del agua en comparación con el TiO 2 puro. nanotubos bajo irradiación de luz visible. La ingeniería de bandas de energía de los TNTs @ MoO 3 la heteroestructura favorece la transferencia de carga y suprime la recombinación de pares de electrones-huecos fotogenerados entre MoO 3 y TiO 2 , lo que conduce a una actividad fotocatalítica mejorada.
Nanomateriales
- Síntesis fácil de compuesto de CuSCN coloreado y conductor recubierto con nanopartículas de CuS
- Síntesis hidrotermal de nanopartículas de In2O3, gemelos híbridos, discos hexagonales, heteroestructuras de ZnO para mejorar las actividades fotocatalíticas y la estabilidad
- Biocompatibilidad mejorada en matrices anódicas TaO x nanotubos
- Un nuevo fotocatalizador de heterounión Bi4Ti3O12 / Ag3PO4 con rendimiento fotocatalítico mejorado
- Matrices de nanotubos de TiO2:fabricadas con una plantilla blanda-dura y la dependencia del tamaño de grano del rendimiento de las emisiones de campo
- Efectos sinérgicos de nanopartículas de Ag / BiV1-xMoxO4 con actividad fotocatalítica mejorada
- Determinación de la actividad catalítica de nanopartículas de TiO2 dopado con metal de transición mediante análisis espectroscópico de superficie
- Efecto del agente peptizante ácido sobre la relación anatasa-rutilo y el rendimiento fotocatalítico de nanopartículas de TiO2
- Un método sencillo para cargar nanopartículas de CeO2 en matrices de nanotubos de TiO2 anódico
- Eficiencia de conversión de energía mejorada de células solares de perovskita con un material de conversión ascendente de Er3 + -Yb3 + -Li + TiO2 tri-dopado
- Influencia del dopaje de Mg en nanopartículas de ZnO para una evaluación fotocatalítica mejorada y análisis antibacteriano



