Efecto del agente peptizante ácido sobre la relación anatasa-rutilo y el rendimiento fotocatalítico de nanopartículas de TiO2
Resumen
TiO 2 Las nanopartículas se sintetizaron a partir de isopropóxido de titanio mediante un método de peptización simple utilizando ácidos sulfúrico, nítrico y acético. El efecto del ácido peptizante sobre las propiedades fisicoquímicas y fotocatalíticas del TiO 2 Se estudió polvos. Las propiedades estructurales del TiO 2 sintetizado los polvos se analizaron utilizando XRD, TEM, N 2 -fisisorción, Raman, DR UV- vis , FTIR y técnicas de espectroscopía de fotoelectrones de rayos X. Los resultados de la caracterización mostraron que la peptización con ácido acético facilitó la formación de fase anatasa pura después del tratamiento térmico a 500 ° C; por el contrario, la peptización con ácido nítrico condujo a una importante formación de fase rutilo (67%). Curiosamente, la muestra peptizada usando ácido sulfúrico produjo 95% de fases de anatasa y 5% de rutilo. La actividad fotocatalítica del TiO 2 sintetizado Se evaluó la degradación de nanopartículas de colorantes orgánicos seleccionados (violeta cristal, azul de metileno y p -nitrofenol) en solución acuosa. Los resultados confirmaron que el TiO 2 La muestra peptizada con ácido nítrico (con fases de rutilo y anatasa en una proporción de 3:1) ofreció la mayor actividad para la degradación de colorantes orgánicos, aunque TiO 2 las muestras peptizadas con ácido sulfúrico y ácido acético poseían un tamaño de partícula más pequeño, una energía de banda prohibida más alta y un área de superficie alta. Curiosamente, TiO 2 La muestra peptizada con ácido nítrico poseía una densidad de fotocorriente teórica relativamente alta (0,545 mAcm −2 ) y diámetro de poro (150 Å), que son responsables de la alta eficiencia de separación de huecos de electrones y la difusión y transporte masivo de reactivos orgánicos durante el proceso de degradación fotoquímica. La actividad superior de TiO 2 La muestra peptizada con ácido nítrico se debe a la transferencia efectiva de electrones fotogenerados entre las fases de rutilo y anatasa.
Antecedentes
Dióxido de titanio (TiO 2 ) es un material semiconductor ampliamente conocido por su uso en muchas aplicaciones, incluida la conversión de energía solar, el control de la contaminación y la fotocatálisis [1, 2, 3]. TiO 2 generalmente tiene tres polimorfos, a saber, anatasa, rutilo y brookita. Se informó que la anatasa y la brookita se pueden transformar en rutilo después de un tratamiento térmico a alta temperatura (<610 ° C) [4, 5]. TiO 2 Se sabe que la anatasa es un fotocatalizador activo para la degradación de contaminantes orgánicos [1, 5, 6, 7, 8]. Se observó que el tamaño, la fase cristalina y la porosidad del TiO 2 las muestras tienen una gran influencia sobre sus aplicaciones [9]. Síntesis a baja temperatura de TiO 2 nanométrico poroso requiere tiempos de síntesis más largos [10,11,12]. Li y col. [13] sintetizó anatasa pura y una mezcla de las fases de rutilo y anatasa mediante el tratamiento térmico del TiO 2 amorfo. . La formación de anatasa pura implica un tratamiento térmico a alta temperatura (500 ° C) [14], que a menudo provoca la sinterización del TiO 2 nanoestructuras. La síntesis de anatasa cristalina pura a temperaturas más bajas es un tema de investigación interesante [15]. Se utilizaron métodos de síntesis hidrotermal y sol-gel [16] para preparar un TiO 2 bien cristalino a baja temperatura y tiempo de reacción corto [17]. Wang y col. [12] nanopartículas de rutilo y anatasa altamente cristalinas sintetizadas por HNO 3 hidrotermal TiO 2 peptizado soles. Sin embargo, el método hidrotermal exige condiciones de síntesis especiales y equipos costosos que podrían soportar pH y temperaturas elevadas [18].
El método de síntesis sol-gel se utilizó utilizando el alcóxido de titanio como precursor de Ti a una temperatura suave (<100 ° C), y produjo TiO 2 nanométrico altamente dispersado. muestras [16]. El método de peptización química se adaptó para la síntesis de nanoestructuras estables de óxidos metálicos, incluido el TiO 2 [19], donde la suspensión coagulada se disuelve y recristaliza en la solución estable de nanopartículas con el agente peptizante [20]. Se informó que la naturaleza del ácido peptizante tiene un efecto sobre las características fisicoquímicas como el tamaño de los cristalitos, la composición y la morfología de las partículas [21]. Zaban y col. [22] TiO 2 sintetizado coloides con HNO 3 y CH 3 COOH en condiciones hidrotermales y se observó la formación de mezcla de anatasa y brookita en ambos casos. Liu y col. [23] obtuvo TiO 2 hidrosol del ácido metatitanico bajo diferentes agentes peptizantes y estudió la influencia de las condiciones peptizantes en las propiedades estructurales y fotocatalíticas del TiO 2 hidrosoles. Kanna y Wongnawa [24] emplearon el método de síntesis sol-gel para obtener rutilo-anatasa amorfo mediante el uso de diferentes ácidos como HCl, HNO 3 , H 2 SO 4 , H 3 PO 4 y CH 3 COOH. Los autores observaron que la presencia de grupos sulfato y fosfato son responsables de la inhibición del crecimiento de la fase rutilo. Posteriormente, Alphonse et al. [25] TiO 2 sintetizado agregados, que se componen de fase anatasa y brookita por hidrólisis de isopropóxido de titanio en un medio altamente ácido. Parra y col. [26] estudiaron la vía de reacción en la síntesis de nanopartículas de anatasa con ácido acético. Utilizaron técnicas FTIR y NMR para concluir que los iones acetato actúan como ligando bidentado entre dos centros de Ti.
Zhou y col. [27] estudiaron el efecto del HCl, HNO 3 y CH 3 COOH en método solvotermal para sintetizar 3D TiO 2 estructuras con diferente morfología. Los autores concluyeron que la muestra sintetizada con HCl 0,68 M poseía ambas fases anatasa / rutilo y ofrecía la mayor actividad fotocatalítica debido a su morfología y propiedades ópticas únicas. Tobaldi y col. [28] adoptó la hidrólisis / peptización controlada del isopropóxido de titanio con HNO 3 , HBr y HCl para sintetizar TiO 2 nanopartículas. Se observó que los iones haluro mejoraron la transición de fase de anatasa a rutilo, y las muestras contenían hasta 77% en peso de rutilo y 5% en peso de brookita después de la calcinación a 450 ° C.
En una publicación anterior [29], síntesis de TiO 2 nanométrico Se realizaron polvos mediante peptización ácida de xerogeles en condiciones de humedad atmosférica. Se observó que la peptización ácida acompañada de vibraciones ultrasónicas tiene efecto sobre el TiO 2 propiedades estructurales. Sin embargo, solo se dedicaron pocos estudios a estudiar el efecto de las condiciones de peptización sobre la formación de la fase rutilo y su efecto posterior sobre la actividad fotocatalítica del TiO 2 nanopartículas. En este artículo, examinamos la influencia de la naturaleza del ácido peptizante (H 2 SO 4 , HNO 3 y CH 3 COOH) en la formación de la fase rutilo y su influencia en la eficiencia fotocatalítica del TiO 2 nanopartículas en la degradación de tres contaminantes orgánicos diferentes (violeta cristal (CV), azul de metileno (MB) y p -nitrofenol ( p -NP)).
Métodos
Preparación de nanopartículas de TiO2 usando diferentes ácidos peptizantes
Tetraisopropóxido de titanio [Ti (OPri) 4 ] se utilizó como precursor de Ti, y la hidrólisis de Ti (OPri) 4 se llevó a cabo en condiciones atmosféricas estándar [29]. El procedimiento de síntesis típico se puede describir de la siguiente manera:50 mL de Ti (OPri) 4 se colocó en una botella de vidrio oscuro y la botella se dejó en la campana de humos durante 15 días. La temperatura y la humedad de la campana extractora se midieron como 25 ± 5 ° C y 50 ± 10%, respectivamente. La hidrólisis del precursor de Ti se completó en 15 días y la solución resultante se transformó en un gel, que luego se secó para obtener xerogel. El ácido peptizante (100 ml de CH 3 1 N COOH o HNO 3 o H 2 SO 4 ) se pipeteó en un vaso de precipitados de vidrio y se añadió lentamente la cantidad conocida de polvo de xerogel amorfo (2,0 g) al ácido peptizante con agitación constante. Luego, el vaso de precipitados se colocó en un baño ultrasónico que se mantuvo a 40 ° C, y la mezcla se sometió a tratamiento ultrasónico durante 10 min. El TiO 2 peptizado Las nanopartículas se recogieron después de la centrifugación. Luego, los materiales se lavaron con agua destilada y se calcinaron durante 3 ha 500 ° C. Las muestras sintetizadas se etiquetaron como TiO 2 prefijo de acrónimo después de su ácido peptizante como "ace", "nit" y "sul" correspondiente a CH 3 COOH, HNO 3 y H 2 SO 4 , respectivamente.
Caracterización del material
Los perfiles de difracción de rayos X en polvo se recogieron utilizando un difractómetro Philips PW1700 con radiación Cu Kα y monocromador de grafito con rendija divergente automática. Los perfiles XRD se indexaron con datos JCPDS estándar. Fórmula de Spurr y Myers [30] [Eq. (1)] se utilizó para determinar las fracciones en peso de las fases anatasa y rutilo.
$$ {X} _ {\ mathrm {R}} =1 / \ left [1 + k \ \ left ({I} _ {\ mathrm {A}} / {I} _ {\ mathrm {R}} \ derecha) \ derecha] $$ (1)donde yo A y yo R son las intensidades integradas de (101) reflexión de anatasa y (110) reflexión de rutilo, respectivamente. La constante empírica k se tomó como 0,80 en este trabajo. El tamaño de cristalito de las muestras sintetizadas se midió usando la fórmula de Scherrer [Eq. (2)] y reflejos de anatasa (101) y rutilo (110).
$$ D =B \ lambda / {\ beta} _ {1/2} \ cos \ theta $$ (2)donde D es el tamaño medio de cristalito de la fase, B es la constante de Scherrer (0.89), λ es la longitud de onda de la radiación de rayos X (1,54056 Å), β 1/2 es el ancho completo a la mitad del máximo de la reflexión, y θ es el ángulo de difracción.
El análisis TEM de las muestras se llevó a cabo utilizando un microscopio Philips CM200FEG equipado con una pistola de emisión de campo a 200 kV. Se aplicó el coeficiente de aberración esférica Cs =1,35 mm. Se tomaron imágenes HRTEM con un tamaño de píxel de 0,044 nm con una cámara CCD. El análisis espectral láser Raman de las muestras se realizó con el espectrómetro Bruker Equinox 55 FT-IR equipado con un módulo FRA106 / S FT-Raman y un N 2 líquido. -detector de Ge enfriado que utiliza la línea de 1064 nm de un láser Nd:YAG con una potencia de salida del láser de 200 mW.
N 2 -Las mediciones de fisisorción se realizaron utilizando el instrumento ASAP 2010, Micromeritics Instrument Corporation, EE. UU. Área de superficie específica ( S APUESTA ) de las muestras se midieron utilizando N 2 -valores de adsorción y la ecuación BET. El ancho de poro y el volumen de poro de las muestras se determinaron aplicando el método BJH.
Reflectancia difusiva UV- vis espectros para TiO 2 sintetizado las muestras se registraron con el espectrofotómetro Thermo Scientific Evolution en el rango de longitud de onda de 220 a 700 nm. La energía de la banda prohibida de las muestras se determinó mediante la transformación de Kubelka-Munk ( K ) como se presenta en la Ec. (3).
$$ K =\ frac {{\ left (1-R \ right)} ^ 2} {2R} $$ (3)donde R es la reflectancia. Las longitudes de onda (nm) se tradujeron en energías (eV), y una gráfica de \ ({\ left (\ mathrm {Kh} \ upnu \ right)} ^ {0.5} \) vs. hν fue dibujado. La energía de la banda prohibida (eV) se estimó como la intersección de las dos pendientes de la curva dibujada.
Los espectros de fotoelectrones de rayos X de las muestras se recogieron utilizando un instrumento Thermo Scientific Escalab 250 Xi XPS con rayos X Al Kα con un tamaño de punto de 650 mm. El cambio de pico debido a la compensación de carga se corrigió utilizando la energía de enlace de C 1s cima. Los datos se adquirieron utilizando energía de paso de 100 eV, tiempo de permanencia de 200 ms con un tamaño de paso de 0,1 eV y 10 a 30 exploraciones.
Degradación fotocatalítica de cristal violeta, azul de metileno y p -Nitrofenol
La degradación fotocatalítica de CV, MB y p -Los experimentos de NP se realizaron en un reactor de vidrio utilizando TiO 2 sintetizado muestras como fotocatalizador bajo irradiación UV para diferentes tiempos de reacción. Se utilizaron un total de seis lámparas UV negras (F20 T8 BLB) con una potencia de 18 W y dimensiones de 60 × 2,5 cm. La potencia total de la irradiación UV en la superficie de una solución acuosa de colorante orgánico se midió con un detector Newport 918DUVOD3, y el medidor de potencia se midió como 13 Wm −2 . Se añadieron cien miligramos de catalizador a 100 ml de solución acuosa de contaminante orgánico (10 ppm). Antes de la evaluación de la eficacia fotocatalítica del catalizador, la solución de colorante orgánico se equilibró con el catalizador agitando durante 45 min para estabilizar la adsorción de colorante orgánico en la superficie del catalizador. La degradación fotocatalítica de CV, MB y p -NP se controló midiendo la absorbancia de colorante orgánico en un intervalo de tiempo regular utilizando un Thermo Fisher Scientific Evolution 160 UV- vis espectrofotómetro. El porcentaje de degradación se calculó mediante la expresión
$$ \ eta =\ left (1-C / {C} _0 \ right) \ times 100 $$ (4)Donde C 0 es la concentración de tinte orgánico antes de la iluminación y C es la concentración después de un cierto tiempo de reacción.
La estabilidad de los fotocatalizadores se analizó mediante experimentos de reutilización. La regeneración del catalizador se llevó a cabo mediante un procedimiento sencillo. Después del primer ciclo de medición de la actividad, el catalizador se filtró del fotorreactor y las alícuotas por centrifugación. El catalizador obtenido se lavó a fondo con agua destilada y acetona. El catalizador se secó a 50 ° C durante 2 hy luego se reutilizó para el siguiente ciclo de las mediciones de fotocatálisis. De manera similar, el experimento se repitió durante varios ciclos para estudiar la estabilidad del catalizador.
Resultados y discusión
Difracción de rayos X en polvo
Los patrones de difracción de rayos X del TiO 2 calcinado -ace, TiO 2 -nit y TiO 2 -sul se muestran en la Fig. 1. Las posiciones e intensidades de los picos de XRD para TiO 2 Las fases presentadas en las muestras se complementan con la base de datos JCPDS. Se sabe que la fase anatasa muestra picos de difracción importantes a 2 θ valores de 24,8 °, 37,3 °, 47,6 °, 53,5 °, 55,1 ° y 62,2 ° coincidentes con (101), (004), (200), (105), (211) y (204) planos de cristal [JCPDS Nº 21-1272]. Por otro lado, la fase de rutilo muestra picos de difracción importantes a 2 θ valores de 27.0 °, 35.6 °, 40.8 °, 54.0 °, 53.9 °, 56.1 ° y 61.0 ° que corresponden a los planos cristalinos de (110), (101), (200), (111), (210), ( 211), (220), (002) y (310) [JCPDS No. 21-1276]. El tamaño de cristalito y las fracciones de peso de las fases de anatasa y rutilo presentadas en las muestras se determinaron utilizando la fórmula de Scherrer y el método de Spurr y Myers, respectivamente. El patrón XRD de polvo de TiO 2 -la muestra mostró que está compuesta de fase anatasa pura (100%) con un tamaño de partícula de 48 nm (Tabla 1).
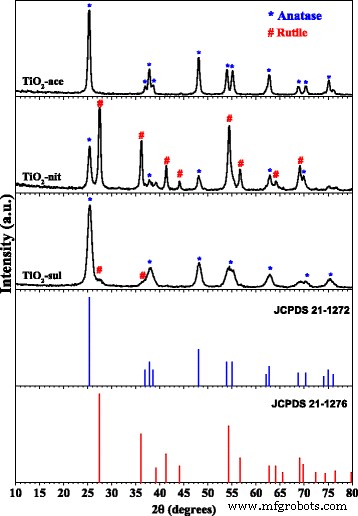
Patrones de XRD en polvo del TiO 2 calcinado samples (reimpreso con permiso de [29]. Copyright @ 2017 Elsevier)
El TiO 2 -la muestra de sul poseía principalmente fase anatasa (95%) con un tamaño de partícula de alrededor de 23 nm; sin embargo, en esta muestra puede verse un pequeño pico de difracción correspondiente al plano (110) de la fase de rutilo. En contraste, TiO 2 La muestra de nitritos mostró reflejos XRD para ambas fases, anatasa y rutilo, con un tamaño de cristalito de 41 nm y 50 nm, respectivamente. Se observa que el rutilo es la fase mayoritaria (67%) en esta muestra. Estos resultados indican que la naturaleza del ácido peptizante juega un papel en la formación de TiO 2 fase.
Microscopía electrónica de transmisión de alta resolución
Se realizó TEM para examinar el tamaño de las partículas, la cristalinidad y la morfología del TiO 2 sintetizado nanopolvos. Las imágenes TEM y HRTEM de TiO 2 sintetizado Los nanopolvos se muestran en la Fig. 2. Se puede ver que el TiO 2 -La muestra de sul consta de partículas de anatasa aglomeradas muy compactas con un tamaño de grano medio estimado de aproximadamente 7 nm. El TiO 2 -La muestra de liendre poseía nanopartículas de tamaño entre 10 y 20 nm con morfología esférica y también grandes láminas de 20 nm de ancho. En contraste, TiO 2 -la muestra consta de TiO 2 Las nanopartículas (15–20 nm) consistían en una morfología esférica mayoritariamente definida. Vinogradov y Vinogradov [31] también observaron el tipo similar de resultados de que los agregados de tamaño pequeño se detectaron cuando ácidos peptizantes fuertes como HNO 3 y H 2 SO 4 se utilizaron para la peptización. El tamaño de cristalito medido por la fórmula de Scherer resultó en tamaños de cristalito más grandes en comparación con el tamaño de grano medido con análisis TEM. Como se informó anteriormente, el tamaño de los cristalitos es diferente del tamaño del grano; sin embargo, el tamaño de los cristalitos podría coincidir con el tamaño del grano en algunos casos [32]. Se puede observar que las imágenes HRTEM de TiO 2 -sul y TiO 2 -Las muestras de acera mostraron partículas que contenían franjas correspondientes a planos de celosía cristalina anatasa con d -espaciado de 0.356 nm para el plano (101) [33], mientras que la imagen HRTEM de TiO 2 -La muestra de liendres mostró partículas con franjas de celosía para el plano de celosía de cristal de rutilo (110) con d -espaciado de 0.325 nm junto con el plano de la red cristalina anatasa (101).

Imágenes TEM y HRTEM del TiO 2 calcinado muestras
Espectroscopia Raman
La espectroscopia Raman también se utilizó para sondear la formación de fase en el TiO 2 sintetizado muestras. La Figura 3 muestra los espectros Raman obtenidos para los tres TiO 2 muestras calcinadas a 500 ° C. Se informa que las fases anatasa y rutilo poseían seis y cinco bandas Raman activas, respectivamente, (anatasa 143, 195, 395, 512 y 638 cm −1 ; rutilo 145, 445, 611 y 826) [34]. De la Fig.3 se desprende claramente que las tres muestras mostraban una banda Raman muy intensa y nítida ( E g ) en el rango de 141-146 cm −1 , que es banda característica debido a la presencia de fase anatasa. En la figura insertada se pueden observar claramente bandas de Raman de baja intensidad debido a las fases anatasa y rutilo. El TiO 2 -nit y TiO 2 -las muestras de sul mostraron bandas Raman debidas tanto a las fases anatasa como a las de rutilo; sin embargo, la intensidad de las bandas Raman debido a la presencia de la fase rutilo es alta en el caso de TiO 2 -muestra de liendres. En contraste, TiO 2 -La muestra de ace mostró bandas Raman debido a la fase anatasa únicamente.
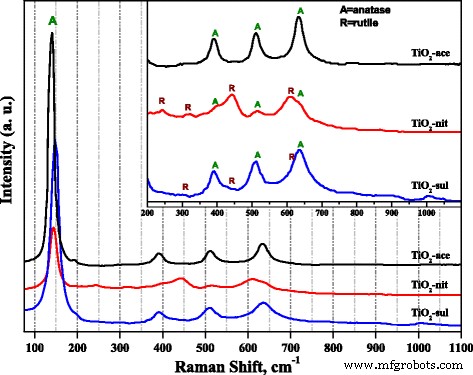
Espectros Raman del TiO 2 calcinado muestras
Se informó que los resultados de la espectroscopía Raman podrían usarse para investigar el tamaño de partícula de TiO 2 nanopartículas, ya que un cambio de banda inusual de las bandas Raman podría correlacionarse con la disminución del tamaño de partícula de las muestras [35]. En la figura 3, el TiO 2 -la muestra exhibida E g banda a 141,5 cm −1 ; sin embargo, la banda se cambió a 146 y 150 cm −1 en el caso de TiO 2 -nit y TiO 2 -sul muestras, respectivamente. Las observaciones de los espectros Raman indican que TiO 2 -La muestra de sul poseía un tamaño de partícula más pequeño que las otras dos muestras, lo cual está de acuerdo con las observaciones de XRD y TEM.
Reflectancia difusa UV- vis
El DR UV- vis espectros del TiO 2 sintetizado Las muestras tratadas térmicamente a 500 ° C se muestran en la Fig. 4. La posición del pico máximo en la derivada de la DR UV- vis Los espectros de tres muestras se muestran en el recuadro de la figura. Muestra claramente que las muestras tienen una fuerte reflectancia electrónica en la región UV. El pico máximo de reflectancia es diferente para las muestras sintetizadas usando tres ácidos diferentes. El TiO 2 -sul muestra un pico máximo a 372 nm, mientras que se desplaza a 383 nm en TiO 2 -ace y 402 nm para TiO 2 -muestra de liendres, respectivamente. Se informa que la anatasa y el rutilo tienen una energía de banda prohibida de 3,2 eV (380 nm) y 3,0 eV (415 nm), respectivamente [1]. Las diferencias en la reflectancia máxima podrían atribuirse al cambio de tamaño de cristalito y estructura de fase de las muestras [36]. El máximo de absorción se desplazó hacia longitudes de onda más altas para las muestras que tienen más porcentaje de fase de rutilo. La energía de la banda prohibida (eV) se calculó para las muestras calcinadas determinando la relación entre hν y (αhν) [2] [Archivo adicional 1:Figura S1]. Los datos revelaron que la energía de la banda prohibida para TiO 2 -sul (3.12 eV) es más alto en comparación con TiO 2 -ace (2,99 eV) y TiO 2 -nit (2,97 eV). La banda prohibida de TiO 2 disminuyó cuando la fase de rutilo está dominada en la muestra. Se informó que la banda de valencia (VB) de las fases de anatasa y rutilo se debe principalmente a O 2p estados; por otro lado, la banda de conducción (CB) está compuesta de Ti 3d estados [37]. La energía de banda prohibida de TiO 2 se establece por las posiciones CB y VB, que está influenciada principalmente por la composición de fase. Por lo tanto, la energía de la banda prohibida de la muestra que contenía las fases de anatasa y rutilo debe estar entre los valores de anatasa pura y rutilo.
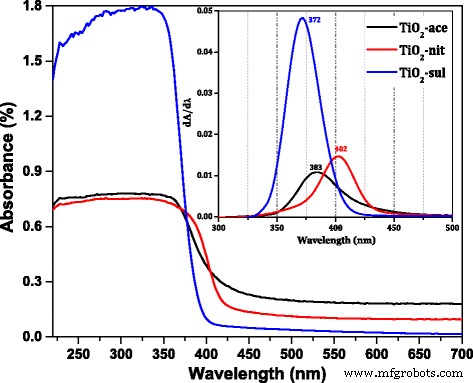
DR UV- vis espectros del TiO 2 calcinado muestras (recuadro; el derivado de DR UV- vis espectros)
N 2 -Medidas de fisisorción
Las isotermas de adsorción-desorción de nitrógeno para las tres muestras sintetizadas se presentan en la Fig. 5a. Se observaron isotermas de tipo IV con bucle de histéresis de tipo H2 para las muestras sintetizadas por peptización con ácido acético (TiO 2 -ace) y ácido sulfúrico (TiO 2 -sul). Esto indica que estas dos muestras poseen mesoporos resultantes de los agregados de TiO 2 nanopartículas. Sin embargo, se observó una isoterma de tipo IV típica con bucle de histéresis de tipo H3 estrecho (característica de poros abiertos y / o en forma de hendidura) para TiO 2 -muestra de liendres. También se puede observar que el circuito de histéresis se cerró a alta presión relativa ( P / P 0 = 1) y esta observación indica la presencia de poros de gran tamaño [38].
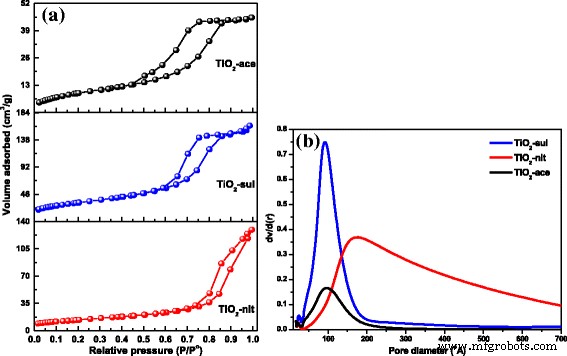
un N 2 isotermas de adsorción-desorción. b Distribución del tamaño de los poros para el TiO 2 calcinado samples (reimpreso con permiso de [29]. Copyright @ 2017 Elsevier)
Las distribuciones de tamaño de poro del modelo BJH para los materiales sintetizados se obtuvieron a partir de los valores de la rama de adsorción de las isotermas. Las distribuciones de tamaño de poro de BJH de las muestras se muestran en la Fig. 5b. Se observaron distribuciones estrechas de tamaño de poro monomodal para TiO 2 -ace y TiO 2 -muestras de sul. Sin embargo, se observó una distribución más amplia del diámetro de los poros para la muestra preparada con ácido nítrico, probablemente debido a que existían espacios vacíos entre las partículas más grandes. Las propiedades de textura de las muestras se presentan en la Tabla 1. Los resultados mostraron que un área de superficie alta (115 m 2 g −1 ) se observó para el TiO 2 -muestra de acelga calcinada a 500 ° C. La orden de S APUESTA el cambio fue TiO 2 -ace> TiO 2 -sul> TiO 2 -liendre. Los resultados observados indican claramente que las condiciones de peptización adaptadas fueron muy efectivas en la generación de nanopartículas con textura porosa.
Espectroscopia infrarroja por transformada de Fourier
La actividad fotocatalítica de TiO 2 depende de la cristalinidad, el tamaño del cristalito, la composición, la tasa de recombinación de los huecos de electrones, el área de la superficie y también la densidad de los grupos hidroxilo de la superficie [39]. Se utilizaron técnicas espectroscópicas FTIR y XPS para investigar la naturaleza de los grupos –OH presentados en el TiO 2 calcinado muestras. La Figura 6 muestra los espectros FTIR para los tres TiO 2 muestras en el rango de 1600 a 4000 cm −1 . Se informa que TiO 2 el soporte podría poseer diferentes tipos de grupos hidroxilo superficiales; se pueden clasificar como Ti-OH aislado, grupos hidroxilo unidos entre sí mediante enlaces de hidrógeno y H 2 químicamente unido O moléculas [40].
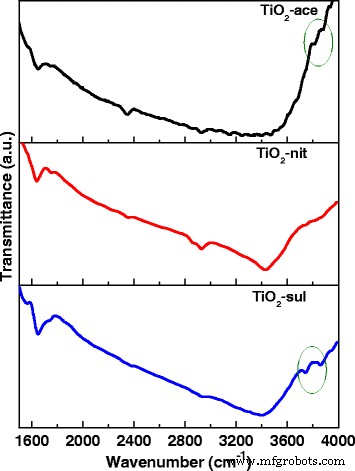
Espectros FTIR del TiO 2 calcinado muestras
Las tres muestras mostraron una banda ancha centrada en 3408 cm −1 , que se atribuye a la vibración de estiramiento de los grupos O-H (moléculas de agua y los grupos OH de la superficie libre). También aparecieron bandas adicionales a 2340 y 1640 cm −1 , que podría asignarse a la vibración de estiramiento O-H y H 2 adsorbido molecularmente O, respectivamente [41]. La existencia de dos vibraciones de estiramiento –OH en caso de anatasa (a 3715 y 3675 cm −1 ) y una banda débil a 3680 cm −1 con rutilo se informó anteriormente [42]. Se puede ver un resultado muy similar en el caso de TiO 2 sintetizado muestras.
Espectroscopia de fotoelectrones de rayos X
La Figura 7 muestra Ti 2p deconvolucionado y O 1s Espectros XP para TiO 2 sintetizado muestras. Las tres muestras mostraron dos picos principales a 457,2 y 463,1 eV correspondientes a 2p 3/2 y 2p 1/2 de Ti 4+ en TiO 2 [43]. Se observaron valores de energía de enlace muy similares en Ti 2p región para los tres TiO 2 muestras que indican que los átomos de Ti en estas muestras existían en el mismo estado de oxidación. También se observaron dos pequeños picos de hombro a 455,8 y 458,7 eV para todas las muestras. El hombro a 455,8 eV podría asignarse a un Ti 3+ estado, debido a una deficiencia de oxígeno en TiO 2 [44], mientras que el otro pico del hombro a 458,7 eV surge de un Ti 4+ estado de la especie Ti-OH [45]. Se desprende claramente del Ti 2p espectros que la contribución de TiO 2 deficiente en oxígeno especie es mayor en TiO 2 -nit que TiO 2 -sul y TiO 2 -muestras de rostros. Todas las muestras mostraron O 1 XP alcanza un máximo de 528,4, 529,3 y 531,3 eV. El pico de XPS a 528,4 eV se puede atribuir a O-Ti 4+ especies en el TiO 2 red cristalina, mientras que otros dos picos a 529,3 y 531,3 eV pueden asignarse a especies de oxígeno presentes en grupos hidroxilo adsorbidos en la superficie [46].
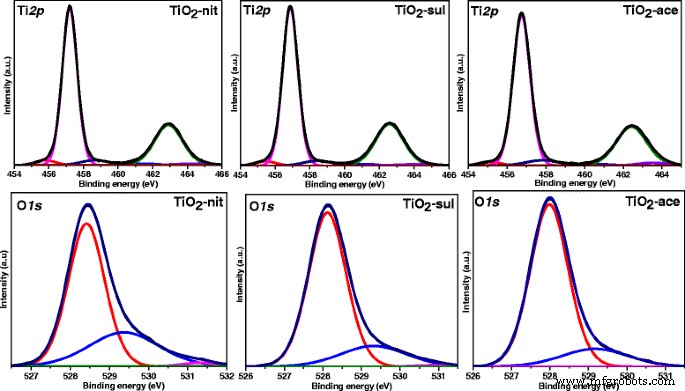
Ti 2p y O 1s Espectros de fotoelectrones de rayos X para el TiO 2 calcinado muestras
McCafferty [47] también observó que los O 1 pico poseía un pico de cola en los valores altos de energía de enlace, lo que podría deberse a la presencia de grupos Ti-OH. Debido a la superficie adsorbida físicamente, los grupos Ti-OH pueden eliminarse fácilmente bajo el vacío ultra alto utilizado para operar el instrumento XPS [48]. Estos grupos –OH presentados en las muestras deben ser debidos al Ti-OH que están químicamente unidos a los defectos superficiales del TiO 2, donde los porcentajes de grupos –OH en especies de oxígeno totales para TiO 2 -nit muestra es ligeramente superior a la de TiO 2 -sul y TiO 2 -ace (Tabla 2).
Degradación fotocatalítica de cristal violeta, azul de metileno y Para -Colorantes de nitro fenol
La actividad fotocatalítica del TiO 2 calcinado nanopartículas para la degradación de CV, MB y p -Se estimó NP. Se informa que la reacción de degradación fotocatalítica generalmente sigue la cinética de Langmuir-Hinshelwood [1]. Por lo tanto, la degradación fotocatalítica de colorantes orgánicos se puede expresar como
$$ - \ mathrm {dc} / \ mathrm {dt} =\ mathrm {kC} $$ (5)y después de la integración, Eq. (4) se puede derivar
$$ C ={C} _0 {\ exp} ^ {\ left (- \ mathrm {kt} \ right)} $$ (6)donde C 0 es la concentración inicial (ppm) de los tintes orgánicos y k es la constante de velocidad, que depende del tiempo de reacción, la temperatura y el pH de la solución. Normalmente, la eficacia fotocatalítica del catalizador aumenta con el tiempo en funcionamiento.
Se realizaron experimentos en blanco para confirmar la importancia del fotocatalizador y la irradiación UV. No se produjo reacción cuando se aplicaron el catalizador y la irradiación UV solos. Se observaron resultados similares en nuestros hallazgos anteriores [49]. Como se notificó en la sección experimental, el TiO 2 Los fotocatalizadores se equilibraron con la solución de colorante orgánico durante 45 minutos para determinar la adsorción de colorantes orgánicos en TiO 2 sintetizado. muestras. El UV- vis espectros de absorción de CV, MB y p -NP se registraron después del equilibrado del fotocatalizador. Archivo adicional 1:Las figuras S2, S3 y S4 muestran la variación en el UV- vis espectros de absorbancia de CV, MB y p -Soluciones de NP (10 ppm) con diferentes tiempos de reacción sobre TiO 2 -ace, TiO 2 -sul y TiO 2 -muestras de liendres, respectivamente. La intensidad de los picos de absorción que corresponde al CV, MB y p -NP disminuyó con el aumento del tiempo de reacción. El UV- vis Los espectros de los productos de reacción indican que los tintes orgánicos se degradaron durante la fotorreacción. El TiO 2 -nit muestra que es el fotocatalizador más eficaz en comparación con TiO 2 -sul y TiO 2 -muestras de rostros. Degradación del 50% de p -NP se observó en 60 minutos para el TiO 2 -nit muestra, mientras que se necesitaron 75 y 100 min para la degradación del 50% p -NP para TiO 2 -ace y TiO 2 -muestras de sul en condiciones similares. Se observaron patrones de actividad fotocatalítica similares para la degradación de tintes MB y CV.
The percentage degradation efficiency of the investigated catalysts was calculated using Eq. (4). Figure 8 shows the percentage changes of CV, MB, and p -NP aqueous solution at room temperature in the presence of calcined TiO2 muestras. After just 10 min of the reaction, the TiO2 -nit sample showed 29% CV degradation efficiency, while TiO2 -ace and TiO2 -sul samples showed only 17 and 9%, respectively. The photocatalytic activity steeply increased with the increase of reaction time over the three samples. However, after 120 min, TiO2 -nit and TiO2 -ace samples showed 99% efficiency; however, TiO2 -sul sample showed only 65% efficiency.
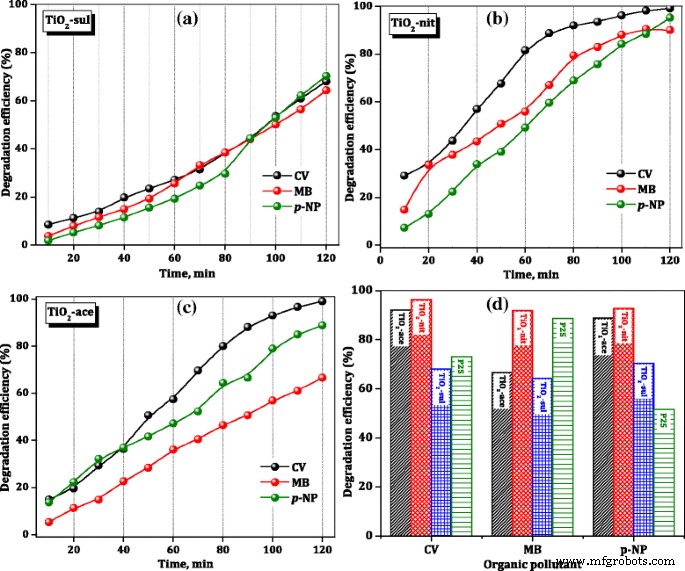
Photocatalytic degradation efficiency of TiO2 catalysts
To compare the photocatalytic performance of synthesized TiO2 samples, the degradation efficiency of the commercial P25 sample for organic dyes after 120 min is included in Fig. 8d. It is clear that TiO2 -nit sample showed better performance than the P25 sample in the degradation of three organic dyes; however, TiO2 -ace and TiO2 -sul samples showed lower activity than the P25 catalyst in case of p -NP degradation. These results are suggesting that the performance of catalysts is influenced by the physicochemical characteristics of the TiO2 samples and nature of the organic dye.
The rate constants for photocatalytic degradation of CV, MB, and p -NP over synthesized TiO2 samples and commercial P25 sample were determined from the slope of the straight line which is plotted between ln(C 0 /C t ) and t , and the results are presented in Table 3. The observed results are indicating that the photocatalytic activity of the degradation of organic dyes was greatly influenced by the composition of TiO2 sample and amount of the surface hydroxyl groups. The activity indeed is not influenced by the particle size, crystallinity, and surface area of TiO2 synthesized in this work. This observation is not consistent with the results observed by Fujishima et al. [8] that the catalyst which possesses lower particle size offered high photocatalytic efficiency.
Previously, it was reported that anatase is a better photocatalyst than rutile due to its high band gap energy and a large number of surface OH groups [50]. It was thought that TiO2 -nit sample would offer low photocatalytic activity due to the presence of more rutile phase (67%). However, Masahashi et al. [51] claimed that rutile exhibited higher performance than anatase MB degradation due to its superior crystalline nature.
Determination of photocurrent values was carried out to obtain a better insight responsible factor for the superior photocatalytic performance of the samples containing more rutile. It was reported that photocatalytic activity is directly related to the electron-hole separation efficiency of a catalyst which is influenced by the photocurrent density [52]. Theoretical photocurrent density of the TiO2 samples was calculated from the absorption edge of the TiO2 samples (obtained from DR UV-vis spectroscopy measurements) and theoretical equations (supporting information) presented in the literature [53]. The results of photocurrent of TiO2 samples are presented in Table 4 along with the percentage of rutile and photocatalytic efficiency values. The photocurrent density of TiO2 -nit (0.545 mA/cm 2 ) is higher than other two synthesized TiO2 samples and also commercial P25 sample (0.401 mA/cm 2 ), manifesting the beneficial role of rutile phase in improving the photoactivity of TiO2 samples.
Previously, Melcher et al. [54] reported that photocatalytic capability of the commercial P25 material originates due to the presence of a mixture of rutile and anatase phases in the sample (75% anatase and 25% rutile). Hirakawa et al. [55] indicated that pure rutile itself is not a powerful photocatalyst, and it is also reported that the light with a wavelength of 380 nm is not powerful enough to generate charge carriers in the pure anatase [56]. Based on XPS spectroscopy results and theoretical calculations, Scanlon et al. [57] concluded that electrons were moved from rutile to anatase and the holes were transported from anatase to rutile, which inhibited the electron-hole recombination. Yu et al. [58] reported a similar observation that TiO2 sample with mixed phases was beneficial to decrease the rate of h + -e − recombination and thus enhance the photocatalytic efficiency of the catalyst.
In literature reports, two possible transfer mechanisms have been proposed for anatase-rutile composite samples [59]. The first mechanism is the interfacial electron transfer from CB of anatase to that of the rutile [60], and the second one is an electron transfer from CB of rutile to lower energy anatase active sites [61]. It is known that the anatase CB possesses higher negative potential than the rutile CB due to the fact that anatase has a higher band gap (3.12 eV) than rutile. Therefore, it is not possible for an electron to move from the rutile CB to the anatase CB because it would have to overcome the energetic barrier between the two bands. The band gap of anatase VB is also slightly higher, than the rutile VB, so the generated holes could be moved to the anatase VB, to achieve an effective charge separation. Most probably, the electron-hole pair is formed in the composite of rutile and anatase in case of TiO2 -nit and TiO2 -sul samples (Fig. 9), and this rate is much higher in TiO2 -nit sample due to predominant rutile formation.
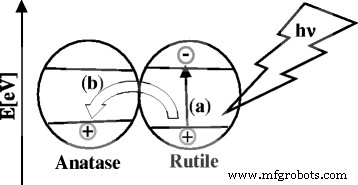
Plausible model of a generation of electron-hole pairs and b effective charge carrier separation via transfer of the generated holes into the anatase valence band
It was reported that increase of crystal growth of initial phase is possible by increasing the mobility of ions presented in precursor solution [62]. Several researchers added small volumes of mineral acids (such as hydrochloric acid and sulfuric acid) to improve the mobility of dissociated ions [63]. Their role is not only to increase the rate of diffusion of ions in a solution but also to alter the surface charge. Under humidity conditions, titanium isopropoxide can subsequently undergo hydroxylation and polymerization to TiO2 .
$$ \mathrm{Ti}{\left(\mathrm{OPri}\right)}_4+4{\mathrm{H}}_2\mathrm{O}\to \mathrm{Ti}{\left(\mathrm{OH}\right)}_4+4\ \mathrm{PriOH}\kern2.5em \left(\mathrm{hydroxylation}\right) $$ (7) $$ \mathrm{Ti}{\left(\mathrm{OH}\right)}_{4\kern0.5em }\to {\mathrm{TiO}}_{2.}x{\mathrm{H}}_2\mathrm{O}+\left(2\hbox{-} x\right)\ {\mathrm{H}}_2\mathrm{O}\kern5em \left(\mathrm{condensation}\right) $$ (8)Depending on the nature of peptizing acid, the transformation of TiO2 leads to anatase or rutile phase [64]. Formation of amorphous TiO2 or metastable anatase phase was observed when the condensation initiated before hydrolysis of Ti precursor. Under highly acidic conditions, the rutile phase formation is favorable as the rate of condensation is slow. Accordingly, the rutile phase was obtained when sulfuric and nitric acids were used for the peptization. The use of weak acid (acetic acid) as a peptizing agent allows the control of both the degree of condensation and oligomerization and persuades the preferential crystallization of TiO2 in the anatase phase. Zeng et al. [20] used polycarboxylic acid as a peptizing agent and observed the formation of nanoparticles of anatase which they attributed to chelation effect of organic acid.
It is known that TiO6 octahedra are a fundamental structural unit for both anatase and rutile phases (D 4h system), and the only difference between these two structures is the assembly of the octahedral chains [65]. Face-shared linking of TiO6 units results in anatase structure, while edge-shared linking results in rutile structure [66]. It is clear that NO 3− anions possessed weaker affinity to Ti atoms in an aqueous solution than CH3 COO − and SO4 2− anions. The strong affinity of CH3 COO − and SO4 2− anions with Ti atoms is responsible for the inhibition of the phase transformation.
In the previously reported studies, many of the photocatalysts have not been tested for reuse mainly due to undergo photocorrosion; hence, their photostability is reduced for further usage. The reusability of the calcined TiO2 samples was examined to study the effectiveness of these photocatalysts. It was observed that the used photocatalyst offered 90% efficiency for three consecutive cycles. The efficiency of the catalyst was reduced to 80 and 75% during fourth and fifth cycle, respectively. The decrease is due to the loss of some amount of catalyst during the filtration and regeneration procedures.
Conclusions
A simple peptization method was adapted to synthesize TiO2 nanoparticles by using sulfuric, nitric, and acetic acid as peptizing agents and titanium isopropoxide as Ti precursor. The influence of acid species on the crystal phase, morphology, textural, and surface composition of TiO2 were studied in detail. El TiO 2 sample peptized with acetic acid possessed pure anatase phase, while the formation of minor (5%) and major (67%) of rutile phase was observed in case of samples peptized with sulfuric acid and nitric acid, respectively. It is observed that TiO2 peptized with nitric acid showed sheet-like structures along with nanoparticles, while TiO2 samples peptized with sulfuric and acetic acids possessed near spherical nanoparticles. The photocatalytic properties of synthesized TiO2 nanostructures were evaluated for photodegradation of aqueous CV, MB, and p -NP solutions. El TiO 2 peptized using nitric acid showed the best photocatalytic activity than commercial P25 and other two peptized samples, and its photodegradation efficiency was reached to 95% in 120 min for p -NP degradation. Although TiO2 samples peptized using sulfuric acid and acetic acid possessed smaller particle size, higher band gap energy, and high surface area, TiO2 sample peptized with nitric acid possessed a higher percentage of rutile and photocurrent density. The observed photocurrent density is dominated by the photoactivity of TiO2 . The results indicate a direct correlation between the photocatalytic activity and the photocurrent density of the TiO2 muestras. The superior activity of TiO2 sample peptized with nitric acid is due to the effective transfer of photogenerated electrons between rutile and anatase phases, and large pore diameter could have enhanced the diffusion and mass transportation of reacting molecules and OH radicals during the photochemical reaction. The synthesized TiO2 photocatalysts can be recycled with a minor change in the activity.
Abreviaturas
- CV:
-
Crystal violet
- DR UV-vis :
-
Diffuse-reflectance ultraviolet-visible spectroscopy
- FTIR:
-
Espectroscopía infrarroja por transformada de Fourier
- HRTEM:
-
High-resolution transmission electron microscopy
- MB:
-
Methylene blue
- NMR:
-
Nuclear magnetic resonance
- p –NP:
-
para –nitro phenol
- TEM:
-
Microscopía electrónica de transmisión
- TiO2 :
-
Titanium oxide
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
X-ray powder diffraction
Nanomateriales
- Ruta de electrohilado de un paso de nanofibras de TiO2 de rutilo modificadas con SrTiO3 y sus propiedades fotocatalíticas
- Alto rendimiento fotocatalítico de dos tipos de fotocatalizadores compuestos de TiO2 modificado con grafeno
- Nanopartículas como bomba de eflujo e inhibidor de biopelícula para rejuvenecer el efecto bactericida de los antibióticos convencionales
- Hacia los nanofluidos de TiO2:Parte 2:Aplicaciones y desafíos
- Efecto de la distribución de nanopartículas de oro en TiO2 sobre las características ópticas y eléctricas de las células solares sensibilizadas por colorante
- Los efectos de la relación Li / Nb en la preparación y el rendimiento fotocatalítico de los compuestos Li-Nb-O
- Actividades fotocatalíticas mejoradas por nanopartículas au-plasmónicas en un fotoelectrodo de nanotubos de TiO2 recubierto con MoO3
- Preparación y rendimiento fotocatalítico de fotocatalizadores LiNb3O8 de estructura hueca
- Propiedades ópticas del infrarrojo cercano visible y estructural del TiO2 dopado con Cr para pigmentos fríos coloreados
- Matrices de nanotubos de TiO2:fabricadas con una plantilla blanda-dura y la dependencia del tamaño de grano del rendimiento de las emisiones de campo
- Determinación de la actividad catalítica de nanopartículas de TiO2 dopado con metal de transición mediante análisis espectroscópico de superficie



