Comparación entre el ácido fólico y la funcionalización basada en péptidos gH625 de nanopartículas magnéticas de Fe3O4 para una internalización celular mejorada
Resumen
Una ruta sintética versátil basada en Fe 3 magnético O 4 Se ha utilizado la prefuncionalización de nanopartículas (MNP) con una monocapa de ácido fosfónico para unir covalentemente el péptido gH625 en la superficie de las nanopartículas. El gH625 es un péptido membranotrópico capaz de atravesar fácilmente las membranas de varias células, incluidos los componentes típicos de la barrera hematoencefálica humana. Se utilizó una ruta sintética similar para preparar otra clase de MNP que tienen un recubrimiento funcional basado en PEG, rodamina y ácido fólico, una molécula diana bien conocida, para comparar el rendimiento de los dos sistemas de penetración celular (es decir, gH625 y fólico ácido). Nuestros resultados demuestran que la captación de MNP decoradas con gH625 en células endoteliales microvasculares del cerebro humano inmortalizadas después de 24 h es más evidente en comparación con las MNP funcionalizadas con ácido fólico, como lo demuestra la microscopía de barrido láser confocal. Por otro lado, ambos sistemas funcionalizados demostraron ser capaces de internalizarse en una línea celular de tumor cerebral (es decir, glioblastoma A-172). Estos hallazgos indican que la funcionalización de las MNP con gH625 mejora su internalización de células endoteliales, lo que sugiere una estrategia viable en el diseño de nanoestructuras funcionales capaces de cruzar primero la BBB y, luego, de llegar a células cerebrales tumorales específicas.
Antecedentes
La barrera hematoencefálica (BBB) es una interfaz dinámica entre la sangre y el cerebro que desempeña un papel crucial en el mantenimiento de la homeostasis del sistema nervioso central (SNC). Los componentes principales de la BHE son las células endoteliales (es decir, astrocitos y pericitos), que forman una lámina continua que cubre la superficie interna de los microvasos del cerebro. Están interconectados por uniones estrechas, que son críticas tanto para el control de la permeabilidad vascular de la BHE [1] como para la protección del cerebro de diversas toxinas circulantes y otras moléculas dañinas [2, 3]. Las neuronas y la microglía, que son otros componentes de la unidad neurovascular, desempeñan un papel diferente en la BHE [4, 5].
Debido a la lámina continua de células endoteliales, el 98% de los fármacos de molécula pequeña y el 100% de los fármacos de molécula grande no atraviesan la BHE, por lo que no logran administrar los fármacos al tejido cerebral [6]. Por lo tanto, para desarrollar sistemas de administración eficientes para el tratamiento de muchas enfermedades cerebrales, es crucial investigar la capacidad de los portadores de atravesar la BBB [7].
En la última década, los sistemas basados en nanopartículas se han estudiado ampliamente como agentes terapéuticos eficaces para la terapia y el tratamiento del cáncer. En este contexto, las nanopartículas de hierro magnéticas funcionalizadas orgánicas (MNP) han atraído mucho interés ya que combinan la versatilidad de la funcionalización de la superficie con las propiedades magnéticas y la naturaleza biocompatible no tóxica de su núcleo. Las MNP se adoptan ampliamente para aplicaciones teranósticas (diagnósticas y terapéuticas) como la clasificación y manipulación de proteínas y células [8, 9], el etiquetado celular [10, 11], la administración de fármacos controlada magnéticamente [12, 13], la resonancia magnética (MRI) [14, 15] e hipertermia [16,17,18,19]. Para que se utilicen de forma eficaz en aplicaciones biomédicas, las MNP deben poder atravesar las membranas celulares y, en particular, las diversas barreras biológicas. La modificación de la superficie de las MNP con moléculas funcionales se ha utilizado a menudo para mejorar su internalización celular, pero en muchos casos, el cruce de la BBB sigue siendo un problema.
En este contexto, se puede observar el uso de péptidos penetrantes en las células (CPP), un grupo de péptidos relativamente cortos (5-40 aminoácidos) que se derivan de fuentes naturales o de construcciones diseñadas sintéticamente, que pueden atravesar fácilmente la bicapa de la membrana. como un enfoque prometedor. Entre los numerosos CPP disponibles, el péptido de 20 residuos gH625, derivado de la glicoproteína H (gH) del virus Herpes simplex 1, se ha desarrollado recientemente y se ha utilizado para cruzar la BBB para mejorar la absorción de una variedad de cargas [20, 21] en el citosol.
En el presente estudio, las MNP se han funcionalizado con dos clases diferentes de recubrimientos dirigidos basados en una capa de acoplamiento de ácido 3-aminopropilfosfónico (NH 2 -PENSILVANIA). Los dos recubrimientos se obtuvieron conectándolos al NH 2 -MNP modificados por PA (NH 2 @MNPs) ya sea el péptido penetrante celular gH625 (gH625 @ MNPs) o moléculas de PEG y ácido fólico (PEG, FA @ MNPs). En particular, la introducción de ácido fólico (FA) en las nanopartículas PEGiladas tiene como objetivo mejorar tanto la captación celular en las células tumorales a través de la internalización mediada por el receptor FA [22] como la biocompatibilidad del nanosistema general [23]. Los efectos de los dos revestimientos superficiales sobre la captación intracelular de MNP en las células endoteliales microvasculares primarias del cerebro humano (HBMEC) se han evaluado mediante microscopía de barrido láser confocal. Para ello, se incorporaron sondas luminiscentes en ambos sistemas. En particular, gH625 se marcó con la sonda 4-cloro-7-nitrobenz-2-oxa-1,3-diazol (NBD), mientras que un carboxi- X -Se agregó sonda de rodamina (rhod) al caparazón de PEG, FA @ MNPs.
El estudio de la captación intracelular de las MNP modificadas con gH625 en las células endoteliales y su comparación con las MNP modificadas con FA, hasta donde sabemos, nunca se ha informado antes.
Además de la capacidad de cruzar la BHE, dirigirse a las células de los tumores cerebrales es otro requisito importante para los agentes terapéuticos para los tumores cerebrales. Por lo tanto, también se evaluó la internalización celular de los dos MNP con recubrimiento diferente en uno de los gliomas malignos humanos más comunes, el glioblastoma A-172.
Nótese que aunque Perillo et al. Han preparado recientemente nanopartículas de hierro funcionalizadas con gH625. [24], en el presente trabajo, reportamos una estrategia sintética diferente basada en una plataforma de ácido fosfónico altamente versátil. En particular, la química del ácido fosfónico permite la formación de enlaces fuertes entre las MNP y las monocapas fosfónicas cuya estabilidad es comparable a la de las MNP silanizadas. Además, dado que la autocondensación de P-O-P es insignificante, el uso de enlazadores fosfónicos supera los inconvenientes de formación de oligómeros que se encuentran a menudo cuando se usan silanos [25].
Métodos
Materiales
Todos los reactivos utilizados para la síntesis y funcionalización de MNP, FeCl 2 · 4H 2 O, FeCl 3 · 6H 2 Ácido O, 3-aminopropilfosfónico, ácido metoxipolietilenglicol acético N -succinimidil éster (PEG-NHS) con peso molecular 5000 Da, ácido fólico, N -hidroxisuccinimida (NHS) y carboxi- X -rodamina N -succinimidil éster (Rhod-NHS) se adquirieron de Sigma-Aldrich y se usaron sin purificación adicional. Los aminoácidos protegidos con 9-fluorenilmetoxicarbonilo (Fmoc) usados para la síntesis de péptidos fueron adquiridos por Romil Del Chimica, Chemicals, y se usaron sin purificación adicional. El agua era de grado Milli-Q (18,2 MO cm) y se filtró a través de un filtro de 0,22 μm.
Síntesis de MNP
Los MNP de óxido de hierro desnudo se sintetizaron mediante la coprecipitación alcalina de Fe 3+ y Fe 2+ , según el protocolo descrito en la literatura [26]. Brevemente, FeCl 2 · 4H 2 O y FeCl 3 · 6H 2 Se disolvieron O (relación molar 1:2) en agua (50 ml) bajo una N 2 atmósfera con agitación vigorosa. NH 3 25% en H 2 Se añadió O (5 ml) a la solución a 80ºC y se continuó la reacción durante 30 min. La suspensión resultante se enfrió a temperatura ambiente y se lavó con agua ultrapura. Las nanopartículas magnéticas desnudas obtenidas (MNP desnudas) se aislaron del disolvente mediante decantación magnética.
Síntesis de gH625
El péptido se preparó como se informó anteriormente [27] adoptando el método estándar de fase sólida 9-fluorenilmetoxicarbonilo (Fmoc). Brevemente, se sintetizaron 50 µmol del péptido en una resina de Wang (0,75 mmol / g) mediante ciclos consecutivos de desprotección y acoplamiento. El péptido unido a resina se hizo reaccionar luego con 4-cloro-7-nitrobenzofurazan (NBD-Cl); la reacción se llevó a cabo durante la noche en presencia de DIPEA. El péptido se escindió de la resina y se desprotegió mediante tratamiento con una mezcla de ácido trifluoroacético (TFA) y depuradores y después se precipitó en éter etílico enfriado con hielo. El péptido se disolvió en agua y se liofilizó. La caracterización del péptido bruto se realizó mediante LC-MS de ionización por electropulverización (ESI) adoptando un gradiente lineal de acetonitrilo (TFA al 0,1%) en agua (TFA al 0,1%) del 20 al 80% en 15 min. Luego se purificó mediante cromatografía líquida de alta resolución de fase inversa preparativa (RP-HPLC).
Síntesis de N -Ester de ácido fólico de hidroxisuccinimida (FA-NHS)
FA-NHS se preparó mediante el siguiente método publicado [28]. Se disolvieron quinientos miligramos de ácido fólico (FA) en 10 ml de dimetilsulfóxido (DMSO) con 240 ml de trietilamina. NHS (260 mg) y N , N Se añadieron -diciclohexilcarbodiimida (470 mg) y la mezcla se hizo reaccionar durante la noche a temperatura ambiente en la oscuridad. El subproducto, diciclohexilurea, se eliminó por filtración. Después, la solución de DMSO se concentró a presión reducida y se precipitó FA-NHS en éter dietílico. El producto se lavó varias veces con éter anhidro y se secó al aire.
Síntesis de MNP funcionalizadas
Síntesis de NH 2 @MNPs
Se dispersaron MNP (200 mg) en H 2 O (25 ml) utilizando un baño de ultrasonidos durante 30 min. NH 2 Se añadió -PA (100 mg) y la suspensión se agitó durante 2 ha temperatura ambiente. Las partículas se separaron magnéticamente y se lavaron cuatro veces con H 2 O y luego con etanol y se seca al aire.
Síntesis de gH625 @ MNPs
NH 2 Se dispersaron @MNP (300 mg) y gH625 (1,2 mg) en DMSO (20 ml). La solución se mezcló durante la noche a 25 ° C. Las partículas obtenidas se separaron magnéticamente; lavado con DMSO, H 2 O y etanol; y se seca al aire.
Síntesis de PEG, FA @ MNPs
NH 2 @MNPs (300 mg), PEG-NHS (30 mg), FA-NHS (3 mg) y Rhod-NHS (3 mg) se dispersaron en DMSO (15 ml) y la solución se mezcló durante la noche a 25 ° C. . Las partículas obtenidas se separaron magnéticamente; lavado con DMSO, H 2 O y etanol; y se seca al aire.
Caracterizaciones de muestra
Las mediciones de difracción de rayos X en polvo (XRD) se realizaron con un θ - θ 5005 Difractómetro Bruker-AXS (Zeiss, Oberkochen, Alemania) que usa radiación Cu Kα operando a 40 kV y 30 mA. La espectroscopia de fotoelectrones de rayos X (XPS) se realizó con un espectrómetro ESCA-Auger de múltiples técnicas PHI 5600 con una fuente de rayos X estándar de Al-Kα. Los análisis se llevaron a cabo con un ángulo de fotoelectrón de 45 ° (con respecto a la superficie de la muestra) con un ángulo de aceptación de ± 7 °. La escala de energía de enlace XPS (B.E.) se calibró centrando el pico C 1s debido a las fracciones de hidrocarburos y el carbono adventicio en 285,0 eV. Las mediciones de UV / Vis se llevaron a cabo con un espectrofotómetro JASCO V-560 UV / Vis y los espectros se registraron con una resolución de ± 0,2 nm. La dispersión de luz dinámica (DLS) y las mediciones de potencial zeta de las MNP se realizaron a 25 ° C con un Zetasizer Nano-ZS (Malvern Instruments, Malvern, Reino Unido) equipado con láser He-Ne (633 nm) y un detector de retrodispersión (173 ° C). ). Las mediciones de transmisión FT-IR se registraron con un espectrómetro JASCO FTIR 430, utilizando la técnica de pellets KBr, con 100 escaneos recolectados por espectro (rango de escaneo 560–4000 cm - 1 , resolución 4 cm - 1 ).
Cultivo celular
Las células endoteliales microvasculares del cerebro humano (HBMEC) y la línea celular de glioblastoma humano A-172 se cultivaron hasta la confluencia en matraces de cultivo de tejidos recubiertos con colágeno tipo I de cola de rata, de acuerdo con el método informado [29]. Brevemente, se cultivaron HBMEC en el medio de células endoteliales suplementado con suero bovino fetal (FBS) al 5% y suplemento de crecimiento de células endoteliales al 1%. La línea celular A-172 se cultivó en DMEM que contenía glutamina 2 mM y FBS al 10% como se describió anteriormente [30]. En ambos casos, también se agregaron a los cultivos 100 U / ml de penicilina y 100 μg / ml de estreptomicina.
Ensayo de viabilidad celular
La viabilidad celular se determinó con [3- (4,5-dimetil-2-tiazolil) -2,5-difenil-2 H Prueba de bromuro de tetrazolio] (MTT) [31]. En todas las condiciones experimentales, la concentración de FBS se redujo al 1% (medio de hambre). Las células se sembraron en placas de 96 pocillos a 7000 células / pocillo para obtener una densidad celular óptima durante todo el experimento. En todos los ensayos, las células se incubaron primero a 37 ° C con MTT durante 3 h; luego, se añadió isopropanol con HCl 0,04 M y se midió la absorbancia a 1 h en un lector de placas (Synergy 2-BioTek) con una longitud de onda de prueba de 570 nm [32].
Microscopía confocal
Se realizó microscopía confocal en células de glioblastoma HBMEC y A-172 cultivadas en cubreobjetos de microscopio colocados en una placa de 24 pocillos. Después de incubaciones con o sin MNP, las células se fijaron mediante la adición de paraformaldehído al 4% en PBS y se procesaron para inmunocitoquímica como se describió anteriormente [33]. Los análisis de microscopía confocal se llevaron a cabo con un microscopio de barrido láser confocal (LSM) Olympus FV1000 equipado con las siguientes fuentes de excitación:láser de diodo (405 nm), láser Ar multilínea (457, 488 y 515 nm), láser HeNe (G) ( 543 nm) y láser HeNe (R) (633 nm). Se utilizó un objetivo de inmersión en aceite (60xO PLAPO) y la luz emitida se detectó en modo secuencial a través de un sistema de filtrado espectral. La ganancia del detector se fijó en un valor constante y se tomaron imágenes de todas las muestras en ubicaciones aleatorias en toda el área del pozo. Se utilizaron los siguientes parámetros de adquisición: λ ex / em =405/425 - 475 nm (canal azul, tinción nuclear por DAPI); λ ex / em =488/500 - 530 nm (canal verde, etiquetado gH625 @ MNPs por NBD); y λ ex / em =633/650 - 700 nm (canal rojo, PEG, etiquetado FA @ MNPs por rhod). El análisis cuantitativo de la fluorescencia se realizó utilizando el software ImageJ (versión 1.50i, NIH).
Resultados y discusión
Síntesis y caracterización de MNP
La estrategia general implementada para preparar gH625 @ MNP y PEG, FA @ MNP a partir de Fe 3 O 4 nanopartículas, obtenidas por coprecipitación, implica dos pasos como se ilustra en la Fig. 1. El primer paso, que es el mismo para ambas clases de nanopartículas, se basa en la funcionalización MNP con un ácido fosfónico que lleva un grupo amino (NH 2 -PENSILVANIA). En el segundo paso, el NH 2 -PA-MNP prefuncionalizados (NH 2 @MNPs) se conjugan además con moléculas funcionales específicas a través de reacciones de acoplamiento NHS. En particular, el N -La forma activada con hidroxisuccinimida de gH625 marcada con NBD se usó para la preparación de gH625 @ MNP, y N Se usaron formas activadas con hidroxisuccinimida de PEG, FA y Rhod para obtener PEG, FA @ MNP. Tenga en cuenta que tanto gH625 @ MNP como PEG, FA @ MNP se han marcado con sondas luminiscentes (es decir, NBD y Rhod, respectivamente) para llevar a cabo estudios de microscopía de barrido láser confocal.
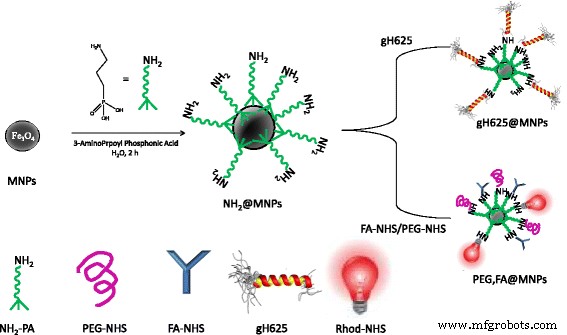
Esquema de reacción. Pasos de reacción para la preparación de MNP funcionalizadas
La caracterización difractométrica de rayos X (XRD) de las MNP desnudas obtenidas después del paso de coprecipitación es similar a la informada en nuestros artículos anteriores [34, 35]. Brevemente, un patrón típico (Fig. 2a) muestra cuatro picos de difracción (2 θ =30,16 °, 35,48 °, 43,10 ° y 57,04 °) que es consistente con la presencia de magnetita, maghemita o cualquier composición intermedia entre las dos fases. La constante de celosía, a , que resultó ser 8.389 (4) Å en buen acuerdo con el parámetro de red de magnetita en masa (8.396 Å), así como el tamaño de cristal promedio de 11.2, determinado aplicando la ecuación de Debye-Scherrer, son comparables con los valores previamente informó [34, 35].
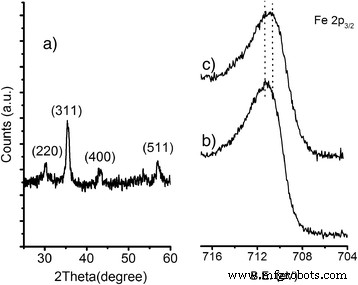
Espectros típicos de XRD y XPS de MNP. Patrón XRD de a) MNP desnudos y Fe 2p 3/2 de alta resolución Regiones espectrales XPS de b) MNP desnudas yc) NH 2 @MNPs
Tenga en cuenta que, dado que la estructura cristalina de Fe 3 O 4 La magnetita es muy similar a la de γ-Fe 2 O 3 maghemita, es muy difícil distinguir las dos fases por XRD. Por esta razón, se utilizó espectroscopia de fotoelectrones de rayos X (XPS) para analizar más a fondo las MNP. La figura 2b muestra Fe 2p 3/2 espectros XPS de alta resolución de MNP desnudos. El centroide de la banda, observado a 710,9 eV, corresponde al Fe 2p 3/2 cima. Este valor es menor que el informado para Fe 3+ ya sea en agujeros octaédricos de α-Fe 2 O 3 (711.6 eV) [36, 37] o en agujeros tetraédricos y octaédricos mixtos de γ-Fe 2 O 3 (711.4 eV), y es consistente con el estado de oxidación mixto de Fe en Fe 3 O 4 [37, 38].
Finalmente, una caracterización magnética detallada de MNP similares se informa en nuestros artículos anteriores [34, 35].
El proceso de funcionalización fue evaluado por FT-IR y XPS. Después de la funcionalización con monocapas fosfónicas, el Fe 2p 3/2 banda (Fig. 2c) no muestra modificaciones relevantes, lo que confirma que el Fe 3 O 4 se conserva la fase. Sin embargo, un ligero cambio (0,4 eV) del Fe 2p 3/2 Se observó centroide hacia una menor energía de unión (B.E), que se asoció al anclaje de la monocapa fosfónica. De hecho, se observaron cambios similares en la adsorción de fosfato de varios óxidos férricos [39] y pueden atribuirse a alguna transferencia de carga desde el adsorbato a los átomos de Fe. El Fe 2p 3/2 La posición de 710.5 eV se mantuvo después de todos los pasos de funcionalización para el anclaje de PEG y FA.
La Figura 3 informa la comparación de las regiones espectrales P2p, N1s y C 1s de NH 2 @MNPs, PEG, FA @ MNPs y gH625 @ MNPs, respectivamente. La posición del pico P2p (133,2 eV) de NH 2 @MNPs se asocia típicamente con la presencia del ácido fosfónico anclado en la superficie de forma bidentada [40,41,42,43]. La posición de la banda P2p en los espectros de gH625 @ MNPs y PEG, FA @ MNPs es la misma que la observada en NH 2 @MNPs, revelando así que las moléculas fosfónicas no se eliminan durante las reacciones de acoplamiento para la inmovilización del péptido y el ácido fólico.
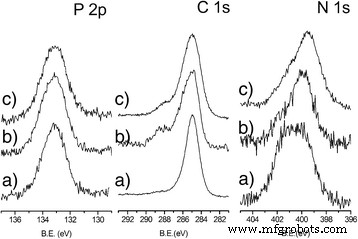
Caracterización XPS de MNP funcionalizadas. Regiones espectrales P 2p, C 1s y N 1s XPS de alta resolución de a) NH 2 @MNPs, b) PEG, FA @ MNPs yc) gH625 @ MNPs
La forma y la posición del pico de los espectros N1 de NH 2 Los @MNP son consistentes con la presencia del NH 2 anclado -PENSILVANIA. La banda consta de dos componentes distintos:el primero a 399,9 eV está asociado con los grupos –NH del aminopropilfosfato anclado, y el segundo componente centrado en 401,5 eV se debe a que los grupos amino interactúan con la superficie de Fe 3 O 4 mediante protonación o formación de enlaces –H.
Después del anclaje del péptido gH625 o FA, PEG y Rhod, el componente N1s a 399,8 eV aumenta en comparación con el componente a 401,8 eV relacionado con restos amino protonados de NH 2 @MNPs. Este incremento se debe a las señales superpuestas de los átomos de N implicados en el enlace amídico (400,2 eV) entre el aminopropilfosfato anclado y las moléculas conjugadas (p. Ej., Gh625, FA, PEG y Rhod), así como de los átomos de N de gh625. y FA (a 399,1 y 400,6 eV).
La banda C 1s de NH 2 El espectro de @MNPs consiste en un solo pico a 285.0 eV asignado a los carbonos alifáticos, como se informó anteriormente [40].
En los espectros C1s de gH625 @ MNPs y PEG, FA @ MNPs, la presencia de un componente C 1s a 288,3 eV se debe a los grupos carboxílico y amídico de las moléculas gh625, FA y Rhod.
Espectros FT-IR de NH 2 @MNPs, gH625 @ MNPs y PEG, FA @ MNPs se informan en la Fig. 4. En todas las muestras, los espectros no muestran las bandas a 1250 cm - 1 debido a P =O y los picos agudos en los 900-1050 cm - 1 rangos debido al estiramiento P – O – H [44,45,46], pero una banda ancha y fuerte a 1040 cm - 1 , que está asociado a las vibraciones del PO 3 2− grupo unido a la superficie de hierro. Esta banda indica, de acuerdo con los resultados de XPS, que los ácidos fosfónicos están desprotonados y anclados a la superficie a través de enlaces P – O – Fe como se informó anteriormente [34, 40, 41]. La región espectral de infrarrojos entre 1500 y 1700 cm - 1 muestra que las bandas pertenecían a los grupos amino y amida de gH625 y FA. En particular, espectro de NH 2 @MNPs muestra un pico agudo alrededor de 1650 cm - 1 asociado al NH 2 flexión [47]. Después del anclaje con PEG, Rhod y FA, 1700-1500 cm - 1 región de PEG, FA @ MNPs muestra bandas más anchas debido a la convolución de las vibraciones del NH 2 sin reaccionar , grupos amida y anillos de benceno de FA y Rhod (1630-1600 cm - 1 ) [35]. De manera análoga, después del anclaje del péptido, las bandas anchas a aproximadamente 1650-1600 cm - 1 puede deberse a la contribución de varias vibraciones debido al NH 2 sin reaccionar y restos amínicos de las cadenas laterales del péptido y del tramo C =O de los enlaces amídicos del péptido [48]. Además, un componente de aproximadamente 1540 cm - 1 debido a la combinación δ Las vibraciones (N – H) / ν (C – N) del péptido [48] también están presentes.
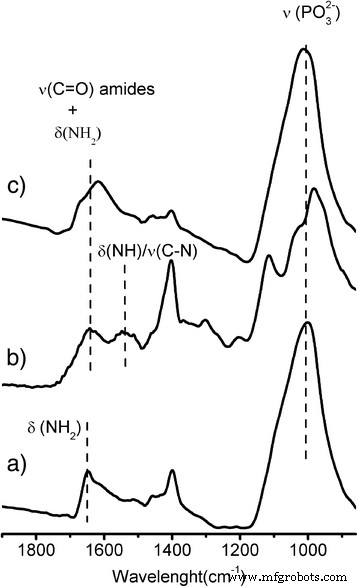
Caracterización FT-IR de MNP funcionalizadas. Región espectral FT-IR en los 850-1900 cm −1 rango de a) NH 2 @MNPs, b) gH625 @ MNPs, yc) PEG, FA @ MNPs
El anclaje de FA en MNP también ha sido probado por los espectros UV / Vis de una solución coloidal de PEG, FA @ MNP. La Figura 5 compara los espectros de NH 2 @MNPs y PEG, FA @ MNPs dispersiones coloidales. Se ha añadido como referencia el espectro de una solución FA (5 μM). Una banda evidente a 274 nm típica de FA es claramente visible tanto en la solución coloidal de referencia como en la de PEG, FA @ MNP, lo que confirma la presencia de FA en las MNP. Tenga en cuenta que el ligero cambio es de la absorción de FA-NHS a 280 nm al valor de 274 nm después del anclaje, probablemente debido al cambio del entorno de FA-NHS libre y FA anclado a nanopartículas. La presencia de cambios variables de la banda de absorción a 280 nm después del anclaje de la superficie de FA o la conjugación con otras moléculas ya se ha observado en la literatura [49,50,51].
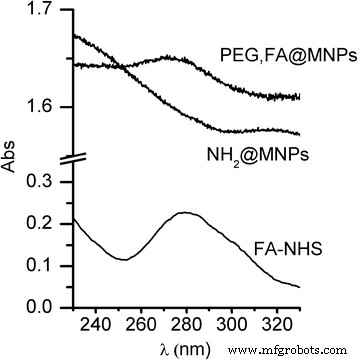
Caracterización UV / Vis de MNP funcionalizadas. Espectros UV / Vis de una solución de FA-NHS 5 μM y de NH 2 @MNPs y PEG, FA @ MNPs dispersiones coloidales. Tenga en cuenta que el alto fondo observado en los espectros de NH 2 @MNPs y PEG, FA @ MNPs se debe a la dispersión de la dispersión coloidal de nanopartículas
El diámetro hidrodinámico medio, el índice de polidispersidad (PDI) y el potencial zeta de las MNP funcionalizadas se determinaron mediante DLS en tampón PBS a pH 7,4 en dispersiones de MNP preparadas y después de 72 h de envejecimiento (Tabla 1). Los diámetros hidrodinámicos de NH 2 -PA @ MNP, gH625 @ MNP y PEG, FA @ MNP fueron 73,0 ± 3,0 nm, 104,0 ± 4,0 nm y 51 ± 2 nm, respectivamente, y los valores de PDI indican una distribución suficientemente estrecha del tamaño de partícula. Como era de esperar, la conjugación con gH625 aumentó el tamaño de las nanopartículas, mientras que la disminución del tamaño de PEG, FA @ MNPs se debe a una mejor dispersión que el NH 2 @MNPs, relacionado con la presencia de las cadenas PEG.
En cualquier caso, tenga en cuenta que se observó un potencial zeta altamente negativo (<- 30 mV) para todos los sistemas. Estos valores de potencial zeta negativos aseguran la estabilidad a largo plazo y evitan la agregación extensa de partículas [52, 53]. De hecho, la carga superficial negativa solo dependía ligeramente del recubrimiento, pero resultó principalmente de la combinación del núcleo cargado negativamente de Fe 3 O 4 nanopartículas [54] y el efecto de los grupos de ácido fosfónico como se observa en sistemas similares [52, 34]. Por lo tanto, en comparación con otras estrategias sintéticas utilizadas para funcionalizar las MNP, el uso de monocapas de ácido fosfónico como enlazadores no solo permite la formación de enlaces estables entre la superficie y los grupos funcionales, sino que también induce un potencial zeta altamente negativo. Después de 72 h de envejecimiento, el tamaño y el potencial zeta del NH 2 -PA @ MNPs, gH625 @ MNPs y PEG, FA @ MNPs permanecen aproximadamente iguales, lo que sugiere que todas las superficies decoradas son estables en el tiempo.
Viabilidad celular
La viabilidad de las células HBMEC y A-172 incubadas con gH625 @ MNPs y FA, PEG @ MNPs se evaluó mediante el ensayo MTT en diferentes tiempos de incubación y en presencia de diferentes concentraciones de nanopartículas (10 y 20 μg / ml). Como se muestra en la Figura 6, no se observó ningún efecto citotóxico dependiente de la concentración o del tiempo (24-48-72 h) de los sistemas decorados en las células HBMEC y A-172.
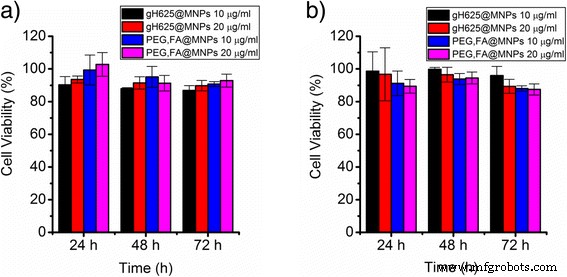
Viabilidad celular. Viabilidad celular de a HBMEC y b Células A-172 incubadas durante 24, 48 y 72 h con gH625 @ MNPs 10 μg / ml (barra negra), gH625 @ MNPs 20 μg / ml (barra roja), PEG, FA @ MNPs 10 μg / ml (barra azul ) y PEG, FA @ MNPs 20 μg / ml (barra magenta)
Captación intracelular
Para determinar si la capacidad de penetración celular del péptido gH625 se retiene después de su inmovilización en la superficie de la nanopartícula, y para comparar la capacidad de gH625 y FA de cruzar la BBB, la internalización en las células endoteliales del cerebro humano de gH625 @ MNP marcadas con NBD y PEG marcado con Rhod, FA @ MNP se ha investigado con microscopía de barrido láser confocal.
Después de 24 h de incubación, la captación de PEG-FA @ MNPs no es evidente, mientras que la internalización de gH625 @ MNPs es claramente visible (Fig. 7). La conjugación con gH625 conduce a una captación más rápida y una intensidad casi dos veces mayor de la fluorescencia intracelular (Fig. 8).
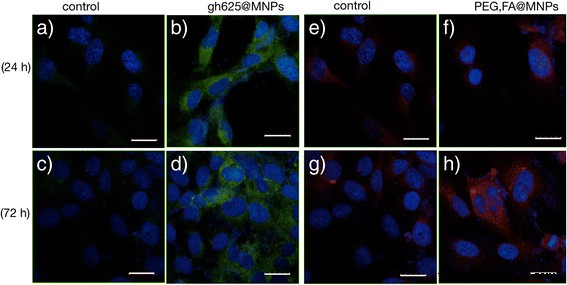
Micrografías de fluorescencia LSM de HBMEC. Micrografías de fluorescencia LSM de HBMEC incubadas durante 24 h ( b , f ) y 72 h ( d , h ) con gH625 marcado con NBD @ MNPs 15 μg / ml ( b , d ) y sus controles ( a , c ) o PEG marcado con rodio, FA @ MNPs 15 μg / ml ( f , h ) y sus controles ( e , g ). Barra de escala =20 μm
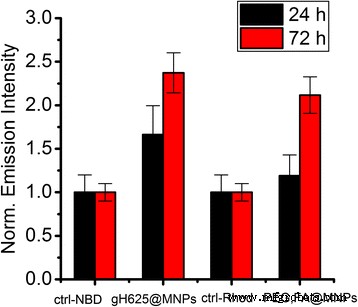
Intensidades normalizadas de fluorescencia intracelular. Análisis cuantitativo de la fluorescencia intracelular después de la incubación de HBMEC a las 24 y 72 h con gH625 @ MNPs marcados con NBD y FA, PEG @ MNPs marcados con Rhod
Para tiempos de incubación más largos (72 h), se reducen las diferencias entre la internalización de los dos sistemas. Este comportamiento no es inesperado, ya que para tiempos de incubación prolongados, pueden ocurrir procesos de internalización inespecíficos de FA, PEG @ MNP y nuestros resultados confirman aún más lo que informamos anteriormente para la absorción de nanopartículas de poliestireno funcionalizadas y no funcionalizadas [55].
Para explorar más a fondo la posibilidad de utilizar gH625 @ MNP como agente terapéutico para tumores cerebrales, se investigaron las captaciones celulares de gH625 @ MNP y FA, PEG @ MNP utilizando la línea celular de glioblastoma A-172. El glioblastoma es uno de los tumores cerebrales primarios más comunes y también uno de los cánceres más letales.
Las captaciones celulares de gH625 @ MNP y FA, PEG @ MNP después de 24 h de incubación son comparables, como se muestra en la Fig. 9.
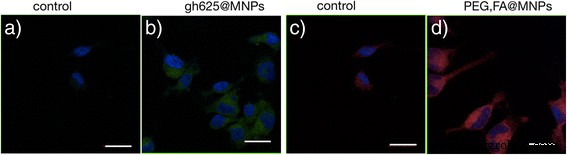
Micrografías de fluorescencia LSM de células de glioblastoma. Micrografías de fluorescencia LSM de células de glioblastoma. Imágenes azul-verde fusionadas:celdas de control ( a ) y células incubadas con 15 μg / ml de gH625 @ MNP marcado con NBD ( b ). Imágenes azul-rojo fusionadas:celdas de control ( c ) y células incubadas con 15 μg / ml de PEG marcado con rhod, FA @ MNP ( d ). Barra de escala =20 μm
Este comportamiento sugiere que el gH625 es capaz de dirigirse al tumor cerebral con la misma eficacia que la unidad de focalización de FA adoptada con mayor frecuencia.
Conclusions
Fe3 O 4 nanoparticles have been functionalized with the gH625 viral cell penetrating peptide adopting a versatile route based on MNP prefunctionalization with a monolayer consisting of a bifunctional phosphonic linker, 3-aminopropylphosphonic acid. The cell internalization capabilities of this system have been evaluated by comparing them with those of a reference system based on MNPs functionalized with PEG, rhodamine, and folic acid, obtained adopting the same NH2 -PA-based platform. The uptake of the two differently decorated MNPs was assessed in primary microvascular endothelial cells from human brain, which are the main components of the BBB and simulate an in vitro model of the BBB. These surface modifications influence the internalization of MNPs in HBMEC and, therefore, their capability to cross the BBB. In fact, conjugation with the gH625 peptide upgraded the delivery of nanoparticles across the in vitro BBB, leading to significant higher cell uptake in HBMEC after 24 h compared with that of FA bearing MNPs (FA,PEG@MNPs). Note that also other strategies have been used to enhance nanoparticle uptake across the BBB. A common approach is to attach targeting ligands in order to activate receptor-mediated endocytosis. As examples, transferrin-coupling nanoparticles can penetrate into the BBB through a transferrin receptor-mediated process [56]. Analogously, the linkage of the apolipoprotein E to the nanoparticles enhances the BBB penetration [57]. Besides, nanoparticles having a surface charges modified with polyethylenimine (PEI) has been reported to cross the BBB by absorptive-mediated transcytosis [58]. Finally, the ability of MNPs to pass through human brain microvascular endothelial cells, used as an in vitro BBB model, can be also facilitated by an external magnet [59]. In our work, we studied a different approach which use a cell penetrating peptide, the gh625, to improve internalization capabilities of Fe3 O 4 nanoparticles. These results are in accordance with those previously obtained by D. Guarnieri et al. using different kinds of MNPs [55, 60] confirming that the gH625-decorated magnetic nanoparticle has a relevant role in crossing the BBB and could be used as a safe and effective drug delivery system.
Abreviaturas
- A-172:
-
Human glioblastoma cell line
- B.E.:
-
Binding energy
- BBB:
-
Blood-brain barrier
- CNS:
-
Central nervous system
- CPPs:
-
Cell-penetrating peptides
- DIPEA:
-
N ,N -Diisopropylethylamine
- DLS:
-
Dynamic light scattering
- DMEM:
-
Medio Eagle modificado de Dulbecco
- DAPI:
-
4′,6-Diamidino-2-phenylindole
- DMSO:
-
Dimethyl sulfoxide
- FA:
-
Folic acid
- FA-NHS:
-
Activated form of FA with NHS
- FBS:
-
Suero fetal bovino
- Fmoc:
-
9-Fluorenylmethoxycarbonyl
- FT-IR:
-
Espectroscopía infrarroja por transformada de Fourier
- gh625:
-
20-Residue peptide derived from the glycoprotein H (gH) of the Herpes simplex virus 1
- gH625@MNPs:
-
NH2 @MNPs functionalized with gh625
- HBMECs:
-
Microvascular endothelial cells from human brain
- MNPs:
-
Magnetic iron nanoparticles
- MTT:
-
3-(4,5-Dimethyl-2-thiazolyl)-2,5-diphenyl-2H -tetrazolium bromide
- NBD:
-
4-Chloro-7-nitrobenz-2-oxa-1,3-diazole
- NH2 @MNPs:
-
MNPs modified with NH2 -PA
- NH2 -PA:
-
3-Aminopropylphosphonic acid
- NHS:
-
N -Hydroxysuccinimide
- PBS:
-
Phosphate-buffered saline
- PDI:
-
Polydispersity index
- PEG:
-
Polyethylene glycol
- PEG,FA@MNPs:
-
NH2 @MNPs functionalized with FA, Rhod and PEG
- PEG-NHS:
-
Methoxypolyethylene glycol acetic acid N -succinimidyl ester
- PEI:
-
Polyethylenimine
- Rhod:
-
Carboxy-X -rhodamine
- Rhod-NHS:
-
Carboxy-X -rhodamine N -succinimidyl ester
- TFA:
-
Trifluoroacetic acid
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
X-ray powder diffraction
Nanomateriales
- Nanofibras y filamentos para una mejor administración de fármacos
- Nanopartículas para la terapia del cáncer:avances y desafíos actuales
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- Preparación y actividad de hidrogenación catalítica mejorada de nanopartículas de Sb / Palygorskita (PAL)
- La detección fotoelectroquímica mejorada de ácido úrico en electrodo de carbono vítreo modificado con nanopartículas de Au
- Estudio in vitro de la influencia de nanopartículas de Au en las líneas celulares HT29 y SPEV
- Síntesis hidrotermal de nanopartículas de In2O3, gemelos híbridos, discos hexagonales, heteroestructuras de ZnO para mejorar las actividades fotocatalíticas y la estabilidad
- Estabilidad mejorada de nanopartículas magnéticas de oro con poli (ácido 4-estirenosulfónico-ácido co-maleico):propiedades ópticas personalizadas para la detección de proteínas
- Profundos efectos interfaciales en CoFe2O4 / Fe3O4 y Fe3O4 / CoFe2O4 Core / Shell Nanoparticles
- Síntesis en un solo recipiente de nanopartículas de núcleo-capa de CoFe2O4 @ Ag monodispersas y su caracterización
- Potencial de activación antiproliferativa y de apoptosis de nanopartículas de lípidos dirigidos a base de paclitaxel con internalización celular mejorada por receptores de transferrina:un estudio …



