Dependencia de la toxicidad de las nanopartículas en sus propiedades físicas y químicas
Resumen
Los estudios sobre los métodos de síntesis de nanopartículas (NP), el análisis de sus características y la exploración de nuevos campos de sus aplicaciones están a la vanguardia de la nanotecnología moderna. La posibilidad de diseñar NPs solubles en agua ha allanado el camino para su uso en diversas investigaciones biomédicas básicas y aplicadas. En la actualidad, los NP se utilizan en el diagnóstico para la formación de imágenes de numerosos marcadores moleculares de enfermedades genéticas y autoinmunes, tumores malignos y muchos otros trastornos. Los NP también se utilizan para la administración dirigida de fármacos a tejidos y órganos, con parámetros controlables de liberación y acumulación de fármacos. Además, existen ejemplos del uso de NP como componentes activos, por ejemplo, fotosensibilizadores en terapia fotodinámica y en la destrucción de tumores hipertérmicos mediante incorporación y calentamiento de NP. Sin embargo, una alta toxicidad de los NP para los organismos vivos es un factor limitante fuerte que dificulta su uso in vivo. Los estudios actuales sobre los efectos tóxicos de los NP destinados a identificar los objetivos y los mecanismos de sus efectos nocivos se llevan a cabo en modelos de cultivo celular; estudios sobre los patrones de transporte, acumulación, degradación y eliminación de NP en modelos animales. Esta revisión sistematiza y resume los datos disponibles sobre cómo los mecanismos de toxicidad NP para los sistemas vivos están relacionados con sus propiedades físicas y químicas.
Antecedentes
La Organización Internacional de Normalización define las nanopartículas (NP) como estructuras cuyos tamaños en una, dos o tres dimensiones están dentro del rango de 1 a 100 nm. Aparte del tamaño, las NP pueden clasificarse en términos de sus parámetros físicos, por ejemplo, carga eléctrica; características químicas, como la composición del núcleo o la cubierta del NP; forma (tubos, películas, varillas, etc.); y origen:NP naturales (NP contenidas en polvo volcánico, partículas virales, etc.) y NP artificiales, que son el foco de esta revisión.
Las nanopartículas se han vuelto ampliamente utilizadas en electrónica, agricultura, producción textil, medicina y muchas otras industrias y ciencias. La toxicidad del NP para los organismos vivos, sin embargo, es el principal factor que limita su uso en el tratamiento y diagnóstico de enfermedades. En la actualidad, los investigadores se enfrentan a menudo al problema del equilibrio entre el efecto terapéutico positivo de los NP y los efectos secundarios relacionados con su toxicidad. En este sentido, la elección de un modelo experimental adecuado para estimar la toxicidad entre in vitro (líneas celulares) e in vivo (animales de experimentación) es de suma importancia. Los efectos tóxicos del NP sobre componentes celulares individuales y tejidos individuales son más fáciles de analizar en modelos in vitro, mientras que los experimentos in vivo permiten estimar la toxicidad del NP para órganos individuales o el cuerpo en su conjunto. Además, el posible efecto tóxico de las NP depende de su concentración, la duración de su interacción con la materia viva, su estabilidad en los fluidos biológicos y la capacidad de acumulación en tejidos y órganos. El desarrollo de NP seguras y biocompatibles que se pueden utilizar para el diagnóstico y el tratamiento de enfermedades humanas solo puede basarse en una comprensión completa de las interacciones entre todos los factores y mecanismos subyacentes a la toxicidad de NP.
Aplicaciones médicas de nanopartículas
En medicina, los NP se pueden utilizar con fines diagnósticos o terapéuticos. En el diagnóstico, pueden servir como marcadores fluorescentes para la detección de biomoléculas y patógenos y como agentes de contraste en resonancia magnética y otros estudios. Además, las NP se pueden utilizar para la administración dirigida de fármacos, incluidas proteínas y sustancias polinucleotídicas; en terapia fotodinámica y destrucción térmica de tumores, y en reparación protésica [1, 2, 3, 4, 5, 6]. Algunos tipos de NP ya se utilizan con éxito en la clínica para la administración de fármacos y la obtención de imágenes de células tumorales [7, 8, 9].
Recientemente, se han ido acumulando ejemplos del uso de NP de oro. Han demostrado ser portadores eficientes de quimioterápicos y otros fármacos. Los NP de oro son altamente biocompatibles; sin embargo, aunque el oro como sustancia es inerte frente a los objetos biológicos, no se puede argumentar que lo mismo ocurre con los NP de oro, ya que todavía no hay datos concluyentes sobre la ausencia de efectos tóxicos retardados [10]. Además de las NP de oro, las basadas en micelas, liposomas [11] y polímeros con "moléculas de captura" unidas [12] ya se utilizan como portadores de fármacos. Los nanotubos de pared simple y múltiple son buenos ejemplos de NP que se utilizan para la administración de fármacos. Son adecuados para unir varios grupos funcionales y moléculas para una entrega dirigida, y su forma única les permite penetrar selectivamente a través de barreras biológicas [13]. El uso de NP como vehículos para fármacos mejora la especificidad de la administración y disminuye la cantidad mínima de NP necesaria para lograr y mantener el efecto terapéutico, reduciendo así la eventual toxicidad. Esto es especialmente importante en el caso de agentes quimio y radioterapéuticos altamente tóxicos y de corta duración [14].
Los puntos cuánticos (QD) constituyen otro grupo de NP con un alto potencial de uso clínico. Los QD son nanocristales semiconductores de 2 a 10 nm de tamaño. Su capacidad de fluorescencia en diferentes regiones espectrales, incluida la infrarroja [15], las hace adecuadas para marcar y obtener imágenes de células, estructuras celulares o agentes biológicos patógenos, así como para diversos procesos en células, tejidos y el cuerpo en su conjunto [ 16,17,18], que tiene importantes implicaciones diagnósticas [19, 20]. Los NP basados en óxido de hierro superparamagnético se utilizan eficazmente como agentes de contraste en la tomografía por resonancia magnética (MRT) para obtener imágenes de tejidos del hígado, la médula ósea y los ganglios linfáticos [21]. También hay un ejemplo en el que se utilizaron nanotubos de carbono de pared simple marcados radiactivamente funcionalizados con fosfolípidos para marcar tumores que contienen integrinas y su posterior detección mediante tomografía por emisión de positrones en experimentos con ratones [22].
Las nanopartículas también se han utilizado en el diseño de biosensores, incluidos los basados en nanotubos de carbono para medir el nivel de glucosa [23], detectar fragmentos y regiones de ADN específicos [24] e identificar células bacterianas [25].
Los NP de plata (o que contienen plata) ejercen efectos antimicrobianos y citostáticos; por esta razón, se utilizan ampliamente en medicina, por ejemplo, para el tratamiento de vendajes, instrumentos quirúrgicos, prótesis y anticonceptivos [13, 22]. Se ha informado que los NP de plata sirven como agentes de conservación eficaces y seguros en la industria cosmética [26].
Sin embargo, los NP pueden seguir siendo altamente tóxicos, incluso si se ha demostrado la seguridad del uso de muchos de sus componentes químicos en la medicina. El efecto tóxico puede ser causado por sus propiedades físicas y químicas únicas, que subyacen a los mecanismos específicos de interacción con los sistemas vivos. En general, esto determina la importancia de estudiar las causas y mecanismos del potencial efecto tóxico de las NP.
Mecanismos de toxicidad por nanopartículas
La toxicidad de los NP está determinada en gran medida por sus características físicas y químicas, como su tamaño, forma, área de superficie específica, carga superficial, actividad catalítica y la presencia o ausencia de un caparazón y grupos activos en la superficie.
El pequeño tamaño de los NP les permite penetrar a través de las barreras epiteliales y endoteliales en la linfa y la sangre para ser transportadas por el torrente sanguíneo y el torrente linfático a diferentes órganos y tejidos, incluidos el cerebro, el corazón, el hígado, los riñones, el bazo, la médula ósea y sistema nervioso [27, 28], y pueden ser transportados al interior de las células mediante mecanismos de transcitosis o simplemente difundirse a través de la membrana celular. Los nanomateriales también pueden aumentar el acceso al torrente sanguíneo a través de la ingestión [29, 30]. Algunos nanomateriales pueden penetrar la piel [31, 32] e incluso micropartículas mayores pueden penetrar la piel cuando se flexiona [33]. Las nanopartículas, debido a su pequeño tamaño, pueden extravasar a través del endotelio en sitios inflamatorios, epitelio (p. Ej., Tracto intestinal e hígado), tumores o penetrar microcapilares [34]. Los experimentos que modelaron los efectos tóxicos de los NP en el cuerpo han demostrado que los NP causan trombosis al mejorar la agregación plaquetaria [35], la inflamación de las vías respiratorias superiores e inferiores, trastornos neurodegenerativos, accidente cerebrovascular, infarto de miocardio y otros trastornos [36,37,38 ]. Tenga en cuenta que las NP pueden entrar no solo en órganos, tejidos y células, sino también en orgánulos celulares, por ejemplo, mitocondrias y núcleos; esto puede alterar drásticamente el metabolismo celular y causar lesiones en el ADN, mutaciones y muerte celular [39].
Se ha demostrado que la toxicidad de los QD está directamente relacionada con la fuga de iones libres de metales contenidos en sus núcleos, como cadmio, plomo y arsénico, tras la oxidación por agentes ambientales. Las QD pueden ser absorbidas por las mitocondrias y causar cambios morfológicos y disfunción de los orgánulos [40]. Entrada de QD a base de cadmio en las células y formación de Cd libre 2+ iones causa estrés oxidativo [41, 42].
Estudios recientes han demostrado que el contacto del tejido pulmonar con NP de aproximadamente 50 nm de tamaño conduce a la perforación de las membranas de las células alveolares de tipo I y la entrada resultante de las NP en las células. Esto, a su vez, causa necrosis celular, como lo demuestra la liberación de lactato deshidrogenasa [43]. Existe evidencia de que la penetración de QD aumenta la fluidez de la membrana celular [44]. Por otro lado, la formación de especies reactivas de oxígeno (ROS) inducida por la peroxidación de los lípidos de la membrana puede conducir a la pérdida de flexibilidad de la membrana, lo que, además de una fluidez anormalmente alta, inevitablemente da como resultado la muerte celular.
La interacción de los NP con el citoesqueleto también puede dañarlo. Por ejemplo, TiO 2 Las NP inducen cambios conformacionales en la tubulina e inhiben su polimerización [45], lo que altera el transporte intracelular, la división celular y la migración celular. En las células endoteliales de la vena umbilical humana (HUVEC), el daño del citoesqueleto dificulta la maduración de los complejos adhesivos de coordinación que unen el citoesqueleto a la matriz extracelular, perturbando así la formación de la red vascular [46].
Además, la citotoxicidad NP puede interferir con la diferenciación celular y la síntesis de proteínas, así como activar genes proinflamatorios y síntesis de mediadores inflamatorios. Cabe señalar especialmente que los mecanismos de protección normales no afectan a los NP; La captación de macrófagos de nanopartículas pegiladas grandes es más eficiente que la captación de pequeñas, lo que conduce a la acumulación de NP en el cuerpo [47]. Se ha demostrado que las NP de óxido de hierro superparamagnéticas alteran o suprimen por completo la diferenciación osteogénica de las células madre y activan la síntesis de moléculas señal, antígenos tumorales, etc. [48, 49]. Además, la interacción de las NP con la célula mejora la expresión de los genes responsables de la formación de lisosomas [50], altera su funcionamiento [51] e inhibe la síntesis de proteínas [52, 53]. Un estudio sobre los efectos tóxicos de las NP de diferentes composiciones sobre las células epiteliales pulmonares y las líneas de células tumorales humanas ha demostrado que las NP estimulan la síntesis de mediadores de la inflamación, por ejemplo, la interleucina 8 [54]. Según Park, que estudió la expresión de citocinas proinflamatorias in vitro e in vivo, las expresiones de interleucina 1 beta (IL-1β) y factor de necrosis tumoral alfa (TNFα) aumentan en respuesta a los NP de silicio [55].
La oxidación, así como la acción de varias enzimas en la cáscara y la superficie de las NP, resulta en su degradación y liberación de radicales libres. Además del efecto tóxico de los radicales libres expresado como oxidación e inactivación de enzimas, mutagénesis y alteración de las reacciones químicas que conducen a la muerte celular, la degradación de los NP conduce a la alteración o pérdida de su propia funcionalidad (p. Ej., La pérdida del momento magnético y los cambios en el espectro de fluorescencia y el transporte u otras funciones) [56, 57].
En resumen, los mecanismos más comunes de citotoxicidad NP son los siguientes:
- 1.
Las NP pueden causar oxidación mediante la formación de ROS y otros radicales libres;
- 2.
Las NP pueden dañar las membranas celulares al perforarlas;
- 3.
Las NP dañan componentes del citoesqueleto, perturbando el transporte intracelular y la división celular;
- 4.
Los NP alteran la transcripción y dañan el ADN, acelerando así la mutagénesis;
- 5.
Las NP dañan las mitocondrias y alteran su metabolismo, lo que conduce a un desequilibrio energético celular;
- 6.
Las NP interfieren con la formación de lisosomas, lo que dificulta la autofagia y la degradación de macromoléculas y desencadena la apoptosis;
- 7.
Las NP provocan cambios estructurales en las proteínas de la membrana y perturban el transporte de sustancias hacia y desde las células, incluido el transporte intercelular;
- 8.
Las NP activan la síntesis de mediadores inflamatorios al alterar los mecanismos normales del metabolismo celular, así como el metabolismo de tejidos y órganos (Fig. 1).
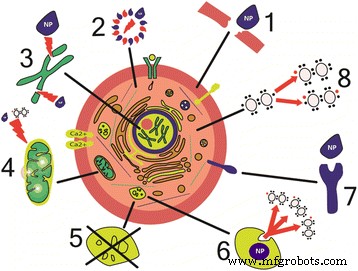
Mecanismos de daño celular por nanopartículas. (1) Daño físico de las membranas [43, 67, 75]. (2) Cambios estructurales en los componentes del citoesqueleto [45, 46]. (3) Alteración de la transcripción y daño oxidativo del ADN [61, 62]. (4) Daño de las mitocondrias [39, 40]. (5) Alteración del funcionamiento de los lisosomas [51]. (6) Generación de especies reactivas de oxígeno [61]. (7) Alteración de las funciones de las proteínas de membrana [172]. (8) Síntesis de factores y mediadores inflamatorios [54, 55]
Aunque existen numerosos mecanismos de toxicidad por NP, es necesario determinar y clasificar el tipo y mecanismo de cada efecto tóxico particular de las NP como dependiente de sus propiedades físicas y químicas.
Relaciones de la toxicidad de las nanopartículas con sus propiedades físicas y químicas
Se considera que la toxicidad de los NP depende de sus características físicas y químicas, incluido el tamaño, la forma, la carga superficial, la composición química del núcleo y la cubierta y la estabilidad. En particular, Oh et al., Utilizando el metanálisis de datos de 307 artículos que describen 1741 muestras de datos relacionados con la viabilidad celular, analizaron recientemente la toxicidad del punto cuántico de CdSe. Se ha demostrado que la nanotoxicidad QD está estrechamente correlacionada con sus propiedades superficiales (incluidas las modificaciones de la capa, el ligando y la superficie), el diámetro, el tipo de ensayo de toxicidad utilizado y el tiempo de exposición [58]. Cuál de estos factores es el más importante está determinado por la tarea y el modelo experimentales específicos; por lo tanto, ahora consideraremos cada factor por separado.
Tamaño y toxicidad de las nanopartículas
El tamaño y la superficie de las NP juegan un papel importante, determinando en gran medida el mecanismo único de interacción de las NP con los sistemas vivos. Las NP se caracterizan por una superficie específica muy grande, lo que determina su alta capacidad de reacción y actividad catalítica. Los tamaños de las NP (de 1 a 100 nm) son comparables con el tamaño de los glóbulos de proteína (2 a 10 nm), el diámetro de la hélice del ADN (2 nm) y el grosor de las membranas celulares (10 nm), lo que les permite fácilmente entrar en células y orgánulos celulares. Por ejemplo, Huo et al. han demostrado que las NP de oro no mayores de 6 nm entran efectivamente en el núcleo celular, mientras que las NP grandes (10 o 16 nm) solo penetran a través de la membrana celular y se encuentran solo en el citoplasma. Esto significa que las NP de varios nanómetros de tamaño son más tóxicas que las NP de 10 nm o más grandes, que no pueden entrar en el núcleo [59]. Pan y col. han rastreado la dependencia de la toxicidad de los NP de oro de su tamaño en el rango de 0,8 a 15 nm. Se ha descubierto que las NP de 15 nm de tamaño son 60 veces menos tóxicas que las NP de 1,4 nm para los fibroblastos, las células epiteliales, los macrófagos y las células de melanoma. También es digno de mención que las NP de 1,4 nm causan necrosis celular (dentro de las 12 h posteriores a su adición al medio de cultivo celular), mientras que las NP de 1,2 nm causan predominantemente apoptosis [60]. Estos datos sugieren no solo que las NP pueden entrar en el núcleo, sino también que la correspondencia del tamaño geométrico de las NP (1,4 nm) con el del surco principal del ADN les permite interactuar de manera efectiva con la columna vertebral de ADN de azúcar-fosfato cargada negativamente y bloquear la transcripción [61, 62].
Además, el tamaño de las NP determina en gran medida cómo interactúan las NP con los sistemas de transporte y defensa de las células y el cuerpo. Esta interacción, a su vez, afecta la cinética de su distribución y acumulación en el organismo. El artículo de revisión de [63] presenta consideraciones teóricas y numerosos datos experimentales que demuestran que los NP menores de 5 nm generalmente superan las barreras celulares de manera inespecífica, por ejemplo, a través de la translocación, mientras que las partículas más grandes ingresan a las células por fagocitosis, macropinocitosis y mecanismos de transporte específicos e inespecíficos. . Se cree que un tamaño de NP de aproximadamente 25 nm es óptimo para la pinocitosis, aunque esto también depende en gran medida del tamaño y tipo de célula [63, 64]. Los experimentos in vivo han demostrado que los NP menores de 10 nm se distribuyen rápidamente entre todos los órganos y tejidos tras la administración intravenosa, mientras que la mayoría de los NP más grandes (50-250 nm) se encuentran en el hígado, el bazo y la sangre [65]. Esto sugiere que los NP grandes son reconocidos por sistemas de defensa específicos del cuerpo y absorbidos por el sistema de fagocitos mononucleares, lo que les impide ingresar a otros tejidos. Además, Talamini et al. afirmó que el tamaño y la forma de los NP influyen en la cinética de acumulación y excreción de NP de oro en los órganos filtrantes, y solo las NP de oro en forma de estrella pueden acumularse en el pulmón. También han demostrado que los cambios en la geometría NP no mejoran el paso NP de la barrera hematoencefálica [66].
La gran superficie específica asegura una adsorción eficaz de NP en la superficie celular. Esto se demostró en un estudio sobre la actividad hemolítica de partículas de silicio mesoporosas de 100 a 600 nm frente a los eritrocitos humanos [67]. Las partículas de 100 nm de tamaño se adsorbieron eficazmente en la superficie de los eritrocitos sin causar destrucción celular ni cambios morfológicos en las células, mientras que las partículas de 600 nm deformaron la membrana y entraron en las células, lo que provocó la destrucción de los eritrocitos (hemólisis) [67].
Forma y toxicidad de las nanopartículas
Las formas características de los NP son esferas, elipsoides, cilindros, láminas, cubos y varillas. La toxicidad de los NP depende en gran medida de su forma. Esto se ha demostrado para numerosos NP de diferentes formas y composiciones químicas [68,69,70,71]. Por ejemplo, las NP esféricas son más propensas a la endocitosis que los nanotubos y las nanofibras [72]. Se ha descubierto que los nanotubos de carbono de pared simple bloquean más eficazmente los canales de calcio en comparación con los fullerenos esféricos [73].
La comparación de los efectos de los NP de hidroxiapatita con diferentes formas (en forma de aguja, en placa, en forma de varilla y esférica) en células BEAS-2B cultivadas ha demostrado que los NP en placa y en forma de aguja causan la muerte de una mayor proporción de células que las NP esféricas y en forma de bastón [74]. Esto se explica en parte por la capacidad de los NP en forma de placa y de aguja para dañar las células y el tejido por contacto directo. Hu y col. [75] obtuvieron datos interesantes al estudiar el daño de las células de mamíferos por nanohojas de óxido de grafeno. La toxicidad de estas NP se determinó por su forma, lo que les permitió dañar físicamente la membrana celular. Sin embargo, se encontró que su toxicidad disminuía con un aumento en la concentración de suero de ternero fetal en el medio de cultivo. Esto se explica por la alta capacidad de las NP de óxido de grafeno para adsorber moléculas de proteínas, que cubren la superficie de las NP, cambiando así la forma de las NP y previniendo en parte el daño de las membranas celulares [75].
Composición química y toxicidad de las nanopartículas
Aunque la toxicidad de los NP depende en gran medida de su tamaño y forma, no se debe ignorar la influencia de otros factores, como la composición química y la estructura cristalina del NP. Comparación de los efectos del dióxido de silicio de 20 nm (SiO 2 ) y las NP de óxido de zinc (ZnO) en fibroblastos de ratón han demostrado que difieren en los mecanismos de toxicidad. Los NP de ZnO causan estrés oxidativo, mientras que el SiO 2 Los NP alteran la estructura del ADN [76].
De hecho, la toxicidad de los NP está determinada en gran medida por su composición química. Se ha demostrado que puede producirse la degradación de las NP y su extensión depende de las condiciones ambientales, por ejemplo, el pH o la fuerza iónica. La causa más común del efecto tóxico de los NP que interactúan con las células es la fuga de iones metálicos del núcleo del NP. La toxicidad también depende de la composición del núcleo de los NP. Algunos iones metálicos, como Ag y Cd, son de hecho tóxicos y, por lo tanto, causan daño a las células. Otros iones metálicos, como Fe y Zn, son biológicamente útiles, pero, en concentraciones elevadas, podrían dañar las vías celulares y, por tanto, provocar una alta toxicidad. Sin embargo, este efecto se puede disminuir, por ejemplo, recubriendo núcleos NP con capas de polímero gruesas, capas de sílice o capas de oro en lugar de ligandos cortos o usando compuestos no tóxicos para la síntesis de NP. Por otro lado, la composición del núcleo podría alterarse mediante la adición de otros metales. Esto puede resultar en una estabilidad química mejorada contra la degradación de NP y la fuga de iones metálicos en el cuerpo [77].
La toxicidad de los NP también depende de su estructura cristalina. La relación entre la estructura cristalina y la toxicidad se ha estudiado utilizando una línea celular de epitelio bronquial humano y NP de óxido de titanio con diferentes tipos de red cristalina. Se ha demostrado que los NP con una estructura cristalina similar al rutilo (TiO 2 en forma de prisma cristales) causan daño oxidativo del ADN, peroxidación de lípidos y formación de micronúcleos, lo que indica una segregación cromosómica anormal durante la mitosis, mientras que las NP con estructura cristalina similar a la anatasa (TiO octaédrico 2 cristales) del mismo tamaño no son tóxicos [78]. Cabe señalar que la estructura cristalina de NP puede variar dependiendo del entorno, por ejemplo, tras la interacción con agua, fluidos biológicos u otros medios de dispersión. Existe evidencia de que la red cristalina de las NP de ZnS se reorganiza en una estructura más ordenada al entrar en contacto con el agua [79].
Toxicidad y carga superficial de nanopartículas
La carga superficial de las NP juega un papel importante en su toxicidad, porque determina en gran medida las interacciones de las NP con los sistemas biológicos [80, 81].
Las superficies NP y sus cargas podrían modificarse injertando polímeros con cargas diferentes. El PEG (polietilenglicol) o el ácido fólico se utilizan a menudo para mejorar la captación intracelular de NP y la capacidad de dirigirse a células específicas [82]. También se ha informado de la síntesis de nanopartículas de TiO2 biocompatibles que contienen grupos funcionales NH2 o SH [83]. También se habían utilizado otras sustancias, como metotrexato, polietilenimina y dextrano, para modificar las superficies NP y su carga [84].
Una alta toxicidad de los NP cargados positivamente se explica por su capacidad para entrar fácilmente en las células, en contraste con los NP neutrales y cargados negativamente. Esto se explica por la atracción electrostática entre las glicoproteínas de la membrana celular cargadas negativamente y las NP cargadas positivamente. La comparación de los efectos citotóxicos de las NP de poliestireno cargadas negativamente y positivamente en células HeLa y NIH / 3T3 ha demostrado que las últimas NP son más tóxicas. Esto no solo se debe a que las NP con carga positiva penetran más eficazmente a través de la membrana, sino también a que se unen más fuertemente al ADN cargado negativamente, lo que provoca su daño y, como resultado, la prolongación de la fase G0 / G1 del ciclo celular. Los NP cargados negativamente no tienen ningún efecto sobre el ciclo celular [85]. Se han obtenido resultados similares para las NP de oro con carga positiva y negativa, las NP positivas son absorbidas por las células en cantidades mayores y más rápidamente que las negativas y son más tóxicas [86].
Los NP cargados positivamente tienen una capacidad mejorada de opsonización, es decir, la adsorción de proteínas que facilitan la fagocitosis, incluidos los anticuerpos y los componentes del complemento, de la sangre y los fluidos biológicos [87]. Las proteínas adsorbidas, denominadas corona de proteínas, pueden afectar las propiedades superficiales de las NP. Por ejemplo, pueden alterar la carga superficial, las características de agregación y / o el diámetro hidrodinámico de las NP. Además, la adsorción de proteínas en la superficie NP conduce a sus cambios conformacionales, que pueden disminuir o inhibir completamente las actividades funcionales de las proteínas adsorbidas. La corona de proteínas consta principalmente de las principales proteínas séricas, como albúmina, fibrinógeno e inmunoglobulina G, así como otras moléculas efectoras, de señal y funcionales [88, 89]. La unión a las NP altera la estructura de la proteína, lo que conduce a la pérdida de su actividad enzimática, la alteración de los procesos biológicos y la precipitación de estructuras poliméricas ordenadas, por ejemplo, fibrillas amiloides [90]. Esto puede provocar diversas enfermedades, como la amiloidosis. Los experimentos in vitro han demostrado que los QD recubiertos con un polímero hidrófilo aceleran la formación de fibrillas de β 2 humanos microglobulina, que luego se organizan en estructuras de múltiples capas en la superficie de la partícula; esto da como resultado un aumento local de la concentración de proteínas en la superficie del NP, precipitación y formación de oligómeros [91].
Xu y col. desarrolló un método para cambiar la carga NP de negativa a positiva mediante varias modificaciones de la superficie. Por ejemplo, las NP poliméricas se modificaron con un polímero sensible al pH para que, al estar cargadas negativamente en un medio neutro, adquirieran una carga positiva en un medio ácido, a pH 5-6 [92]. Esta técnica permite aumentar sustancialmente la tasa de absorción de NP por las células, que podría usarse para la administración de fármacos a las células tumorales. La estimación de la citotoxicidad de las NP de óxido de cerio de superficie modificada para células H9C2, HEK293, A549 y MCF-7 ha demostrado que se pueden obtener básicamente diferentes efectos biológicos y tóxicos utilizando diferentes polímeros para producir NP con carga positiva o negativa o neutra. Específicamente, las NP neutras y cargadas positivamente son absorbidas por todos los tipos de células a la misma velocidad, mientras que las NP cargadas negativamente se acumulan predominantemente en las células tumorales [93]. Por lo tanto, la modificación de la carga de NP permite controlar su localización y toxicidad, lo que podría usarse para desarrollar sistemas efectivos para la administración de fármacos quimioterapéuticos a los tumores.
Concha de nanopartículas y toxicidad
La aplicación de un caparazón sobre la superficie de las NP es necesaria para cambiar sus propiedades ópticas, magnéticas y eléctricas; se utiliza para mejorar la biocompatibilidad y solubilidad de las NP en agua y fluidos biológicos al disminuir su capacidad de agregación, aumentar su estabilidad, etc. Así, la cáscara disminuye la toxicidad de las NP y les otorga la capacidad de interacción selectiva con diferentes tipos de células y moléculas biológicas. Además, la cáscara influye considerablemente en la farmacocinética de NP, cambiando los patrones de distribución y acumulación de NP en el cuerpo [94].
Como se señaló anteriormente, la toxicidad de NP está relacionada en gran medida con la formación de radicales libres [40, 57, 95, 96]. Sin embargo, la cáscara puede mitigar o eliminar considerablemente este efecto negativo, así como estabilizar las NP, aumentar su resistencia a los factores ambientales, disminuir la liberación de sustancias tóxicas de ellas o hacerlas específicas de tejido [97]. Por ejemplo, Cho et al. NP poliméricas modificadas revistiéndolas con lectinas. Las NP modificadas se unían selectivamente a las células tumorales que presentaban moléculas de ácido siálico en la superficie, lo que las hacía adecuadas para marcar específicamente las células cancerosas [98].
La superficie del NP puede modificarse con compuestos tanto orgánicos como inorgánicos, por ejemplo, polietilenglicol, ácido poliglicólico, ácido poliláctico, lípidos, proteínas, compuestos de bajo peso molecular y silicio. Esta variedad de modificadores permite formar sistemas complejos en la superficie del NP para cambiar las propiedades del NP y para su transporte y acumulación específicos.
Las nanopartículas recubiertas con capas de polímeros sintéticos se utilizan para la liberación de antígenos, por lo que sirven como adyuvantes que estimulan la respuesta inmunitaria. Esto permite obtener vacunas contra los antígenos que son objetivos de una fuerte inmunidad celular natural inespecífica [99].
El caparazón se usa a menudo para mejorar la solubilización y disminuir la toxicidad de los QD, porque sus núcleos metálicos son hidrófobos y consisten principalmente en metales pesados tóxicos, como cadmio, telurio y mercurio. La cáscara aumenta la estabilidad del núcleo QD y evita su desalinización y degradación oxidativa o fotolítica. Esto, a su vez, disminuye la fuga de iones metálicos fuera del núcleo QD y, por lo tanto, la toxicidad de los QD [100,101,102].
Estudio de la toxicidad de las nanopartículas
Durante las últimas dos décadas, el uso de NP se ha extendido enormemente y ha conducido a la fundación de la nanotoxicología, una nueva ciencia que estudia los efectos tóxicos potenciales de las NP en sistemas biológicos y ecológicos. El objetivo general de la nanotoxicología es desarrollar las reglas de síntesis de NP seguras [103]. Esto requiere un enfoque sistémico integral para el análisis de las propiedades tóxicas de los NP y sus efectos en las células, los tejidos, los órganos y el cuerpo en general.
Hay dos enfoques de rutina para el estudio de los efectos de diversas sustancias en los sistemas vivos, que también son aplicables a los efectos tóxicos de NP:experimentos in vitro en líneas celulares modelo y experimentos in vivo en animales de laboratorio. No consideramos aquí el tercer enfoque posible para estimar la toxicidad de las NP, la simulación por computadora, porque las vías y los mecanismos de los efectos tóxicos de las NP no se conocen lo suficientemente bien como para que un modelo de computadora pueda predecir las consecuencias de las interacciones entre las NP y la materia viva para un período de tiempo. amplia gama de NP con suficiente fiabilidad.
Tanto el cultivo celular como los modelos experimentales con animales para estudiar la toxicidad de NP tienen sus ventajas y desventajas específicas. Los primeros permiten una comprensión más profunda de los mecanismos moleculares de toxicidad y la identificación de los objetivos primarios de las NP; sin embargo, no se tienen en cuenta los patrones de distribución de NP en el cuerpo y su transporte a diferentes tejidos y células. The study of NP toxicity in animal experiments allows the delayed effects of NP action in vivo to be estimated. However, the general pattern of toxicity manifestations becomes so complicated that it is impossible to determine which of them is the primary cause of the observed effect and which are its consequences.
Study of Toxicity in Cell Cultures
Many studies of NP toxicity are carried out in primary cell cultures serving as models of various types of human and animal tissues. In some cases, tumor cell lines are used, e.g., for estimating the toxic effects of NPs used in cancer chemotherapy. The type of cells is selected according to the potential route by which NPs enter the body. This may be oral uptake (mainly by ingestion), transdermal uptake (through the skin surface), inhalation uptake of NPs contained in the breathing air, or intentional NP injection in clinic. Intestinal epithelium cells (Caco-2, HT29, and SW480) are often used in experimental models for studying the toxicity of ingested NPs (Table 1). In these models, the kinetics of NP uptake by cells and the viability of cells upon the NP uptake are studied.
The NPs that serve as carriers of drugs or contrast agents, or those used for imaging, are administered by injection. The toxicity of these NPs is studied in primary blood cell cultures. Most commonly, hemolysis, platelet activation, and platelet aggregation are estimated. In addition to primary blood cell cultures, cultured HUVECs, mesenchymal stem cells, mononuclear blood cells, and various tumor cell lines (HeLa, MCF-7, PC3, C4-2, and SKBR-3) are used (Table 2).
The toxicity of inhaled NPs is studied using the cell lines modeling different tissues of the respiratory system, e.g., A549 and C10 cells of pulmonary origin, alveolar macrophages (RAW 264.7), various epithelial cells and fibroblasts (BEAS-2B, NHBE, 16-HBE, SAEC), as well as human monocytes (THP-1) (Table 3).
The toxicity of NPs that enter the body transdermally is usually studied in keratinocytes, fibroblasts, and, more rarely, sebocytes (cells of sebaceous glands) (Table 4).
Co-cultured Cell Lines and 3D Cell Cultures
Although the majority of in vitro nanotoxicity studies are carried out on cell monocultures, studies using two other approaches are increasingly often reported in the literature. One of them is co-culturing of several types of cells; the other is the use of 3D cultures. The rationale for these approaches is the need for more realistic models of mammalian tissues and organs. For example, co-cultured Caco-2 epithelial colorectal adenocarcinoma cells and Raji cells (a lymphoblast cell line) have served as a model of the human intestinal epithelium in experiments on the toxicity of silver NPs [104]. A co-culture of three cell lines derived from lung epithelial cells, human blood macrophages, and dendritic cells has been used as an experimental model in a study on the toxic effects of inhaled NPs [105]. A model of skin consisting of co-cultured fibroblasts and keratinocytes has been suggested [106].
It is known that the cell phenotype, as well as cell functions and metabolic processes, is largely determined by the complex system of cell interactions with other cells and the surrounding extracellular matrix [107]. Therefore, many important characteristics of cells with an adhesive type of growth in a monolayer culture substantially differ from those of the same cells in the living tissue; hence, conclusions from many experiments on the NP toxic effects on cells growing in a monolayer are somewhat incorrect [108]. Experimental 3D models of tissues and organs have been used for analysis of NP toxicity and penetration into cells in several published studies. For example, there are 3D models based on polymer hydrogels [109] and models constructed in special perfusion chambers containing a semipermeable membrane to which the cells are attached. Li y col. and Lee et al. [110, 111] used multicellular spheroids about 100 μm in size to obtain a 3D model of the liver and compare the toxicities of CdTe and Au NPs in experiments on this model and a monolayer culture of liver cells [111]. The results obtained using the 3D model were more closely correlated with the data obtained in experiments on animals, which indicates a considerable potential of this approach for adequate and informative testing of NP toxicity.
In vivo Study of Nanoparticle Toxicity
In addition to the study of multilayered and 3D cell cultures, the behavior of NPs in the living body is being extensively studied. Since these studies are focused on the biomedical applications of NPs, the NP toxicity for living organisms remains an important issue. Although NPs are highly promising for various clinical applications, they are potentially hazardous. This hazard cannot be estimated correctly in vitro, following from the comparison of the in vivo and in vitro effects of NPs.
Titanium dioxide (TiO2 ) particles are among the most widely used NPs, in particular, in environment protection measures. Therefore, it was exceptionally important to estimate their toxicity in the case of a 100% bioavailability, namely, in experiments with their intravenous injection to experimental animals. This study has been performed by Fabian et al. [112]. Experimental animals (rats) were injected with a suspension of TiO2 NPs at a dose of 5 mg/kg, and their biodistribution, as well as the general condition of the animals, was monitored. The results have shown that the animals exhibit no signs of ailment or disorder, nor is inflammation or another manifestation of a toxic effect observed, within 28 days. This suggests that TiO2 NPs are relatively harmless.
Silver NPs are another example of NPs potentially useful in medicine, owing to their antimicrobial activity. Their toxicity and biodistribution were analyzed in an experiment where CD-1 mice were intravenously injected with 10 mg/kg of silver NPs of different sizes (10, 40, and 100 nm) coated with different shells. Although each type of NPs was found to cause toxic damage of tissues, larger particles were less toxic, probably, due to their lower penetration capacity [113]. Asare et al. [114] estimated the genotoxicity of silver and titanium NPs administered at a dose of 5 mg/kg. They have found that silver NPs cause DNA strand breaks and oxidation of purine bases in the tissues examined. Gold nanoparticles have a similar effect [115]. They have been shown to be toxic for mice, causing weight loss, decrease in the hematocrit, and reduction of the red blood cell count.
Targeted drug delivery is one of the most important applications of NPs. In this case, it is also paramount to know their toxic properties, because the positive effect of their use should prevail over the negative one. Kwon et al. [116] have developed antioxidant NPs from the polymeric prodrug of vanillin. Their study has shown that the NPs have no toxic effect on the body, specifically the liver, at doses lower than 2.5 mg/kg. Similar results have been obtained for gelatin NPs modified with polyethylene glycol, which are planned to be used for targeted delivery of ibuprofen sodium salt [117]. The NPs have proved to be nontoxic at the dose that is necessary for effective drug delivery (1 mg/kg), which has been confirmed by measuring the inflammatory cytokine levels in the animals studied, as well as histological analysis of their organs.
Quantum dots are among the NPs that are most promising for medical applications (Fig. 2). However, they are potentially hazardous for human health, because they exhibit various toxic effects in both in vitro and in vivo experiments [118,119,120,121,122].
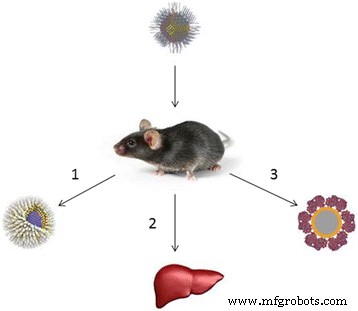
The possible reasons why quantum dots may be nontoxic in animal models. (1) The shell prevents the leakage of heavy metals into the body [129, 135]. (2) Quantum dots are localized in the liver and subsequently eliminated from the body [135, 173]. (3) The protein crown around quantum dots protects the body from heavy metals [132, 174]
Toxic effects of QDs in vivo are usually studied in experiments on mice and rats [123]. A study on the toxicity of cadmium-based QDs for mice showed that QDs were distributed throughout the body as soon as 15 min after injection to the caudal vein, after which they accumulated in the liver, kidneys, spleen, red bone marrow, and lymph nodes. Two years after the injection, fluorescence was mainly retained in lymph nodes; in other organs, no QDs were detected [124]. It should be also noted that the fluorescence spectrum was shifted to the blue spectral region because of the destruction of the QD shell and changes in the shape, size, and surface charge of the QDs. This, however, occurred rather slowly, because the QDs were found to be nontoxic after their injection at the doses at which pure cadmium ions would have had a lethal effect. Similar results were obtained by Yang et al. [125]. Zhang y col. [95] showed that CdTe QDs predominantly accumulated in the liver, decreasing the amount of antioxidants in it and inducing oxidative stress in liver cells.
Cadmium and tellurium ions tend to accumulate in various organs and tissues upon degradation and decay of the cores of CdTe/ZnS QDs. Experiments on mice have shown that cadmium predominantly accumulates in the liver, kidneys, and spleen, whereas tellurium accumulates almost exclusively in the kidneys [126]. Ballou et al. [127] found that cadmium-containing QDs coated with polymer shells of polyacrylic acid or different derivatives of polyethylene glycol had no lethal effect on experimental mice and remained fluorescent for 4 months. СdSe/ZnS NPs also had no detectable pathological effect on mice [128]; however, the absence of distinct signs of pathology still does not mean that the QDs are absolutely nontoxic.
Hu et al. [129] found that lead-containing QDs had no toxic effect on mice for 4 weeks; however, this was most probably because the QDs studied were coated with a polyethylene glycol shell.
Since heavy metals contained in QDs are a factor of their toxicity, several research groups suggested that heavy-metal-free NPs be synthesized. For example, Pons et al. [130] synthesized CuInS2/ZnS QDs fluorescing in the near-infrared spectral region (at a wavelength of about 800 nm) and supposed that this composition would make the QDs nontoxic for experimental animals. Comparison of the effects of CuInS2 /ZnS and CdTeSe/CdZnS QDs on regional lymph nodes in mice showed that the lymph nodes were only slightly, if at all, enlarged upon injection of the QDs not containing heavy metals, whereas injection of the CdTeSe/CdZnS QDs induced a distinct immune response in them [130]. QDs in which silicon was substituted for heavy metals also had no toxic effect on mice [131].
Even QDs containing heavy metals are often found to be nontoxic. One of the possible explanations is that QDs are coated with the protein crown upon entering the living body; this crown shields their surface and protects cells against damage [132]. Usually, the proteins that are included in the NP molecular corona are major serum proteins, such as albumin, immunoglobulin G (IgG), fibrinogen, and apolipoproteins [133]. Molecular corona also can influence on the interaction of NPs with cells. Zyuzin et al. have demonstrated that, in human endothelial cells, the NP protein corona decreases the NP nonspecific binding to the cell membrane, increases the residence time of NP in early endosomes, and reduces the amount of internalized NPs [134].
However, even in the absence of direct signs of intoxication in experimental animals, it remains unclear whether the use of QDs in medicine is safe for humans. In some cases, the QD toxicity was not detected in mice because the NPs were neutralized by the liver and accumulated in it [135]; in other cases, QDs coated with phospholipid micelles exhibited reduced toxicity owing to the shell [129]. Despite the extensive in vivo studies on QD toxicity, their use in biomedicine remains an open question. One of the main reasons is that all the delayed effects of QDs cannot be monitored in experimental animals, because their lifespan is as short as a few years, which is insufficient for complete elimination or degradation of NPs.
Conclusions
The potential toxicity of NPs is the main problem of their use in medicine. Therefore, not only positive results of the use of NPs, but also the possible unpredictable negative consequences of their action on the human body, should be scrutinized. The toxicity of NPs is related to their distribution in the bloodstream and lymph stream and their capacities for penetrating into almost all cells, tissues, and organs and interacting with various macromolecules and altering their structure, thereby interfering with intracellular processes and the functioning of whole organs. The NP toxicity strongly depends on their physical and chemical properties, such as the shape, size, electric charge, and chemical compositions of the core and shell. Many types of NPs are not recognized by the protective systems of cells and the body, which decreases the rate of their degradation and may lead to considerable accumulation of NPs in organs and tissues, even to highly toxic and lethal concentrations. However, a number of approaches to designing NPs with a decreased toxicity compared to the traditional NPs are already available. Advanced methods for studying the NP toxicity make it possible to analyze different pathways and mechanisms of toxicity at the molecular level, as well as reliably predict the possible negative effect at the body level.
Thus, it is obvious that designing NPs that have small or no negative effects is impossible unless all qualitative and quantitative physical and chemical properties of NPs are systematically taken into consideration and a relevant experimental model for estimating their influence on biological systems is available.
Abreviaturas
- FDA:
-
Administración de Alimentos y Medicamentos
- IL-1β:
-
Interleukin-1-beta
- MRT:
-
Magnetic resonance tomography
- NP:
-
Nanoparticle
- QD:
-
Punto cuántico
- ROS:
-
Reactive oxygen species
- SEM:
-
Microscopía electrónica de barrido
- TEM:
-
Microscopía electrónica de transmisión
- TNFα:
-
Tumor necrosis factor alpha
Nanomateriales
- Propiedades físicas y químicas del tungsteno
- Propiedades físicas del titanio
- Propiedades químicas del titanio
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- Propiedades paramagnéticas de nanomateriales derivados del fullereno y sus compuestos poliméricos:efecto de bombeo drástico
- Propiedades de las oscilaciones electromagnéticas longitudinales en metales y su excitación en superficies planas y esféricas
- Síntesis de puntos cuánticos de sulfuro de antimonio solubles en agua y sus propiedades fotoeléctricas
- Síntesis verde de nanopartículas de metal y óxido de metal y su efecto sobre el alga unicelular Chlamydomonas reinhardtii
- Propiedades de los materiales de ingeniería:generales, físicas y mecánicas
- 20 tipos diferentes de metales y sus propiedades
- Tipos de metales y sus propiedades.



