Anclaje de nanocristales Plasmonic Ag @ AgCl en microesferas de ZnCo2O4 con actividad fotocatalítica visible mejorada
Resumen
En este trabajo, una investigación exhaustiva del compuesto Ag @ AgCl / ZnCo 2 O 4 Se presenta el fotocatalizador de microesferas, preparado mediante un sencillo método de dos pasos, y utilizando herramientas de caracterización complementarias como difracción de rayos X (XRD), microscopía electrónica de barrido (SEM), espectroscopía de rayos X de dispersión de energía (EDX), microscopía electrónica de transmisión ( TEM), microscopía electrónica de transmisión de alta resolución (HR-TEM), difracción electrónica de área seleccionada (SAED), espectroscopía de fotoelectrones de rayos X (XPS), espectroscopía de reflectancia difusa UV-Vis (DRS) y Brunauer-Emmett-Teller (BET ). Los resultados muestran que el compuesto Ag @ AgCl / ZnCo 2 O 4 El fotocatalizador tiene una buena morfología de microesferas y un alto nivel de cristalización y su intensidad de absorción en todo el rango del espectro es más alta que la del ZnCo puro 2 O 4 . Se observa que la superficie específica del compuesto Ag @ AgCl / ZnCo 2 O 4 fotocatalizador y la eficiencia de adsorción de rodamina B (RhB) aumentan como resultado de la deposición de Ag @ AgCl. En el Ag @ AgCl / ZnCo 2 O 4 sistema de degradación de RhB, la tasa de degradación fotocatalítica de 0.2Ag@AgCl/ZnCo 2 O 4 se convierte en 99,4% en 120 min y RhB se degrada casi por completo. La constante de velocidad de reacción del compuesto 0.2Ag@AgCl/ZnCo 2 O 4 Se encuentra que el fotocatalizador es 0.01063 min −1 , que es 1,6 veces mayor que el de Ag @ AgCl y 10 veces el valor mínimo de ZnCo 2 O 4 . Además, el experimento de captura de radicales indica que, en el sistema de reacción de Ag @ AgCl / ZnCo 2 O 4 , la principal especie oxidativa de Ag @ AgCl / ZnCo 2 O 4 fotocatalizador son aniones superóxido (O · - 2 - 2 ) y agujero (h + ) y no radical hidroxilo (· OH). Según los resultados, un mecanismo fotocatalítico de plasmón de esquema Z de Ag @ AgCl / ZnCo 2 O 4 Se propone un sistema compuesto para dilucidar la degradación del RhB.
Antecedentes
Los problemas ambientales causados por contaminantes nocivos en el agua se han convertido en un problema mundial [1] y requieren la atención inmediata de científicos y tecnólogos [2, 3, 4]. La degradación fotocatalítica de nano-semiconductores de contaminantes orgánicos en aguas residuales por luz visible es un área de investigación fascinante y prometedora debido a su alta eficiencia, potencial de protección ambiental [5, 6, 7] y utilización efectiva de la radiación solar [8, 9]. Como uno de los materiales fotocatalíticos más importantes, TiO 2 ha sido ampliamente investigado debido a su alta actividad fotocatalítica, no toxicidad, bajo costo y buena estabilidad química [10]. Sin embargo, su aplicación práctica se ve inhibida en gran medida debido a su amplia banda prohibida (3,2 eV para anatasa y 3,0 eV para rutilo), lo que significa que solo puede utilizar luz ultravioleta (5% de la energía solar) [11]. Por lo tanto, un sistema fotocatalítico de luz visible (43% de la energía solar) con alta actividad fotocatalítica es deseable para la utilización eficiente de la radiación solar [12, 13].
ZnCo 2 O 4 pertenece a un grupo de óxidos de espinela [14] con Zn 2+ residiendo en la posición tetraédrica y el Co 3+ permaneciendo en el lugar octaédrico [15]. Debido a la brecha de banda relativamente estrecha de 2,67 eV [16] y la respuesta a la luz de largo alcance (200-800 nm) [17], ZnCo 2 O 4 podría ser un candidato adecuado para la degradación de contaminantes orgánicos fotocatalíticos [18]. Sin embargo, ZnCo 2 O 4 muestra un bajo rendimiento cuántico debido a la baja separación de pares de electrones-huecos inspirados en la foto y la fotoabsorción de luz visible en la superficie de una semana. Esto da como resultado una eficiencia fotocatalítica inferior que limita su aplicabilidad práctica. Para superar estos inconvenientes, el acoplamiento de ZnCo 2 O 4 con otros semiconductores podría ser una buena estrategia que podría conducir a una mejor separación de electrones fotoinducidos y alta actividad fotocatalítica. Por ejemplo, Rajakumar Ananthakrishnan et al. ZnO-ZnCo 2 sintetizado heteroestructurado dopado con cationes O 4 Se descubrió que los nanocompuestos y la tasa de decoloración del naranja de metilo alcanzaban el 92% bajo luz visible [19].
La literatura muestra el estudio de diferentes sistemas fotocatalíticos heterogéneos basados en Ag @ AgCl como H 2 WO 4 .H 2 O / Ag / AgCl [20], Ag @ AgCl-Bi 2 MoO 6 [21], Ag @ AgCl / WO 3 [22] y Ag @ AgCl / rGO [23]. El ancho de banda de AgCl es de 3,25 eV, que no puede absorber la luz visible. Ag @ AgCl demuestra una excelente absorción de luz visible, que proviene del efecto de resonancia de plasmón superficial (SPR) producido por el Ag metálico en la superficie de AgCl [24]. El AgCl disperso puede promover la eficiencia de separación de los portadores de carga fotoinducida. Tanto la excelente absorción de luz visible de Ag @ AgCl como la separación mejorada de los portadores pueden conducir a la mejora de la actividad fotocatalítica.
Del análisis anterior se desprende que el ZnCo 2 O 4 La actividad fotocatalítica evidentemente se puede mejorar anclando nanocristales plasmónicos Ag @ AgCl en ZnCo 2 O 4 . Aquí, el Ag @ AgCl / ZnCo 2 O 4 El material compuesto se preparó con un sencillo método solvotermal de dos pasos. El compuesto se caracterizó por difracción de rayos X (XRD), microscopía electrónica de barrido (SEM), espectroscopía de rayos X de dispersión de energía (EDX), microscopía electrónica de transmisión (TEM), microscopía electrónica de transmisión de alta resolución (HR-TEM), área seleccionada difracción de electrones (SAED), espectroscopía de fotoelectrones de rayos X (XPS), espectroscopía de reflectancia difusa UV-Vis (DRS) y Brunauer-Emmett-Teller (BET). La influencia de ZnCo 2 O 4 Las características estructurales y las propiedades de absorbancia antes y después de la carga de Ag @ AgCl se investigan cuidadosamente. También se presentan la actividad y estabilidad de la degradación fotocatalítica de rodamina B (RhB). Un mecanismo para iluminar el mecanismo de degradación de RhB en Ag @ AgCl / ZnCo 2 O 4 Se propone un sistema fotocatalítico.
Métodos
Síntesis de ZnCo 2 O 4 Microesferas por método asistido por microondas
En un procedimiento de síntesis típico, 2,3 g Zn (NO 3 ) 3 .6H 2 O, 4,48 g Co (NO 3 ) 3 .6H 2 O, 3,6 g CO (NH 2 ) 2 y 1,14 g de NH 4 F se disolvieron en 100 mL de agua desionizada con agitación durante 30 min y luego se dispersaron por ultrasonidos 30 min para obtener una solución rosa. La solución rosa anterior se transfirió a un reactor de politetrafluoroetileno de 300 ml y luego el reactor se conectó al aparato de reacción de microondas. La velocidad de calentamiento se fijó a 8 ° C / min y el microondas se hizo reaccionar a 130 ° C durante 30 min. Una vez finalizada la reacción, el reactor se enfrió a temperatura ambiente. El precursor rosa pálido se recogió mediante centrifugación, se lavó tres veces con agua desionizada y etanol absoluto respectivamente para eliminar los posibles residuos, luego se secó a 80 ° C durante 10 h en horno y se calcinó a 350 ° C durante 2 h en horno de mufla de tubo. a 1 ° C / min para obtener las muestras.
Síntesis de Ag @ AgCl / ZnCo 2 O 4 Microesferas
En una síntesis típica de Ag @ AgCl / ZnCo 2 O 4 microesferas, 0,17 g de AgNO 3 se disolvió en 80 ml de disolvente mixto de alcohol y agua con una relación de volumen de 3:5. Luego, 0,2 g de ZnCo 2 O 4 y se añadieron 0,1-11 g de PVP a la solución mixta anterior con agitación magnética. Después de calentar a 130 ° C durante 3 h, el Ag + -ZnCo 2 O 4 solución formada. Además, 1,5 g L −1 de solución acuosa de NaCl (20 ml) a la solución anterior, luego se ajustó el pH a aproximadamente 2,5 con HCl (12% en peso). La solución se agitó durante 24 h evitando la luz y la fuerza magnética. Algunos Ag + en la solución se redujo a Ag irradiando la solución con una lámpara de xenón de 1000 W durante 30 min. Ag @ AgCl / ZnCo 2 O 4 El catalizador se preparó mediante separación centrífuga, se lavó tres veces con agua desionizada y etanol anhidro respectivamente, secándose a 80 ° C durante 6 h en horno.
Además, el catalizador Ag @ AgCl se preparó sin la presencia de ZnCo 2 O 4 con otra condición sin cambios.
Caracterización
La composición de fase de la muestra obtenida se registró en un difractómetro de rayos X D / MaxRB (Japón) con fuente de radiación Cu-Kα a 35 kV, con una velocidad de barrido de 0,02 ° s −1 en el rango de 2θ de 10 ° a 75 °. Las morfologías se estudiaron mediante microscopía electrónica de barrido (SEM) JSM-6510 y microscopía electrónica de transmisión (TEM) JSM-2100 equipada con un espectro de rayos X de dispersión de energía (EDX). Los datos de espectroscopía de fotoelectrones de rayos X (XPS) se obtuvieron con un espectrómetro de electrones ESCALab220i-XL de VG Scientific usando radiación AlKα de 300 W. La presión base era de aproximadamente 3 × 10 −9 mbar. Las energías de unión se referenciaron a la línea C1s a 284,6 eV del carbono amorfo. El área de superficie específica BET de las muestras fue investigada por un analizador de tamaño de poro y área automatizado de alta velocidad (3H-2000PS1, China).
Medida de actividad fotocatalítica
La actividad fotocatalítica de Ag @ AgCl ZnCo 2 preparado O 4 Los catalizadores de microesferas se evaluaron mediante la fotodegradación de rodamina B (RhB) en solución acuosa. En cada experimento, se dispersaron 50 mg de catalizadores en 50 ml de solución acuosa de RhB (10 mg L −1 ). Antes de la irradiación de la luz, la suspensión se agitó lo suficiente en la oscuridad durante 30 minutos para asegurar el equilibrio de adsorción-desorción. La temperatura de las suspensiones se mantuvo por debajo de 283 K mediante un flujo de agua de refrigeración durante la reacción y la irradiación se realizó con una lámpara de xenón de 1000 W. El cambio de las concentraciones de RhB (C) basado en el tiempo de irradiación se midió con un espectrofotómetro ultravioleta / visible LAMBDA35 (λ =553 nm, Perkin Elmer Instruments Co, Ltd., América). Como función de tiempo, la tasa de decoloración se expresa como C t / C 0 , donde C 0 es la concentración inicial de RhB y C t es la concentración instantánea en la solución. La estabilidad del ciclo de la muestra se detecta como sigue. Después del rendimiento fotocatalítico, las muestras se recogen después de varios lavados y secados. Luego, se repitieron cuatro tiempos de reutilización del experimento mencionado anteriormente.
Resultados y discusión
La estructura de fase y la forma cristalina de los catalizadores se determinaron mediante XRD. En la figura 1, los espectros XRD de ZnCo 2 O 4 , Ag @ AgCl / ZnCo 2 O 4 Se mostraron catalizadores. Los picos de difracción de ZnCo 2 O 4 a 18.96 °, 31.215 °, 36.805 °, 44.738 °, 59.282 ° y 65.149 ° se observaron, correspondientes a (111), (220), (311), (400), (511) y (440) caras de cristal de la espinela cúbica estructurada ZnCo 2 O 4 (JCPDS No. 23-1390), respectivamente, lo que indica que el ZnCo 2 O 4 fue sintetizado por el método asistido por microondas. Después de cargar Ag @ AgCl, los picos de difracción característicos de 27,8 °, 32,2 °, 46,2 °, 54,8 °, 57,5 ° y 67,5 ° de Ag @ AgCl / ZnCo 2 O 4 corresponden a las caras (111), (200), (220), (311), (222) y (400) de AgCl cúbico (JCPDS No. 85-1355). Además, combinado con Ag cúbico (JCPDS No. 87-0719), los espectros XRD de Ag @ AgCl / ZnCo 2 O 4 muestran que hay un pico de difracción característico de nanopartículas de Ag a 38,2 °, lo que indica la existencia de Ag en el catalizador. Porque algunos Ag + se reduce a partículas de Ag en el proceso de foto-reducción, lo que hace que el rendimiento fotocatalítico de Ag @ AgCl / ZnCo 2 O 4 mejorado significativamente bajo luz visible.
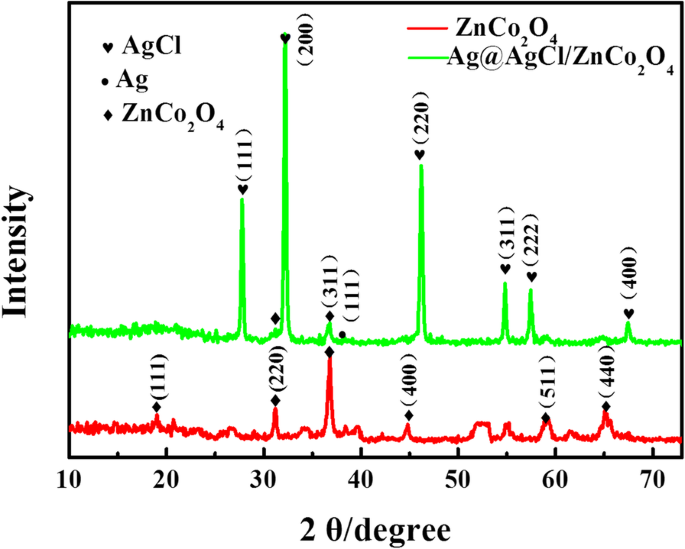
Los patrones XRD del ZnCo 2 preparado O 4 y Ag @ AgCl / ZnCo 2 O 4 muestras de microesferas
En la Fig. 2a, ZnCo 2 esférico O 4 Se prepararon con éxito microestructuras con diámetros que iban de 5 a 8 μm mediante un método asistido por microondas. ZnCo 2 O 4 La estructura de las microesferas consta de láminas apiladas (Fig. 2b). La Figura 2c es la imagen SEM de Ag @ AgCl / ZnCo 2 O 4 después de cargar. Se puede ver que los nanocristales Ag @ AgCl se cargaron en la superficie de ZnCo 2 esférico O 4 . Para seguir observando la morfología de Ag @ AgCl / ZnCo 2 O 4 , la imagen TEM de Ag @ AgCl / ZnCo 2 O 4 se muestra en la Fig. 2d. En la imagen TEM, se puede ver que nanopartículas de Ag de 10 a 50 nm están unidas uniformemente a la superficie de ZnCo 2 O 4 y partículas de AgCl de 20 a 100 nm se dispersan en la superficie de ZnCo 2 O 4 . La Figura 2e muestra el HRTEM de Ag @ AgCl / ZnCo 2 O 4 . Se puede ver que las partículas de Ag y AgCl se cargan en ZnCo 2 O 4 , y las franjas espaciadas d de Ag, AgCl y ZnCo 2 O 4 son 0.235, 0.196 y 0.244 nm, correspondientes a las caras del cristal Ag (111), AgCl (220) y ZnCo 2 O 4 (220), respectivamente. La figura 2f es SAED de Ag @ AgCl / ZnCo 2 O 4 . El anillo de difracción de Ag @ AgCl / ZnCo 2 O 4 Es regular y brillante, lo que indica que es un policristalino con buen cristalino. Los tres planos de cristal tienen un espaciado de celosía de 0,244 nm, 0,235 nm y 0,196 nm, lo que concuerda bien con los resultados de HRTEM. La imagen EDX de Ag @ AgCl / ZnCo 2 O 4 En la Fig. 2g se muestra que la muestra se compone de cinco elementos:O, Co, Zn, Cl y Ag. La intensidad de los picos en la imagen representa el contenido de cada elemento. Zn, Co y O se componen de ZnCo 2 O 4 , mientras que Ag y Cl se componen de Ag @ AgCl. EDX confirmó los elementos químicos correspondientes a Ag @ AgCl / ZnCo 2 O 4 y no detectó otros elementos. En conclusión, se puede determinar claramente que Ag @ AgCl está uniformemente disperso y cargado en la superficie de ZnCo 2 O 4 microesferas.
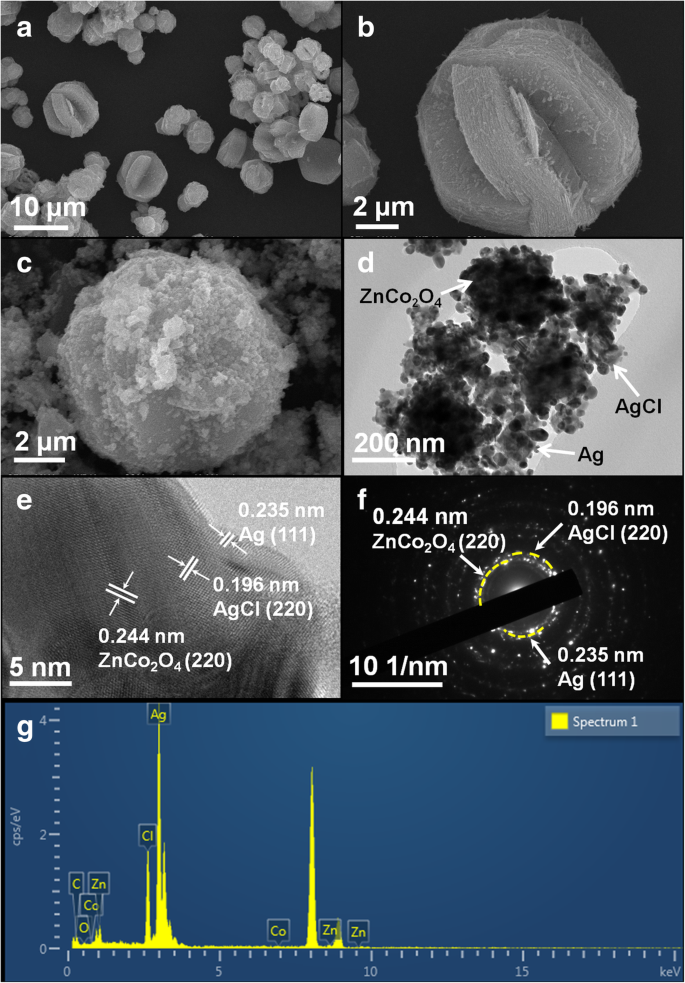
un , b Imágenes SEM del ZnCo 2 O 4 microesferas. c - e Imágenes SEM, TEM y HRTEM de Ag @ AgCl / ZnCo 2 O 4 microesferas. f , g SAED y los patrones de EDS correspondientes de Ag @ AgCl / ZnCo 2 O 4
Se utilizó espectroscopia de fotoelectrones de rayos X (XPS) para determinar la composición y valencia química de los productos. Como se muestra en la Fig. 3, la Fig. 3a es una exploración de espectro completo del producto. Puede verse que el producto contiene seis elementos, a saber, Zn, Co, O, Ag, Cl y C, de los cuales C es la base. La Figura 3b muestra los espectros de emisión de Zn 2p. Aparecen dos picos principales a 1045 eV y 1022 eV, correspondientes a los picos regionales de Zn 2p 1/2 y Zn 2p 3/2 [25, 26]. Puede verse que el pico de Zn 2p 3/2 cerca de 1022 eV es un solo pico, que es un estado de oxidación típico de Zn 2+ . La Figura 3c muestra los picos XPS de Co, que corresponden a los picos regionales de Co 2p 1/2 y Co 2p 3/2 a 781,4 eV y 796,9 eV, y los picos de satélite obvios observados a 785,2 eV son picos característicos de Co 3+ estado de oxidación [27]. La figura 3d son los espectros XPS de O1. Los picos asimétricos se pueden dividir en dos grupos de picos característicos con energías de unión de 530,5 eV y 535,01 eV, respectivamente. Estos dos grupos de picos característicos corresponden al oxígeno en la espinela ZnCo 2 O 4 red y las moléculas de agua o grupos · OH adsorbidos en la superficie del material [28]. Los espectros XPS de las órbitas de Ag 3d se muestran en la Fig. 3e. Las energías de unión de Ag 3d a 367,3 eV y 373,5 eV corresponden a las órbitas de escisión de espín de Ag 3d 5/2 y Ag 3d 3/2 , respectivamente [29]. Las órbitas de división de giro de Ag 3d 5/2 se puede descomponer aún más en picos de 368,0 eV y 366,8 eV mediante el software de división de picos. De manera similar, las órbitas de división de giro de Ag 3d 3/2 se puede descomponer en picos de 374,0 eV y 372,6 eV, de los cuales 368,0 eV y 374,6 eV pertenecen a Ag 0 , mientras que 366,8 eV y 372,6 eV pertenecen a Ag + , lo que indica que se forman AgCl y Ag en el catalizador. La Figura 3f es el diagrama analítico XPS de Cl 2p, y la energía de enlace de electrones de Cl 2p aparece en 197,9 eV.
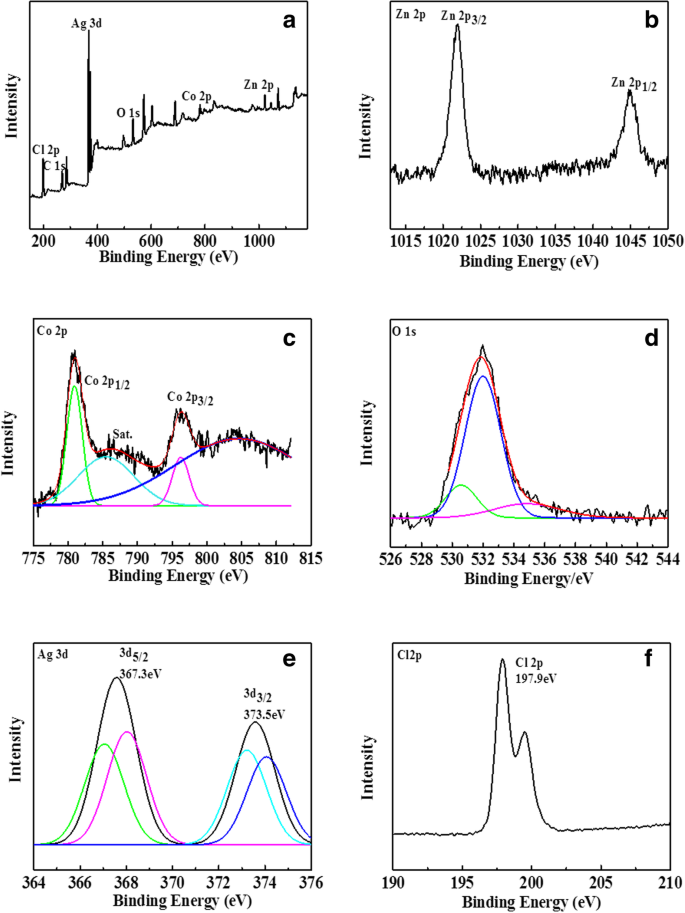
Espectro XPS de Ag @ AgCl / ZnCo 2 O 4 : a escaneo de la encuesta, b Zn 2p, c Co 2p, d O 1 s, e Ag 3d y f Cl 2p
Los espectros de absorción de reflectancia difusa UV-Vis de ZnCo 2 O 4 y 0.2Ag@AgCl/ZnCo 2 O 4 los catalizadores se compararon en la Fig. 4a, c. Los resultados mostraron que todas las muestras exhibieron una fuerte absorción en la región UV-Vis y 0.2Ag@AgCl/ZnCo 2 O 4 tiene una capacidad de absorción más fuerte que ZnCo 2 O 4 . El ancho de banda prohibido de ZnCo 2 O 4 y Ag @ AgCl / ZnCo 2 O 4 catalizadores se calcula de acuerdo con la fórmula de Kubelka-Munk [30]:
$$ \ mathrm {A} hv =\ mathrm {c} {\ left (hv- \ mathrm {Eg} \ right)} ^ n $$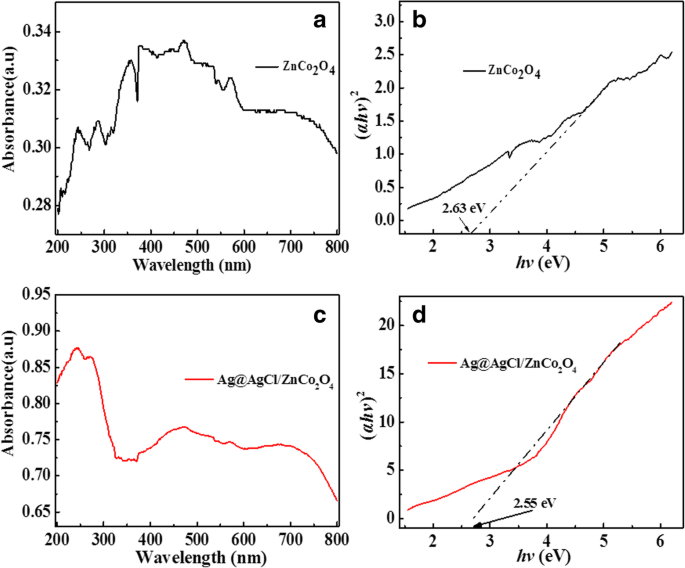
un Espectros de reflectancia difusa UV-Vis de ZnCo 2 O 4 . b Gráficas de ( αhv ) 2 versus energía ( hv ) para la energía de banda prohibida de ZnCo 2 O 4 . c Espectros de reflectancia difusa UV-Vis de 0.2Ag@AgCl/ZnCo 2 O 4 . d Gráficas de ( αhv ) 2 versus energía ( hv ) para la energía de banda prohibida de 0.2Ag@AgCl/ZnCo 2 O 4
Entre ellos, A es el coeficiente de absorción, h es la constante de Planck, v es la frecuencia de la luz, c es la constante, Eg es el ancho de banda prohibida y n es el coeficiente constante, para semiconductores directos, n =1/2, para semiconductores indirectos, n =2.
La Figura 4b, d muestra la energía de la banda prohibida ( αhv ) 2 y energía ( hv ) diagramas de ZnCo 2 O 4 y Ag @ AgCl / ZnCo 2 O 4 catalizadores. Los anchos de banda prohibida son 2,63 eV y 2,55 eV, respectivamente. Comparado con ZnCo 2 O 4 , Ag @ AgCl / ZnCo 2 O 4 Los catalizadores tienen una banda prohibida estrecha y la luz visible los excita más fácilmente para producir radicales libres, por lo que se espera que el rendimiento fotocatalítico de Ag @ AgCl / ZnCo2O4 sea mejor.
La superficie específica es uno de los factores importantes para la actividad de los fotocatalizadores. El área de superficie específica y la distribución del tamaño de los poros de ZnCo 2 O 4 y 0.2Ag@AgCl/ZnCo 2 O 4 las muestras fueron obtenidas por N 2 medición isotérmica de adsorción-desorción. Las curvas obtenidas se muestran en la Fig. 5. El N 2 Las isotermas de adsorción-desorción de las dos muestras mostraron obvios bucles de histéresis y pertenecían a isotermas de tipo IV, lo que demostró que las microesferas compuestas por nanoláminas tenían estructura mesoporosa. La formación de ZnCo 2 mesoporoso O 4 Las microesferas se atribuyeron principalmente a los vacíos formados durante el autoensamblaje de nanohojas y al apilamiento aleatorio de nanopartículas durante la carga de Ag @ AgCl. Las áreas de superficie específicas BET de ZnCo 2 O 4 y Ag @ AgCl / ZnCo 2 O 4 las muestras se midieron con N 2 método de adsorción. Las áreas de superficie específicas BET de las muestras son 9,977 m 2 / gy 11,67 m 2 / g, respectivamente. Los resultados muestran que el área de superficie específica de ZnCo 2 O 4 las microesferas se pueden aumentar cargando Ag @ AgCl, lo que se debe principalmente a la gran superficie específica de las nanopartículas de Ag @AgCl con un diámetro de 50 a 100 nm. Una gran superficie específica no solo puede hacer que el material tenga un mejor rendimiento de adsorción, sino que también proporciona sitios más activos y facilita la transferencia de portadores de carga, lo que es útil para promover aún más el rendimiento fotocatalítico del material.
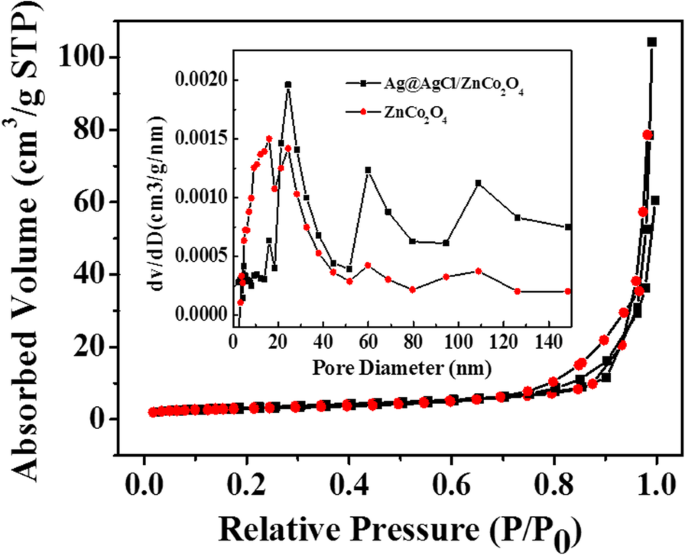
Isotermas de adsorción-desorción de nitrógeno y distribución del tamaño de poro de ZnCo 2 O 4 y 0.2Ag@AgCl/ZnCo 2 O 4 muestras
Además, las curvas de las ramas de desorción del N 2 Las isotermas de adsorción-desorción de las dos muestras se han calculado mediante el modelo de Barrett-Joyner-Halender (BJH). Las curvas de distribución del tamaño de los poros de las muestras se muestran en el inserto de la Fig. 5. Las curvas de distribución del tamaño de los poros muestran que la distribución del tamaño de los poros de ZnCo 2 O 4 es principalmente a 15,96 nm, mientras que el de Ag @ AgCl / ZnCo 2 O 4 es principalmente a 24,47 nm. Dicha estructura de poros es muy propicia para la adsorción de reactivos, el transporte de productos y la captura de fotoenergía, mejorando así las propiedades fotocatalíticas de los materiales.
Para estudiar la actividad fotocatalítica de las muestras preparadas, se llevaron a cabo experimentos de degradación de RhB bajo luz visible. El cambio de RhB durante la degradación fotocatalítica de 0.2Ag@AgCl/ZnCo 2 O 4 se analizó mediante barrido de longitud de onda completa UV-Vis. Los resultados se muestran en la Fig. 6a. El pico de absorción de RhB está cerca de 553 nm, que es la absorción característica del enlace azo en la molécula de RhB, es decir, el grupo cromogénico de la molécula de tinte RhB. A medida que avanzaba el tiempo de reacción, la intensidad máxima a 553 nm se hacía cada vez más baja, lo que indicaba que el grupo cromóforo de RhB se destruía bajo la acción del fotocatalizador. Después de 120 min de irradiación, la molécula de RhB se decoloró por completo y la intensidad máxima a 550 nm era casi cero, lo que indica que la estructura azoica del colorante RhB se había destruido por completo. Además, durante el proceso de degradación, la forma del pico de absorción de la molécula de RhB cambió ampliamente y apareció un ligero desplazamiento azul del pico, lo que indicó que se produjeron algunos intermedios moleculares pequeños durante el proceso de degradación.
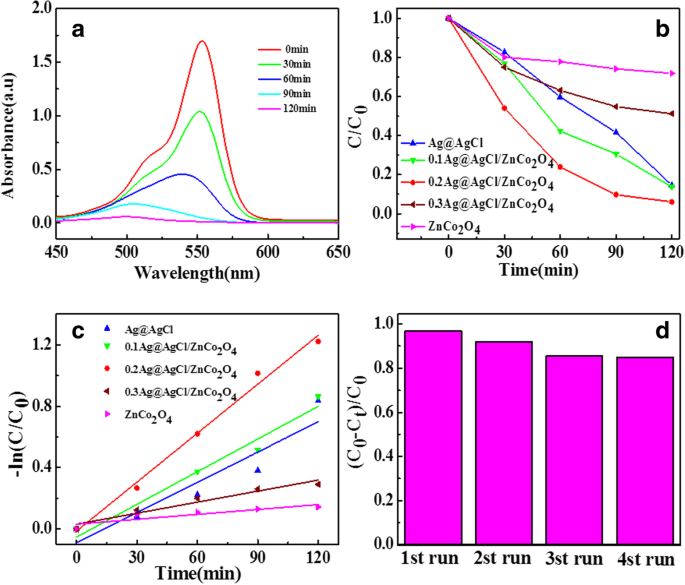
un Patrón de escaneo de luz visible de 0.2Ag@AgCl/ZnCo 2 O 4 degradación de RhB. b Efectos de diferentes catalizadores sobre la degradación fotocatalítica de RhB bajo luz visible. c Gráficos de ajuste cinético de primer orden para la degradación de RhB por diferentes catalizadores. d Ciclos de carreras de 0.2Ag@AgCl/ZnCo 2 O 4 microesferas para la degradación de RhB
Como se muestra en la Fig. 6b, el proceso de degradación fotocatalítica de RhB sobre ZnCo 2 O 4 , 0.1Ag@AgCl/ZnCo 2 O 4 , 0.2Ag@AgCl/ZnCo 2 O 4 , 0.3Ag@AgCl/ZnCo 2 O 4 , y se investigaron los catalizadores Ag @ AgCl. Se analizan y comparan los rendimientos fotocatalíticos de diferentes catalizadores. Los resultados indican que el ZnCo 2 puro O 4 La degradación fotocatalítica fue la peor y la tasa de degradación fotocatalítica durante 120 min fue solo del 28%. La tasa de degradación fotocatalítica de 0.3Ag@AgCl/ZnCo 2 O 4 en 120 min es 48,8%. La tasa de degradación fotocatalítica de 0.1Ag@AgCl/ZnCo 2 O 4 en 120 min se ve que es 85,4%, que está muy cerca de la tasa de degradación fotocatalítica de Ag @ AgCl 86,3%. Los resultados indican que en 120 min, 99,4% de degradación fotocatalítica de 0,2Ag@AgCl/ZnCo 2 O 4 tiene lugar y RhB se encuentra completamente degradado. Los resultados experimentales muestran que Ag @ AgCl puede mejorar eficazmente el rendimiento de degradación fotocatalítica de ZnCo 2 O 4 fotocatalizador.
Para estudiar el modelo cinético de reacción fotocatalítica de diferentes catalizadores, la Fig. 6c se obtuvo a partir de la ecuación –ln (C / C 0 ) =Kt. Es evidente en el gráfico que ( C / C 0 ) se correlaciona linealmente con el tiempo de reacción t y k es la constante de velocidad de reacción aparente, que indica que la degradación fotocatalítica de RhB sigue un modelo cinético de pseudoprimer orden. Como se muestra en la Tabla 1, el k Los valores de cada muestra se calcularon después del ajuste lineal de la curva. Como se muestra en la Tabla 1, las constantes de velocidad de reacción de ZnCo 2 O 4 , 0.1Ag@AgCl/ZnCo 2 O 4 , 0.2Ag@AgCl/ZnCo 2 O 4 , 0.3Ag@AgCl/ZnCo 2 O 4 y Ag @ AgCl son 0,00107 min −1 , 0,0071 min −1 , 0,01063 min −1 , 0,00239 min −1 y 0,00657 min −1 , respectivamente. Entre ellos, la constante de velocidad de reacción de 0.2Ag@AgCl/ZnCo 2 O 4 es el más grande, 0,01063 min −1 , 1,6 veces Ag @ AgCl y 10 veces el valor mínimo de ZnCo 2 O 4 . Esto muestra que el compuesto de Ag @ AgCl y ZnCo 2 O 4 puede soportar Ag @ AgCl en la superficie de ZnCo 2 O 4 y promover la dispersión de Ag @ AgCl, que puede aumentar el área de superficie específica del catalizador y proporcionar sitios más activos para mejorar la actividad fotocatalítica de los sustratos.
La estabilidad del catalizador es un factor importante para su aplicación práctica. La Figura 6d son los resultados de la prueba de estabilidad de 0.2Ag@AgCl/ZnCo 2 O 4 reciclado cuatro veces. Puede verse en la Fig. 6d que el efecto de degradación del catalizador no tiene ningún cambio evidente después de cuatro reciclados. La tasa de degradación de la muestra disminuye del 99,4 al 85%. La disminución de la tasa de degradación puede deberse a la pequeña cantidad de catalizador que se pierde durante cada ciclo. La pérdida de catalizador puede reducirse mediante centrifugación a alta velocidad durante el lavado. En resumen, la estabilidad de 0.2Ag@AgCl/ZnCo 2 O 4 sigue siendo muy bueno si se permiten las condiciones experimentales sin pérdida de catalizador, por lo que 0.2Ag@AgCl/ZnCo 2 O 4 como nuevo tipo de fotocatalizador visible tiene un gran valor y potencial para la producción práctica.
Para comprender los factores activos en el Ag @ AgCl / ZnCo 2 O 4 Se exploró la degradación fotocatalítica del proceso RhB, el experimento de captura fotocatalítica. Aquí, radicales hidroxilo (· OH), aniones superóxido (O · - 2 ) y agujeros (h + ) se apagan añadiendo 1 mmol de isopropanol (IPA), p-benzoquinona (BQ) y trietanolamina (TEOA), respectivamente. La Figura 7 muestra el efecto de la captura de diferentes factores activos sobre la velocidad de reacción en el proceso de reacción fotocatalítica. Puede verse en el gráfico que la tasa de degradación de RhB es casi no menor que la de RhB después de agregar 1 mmol de IPA durante 30 min. Después de agregar BQ o TEOA, el grado de degradación de RhB disminuyó mucho, especialmente cuando se agregó TEOA, la tasa de degradación fue cercana a cero. Por tanto, podemos inferir que los principales factores activos de Ag @ AgCl / ZnCo 2 O 4 fotocatalizador son aniones superóxido (O · - 2 ) y agujero (h + ), no radical hidroxilo (· OH).
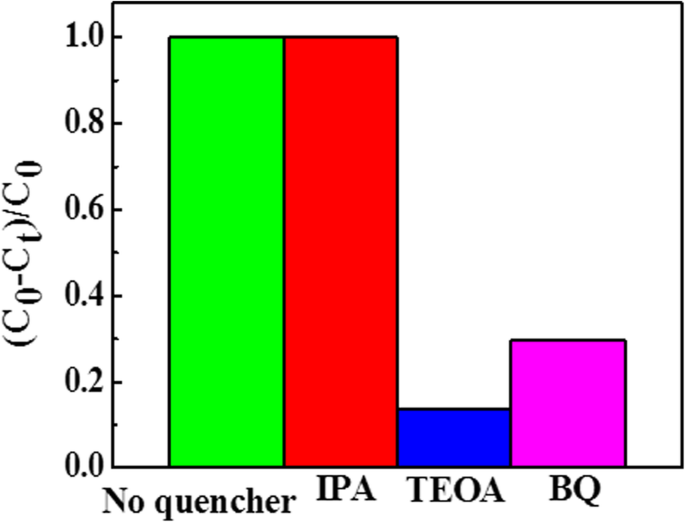
Experimentos de captura de especies activas durante la reacción fotocatalítica
Con base en los resultados experimentales y los estudios teóricos, propusimos un mecanismo de esquema Z para la degradación fotocatalítica RhB. Como se muestra en el Esquema 1, nanopartículas de Ag y ZnCo 2 O 4 las microesferas se excitaron para generar pares de electrones-huecos fotogenerados bajo irradiación de luz visible. Los electrones de las nanopartículas de Ag se transfieren a la banda conductora de AgCl y O 2 adsorbido en la superficie de AgCl atrapa los electrones para producir O · - 2 , mientras que los huecos fotogenerados permanecen en la banda de valencia de las nanopartículas de Ag. Para ZnCo 2 O 4 , el área de superficie relativamente específica es grande y la capacidad de adsorción es fuerte, lo que puede proporcionar más sitios de adsorción para contaminantes. Los contaminantes adsorbidos se pueden transferir al centro de degradación de la superficie del catalizador para la degradación de los contaminantes. La banda prohibida de ZnCo 2 O 4 es 2,63 eV. Los niveles de energía de la banda de conducción y la banda de valencia de ZnCo 2 O 4 son ca. - 1,98 eV y 0,65 eV (frente a NHE), respectivamente [31]. Muestra que los agujeros fotogenerados en la banda de valencia de ZnCo 2 O 4 no están directamente involucrados en la degradación del contaminante objetivo, principalmente porque la energía de los agujeros fotogenerados es 0,65 eV (frente a NHE) menor que la energía potencial de reacción (E (OH - / · OH) =1,99 eV (frente a NHE)). Mientras que los electrones fotogenerados en el ZnCo 2 O 4 transferencia de banda de conducción a nanopartículas de Ag por la barrera de Schottky y recombinarse con los agujeros fotogenerados que quedan en las nanopartículas de Ag. Como el ancho de banda prohibida de AgCl es 3,25 eV, los niveles de energía de la banda de conducción y de la banda de valencia de AgCl son aprox. - 0,09 eV y 3,16 eV (frente a NHE) respectivamente, que no pueden excitarse con luz visible; Los electrones fotogenerados en las nanopartículas de Ag se transfieren a la banda de conducción de AgCl y participan en la degradación de los contaminantes objetivo, principalmente porque la energía de los electrones fotogenerados - 0.09 eV (frente a NHE) es más negativa que la energía potencial de reacción en O 2 / O · - 2 (E (O 2 / O · - 2 ) =- 0,0 46 eV (frente a NHE)) [32]. Los agujeros fotogenerados en la banda de valencia de ZnCo 2 O 4 se transfieren a la superficie de AgCl y se combinan con Cl - en AgCl para formar Cl · radicales. Cl · Los radicales se oxidan fuertemente y pueden degradar el RhB de manera efectiva y mineralizarse en pequeñas moléculas inorgánicas como CO 2 y H 2 O, y se reduce a Cl - . Estos Cl - luego se combinan con Ag + para regenerar AgCl para asegurar la estabilidad del sistema. Los resultados son consistentes con el experimento de extinción. En el proceso de degradación fotocatalítica de Ag @ AgCl / ZnCo 2 O 4 , los principales factores activos son el anión superóxido (O · - 2 ) y agujero (h + ), no radical hidroxilo (· OH).
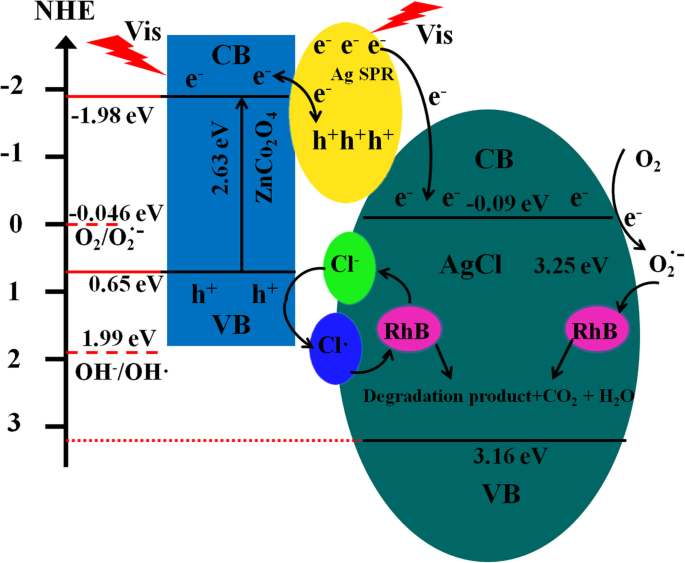
Ilustración esquemática del mecanismo fotocatalítico de Ag @ AgCl / ZnCo 2 O 4 microesferas
En resumen, la formación, migración y transformación de pares de agujeros de electrones fotoinspirados y las vías de degradación final de los contaminantes durante la reacción fotocatalítica se resumen a continuación:
- (1)
Generación de pares de agujeros de fotoelectrones:
- (2)
Migration and transformation of photogenerated hole electron pairs:
- (3)
Degradation of pollutants:
Conclusiones
In summary, the composite Ag@AgCl/ZnCo2 O 4 microspheres photocatalyst was prepared by a facile two-step method and characterized by a set of complementary structural and electronic characterization tools such as X-ray diffraction (XRD), scanning electron microscopy (SEM), energy dispersive X ray spectroscopy (EDX), transmission electron microscopy (TEM), high-resolution transmission electron microscopy (HR-TEM), selected area electron diffraction (SAED), X-ray photoelectron spectroscopy (XPS), UV-Vis diffuse reflectance spectroscopy (DRS), and Brunauer-Emmett-Teller (BET). Present results show that the composite photocatalyst has good crystal morphology, is highly crystalline, and the absorption intensity of Ag@AgCl/ZnCo2 O 4 composite photocatalyst in the whole spectrum range is higher than that of pure ZnCo2 O 4 . The specific surface area of Ag@AgCl/ZnCo2 O 4 composite photocatalyst and the adsorption efficiency of RhB are found to increase as a result of Ag@AgCl deposition. In the degradation system of RhB, the photocatalytic degradation of pure ZnCo2 O 4 was the worst and the photocatalytic degradation rate for 120 min is found to have a very low value of 28%. The photocatalytic degradation rate of Ag@AgCl for 120 min is seen to be 86.3%. The results indicate that within 120 min, 99.4% photocatalytic degradation of 0.2Ag@AgCl/ZnCo2 O 4 takes place and RhB is found to be completely degraded. The reaction rate constant of 0.2Ag@AgCl/ZnCo2 O 4 composite photocatalyst is the highest showing a value of 0.01063 min −1 , which is 1.6 times that of Ag@AgCl and 10 times of the minimum value of ZnCo2 O 4 . In the reaction system of Ag@AgCl/ZnCo2 O 4 , the main active factors of Ag@AgCl/ZnCo2 O 4 photocatalyst are found to be superoxide anion (O ·− 2 ) and hole (h + ) and not hydroxyl radical (·OH). The photocatalytic mechanism of composite Ag@AgCl/ZnCo2 O 4 photocatalyst for the RhB degradation can be explained by a plasmonic Z-scheme photocatalytic mechanism, where the photogenerated electrons from the ZnCo2 O 4 conduction band at the contact interface of composite photocatalyst Ag@AgCl/ZnCo2 O 4 transfer to Ag nanoparticles by the Schottky barrier and recombine with photogenerated holes left on the Ag nanoparticles.
Abreviaturas
- APUESTA:
-
Brunauer-Emmett-Teller
- BQ:
-
p-Benzoquinone
- DRS:
-
UV-Vis diffuse reflectance spectroscopy
- EDX:
-
Energy dispersive X ray spectrometer
- HR-TEM:
-
Microscopía electrónica de transmisión de alta resolución
- IPA:
-
Isopropanol
- RhB:
-
Rodamina B
- SAED:
-
Difracción de electrones de área seleccionada
- SEM:
-
Microscopía electrónica de barrido
- SPR:
-
Resonancia de plasmón superficial
- TEM:
-
Microscopía electrónica de transmisión
- TEOA:
-
Triethanolamine
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X
Nanomateriales
- Preparación y actividad de hidrogenación catalítica mejorada de nanopartículas de Sb / Palygorskita (PAL)
- Actividades fotocatalíticas mejoradas por nanopartículas au-plasmónicas en un fotoelectrodo de nanotubos de TiO2 recubierto con MoO3
- Rendimiento fotocatalítico de luz visible de nanocompuestos de ZnO / g-C3N4 dopado con N
- Un nuevo fotocatalizador de heterounión Bi4Ti3O12 / Ag3PO4 con rendimiento fotocatalítico mejorado
- Efectos sinérgicos de nanopartículas de Ag / BiV1-xMoxO4 con actividad fotocatalítica mejorada
- Síntesis en un solo recipiente de nanoplacas de Cu2ZnSnSe4 y su actividad fotocatalítica impulsada por la luz visible
- Evolución mejorada del hidrógeno fotocatalítico mediante la carga de Cd0.5Zn0.5S QD en nanohojas porosas de Ni2P
- Crecimiento in situ de nanocristales de sulfuro metálico en películas de éster metílico de poli (3-hexiltiofeno):[6,6] -fenilo C61-butírico para Células solares híbridas invertidas con fotocorr…
- Síntesis fácil y actividad fotocatalítica de luz visible mejorada de nuevos compuestos de heterounión p-Ag3PO4 / n-BiFeO3 para la degradación del tinte
- Propiedades fotocatalíticas sensibles a la luz visible mejoradas de los compuestos de nanohojas Ag / BiPbO2Cl
- Síntesis in situ de fotocatalizadores BiOBr0.3I0.7 / Ag / AgI de esquema Z totalmente de estado sólido con actividad fotocatalítica mejorada bajo irradiación de luz visible



