Fabricación de microesferas huecas de TiO2 promovidas por CdTe QD / BiOI con un rendimiento fotocatalítico superior bajo la luz solar simulada
Resumen
Las arquitecturas huecas y heteroestructuradas se reconocen como un enfoque eficaz para mejorar el rendimiento fotocatalítico. En este trabajo, el ternario TiO 2 / CdTe / BiOI con estructura hueca se construyó mediante un método paso a paso. Además, el efecto de TiO 2 Regulación estructural y alineación de bandas de energía de puntos cuánticos de BiOI y CdTe (CdTe QD) con TiO 2 en TiO 2 También se estudiaron / CdTe / BiOI sobre la eliminación de colorantes fotocatalíticos. Los resultados revelan que el TiO 2 / CdTe / BiOI heteroestructuras con sustratos huecos exhiben actividades fotocatalíticas mucho más altas que el TiO 2 puro , P25, TiO 2 / CdTe y TiO 2 / BiOI y TiO ternario 2 / CdTe / BiOI con sustratos sólidos. Para TiO 2 (H) / CdTe / BiOI, varios factores sinérgicos pueden ser responsables del notable rendimiento de la fotodegradación de la luz visible, como una fuerte absorción de la luz visible por BiOI y una mayor superficie específica.
Antecedentes
Debido al ahorro de energía y los méritos ecológicos, la fotocatálisis de semiconductores ha atraído un interés creciente en la conservación del medio ambiente. Los fotocatalizadores se pueden utilizar en varios aspectos, como la autolimpieza, el tratamiento del agua, la purificación del aire y los antibacterianos [1, 2]. Entre ellos, debido a las ventajas de bajo costo, excelente estabilidad y no toxicidad [3], el dióxido de titanio (TiO 2 ) ha sido ampliamente investigado. Sin embargo, solo puede utilizar una pequeña porción del espectro solar debido a su amplio intervalo de banda y a la recombinación de carga relativamente rápida, lo que limita la eficiencia de la fotoconversión [4].
Con el fin de mejorar la eficacia fotocatalítica de la luz visible de la titania, se han adoptado varias estrategias que incluyen el dopaje iónico, la carga de metales nobles, la construcción de heterouniones y la sensibilización [5,6,7,8]. Entre estas estrategias, se supone que la heterounión formada por el acoplamiento con semiconductor de banda prohibida estrecha es uno de los métodos más efectivos para mejorar la respuesta a la luz visible y reducir la recombinación de carga simultáneamente [9].
Los oxihaluros de bismuto han atraído una atención considerable debido a su bajo costo, buena estabilidad y amplio rango de respuesta a la luz [10, 11], que tienen una estructura en capas isotrópicas con [Bi 2 O 2 ] 2+ capas intercaladas por X - iones (X =F, Cl, Br, I) [12]. Entre los oxihaluros de bismuto, BiOI con la banda prohibida más pequeña (1,72–1,9 eV) [13] ha demostrado ser un fotocatalizador de luz visible eficaz para la degradación de RhB [14] y MO [15]. El campo eléctrico interno entre el [Bi 2 O 2 ] 2+ y yo - Las capas pueden promover la separación de cargas fotoinducidas y mejorar la actividad fotocatalítica [16]. Aunque los potenciales de la banda de conducción y de la banda de valencia se encuentran entre los de TiO 2 , la heterounión de tipo II podría formarse mediante el acoplamiento de BiOI de tipo p y TiO de tipo n 2 juntos cuando los niveles de Fermi alcanzan el equilibrio, lo que hace que los electrones de la banda de conducción de BiOI migren a TiO 2 [17]. Hasta ahora, aunque se han dedicado muchos esfuerzos a desarrollar fotocatalizadores heteroestructurados binarios, la respuesta limitada a la luz visible y la eficiencia de separación de carga relativamente baja siguen siendo el obstáculo.
Para resolver los problemas mencionados anteriormente, se han desarrollado sistemas de heterounión multicomponente. El telururo de cadmio (CdTe), como importante semiconductor compuesto de tipo p II-VI, ha recibido mucha atención debido a su banda prohibida directa de 1,44 eV [18] y un gran coeficiente de absorción óptica en el espectro solar [19]. Los puntos cuánticos CdTe (CdTe QD) se han utilizado ampliamente para modificar varios semiconductores:Feng et al. [20] sintetizó el TiO 2 decorado con CdTe matrices de nanotubos mediante un método de electrodeposición por pulsos, y los resultados indicaron CdTe / TiO 2 matrices de nanotubos (CdTe / TiO 2 NTA) exhibieron propiedades fotocatalíticas sobresalientes que el TiO 2 desnudo NTA; Liu y col. [21] informó de la síntesis de nanocompuestos de CdTe / ZnO mediante un método de baño caliente, y los resultados mostraron que CdTe / ZnO debía una mejor actividad fotocatalítica para la rodamina B que el ZnO desnudo. Sin embargo, aparte de los fotocatalizadores heteroestructurados binarios, el TiO 2 ternario-heteroestructurado / BiOI modificado con CdTe QD puede presentar un rendimiento fotocatalítico fascinante y ser digno de ser estudiado más a fondo.
En el presente trabajo, CdTe QDs / TiO 2 modificado con BiOI se preparó para la aplicación fotocatalítica mediante un método de dos pasos, y TiO 2 sólido y hueco se aplicaron microesferas como precursores. Además, la evolución estructural de TiO 2 / CdTe / BiOI composites y el efecto sinérgico de CdTe y BiOI en el proceso fotocatalítico también se estudiaron en detalle.
Métodos
Materiales
Se adquirieron isopropóxido de titanio (TTIP, 97%) y nitrato de bismuto pentahidratado (AR, 99,0%) de Macklin Inc. Hemi-pentahidrato de cloruro de cadmio (CdCl 2 · 2.5H 2 O, 99,0%), telurito de sodio (Na 2 TeO 3 , 98,0%), N -acetilo- L -cisteína (98,0%), borohidruro de potasio (KBH 4 , 97%), hidróxido de sodio (NaOH, 96,0%), nitrato de potasio (KNO 3 , 99%), bromuro de potasio (KBr, 99%), ácido clorhídrico (HCl, 36–38%), peróxido de hidrógeno (H 2 O 2 , 30%), etilenglicol y etanol absoluto fueron todos de grado analítico y se compraron a Sinopharm Chemical Reagent Co., Ltd.
Síntesis de TiO 2 Microesferas sólidas y microesferas huecas
En un procedimiento típico, 0.8 mL de KNO 3 La solución (0,1 mol / L) se disolvió en 200 ml de etanol. Luego, se agregaron 4,4 ml de TTIP a la solución anterior y se agitó hasta que se generó un precipitado blanco. Añejada durante 12 h, la suspensión blanca obtenida se centrifugó y se lavó con agua desionizada y etanol varias veces, y el TiO 2 amorfo (TiO 2 · NH 2 O) podría obtenerse. Después de secarse más a 60 ° C durante 12 hy calcinarse a 450 ° C durante 2 h, TiO 2 microesferas sólidas (TiO 2 (S)) podría obtenerse.
En cuanto a TiO 2 microesferas huecas, se fabricaron mediante un proceso hidrotermal. Normalmente, TiO 2 · NH 2 O (200 mg) se dispersaron en 40 ml de 0,05% en peso de H2 2 O 2 y se agita durante 10 min. Luego, se disolvieron 480 mg de polvos de NaOH en la suspensión anterior, y la mezcla se transfirió a un autoclave revestido de teflón y se mantuvo a 180ºC durante 4 h. Los precipitados se recogieron y luego se sumergieron en ácido clorhídrico (0,1 mol / L). Después de lavarse con agua desionizada varias veces, los resultantes se secaron y calcinaron como en el procedimiento anterior y, por lo tanto, TiO 2 microesferas huecas, etiquetadas como TiO 2 (H), se obtuvieron.
Síntesis de TiO 2 Esferas modificadas con CdTe QDs
TiO 2 Los polvos (2,0 g) se dispersaron en 40 mL de agua desionizada y luego, 97,9 mg de N -acetilo- L -cisteína, 114,2 mg de CdCl 2 · 2.5H 2 O, y 178 mg de KBH 4 posteriormente se añadieron a la mezcla a intervalos de 30 minutos. Posteriormente, 10 mL de Na 2 TeO 3 (0,01 mol / L) se añadió una solución acuosa a la mezcla anterior con 5 ml / min. Luego, la temperatura del sistema se elevó a 100 ° C en 30 min y se calentó a reflujo durante 6 h. Finalmente, los productos se lavaron con agua y alcohol etílico varias veces y se secaron a 60 ° C durante 12 h, y los productos se etiquetaron como TiO 2 / CdTe .
Fabricación de TiO 2 / CdTe / BiOI Ternary Composites
Brevemente, TiO 2 Los polvos de CdTe (258 mg) obtenidos anteriormente se dispersaron en 10 ml de EG, formando una suspensión blanca. Posteriormente, un Bi (NO 3 ) 3 solución preparada disolviendo 627,6 mg de Bi (NO 3 ) 3 en 28 ml de EG se vertió en la suspensión anterior en 15 min. Luego, se vertió una solución que contenía 214,8 mg de KI y 24 ml de EG en la mezcla anterior. Después de agitar durante 1 h, se transfirió una solución amarilla al autoclave revestido de teflón y se mantuvo a 80ºC durante 3 h. Los precipitados resultantes se recogieron, se lavaron suficientemente con etanol y agua desionizada y se secaron, que se etiquetaron como TiO 2 / CdTe / BiOI.
TiO binario 2 / Las heteroestructuras de BiOI se obtuvieron mediante un procedimiento similar al agregar un solo componente TiO 2 en la solución anterior.
Caracterización
Los patrones de difracción de rayos X (XRD) se obtuvieron en un difractómetro de rayos X Rigaku D-MAX2500 equipado con radiación Cu Kα. La microscopía electrónica de barrido (SEM) se obtuvo usando un microscopio electrónico de barrido por emisión de campo JSM-6700F (JEOL, Japón). Se obtuvieron imágenes de microscopía electrónica de transmisión (TEM) de las muestras en un microscopio JEM-2100 (JEOL, Japón) a un voltaje de aceleración de 200 kV. Las isotermas de adsorción / desorción de nitrógeno se midieron a 77 K usando un analizador de área de superficie y tamaño de poro (NOVA 1000e, Quantachrome Instruments), y se aplicó el método Brunauer-Emmett-Teller (BET) para evaluar el área de superficie específica. El análisis de espectroscopía de fotoelectrones de rayos X (XPS) se realizó en un XSAM800 (Kratos Corporation, Reino Unido) con una fuente de rayos X acromática de Al Kα (1486,6 eV). Los espectros de absorción óptica y los espectros de reflexión difusa (DRS) se obtuvieron utilizando un espectrofotómetro ultravioleta-visible (CARY500UV, Varian). Los espectros de fotoluminiscencia se registraron usando Shimadzu RF-5301 con una longitud de onda de excitación de 365 nm. La fotocorriente transitoria se analizó en una estación de trabajo electroquímica (CHI760E, Shanghai Chenhua, China) con un sistema estándar de tres electrodos que usaba vidrio FTO depositado con catalizador como electrodo de trabajo, Pt como contraelectrodo y SCE como electrodo de referencia en el electrolito de 0,5 M Na 2 SO 4 .
Rendimiento fotocatalítico
Se probó la actividad fotocatalítica de los compuestos sintetizados basándose en la degradación del naranja de metilo (MO), utilizando una lámpara de arco Xe de 500 W como fuente de luz. Aquí, se agregó una cantidad de 140 mg de fotocatalizadores a 50 ml de solución de MO (5 mg / L) tomados en un vaso de precipitados de cuarzo. Antes de la iluminación, la suspensión se agitó durante 30 min en una cámara oscura para lograr el equilibrio de adsorción-desorción entre los fotocatalizadores y la solución de MO. Después, la mezcla se irradió durante 180 min y se tomaron muestras de una alícuota de 4 ml de solución a intervalos de 45 min. La mezcla se centrifugó a 8000 rpm durante 3 min para eliminar los catalizadores del sobrenadante. En la prueba de estabilidad del fotocatalizador, las muestras se lavaron con agua desionizada después de cada ciclo y luego se agregaron a una nueva solución de MO para el siguiente ciclo. La concentración residual de MO se controló con un espectrofotómetro UV-vis (CARY500UV, Varian) y el porcentaje de degradación se analizó cuantitativamente comparando la absorción máxima a 465 nm.
Generalmente, los agujeros (h + ), electrones (e - ), radicales superóxido (• O - 2 ), y los radicales hidroxilo (• OH) podrían producirse en el sistema fotocatalítico semiconductor bajo irradiación. Se llevó a cabo una prueba de eliminación de radicales para las especies activas fotoinducidas. El experimento de eliminación fue similar a las pruebas de descomposición fotocatalítica, donde la sal disódica del ácido etilendiaminotetraacético (EDTA-2Na, 2 mmol / L), bromato de potasio (KBrO 3 , 10 mmol / L), benzoquinona (BQ, 1 mmol / L) y alcohol isopropílico (IPA, 10 mmol / L) se utilizaron para eliminar el h + , e - , • O - 2 y • Especies reactivas con OH, respectivamente.
Resultados y discusiones
La Figura 1 presenta los patrones de difracción de rayos X de polvo de TiO 2 , TiO 2 / CdTe, TiO 2 / BiOI y TiO 2 / CdTe / BiOI. Se observa que TiO 2 Los picos característicos se pueden seleccionar en todas las muestras, y los picos con valores de 2θ a 25,5 °, 37,8 °, 48,8 °, 53,5 ° y 55,6 ° se pueden indexar a (101), (004), (200) y ( 105), (211) facetas de la anatasa (JCPDS # 84-1285) [22]. A partir de los patrones que se muestran en la Fig. 1c, d, los picos de difracción a 2θ de 29,7 °, 31,7 °, 45,5 ° y 51,3 ° se muestran además de los picos de TiO 2 , que es consistente con BiOI tetragonal (JCPDS # 73-2062) [23]. Sin embargo, los picos de BiOI son mucho más evidentes en TiO 2 / BiOI que los de TiO 2 / CdTe / BiOI. En cuanto a TiO 2 / CdTe (Fig. 1b), no se encuentran claramente otros picos en el patrón XRD además de TiO 2 , debido al pequeño tamaño de los cristales o una pequeña cantidad de dosis de CdTe QD.
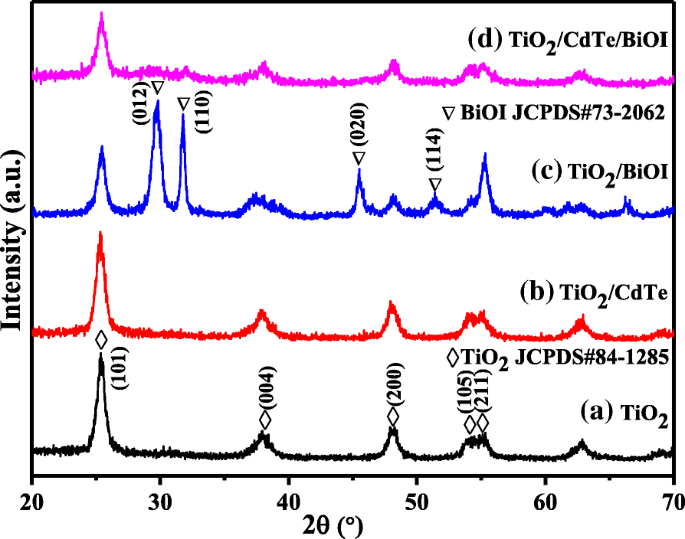
Patrones XRD de a desnudo TiO 2 , b TiO 2 / CdTe, c TiO 2 / BiOI y d TiO 2 / CdTe / BiOI
La morfología externa del TiO binario 2 / CdTe y ternario TiO 2 / CdTe / BiOI se caracteriza mediante SEM, como se muestra en la Fig. 2. La observación general de todos los TiO 2 Los compuestos a base de partículas exhiben una morfología esférica, con un diámetro de aproximadamente 200-400 nm, y BiOI en forma de escamas depositado en la superficie de TiO 2 esferas excepto TiO 2 / CdTe se muestra en la Fig. 2a. La imagen SEM de TiO 2 (S) / CdTe / BiOI que se muestra en la Fig. 2b muestra una situación similar a TiO 2 (S) / CdTe y TiO 2 Las esferas (S) están cubiertas por una gran cantidad de escamas de BiOI con morfologías relativamente regulares. Sin embargo, el caso es bastante diferente para TiO 2 (H) / CdTe / BiOI, en el que las partículas poseen una morfología no uniforme con varios tamaños y una superficie similar a una coliflor, como se muestra en la Fig. 2c, d. Además, las escamas de BiOI parecen ser más fáciles de unir en TiO 2 (H) / CdTe causado por una superficie rugosa originada por TiO 2 (H) y la estructura hueca prístina de TiO 2 La matriz (H) podría identificarse en la vista ampliada.

Imágenes SEM de a TiO 2 (S) / CdTe, b TiO 2 (S) / CdTe / BiOI y c - d TiO 2 (H) / CdTe / BiOI
Las imágenes TEM brindan más información sobre la evolución estructural del ternario TiO 2 / CdTe / BiOI, como se muestra en la Fig. 3. TiO 2 esférico sólido de tamaño uniforme y bien disperso se puede observar claramente en la Fig. 3a, y algunas partículas diminutas también se encuentran en la región. Espaciado de celosía de 0.238 nm y 0.33 nm correspondiente al plano (004) de TiO 2 y el plano (111) de CdTe se puede identificar en la Fig. 3b, lo que demuestra la formación de heterouniones entre TiO 2 esferas y QD de CdTe. Puede verse en la Fig. 3c que se adhirieron numerosas escamas a la superficie de TiO 2 esférico sólido , y la franja de la red era de 0,282 nm en la Fig. 3d, que está de acuerdo con la dirección [110] del cristal BiOI. Además, la ampliación de la interfaz también atestigua la existencia de escamas de CdTe QD y BiOI en TiO 2 (S) / CdTe / BiOI. En contraste, la Fig. 3e muestra el TiO 2 (H) / CdTe / BiOI que aparece en la morfología de esferas huecas agregadas sin granos aparentes en forma de escamas adheridos. El fenómeno implica que los componentes de BiOI probablemente consisten en partículas mucho más pequeñas que la enorme superficie de TiO 2 (H) esferas, que están compuestas por una gran cantidad de TiO 2 primario nanopartículas, descentraliza los sitios de nucleación. De manera similar, la vista ampliada de la interfaz confirma la presencia de TiO 2 ternario heteroestructurado Los compuestos (H) / CdTe / BiOI, como se muestra en la Fig. 3f, y el plano cristalino (111) de CdTe y (002) de BiOI se pueden encontrar claramente.

Imágenes TEM de a - b TiO 2 (S) / CdTe, c - d TiO 2 (S) / CdTe / BiOI y e - f TiO 2 (H) / CdTe / BiOI
La Figura 4 muestra las isotermas de adsorción / desorción de nitrógeno del ternario TiO 2 (S) / CdTe / BiOI y TiO 2 Heteroestructuras (H) / CdTe / BiOI. Ambas isotermas exhiben características similares de una isoterma de tipo IV, según la clasificación de la IUPAC [24]. Sin embargo, el TiO 2 (S) / CdTe / BiOI posee un bucle de histéresis de tipo H2 en el rango 0,4-0,8 [25], lo que indica la acumulación de TiO 2 uniforme granos por calcinación directa, mientras que TiO 2 (H) / CdTe / BiOI con un bucle de histéresis tipo H3 debido a los poros de replanteo se deriva de nanohojas hidrotermales o precursores de nanotubos [10], y los resultados están de acuerdo con imágenes SEM y TEM. Además, el área de superficie específica de TiO 2 (S) / CdTe / BiOI y TiO 2 (H) / CdTe / BiOI se calculó en 77,7 y 91,6 m 2 g −1 utilizando el método Brunauer-Emmett-Teller (BET). Una superficie relativamente mayor de TiO 2 Las microesferas (H) / CdTe / BiOI podrían proporcionar sitios más activos para la adsorción de moléculas reactivas, dando como resultado un rendimiento fotocatalítico más eficiente.
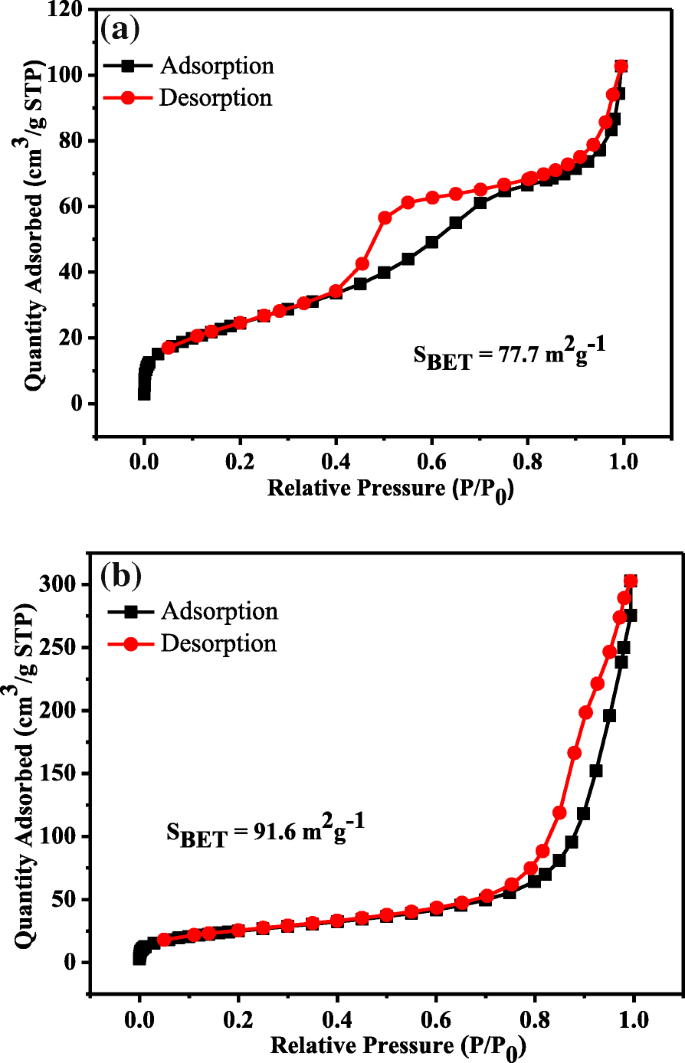
Isotermas de absorción-desorción de nitrógeno de a TiO 2 (S) / CdTe / BiOI y b TiO 2 (H) / CdTe / BiOI
Según la discusión anterior, la evolución de TiO 2 Las heteroestructuras de / CdTe / BiOI se pueden ilustrar mediante el esquema 1. Alternativamente, TiO 2 amorfo las microesferas también se pueden transformar en TiO 2 microesferas sólidas directamente mediante un sencillo procedimiento de calcinación. Durante el siguiente proceso hidrotermal, el TiO 2 preexistente / Las microesferas CdTe QD podrían actuar como sitios de nucleación para la cristalización de BiOI y, por lo tanto, el TiO 2 ternario Las heteroestructuras / CdTe / BiOI se forman simultáneamente. Es bien sabido que BiOI tiene una tasa de nucleación y una tasa de crecimiento intrínsecamente rápidas; como resultado, las partículas de BiOI con un tamaño relativamente grande y pocas cantidades se forman en el TiO 2 (S), en forma de escamas a medida que crece a lo largo de la dirección [110]. Sin embargo, en el caso de TiO 2 Las microesferas (H), que poseen una superficie más grande para la cristalización de BiOI, las partículas de BiOI tienden a existir en una forma que es relativamente pequeña en tamaño y abundante en cantidad. Por lo tanto, la morfología de la superficie de TiO 2 microesferas determina la forma y la forma de las partículas de BiOI, como sugirieron los resultados de SEM y TEM.
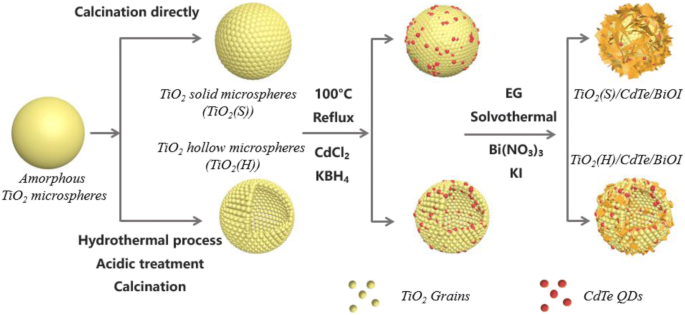
Evolución estructural de TiO 2 amorfo a TiO 2 / CdTe / Heteroestructuras BiOI
XPS se emplea para investigar los estados electrónicos de la superficie y la composición química de las muestras preparadas, y los resultados se muestran en la Fig. 5. Puede verse en el espectro de la encuesta XPS que el TiO 2 / CdTe / BiOI contiene elementos Ti, O, Bi, I, Cd y Te. La Figura 5b muestra que los picos en el espectro XPS de alta resolución de Ti 2p correspondientes a energías de enlace de 458,5 eV y 464,2 eV se atribuyen a Ti 2p 3/2 y Ti 2p 1/2 , que indicó un estado de oxidación de Ti (IV) [26], y la separación de energía de unión (BE) medida de 5,7 eV es consistente con TiO 2 [27]. Sin embargo, las energías de enlace de Ti 2p 1/2 y Ti 2p 3/2 para TiO 2 / CdTe y TiO 2 / CdTe / BiOI son 457,5 y 463,3 eV, respectivamente, y ambos tienen un cambio de aproximadamente 0,8 eV a la región de menor energía en comparación con el TiO 2 desnudo. , lo que demuestra una fuerte interacción entre CdTe y TiO 2 . El espectro del nivel del núcleo de O 1 s (Fig. 5c) en alrededor de 529.5 eV está asociado con la red O en el TiO 2 desnudo. muestras, que está relacionado con los enlaces Ti-O [28]. Merece mencionarse que un cambio hacia la energía de enlace más baja del pico de O 1 s en el TiO 2 / CdTe y TiO 2 / Las muestras de CdTe / BiOI indican pérdida de iones de oxígeno [27], que se puede atribuir a la oxidación parcial de CdTe en TiO 2 . Este resultado encaja bien con el cambio de Ti 2p e implica la formación de la interfaz entre TiO 2 , BiOI y CdTe en heterounión. El Te 3d 5/2 Los espectros (Fig. 5e) revelan dos estados de telurio en BE de 564,1 eV y 577,1 eV, respectivamente, que son característicos de CdTe.
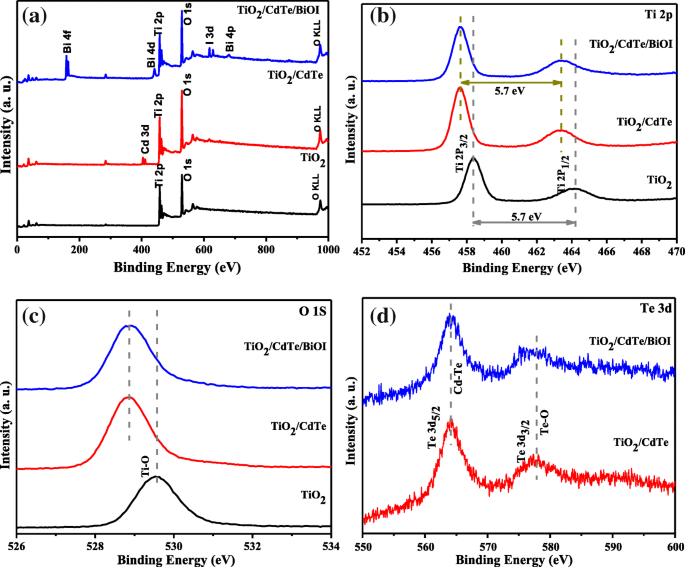
un Espectro de escaneo XPS de las muestras de TiO 2 , TiO 2 / CdTe, TiO 2 / CdTe / BiOI. b - d Espectros XPS de alta resolución de Ti, O y Te
Como se supone que las propiedades de adsorción óptica son críticas para los semiconductores de componentes múltiples, los espectros de absorción óptica de TiO 2 (S), TiO 2 (S) / CdTe, TiO 2 (S) / BiOI, TiO 2 (S) / CdTe / BiOI y TiO 2 (H) / CdTe / BiOI se muestran en la Fig. 6a. El TiO 2 preparado muestra una tendencia similar a la P25 comercial, lo que sugiere una característica típica de respuesta ultravioleta. En cuanto a los compuestos binarios y ternarios, el TiO 2 (S) / CdTe / BiOI posee una absorción mucho más obvia en la región visible que TiO 2 (S) / CdTe y TiO 2 (S) / BiOI, que refleja una conexión mejorada entre los componentes mediante la carga de CdTe QD. Y la absorción de TiO 2 (S) / CdTe / BiOI en el rango visible es un poco más débil que el de TiO 2 (H) / CdTe / BiOI; atribuimos este fenómeno al efecto dispersivo del TiO 2 de estructura hueca microesferas como se discutió anteriormente. La imagen insertada muestra los gráficos Tauc de (Ahv) 1/2 versus el hv de muestras. La banda prohibida de TiO 2 (S), TiO 2 (S) / CdTe / BiOI y TiO 2 (H) / CdTe / BiOI se estiman extrapolando la línea recta al eje de abscisas y se estiman en 3,02 eV, 2,57 eV y 2,45 eV, respectivamente. Vale la pena señalar que TiO 2 (S) / CdTe / BiOI muestra una pequeña protuberancia diferente a TiO 2 (H) / CdTe / BiOI, independientemente del cambio azul en 0,12 eV, lo que sugiere una distribución no uniforme de partículas grandes de BiOI como los resultados de SEM implicados anteriormente.
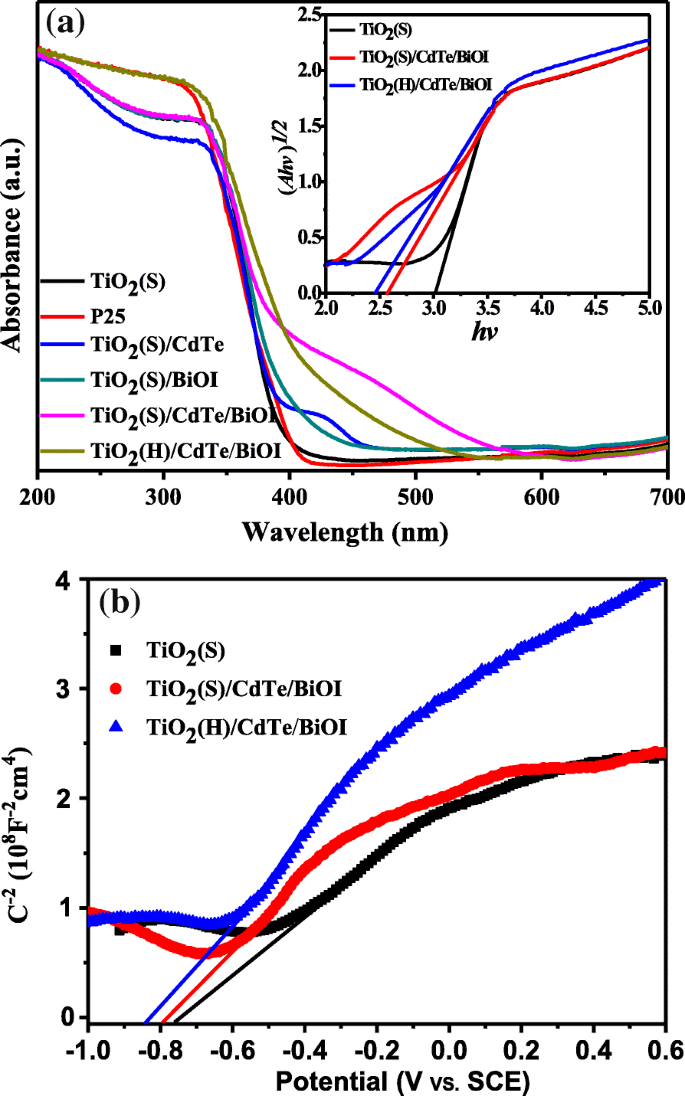
un Espectros de reflectancia difusa UV-Vis de todas las muestras y los correspondientes gráficos de Tauc de TiO 2 (S), TiO 2 (S) / CdTe / BiOI y TiO 2 Muestras (H) / CdTe / BiOI. b Mott-Schottky traza en 0,5 M Na 2 SO 4 a una frecuencia de 1 KHz de TiO 2 (S), TiO 2 (S) / CdTe / BiOI y TiO 2 (H) / CdTe / BiOI samples
Para comprender mejor las propiedades electrónicas y la estructura de ambos fotocatalizadores, el experimento electroquímico de Mott-Schottky se realiza en 0,5 M Na 2 SO 4 , como se muestra en la Fig. 6b. De la Fig. 6b, todas las muestras muestran una pendiente positiva en los gráficos de Mott-Schottky, lo que indica que los compuestos preparados son aparentes semiconductores de tipo n [29, 30]. Y la energía de la posición de la banda de conducción (CB) de las muestras puede ser aproximadamente igual al potencial de la banda plana ( E fb ) extrapolando la X intersecciones de la porción lineal en los gráficos de Mott-Schottky. El valor de E fb del TiO 2 (S), TiO 2 (S) / CdTe / BiOI y TiO 2 (H) / CdTe / BiOI es - 0,76 V (frente a SCE), - 0,80 V (frente a SCE) y - 0,85 V (frente a SCE), respectivamente. Dado que el SCE que usamos en la medición de Mott-Schottky posee un valor de - 0.24 V versus NHE [31], el CBM de TiO 2 (S), TiO 2 (S) / CdTe / BiOI y TiO 2 Las muestras de (H) / CdTe / BiOI podrían calcularse en - 0,52 V (frente a NHE), - 0,56 V (frente a NHE) y - 0,6 V (frente a NHE), respectivamente, que es más negativo que el potencial de reducción de O 2 / • O - 2 (E 0 (O 2 / • O - 2 ) =- 0,33 V frente a NHE). Además, combinado con el valor de banda prohibida de la Fig. 6, el máximo de la banda de valencia (VBM) se ubica en 2,5 V (frente a NHE), 2,01 V (frente a NHE) y 1,85 V (frente a NHE), respectivamente.
La Figura 7a muestra la degradación fotocatalítica de MO en soluciones sin catalizador y sobre diferentes fotocatalizadores. Puede verse claramente que TiO 2 las microesferas sólidas y P25 poseen actividades fotocatalíticas relativamente pobres bajo luz solar simulada, y la degradación es causada por la pequeña porción ultravioleta de la fuente de luz. Por el contrario, el rendimiento fotocatalítico de TiO 2 (S) / BiOI y TiO 2 (S) / CdTe se mejora ligeramente, y el porcentaje de eliminación de MO alcanzó el 46,3% y el 57,5% después de 180 min de irradiación, respectivamente. Cabe señalar que la degradación fotocatalítica de MO podría alcanzar el 88,4% en 180 min y el 99,7% en 90 min para TiO 2 (S) / CdTe / BiOI y TiO 2 (H) / CdTe / BiOI, respectivamente, debido al componente sinérgico binario de respuesta visible BiOI y CdTe QD. Además, el TiO 2 más eficiente (H) / CdTe / BiOI sobre TiO 2 (S) / CdTe / BiOI probablemente sea causado por una superficie específica ligeramente mayor (91,6 m 2 g −1 más de 77,7 m 2 g −1 ) como se ha mencionado más arriba. La Figura 7b muestra el experimento de degradación del ciclo de TiO 2 (S) / CdTe / BiOI y TiO 2 Compuestos (H) / CdTe / BiOI. Hay una ligera reducción de la eficacia de la fotodegradación después de tres ciclos.
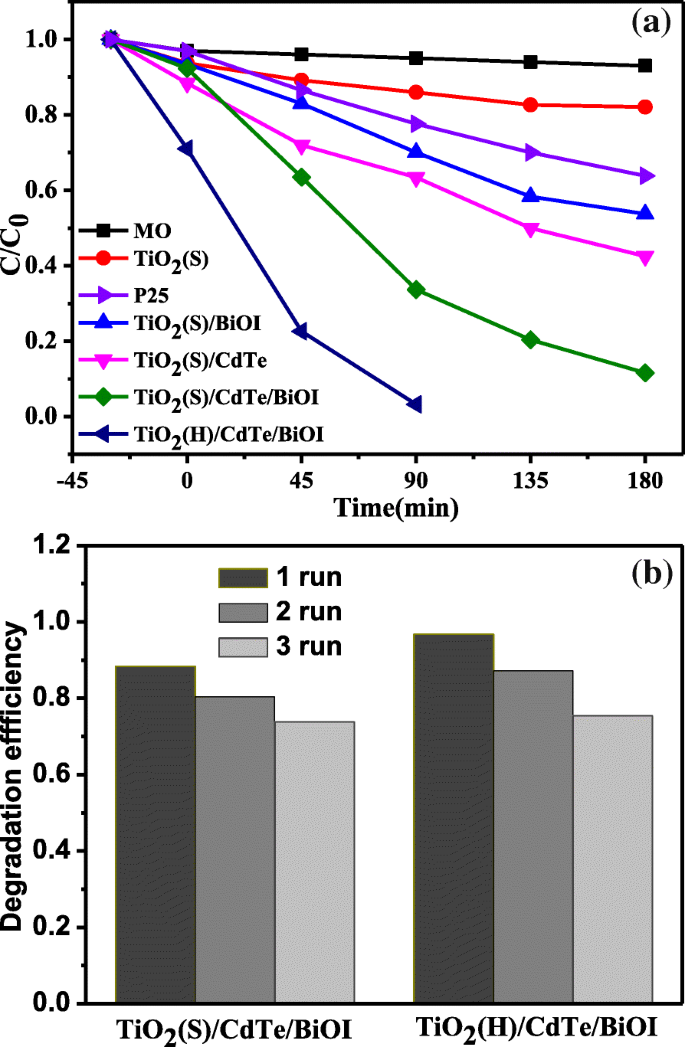
un Rendimiento fotocatalítico de las muestras para la eliminación de MO. b Experimentos de reciclaje fotocatalítico para el TiO 2 (S) / CdTe / BiOI y TiO 2 (H) / CdTe / BiOI samples
Con el fin de evaluar la ruta de degradación fotocatalítica del MO por el TiO 2 / CdTe / BiOI, el efecto de h + , e - , • OH y • O - 2 fue investigado mediante un experimento de captura con EDTA-2Na (h + ), KBrO 3 (e - ), BQ (• O - 2 ) e IPA (• OH). La Figura 8 muestra la eficiencia de degradación de MO durante estos experimentos fotocatalíticos en presencia de los captadores seleccionados. Se puede encontrar que el proceso fotocatalítico se suprime sin ningún limpiador y la eficiencia de degradación es casi nula en presencia de EDTA-2Na. Sin embargo, e - scavenger podría acelerar la degradación, lo que demostró que los agujeros (h + ) son las principales especies activas para la degradación del MO. El BQ como • O - 2 carroñero solo influyó en la degradación en un pequeño grado, lo que sugiere que • O - 2 son parcialmente responsables del proceso de oxidación fotocatalítica. Además, la influencia de IPA en el TiO 2 / CdTe / BiOI muestra de eliminación de MO apenas se observa, lo que indica que • Los radicales OH apenas son útiles en el sistema fotocatalítico actual.
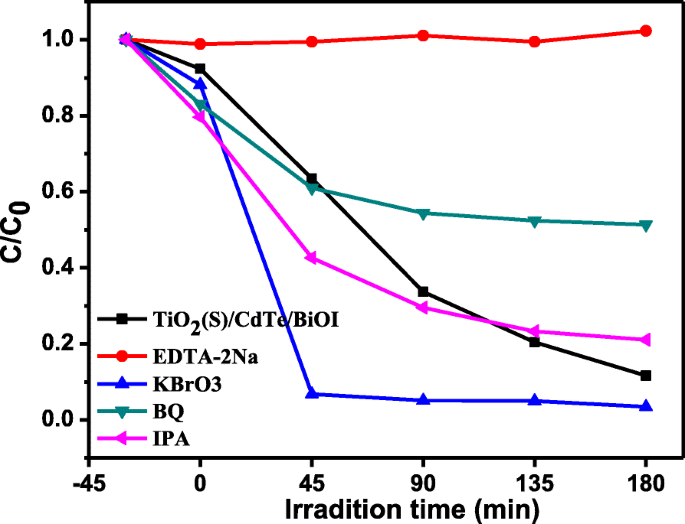
Las parcelas de rendimiento fotodegradado de MO al atrapar las diferentes especies activas fotogeneradas de TiO 2 Muestra (S) / CdTe / BiOI
La espectroscopía de emisión de fotoluminiscencia (PL) se lleva a cabo para estudiar más a fondo el comportamiento de transferencia de los portadores de carga fotogenerados. Como se muestra en la Fig. 9, todas las muestras muestran un pico de emisión PL amplio a aproximadamente 450-500 nm con la excitación a 365 nm. El desnudo TiO 2 (S) tiene un pico de emisión fuerte, mientras que TiO 2 La muestra (S) / CdTe / BiOI muestra una intensidad más baja que la de TiO 2 (S). Este fenómeno indica que la tasa de recombinación de los portadores de carga fotogenerados se restringió de manera eficiente después de decorar CdTe y BiOI en la superficie de TiO 2 . Además, el TiO 2 (H) / CdTe / BiOI exhibe una intensidad de PL significativamente disminuida en comparación con las otras muestras, lo que se debe a la transferencia más rápida de electrones y huecos de CdTe QD o nanohojas de BiOI a la superficie de TiO 2 . Los resultados de PL son consistentes con el resultado del experimento de fotodegradación.
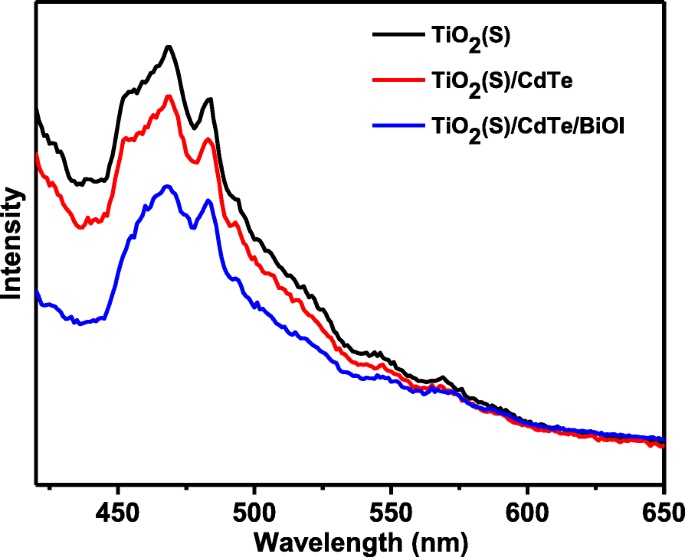
Espectros de fotoluminiscencia del TiO 2 desnudo (S), TiO 2 (S) / CdTe / BiOI y TiO 2 Muestras (H) / CdTe / BiOI ( λ excitación =365 nm)
La fotocorriente de las muestras se muestra en la Fig. 10. Vale la pena señalar que el TiO 2 Los compuestos (S) / CdTe mostraron una respuesta de fotocorriente más alta que la del TiO 2 puro (S) y TiO 2 Compuestos (S) / CdTe / BiOI. Por lo tanto, el aumento de la fotocorriente podría atribuirse principalmente a la eficiente separación y migración fotogenerada, que beneficia al rendimiento fotocatalítico.
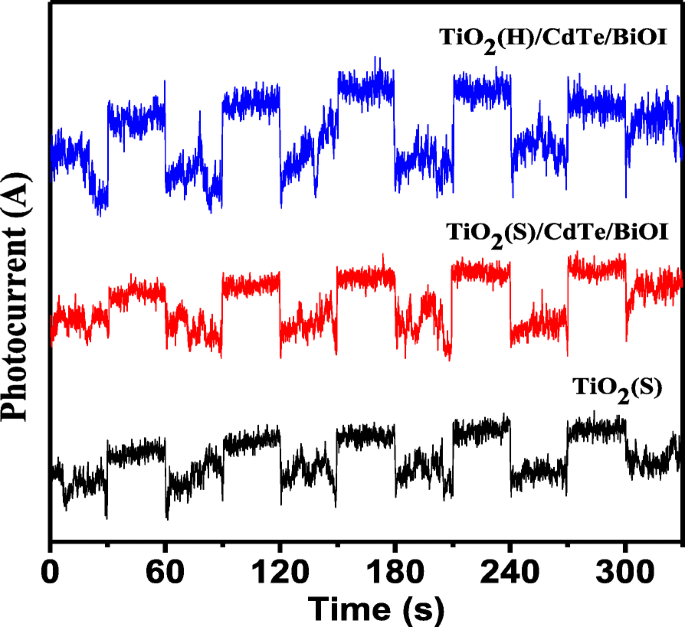
La respuesta de fotocorriente transitoria de TiO 2 (S), TiO2 (S)/CdTe/BiOI, and TiO2 (H)/CdTe/BiOI
Based on the results and discussions above, we propose a synergistic CdTe QDs/BiOI sensitization mechanism of the exciton transfer in TiO2 /CdTe/BiOI to explain the enhanced photo activity, as illustrated in Scheme 2. It is well known that TiO2 with a wide bandgap (3.02 eV) could only utilize the UV region in solar light, while the narrow bandgap CdTe QDs (~ 1.5 eV) [32] and BiOI nanostructures (~ 1.8 eV) [33] can be excited by photons in the visible range. In addition, a p-n junction is formed between p-type BiOI and n-type TiO2 when Fermi levels reached equilibrium, which facilitate photo-induced electrons to migrate from CB of BiOI to that of TiO2 [17, 34]. Similarly, a type II heterojunction is formed between p-type CdTe [18] and TiO2 microspheres; thus, electrons in the CB of CdTe QDs can transfer to TiO2 [35]. Therefore, the lifetime of the photogenerated electron and hole is prolonged, which is beneficial for the degradation towards MO.
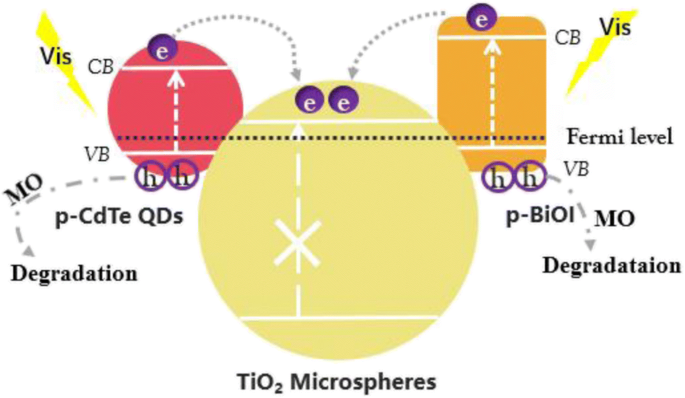
Illustration of photo-induced charge transfer in ternary TiO2 /CdTe/BiOI photocatalytic system
Conclusiones
In summary, a series of TiO2 -based photocatalysts were synthesized by a facile hydrothermal method. Modifications by BiOI and CdTe QDs were carried out to fabricate binary and ternary heterostructures, and the narrow bandgap semiconductors extended light response for the hybrid photocatalysts. In the case of ternary TiO2 /CdTe/BiOI heterostructured photocatalyst, the BiOI flakes and CdTe QDs act as sensitizers on one hand, which are excited by simulated solar light and transfer electrons to TiO2 . Meanwhile, the TiO2 microspheres serve as separation centers for the photo-induced charges on the other hand; thus, the synergistic effect among TiO2 , CdTe, and BiOI enhances the photocatalytic removal of MO. In addition, hollow TiO2 precursors were also employed to fabricate TiO2 /CdTe/BiOI heterostructures, and the improved photocatalytic performance towards MO degradation is attributed to a higher surface area and dispersion of BiOI components. The strategy of material regulation and incorporation will provide possibilities for the design of the multi-component semiconductor photocatalysts.
Abreviaturas
- TiO2 (H):
-
TiO 2 hollow microspheres
- TiO2 (S):
-
TiO 2 solid microspheres
- TiO2 /BiOI:
-
TiO 2 spheres modified with BiOI
- TiO2 /CdTe:
-
TiO 2 spheres modified with CdTe QDs
- TiO2 /CdTe/BiOI:
-
TiO 2 , CdTe, and BiOI ternary composites
Nanomateriales
- Alto rendimiento fotocatalítico de dos tipos de fotocatalizadores compuestos de TiO2 modificado con grafeno
- Hacia los nanofluidos de TiO2:Parte 2:Aplicaciones y desafíos
- Actividades fotocatalíticas mejoradas por nanopartículas au-plasmónicas en un fotoelectrodo de nanotubos de TiO2 recubierto con MoO3
- Heteroestructura jerárquica de esferas huecas de ZnO @ TiO2 para una evolución fotocatalítica de hidrógeno altamente eficiente
- Preparación y rendimiento fotocatalítico de fotocatalizadores LiNb3O8 de estructura hueca
- Un nuevo fotocatalizador de heterounión Bi4Ti3O12 / Ag3PO4 con rendimiento fotocatalítico mejorado
- Matrices de nanotubos de TiO2:fabricadas con una plantilla blanda-dura y la dependencia del tamaño de grano del rendimiento de las emisiones de campo
- Efecto del agente peptizante ácido sobre la relación anatasa-rutilo y el rendimiento fotocatalítico de nanopartículas de TiO2
- Actividad fotocatalítica de nanocompuesto ternario de atapulgita-TiO2-Ag3PO4 para la degradación de rodamina B bajo irradiación solar simulada
- Eficiencia de conversión de energía mejorada de células solares de perovskita con un material de conversión ascendente de Er3 + -Yb3 + -Li + TiO2 tri-dopado
- Fabricación de heteroestructuras jerárquicas de núcleo-capa de ZnO @ NiO para un rendimiento fotocatalítico mejorado



