Matrices de nanotubos de TiO2 bien alineadas con nanopartículas de Ag para una detección altamente eficiente de iones Fe3 +
Resumen
Hoy en día, la determinación de iones de hierro con alta sensibilidad y selectividad con métodos novedosos se convierte en una cuestión de urgencia para monitorear la salud del cuerpo y el medio ambiente. En este documento, por primera vez, presentamos un conjunto de TiO 2 de alto rendimiento matrices de nanotubos que son bastante sensibles a los iones de hierro. En primer lugar, se adoptó el método de oxidación anódica para preparar TiO 2 ordenado matrices de nanotubos, seguidas de la deposición de nanopartículas de Ag funcionalizadas con la capacidad de mejora en la detección de iones de hierro. Además, el espectro del TiO 2 El nanotubo con / sin las nanopartículas de Ag se analizó con un espectrómetro de fotoelectrones de rayos X, que muestra que las nanopartículas de Ag pueden reducir eficazmente la tasa de recombinación de electrones y huecos, y aumentar la conductividad y la tasa de transferencia de carga de los electrodos. Además, cuando se funcionalizan nanopartículas de Ag en TiO 2 bien ordenado Se utilizaron matrices de nanotubos, se investigó la detección de iones de hierro con el método de voltamperometría de separación anódica para validar el gran potencial del TiO 2 matrices de nanotubos con una sensibilidad de aproximadamente 30 μA / ug / L para convertirse en Fe 3+ sensores. Este método crea nuevas posibilidades para desarrollar sensores para el monitoreo de Fe 3+ en muestras biológicas sin ningún procedimiento de pretratamiento de la muestra.
Antecedentes
El hierro es un elemento nutriente importante para la salud humana, que generalmente es responsable de la transferencia y transporte de oxígeno y materiales de bloque, y ocupa el segundo lugar entre los elementos metálicos más esenciales del cuerpo humano. Sin embargo, una cantidad excesiva de iones de hierro en una célula viva puede catalizar la producción de especies reactivas de oxígeno (ROS) a través de la reacción de Fenton, que puede conducir a enfermedades, como enfermedad renal, y alterar la homeostasis celular que resulta en Alzheimer, Wilson y Enfermedades de Menkes [1, 2]. De hecho, debido a su amplia aplicación en la industria y la agricultura, los posibles efectos tóxicos del hierro de los ríos, lagos u océanos contaminados en los seres humanos siguen siendo un desafío mundial [3, 4]. En consecuencia, es particularmente necesario monitorear el cuerpo y el medio ambiente saludables para desarrollar tecnologías prácticas y eficientes que se utilicen para determinar rápidamente los iones de hierro con alta sensibilidad y selectividad.
Hoy en día, existen muchos métodos para detectar iones metálicos, tales como espectrometría de absorción atómica, espectrometría de masas de plasma acoplado inductivamente y espectrometría de emisión de plasma acoplado inductivamente. Sin embargo, en estos métodos se necesitan equipos complicados y pasos de preparación de muestras, que también resultarán en un gran costo. Recientemente, se ha realizado un enorme esfuerzo en estudios sobre nanopartículas, como el grafeno [5,6,7,8,9,10,11,12], puntos cuánticos de grafeno [13,14,15,16,17,18] , puntos de carbono [19,20,21] y nanopartículas o nanoclusters de metales nobles en la dimensión deseada para la detección de iones metálicos, que han atraído mucha atención debido a su buena selectividad, alta sensibilidad y fácil operación. Vinod Kumar Gupta y col. han desarrollado un método para sintetizar imina a través de una reacción de condensación simple y han explorado sus capacidades de detección de metales a través de métodos electroquímicos y ópticos. Fe 3+ detectado por colorimétrico (L2) a baja concentración puede alcanzar 1,29 × 10 −6 M. Pero este método está limitado debido a factores como límites de detección altos y una fuerte interferencia [22]. Xiaohui Gao y col. informó de un sensor colorimétrico fácil basado en nanopartículas de Ag estabilizadas con N-acetil-L-cisteína (NALC) (NALC-Ag NP) para la detección de iones Fe3 + en solución acuosa. Este método se puede utilizar para realizar una detección sensible y selectiva de Fe 3+ iones en agua con un rango lineal de 80 nM a 80 mM y un límite de detección de 80 nM [23]. Kailasa S K y col. han desarrollado un método colorimétrico selectivo y sensible para la determinación de Fe 3+ ion mediante el uso de nanopartículas de oro funcionalizadas con ditiocarbamato de ácido p-amino salicílico (DTC-PAS-Au NP) como sondas colorimétricas [24, 25]. Sobre la base de dicha detección, se adoptó preferentemente el análisis de plasma acoplado inductivamente (ICP) junto con espectrometría de masas (MS) o espectroscopia de emisión óptica (OES) para el análisis de iones de hierro [26].
Por otro lado, TiO 2 Los nanotubos, con alta estabilidad química, se aplican ampliamente en diversas industrias debido a sus excelentes propiedades fotoelectroquímicas, catalíticas y de adsorción, así como a su no toxicidad, como sensores de gas / humedad [27], descomposición fotocatalítica del agua en hidrógeno [28] , degradación fotocatalítica de contaminantes orgánicos [29], células solares sensibilizadas por colorante [30], biosensores [31] y supercondensadores [32]. Particularmente, TiO 2 bien estructurado y altamente ordenado Los nanotubos son muy adecuados para la transferencia direccional y rápida de cargas eléctricas [33,34,35,36]. Además, la funcionalización de la superficie de Ag NP juega un papel crucial en el aumento de la aplicabilidad analítica para TiO 2 Detección de nanotubos de analitos traza con alta selectividad y sensibilidad. Por lo tanto, considerando la combinación de TiO 2 La detección de nanotubos e iones metálicos a nivel de trazas es muy deseable. Hasta donde sabemos, hay muy pocos informes sobre el uso de TiO 2 funcionalizado nanotubos como sonda basada para Fe 3+ detección.
En este documento, un conjunto de TiO 2 de alto rendimiento Se presentan matrices de nanotubos que son bastante sensibles a los iones de hierro. En primer lugar, se adoptó el método de oxidación anódica para preparar TiO 2 ordenado matrices de nanotubos, seguidas de NP de Ag funcionalizadas con la capacidad de detectar iones de hierro. Además, el espectro del TiO 2 El nanotubo con / sin Ag NPs se analizó con un espectrómetro de fotoelectrones de rayos X. Además, detección de iones de hierro con el uso de NP de Ag funcionalizadas en TiO 2 bien ordenado Se investigaron matrices de nanotubos mediante el método de voltamperometría de separación anódica para validar el gran potencial de los sensores de metales pesados de TiO 2 matrices de nanotubos. Este método crea nuevas posibilidades para desarrollar sensores para monitorear Fe 3+ en muestras biológicas sin ningún procedimiento de pretratamiento de la muestra.
Métodos
Principios de detección de iones de hierro con TiO 2
Los electrones superarán la banda prohibida y pasarán de la banda de valencia (VB) a la banda de conductancia (CB) cuando absorban suficiente energía en TiO 2 nanotubos. Como resultado, habrá un estado electrónico no ocupado (agujero) en VB, que es positivo, como se explica en la Fig. 1a. En este proceso, cuando un electrón se excita desde el VB al CB, puede difundirse a la superficie permitiendo la transferencia de carga a un adsorbato o puede quedar atrapado dentro de una trampa de electrones en la banda prohibida. Si la superficie de los nanotubos estaba cubierta por nanopartículas metálicas, se produciría una transferencia de carga entre el adsorbato y el TiO 2 nanotubo debido a la transición de electrones. Con base en esta transferencia, se puede conocer la cantidad de nanopartículas metálicas cuando se detecta la cantidad de carga eléctrica, como se muestra en la Fig. 1b y las Ecs. (1) - (3). A partir de estas ecuaciones, se puede ver que la distribución de carga en exceso define el potencial que atrae a los receptores de electrones (O 2 ) y repele la donación de electrones (H 2 O) moléculas a O b defectos de vacancia cuando las partículas metálicas se adsorben en el TiO 2 superficie. Por lo tanto, podemos detectar la concentración y las especies de nanopartículas metálicas directamente midiendo la cantidad de transferencia de carga con las siguientes ecuaciones [37]:
$$ {\ mathrm {Ti}} _ {(6c)} \ \ left [{(4s)} ^ 2 {(3d)} ^ 2 \ \ mathrm {of} \ {\ mathrm {Ti}} _ {( 6c)} \ right] =4 \ times \ left [{\ mathrm {O}} _ {\ left (3 \ mathrm {C} \ right)} \ right] +2 \ times \ left [{\ mathrm {O }} _ {\ mathrm {b} \ left (2 \ mathrm {C} \ right)} \ right] $$ (1) $$ \ kern1.5em \ left [{(4s)} ^ 2 {(3d) } ^ 2 \ \ mathrm {de} \ {\ mathrm {Ti}} _ {(6c)} \ right] + \ left [{\ left (1 \ mathrm {s} \ right)} ^ 1 \ \ mathrm { de} \ \ mathrm {H} \ right] =4 \ times \ left [{\ mathrm {O}} _ {\ left (3 \ mathrm {C} \ right)} \ right] +1 \ times \ left [ {\ mathrm {O}} _ {\ mathrm {b} \ left (2 \ mathrm {C} \ right)} \ right] + \ left [\ mathrm {OH} \ right] + {\ mathrm {e}} ^ {-} $$ (2) $$ {\ mathrm {Ti}} _ {(5c)} \ \ left [{(4s)} ^ 2 {(3d)} ^ 2 \ \ mathrm {electrones} \ \ mathrm {de} \ {\ mathrm {Ti}} _ {(5c)} \ right] =5 \ times \ left [{\ mathrm {O}} _ {\ left (3 \ mathrm {C} \ right)} \ right] $$ (3)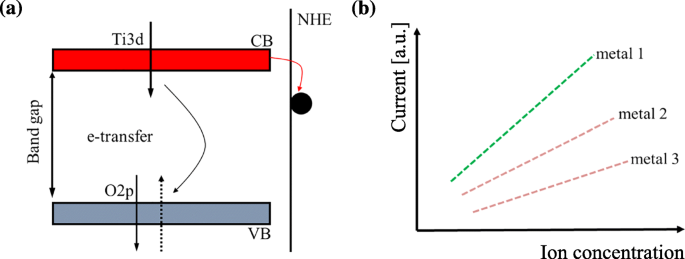
un El diagrama esquemático de la transferencia de carga superficial entre el metal y TiO 2 . b Determinación de la concentración y especies de iones metálicos en función de la magnitud de la corriente inducida por la transferencia de carga
El método de voltamperometría de arrastre se puede utilizar para identificar la concentración y las especies de metales en la superficie de TiO 2 matrices de nanotubos. En este método, la dependencia de la corriente de la concentración y la especie de metales se puede mostrar en la Ec. (4) [38]:
$$ \ Delta {i} _p =\ frac {nFA {D} ^ {1/2} \ mathrm {C}} {\ sqrt {\ pi {t} _m}} \ left (\ frac {1- \ sigma } {1+ \ sigma} \ right) $$ (4)Donde, σ =exp [( nF / RT ) ( ∆E / 2)] y N es el número de electrones que participan en reacciones con metales. F , A , D , C y t m representan la constante de Faraday, el área del electrodo, el coeficiente de difusión y la concentración de iones metálicos y el ancho de pulso, respectivamente. Se puede ver en esta ecuación que la corriente es proporcional a la concentración de metal.
Detalles experimentales
Se pulió químicamente una hoja de titanio puro (20 x 20 x 0,1 mm; pureza del 99,9%) para eliminar la capa de óxido y crear una superficie lisa. Para ser específicos, se vertió una cantidad adecuada de ácido HF con una concentración del 40% en agua ionizada proporcionalmente (0,5%); luego, la hoja de titanio se sumergió en la solución preparada previamente durante 10 sy se sacó instantáneamente y luego se secó con nitrógeno. A continuación, se lavó ultrasónicamente en acetona, alcohol etílico absoluto y agua desionizada a 30 ° C durante 12 min, respectivamente. En el proceso, se utilizó principalmente acetona para limpiar la superficie de la hoja de Ti con una rugosidad de 0,139 μm y 0,066 μm antes y después del tratamiento, respectivamente. El pretratamiento de las láminas de Ti es necesario antes de los experimentos para lograr una mayor suavidad. La configuración experimental se aplicó en la Ref. [39]. Se utilizó el espectrómetro de fotoelectrones de rayos X (XPS) AMICUS de Shimadzu para la definición de composición cuantitativa del TiO 2 preparado matrices de nanotubos.
Se depositaron nanopartículas (NP) de agricultura de varios tamaños en el TiO 2 superficie de nanotubos (QPrep400, Mantis) con la potencia de 60 W en condiciones de vacío de 10 −3 Torr. La pureza de la placa de Ag fue del 99,9999%.
Se utilizó una estación de trabajo electroquímica (CHI660E, Shanghai Chenhua) para realizar los experimentos de voltamperometría de extracción para detectar la concentración de Fe 3+ iones. Se utilizó un sistema de tres electrodos (electrodo de trabajo, de referencia y electrodos auxiliares) que consta de dos bucles para monitorear el proceso de reacción electroquímica del electrodo de trabajo y para mantener el equilibrio de la reacción química.
En los experimentos, cuatro tipos de Fe 3+ con las concentraciones de 10 μg / L, 20 μg / L, 30 μg / L, 40 μg / L y 50 μg / L se mezclaron en cloruro de amonio, respectivamente. Cuando se detectó, el hierro neutro se adsorbió primero en el TiO 2 superficie de nanotubos con / sin deposición de Ag después de la reacción de reducción con sustrato de Ti, seguido de re-oxidado cuando se aplicó polarización inversa. El voltaje escaneado osciló entre - 1 V y 1 V con un paso de 0,005 V. La corriente mínima detectable fue 10 −5 A, y la duración detectada fue de 120 s. Concentración de Fe 3+ iones se evaluó a partir de la dependencia del pico de la corriente de disolución del voltaje.
Resultados y discusión
Preparación y caracterización de TiO 2 Matrices de nanotubos
TiO 2 matrices de nanotubos producidas en un electrolito compuesto de glicol, 2% en volumen de agua y 0,3% en peso de fluoruro de amonio con un voltaje de oxidación de 60 V, un tiempo de oxidación de 2 h, una temperatura de oxidación de 40 ° C y una temperatura de calcinación de 500 ° C tenía la morfología y el rendimiento óptimos [39]. Imágenes topográficas y de microscopio electrónico de barrido (SEM) de vista lateral del TiO 2 Las matrices de nanotubos se muestran en la Fig. 2a, b, respectivamente. En la Fig. 2a, el TiO 2 Las matrices de nanotubos están bien dispuestas con un diámetro medio de 50 nm. En la Fig. 2b, la longitud del nanotubo es de aproximadamente 19,2 μm con un ángulo de inclinación relativo de 30 ° con el sustrato cuando se mide. A partir de estos resultados, se puede ver que el área de contacto con Fe 3+ Los iones para las matrices de nanotubos se pueden aumentar obviamente a medida que aumenta la longitud del tubo, lo que puede mejorar la sensibilidad de detección de manera efectiva.

Topografía ( a ) y vista lateral ( b ) Imágenes del TiO 2 Matrices de nanotubos, respectivamente
La Figura 3a – d muestra imágenes SEM de TiO 2 nanotubos con deposición de nanopartículas de Ag con duraciones de 30 s, 35 s, 40 sy 45 s respectivamente. En la Fig. 3a, cuando la duración de la deposición fue de 30 s, el diámetro promedio y el espesor de cobertura de las nanopartículas de Ag adsorbidas en la pared de los nanotubos fueron aproximadamente de 10 nm y 5 nm respectivamente. A partir de estos resultados, se puede ver que las nanopartículas tienen una distribución de tamaño uniforme. En la Fig. 3b, c, cuando la duración de la deposición se extendió a 35 sy 40 s, el estado de las nanopartículas de Ag se convirtió en estado de agrupamiento gradualmente y los diámetros de las partículas de Ag aumentaron a 20 nm y 25 nm respectivamente. Los diámetros de las nanopartículas de Ag aumentaron aún más hasta que se convirtieron en grupos que cubren parcialmente la superficie del TiO 2 nanotubo cuando el tiempo de deposición aumentó a 45 s, que se muestra en la Fig. 3d.
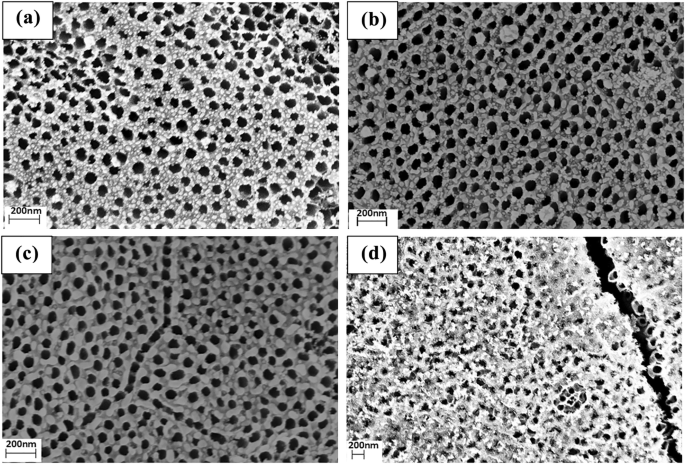
Imágenes SEM de TiO 2 cargado con nanopartículas de Ag Matrices de nanotubos con duraciones de pulverización catódica de 30 s, 35 s, 40 sy 45 s correspondientes a ( a ) - ( d ), respectivamente
Para confirmar la composición del TiO 2 Se realizaron matrices de nanotubos con / sin adsorción de partículas de Ag con una duración de 30 s, se realizaron experimentos XPS, que se muestran en la Fig. 4a – d. En la Fig.4a, los espectros de Ag se dieron con las intensidades de 3200 y 2400 recuentos cuando los valores de energía de enlace eran 368,24 eV y 374,25 eV, respectivamente, lo que mostró que FWHM (onda completa a la mitad del máximo) de Ag era aproximadamente 1 eV. A partir de estos resultados, se puede ver que solo un estado químico Ag 0 se detectó después de la deposición de Ag.
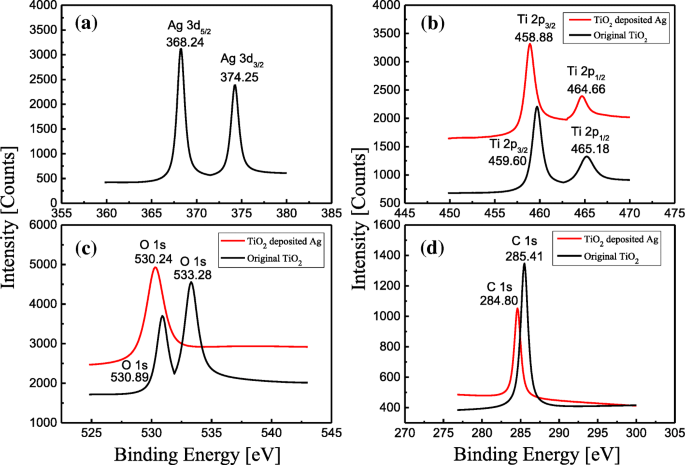
Espectroscopía fotoelectrónica de los espectros de Ag en ( a ); y las espectroscopias de TiO 2 Nanotubos con / sin depósito de Ag en ( b ), ( c ) y ( d ) Medido por XPS, respectivamente
En la Fig. 4b, se dieron los espectros de Ti con / sin deposición de Ag y se marcaron con líneas rojas y negras. Antes de la deposición de Ag, los valores observados de energía de enlace de Ti eran 459,60 eV y 465,18 eV con intensidades de 2250 y 1250 recuentos, respectivamente. Por el contrario, los valores de la energía de enlace de Ti fueron 458,88 eV y 464,66 eV, siendo las intensidades crecientes 3250 y 2700 recuentos respectivamente después de la deposición. La diferencia en la energía de enlace antes de la deposición de Ag fue de 5,58 eV; por el contrario, la diferencia después de la deposición cambió a 5,78 eV, que se incrementó aproximadamente en 0,3 eV. Además, los dos cambios de pico de titanio fueron 0,72 eV y 0,52 eV respectivamente. Este fenómeno fue causado por la interacción de Ag NP.
Se observaron fenómenos similares en los espectros para oxígeno y carbono con / sin deposición de Ag, que se muestran en la Fig. 4c, d respectivamente. Antes de la deposición, los valores de la energía de enlace del oxígeno eran 530,89 eV y 533,28 eV con intensidades de 3500 y 4500 recuentos, respectivamente. Estos resultados mostraron que el oxígeno estaba en un estado de dos valencia negativo (oxígeno reticulado) y consistía en TiO 2 con titanio. Por otro lado, el valor de la energía de enlace del oxígeno fue de 530,24 eV con una intensidad de 4900 recuentos después de la deposición. Además, el valor del pico de oxígeno de la energía de enlace, 533,28 eV, desapareció después de la deposición, y el cambio del pico de oxígeno fue de 0,67 eV. Estos resultados demostraron que el estado del oxígeno cambió de oxígeno reticular a oxígeno adsorbido debido a la reacción con NP de Ag después de la deposición.
En la Fig. 4d, detectamos el espectro de contaminación por carbono en TiO 2 matrices de nanotubos con / sin deposición de Ag, que se marcaron con líneas rojas y negras respectivamente. El valor de la energía de enlace de la contaminación por carbono fue de 285,41 eV, siendo la intensidad del número de fotones aproximadamente 1350 recuentos antes de la deposición. Por el contrario, el valor de la energía de enlace de la contaminación por carbono fue 284.80 eV con la intensidad del número de fotones de aproximadamente 1050 recuentos después de la deposición de Ag, lo que significó que el valor de la energía de enlace y el número de fotones de carbono se redujo en 0,59 eV y 30% respectivamente. Estos resultados indicaron que la cantidad de contaminación por carbono se redujo significativamente después de la deposición de NP de Ag. En otras palabras, la deposición de Ag NP puede reducir la contaminación del electrodo y mejorar la eficiencia de la transferencia de carga. Cabe señalar que el desplazamiento de la energía de enlace medido después de la deposición fue de aproximadamente 0,8 eV, que se debió principalmente al desplazamiento del carbono.
Por lo tanto, TiO 2 Las matrices de nanotubos depositadas con Ag NP pueden reducir eficazmente la tasa de recombinación de electrones y huecos, y aumentar la conductividad y la tasa de transferencia de carga de los electrodos en comparación con TiO 2 matrices de nanotubos sin Ag NP.
Detección de Fe 3+ Iones con / sin depósito de NP de Ag
Para obtener los resultados experimentales, se utilizó voltamperometría de stripping electroquímico para detectar Fe 3+ metálico iones con TiO 2 matrices de nanotubos sin deposición de NP de Ag. La concentración de Fe 3+ iones se establece dentro de un rango de 10 μg / L a 50 μg / L. Dependencia de la corriente de disolución del voltaje cuando Fe 3+ Los iones detectados se muestran en la Fig. 5. Durante la medición, cuando el voltaje aplicado era menor que - 0.3 V, la corriente de disolución se mantuvo constante y permaneció aproximadamente 0 A. Cuando el voltaje aplicado estaba dentro de un rango de - 0.3 V a - 0.16 V, la corriente cayó rápidamente y el pico se redujo aproximadamente de - 1,16 × 10 −4 A hasta - 1,28 × 10 −4 A con Fe 3+ el incremento de concentración de iones está dentro de un rango de 10 μg / L a 50 μg / L y con los cambios de voltaje dentro de un rango de - 0.18 V a - 0.16 V, respectivamente. El recuadro muestra la dependencia del pico de corriente del voltaje aplicado, como se muestra en la Fig. 5. Cuando el voltaje aplicado V> - 0.16 V, la corriente de disolución aumentó exponencial y gradualmente, y se mantuvo dentro de un rango de - 0.2 × 10 - 4 A a - 0,4 × 10 −4 A. A partir de este resultado, se puede ver que el pico de la corriente disminuye con el aumento de Fe 3+ concentración de iones, y que el TiO 2 La matriz de nanotubos se puede utilizar como Fe 3+ sensor de detección.
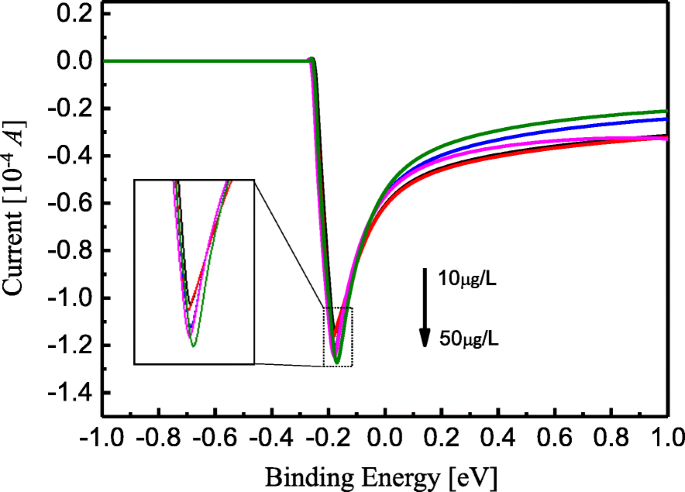
La dependencia de la corriente de disolución del voltaje cuando se detecta Fe 3+ iones
Dependencia de los picos de corriente en la Fig.5 de Fe 3+ La concentración de iones (de 10 μg / L a 50 μg / L) también se resume en la Fig. 6. La línea continua es el ajuste de datos y está alineada con la linealidad de una manera razonable. Los resultados de los ajustes se pueden calcular con y =0,00373 x + 1.1027, donde y y x representan las concentraciones de iones y corriente, respectivamente. Este resultado de ajuste es suficiente para mostrar que el Fe 3+ mínimo detectable concentración de iones cuando TiO 2 Se adoptan matrices de nanotubos sin que la deposición de NP de Ag sea de 37,3 μA / μg / L. El límite de detección de Fe 3+ ( δx =( dy / dx ) −1 · (1 / dy )) cuando el TiO 2 Las matrices que se utilizan deben ser de 15.01 nM teniendo en cuenta el rango lineal. Aquí, dy / dx =37,3 μA / μg / L y δy =0,01 μA, M Fe =56, respectivamente. Este resultado es comparable al de la Ref [25]. En este artículo, la relación de extinción A700 nm / A520 nm es lineal con la concentración de Fe 3+ que van desde 40 mM a 80 mM, que pueden realizar una detección sensible de Fe 3+ iones con un límite de detección de 14,82 nM cuando el método UV-visible basado en DTC-PASAu NP para la detección in situ y en tiempo real de Fe 3+ en muestras biológicas.
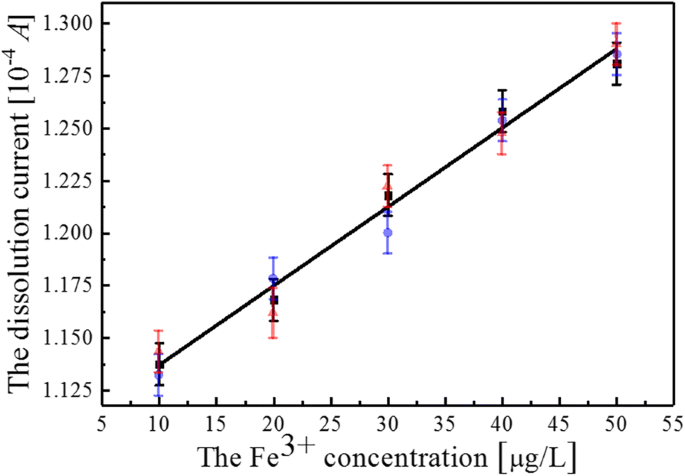
Los picos actuales de dependencia del Fe 3+ concentración de iones
A continuación, mejora de la sensibilidad de Fe 3+ detección de concentración de TiO 2 Se investigaron matrices de nanotubos con deposición de Ag, con duraciones de deposición de 30 segundos, 35 segundos y 40 segundos, respectivamente. El Fe 3+ La concentración se estableció en 10 μg / L, y el resultado se muestra en la Fig. 7. Cuando el voltaje V aplicado fue menor que - 0.3 V, la corriente de disolución se mantuvo casi constante y fue aproximadamente 0 A. Cuando el voltaje aplicado estaba dentro de un rango de - 0.3 V a - 0.2 V, la corriente cayó rápidamente a aproximadamente - 1.35 × 10 −4 A, y cuando el voltaje aplicado fue mayor que - 0.2 V, la corriente de disolución aumentó exponencial y gradualmente, y se mantuvo dentro de un rango de - 0.08 × 10 −4 A a - 0,4 × 10 −4 A. El recuadro muestra la dependencia del pico actual del voltaje aplicado, como se muestra en la Fig. 7. La dependencia de los picos en la Fig. 7 en la deposición de Ag NPs con la duración dentro de un rango de 0 sa 40 s también se resume en Fig. 8, y la línea continua presentó el ajuste de datos. Se puede ver que la corriente alcanzó el valor máximo (aproximadamente - 1,38 × 10 −4 A) cuando el tiempo de deposición de Ag NPs fue de 30 s. En particular, en comparación con el valor de la corriente antes de la deposición de Ag sobre TiO 2 matrices de nanotubos, el valor de la corriente aumentó a aproximadamente - 1,15 × 10 −4 A, lo que significa que la sensibilidad del Fe 3+ la detección se mejoró en un 20% cuando se produjo la deposición de NP de Ag en TiO 2 superficie. Además, se consideró que el valor máximo de corriente en la duración de la deposición de 30 s estaba directamente relacionado con los diámetros y la distribución uniforme de Ag NP en TiO 2 superficie. En consecuencia, TiO 2 Los arreglos de nanotubos se caracterizan por una fabricación relativamente simple, alta sensibilidad y reproducibilidad en comparación con otros Fe 3+ métodos de detección. Además, el cambio de color de la solución coloidal de Ag se puede distinguir a simple vista, que también se puede utilizar para comprobar directamente si el Fe 3+ existe en la solución y sirve como una base sólida para esta investigación. Por lo tanto, NP de Ag funcionalizado en TiO 2 bien ordenado Los arreglos de nanotubos proporcionaron una respuesta de detección de sensibilidad, alta selectividad y bajo costo para Fe 3+ con un límite bajo de detección en condiciones ambientales. En particular, mejora de la sensibilidad de Fe 3+ La detección también se puede realizar para otros Fe 3+ soluciones con diferentes concentraciones.
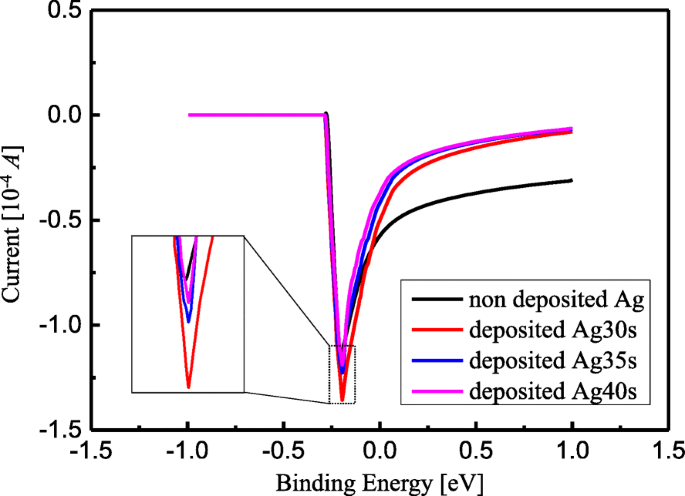
Detección de Fe 3+ iones por TiO cargado con Ag 2 matrices de nanotubos con varias concentraciones
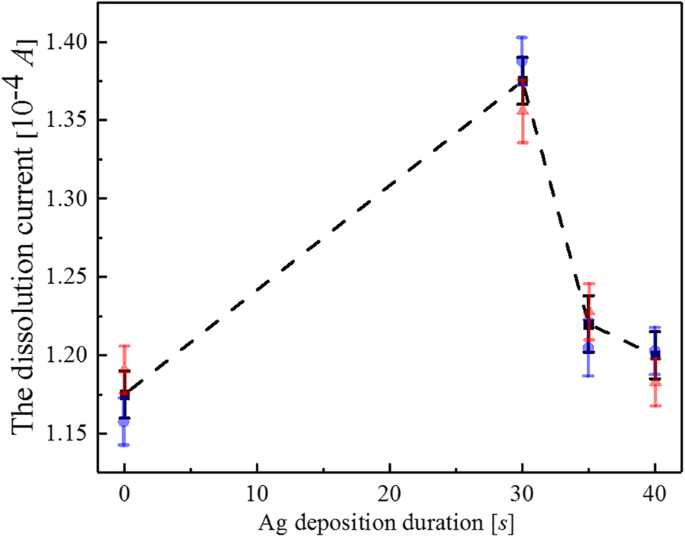
La relación entre el tiempo de deposición de iones de Ag en TiO 2 matriz de nanotubos y la concentración de detección de Fe 3+ ion
Para demostrar la selectividad de TiO 2 -Ag NP para Fe 3+ iones, se llevaron a cabo experimentos competitivos en presencia de otros iones metálicos cuando se utilizó resonancia de plasmón de superficie (SPR), espectrometría UV-visible, etc. Teóricamente, el cambio de pico característico debería ocurrir solo con la solución mixta de iones metálicos que contienen Fe 3+ iones como se indica en las Ecs. (1) - (4). A continuación, nos centraremos en los experimentos competitivos.
Conclusiones
TiO 2 es un material funcional importante que no solo se usa ampliamente en detectores UV, fotocatalizadores y células solares sensibilizadas con colorante, sino que también se usa en importantes aplicaciones potenciales en sensores ultrasensibles. En este artículo, presentamos un método que utiliza TiO 2 bien alineado matrices de nanotubos con nanopartículas de Ag como sensor de voltamperometría para una detección altamente eficiente de Fe 3+ Ion. Al principio, se adoptó el método de oxidación anódica para preparar TiO 2 ordenado matrices de nanotubos, seguidas de NP de Ag funcionalizadas con la capacidad de detectar iones de hierro. Luego, los espectros del TiO 2 Los nanotubos con / sin Ag NP fueron comparados por XPS, lo que demostró que el oxígeno reticulado en TiO 2 Las matrices de nanotubos se liberaron al oxígeno adsorbido debido a la interacción de Ag NP. Por lo tanto, cuando se utilizaron NP de Ag funcionalizadas en matrices de nanotubos, se investigó la detección de iones de hierro realizada con el método de voltamperometría de separación anódica para validar su gran potencial para convertirse en sensores de metales pesados, lo que demostró que las NP de Ag funcionalizadas en TiO 2 bien ordenado Los arreglos de nanotubos proporcionaron una respuesta de detección de sensibilidad, alta selectividad y bajo costo para Fe 3+ con un límite bajo de detección en condiciones ambientales. Este método crea nuevas posibilidades para desarrollar sensores para el monitoreo de Fe 3+ en muestras biológicas sin ningún procedimiento de pretratamiento de la muestra.
Abreviaturas
- CB:
-
Banda de conducta
- FWHM:
-
Ola completa a la mitad del máximo
- NALC:
-
N-acetil-L-cisteína
- NP:
-
Nanopartículas
- ROS:
-
Especies reactivas de oxígeno
- SEM:
-
Microscopio electrónico de barrido
- Ti:
-
Titanio
- VB:
-
Banda de valencia
- XPS:
-
Espectrómetro de fotoelectrones de rayos X
Nanomateriales
- S, N Co-Doped Graphene Quantum Dot / TiO2 Composites para la generación eficiente de hidrógeno fotocatalítico
- Nanofibras poliméricas electrohiladas decoradas con nanopartículas de metales nobles para detección química
- Membranas compuestas que contienen nanopartículas de intercambiadores de iones inorgánicos para la desalación electrodialítica de glicerol
- Nanopartículas de albúmina cargadas con resveratrol con circulación sanguínea prolongada y biocompatibilidad mejorada para una terapia de tumores pancreáticos dirigida altamente eficaz
- Actividades fotocatalíticas mejoradas por nanopartículas au-plasmónicas en un fotoelectrodo de nanotubos de TiO2 recubierto con MoO3
- Estabilidad mejorada de nanopartículas magnéticas de oro con poli (ácido 4-estirenosulfónico-ácido co-maleico):propiedades ópticas personalizadas para la detección de proteínas
- Método de postratamiento para la síntesis de nanopartículas de FePt-Fe3O4 binarias monodispersas
- Heteroestructura jerárquica de esferas huecas de ZnO @ TiO2 para una evolución fotocatalítica de hidrógeno altamente eficiente
- Un método sencillo para cargar nanopartículas de CeO2 en matrices de nanotubos de TiO2 anódico
- Fotocatalizadores eficientes fabricados mediante decoración uniforme de nanopartículas de Cu2O en matrices de nanocables de Si con baja reflectividad visible
- Síntesis en solución fácil de nanopartículas de fósforo rojo para ánodos de baterías de iones de litio



