Generación de especies reactivas de oxígeno en soluciones acuosas que contienen GdVO4:nanopartículas de Eu3 + y sus complejos con azul de metileno
Resumen
En esta carta, informamos el estudio de los radicales libres y la generación de especies reactivas de oxígeno (ROS) en soluciones acuosas que contienen gadolinio ortovanadato GdVO 4 :Eu 3+ nanopartículas (VNP) y sus complejos con fotosensibilizador de azul de metileno (MB). La actividad catalítica se estudió bajo radiación UV-Vis e irradiación de rayos X por tres métodos (prueba de dienos conjugados, radical OH · y detección de oxígeno singlete). Se ha demostrado que los complejos VNPs-MB revelan alta eficiencia de generación de ROS bajo irradiación UV-Vis asociada tanto con alta eficiencia de generación de radicales OH · por VNPs como generación de oxígeno singlete por MB debido a transferencia de energía de excitación no radiativa de VNPs a moléculas MB . Al contrario que bajo la irradiación de rayos X, el fuerte OH . Se ha observado la captación de radicales por VNP.
Antecedentes
La radioterapia (RT) sigue siendo un componente importante del tratamiento del cáncer con aproximadamente el 50% de todos los pacientes con cáncer que reciben RT durante el curso de su enfermedad [1, 2, 3]. El mecanismo exacto de muerte celular debido a la radiación es todavía un área de investigación activa. Las roturas bicatenarias del ADN nuclear se consideran el efecto celular más importante de la radiación que conduce a la pérdida irreversible de la integridad reproductiva de la célula y, finalmente, a la muerte celular [4]. Este daño por radiación puede ser causado por (i) ionización directa e (ii) ionización indirecta a través de radicales libres y especies reactivas de oxígeno (ROS), especies químicamente reactivas que contienen oxígeno, formadas a partir de la radiólisis de moléculas de oxígeno y agua celular [2,3, 4]. En la terapia clínica, el daño suele ser ionizante indirecto. En el proceso, el agua pierde un electrón y se vuelve altamente reactiva. Luego, mediante una reacción en cadena de tres pasos, el agua se convierte secuencialmente en varios radicales y productos moleculares:electrones hidratados (\ ({e} _ {aq} ^ {-} \ Big) \), átomo de hidrógeno ( H ∙ ), radical hidroxilo OH ·, radical hidroperoxilo (\ ({HO} _2 ^ {.} \ Big) \), peróxido de hidrógeno (H 2 O 2 ) y moléculas de hidrógeno (H 2 ) [5, 6]. Los electrones hidratados y los átomos de hidrógeno son fuertes agentes reductores. Por el contrario, los radicales hidroxilo son especies oxidativas muy fuertes y eliminan inmediatamente los electrones de cualquier molécula en su camino, convirtiendo esa molécula en un radical libre y propagando así una reacción en cadena [5]. Cuando se presenta oxígeno molecular disuelto en agua irradiada, su reducción produce un radical superóxido (\ ({O} _2 ^ {.-} \)) y es el precursor de la mayoría de los demás ROS, incluido el oxígeno singlete ( 1 O 2 ) [7].
Recientemente, se ha demostrado que nanopartículas (NP) de alto número atómico (Au, Ag, Hf, Gd, Ti) [8,9,10,11], NP semiconductoras (óxido de metal TiO 2 ZnO, CuO, Director ejecutivo 2 , Al 2 O 3 ; puntos cuánticos ZnS, ZnS, LaF 3 , etc.) [8, 12,13,14], y algunas NP inorgánicas (nanotubos de carbono) [15, 16] mejoran la eficiencia de la RT. Los principios teóricos de la interacción rayos X-NP están bien descritos [8, 12, 14]. Se produce una interacción en cascada de fotones de alta energía con la red del NP a través del efecto fotoeléctrico y el efecto de dispersión de Compton principalmente. Los electrones Compton, Photo o Auger pueden inducir la emisión de electrones secundarios, que pueden escapar al medio ambiente y serán capturados por un aceptor (es decir, agua, biomolécula, oxígeno, óxidos de nitrógeno) localizado cerca de la superficie de las NP e inducir Radicales biomoleculares y producción de ROS [8, 12, 14]. Los efectos radiosensibilizantes de las NP se asocian con los radicales biomoleculares y la generación de ROS como etapa final de la interacción de los rayos X con las NP. En las NP de semiconductores, como las NP de óxido metálico, el efecto citotóxico asociado con la generación de ROS también puede ser inducido por la irradiación UV [17,18,19,20]. El mecanismo es que cuando las NP se irradian con luz ultravioleta (energía mayor que la banda prohibida), se induce la separación de carga generando un agujero (h + ) en la banda de cenefa y un electrón (e - ) en la banda de dirección. Los electrones y los huecos exhiben una alta capacidad reductora y oxidante, respectivamente [18]. Los electrones pueden reaccionar con el oxígeno molecular para producir radicales superóxido (\ ({O} _2 ^ {\ cdotp -} \)) a través de un proceso reductor, mientras que los huecos pueden extraer electrones del agua y / o iones hidroxilo generando radicales hidroxilo (OH ·) A través de un proceso oxidativo [18,19,20]. Para TiO 2 , Director ejecutivo 2 , Al 2 O 3 y nanopartículas de ZnO, el 1 O 2 Se informó la generación a través de la oxidación de \ ({O} _2 ^ {\ cdotp -} \) [18, 21, 22].
Chen y Zhang [23] propusieron un enfoque más para mejorar la eficacia de la terapia del cáncer (terapia fotodinámica, TFD) utilizando NP centelleantes [23]. Este enfoque combina NP (centelleantes) excitadas por rayos X y moléculas fotosensibilizadoras (PS). Los NP centelleantes sirven como un transductor de energía que transfiere la energía recolectada de la irradiación de rayos X al PS que genera oxígeno singlete para la destrucción del tumor. Este enfoque permite un tratamiento profundo del cáncer y mejora tanto la TFD como la RT. Hasta ahora, una variedad de NP de centelleo y sus complejos con PS se han estudiado como agentes fotodinámicos inducibles por rayos X [12, 14, 23,24,25,26,27,28].
Recientemente, hemos informado sobre la creación de complejos sobre la base de NP de ortovanadato de gadolinio centelleante dopado con iones de europio GdVO 4 :Eu 3+ (VNPs) y fotosensibilizador de azul de metileno (MB) y estudio de la transferencia de energía de excitación electrónica en los complejos [29]. Se demostró que debido a la conversión de energía de excitación efectiva en los complejos, podrían ser prospectivos como un agente fotodinámico inducible por rayos X. El objetivo de este trabajo fue estudiar la eficiencia de la generación de ROS en soluciones acuosas que contienen VNP y sus complejos con MB bajo irradiación de rayos X y UV.
Experimental
Productos químicos
Cloruro de gadolinio GdCl 3 · 6H 2 O (99,9%), cloruro de europio EuCl 3 · 6H 2 O (99,9%), EDTA disódico · 2Na (99,8%) y metavanadato de sodio anhidro NaVO 3 (96%) se obtuvieron de Acros organic (EE. UU.) Y todos se usaron sin purificación adicional. Se compró hidróxido de sodio NaOH (99%) de Macrohim (Ucrania). Ortovanadato de sodio Na 3 Voz 4 La solución se obtuvo agregando una solución 1 M de NaOH en solución acuosa NaVO 3 a pH =13. L-a-fosfatidilcolina (PC) de yema de huevo, colorante catiónico cloruro de 3,7-bis (dimetilamino) fenazationio (azul de metileno (MB), M w =373,90 g / mol), 1,2-benzopirona (cumarina, M w =146,14 g / mol) se adquirieron de Sigma-Aldrich (EE.UU.) y se utilizaron tal como se recibieron. Sal disódica del ácido antraceno-9,10-dipropiónico (ADPA, M w =366,32 g / mol) se obtuvo de la colección de tintes del Dr. Igor Borovoy (Instituto de Materiales de Centelleo, NAS de Ucrania) con la pureza controlada por cromatografía en capa fina. Todos los demás productos químicos eran de calidad analítica.
Síntesis de GdVO 4 :Eu 3+ soluciones coloidales
Soluciones coloidales acuosas de nanopartículas de ortovanadato de gadolinio dopadas con iones de europio Gd 0.9 Eu 0.1 Voz 4 (GdVO 4 :Eu 3+ ) se sintetizaron de acuerdo con el método descrito anteriormente [30]. Primero, se mezclaron 0,4 ml de solución acuosa de cloruro de gadolinio (1 M) con 0,05 ml de cloruro de europio (1 M) y luego se añadieron a la mezcla 49,55 ml de agua bidestilada. Luego, la solución obtenida se mezcló con 37,5 ml de solución de EDTA disódico (0,01 M). Luego, 37,5 mL de Na 3 Voz 4 (0,01 M) se hizo fluir gota a gota (рН =10,5). La mezcla se agitó intensamente usando un agitador magnético y se calentó en un baño de agua bajo un condensador de reflujo durante 24 ha 100 ° С. La solución transparente incolora obtenida dispersa la luz bajo la iluminación lateral (el cono de Tyndall). Luego, la solución se enfrió y se dializó contra agua durante 24 h para eliminar el exceso de iones. Para ello, la solución obtenida se purificó en un saco de diálisis (Cellu Sep T2, membrana con un corte de peso molecular de 12 KDa, tamaño de poro ~ 2,5 nm) y se colocó en un vaso de 2 L con agua destilada. Después de cada 6 h, se refrescó el agua.
Instrumentación y caracterización
Los VNP sintetizados se caracterizaron mediante microscopía electrónica de transmisión (microscopio electrónico TEM-125 K, Selmi, Ucrania) y el método de dispersión de luz dinámica (analizador ZetaPALS, Brookhaven Instruments Corp., EE. UU.). Los espectros de absorción se midieron utilizando un espectrómetro Specord 200 (Analytik Jena, EE. UU.). Los espectros de fluorescencia y excitación de fluorescencia se tomaron con un espectrofluorímetro Lumina (Thermo Scientific, EE. UU.).
Preparación de complejos VNP-MB
Las soluciones para las investigaciones se prepararon como sigue. Primero, se prepararon soluciones madre de MB en agua (1 mmol / L). Para obtener soluciones acuosas de VNPs-MB, la cantidad requerida de la solución madre de tinte y la solución acuosa de VNPs se agregaron en un matraz y se agitaron cuidadosamente usando un evaporador rotatorio (Rotavapor R-3, Buchi) durante 1 h hasta la evaporación completa del cloroformo. Luego, se agregó 1 mL de una solución acuosa de VNPs en un matraz y se agitó suavemente durante 1 h para la formación del complejo VNPs-MB. La concentración de MB en la solución obtenida fue de 10 μmol / L. Las concentraciones de nanopartículas fueron 0.1, 1 o 10 mg / mL.
Detección de especies de radicales libres y oxígeno activo
La formación de ROS bajo la irradiación de rayos UV / X de soluciones acuosas que contienen VNP, MB o complejos VNPs-MB se detectó espectroscópicamente utilizando varios métodos.
Prueba de formación de dienos conjugados
La oxidación de lípidos bajo irradiación UV se midió usando una suspensión de liposomas de PC. Las vesículas lipídicas unilaminares de PC se prepararon mediante el método de extrusión [31]. Brevemente, se colocó una cantidad apropiada de PC (25 mg / ml) en cloroformo en un matraz y se secó hasta la evaporación completa del cloroformo usando un evaporador rotatorio (Rotavapor R-3, Buchi). La fina película de tintes lipídicos se hidrató luego con 10,8 ml de agua bidestilada. La suspensión de lípidos obtenida se extruyó finalmente a través de un filtro de policarbonato de tamaño de poro de 100 nm usando una mini-extrusora (Avanti Polar Lipids, Inc., EE. UU.). La concentración de PC fue de 1,2 mmol / L. Para la prueba de formación de dienos conjugados, se mezcló 1 ml de la suspensión de liposomas PC con 1 ml de solución acuosa de VNP (solución acuosa MB o solución acuosa VNP-MB). La concentración final de MB fue 10 μmol / L y VNP, 1 g / L. La concentración de PC en las soluciones fue de 0,6 mmol / L. Las soluciones acuosas obtenidas se colocaron en cubetas de cuarzo (10 × 10 mm) y se irradiaron con lámpara de mercurio de 250 W (paso de banda l =310–400 nm, el flujo de luz fue de 43 W / cm 2 ) durante 30 min. Luego, se registró la absorbancia de las suspensiones a 234 nm (dienos conjugados máximo) usando un espectrofotómetro Specord 200 (Analytik Jena, Alemania). Se tomó como control la concentración de dienos conjugados formados en agua sin ningún aditivo (NP, MB o complejos VNP-MB). Cada punto experimental fue el valor medio de al menos tres pruebas independientes. El procesamiento estadístico se realizó mediante el paquete de software Statistika v. 5.0 (StatSoft, EE. UU.).
OH · detección de radicales
Para detectar la formación de radicales hidroxilo en la solución bajo irradiación UV, se utilizó cumarina como molécula sonda. La cumarina reacciona con los radicales OH · produciendo 7-hidroxicumarina altamente fluorescente [32, 33]. El procedimiento experimental fue el siguiente. La solución acuosa de cumarina (0,1 mmol / L) se mezcló con MB (10 µmol / L), VNP (0,1, 1 o 10 g / L) o VNP-MB soluciones acuosas. Las soluciones acuosas obtenidas se colocaron en cubetas de cuarzo (10 × 10 mm) y se irradiaron con láser He-Cd λ exc =325 nm durante 1 h. En caso de irradiación con rayos X, la cubeta se irradió desde arriba (desde la parte abierta) mediante rayos X utilizando un aparato ISOVOLT 160 Titan E con un cátodo de tungsteno durante 30 min. El voltaje en el tubo fue de 30 kV (20 mA). La distancia del tubo de rayos X a las muestras irradiadas fue de 25 cm. Los espectros de fluorescencia (excitados a 325 nm) de las soluciones se registraron con un espectrofluorímetro Lumina (Thermo Scientific, EE. UU.). Se analizó la intensidad relativa de la fluorescencia de la 7-hidroxicumarina.
Detección de oxígeno singlete
1 O 2 La producción en las soluciones que contienen VNP, MB o complejos VNP-MB se analizó en la evaluación de los espectros de fluorescencia de ADPA [34, 35]. Las medidas se realizaron en cubetas de cuarzo (10 x 10 mm). La solución acuosa de ADPA (10 μmol / L) se mezcló con soluciones acuosas de MB (10 μmol / L), NP (1 g / L) o VNP-MB en cubetas. Las soluciones se irradiaron a 457 nm usando láser azul de estado sólido de alta estabilidad MBL-457, 50 mW (Changchun New Industries Optoelectronics Tech. Co., Ltd.). La emisión de fluorescencia de ADPA excitada a 378 nm se recogió en diferentes escalas de tiempo (0, 10, 20, 30, 40 y 60 min) utilizando un espectrofluorímetro Lumina (Thermo Scientific, EE. UU.).
Resultados y discusiones
Característica de los VNP sintetizados
Figura 1 ay archivo adicional 1:La figura S1 muestra las imágenes TEM de VNP sintetizados con un histograma de distribución lateral y un patrón XRD, que admiten GdVO 4 :Eu 3+ NPs estructura cristalina. GdVO sintetizado 4 :Eu 3+ Los NP tienen forma de huso con un tamaño de 8 × 25 nm ± 5 nm y una estructura de fase tetragonal de tipo circón. La carga negativa de la superficie de las NP (el potencial ζ es - 18,75 ± 0,15 mV, pH =7,8) se debe a los grupos carboxilato del estabilizador de EDTA disódico utilizado durante la síntesis. El diámetro hidrodinámico excedente de GdVO 4 :Eu 3+ nanopartículas es 44,0 ± 0,3 nm. El espectro de absorción de GdVO 4 :Eu 3+ NP representa la banda ancha intensa en el rango espectral de 250-350 nm que corresponde a una transferencia de carga de los ligandos de oxígeno al átomo de vanadio en el grupo \ ({VO} _4 ^ {3-} \) (Fig. 1b) [36 ]. Dopaje GdVO 4 NP con Eu 3+ iones imparte una fuerte fluorescencia a los VNP en el rango espectral rojo, que se rige por la transición dentro de la configuración del electrón f de los iones de europio [37] (no se discutirá en este documento).
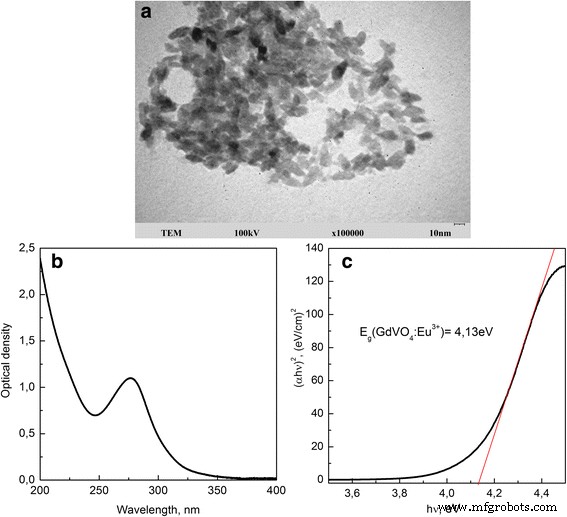
Imagen TEM ( a ), espectro de absorción ( b ) y la dependencia energética de ( αhv ) 2 ( c ) de GdVO 4 :Eu 3+ nanopartículas
Se sabe que el tamaño de las NP afecta la brecha de energía óptica en los materiales semiconductores. La energía de la banda prohibida, E g , se puede estimar a partir de la longitud de onda del borde de absorción de la transición entre bandas de acuerdo con la relación de Tauc [38]:
$$ {\ left (a \ mathrm {hv} \ right)} ^ {\ left (1 / n \ right)} =A \ cdot \ left (\ mathrm {hv} - {E} _g \ right), $ $ (1)donde a es el coeficiente de absorción, hv es la energía del fotón incidente, A es la constante independiente de la energía (el parámetro de cola de banda), y n es la constante (factor de potencia del modo de transición), que depende de la naturaleza material (cristalina o amorfa). El valor de n denota la naturaleza de la transición, n =1/2 para transiciones directas permitidas, n =3/2 para transiciones prohibidas directas, n =2 para transiciones indirectas permitidas y n =3 para transición prohibida indirecta [39]. GdVO 4 es un semiconductor de brecha directa, para el cual n =1/2 [40] Por lo tanto, la ecuación. (1) se puede reescribir como:
$$ {\ left (\ alpha \ mathrm {hv} \ right)} ^ 2 =A \ cdot \ left (\ mathrm {hv} - {E} _g \ right) $$ (2)Coeficiente de absorción ( a ) se calcula a partir de la absorbancia como a =2.303 D / l , donde D es la absorbancia y l es la longitud de la ruta óptica.
La figura 1c representa la dependencia energética de ( a hv) 2 para GdVO sintetizado 4 :Eu 3+ nanopartículas. El valor de la banda prohibida E g se determinó por extrapolación de la parte lineal de ( a hv) 2 curva frente a la energía del fotón hv a cero. El valor obtenido E g =4.13 eV es más alto que el informado para GdVO 4 :Eu 3+ polvos con un tamaño de cristalito que varía entre 14,4 y 43 nm (3,56–3,72 eV) [41, 42]. Suponemos que podría deberse a la diferencia en los métodos de síntesis utilizados que, en nuestro caso, dan NP más pequeñas con una banda de absorción angosta y desplazada al azul en comparación con la obtenida por los métodos hidrotermal o de Pechini.
Generación de radicales libres fotoinducidos (prueba de dienos conjugados)
Se acepta comúnmente que los tipos de árbol de ROS (\ (\ mathrm {OH} \ cdotp, {\ mathrm {O}} _ 2 ^ {\ cdotp -} \) y 1 O 2 ) que se generan en los sistemas NP bajo irradiación UV contribuyen al principal estrés oxidativo en los sistemas biológicos [43, 44]. Aunque la actividad fotocatalítica de NP de óxidos metálicos como TiO 2 , ZnO, CuO, Director ejecutivo 2 , Al 2 O 3 y Fe 2 O 3 está bien descrito [17,18,19,20], poca investigación ha estudiado la actividad fotocatalítica de ReVO 4 NP [45,46,47,48]. Se demostró que ReVO 4 Los NP son eficaces en la destrucción fotocatalítica de contaminantes orgánicos. Sin embargo, ninguna investigación ha estudiado los tipos de ROS generados por ReVO 4 NP bajo irradiación UV.
Para imitar el entorno biológico, utilizamos una suspensión de liposomas de PC y detectamos la generación de radicales libres bajo irradiación UV en las suspensiones que contienen MB, VNP o complejos VNP-MB en la oxidación de lípidos (prueba de formación de dienos conjugados) [49,50,51]. La oxidación de lípidos por el oxígeno molecular a través de reacciones en cadena de radicales puede iniciarse mediante radiación ionizante cuando aparecen ROS y radicales libres en el sistema [43, 44]. Las reacciones en cadena radicales que involucran ácidos grasos poliinsaturados causan una reordenación de los dobles enlaces que conducen a dienos conjugados. Los dienos conjugados resultantes exhiben una banda de absorción a 234 nm que podría detectarse fotométricamente. La Figura 2 muestra las concentraciones relativas de dienos conjugados formados en suspensiones de lípidos que contienen MB, VNP o complejos VNP-MB. Se pudo ver que en todas las soluciones, la concentración de dienos conjugados aumenta en comparación con la suspensión de liposomas PC pura. Sin embargo, la eficiencia de este proceso es diferente. El azul de metileno es una de las moléculas fotosensibilizadoras convencionales con el máximo de absorción principal λ máx =665 nm y una banda de absorción menos intensa en el rango espectral UV (archivo adicional 1:Figura S2). Bajo irradiación UV de MB, pueden tener lugar los dos procesos fotoquímicos principales [34, 52]. El MB excitado por la luz ultravioleta se somete a un proceso de cruce entre sistemas ( Q p =0.54 [53]) al estado de triplete de larga duración ( 3 MB * ) y reacciona con moléculas de oxígeno ( 3 O 2 ) formando oxígeno singlete ( 1 O 2 ):
$$ {\ mathrm {MB}} ^ {+} + hv \ to {} ^ 3 {\ mathrm {MB}} ^ {+ ^ {\ ast}} $$ (3) $$ {} ^ 3 {\ mathrm {MB}} ^ {+ ^ {\ ast}} + {} ^ 3 {\ mathrm {O}} _ 2 \ to {\ mathrm {MB}} ^ {+} + {} ^ 1 {\ mathrm {O }} _ 2 $$ (4)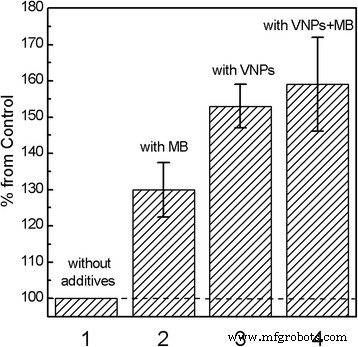
Eficacia relativa de la formación de dienos conjugados en suspensiones lipídicas:1 - sin aditivos; 2 - con MB; 3 - con VNP; 4 - con complejos VNPs-MB
El segundo proceso fotoquímico puede tener lugar a altas concentraciones de MB. Las moléculas de MB en el estado fundamental pueden actuar como agentes reductores donando un electrón al triplete de MB y formando el radical semi-reducido (MB ·) y el radical semi-reducido, respectivamente (MB · 2+ ) [52]:
$$ {} ^ 3 {\ mathrm {MB}} ^ {+ ^ {\ ast}} + {\ mathrm {MB}} ^ {+} \ to \ mathrm {MB} \ cdotp + {\ mathrm {MB} } ^ {\ cdotp 2+} $$ (5)La oxidación de MB · por el oxígeno molecular que devuelve el colorante en estado fundamental y conduce a la producción de radicales superóxido (\ ({O} _2 ^ {\ cdotp -} \)):
$$ \ mathrm {MB} \ cdotp + ^ 3 {\ mathrm {O}} _ 2 \ kern0.5em \ to {\ mathrm {MB}} ^ {+} + {O} _2 ^ {\ cdotp -} $$ (6)Los radicales singlete de oxígeno y superóxido, así como los radicales MB formados en las Reacciones (4) - (6) pueden afectar el proceso de oxidación de lípidos. En solución diluida donde no se observa formación de dímero MB ([MB] <20 µM), predominarán las Reacciones (3) y (4) [52]. Sin embargo, en los complejos VNPs-MB debido al aumento de la concentración de MB dentro de la superficie de las VNPs [29], puede tener lugar el segundo proceso fotoquímico. Por lo tanto, el aumento de la formación de dieno conjugado en la suspensión de lípidos que contiene MB puede explicarse por la acción de MB como 1 O 2 fotogenerador bajo irradiación UV. Cabe señalar que la eficiencia de este proceso es mucho menor que la de la excitación MB dentro del máximo de absorción de longitud de onda larga.
En la suspensión que contiene GdVO 4 :Eu 3+ nanopartículas, la oxidación de lípidos es más eficaz. Este efecto podría atribuirse al comportamiento fotocatalítico de las VNP bajo irradiación UV. Electrones de banda conductora (e - ) y agujeros de la banda de valencia (h + ) formado bajo irradiación UV ( E > E g ) pueden interactuar con moléculas de agua y oxígeno molecular adsorbidas en la superficie de las NP mediante las siguientes reacciones [18, 20, 47]:
$$ {} ^ 3 {\ mathrm {O}} _ 2+ {e} ^ {-} \ to \ kern0.5em {\ mathrm {O}} _ 2 ^ {.-} $$ (7) $$ {\ mathrm {H}} _ 2 \ mathrm {O} + {\ mathrm {h}} ^ {+} \ to \ mathrm {OH} \ cdot $$ (8)Los iones hidroxilo formados durante la fotólisis del agua y adsorbidos en la superficie de las NP también pueden interactuar con los orificios para producir radicales hidroxilo:
$$ {\ mathrm {OH}} ^ {-} + {\ mathrm {h}} ^ {+} \ to \ mathrm {OH} \ cdot $$ (9)Además, la oxidación de \ ({O} _2 ^ {\ cdotp -} \) produce oxígeno singlete [18, 21, 22]:
$$ {\ mathrm {O}} _ 2 ^ {\ cdotp -} + {\ mathrm {h}} ^ {+} {\ to} ^ 1 {\ mathrm {O}} _ 2 $$ (10)Su reacción con iones de hidrógeno conduce a la formación de peróxido de hidrógeno:
$$ 2 {\ mathrm {O}} _ 2 ^ {\ cdotp -} + 2 {\ mathrm {H}} ^ {+} \ to {\ mathrm {H}} _ 2 {\ mathrm {O}} _ 2 $$ (11)como resultado de su interacción con electrones, se pueden formar radicales hidroxilo e iones hidroxilo:
$$ {\ mathrm {H}} _ 2 {\ mathrm {O}} _ 2 + {\ mathrm {e}} ^ {-} \ to \ mathrm {OH} \ cdot + {\ mathrm {O} \ mathrm {H} } ^ {-} $$ (12)Por lo tanto, el aumento en la eficiencia de la concentración de dienos conjugados en una suspensión que contiene VNP (Fig. 2, columna 3) puede atribuirse a los productos que se generan a través de las Reacciones (7) - (12) y facilitan la oxidación de lípidos.
En la suspensión de lípidos que contiene complejos VNPs-MB, las concentraciones más altas de dienos conjugados pueden explicarse por productos generados tanto a través de las Reacciones (3) - (6) como de la Reacción (7) - (12) (Fig. 2, columna 4). Además, en los complejos VNPs-MB en la Reacción (3) y (4), la generación de oxígeno singlete podría tener lugar debido a la excitación directa de MB y mediante la transferencia de energía de excitación no radiativa de VNP a MB que es bastante eficaz en esta composición [29].
Detección de radicales hidroxilo
El siguiente paso fue examinar más exactamente la eficiencia de OH · y 1 O 2 generación en las soluciones bajo irradiación de rayos X / UV. La cumarina se utilizó como molécula sonda para validar la aparición de radicales hidroxilo en las soluciones consideradas. Se sabe que los radicales OH · son uno de los principales productos de la fotólisis / radiólisis del agua bajo radiación UV / rayos X [5, 6]. En solución acuosa, los radicales OH · interactúan con las moléculas de cumarina para formar un producto altamente fluorescente 7-hidroxicumarina (ver esquema en la Fig. 3) que podría detectarse espectroscópicamente por la aparición de una nueva banda ( λ máx ~ 460 nm) se desplazó hacia la región espectral de longitud de onda larga con respecto a la banda de fluorescencia de cumarina ( λ máx ~ 400 nm), Fig. 3 [32, 33]. Cuanto mayor es la concentración de radicales OH · en la solución, más eficaz es la oxidación de la cumarina y, en consecuencia, más intensa es la banda de longitud de onda larga. Por lo tanto, el análisis de la intensidad relativa de la banda de longitud de onda larga podría proporcionar información sobre la concentración de radicales OH · en la solución bajo el efecto de varios factores.
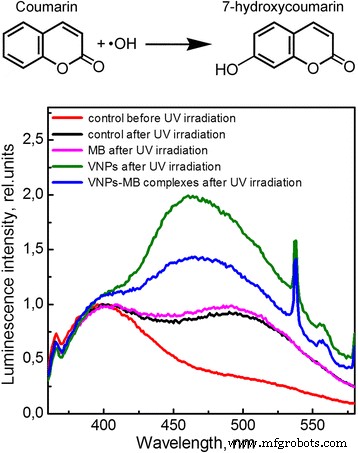
Reacción de cumarina con radical hidroxilo para formar 7-hidroxicumarina fluorescente. Espectros de fluorescencia normalizados de una solución acuosa de cumarina, λ exc =325 millas náuticas
Los espectros de emisión de fluorescencia de la solución de agua de cumarina que contiene MB, VNP o complejos de VNP-MB medidos después de 1 h de iluminación UV se presentan en la Fig. 3. Se muestra que la irradiación UV de la solución de agua de cumarina sin ningún aditivo (control) provoca una formación de una nueva banda de fluorescencia de longitud de onda larga que indica la generación de radicales OH · y oxidación de cumarina (Fig. 3). En presencia de moléculas de MB en la solución, la intensidad relativa de esta banda no cambia, lo que indica que no hay efectos adicionales de MB en la generación de radicales OH · (Fig. 3). En la solución que contiene VNP, la intensidad de la banda de 7-hidroxicumarina aumenta notablemente (Fig. 3) debido a la actividad fotocatalítica de VNP bajo irradiación UV, Reacciones (8), (9) y (12). Observemos que los picos agudos alrededor de 535–540 nm pertenecen a la fluorescencia del ión europio en GdVO 4 :Eu 3+ nanopartículas (transiciones de intraconfiguración). En la solución que contiene complejos VNPs-MB, la intensidad relativa de la banda de 7-hidroxicumarina fue aproximadamente dos veces más pequeña en comparación con la de la solución que contiene VNPs que apunta a la producción de radicales OH · menos efectiva (Fig. 3). Esto puede explicarse por el hecho de que la adsorción del colorante MB dentro de la superficie de las VNP puede prevenir la adsorción de moléculas de agua e iones hidroxilo y, en consecuencia, reduce la actividad fotocatalítica de las VNP en relación con la generación de radicales OH · a través de las Reacciones (8) y (9). Además, en los complejos VNPs-MB, una parte de la energía adsorbida se transfiere de forma no radiativa a las moléculas MB [29], lo que también disminuye la eficiencia de la producción de pares de electrones y huecos y, en consecuencia, la capacidad de las VNP para la generación de radicales OH · en dichos complejos.
Se observaron resultados inesperados bajo la irradiación de rayos X de las soluciones que contenían VNP (Fig. 4). Contrariamente al caso de la irradiación UV, observamos que la intensidad relativa de la banda de 7-hidroxicumarina disminuye en comparación con la solución acuosa de cumarina sin nanopartículas que indica la captación de radicales OH · formados en las soluciones como resultado de la radiólisis del agua. El efecto observado depende en gran medida de las concentraciones de VNP (Fig. 4). Cabe señalar que la discusión principal sobre la capacidad de las nanopartículas para servir como eliminador de ROS se centra principalmente en CeO 2 nanocristales (nanoceria) [54,55,56,57]. Las principales características que obligan a nanoceria a actuar como eliminador de ROS se atribuyen generalmente al alto contenido de vacantes de oxígeno y Ce 3+ iones en nanoceria y su cambio entre estados de oxidación 3+ y 4+. Sin embargo, la dependencia crítica de la actividad biológica de la nanoceria en su tamaño y mecanismo de autorregeneración todavía está en discusión [54,55,56,57]. Observamos también que los efectos protectores de GdVO 4 :Eu 3+ y director ejecutivo 2 NPs contra daños inducidos por rayos X se observaron en experimentos in vivo anteriores de nuestro grupo [57]. A nuestro leal saber y entender, la capacidad de GdVO 4 :Eu 3+ La nanopartícula para barrer los radicales OH · generados en la solución de agua bajo irradiación de rayos X se ha observado por primera vez y requiere una investigación más profunda.
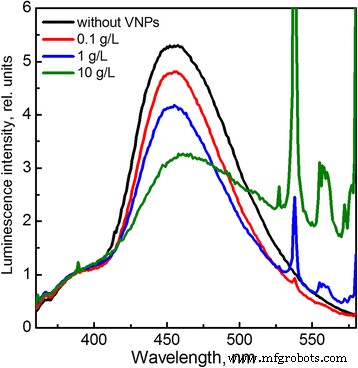
Espectros de fluorescencia normalizados de una solución acuosa de cumarina que contiene diferentes concentraciones de VNP registrados después de 30 min de irradiación con rayos X
Generación de oxígeno singlete
Evaluar la eficiencia de los complejos VNP-MB de 1 O 2 generación en agua, utilizamos el método de oxidación ADPA basado en oxígeno singlete con formación de endoperóxido no fluorescente ADPAO 2 (Figura 5). Por tanto, en presencia de oxígeno singlete, la fluorescencia de ADPA se apaga de forma irreversible. Debemos tener en cuenta que bajo la irradiación UV, las moléculas de ADPA se someten a un fuerte fotoblanqueo que complica la identificación de los impactos de MB, VNP o complejos VNP-MB asociados con el 1 O 2 Generacion. Para superar este inconveniente, aplicamos irradiación láser a 457 nm, que coincide con uno de los picos de excitación de Eu 3+ iones dopados en GdVO 4 nanocristales (archivo adicional 1:Figura S3). La Figura 5 muestra que las moléculas de ADPA no experimentan reacciones fotoquímicas con la irradiación de luz de 457 nm. En la solución que contiene MB, se pudo observar una ligera disminución de la intensidad de ADPA en el tiempo (Fig. 5) que se asocia con una ligera excitación de MB a esta longitud de onda y acción como fotosensibilizador según la Reacción (3) y (4). El mismo efecto se observa para la solución que contiene VNP (Fig.5) y podría atribuirse a la formación de radicales \ ({O} _2 ^ {\ cdotp -} \) en la superficie de los VNP (Reacción (7)) seguida por su oxidación según la Reacción (10) con generación de oxígeno singlete. La extinción de la fluorescencia de ADPA más fuerte se observa en los complejos VNPs-MB. La eficiencia de este proceso es dos veces mayor que en la solución con MB o VNP. La mayor eficiencia de la generación de oxígeno singlete en la solución que contiene los complejos VNP-MB está asociada con la transferencia de energía de los VNP al MB en los complejos, en los que los VNP sirven como transductor de energía para el fotosensibilizador de MB.
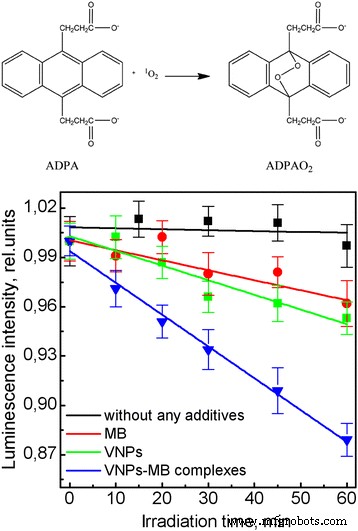
Reaction of ADPA with singlet oxygen to form endoperoxide ADPAO2 . ADPA photobleaching after irradiation with λ = 457 nm in water solutions
Unfortunately, due to ADPA sensor instability, we were not successful to measure the efficiency of the 1 O 2 generation in water solution under X-ray excitation.
Conclusiones
The efficiency of ROS generation in water solutions containing GdVO4 :Eu 3+ nanoparticles and their complexes with MB have been analyzed under UV-Vis and X-ray irradiation by three methods (conjugated dienes test, OH· radical, and singlet oxygen detection). Complexes VNPs–MB reveal high efficiency of ROS generation under UV-Vis irradiation associated with both high efficiency of OH· radicals generation by VNPs and 1 O 2 generation by MB due to nonradiative excitation energy transfer from VNPs to MB molecules. For the first time, the strong OH· radicals scavenging by VNPs has been observed under X-ray irradiation. Our observation indicates that VNPs–MB complexes can be potentially used to activate photodynamic therapy.
Abreviaturas
- MB:
-
Methylene blue
- PD:
-
Photosensitizer
- ROS:
-
Reactive oxygen species
- VNPs:
-
Gadolinium orthovanadate GdVO4 :Eu 3+ nanopartículas
Nanomateriales
- Problemas legales en la computación en la nube y sus soluciones
- Explicación del mantenimiento reactivo:desafíos y soluciones comunes
- Nanopartículas de oro multifuncionales para aplicaciones terapéuticas y diagnósticas mejoradas:una revisión
- Preparación de nanopartículas de mPEG-ICA cargadas con ICA y su aplicación en el tratamiento del daño celular H9c2 inducido por LPS
- Adaptación de la toxicidad de las especies reactivas del oxígeno a la terapia tumoral avanzada
- Estados electrónicos de nanocristales dopados con oxígeno y emisión visible en silicio negro Preparado por ns-Laser
- Síntesis fácil de compuesto de CuSCN coloreado y conductor recubierto con nanopartículas de CuS
- La preparación de la nanoestructura yema-cáscara de Au @ TiO2 y sus aplicaciones para la degradación y detección del azul de metileno
- Promoción del crecimiento celular SH-SY5Y mediante nanopartículas de oro modificadas con 6-mercaptopurina y un péptido penetrante de neuronas
- Síntesis fácil y respetuosa con el medio ambiente de nanocables de Co3O4 y su prometedora aplicación con grafeno en baterías de iones de litio
- Síntesis y caracterización de BiOCl modificado y su aplicación en la adsorción de tintes de baja concentración a partir de una solución acuosa



