La preparación de la nanoestructura yema-cáscara de Au @ TiO2 y sus aplicaciones para la degradación y detección del azul de metileno
Resumen
Este artículo informa la síntesis de un nuevo tipo de Au @ TiO 2 nanoestructuras yema-cáscara mediante la integración del método de pulverización iónica con la técnica de deposición de capa atómica (ALD) y sus aplicaciones como fotocatalizador de luz visible y sustrato de espectroscopía Raman mejorada en la superficie (SERS). Tanto el tamaño como la cantidad de nanopartículas de oro confinadas en TiO 2 Los nanotubos podrían controlarse fácilmente ajustando correctamente el tiempo de pulverización catódica. La estructura y morfología únicas del Au @ TiO 2 resultante Las muestras se investigaron mediante el uso de diversas técnicas espectroscópicas y microscópicas en detalle. Se ha encontrado que todas las muestras analizadas pueden absorber luz visible con una absorción máxima en longitudes de onda de resonancia de plasmón superficial localizado (LSPR) (550–590 nm) que están determinadas por el tamaño de las nanopartículas de oro. El Au @ TiO 2 Se utilizaron compuestos de yema y cáscara como fotocatalizador para la degradación del azul de metileno (MB). En comparación con TiO 2 puro nanotubos, Au @ TiO 2 los compuestos exhiben propiedades fotocatalíticas mejoradas frente a la degradación de MB. El efecto SERS de Au @ TiO 2 También se realizaron compuestos de yema y cáscara para investigar la sensibilidad de detección de MB.
Antecedentes
Los nanocompuestos heterogéneos de metales / semiconductores han atraído un enorme interés de investigación debido a sus propiedades físico-químicas únicas y sus aplicaciones potenciales en la conversión de energía solar [1], biomedicina [2], dispersión Raman mejorada en la superficie [3], diodos emisores de luz [4 ] y remediación ambiental [5]. Motivados por sus diversas aplicaciones, se han realizado un gran número de esfuerzos para diseñar y modular las composiciones, nanoestructuras y dimensiones de dichos materiales [6, 7, 8]. Por ejemplo, Yin et al. [9] sintetizó nanoestructuras híbridas de ZnO / Ag y ZnO / Pd y descubrió que la deposición de Ag o Pd sobre ZnO mejoraba enormemente la actividad fotocatalítica de ZnO. Sun y col. [10] demostró que Au-Fe 3 O 4 nanopartículas con interacciones a nanoescala entre Au y Fe 3 O 4 exhibió una rica variedad de propiedades magnéticas, físicas y químicas.
En los últimos años, se han realizado avances significativos en la síntesis controlada de metales / semiconductores aplicados a la fotocatálisis debido a los problemas ambientales cada vez más graves, como la contaminación del aire [11, 12] y las posibles aplicaciones técnicas en la conversión de energía [13]. Entre los diversos compuestos de metal / semiconductores que se han propuesto, los que involucran TiO 2 y nano Au son los más prácticos ya que dicha heteroestructura tiene una fuerte resonancia de plasmón de superficie localizada (LSPR) en el rango del espectro visible y lo convierte en un nuevo tipo de fotocatalizador de respuesta de amplio espectro [14, 15, 16]. Otra función ventajosa de Au / TiO 2 nanocomposites es que las nanopartículas de Au funcionan como almacenamiento de electrones, reduciendo eficazmente la recombinación de pares de electrones-huecos fotoexcitados y, finalmente, aumentando el rendimiento cuántico de la fotocatálisis [17, 18]. Algunas investigaciones innovadoras basadas en Au / TiO 2 El sistema compuesto aplicado en la degradación de colorantes orgánicos, la división del agua solar y la conversión de compuestos orgánicos han demostrado sus eficientes características fotocatalíticas de luz visible, lo que indica un papel crucial de los efectos plasmónicos de Au en Au / TiO 2 sistema [17, 19, 20].
Sin embargo, una de las principales limitaciones de Au / TiO 2 nanocomposites traducidos a aplicaciones prácticas es la escasa estabilidad de los catalizadores de oro soportados. Las excelentes propiedades presentadas en las nanopartículas originales pueden debilitarse, ya que tienden a aglomerarse y crecer en partículas más grandes bajo una variedad de condiciones de reacción [21, 22]. Y en algunos otros casos, se ha demostrado que las nanopartículas de Au depositadas en las superficies de TiO 2 es probable que sufran corrosión o disolución durante una reacción catalítica [23]. El diseño y la construcción de compuestos estructurados núcleo-cáscara y yema-cáscara se consideran un método eficaz para abordar estos problemas. Gong y col. [24] informó de la fabricación de nanovarillas de oro @ TiO 2 Catalizadores yema-cáscara con diferentes relaciones de aspecto de nanovarilla de oro a través de un método mediado por semillas. Los nanocompuestos híbridos multicomponente también presentan actividades fotocatalíticas mejoradas en la reacción de oxidación del alcohol bencílico. Zaera y colaboradores [21] informaron sobre la síntesis y caracterización de un nuevo Au @ TiO 2 catalizador nanoestructurado de cáscara de yema, que muestra una actividad promotora comparable a la observada con Au / TiO 2 más convencional catalizadores pero una estabilidad mejorada frente a la sinterización. Kim y col. [25] nanoestructuras plasmónicas de núcleo-capa sintetizadas que consisten en Au-TiO 2 compatible con SiO 2 esferas en células solares sensibilizadas con colorante (DSSC), que exhibieron eficiencias de conversión de energía mejoradas de forma observable de ~ 14%. A pesar de que se han realizado enormes esfuerzos de investigación, la síntesis fácil de Au @ TiO 2 los compuestos con una estructura de núcleo-cáscara / yema-cáscara bien definida siguen siendo un desafío para la aplicación masiva.
Recientemente, muchos estudios confirmaron que la quiralidad controlada a nanoescala podría inducir un mayor efecto LSPR porque una nanoestructura quiral multihelical puede dar lugar a birrefringencia inducida a escala microscópica y generar el efecto Kerr causado por un campo eléctrico inducido a escala macroscópica [26, 27,28]. En este estudio, Au @ TiO 2 Los nanocompuestos de yema y cáscara con estructura helicoidal similar a una fibra se han sintetizado con éxito mediante una estrategia fácil y controlable. Las nanopartículas de oro cargadas en la superficie de las nanobobinas de carbono (CNC) se produjeron mediante pulverización iónica. El TiO 2 películas con un espesor muy uniforme y controlado podrían integrarse de forma estable en la superficie de las nanopartículas de oro mediante una tecnología de deposición de capa atómica (ALD). Seguido de un paso de recocido, el Au @ TiO 2 Se obtuvieron nanocompositos. El método desarrollado anteriormente también se puede extender para fabricar otro metal (Pt, Ag) @TiO 2 nanocompuestos yema-concha con nanoestructura helicoidal. Como fotocatalizador representativo, las actividades fotocatalíticas del Au @ TiO 2 obtenido Los nanocompuestos se evaluaron mediante la degradación del azul de metileno (MB) bajo irradiación de luz visible. Además, las actividades de espectroscopía Raman mejorada en superficie (SERS) de Au @ TiO 2 Los nanocompuestos también se investigaron mediante la detección de MB.
Experimental
Síntesis de Au @ TiO 2
Los CNC utilizados como plantillas se prepararon mediante el método de deposición de vapor químico como se informó anteriormente. Brevemente, se utilizaron nanopartículas de acetileno y cobre como fuente de carbono y los catalizadores apropiados, respectivamente. El crecimiento de los CNC se realizó a presión atmosférica en un tubo de cuarzo horizontal. Se colocó en el reactor una placa de cerámica que contenía los catalizadores de cobre. Después de calentar el tubo a 250 ° C al vacío, se introdujo acetileno en el reactor [29, 30, 31]. Después de que el aparato se enfrió a temperatura ambiente, se obtuvieron los CNC preparados.
Los CNC obtenidos se dispersaron en etanol con agitación ultrasónica y luego se untaron uniformemente sobre la superficie de un portaobjetos de vidrio. Después de secarse al aire ambiente, la capa de Au se depositó mediante un instrumento de pulverización iónica (Hitachi, E-1010). El tamaño y el espesor de las películas de Au se determinaron mediante la corriente de descarga y el tiempo de pulverización catódica. En este paso, la corriente de descarga fue de 10 mA y el tiempo de pulverización varió de 30 a 120 s. Las muestras obtenidas se marcaron como CNCs @ Au- x , en el que x se refiere al tiempo de pulverización catódica (segundos). Posteriormente, las muestras se dispersaron en etanol mediante agitación ultrasónica y luego se extendieron sobre una oblea de cuarzo para recubrirlas con TiO 2 por proceso ALD. ALD es un tipo de técnica de preparación de revestimiento en fase de vapor y puede lograr un control preciso del espesor y una excelente uniformidad de las películas [32,33,34,35,36]. El proceso ALD se llevó a cabo en un reactor ALD tipo flujo de pared caliente a 145 ° C con tetraisopropanolato de titanio (TTIP) y H 2 desionizado O utilizado como precursores de titanio y oxígeno, respectivamente. Finalmente, después del proceso ALD, las nanobobinas recubiertas anteriormente se calcinaron a 450 ° C durante 2 h en aire a presión ambiente para eliminar los núcleos de carbono y el TiO 2 helicoidal. Se obtuvieron estructuras de caparazón de yema de Au recubiertas. A modo de comparación, el TiO 2 puro El tubo helicoidal también se recogió con TiO 2 calcinado -revestidos CNC sin pulverización catódica de Au y se denota como TiO 2 en la siguiente discusión.
Caracterización del material
Los patrones de difracción de rayos X (XRD) se registraron en un difractómetro Bruker D8 Advance con cobre Kα ( λ =0,154056 nm) fuente de radiación. Las imágenes de microscopía electrónica de barrido (SEM) se adquirieron con un microscopio Hitachi S-4800. Se obtuvieron imágenes de microscopía electrónica de transmisión (TEM), difracción electrónica de área seleccionada (SAED) y TEM de alta resolución (HRTEM) utilizando un instrumento de microscopio JEOL JEM-2100 operado a 200 kV. Los datos de espectroscopía de fotoelectrones de rayos X (XPS) se adquirieron usando un espectrómetro PHI5000 Versaprobe-II con una fuente monocromática de Al Kα (1486,6 eV). Los espectros de absorción óptica se registraron utilizando un espectrofotómetro de absorción PerkinElmer Lambda 750s UV-Vis-NIR. Los espectros de dispersión Raman se registraron en un espectrómetro Renishaw Invia Reflex Laser Raman. La longitud de onda de excitación fue de 514 nm de un láser de iones de argón enfriado por aire con una potencia efectiva de 2 mW.
Evaluación de actividades fotocatalíticas
Las actividades fotocatalíticas de los catalizadores se investigaron mediante la fotodegradación de colorantes MB en soluciones acuosas usando el procedimiento que se describe a continuación. Se esparcieron uniformemente dos miligramos de catalizador en un fotorreactor de 100 ml equipado con tuberías de agua de refrigeración circulantes. Luego, se añadieron al fotorreactor 20 ml de soluciones de MB 0,01 mg / ml. Antes de la fotoirradiación, el sistema se mezcló ultrasónicamente durante 2 min y se agitó magnéticamente bidireccionalmente durante 30 min en la oscuridad para equilibrar la adsorción-desorción entre los fotocatalizadores y MB. A continuación, se irradió la suspensión que contenía el fotorreactor de 100 ml anterior bajo una lámpara de xenón de 300 W (Beijing Perfectlight Technology Co. Ltd., PLS-SXE300C) con filtros de corte para que las longitudes de onda de luz entre 420 y 780 nm alcanzaran las soluciones. Durante el proceso de reacción fotocatalítica, la intensidad de irradiación fue de ~ 154 mW cm −2 y el agua de refrigeración se mantuvo fluyendo para disipar el efecto térmico del sistema. En los intervalos de tiempo de cada 10 min durante un tiempo total de 90 min, se pipeteó una porción (1 mL) de las suspensiones y se diluyó inmediatamente a 3 mL, y se recogieron 2 mL de sobrenadante después de la separación centrífuga. Finalmente, la concentración residual de MB en el sobrenadante se analizó utilizando un espectrofotómetro UV-Vis-NIR en la longitud de onda característica de la solución ( λ MB =664 nm).
Resultados y discusión
Análisis de estructura de fase y morfología
La Figura 1a muestra un flujo de preparación esquemático de Au @ TiO 2 heteroestructura yema-cáscara, incluida la pulverización catódica de Au, TiO 2 procesos de recubrimiento y calcinación. La Figura 1b-e muestra imágenes TEM típicas correspondientes a cada procedimiento anterior. Los CNC utilizados como plantilla de partida en este trabajo tienen un diámetro de fibra, un diámetro de bobina y un paso de bobina uniformes, y el diámetro medio de la fibra es de aproximadamente 80 nm (archivo adicional 1:Figura S1). Después del tratamiento de pulverización catódica de Au, la capa exterior de los CNC se revistió con numerosas nanopartículas uniformes de Au como se muestra en la Fig. 1c. Como se ve en la imagen TEM que se muestra en la Fig.1d, aplicando 200 ciclos ALD para TiO 2 deposición, un TiO 2 uniforme Recubrimiento con un espesor de aproximadamente 8 nm se recubre en la superficie de Au / CNC. Generalmente, la fase anatasa de TiO 2 tiene un rendimiento fotocatalítico mucho mejor que el del rutilo [37, 38]. Por esta razón, elegimos 450 ° C como temperatura de calcinación adecuada para eliminar los núcleos de carbono y obtener el Au @ TiO 2 final estructura yema-cáscara. Como se muestra en la Fig.1e, el TiO 2 Se formaron nanotubos con nanopartículas de Au encapsuladas y espacio libre. Después de todos los pasos de procesamiento, la elegante morfología helicoidal de los CNC de arranque se puede mantener bien.
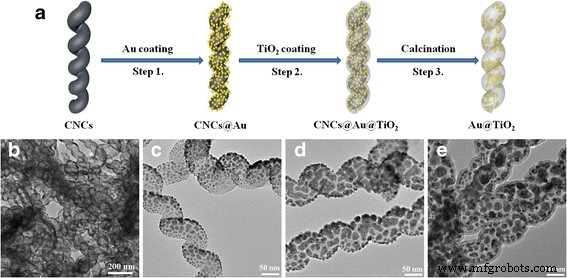
un Ilustración esquemática del proceso sintético de Au-x @ TiO 2 . b - e Las imágenes TEM revelan la evolución morfológica
La cristalinidad y las estructuras de todas las muestras se midieron mediante XRD. Como se observa en la Fig. 2a, los picos de difracción para TiO 2 puro La muestra se puede atribuir a una fase anatasa bien cristalizada (JCPDS 21-1272), sin picos de impurezas adicionales. Para Au / TiO 2 , los picos de difracción adicionales en la Fig. 2b-e se pueden indexar bien al Au cúbico centrado en la cara (FCC) (JCPDS 01-1174), que conformó el recubrimiento exitoso de nanopartículas de Au en la superficie de los CNC mediante bombardeo iónico. El TiO 2 El pico (004) a 38,2 ° tiene una gran superposición con el pico de Au (111) a 38,3 °. Es interesante que un pico débil ubicado a 35,5 grados en la Fig. 2b-e pueda indexarse al plano (020) de γ -Ti 3 O 5 , lo que indica que la relación atómica Ti / O no es exactamente 1/2 para Au / TiO 2 . En el presente trabajo, la fuerte acción reductora de la fibra de carbono y las nanopartículas de Au a altas temperaturas probablemente induce la producción de vacantes de oxígeno y estados de oxidación más bajos del titanio. Además, debido a la disminución del contenido relativo de TiO 2 , se puede observar que todo el TiO 2 los picos de difracción se vuelven más débiles con el aumento del tiempo de pulverización catódica de 30 a 120 s.
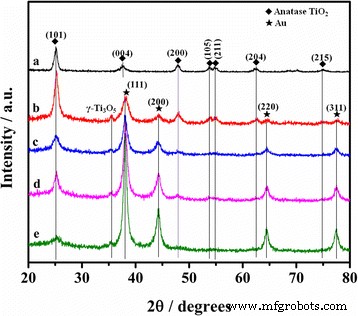
Patrones XRD. a TiO 2 . b Au-30 @ TiO 2 . c Au-50 @ TiO 2 . d Au-80 @ TiO 2 . e Au-120 @ TiO 2
La Figura 3 muestra las imágenes TEM de TiO 2 y Au-x @ TiO 2 con diferente tiempo de pulverización de Au ( x significa tiempo de chisporroteo, x =30, 50, 80, 120). Para TiO 2 , se puede observar que la muestra presenta una estructura tubular helicoidal similar a la de las plantillas CNC. No se produjo ningún colapso de los materiales de la cáscara durante el proceso de recocido para eliminar los núcleos de carbono. El TiO 2 la capa tiene un grosor de aproximadamente 8 nm después de 200 ciclos. Debido a un mayor número atómico de Au en comparación con el de Ti en Au @ TiO 2 , Las nanopartículas de Au muestran un contraste más oscuro que resulta en una morfología de la cáscara de la yema claramente visible. El diámetro medio de las nanopartículas de Au aumenta claramente con el aumento del tiempo de pulverización catódica. Asciende a aproximadamente 4.5, 5.5, 10.5 y 20.5 nm correspondientes al tiempo de pulverización catódica de 30, 50, 80 y 120 s, respectivamente (archivo adicional 1:Figura S2, a2-d2). Como se muestra en la Fig. 3b – d, el TiO 2 homogéneo También se obtiene una película delgada con un espesor de aproximadamente 8 nm para Au-30 @ TiO 2 , Au-50 @ TiO 2, y Au-80 @ TiO 2 nanocomposites con el mismo ALD TiO 2 declaración. Sin embargo, el espesor de TiO 2 carcasa para Au-120 @ TiO 2 disminuye a unos 5 nm (Fig. 3e), lo que puede atribuirse a la influencia del gran tamaño y las importantes conglomeraciones de nanopartículas de Au.
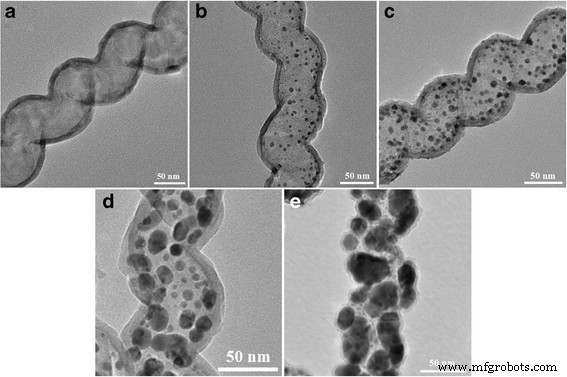
Imágenes TEM. un TiO 2 . b Au-30 @ TiO 2 . c Au-50 @ TiO 2 . d Au-80 @ TiO 2 . e Au-120 @ TiO 2
Las estructuras microscópicas detalladas del TiO 2 y Au-30 @ TiO 2 Las nanocomposiciones fueron investigadas más a fondo por HRTEM. Como se observa en la Fig. 4a-b, tanto TiO 2 las conchas y las nanopartículas de Au están bien cristalizadas asignadas a la anatasa TiO 2 (101) (0,3565 y 0,3501 nm) y redes cristalinas de Au (111) (0,2399 nm), respectivamente. Cabe señalar que la interfaz en Au / TiO 2 Las nanoestructuras yema-cáscara son claramente visibles (Fig. 4b) debido al diferente contraste. Esta rica interfaz es importante para la siguiente aplicación de fotocatálisis, ya que puede proporcionar el acceso para el transporte de electrones calientes desde nanopartículas de Au a TiO 2 tras la excitación LSPR [20]. El recuadro de la Fig. 4b muestra el patrón SAED registrado en Au-30 @ TiO 2 nanoestructura. Los anillos de difracción claros se pueden atribuir a (101) y (211) planos cristalinos de anatasa TiO 2 y planos cristalinos (220) y (111) de Au, respectivamente, de acuerdo con los resultados de XRD. Para analizar el estado químico del Au y adquirir información fundamental en profundidad sobre la interacción del Au con el TiO 2 , Au-30 @ TiO 2 El nanocompuesto se investigó más a fondo mediante mediciones de XPS. Los espectros de alta resolución de Ti 2p y Au 4f se presentan en la Fig. 4c yd, respectivamente. Como se muestra en la Fig. 4c, se pueden asignar dos picos con la energía de enlace de aproximadamente 458,4 y 464,2 eV a Ti 2p 3/2 y Ti 2p 1/2 componentes de la órbita de giro de Ti 4+ , respectivamente [39]. La Figura 4d muestra el espectro Au 4f XPS con dos picos que aparecieron a 83,6 y 87,4 eV para Au 4f 7/2 y Au 4f 5/2 niveles, respectivamente, lo que sugiere que las especies de Au existen en estado metálico. El cambio negativo relativo (0,4 eV) de Au 4f 7/2 pico en comparación con Au a granel (4f 7/2 a 84,0 eV) se puede atribuir a la transferencia de electrones de las vacantes de oxígeno del TiO 2 a Au, lo que confirma el fuerte Au / TiO 2 interacción [40, 41].
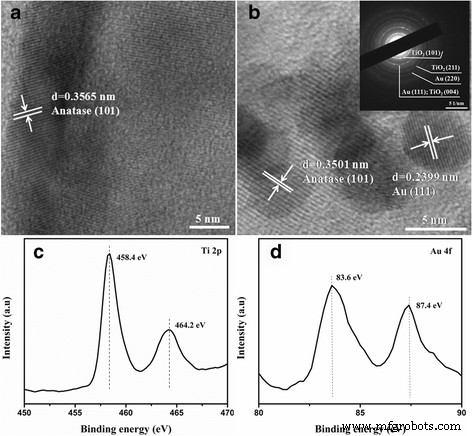
Imágenes HRTEM de a TiO 2 y b Au-30 @ TiO 2 , en el que la inserción superior derecha en b muestra los patrones SAED de Au-30 @ TiO 2 nanoestructura. XPS de alta resolución de c Ti 2p y d Au 4f de Au-30 @ TiO 2
La Figura 5 muestra los espectros de reflexión difusa UV-Vis del TiO 2 y Au-x @ TiO 2 nanoestructuras. Se observa una banda de absorción intensa por debajo de 400 nm para todas estas muestras, lo que puede deberse a la gran banda prohibida de la anatasa TiO 2 [42]. Comparado con TiO 2 , se puede encontrar que el Au-x @ TiO 2 no solo tiene una absorción similar por debajo de 400 nm, sino también un rango de absorción mejorado de 400 a 800 nm con un pico de absorción amplio a aproximadamente 580 nm derivado del efecto LSPR de las nanopartículas de Au [43]. Estos resultados indican que una mejor actividad fotocatalítica para Au-x @ TiO 2 se puede esperar bajo irradiación de luz visible, especialmente para Au-80 @ TiO 2 con mayor intensidad de absorción. El ligero cambio de la absorción LSPR para Au @ TiO 2 Las nanoestructuras con diferentes tiempos de pulverización catódica también son razonables, ya que las nanopartículas de Au son sensibles a su tamaño y al entorno circundante [24, 42]. Estas observaciones declaran que el Au-x @ TiO 2 Los fotocatalizadores pueden poseer un rango de captación de luz sintonizable mediante el ajuste de la forma, el diámetro y la morfología de las nanopartículas de Au [44].
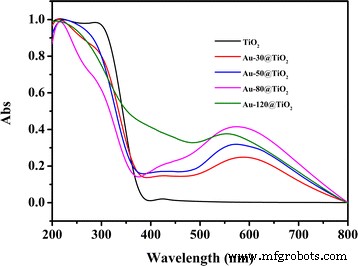
Espectros de absorción UV-Vis de TiO 2 y Au-x @ TiO 2
Actividad fotocatalítica
La eliminación de contaminantes orgánicos de las aguas residuales producidas por la industria y los hogares ha atraído mucha atención [45,46,47,48]. El MB se emplea con frecuencia como contaminante dirigido para evaluar la eficiencia catalítica en reacciones fotocatalíticas porque el color azul del MB de la absorción a 664 nm se desvanecería gradualmente con el proceso de degradación [49, 50] y se puede monitorear fácilmente mediante espectros de absorción UV-Vis. . Las actividades fotocatalíticas del TiO 2 y Au-x @ TiO 2 Los compuestos se evaluaron controlando la absorbancia del tinte MB a 664 nm para detectar la tasa de degradación bajo irradiación de luz visible (420 a 780 nm). Los cambios de la concentración relativa de MB frente al tiempo de irradiación sobre los diferentes catalizadores se presentan en la Fig. 6a. A modo de comparación, la actividad fotocatalítica del TiO 2 puro Primero se examinaron los nanotubos. Se puede encontrar que aproximadamente el 60% de MB se degradó con TiO 2 como fotocatalizador bajo irradiación de luz visible durante 90 min. La eficiencia fotocatalítica relativamente baja de TiO 2 se debe a su escasa capacidad de absorción de la luz visible. En comparación con el experimento en blanco anterior, el Au-x @ TiO 2 Los fotocatalizadores exhiben una mayor eficiencia de degradación y la eficiencia de degradación para Au-80 @ TiO 2 asciende a aproximadamente el 90% en las mismas condiciones experimentales. Las propiedades fotocatalíticas promotoras pueden atribuirse a una mayor tasa de generación de huecos de electrones debido a la presencia de heterointerfaz y la correspondiente absorción de luz mejorada por plasmón [51, 52]. Se sabe que tanto el plano de alta energía (200) de Au como el espesor de TiO 2 las conchas son parámetros importantes que afectan la actividad [24, 53]. Entre Au-x @ TiO 2 fotocatalizadores, con el aumento del tiempo de pulverización catódica, el pico de Au (200) exhibe más planos de alta energía, como se muestra en la intensidad del pico correspondiente de XRD. Además, Au-120 @ TiO 2 con TiO 2 más delgado shell (5 nm) no puede proporcionar suficientes sitios de reacción para el consumo de electrones. Por lo tanto, en base al espesor apropiado y similar de TiO 2 shell sobre diferentes Au-x @ TiO 2 , Au-80 @ TiO 2 muestra la actividad más alta.
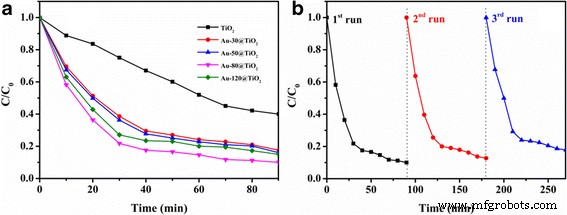
un Evaluación de la concentración de MB frente al tiempo de reacción en diferentes condiciones. b Reciclabilidad de la degradación fotocatalítica de solución acuosa de MB usando Au-80 @ TiO 2 con tres ciclos
Como catalizadores heterogéneos, la reutilización del catalizador también es muy importante en la aplicación práctica. Realizamos tres operaciones consecutivas para investigar la reutilización del Au-80 @ TiO 2 . Como se muestra en la Fig. 6b, no se observa una desactivación notable, lo que indica una excelente durabilidad de Au-80 @ TiO 2 . Imagen TEM de Au-80 @ TiO 2 (Archivo adicional 1:Figura S3) después del reciclaje de tres veces revela que las estructuras helicoidales de yema y cáscara de los catalizadores están bien mantenidas, lo que confirma además que el efecto confinado del TiO 2 Los nanotubos pueden prevenir la pérdida de Au y, por lo tanto, mejoran la estabilidad de los catalizadores.
Con base en los resultados anteriores, proponemos un proceso fotocatalítico para la degradación de MB utilizando Au @ TiO 2 helicoidal nanoestructuras (Fig. 7). Bajo irradiación de luz visible, los electrones calientes son producidos por el efecto LSPR de nanopartículas de Au dentro del TiO 2 nanotubos. Los electrones posteriores se transferirían de Au a la banda de conducción de TiO 2 . La degradación del MB adsorbido comenzaría a partir de agujeros (• Au + ) porque los agujeros pueden eliminar el agua adsorbida en la superficie, generando especies de radicales hidroxilo altamente reactivos [24, 51, 54]. Simultáneamente, el electrón inyectado en la banda de conducción de TiO 2 pueden ser atrapados por moléculas de oxígeno para formar radicales superóxido reactivos • O 2 - . Entonces, puede reaccionar más con H + para producir activos • HO 2 - y • radicales OH. Finalmente, los contaminantes orgánicos pueden ser destruidos por estos radicales formadores. En este trabajo, se cree que la luz polarizada rotada por la hélice quiral Au @ TiO 2 La estructura puede acelerar la excitación de LSPR, lo que mejora aún más la actividad fotocatalítica de Au @ TiO 2 helicoidal . Además, la molécula de MB adsorbida puede excitarse y transfiere un electrón a la banda de conducción de TiO 2 como el puro TiO 2 Los nanotubos muestran una pequeña actividad fotocatalítica bajo irradiación de luz visible. Por lo tanto, el efecto de fotosensibilización de MB también debería conducir a una pequeña parte de la descomposición de MB.
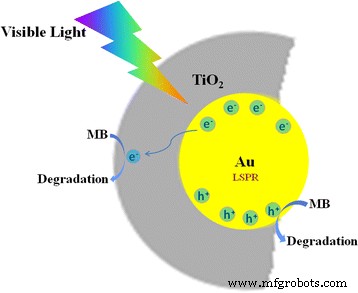
Representación esquemática del mecanismo de degradación fotocatalítica de MB sobre Au @ TiO 2
Actividad de SERS
Para aprovechar la aplicación multifuncional de tales catalizadores, llevamos a cabo los experimentos adicionales utilizando Au-x @ TiO 2 como sustratos de SERS para detectar las moléculas de MB adsorbidas en la superficie de las nanopartículas de oro. Como podemos ver en la Fig. 8a, al probarlo con 1.0 × 10 −5 Solución de MB M, la actividad de SERS del sustrato preparado disminuye con el aumento del tiempo de pulverización catódica de Au de 30 a 120 s. Este resultado indicó que Au-30 @ TiO 2 tiene el rendimiento SERS más excelente, lo que implica que las nanopartículas de Au entraron en contacto con TiO 2 las nanopartículas pueden formar un gran número de puntos calientes, lo que puede facilitar una mejora eficaz de la SERS [55]. Explorar la influencia de diferentes concentraciones de solución de MB en la capacidad de detección de Au-30 @ TiO 2 También se llevó a cabo la medición Raman. Como se presenta en la Fig. 8b, la intensidad de la señal Raman disminuye con la disminución de las concentraciones de MB que van desde 10 −4 a 10 −6 M. La señal Raman discernible de 10 −6 M MB con la banda Raman que varía de 900 a 1500 cm −1 , lo que indica que Au-30 @ TiO 2 actuó como sustrato de SERS, puede detectar concentraciones de MB tan bajas como 10 −6 M, que muestra posibles aplicaciones para la detección de contaminantes [56].
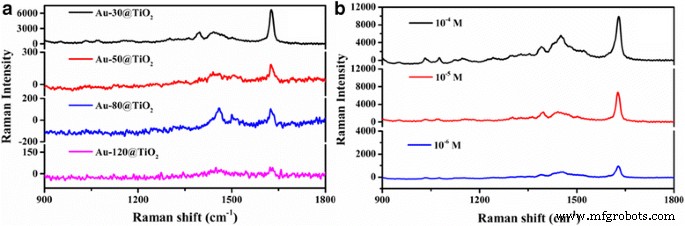
un Los espectros SERS de 1.0 × 10 −5 Solución de M MB recogida en los sustratos con diferentes Au-x @ TiO 2 . b Los espectros SERS de MB con diferentes concentraciones recogidos en el Au-30 @ TiO 2 sustrato
Conclusiones
En este estudio, hemos sintetizado con éxito Au @ TiO 2 nanocompuestos heterogéneos de concha de yema con morfología helicoidal en forma de espiral e investigaron su uso multifuncional, incluida la fotocatálisis y el efecto SERS. La degradación visible por fotocatálisis de MB muestra que el Au-x @ TiO 2 obtenido El compuesto con el tiempo de pulverización catódica de las nanopartículas de Au de 80 s muestra el mayor rendimiento fotocatalítico debido al aumento de la absorción de luz y la restricción de la recombinación de los pares de electrones y huecos fotoexcitados por el efecto LSPR de las nanopartículas de Au. Las mediciones Raman sugieren que el Au-x @ TiO 2 se pueden utilizar como sustratos activos SERS eficientes. Teniendo en cuenta sus fascinantes propiedades y características, el novedoso nanocompuesto heterogéneo puede proporcionar inspiración en varias áreas, incluida la división de agua y las células solares. Además, la cáscara de yema helicoidal Au @ TiO 2 El sistema modelo estudiado aquí puede extenderse al diseño de otras heteroestructuras, como Ag @ TiO 2 , Au @ ZnO y Au @ NiO, para su aplicación en conversión solar.
Nanomateriales
- Aprendizaje automático y visión inteligente para el sector industrial
- Nanopartículas de oro multifuncionales para aplicaciones terapéuticas y diagnósticas mejoradas:una revisión
- Nanopartículas para la terapia del cáncer:avances y desafíos actuales
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- Preparación de nanopartículas de mPEG-ICA cargadas con ICA y su aplicación en el tratamiento del daño celular H9c2 inducido por LPS
- Fabricación, caracterización y citotoxicidad de nanopartículas de carbonato de calcio derivadas de concha de oro-berberecho conjugado de forma esférica para aplicaciones biomédicas
- Una sonda fluorescente reanudable BHN-Fe3O4 @ SiO2 Nanoestructura híbrida para Fe3 + y su aplicación en bioimagen
- Saponinas Platycodon de Platycodi Radix (Platycodon grandiflorum) para la síntesis verde de nanopartículas de oro y plata
- Generación de especies reactivas de oxígeno en soluciones acuosas que contienen GdVO4:nanopartículas de Eu3 + y sus complejos con azul de metileno
- Las cáscaras de diatomeas de sílice diseñadas con nanopartículas de Au permiten el análisis sensible de moléculas para aplicaciones biológicas, de seguridad y medioambientales
- Preparación de NP de Ag encapsulado de silicalita-1 poroso jerárquico y su rendimiento catalítico para la reducción de 4-nitrofenol



