Fabricación, caracterización y citotoxicidad de nanopartículas de carbonato de calcio derivadas de concha de oro-berberecho conjugado de forma esférica para aplicaciones biomédicas
Resumen
La evolución de los nanomateriales en la ciencia ha provocado un aumento creciente en los campos de la nanotecnología, la biomedicina y la ingeniería. Este estudio tuvo como objetivo la fabricación y caracterización de nanopartículas de carbonato de calcio conjugadas de oro-cáscara de berberecho derivadas (Au-CSCaCO 3 NP) para aplicación biomédica. La técnica sintética empleada utilizó el método de reducción de citrato de nanopartículas de oro y un método de precipitación simple junto con el uso mecánico de un molino de bolas de rodillos programable. El nanomaterial conjugado sintetizado se caracterizó por sus propiedades fisicoquímicas utilizando microscopio electrónico de transmisión (TEM), microscopio electrónico de barrido de emisión de campo (FESEM) equipado con rayos X de energía dispersiva (EDX) y espectroscopia infrarroja por transformada de Fourier (FTIR). Sin embargo, la complejidad de los mecanismos celulares puede resultar un desafío para nanomateriales como Au-CSCaCO 3 NP y, por tanto, la necesidad de una evaluación de la citotoxicidad. Las nanopartículas de forma esférica obtenidas (verde violáceo claro) tienen un tamaño de diámetro medio de 35 ± 16 nm, una composición de alto contenido de carbono y oxígeno. El nanomaterial conjugado también posee un espectro único para el polimorfo de aragonito y el enlace carboxílico que respalda significativamente las interacciones entre las nanopartículas conjugadas. La carga superficial negativa y el espectro de absorbancia destacaron su estabilidad. El Au-CSCaCO 3 conjugado de forma esférica resultante Los NP podrían ser un gran nanomaterial para aplicaciones biomédicas.
Antecedentes
La producción de nanopartículas monodispersas ha surgido de manera significativa en aplicaciones electrónicas, ópticas, biomédicas y magnéticas [1, 2, 3, 4]. Su evolución y la de los biomateriales ha mejorado favorablemente los productos farmacéuticos [5], los sistemas biomédicos [6], los sistemas de administración de fármacos [7], los cosméticos y el tratamiento del agua [7,8,9]. En el mismo sentido, el desarrollo de materiales conjugados que sean biocompatibles, biogénicos y no tóxicos podría tener valiosas contribuciones en los campos de la biociencia y la biomedicina [10]. Además, los bio y nanomateriales conjugados metálicos biocompatibles podrían contribuir a más avances científicos para aplicaciones biomédicas como la ingeniería de tejidos [5], la terapéutica [11] y la administración de fármacos [12]. Esto se ha demostrado en trabajos recientes de manera elaborada, como el uso de hidrogel híbrido inyectable de colágeno-oro autoensamblado [13], nanoconjugados coloidales de oro-colágeno con núcleo y caparazón [14] y nanofármacos co-ensamblados sin portadores para la terapia antitumoral [15]. Varios estudios también han documentado que las nanopartículas metálicas pueden producir electrodos enzimáticos en biosensores electroquímicos con materiales porosos inorgánicos sin sílice [16]. Además, los nanohíbridos sintetizados de óxido de grafeno y albúmina también han mostrado su beneficio potencial hacia una terapia fotodinámica mejorada [17]. En conjunto, esto solo ha despertado más interés con otras posibles aplicaciones, como las imágenes biomédicas y los sistemas bio-sensoriales [16, 18].
El carbonato de calcio como mineral natural crudo se ha utilizado en una amplia gama de aplicaciones, incluidas las biomédicas, industriales y nanotecnológicas [10, 19,20,21]. La aragonita como polimorfo de carbonato de calcio existe en abundancia en la cáscara de berberecho ( Anadara granosa ), un moluscos que se encuentran popularmente también en Malasia [22]. La aragonita es biogénica a diferencia de los otros polimorfos de carbonato de calcio de la calcita y la vaterita, y constituye hasta el 95-98% de la cáscara de berberecho. El carbonato de calcio, un material inorgánico de polimorfo de aragonito, existe de forma natural y común dentro de las conchas de berberecho [23]. El polimorfo de aragonito ha atraído cada vez más la atención en el campo de la investigación debido a sus propiedades de biocompatibilidad y su potencial prometedor en el desarrollo de sistemas de administración de fármacos contra el cáncer [24] y de imágenes biomédicas [25, 26]. Actualmente, la mayoría de los estudios de investigación anteriores han revelado principalmente dos métodos de producción de carbonato de calcio [26]. Incluyen la coprecipitación o doble descomposición y carbonatación de CO 2 gas a través del hidróxido de calcio en entornos controlados, que lamentablemente ninguno produce carbonato de calcio biogénico [26,27,28]. Por tanto, los productos contienen una mezcla de calcita y vaterita en grandes cantidades que no son aptas para uso biomédico debido a sus informes de no biocompatibilidad y alta toxicidad [26].
Sin embargo, con el uso cada vez mayor de la nanotecnología en aplicaciones biomédicas, el presente estudio se centra en la síntesis de nanopartículas controladas de carbonato de calcio derivadas de la cáscara de berberecho (CSCaCO 3 NP) con tamaño y forma únicos utilizando dodecil dimetil betaína (BS-12) [29]. Esto está inspirado en trabajos anteriores que utilizan BS-12 como catalizador de biomineralización en la síntesis de CSCaCO 3 NP que se pueden manipular fácilmente para bioaplicaciones, nanopartículas rentables y relativamente puras [30]. La morfología y el tamaño de las nanopartículas sintetizadas son cruciales para determinar sus propiedades fisicoquímicas, con especial atención a las nanopartículas metálicas debido a sus vastas aplicaciones biomédicas potenciales [31]. Las nanopartículas de oro (AuNP) se han utilizado continuamente debido a sus propiedades ópticas, diferentes rangos de tamaño y color, que dependen de las variaciones máximas de absorción o del método de síntesis empleado [32]. El tamaño y la forma de las AuNPs afectan sus características de absorción y emisión en el espectro de luz visible, haciéndolas variar de regiones visibles a infrarrojas cercanas. Por tanto, debido a su síntesis [33], propiedades fisicoquímicas [34], biocompatibilidad [35] y funcionalización de la superficie [36], pueden manipularse para aplicaciones diferentes y particulares [37]. Además, también se ha afirmado que en el diagnóstico médico no se utilizan por completo y su valor posiblemente sea oscuro [37].
Entonces, tal vez con una funcionalización adecuada, podrían rediseñarse para la obtención de imágenes del cáncer [38], el tratamiento del cáncer [39], la administración de fármacos [40] y los dispositivos sensoriales [41]. Un recubrimiento es esencial para fabricar biomaterial nanohíbrido con propiedades funcionalizadas como nanopartículas de oro (AuNP) conjugadas con nanoesferas porosas de carbonato de calcio [16, 42]. El nanomaterial conjugado de carbonato de calcio y oro resultante o híbrido nanocompuesto, que podría conservar los rasgos parentales ventajosos tales como biocompatibilidad, buena solubilidad y dispersabilidad en solución [16]. Las nanopartículas de oro conjugadas que exhiben un fuerte cambio de color y resonancia de plasmón de superficie localizada (LSPR) podrían ser excelentes candidatos para posibles sistemas de múltiples receptores como aptámeros, péptidos y anticuerpos [35, 43, 44, 45]. La fabricación de polímeros conjugados solubles en agua y sus aplicaciones en biosensores, imágenes de fluorescencia y administración de fármacos se han realizado con éxito [46,47,48]. Sin embargo, las nanopartículas o nanomateriales conjugados han mejorado progresivamente ventajas como la fotoestabilidad [48, 49] y la baja citotoxicidad [50] a lo largo de los años, excepto por una preparación más amigable [51] y características de separación [48].
Adjunto, las AuNP y CSCaCO 3 Los NP se sintetizan de forma controlada y se utilizan para fabricar y caracterizar nanopartículas de carbonato de calcio biogénicas conjugadas de oro y cáscara de berberecho derivadas de carbonato de calcio (Au-CSCaCO 3 NP) cuyo tamaño de diámetro oscila entre 19 y 51 nm. Inicialmente, la preparación de AuNPs se inspira en el método clásico de Turkevich [52] y las nanopartículas derivadas de la cáscara de berberecho utilizando el enfoque sintético de dodecil dimetil betaína [26]. Las modificaciones en los parámetros sintéticos, como la concentración, podrían disminuir o aumentar su tamaño de manera competente. En consecuencia, el nanomaterial sintetizado se caracterizó e investigó para determinar su citotoxicidad. El Au-CSCaCO 3 Las ventajas adicionales de la preparación de NP son; síntesis fácil y rentabilidad.
Métodos / Experimental
Materiales y reactivo químico
La sal de oro (ácido tetracloroáurico que contiene una solución de oro al 49%) y el citrato trisódico se adquirieron en prima nexus Sdn Bhd (Malasia). La cáscara de berberecho fresca se obtuvo del mercado local (Pasar borong, Seri Kembangan, Selangor, Malasia). Se adquirieron dodecil dimetil betaína (BS-12) y colorante verde de indocianina (ICG) de Sigma-Aldrich (Steinheim, Alemania). Medio de Eagle modificado de Dulbecco (DMEM), suero fetal bovino (FBS), combinación de antibióticos (glutamina 100 mmol / L, penicilina 100 U / mL y estreptomicina 100 μg / mL), solución salina tamponada con fosfato (PBS), dimetilsulfóxido (DMSO ) y MTT (colorante de bromuro de 3-dimetiltiazo-2,5-difiniltetrazolio) se adquirieron en Naclai tesque, Inc., Kyoto, Japón. Todos los demás reactivos utilizados fueron de calidad analítica.
Síntesis de nanopartículas de oro
La síntesis se logró utilizando un método descrito anteriormente por Verma et al. [53] con ligeras modificaciones en las concentraciones, 1% de ácido tetracloroáurico que contiene 49% de solución de oro. Aproximadamente, se preparó 0.1% de la solución de oro y se diluyó en una serie de concentraciones de 15, 25 y 20 mM en diferentes matraces cónicos, respectivamente. A continuación, las soluciones se calentaron a 100ºC en una placa calefactora acoplada con agitación magnética (en posición 6, WiseStir® Korea). A continuación, se añadió aproximadamente 1% de citrato trisódico a la solución en ebullición con agitación magnética continua hasta que se observó una transición de color (la solución de oro amarillento se volvió incolora, luego negra y finalmente roja brillante). El calor se apagó después de 15 min y se dejó enfriar a temperatura ambiente. Las nanopartículas de oro sintetizadas se almacenaron luego a -4 ° C para su uso posterior. La reacción se mostró en la siguiente ecuación:
$$ 2 {\ mathrm {H} \ mathrm {AuCl}} _ 4 + 3 {\ mathrm {C}} _ 6 {\ mathrm {H}} _ 8 {\ mathrm {O}} _ 7 \ left (\ mathrm {cítrico} \ \ mathrm {ácido} \ derecha) \ a 2 \ mathrm {Au} +3 {\ mathrm {C}} _ 3 {\ mathrm {H}} _ 6 {\ mathrm {O}} _ 5 \ left (3- \ mathrm {cetoglutárico} \ \ mathrm {ácido} \ derecha) +8 \ mathrm {HCl} +3 {\ mathrm {C} \ mathrm {O}} _ 2 $$Preparación y síntesis de nanopartículas de carbonato de calcio derivadas de la concha de berberecho (CSCaCO 3 NP)
Se limpiaron a fondo, se restregaron y lavaron tres kilogramos de conchas de berberecho recién obtenidas. El polvo de cáscara de berberecho se produjo según el método descrito por Islam et al. [54]. La cáscara de berberecho limpia se secó en un horno (Memmert UM500, GmbH Co, Alemania) a 50 ° C durante 7 días. Las cáscaras de berberechos se trituraron en polvo usando una licuadora (Blender HCB, 550, EE. UU.) Y se tamizaron con un tamiz de prueba de laboratorio de acero inoxidable (Endecott Ltd., fabricado en Londres, Inglaterra) con una apertura de 90 μm para obtener un polvo de tamaño micrón. El polvo se secó durante 7 días a 74 ° C en el horno. El polvo se empaquetó adicionalmente en una bolsa de plástico de polietileno hermética para su uso posterior. Las nanopartículas de carbonato de calcio derivadas de la cáscara de berberecho se sintetizaron de acuerdo con el enfoque descrito por Islam et al. [55], con ligeras modificaciones en el método y los parámetros de síntesis. Se tomaron dos gramos de polvo de cáscara de berberecho en un matraz cónico de 250 ml seguido de 50 ml de agua doblemente desionizada y se añadió una concentración de 0,5 ml de BS-12 al matraz cónico. La mezcla en el matraz cónico se agitó vigorosamente a 1000 rpm, con una temperatura de 50 ° C durante 135 min utilizando una placa calefactora múltiple sistemática y un agitador magnético con una pequeña barra magnética. La muestra preparada se separó del líquido madre utilizando papel de filtro de doble anillo de tamaño 125 mm (Filtres Fioroni, China). A continuación, el residuo se lavó minuciosamente para eliminar el exceso de BS-12. Los productos finales, CSCaCO 3 NP en polvo, se envasaron en un recipiente de limpieza en seco y se secaron durante 3 días (Oven Memmert UM500, GmbH Co, Alemania) a 74 ° C. El recipiente se envolvió y selló correctamente con película Para después de la adición de múltiples bolas de mármol pequeñas en el interior. El recipiente se colocó en un molino de bolas de rodillos programable (BML-6, Wisemix® Korea) a una velocidad de 200 rpm durante 5 días. La muestra se almacenó en polietileno hermético en un horno para su uso posterior.
Síntesis de nanopartículas conjugadas de carbonato de calcio derivadas de la concha de berberecho de oro (Au-CSCaCO 3 NPs) e Incooperación de tinte de infrarrojo cercano (NIR)
En este procedimiento, 0,2 g de CSCaCO 3 Se dispersaron NP y 5 mg de colorante verde de Indocianina (ICG) en el infrarrojo cercano (NIR) en 20 ml de solución de coloide de oro (pH 7) (solución de AuNP), como describen de manera similar Cai et al. [16], en un matraz cónico vacío y limpio. Se realizaron modificaciones de síntesis adicionales, donde la muestra se sonicó durante 20 min y se incubó en un agitador magnético con una pequeña barra magnética a 200 rpm durante 3 días. La muestra se ultracentrifugó a una velocidad de 10,000 rpm durante 10 min para obtener Au-CSCaCO 3 de color verde claro-violáceo. Compuesto NP. Se decantó el sobrenadante y se lavó el sedimento con una serie de agua desionizada. El material compuesto preparado se secó en el horno durante 4 días y se almacenó en un horno de polietileno hermético para su posterior análisis.
Caracterización de nanopartículas conjugadas de carbonato de calcio derivadas de la concha de berberecho de oro (Au-CSCaCO 3 NP)
El tamaño de partícula y la morfología del nanomaterial se analizaron utilizando un microscopio electrónico de transmisión (TEM). El nanomaterial se dispersó en alcohol absoluto y se sonicó durante 40 min. Aproximadamente, se pipetearon 5 µl de la solución de muestra suspendida sobre un soporte de muestra de agarre de cobre. La muestra se observó bajo TEM (Hitachi H-7100). El microscopio electrónico de barrido de emisión de campo (FESEM) (Modelo JOEL 7600F) funcionaba a un voltaje de 5 KV y estaba equipado con una unidad de espectroscopia de rayos X de dispersión de energía (EDX). Esto se utilizó para caracterizar las características de la superficie de Au-CSCaCO 3 NP. El material se dispersó en alcohol absoluto y se sonicó durante 1 h. Aproximadamente 50 µl de la solución de muestra suspendida se pipetearon sobre un soporte de muestra de agarre de cobre, se secaron durante la noche y se escanearon usando los haces de electrones. Además, el espectrómetro de infrarrojos por transformada de Fourier (FTIR) también se utilizó para el análisis funcional del nanomaterial conjugado sintetizado; el nanomaterial se calibró al 1% en peso en Ker (FTIR Modelo 100, Perkin Elmer) en el rango de 400 a 4000 cm −1 . Además, el análisis del tamaño del nano conjugado sintetizado y el potencial zeta se realizó utilizando zetasizer (Nano ZS, Malvern Instruments). El material se suspendió en agua desionizada y se sonicó durante 50 min; la suspensión homogénea se depositó en la cubeta zetasizer y se examinó para determinar el tamaño de partícula y el potencial zeta. La presencia de diferentes analitos del nanocompuesto conjugado se controló utilizando un espectrofotómetro Uv-Vis (UV - 2600) a diferentes longitudes de onda que van desde 300 a 800 nm.
Estudios de citotoxicidad y cultivo celular
La línea celular de adenocarcinoma de mama humano (JCRB:MCF-7) y la línea celular de fibroblastos de ratón (JCRB:NIH3T3) se cultivaron en DMEM (glucosa alta) suplementado con FBS al 10% y combinación de antibióticos (glutamina 100 mmol / L, penicilina 100 U / mL y estreptomicina 100 μg / mL). Los matraces de cultivo (cultivo Eppendorf T-25 y T-75) se incubaron en dióxido de carbono al 5% a 37 ° C, y se utilizaron células con una confluencia del 80-90% para el proceso de siembra y tratamiento.
Siembra y tratamiento de células
Las células se sembraron en placas estériles de 96 pocillos a una densidad de 5 × 10 3 células por pocillo y se incubaron durante 24 h durante la noche. Se retiraron los medios de cada pocillo, y las células se trataron y se cultivaron conjuntamente en réplicas con una suspensión de nanocompuesto conjugado (Au-CSCaCO 3 NP) durante un período de 24, 48 y 72 h. Una vez completada la exposición al tratamiento, los medios de los pozos se aspiraron y lavaron con PBS antes de reemplazarlos con otros medios nuevos antes de los tratamientos experimentales.
Preparación de Au-CSCaCO 3 NP para tratamiento
Solución madre de Au-CSCaCO 3 Se prepararon NP a una concentración de 1 mg / ml en medio DMEM sin suero al 10%. Después de la siembra celular de células MCF-7 y células NIH3T3 en placas de 96 pocillos, las placas se trataron e incubaron con diferentes concentraciones en microgramos (100-1,56) de Au-CSCaCO 3 Soluciones NPs.
(MTT) Protocolo y preparación del reactivo de bromuro de 3-dimetiltiazo-2, 5-difiniltetrazolio
Típicamente, se disolvieron 5 mg de polvo de reactivo MTT en 1 ml de PBS facilitado por vórtice de sonicador para una mezcla uniforme. Después de la siembra y el tratamiento de las células, se limpiaron las placas de los pocillos y se añadieron 20 µl de reactivo MTT a cada pocillo. Inmediatamente después, las placas se dejaron incubar durante 3-4 h para permitir la unión del MTT a las mitocondrias de las células. Después de la incubación, se añadió 1 ml de DMSO a cada uno de los pocillos que liberaron el producto de color en la solución. Las placas se mantuvieron en una habitación oscura durante 30 min y se midió la densidad óptica (DO) de la solución con un lector de microplacas a una longitud de onda de 570 nm [56]. Los experimentos se realizaron por triplicado para cada línea celular y se registraron los valores medios. El porcentaje de viabilidad celular se determinó mediante la fórmula siguiente.
$$ \ mathrm {Porcentaje} \ \ mathrm {de} \ \ mathrm {celda} \ \ mathrm {viabilidad} =\ left (\ A \ Sample / A \ Control \ right) \ times 100 $$donde A Muestra fue la lectura de DO promedio de diferentes células tratadas incubadas de ambas líneas celulares y A Control fue la lectura de DO promedio de las diferentes células incubadas en medios de cultivo completos solamente. Luego, se evaluó la citotoxicidad de las células a partir de los valores promedio por triplicado y se mostró como media ± desviación estándar (DE).
Análisis estadístico
El análisis de datos estadísticos se realizó utilizando el software SPSS (Versión 10, Chicago, EE. UU.). Los experimentos se realizaron por triplicado y se expresaron como media ± desviación estándar (M ± DE). El umbral de significación fue p <0.01.
Resultados y discusión
Propiedades fisicoquímicas del conjugado Au-CSCaCO 3 NP
Microscopio electrónico de transmisión
El propósito de las micrografías TEM fue evaluar el tamaño del Au-CSCaCO 3 conjugado sintetizado NP que muestran nanopartículas bien dispersas con un tamaño de diámetro promedio de 35 ± 16 nm dentro del rango de (19–51 nm). Las diferencias de tamaño atribuidas a las condiciones de síntesis se muestran en la Fig. 1.
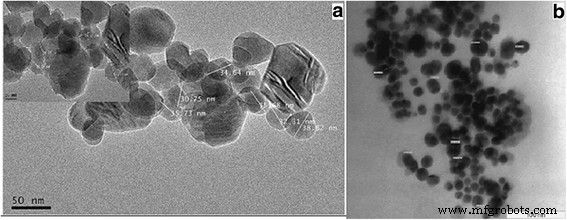
TEM ( a , b ) imágenes del Au-CSCaCO 3 NP que caracterizan sus diferentes tamaños de nanopartículas
Las micrografías TEM del nano conjugado mostraron un diámetro de entre 19 y 51 nm y nanopartículas dispersas. El tamaño nanométrico obtenido de forma única podría atribuirse a las condiciones sintéticas controladas empleadas. Otra posible explicación para la dispersión de las nanopartículas podría deberse a la capa cargada negativamente de iones citrato que ayudaron a las repulsiones de las nanopartículas entre sí y también, debido a la repulsión electrostática y la capa superficial de hidratación conjugada que previene la agregación y aumenta la estabilidad del conjugado como se informó de manera similar. por Jazayeri et al. [56]. Además, el reactivo de protección con citrato juega un papel en la síntesis, lo que permitió una mayor dispersión y estabilidad del conjugado de nanopartículas, como informaron Rawat et al. [57]. El tamaño de partícula único mostró las diferentes nanopartículas de oro absorbidas dentro de la matriz de nanoesferas de carbonato de calcio similar al trabajo realizado por Cai et al. [16], lo que contribuye al tamaño de partícula resultante observado que se muestra. Sin embargo, este resultado también confirma los informes de que la calcita tiene poca capacidad para acomodar nanopartículas de oro [16].
Microscopía electrónica de barrido de emisión de campo (FESEM) y espectroscopía de rayos X de dispersión de energía (EDX)
La micrografía de FESEM evaluó la morfología y la forma de las nanopartículas sintetizadas que muestran Au-CSCaCO de forma esférica y en forma de cadena 3 Nanopartículas de NP con un pequeño grado de agregación como se muestra en la Fig. 2. Los espectros elementales (Fig. 2b) analizaron la composición elemental de las nanopartículas conjugadas que presentan 64,98% de carbono, 13,53% de oxígeno, 0,02% de calcio, 17,63% de cobre y 3,85% de oro como se presenta en la Tabla 1.

FESEM a Micrografía FESEM de Au-CSCaCO 3 NP que describen la morfología. b Espectros EDX de Au-CSCaCO 3 NP
Las micrografías de FESEM describieron la morfología única como forma esférica, superficie suavizada y nanopartículas conjugadas estructuradas en forma de cadena cuyas propiedades físicas o químicas podrían explicarse como resultado de las condiciones de preparación y los métodos sintéticos [58]. De manera similar, la naturaleza estructural esférica mostrada por las nanopartículas conjugadas fue similar a las informadas por Verma et al. [53], pero contrario al pequeño grado de agregación presentado. Una posible explicación de este resultado podría deberse a las interacciones hidrófobas y electrostáticas entre las nanopartículas de oro y las nanopartículas de carbonato de calcio derivadas de la cáscara de berberecho que conducen a una fuerte unión [48]. Además, el papel de BS-12 empleado en la síntesis se reflejó en la descomposición de las nanopartículas en forma esférica análoga al trabajo documentado por Islam et al. [55]. El perfil elemental (Tabla 1) no reveló cambios significativos contrarios al resultado esperado. De manera similar, los hallazgos observados con la composición química de las nanopartículas conjugadas están documentados como se mostró anteriormente en trabajos anteriores [26, 54].
Distribución de tamaño y carga de superficie por intensidad
Se realizó el potencial zeta de las nanopartículas conjugadas, con el fin de evaluar su carga superficial, estabilidad y distribución de tamaño por intensidad, lo que revela una carga negativa de - 16,4 ± 3,81 mV y un tamaño medio de nanopartículas conjugadas de 57,97 nm como se muestra en la Fig.3 y Tabla 2.
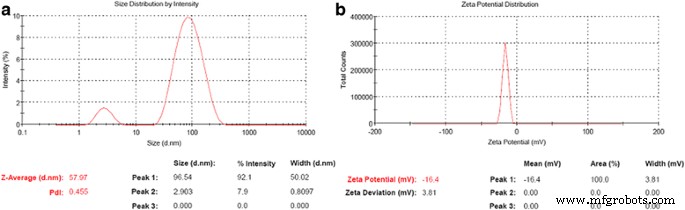
un Distribución del tamaño de partículas por intensidad de Au-CSCaCO 3 NP. b Potencial Zeta del Au-CSCaCO 3 NP que muestran la carga superficial
El potencial zeta es un ensayo importante para evaluar la carga electrostática de la superficie de las nanopartículas que se determinó utilizando un medidor zeta. Esto explicó además la dispersidad del nanomaterial en solución, lo que nos permitió comprender la estabilidad general, la vida útil de las nanopartículas, las interacciones de las partículas entre las partículas cargadas y sus implicaciones [59]. La evaluación del potencial zeta del nanomaterial conjugado indicó la estabilidad de las nanopartículas a - 16,4 mV y un índice de polidispersidad (PdI) de menos de 0,5. Una posible explicación podría atribuirse a la presencia de más electro-repulsión entre las partículas en suspensión durante la medición. Además, las tendencias a la aglomeración también pueden haber influido en la distribución de tamaños que conducen a un tamaño mayor debido a los métodos sintéticos. Estudio previo de Hoque et al. ha documentado de manera similar [60] que el potencial zeta altamente positivo o negativo disminuye la agregación y aumenta la estabilidad. Además, las diferencias fisicoquímicas de las nanopartículas sintetizadas podrían atribuirse a los métodos de síntesis utilizados. Los trabajos de Kanaujia y colaboradores [61] también han enfatizado que valores altos negativos o positivos del potencial zeta indican estabilidad y evitan la agregación de partículas, debido a la repulsión eléctrica que estabiliza eléctricamente la dispersión de nanopartículas también reportada por Isa et al. [62].
Espectrómetro infrarrojo de transformación de Fourier (FTIR)
El espectro FTIR de Au-CSCaCO 3 NP muestra que el pico más destacado apareció a 1455,09 cm −1 seguido de picos observados a 1059,12 cm −1 , 854.80 cm −1 y 464,16 cm −1 , respectivamente. Además, se observaron picos débiles a 706,40 cm −1 y 1785,68 cm −1 como se presenta en la Fig. 4.
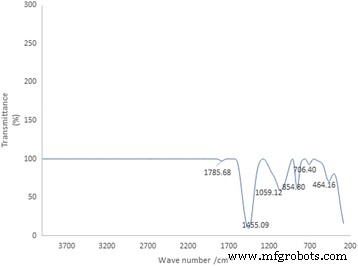
Espectrómetro de infrarrojos por transformada de Fourier de los principales picos característicos de Au-CSCaCO 3 NP. Todas las marcas corresponden a las frecuencias discutidas en el texto
El espectro FTIR de Au-CSCaCO 3 Los NP tal como se presentaron mostraron que el pico más destacado apareció a 1455,09 cm −1 , que atestigua los enlaces oxígeno-hidrógeno (O – H) presentes en los grupos carboxílicos de las nanopartículas de oro [14] y las nanopartículas de cáscara de berberecho, seguidas de los picos que mejor mostraron la presencia del marcador polimorfo de aragonito observado a 1059,12 cm -1 , 854.80 cm −1 y 706,40 cm −1 , que se sabe que informan sobre el grupo alquilo presente en las nanopartículas derivadas de la cáscara de berberecho que eran consistentes con los picos del espectro [55]. De manera similar, el pico débil se observó a 1785,68 cm −1 debido a la presencia del grupo carboxílico [54], y se observó un pico adicional a 464,16 cm −1 . Todos los picos mostraron características significativas de la presencia de enlaces covalentes, enlaces carbono-carbono (C-C), carbono-oxígeno (C-O) y carbono-nitrógeno (C-N) cuyos grupos funcionales apropiados estaban presentes en nuestro conjugado nanopartículas. El FTIR identificó esencialmente los grupos funcionales presentes, obteniendo los picos del espectro infrarrojo del nanomaterial conjugado y recopilando simultáneamente datos de alta resolución espectral en un amplio rango espectral (400–4000 cm −1 ) [63]. Sin embargo, se informa que el polimorfo de calcita del carbonato de calcio tiene picos que van desde 2000 a 2900 cm −1 con las nanopartículas fabricadas mediante el método de carbonatación [64].
Espectrofotómetro Uv-Vis
Las nanopartículas conjugadas sintetizadas muestran un alto pico de absorción a 530 nm como se muestra en la Fig. 5.
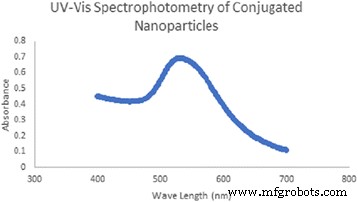
Espectro de absorbancia del espectrofotómetro Uv-Vis de Au-CSCaCO 3 NP como se analiza en el texto
Las nanoestructuras de oro tienen una amplia absorbancia de luz debido al efecto de resonancia de plasmón superficial localizado de las AuNP [65, 66]. Varios informes han demostrado que las partículas de oro a menudo tienen un pico de absorbancia agudo observado entre 500 y 520 nm [66,67,68,69]. Esta técnica permitió una evaluación adicional del conjugado Au-CSCaCO 3 Tamaño, concentración y nivel de agregación de las NP [65]. También se sabe que la banda de absorbancia cambia a las longitudes de onda más pequeñas, lo que indica la reducción en el tamaño de las partículas, y la forma simétrica de los espectros de absorción indica una distribución del tamaño de partícula estrecha [70], lo que confirma nuestra conjugación Au-CSCaCO 3 NP que mostraron un pico de absorción más amplio entre 500 y 550 nm y el punto más alto a una longitud de onda de 530 nm. Aceptablemente en la región del espectro visible del infrarrojo cercano, en la que la luz es fácilmente atenuada por el tejido y el pico de absorción cambia significativamente a una longitud de onda más larga [71]. Una posible explicación de esto podría deberse a la síntesis y conjugación del nanomaterial. También en consonancia con Srinath et al., Quienes revelaron que la posición de la banda de absorción depende principalmente de la variación de color, la agregación y las especies adsorbidas en la superficie [72]. Además, el espectro de absorción de las nanopartículas podría cambiar según el color, la morfología y el tamaño debido a la propiedad de resonancia del plasmón de oro [73]. Las nanoestructuras con propiedades fototérmicas NIR tienen la capacidad de dispersar la luz con fuerza, lo que tiene aplicaciones importantes en la obtención de imágenes biomédicas [74, 75].
Estudios de citotoxicidad
MTT (bromuro de 3-dimetiltiazo-2, 5-difiniltetrazolio)
Los estudios de citotoxicidad en células de carcinoma de mama humano (MCF-7) y células de fibroblastos embrionarios de ratón (NIH3T3) revelan que el Au-CSCaCO 3 Los NP inhibieron más del 70% de la proliferación celular, lo que provocó la muerte de las células cancerosas y casi el 40% de inhibición de las células de fibroblastos en dosis de 100 μg. El IC 50 y dosis de concentraciones más bajas, como 25 μg, también resultaron tóxicas para las células cancerosas, revelando una baja viabilidad celular y también inhibiendo más del 50% de la proliferación celular de las células cancerosas para las nanopartículas. Por otro lado, dosis de concentración idénticas a las de las células de fibroblastos mostraron una viabilidad celular aumentada y constante de las células de fibroblastos. El IC 50 mostró hasta un 80% de viabilidad celular de las células de fibroblastos, como se presenta en la Fig. 6.
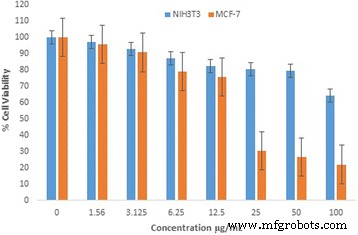
Evaluación de la citotoxicidad del Au-CSCaCO 3 tratado con MCF-7 y NIH3T3 Células NPs que utilizan un ensayo MTT que proporciona un porcentaje de viabilidad celular
3-Dimethylthiazo-2,5-diphynyltetrazolium Bromide (MTT) is a colorimetric assay acceptably used to determine cell viability [76]. Utilizing mitochondrial enzymes in the electron transport chain [77], viable cells with active metabolism converted MTT into purple-colored formazon crystals in the cellular cytosol [78]. The crystals were dissolved after cell lysis on adding an organic solvent dimethyl sulfoxide (DMSO) which is proportional to live cell number, unlike dead cells, due to cytotoxicity that are unable to carry out the reaction [79]. The conjugated nanoparticles displayed consistent cell death against the cancer cells and reliable cell viability of the fibroblast cells with concentration doses ranging from 25–100 μg. Furthermore, attesting low cytotoxicity and highlighting the biocompatibility of Au-CSCaCO3 NPs and potential usefulness for biomedical applications, the cytotoxicity could be due to the internalization of the nanoparticles which possibly triggered intracellular responses and thus induced cellular damage because of interaction with cell organelles. Despite contrary cytotoxicity findings with works done on HeLa cells (human cervical cancer cell line) due to nanoparticles inducing oxidative damage [35, 80], Zhang et al. demonstrated the biocompatibility of the nanoparticles and its likely use for drug delivery systems [80]. Similarly, reports of gold nanoparticles confirmed nontoxic dependent on their size [81] and concentration [39]. Studies strongly confirmed that biogenic gold conjugates are stable and nontoxic nanocarrier used in biomedical application [35, 39] suggesting use for biomedical applications such as drug delivery and cancer therapy [82].
Conclusiones
Spherical-shaped conjugated gold-cockle shell-derived calcium carbonate nanoparticles (Au-CSCaCO3 NPs) were obtained. The conjugated nanoparticles were synthesized using a simpler, environmental friendly, and cost-efficient synthetic approach. Furthermore, based on the results, the obtained conjugated nanoparticles were relatively pure and stable. The source of material used for the cockle shell-derived nanoparticles is biogenic, readily available, and naturally occurring as seawater mollusca cockle shell. Based on the presented evidences, the conjugated Au-CSCaCO3 NPs could be a good biomaterial for biomedical applications.
Abreviaturas
- Au-CSCaCO3 NPs :
-
Synthesized Conjugated Gold-Cockle Shell Derived Calcium Carbonate Nanoparticles
- AuNPs:
-
Gold nanoparticles
- BS-12:
-
Dodecyl dimethyl betaine
- C–C:
-
Carbon-carbon bond
- C–N:
-
Carbon-nitrogen bond
- C–O :
-
Carbon-oxygen bond
- DMEM:
-
Medio Eagle modificado de Dulbecco
- DMSO:
-
Dimethyl sulfoxide
- EDX:
-
Energy dispersive X-ray
- FBS:
-
Suero fetal bovino
- FESEM:
-
Field emission scanning electron microscope
- FRGS:
-
Fundamental Research Grant Scheme
- FTIR:
-
Fourier transform infrared spectroscopy
- HeLa cells:
-
Human cervical cancer cell line
- IC50 :
-
50% inhibition concentration
- ICG:
-
Indocyanine green dye
- JCRB:
-
Japanese Collection Research Bioresource
- LSPR:
-
Localized surface plasmon resonance
- MCF-7:
-
Human breast adenocarcinoma cell line
- MTT:
-
3-Dimethylthiazo-2, 5-diphynyltetrazolium Bromide Dye
- NIH-3T3:
-
Mouse embryonic fibroblast cell line
- NIR:
-
Infrarrojo cercano
- O–H:
-
Oxygen-hydrogen bond
- OD:
-
Optical density
- PBS:
-
Phosphate-buffered saline
- TEM:
-
Transmission electron microscope
Nanomateriales
- Qué sigue para la impresión 3D:aplicaciones biomédicas
- APLICACIONES GENERALES DE CARBONATO DE CALCIO
- Aplicaciones del masterbatch de carbonato de calcio. Carbonato de calcio para hacer masterbatch de relleno
- Nanopartículas de oro multifuncionales para aplicaciones terapéuticas y diagnósticas mejoradas:una revisión
- Nanopartículas para la terapia del cáncer:avances y desafíos actuales
- Avances y desafíos de los nanomateriales fluorescentes para síntesis y aplicaciones biomédicas
- Compuestos de grafeno y polímeros para aplicaciones de supercapacitores:una revisión
- Nuevas nanopartículas de Au Nanostars @ PEG biocompatibles para la obtención de imágenes de TC in vivo y las propiedades de depuración renal
- La preparación de la nanoestructura yema-cáscara de Au @ TiO2 y sus aplicaciones para la degradación y detección del azul de metileno
- Avances recientes en métodos sintéticos y aplicaciones de nanoestructuras de plata
- Fabricación y caracterización de nanoclips de ZnO mediante el proceso mediado por poliol



