Defectos en la superficie del nanofósforo de MgAl2O4 dopado con Ti
Resumen
Nano MgAl 2 dopado con Ti O 4 para la emisión de blancos se sintetizó mediante el método de combustión. Defectos extrínsecos de Schottky, vacantes de Al y Ti 4+ dopantes en sitios de Al, que se consideran responsables de la emisión de color blanco azulado, fueron observados por STEM en la superficie de nano MgAl 2 dopado con Ti O 4 polvo. Las estabilidades de los asociados al defecto de Schottky, (Ti Al · –V Al ′ ′ ′) ′ ′, Se demostraron mediante el cálculo de DFT. El comportamiento de las emisiones se interpretó con estos resultados.
Antecedentes
La transición del dominio a granel o micrónico al de tamaño nanométrico afecta en gran medida a un material, alterando, por ejemplo, sus propiedades mecánicas, ópticas y eléctricas [1, 2, 3, 4, 5, 6]. Estos cambios se atribuyen principalmente al tamaño y la estructura asociada de no equilibrio. Un ejemplo son las propiedades únicas de fosforescencia y emisión que pueden alcanzar las nanopartículas [2, 7]. Las propiedades de emisión de nanofosforas se pueden modular mediante dopaje, además de los efectos de confinamiento cuántico descritos [8, 9]. La valencia de carga de un dopante y el sitio en la estructura que ocupa generalmente afectan las propiedades de emisión de un fósforo. Los dopantes a menudo se pueden ubicar en un nanofósforo en sitios (por ejemplo, en la superficie de una partícula) distintos de los sitios habituales en un fósforo del tamaño de una micra. Por tanto, las superficies de las nanopartículas se convierten en sitios importantes para los dopantes que normalmente no ocupan dichos sitios en sistemas a granel o micrones. Los cambios en el comportamiento de las emisiones se han informado debido al lugar de ocupación, que está asociado con otros defectos [8, 9].
Pure MgAl 2 O 4 tiene un defecto intrínseco de un Mg 2+ vacante, V Mg ′ ′, Que es el centro de una emisión roja a 720 nm. Se observa una fuerte emisión azul de los monocristales de MgAl 2 dopado con Ti O 4 ; la desaparición de la emisión roja se atribuye a la compensación de carga mediante la adición de Ti 4+ [10, 11]. Sin embargo, en nuestro trabajo anterior, encontramos que MgAl 2 de tamaño micrón dopado con Ti O 4 el polvo tratado térmicamente en el aire produjo una emisión blanca [12]. La diferencia se explicó a través de la aparición de emisiones rojas y verdes además del azul observado en el MgAl 2 dopado con Ti O 4 cristales individuales. Nuestro trabajo anterior [12] también simuló el mecanismo para la emisión de rojo a través del asociado de defecto intrínseco de Schottky, (V O ·· –V Mg ′ ′) x . El presente trabajo reporta la observación visual de defectos extrínsecos de Schottky en la superficie de MgAl 2 dopado con Ti O 4 nanopolvo y lo relaciona con la diferencia en los espectros de emisión entre micrones y nano sistemas.
Métodos
Mg (NO 3 ) 2 · 6H 2 O (nitrato de Mg; 2,46 g, Aldrich), Al (NO 3 ) 3 · 9H 2 O (nitrato de Al; 7,246 g, Aldrich), CO (NH 2 ) 2 (urea; 5,231 g, Aldrich) y C 10 H 14 O 5 Ti (Ti oxiacetil acetonato; 0,1 g, Aldrich,) se utilizó como materiales de partida para la síntesis de nano MgAl 2 dopado con Ti O 4 . Se utilizaron nitrato de Mg y nitrato de Al en una relación molar de 1:2 en la síntesis, y oxiacetil-acetonato de Ti proporcionó un dopaje de Ti al 2% en moles. Los materiales de partida se disolvieron en agua desionizada y la mezcla se homogeneizó mediante agitación antes de que el agua se evaporara en una placa caliente. La mezcla restante se colocó en un crisol de alúmina y se quemó a 500ºC durante 1 h al aire.
Las fases del nanopolvo sintetizado se analizaron mediante difractometría de rayos X (XRD; Rigaku) y las propiedades de fotoluminiscencia se midieron mediante espectrofotometría de fluorescencia (PSI, sistema PL Darsa pro-5000) utilizando luz monocromática de 260 y 360 nm de una lámpara Xe. La morfología y el tamaño del polvo se observaron mediante microscopía electrónica de transmisión de alta resolución (TEM; JEOL, JEM-2100F). Las imágenes del dopante Ti y las vacantes de Al también se obtuvieron mediante TEM de escaneo de alta resolución (HR-STEM; JEOL, JEM-2100F).
Los cálculos de la teoría funcional de la densidad de los primeros principios (DFT) se realizaron basados en la aproximación de gradiente generalizada de Perdew-Burke-Ernzerhof y pseudopotenciales de onda plana aumentada por proyector implementados en el paquete de simulación ab initio de Viena (VASP) [13,14,15] con un corte de energía de 500 eV y una convergencia de campo de autoconsistencia de 10 −5 eV. Las estabilidades de varios defectos asociados se examinaron mediante cálculo para investigar su dependencia de las posiciones de los dopantes y las vacantes y las distancias relativas entre ellos.
La energía superficial del plano de superficie (100) en el MgAl 2 O 4 se calculó el cristal; También se examinó su variación con el sitio Ti. La celda unitaria, cuya estructura cristalina se optimizó previamente para permitir la relajación completa del parámetro de la red, la forma del cristal y las posiciones atómicas, se expandió a una supercélula de 4 × 1. Se crearon {100} superficies insertando una placa de vacío dentro de la supercélula. Se varió la posición de inserción de la placa de vacío que es del tamaño de una supercélula 2 × 1 para examinar el cambio de la energía de formación de la superficie con la distancia entre la superficie y el dopante de Ti. La terminación de la superficie con un 50% de capa de Mg se consideró principalmente porque se encontró que esta era la superficie más estable (10 0) de MgAl 2 O 4 .
Resultados y discusión
La Figura 1 muestra el patrón XRD para MgAl 2 dopado con Ti O 4 nano fósforos con gráficos TEM. La Figura 1a confirma claramente que MgAl 2 O 4 fue sintetizado a 500 ° C por el método de combustión, dada su similitud con el patrón JCPDS XRD para MgAl 2 puro O 4 . Los picos anchos indican la presencia de nanocristalitos y están relacionados con las partículas de <20 nm mostradas en la Fig. 1b. Por el contrario, el MgAl 2 de tamaño micrométrico dopado con Ti O 4 de nuestro trabajo anterior [12] muestra una alta cristalinidad, atribuida al tratamiento a alta temperatura del MgAl 2 O 4 polvo (1300 ° C durante 2 h).
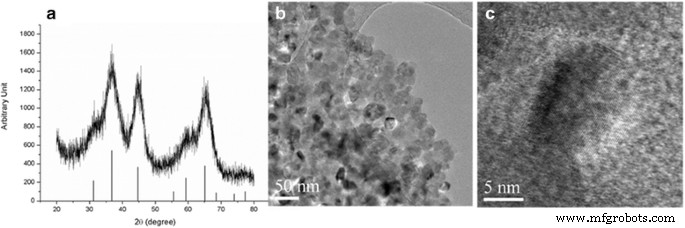
un Patrón XRD para nano MgAl 2 dopado con Ti O 4 polvo sintetizado a 500 ° C 1 h con picos de referencia de MgAl 2 O 4 de JCPDS y b , c Imágenes TEM del polvo
Los espectros de emisión de fotoluminiscencia de MgAl 2 dopado con Ti O 4 muestran emisión blanca a una excitación de 260 nm (Fig. 2a) para muestras de tamaño nano y micrónico sintetizadas a 500 ° C durante 1 hy 1300 ° C durante 2 h en las Fig. 2b, c, respectivamente. Sin embargo, las dos bandas de emisión dan como resultado colores ligeramente diferentes:el del nanopolvo sintetizado a 500 ° C se desplaza hacia el azul en relación con el del polvo de escala micrométrica preparado a 1300 ° C. La emisión azul de MgAl 2 dopado con Ti O 4 los cristales simples se atribuyen a Ti 4+ en sitios Al (octaédricos), que era la única forma de iones Ti en los monocristales [10, 11]. Sin embargo, MgAl 2 dopado con Ti O 4 Se demostró que el polvo del tamaño de una micra tiene Ti 3+ y Ti 4+ ocupando igualmente los sitios Al (octaédrico) y Mg (tetraédrico) [12].
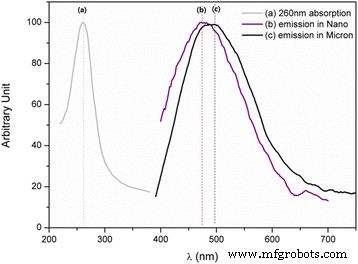
Fotoluminiscencia de MgAl 2 dopado con Ti O 4 : a Excitación de 260 nm, b nano y c micrones [12] polvos sintetizados a 500 ° C, 1 hy 1300 ° C, 2 h, respectivamente
La Figura 3a muestra una imagen HR-STEM tomada cerca de la superficie de nano MgAl 2 dopado con Ti O 4 . La imagen ampliada en la Fig. 3b muestra que la distancia entre las matrices es 0.2057 nm, que coincide bien con la distancia plana (400) de MgAl 2 O 4 (0,202 nm). Muestra que la disposición atómica dejó una vacante relativamente oscura entre los puntos (ver flechas en la Fig. 3a, b). El brillo menor en la vacante podría haberse originado a partir de átomos en las capas inferiores. El punto de defecto también se identifica en el gráfico de intensidad de contraste en el recuadro, que muestra los picos de contraste para los átomos dentro del cuadro rojo de la Fig. 3b. La vacante se muestra claramente por la baja intensidad de contraste del quinto sitio desde la izquierda. Para identificar el sitio vacante, realizamos la transformación de Fourier de la imagen en la Fig. 3a y encontramos que el eje del haz está cerca de [001] (recuadro, Fig. 3a). Se observa en la vista proyectada [001] de un MgAl 2 O 4 cristal de que los átomos de Mg están ubicados independientemente en el plano (004), mientras que los átomos de Al y O aparecen superpuestos en el mismo plano. Por lo tanto, si la fluctuación mostrada en la intensidad del contraste se debe solo a los átomos constituyentes en el plano, es más probable que la vacante se origine en un sitio de Al vacante en lugar de un sitio de Mg vacante.
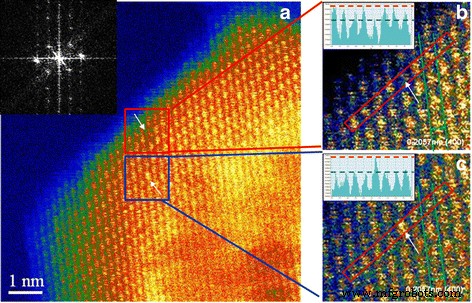
Imágenes HR-STEM de nano MgAl 2 dopado con Ti O 4 ; un . La imagen muestra Al 3+ vacante y Ti 4+ dopante en las proximidades con la transformación de Fourier de la imagen. b La imagen ampliada en el cuadro rojo de ( a ) y Al 3+ la vacante se revela a partir de la imagen STEM con una intensidad de contraste correspondiente, inserto de ( b ). c La intensidad del contraste, inserto de ( c ), confirma que Ti 4+ dopante ocupa un sitio de AI. Las flechas indican las ubicaciones de Al vacante y Ti en el sitio Al, respectivamente
En la Fig. 3c, el punto de celosía indicado por una flecha en el cuadro rojo es mucho más brillante que los demás. Teniendo en cuenta que los átomos de Mg y Al no se pueden distinguir por el contraste z debido a sus números atómicos similares y que es difícil detectar los átomos de oxígeno debido a su bajo número atómico, se concluye que este punto más brillante se debe al dopante Ti. El gráfico de intensidad de contraste correspondiente (recuadro, Fig. 3c) enfatiza el punto más brillante, lo que indica la presencia de un elemento de mayor número atómico, definitivamente Ti en este sistema. El Ti en un sitio de Al causa un error de desplazamiento, porque su valencia de carga y su radio iónico son diferentes a los de Al 3+ . El átomo más brillante de la figura parece más grande que los demás, de acuerdo con los radios iónicos efectivos más grandes de Ti 3+ (0,081 nm) y Ti 4+ (0,0745 nm) en comparación con el de Al 3+ (0,0675 nm) [16]. El radio iónico efectivo de Mg 2+ se informa como 0.086 nm, que es más grande que los de los iones Ti. Por lo tanto, llegamos a la conclusión de que los defectos que se muestran en la Fig. 3 (es decir, Fig. 3b, c) son V Al ′ ′ ′ Y Ti Al · , respectivamente, esperando que Ti 4+ Los iones de un tamaño más pequeño (0.0745 nm) tienen más posibilidades de ocupar sitios de Al vacantes que Ti 3+ (0,081 nm).
La Figura 4a muestra el cambio en la energía superficial de un MgAl 2 dopado con Ti O 4 cristal perfecto calculado con respecto a la posición del dopante. La energía de la superficie, que puede ser un factor importante que influye en la energía de formación de un nanosistema, disminuye a medida que el Ti se acerca a la superficie, lo que indica que el cristal es más estable cuando el Ti está más cerca de la superficie. El resultado indica una tendencia común para Ti en un sitio de Al y Ti en un sitio de Mg; sin embargo, el dopante es más estable en un sitio de Mg que en un sitio de AI. Esto se atribuye al mayor radio iónico efectivo de Mg 2+ (0.086 nm) que Ti 4+ (0,0745 nm) o Al 3+ (0.0675 nm) [16]. Por lo tanto, la tendencia es más probable cuando el MgAl 2 dopado con Ti O 4 tiene una alta cristalinidad. Sin embargo, puede que no sea siempre cierto para un nanosistema de baja cristalinidad, al menos cerca de la región de la superficie.
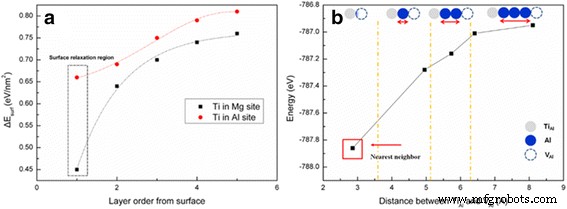
un Estabilidades de Ti en Mg o Al sitio vacante en la superficie de MgAl 2 O 4 :el círculo rojo muestra la energía superficial de Ti en el sitio de Al y el punto negro es el de Ti en el sitio de Mg y b la energía de enlace de los asociados con defectos, Ti Al · –V Al ′ ′ ′ En función de la distancia
También se realizaron cálculos de DFT para investigar la posición del dopante Ti y la vacante de Al. La energía calculada de un Ti 1 Mg 15 Al 31 O 64 cristal, espinela que contiene un dopante de Ti (Ti Al · ) y una vacante de Al (V Al ′ ′ ′), Aumenta a medida que el dopante y la vacante se separan como se muestra en la Fig. 4b. Por lo tanto, se logra una mayor estabilidad cuando los dos defectos están cerca uno del otro y forman asociados de defectos como (Ti Al · –V Al ′ ′ ′) ′ ′ Que son responsables de la emisión azul. Este resultado se atribuye a la estabilidad estructural y la fuerza de Coulombic entre los dos defectos puntuales. Sin embargo, surge un compromiso entre estos factores y la entropía configuracional para estabilizar el sistema a temperatura elevada, lo que da como resultado que los dos defectos estén separados por 2-3 átomos, como se muestra en la Fig. 3a.
En general, la energía de formación de una vacante de Al o Mg es mucho menor (~ 4.5 eV) que la de un intersticial de oxígeno (~ 7.0 eV) en MgAl 2 O 4 [17, 18]. Además, la energía de formación de defectos intrínsecos de Schottky para MgAl 2 O 4 (4,15 eV / defecto) es mucho más bajo que el de los óxidos individuales, MgO (7,7 eV) y α-Al 2 O 3 (4,2–5,1 eV). Según estimaciones de Coulomb, las energías de asociación de defectos de los pares de Schottky extrínsecos son más pequeñas que las de los pares de Schottky intrínsecos en varios sistemas iónicos [19]. Cuando MgAl 2 dopado con Ti O 4 se sintetiza químicamente por el método de combustión a través del proceso de nucleación y precipitación, como para el nano sistema de este estudio, en lugar de por difusión en estado sólido, la formación de defectos y defectos asociados, incluyendo O 2− las vacantes que se observan comúnmente en las cerámicas de óxido, se facilitarían significativamente en las superficies de las partículas. Los resultados generales indican que el defecto se asocia, es decir, (Ti Al · –V Al ′ ′ ′) ′ ′, Prevalecen en la superficie de MgAl 2 dopado con Ti O 4 nanopolvos, que provocan el cambio azul en la emisión blanca de nanopolvos en comparación con la de los polvos micrones.
Conclusiones
La sustitución de Ti en los sitios Al de MgAl 2 O 4 fue observado por HR-STEM. Se detectaron una vacante de Al y un dopante de Ti cerca de la superficie de nano MgAl 2 dopado con Ti O 4 . Estas observaciones demuestran la presencia de Ti 4+ en los sitios de Al. El cambio de azul en relación con el espectro del sistema de escala de micras se atribuye a la presencia de más Ti 4+ iones en sitios de Al en la superficie. Sería energéticamente más favorable para Ti 4+ iones para tomar sitios de Mg en la estructura de la espinela. Sin embargo, Ti 4+ Los iones tienden a tomar sitios de Al en el nano MgAl 2 dopado con Ti O 4 . Esta diferencia en la luminiscencia del nanosistema surgió de su baja cristalinidad que es el resultado de la baja temperatura de procesamiento.
Abreviaturas
- Nitrato de Al:
-
Al (NO 3 ) 3 · 9H 2 O
- DFT:
-
Teoría funcional de la densidad
- HR-STEM:
-
TEM de escaneo de alta resolución
- Nitrato de magnesio:
-
Mg (NO 3 ) 2 · 6H 2 O
- PL:
-
Fotoluminiscencia
- TEM:
-
Microscopía electrónica de transmisión
- Oxi-acetil-acetonato de Ti:
-
C 10 H 14 O 5 Ti
- Urea:
-
CO (NH 2 ) 2
- VASP:
-
Paquete de simulación de Viena ab initio
- XRD:
-
Difractometría de rayos X
Nanomateriales
- Defectos en la superficie de las aleaciones de titanio
- El diseño de la capa de emisión para multiplicadores de electrones
- Ajuste de las morfologías de la superficie y las propiedades de las películas de ZnO mediante el diseño de la capa interfacial
- De principio a fin:los fundamentos de la medición de superficies
- Análisis de emisiones fotoinducidas para identificar contaminantes superficiales
- ¿Cómo lograr el defecto cero?
- Software:el camino hacia cero defectos
- ¿Cuáles son los diferentes tipos de drenaje de aguas superficiales?
- Los principios fundamentales del rectificado de superficies
- Rectificado de superficies a la antigua usanza
- Agujero pasante Vs Montaje en superficie:¿Cuál es la diferencia?



