Progreso de los electrocatalizadores a base de carbono para baterías flexibles de zinc-aire en los últimos 5 años:estrategias recientes para el diseño, la síntesis y la optimización del rendimiento
Resumen
La creciente popularidad de los dispositivos electrónicos portátiles ha llevado al rápido desarrollo de sistemas flexibles de conversión de energía. Las baterías de zinc-aire recargables flexibles (ZAB) con altas densidades de energía teóricas demuestran un potencial significativo como dispositivos de energía flexible de próxima generación que se pueden aplicar en productos electrónicos portátiles. El diseño de cátodos altamente eficientes y estables al aire que pueden catalizar electroquímicamente tanto la reacción de reducción de oxígeno (ORR) como la reacción de desprendimiento de oxígeno (OER) son muy deseables pero desafiantes. Los catalizadores flexibles a base de carbono para catálisis ORR / OER pueden clasificarse ampliamente en dos tipos:(i) catalizadores autoportantes basados en la modificación in situ de sustratos flexibles; (ii) catalizadores no autoportantes basados en revestimientos superficiales de sustratos flexibles. Los métodos utilizados para optimizar el rendimiento catalítico incluyen el dopaje con átomos y la regulación de la estructura electrónica y el entorno de coordinación. Esta revisión resume las estrategias propuestas más recientemente para la síntesis de electrocatalizadores de diseño basados en carbono y la optimización de sus rendimientos electrocatalíticos en electrodos de aire. Y nos centramos significativamente en el análisis de los sitios activos inherentes y sus mecanismos electrocatalíticos cuando se aplican como catalizadores ZAB flexibles. Los hallazgos de esta revisión pueden ayudar en el diseño de electrodos de aire a base de carbono más valiosos y sus ZAB flexibles correspondientes para su aplicación en dispositivos electrónicos portátiles.
Introducción
El uso excesivo actual de energía no renovable ha suscitado preocupaciones con respecto a la crisis energética. Por lo tanto, para aliviar la actual escasez de energía, es necesario establecer dispositivos de suministro de energía más eficientes y respetuosos con el medio ambiente. Además, la aparición y popularización de dispositivos electrónicos portátiles que se pueden estirar, plegar y doblar ha impulsado el rápido crecimiento y desarrollo de los sistemas de almacenamiento de energía flexibles [1, 2, 3]. Las baterías de zinc-aire (ZAB) presentan una densidad de energía teórica de 1086 Wh kg −1 , que es aproximadamente cinco veces mayor que la de las baterías recargables de iones de litio de uso generalizado. Además, el zinc tiene las ventajas de tener abundantes reservas y una amplia disponibilidad [4, 5]. Los ZAB típicos utilizan zinc como electrodo negativo, oxígeno como electrodo positivo e hidróxido de potasio como electrolito. Debido a la introducción de ánodos de zinc altamente estables y electrolitos a base de agua, los ZAB no son tóxicos, no dañan el medio ambiente y son seguros y han recibido una atención generalizada como sistemas de almacenamiento de energía prometedores [6]. El principio de funcionamiento básico de los ZAB implica una reacción electroquímica entre el zinc en el electrodo negativo de la batería y el OH - en la solución de electrolitos dando como resultado la liberación de electrones. Simultáneamente, los catalizadores en el electrodo de difusión de gas o la capa de reacción del cátodo de aire entran en contacto con el electrolito y el oxígeno en el aire, y luego se produce la transferencia de carga. Durante el funcionamiento de los ZAB recargables, la conversión entre oxígeno y agua se produce en el electrodo de aire; esto incluye ORR y OER, los cuales son procesos de recombinación de múltiples electrones. Las reacciones específicas que ocurren en soluciones alcalinas son las siguientes:
$$ {\ text {ORR}}:\, {\ text {O}} _ {2} \ left ({\ text {g}} \ right) + 2 {\ text {H}} _ {2} { \ text {O}} \, \ left ({\ text {l}} \ right) + 4 {\ text {e}} ^ {-} \ to 4 {\ text {OH}} ^ {-} $$ (1) $$ {\ text {OER}}:\, 4 {\ text {OH}} ^ {-} \ to {\ text {O}} _ {2} \ left ({\ text {g}} \ right) + 2 {\ text {H}} _ {2} {\ text {O}} \ left ({\ text {l}} \ right) + 4 {\ text {e}} ^ {-} $ $ (2)Se han desarrollado varios modelos cinéticos para comprender las vías de reacción involucradas durante la ORR. El primer modelo, desarrollado por Damjanovic et al. [7, 8], implica la formación de peróxido de hidrógeno en una vía de reacción paralela a aquella en la que O 2 se reduce a agua sin la formación de peróxido de hidrógeno como intermedio. Esto está representado esquemáticamente por la ecuación. 1 y 2.
$$ {\ text {O}} _ {{2}} \ to ^ {{{\ text {I}} _ {{1}}}} {\ text {H}} _ {{2}} {\ text {O}} $$ (1) $$ \ begin {array} {* {20} c} {{\ text {O}} _ {{2}} \ mathop {\ longrightarrow} \ limits ^ {{{ \ text {I}} _ {{2}}}} {\ text {H}} _ {{2}} {\ text {O}} _ {{2}} \ mathop {\ longrightarrow} \ limits ^ { {{\ text {I}} _ {{3}}}} {\ text {H}} _ {{2}} {\ text {O}}} \\ {\ flecha abajo {\ text {I}} _ {4}} \\ {{\ text {to}} \, {\ text {solución}} \, {\ text {y}} \, {\ text {ring}} \, {\ text {electrodo}} } \\ \ end {matriz} $$ (2)El peróxido de hidrógeno, formado como un intermedio de reacción en la ruta 2, se reduce parcialmente en el mismo electrodo de disco que el agua y se transfiere parcialmente desde el electrodo de disco a la solución y al electrodo de anillo por difusión convectiva. Yo 1 , Yo 2 y yo 3 representan las corrientes respectivas. Yo 4 representa la velocidad a la que el peróxido de hidrógeno se difunde desde el electrodo de disco como una corriente. Sin embargo, el intermedio de peróxido generado es inestable, lo que puede complicar el proceso de reacción, dañar la membrana del electrolito y reducir la actividad del catalizador, así como el voltaje de salida y la tasa de conversión de energía de la pila de combustible [9]. Por lo tanto, el 4e directo - La ruta (Ec. 1) se considera la ruta ideal para el ORR, ya que tiene un voltaje de salida y una conversión de energía más altos que el 2e - vía (ecuación 2).
Debido a que se requiere un sobrepotencial considerable de la ORR para superar las barreras de energía asociadas con la transferencia de electrones de múltiples pasos [10], el principal desafío al que se enfrenta el desarrollo de ZAB recargables flexibles que se pueden aplicar a gran escala es el uso de cátodos de aire. en las ZAB que exhiben un potencial excesivo [11] y una baja reversibilidad del oxígeno causada por la ORR y la REA lentas durante la carga y descarga [12]. Los electrodos de Pt / C demuestran el mejor rendimiento catalítico para el ORR, mientras que IrO 2 / RuO 2 demuestra un excelente desempeño catalítico en los REA. Sin embargo, estos catalizadores también adolecen de varios inconvenientes, como las escasas reservas, el elevado coste, la actividad catalítica única y la escasa estabilidad, que dificultan gravemente su aplicación a gran escala [13]. Por lo tanto, el desarrollo de un catalizador con excelentes rendimientos catalíticos ORR / OER bifuncionales que sea asequible es vital para la comercialización de ZAB flexibles. Los metales no nobles, en particular los metales de transición, han atraído una amplia atención debido a su alta actividad y excelente estabilidad térmica. Además, los catalizadores a base de carbono poseen ventajas significativas, que incluyen flexibilidad estructural, excelente conductividad eléctrica, buena estabilidad química y térmica y funcionalización química simple, además de ser livianos. Por lo tanto, se consideran materiales candidatos prometedores para su uso en productos electrónicos portátiles. Existen varios cátodos de aire excelentes basados en CC (tela de carbono); sin embargo, uno de los principales desafíos es la identificación de materiales con excelente conductividad que puedan crecer uniformemente en CC. Si los materiales crecen de manera desordenada en el CC, se reduce el número de sitios activos en el catalizador. Las ZAB tradicionales utilizan una solución acuosa como electrolito, que no puede cumplir con los requisitos de las ZAB flexibles de estado sólido. Por lo tanto, la mayoría de los ZAB de estado sólido que exhiben excelentes rendimientos utilizan electrolitos de gel para conducir la electricidad, como el alcohol polivinílico, el óxido de polietileno (PEO), la poliacrilamida (PAM) y el ácido poliacrílico (PAA). Estos electrolitos en gel se utilizan cada vez más en ZAB, ya que poseen una gran plasticidad y buena conductividad. Específicamente, el poliacrilato de sodio es estable en la aplicación práctica de electrolitos en gel a base de agua, debido a su efecto tampón en electrolitos alcalinos. [1]
En los últimos años, ha aumentado el número de estudios sobre ZAB flexibles, lo que proporciona una base teórica para la producción práctica y la aplicación de ZAB flexibles. Aunque Zhu et al. publicó una revisión detallada de baterías unidimensionales [14] y Shi et al. introdujo catalizadores bifuncionales en detalle [15], no se ha informado de los avances recientes, en particular en los últimos cinco años, de los ZAB flexibles que contienen catalizadores basados en carbono. Por lo tanto, este trabajo resume las estrategias para la síntesis de catalizadores a base de carbono y la optimización de sus rendimientos electrocatalíticos en electrodos de aire, con un enfoque significativo en el análisis de sus sitios activos inherentes y su mecanismo electrocatalítico cuando se aplican como catalizadores ZAB flexibles.
Electrocatalizadores de diseñador basados en carbono
Los materiales a base de carbono se utilizan ampliamente en los catalizadores ZAB debido a sus excelentes propiedades. Estos materiales son principalmente materiales a base de grafeno (incluidos grafeno funcionalizado y perfiles de grafeno); sin embargo, también se utilizan grafito, fullereno y nanotubos de carbono (CNT) [16]. Sin embargo, los materiales a base de carbono todavía adolecen de muchos defectos durante la aplicación práctica de ZAB. Por tanto, es necesario optimizar el tratamiento aplicado a los materiales de carbono. Un ejemplo de esto son los materiales de carbono poroso dopado con N, que exhiben un rendimiento electrocatalítico bifuncional excepcional en el ORR y OER [17, 18]. Entre la variedad de métodos utilizados para modificar materiales de carbono, el dopado con átomos individuales, como N, P y S, puede mejorar significativamente la actividad del catalizador. En vista de esto, algunos investigadores han utilizado el codopaje con N y P y han descubierto que el catalizador codopado tiene una excelente actividad. Además, otros métodos, como el dopaje de un solo metal, el dopaje bimetálico y los nanomateriales, tienen un efecto positivo definitivo en la optimización del rendimiento del catalizador de los materiales de carbono. Sin embargo, apenas se han explorado métodos para desarrollar electrocatalizadores de alto rendimiento para ZAB. Los estudios han demostrado que la modificación de materiales de carbono, como el grafeno y los CNT, mediante el dopaje, puede optimizar las propiedades superficiales de los materiales de carbono. La estrategia más típica para optimizar el rendimiento del catalizador es combinar nanomateriales de carbono dopados con heteroátomos con material a base de metales de transición (óxidos, calcogenuros como sulfuros a base de Ni, etc. [19,20,21], fosfuros de metales de transición (TMP [ 22]) y compuestos de nitruro). Dado que los electrocatalizadores ZAB todavía tienen numerosas deficiencias, es vital optimizar su estructura catalítica. Actualmente, el ajuste de la estructura electrónica, los defectos de oxígeno, los enlaces metal-oxígeno, la tensión de la interfaz y el dopaje atómico se han utilizado ampliamente en el diseño de catalizadores ZAB.
Crecimiento de catalizadores de alta eficiencia en electrodos flexibles
El electrodo flexible está representado por la capa de difusión de gas en ZAB flexibles. El cátodo de aire se forma haciendo crecer directamente un catalizador de alta eficiencia en el electrodo flexible, que tiene las ventajas de ser autoportante y tener un área de contacto de electrodo grande y una gran capacidad de plegado. Autoportante indica que no se requiere adhesivo no conductor, evitando así el deterioro del rendimiento del electrodo y la pérdida del catalizador durante la deformación repetida del electrodo. Además, la reducción de los sitios activos y el aumento de la impedancia de la interfaz se evitan mediante el uso de adhesivos no conductores. El crecimiento del catalizador sobre el electrodo expansible se puede combinar con otros métodos, como la electrodeposición, el método hidrotermal y la vulcanización a temperatura ambiente. Los electrodos flexibles de uso común incluyen espuma de carbono dopada con nitrógeno, tela de fibra de carbono, papel de carbón y fieltro de carbón, que poseen una excelente conductividad eléctrica.
Crecimiento de catalizadores de alta eficiencia en telas de fibra de carbono
La tela de fibra de carbono, una tela tejida construida a partir de fibras de carbono, es el material de sustrato flexible más utilizado. El cultivo de catalizadores de alta eficiencia directamente sobre tela de fibra de carbono es un método simple y eficaz, que se puede lograr mediante reacciones en solución (Fig. 1a-c), electrodeposición y una combinación de otros métodos, como espacios confinados, tratamiento térmico [2] (Fig. 1d, e), carbonización-oxidación CC y calcinación asistida por ligando (preparación de un CoO X ultrafino capa [23]). Un ejemplo de carbonización-oxidación incluye el crecimiento de diferentes estructuras de cristales, morfologías y tamaños de partículas de MOF basados en cobalto 3D y 2D en CC para la preparación de un cátodo libre de aglutinantes, seguido del anclaje de capas de Co 3 O 4 nanopartículas en nanoarrays de carbono dopado con nitrógeno [24]. La red de nanofibras se basa en CC en una atmósfera de nitrógeno para obtener un cátodo de aire bifuncional con un excelente rendimiento catalítico y una notable flexibilidad [25]. Aunque el método de electrodeposición se ha utilizado ampliamente para preparar materiales de electrodos, debido a la conductividad inherentemente pobre del Co 3 O 4 , los métodos de electrodeposición convencionales presentan limitaciones en la formación de un Co 3 O 4 capa con una gran área de contacto sobre un portador conductor. Co 3 O 4 se puede cultivar in situ sobre la tela de fibra de carbono para formar un Co 3 ultrafino de crecimiento uniforme O 4 capa. En particular, el ultrafino Co 3 O 4 Las capas tienen un área de contacto máxima sobre el soporte conductor, lo que facilita el transporte rápido de electrones y evita la agregación de las capas ultrafinas durante el proceso de preparación del electrodo [26]. Además, Co 3 O 4 se puede convertir en un nano-microarray con una estructura en capas [24], como se muestra en la Fig. 1f. Esta capa ultrafina de óxido de cobalto también se puede utilizar como electrocatalizador en ZAB [23], como se muestra en la Fig. 1g.
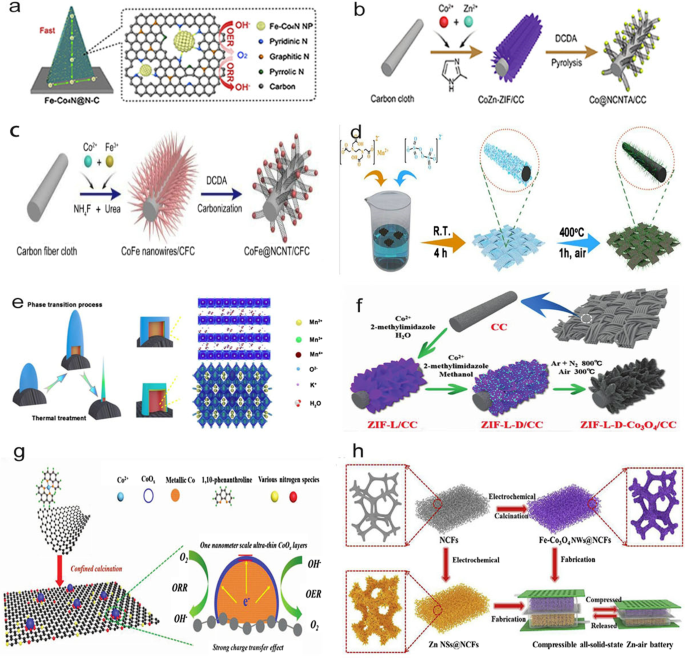
un Esquema del Fe-Co 4 Nanohoja de N @ N – C cultivada en CC para su aplicación en la reacción bifuncional del oxígeno [56]. b Esquema que representa el proceso sintético para Co @ NCNTAs [85]. c Esquema del proceso sintético para CoFe @ NCNT / CFC [98]. d Esquema de la preparación de MnO x -CC-400 [2]. e Propuesta de transición de fase de óxido de manganeso en CC mediante un tratamiento térmico [2]. f Esquema de ZIF-L-D-Co 3 O 4 / Proceso de formación de CC [24]. g Esquema de una x de 1 nm-CoO capa sobre el sustrato metálico de Co / N-RGO [23]. h Esquema de los procesos de fabricación de las ZAB de estado sólido comprimibles y recargables [27]
Crecimiento de catalizadores eficientes en materiales de espuma de fabricación propia
Los materiales de espuma hechos a sí mismos se refieren principalmente a espuma de carbono y espuma de níquel. Pan y col. usó una esponja de melamina recocida a una temperatura de 800 ° C para formar un material de carbono espumado flexible, que luego se usó como electrodo de trabajo para electrodepositar el precursor de Fe-Co 3 O 4 NWS @ NCF mediante un método de electrodeposición escalable. En consecuencia, el material de carbono espumado flexible podría aplicarse en baterías de esponja totalmente sólidas [27], como se muestra en la Fig. 1h. El material de espuma de níquel es un tipo de esponja metálica reticulada. Jiang y col. indicó que el crecimiento de electrodos de catalizador in situ sobre un sustrato flexible causaría desorden y formaría áreas irregulares densas, lo que reduciría la actividad catalítica. Por lo tanto, construyeron una matriz multidimensional ordenada de CNT 1D decoradas con nanopartículas de cobalto 0D (llamadas MPZ-CC @ CNT) y nano-crestas de carbono 2D en un material de espuma de níquel. Durante la pirólisis del marco de coordinación bimetálico de ZnCo 2D, los CNT que contienen un alto contenido de N-dopaje se cultivaron in situ a partir del cobalto altamente disperso, formando así una matriz abierta y ordenada [28], como se muestra en la Fig. 2a.
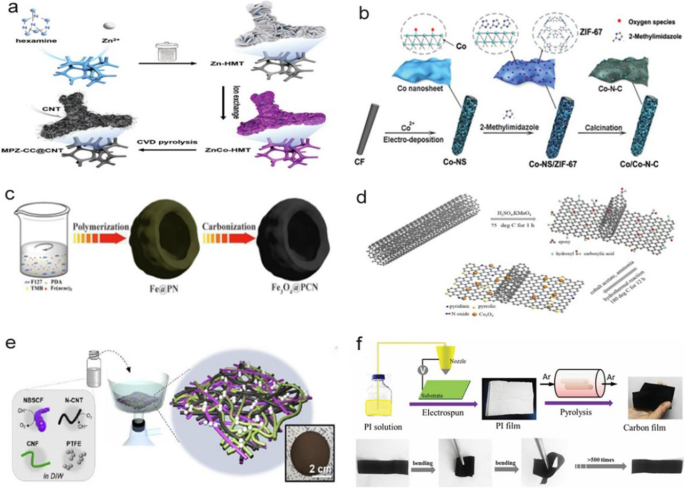
un Esquema del proceso de preparación para MPZ-CC @ CNT [28]. b Síntesis del catalizador Co / Co – N-C [29]. c Esquema de la preparación del Fe 3 O 4 Catalizadores @PCN [40]. d Esquema que representa al Co 3 O 4 / Síntesis de catalizadores compuestos de N-p-MCNTs [41]. e Esquema del procedimiento de fabricación del cátodo de aire de papel MH, junto con su fotografía [43]. f Representación esquemática del procedimiento de fabricación del NCNF y fotografías del NCNF flexible resultante [44]
Síntesis de catalizadores de alta eficiencia en fieltro de carbono
El fieltro de carbono es una tela no tejida. Yu y col. [29] desarrolló una nueva estrategia para sintetizar nanohojas de Co-N-C soportadas en fieltro de carbono (Co / Co-N-C), que contienen nano-islas de Co con una estructura de capas 3D, como se ilustra en la Fig. 2b. Esta estructura inusual da como resultado un buen contacto entre las nano-islas de Co y las nanohojas de Co-N-C. Además, la convivencia de Co 0 y Co 2+ mejoró el rendimiento electrocatalítico del catalizador bifuncional (ORR / OER). Por lo tanto, la estructura en capas única general puede promover aún más el transporte eficaz de electrones / iones en ORR y OER [29]. Además de cultivar nanoelectrodos 3D sobre fieltro de carbono, también se puede fabricar una capa ultrafina de óxido de cobalto (CoOx) a nanoescala sobre fieltro de carbono (es decir, un sustrato de grafeno dopado con Co / N metálico) [23]. Esta estructura ultrafina proporciona condiciones favorables para su aplicación en ZAB.
Síntesis de catalizadores de alta eficiencia en papel carbón
El papel de fibra de carbono (CFP) está compuesto de fibra de carbono y se produce mediante el proceso de fabricación de papel. La CFP se puede utilizar para mejorar el rendimiento de ORR y OER de electrocatalizadores no metálicos, como g- C 3 N 4 . G-C 3 N 4 tiene un alto contenido de nitrógeno y, por lo tanto, puede proporcionar un número suficiente de sitios activos para reacciones electrocatalíticas y reducir el potencial de ORR [30]. Sin embargo, su rendimiento electrocatalítico está significativamente limitado debido a su falta de conductividad, lo que da lugar a una escasa capacidad de transferencia de electrones [30]. G-C 3 N 4 con diferentes morfologías se pueden preparar utilizando diferentes métodos de tratamiento térmico [30]. El rendimiento de ORR y OER del catalizador se puede optimizar aplicando tratamientos a g-C 3 N 4 , como 1) sintetizar un catalizador de alta eficiencia usando g-C 3 N 4 como plantilla [31, 32], 2) aplicando un g-C 3 N 4 -estrategia de pirólisis asistida [33,34,35], o 3) introduciendo g-C 3 N 4 en carbono. G-C 3 dopado con fósforo N 4 puede crecer directamente en CFP, que puede diseñarse como un electrodo de oxígeno flexible. Este es el primer electrocatalizador bifuncional ORR / OER no metálico formado por la combinación de Pg-C 3 similar a una flor N 4 compuesto por delgadas nanohojas de g-C 3 N 4 y CFP. El electrocatalizador contiene una red híbrida 3D con un alto contenido de N y una gran cantidad de dopaje P, que produce una excelente actividad y durabilidad de ORR y OER [36], y un buen rendimiento de carga y descarga, incluso en el caso de deformación por flexión. .
Síntesis de catalizadores de alta eficiencia en espacios confinados
La síntesis de catalizadores de alta eficiencia en espacios confinados puede aumentar la eficiencia del dopaje, reducir la pérdida de calor y aumentar las propiedades mesoporosas, mejorando así su rendimiento de ORR. Los espacios confinados pueden ser nanocanales de tamices moleculares, como montmorillonita, 2-4-6 tripiridil triazina, CNT, nanoláminas de carbono y capas de carbono dopadas. Numerosos experimentos también han demostrado que los catalizadores preparados en espacios reducidos exhiben un efecto catalítico mejorado. El dopaje de elementos de transición y elementos no metálicos en espacios reducidos puede mejorar significativamente la eficiencia catalítica. Se han notificado casos de dopaje N y S [13], dopaje N y P [12], dopaje bidimensional con nitrógeno [37, 38], etc. Además, se ha establecido que si se utiliza una estrategia asistida por plasma para el dopaje en un espacio confinado, el efecto de grabado del plasma puede dotar de porosidad al espacio confinado, exponiendo así sitios más activos, lo que favorece el largo plazo. durabilidad y transporte eficaz de electrones del electrocatalizador [39]. Zhang y col. utilizó un método de membrana blanda para preparar Fe 3 O 4 envuelto en un nano-recipiente de carbono poroso, que demuestra un excelente rendimiento catalítico y durabilidad a largo plazo [40], como se muestra en la Fig. 2c. El Co 3 O 4 Las nanopartículas se anclaron en los NTC de paredes múltiples parcialmente exfoliados dopados con nitrógeno, lo que resultó en un rendimiento catalítico sobresaliente [41], como se muestra en la Fig. 2d.
Combinación de catalizadores flexibles de alta eficiencia
Un catalizador combinado comprende un catalizador funcional único compuesto por el mismo material en diferentes formas o un catalizador bifuncional compuesto por diferentes materiales. Xu y col. logró un cátodo de aire ORR de función única al diseñar simultáneamente láminas de CNT alineadas, apiladas cruzadas y porosas, donde las láminas de CNT funcionaban como una capa de difusión de gas, una capa de catalizador y un colector de corriente, y sintetizaron una nueva ZAB fibrosa, flexible y estirable [42]. El catalizador de cátodo de aire en los ZAB flexibles típicamente exhibe una actividad catalítica de ORR / OER insuficiente y requiere condiciones de síntesis severas, incluidas altas temperaturas / altas presiones y soluciones ácidas (o alcalinas). Además de los problemas de los catalizadores de aire bifuncionales, las propiedades mecánicas del cátodo de aire dependen en gran medida de las propiedades mecánicas de su sustrato, lo que da como resultado una falta de diversidad de formas y deformabilidad en la hoja del cátodo de aire. Sobre esta base, Lee et al. utilizó un catalizador flexible combinado de alta eficiencia para los REA y los CNT dopados con nitrógeno para los REA [43], como se muestra en la Fig. 2e. El cátodo de aire monolítico de papel hetero-nano-mat comprende una mezcla de catalizador bifuncional 1D, nanofibras de celulosa y nanopartículas de politetrafluoroetileno, sin necesidad de colectores de corriente convencionales ni capas de difusión de gas [43]. Zhang y col. sintetizó un nuevo tipo de NiCo 2 O 4 / Electrocatalizador bifuncional de nano-malla de carbono dopado con N compuesto de NiCo hueco 2 O 4 nanoesferas y nano-mallas de carbono dopado con N [40]. El electrocatalizador bifuncional se sintetizó a través de una síntesis en fase líquida y posteriormente se trató con calor, después de lo cual se ensambló en una batería.
Película de cátodo flexible hecha en casa
Liu y col. preparó una película de nanofibras de carbono nanoporosas (NCNF) pirolizando una película de poliimida (PI) electrohilada en una atmósfera de Ar. Como se muestra en la Fig. 2f, el NCNF posee flexibilidad y alta resistencia mecánica y a la tracción. La resistencia a la tracción del NCNF es de 1,89 MPa y el módulo de tracción es de 0,31 GPa. NCNF exhibe una estructura de red de carbono nanoporoso 3D y una gran área de superficie específica, que puede proporcionar rutas electrón / ión cortas y rápidas y abundantes canales de difusión de gas. Más importante aún, el diseño del electrodo también tiene las ventajas de eliminar los aglutinantes de polímero y simplificar el proceso de fabricación, minimizando el tamaño y el costo de la batería. Los ZAB recargables totalmente sólidos y flexibles que contienen el cátodo de aire NCNF exhiben un alto voltaje de descarga (~ 1.0 V a 2 mA cm −2 ), voltaje de carga bajo (~ 1,8 V a 2 mA cm −2 ), alta densidad de energía de 378 Wh kg −1 y excelente estabilidad mecánica y cíclica. Estos resultados sugieren la posibilidad de aplicaciones a gran escala de las ZAB [44].
Estrategias de optimización para el rendimiento del catalizador de ZAB
En los últimos años, la investigación sobre electrocatalizadores económicos y altamente eficientes para ORR y OER se ha desarrollado rápidamente. Aunque existen muchas controversias con respecto al proceso catalítico específico que ocurre durante la electrocatálisis, es seguro que un mayor número de sitios activos efectivos en el catalizador conduce a una mejor actividad catalítica. En el proceso de optimización del rendimiento de los catalizadores ZAB, el dopaje atómico sobre carbono puede provocar sinergias y defectos estructurales, así como el ajuste de la estructura electrónica, el entorno de coordinación y la estructura del catalizador. Por lo tanto, el efecto electrocatalítico del catalizador se puede mejorar dopando los materiales de carbono con átomos específicos. El dopaje atómico se puede clasificar en dopaje de un solo átomo y dopaje de múltiples átomos, donde los átomos pueden ser átomos metálicos o heteroátomos. Tanto el dopaje de un átomo como el de varios átomos pueden mejorar el rendimiento electrocatalítico del catalizador.
Dopaje atómico
Mediante el análisis composicional y el cálculo de la teoría funcional de la densidad, Yu et al. estableció que el dopaje con N puede mejorar eficazmente la conductividad y la capacidad de absorción de oxígeno del catalizador; sin embargo, el dopaje N excesivo provoca una disminución de la cinética de reacción [45]. El efecto sinérgico y los defectos estructurales se pueden lograr mediante el dopaje con heteroátomos.
Dopaje de un solo átomo
Se pueden usar heteroátomos (N, P, S, etc.) y metales (Fe, Co, Mn, etc.) para el dopaje de un solo átomo. Entre ellos, el dopaje N es el dopaje de átomo único sobre carbono más utilizado. El dopaje N puede aumentar la eficiencia del transporte de electrones y la fuerza de adsorción de oxígeno, así como mejorar la cinética de reacción del catalizador, lo que da como resultado defectos y la exposición de sitios más activos. Por ejemplo, Yu et al. demostró que el dopaje N puede mejorar significativamente la conductividad electrónica y el O 2 capacidad de adsorción de Co 3 O 4 nanocables a través de investigaciones experimentales y cálculos de la teoría funcional de la densidad (DFT) [45]. Debido al espacio entre las láminas, los metales de transición, como Co [5], Ni, Mn [46, 47] (como se muestra en la Fig. 3b, c), Fe y Cu, se pueden dopar en materiales de sustrato activo, como como materiales de carbono (grafeno, CNT, etc.). También se ha confirmado que los heteroátomos 2D que exhiben estructuras únicas y propiedades físicas y químicas, como N, P, S [22, 48] y B [49,50,51,52,53,54] (como se muestra en la Fig. 3d, e), puede mejorar el rendimiento electroquímico y electrocatalítico de los catalizadores.
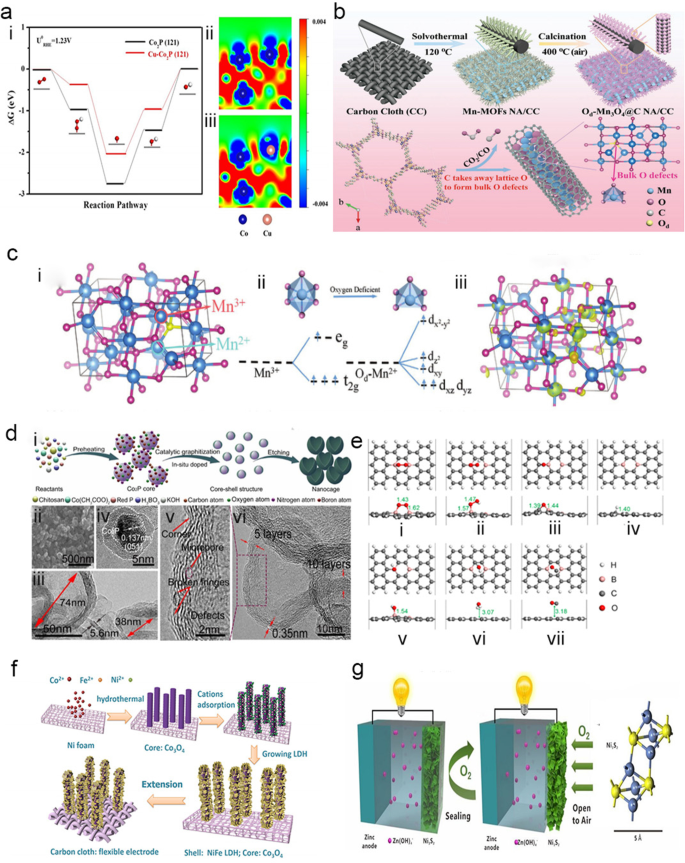
un (i) Diagrama de energía libre de la ORR sobre Co 2 P y Co 2 dopado con Cu Superficies P. Las diferentes densidades de carga de (ii) Co 2 P (121) y (iii) Co 2 dopado con Cu P (121). Las regiones azul y roja indican por separado el agotamiento y la acumulación de electrones [22]. b Ilustración del procedimiento de síntesis del Od-Mn 3 O 4 @ Nanoestructura CNA / CC, y sus mecanismos de formación a escala atómica. Las esferas azul, rosa, gris y amarilla representan los átomos de Mn, O, C y Od, respectivamente [46]. c (i) Modelo de supercélula de Mn 3 O 4 . (ii) Campos cristalinos octaédricos y piramidales de Mn-O y las configuraciones de división del orbital d. (iii) Diferencias de densidad de electrones de Od-Mn 3 O 4 (el círculo rosa representa Mn 3+ , el círculo azul cielo representa Mn 2+ ) [47]. d Síntesis y caracterización morfológica de NB-CN [52]. (i) Ilustración del mecanismo de formación de la nanojaula de carbono grafítico. (ii) Imagen SEM e (iii) Imagen TEM de NB-CN. (iv) imagen HR-TEM de NB-CN antes del lavado con ácido y (v) imagen HR-TEM de NB-CN. e Estructuras de adsorción optimizadas de los intermedios ORR y CO en BGNR [54]:(i) O 2 , (ii) OOH, (iii) O, (iv) H, (v) OH, (vi) H 2 O y (vii) CO. f Diagrama esquemático del proceso sintético del Co 3 O 4 @NiFe Conjuntos de nanocables híbridos LDH sobre espuma de Ni y tela de carbono flexible, respectivamente [24]. g Ilustración esquemática de Zn-Ni 3 S 2 batería y batería de zinc-aire y diagrama de estructura de Ni 3 S 2 molecular, respectivamente [23]
Dopaje de múltiples átomos
El dopaje de múltiples átomos incluye tanto el codopaje de heteroátomos (NS, NP, NB, etc.) como el codopaje de heteroátomos y metales [55] (Fe-Co – N [56], Mn-N [57], Fe– N [58], Co-Fe – NP [12], Co-Fe – N [39], Co-Mn-NP [59], Co – Cu-N [60, 61], Co – Cu-P, etc. .). Por un lado, el dopaje con heteroátomos puede generar efectivamente efectos de defectos sinérgicos en el catalizador, lo que conduce a una mayor actividad catalítica [62, 63]. Por otro lado, se ha confirmado que el dopaje conjunto con átomos y heteroátomos de metales de transición puede mejorar eficazmente el rendimiento de reducción de oxígeno del catalizador [64, 65]. Además, existe un efecto sinérgico entre multimetal y heteroátomos que aumenta la actividad electrocatalítica del catalizador. Los multimetales pueden mejorar la conductividad y el estado de oxidación del catalizador, aumentando así la cantidad de transferencia de carga del catalizador [66] y el rendimiento electrocatalítico del catalizador [60]. Por ejemplo, Diao et al. estableció mediante DFT que el dopaje con Cu puede conducir a sitios más positivos adyacentes al Co y debilitar la fuerza de unión entre los sitios activos de superficie y los intermedios adsorbidos, aumentando así las tasas de transferencia de masa y carga y la exposición de los sitios activos [61]. Como se muestra en la Fig. 3a, en Co 2 dopado con Cu P, se produce un claro agotamiento de electrones en los sitios de Co vecinos de los átomos de Cu, lo que indica que el dopaje con Cu puede cambiar la distribución de electrones de Co 2 P [22].
Efecto sinérgico
Un efecto sinérgico en la catálisis se puede definir como una mejora significativa en la actividad catalítica cuando se combinan varios elementos (metales o no metales) o compuestos, en comparación con cuando estos elementos o compuestos se utilizan por sí solos. El efecto sinérgico puede ayudar en la regulación de la estructura electrónica del sustrato del catalizador, mejorando la actividad electrocatalítica [37, 67], y puede producir una fuerte coordinación para producir sitios más activos [56]. Esta colaboración se puede clasificar en las siguientes categorías:
-
Los grupos metálicos / no metálicos altamente activos experimentan sinergismo con los sustratos conductores de carbono / nitrógeno dopados. Un ejemplo de esta categoría son los compuestos de metal-nitrógeno-carbono (M – N-C) [68,69,70], como los compuestos de Co – N-C. Pueden existir sitios activos de Co-N-C en la interfaz entre el Co y el carbono dopado con N, lo que puede facilitar la formación / deposición de O *. Además, se ha demostrado que el Co-N x Los sitios y el N incrustado en la matriz de carbono son sitios activos en catalizadores híbridos ORR de metales no nobles [68]. Otros ejemplos incluyen metales de transición (Co y Fe) en carbono N-dopado [39, 71, 72], piridina-N [58], grafitización-N [71], especies Co-azo [71], N, P co- materiales dopados, nanofibras de carbono heteroporosas en capas dopadas con N que poseen excelentes rutas de transporte de electrones y una alta superficie específica [10] y nanocompuestos de grafeno. Los nanocompuestos de grafeno se han sintetizado a través del crecimiento hidrotermal in situ de CoSe y nanopartículas de seleniuro de níquel en nanoláminas de grafeno (GN). El efecto sinérgico entre las nanopartículas compuestas y el grafeno mejora el rendimiento electroquímico del catalizador [73, 74]. Lo más importante es que se ha demostrado que la fuerte coordinación entre el centro metálico y la piridina-N puede promover la formación de sitios activos piridina-NM, y la piridina-N rica en electrones puede acelerar eficazmente la transferencia de carga al centro metálico, por lo que mejorando enormemente la actividad de ORR [75, 76].
-
La sinergia entre metales confiere a los catalizadores un efecto de aleación que ajusta la estructura electrónica del sistema y optimiza la combinación de oxígeno [74, 77]. El efecto sinérgico de los sitios activos bimetálicos sobre la electrocatálisis de oxígeno se ha estudiado previamente. Para NiCo 2 S 4 @ g-C 3 N 4 -Electrodo flexible integrado CNT, los electrones se transfieren desde el sitio activo bimetálico de Ni / Co a la abundante piridina-N en g-C 3 N 4 y cooperar con el CNT conductor acoplado para promover la electrocatálisis de oxígeno reversible. Los cálculos teóricos indican que la especie piridina metal-N (Ni, Co-N 2 ) tiene un efecto de coactivación único en el átomo bimetálico de Ni / Co. Reduce su centro de banda d y facilita la adsorción / desorción de intermediarios de oxígeno, acelerando así la cinética de reacción. En un Fe-O 4 codopado N @ NC, el centro de metal puede generar un fuerte efecto de coordinación con la piridina-N, y el codopaje de Fe y N promueve significativamente la formación de un gran número de sitios activos de piridina-NM en la ORR [78,79 , 80,81]. En Co 3 poroso hibridado O 4 anclado en MnO 2 , Co y Mn generan un efecto de acoplamiento, acelerando así la velocidad de transporte de electrones, formando una zona tampón y acelerando la separación de los productos de la superficie del catalizador [82]. Otro ejemplo son las GN dopadas con N y Co-modificadas con nanopartículas de Co [60]. Además, la excelente actividad electrocatalítica del Co 2 P @ CNF se puede explicar por la fuerte interacción entre el Co 2 Los nanocristales de P y el revestimiento de carbono poroso se doparon conjuntamente con CoNx y N y P, lo que da como resultado un transporte de carga interfacial mejorado y la regulación del Co 2 P actividad electrocatalítica [83]. Un nuevo 2D MoSe 2 -Ni (OH) 2 El material también se ha preparado mediante una simple síntesis hidrotermal de un solo paso. El 2D MoSe 2 -Ni (OH) 2 El nanohíbrido, con una estructura de nanohojas de orientación vertical única, proporciona una gran cantidad de superficie específica electroactiva, acortando la longitud de difusión de los iones de electrolito y mejorando así la cinética de la reacción electroquímica [84].
Defectos estructurales
Se considera que los defectos, incluida la distorsión de la celosía, las rayas rotas y los sitios de los bordes en las esquinas, tienen un efecto positivo sobre la actividad catalítica. Se ha establecido que los defectos en los bordes de DG (grafeno defectuoso) pueden reducir los cambios de energía libre de ORR y OER, mejorando así la actividad catalítica y la conductividad de DG [85]. Por ejemplo, la introducción de átomos de P en la matriz de carbono dopado con N puede producir eficazmente un efecto de defecto sinérgico y una estructura N-P, optimizando así el rendimiento catalítico en los REA y ORR [12]. Mientras tanto, H 2 [86] y el grabado con plasma de Ar también se puede utilizar para formar materiales con estructuras ricas en defectos.
Ajuste de la estructura electrónica y el entorno de coordinación
Con respecto a la estructura electrónica del catalizador, se ha estimado ampliamente que la distribución de carga superficial del catalizador se puede ajustar introduciendo defectos, como cationes heterometálicos dopados. Los defectos, incluidas las vacantes de oxígeno (VO) [77], pueden aumentar el número de sitios catalíticos activos o proporcionar al catalizador una nueva actividad catalítica [87]. El VO se puede lograr mediante grabado con plasma de Ar [88]. En medios alcalinos, un catalizador ORR eficiente debería poder reducir completamente el oxígeno a hidróxido a través del proceso de reducción de cuatro electrones, mientras que un catalizador ORR más débil termina la secuencia de reacción en medio del proceso de transferencia de dos electrones. Por ejemplo, Lian et al. demostró que una configuración orbital 3D del centro metálico promueve la ORR ajustando el estado de oxidación y el estado electrónico del centro metálico. Además, la coordinación local puede acelerar aún más la tasa de conversión de las sustancias redox objetivo [10]. Los átomos de Co también tienen una excelente actividad debido a sus diferentes estados de valencia posibles. Co 2+ y Co 3+ ocupar los sitios tetraédricos y octaédricos de Co 3 O 4 , respectivamente, lo que ayuda a promover la transferencia de electrones en los REA [11]. Además, la deposición de hidróxidos dobles ultrafinos en capas de NiFe (NiFe LDH) en la superficie de Co 3 O 4 puede ajustar la valencia química de la superficie de Co, Ni y Fe cambiando el donador de electrones y / o el efecto de absorción de electrones, lo que da como resultado el equilibrio y la optimización del rendimiento de ORR y OER [89], como se muestra en la Fig. 3f.
Aumentar el número de estructuras de poros
Los materiales nanoestructurados tienen estructuras de poros ricas y un gran número de canales mesoporosos, que desempeñan un papel vital en la modificación de los canales de transmisión de oxígeno [11], prolongando el tiempo de captura de las moléculas de oxígeno y mejorando su interacción con los sitios catalíticos activos. Algunos materiales nanoestructurados presentan una estructura 2D / 3D [90], que tiene una superficie específica más grande y aumenta el número de interfaces trifásicas. Mediante un diseño racional, se puede construir un material poroso nanoestructurado con una gran superficie y alta conductividad para garantizar que más nanopartículas estén en contacto directo con el electrolito, lo que resulta en una menor resistencia entre el material activo y el electrolito [83]. Una estructura de poros rica puede acelerar la transferencia de carga y la difusión entre cargas y aumentar la transferencia de masa, mejorando así el rendimiento del catalizador [11, 39]. Las superficies de los materiales nanoestructurados tienen un índice de refracción bajo estable y pueden exhibir energías de adsorción de oxígeno similares a las de la superficie de Pt [91]. Esta característica es parte de las condiciones requeridas para el desempeño catalítico altamente eficiente del catalizador. Los materiales nanoestructurados que se pueden usar como cátodo de aire de ZAB incluyen Ni 3 Nanohojas C / NC (2D), Ni 3 S 2 / Matrices de nanohojas de Ni [1] (como se muestra en la Fig. 3g), Co 3 poroso uniforme O 4 nanopartículas / nanoláminas [11, 45], CNT dopado con N (generalmente utilizado como sustrato activo), NiCo hueco 2 O 4 nanoesferas, CNT dopados con N [92] y MoSe 2 / G nanohíbridos [93].
Ajuste de la estructura del catalizador
Se requiere un catalizador con una estructura razonable para catalizar una reacción. Los óxidos de metales de transición con estructura de espinela pueden ayudar a reducir los sobrepotenciales, mejorando así la eficiencia de conversión de energía del catalizador [82, 94]. La estructura 2D / 3D del catalizador puede resultar en una excelente actividad catalítica debido al área de contacto ampliada entre el sitio activo y el electrolito. Por ejemplo, flores nanoporosas de NiO codopadas, en las que el efecto sinérgico entre el marco hexagonal 2D y una gran cantidad de nanoporos en el costado de la nanocapa aumenta el número de sitios activos catalíticos efectivos para O 2 adsorción / difusión [5]; y la estructura única del sistema Co / Co-NC en capas 3D que puede proporcionar un número eficiente de sitios activos [29]. Otros ejemplos incluyen un nuevo material compuesto de punto cuántico dopado con hidrógeno de grafeno / B que tiene una estructura 3D única, alta porosidad y gran área de superficie específica, que exhibe una abundancia de sitios catalíticamente activos y un mejor transporte de masa de electrolitos y difusión de iones [95], y un Co-MOF 2D que se cultiva directamente en CC proporcionando el espacio de crecimiento 3D Co-MOF suficiente para formar una estructura de sistema MOF en capas 3D-sobre-2D. En comparación con un MOF exclusivamente 3D o 2D, se exponen sitios más catalíticamente activos [24]. Además, el marco 3D facilita la penetración total del electrolito y promueve el transporte de electrones en la estructura de red porosa [41]. Además, la miniaturización del volumen del material catalítico también puede mejorar la eficacia catalítica. Por ejemplo, a escala atómica, un CoO ultradelgado x La capa acelera eficazmente la conducción de electrones y proporciona abundantes sitios activos. Esto se debe a la introducción de oxidación de Co en las nanoláminas que pueden aumentar el número de centros activos expuestos [23]. Otro ejemplo incluye un 2D La (OH) 3 -nanohíbrido de grafeno, preparado mediante una técnica de reducción solvotermal simple y económica, que se ancla electrostáticamente en GN 2D para evitar la agregación de hidróxido de lantano y proporcionar varios centros electroactivos para la reacción [96].
Conclusiones y perspectivas futuras
Aunque la investigación actual sobre ZAB ha logrado algunos avances sustanciales, todavía existen grandes desafíos, incluido el desarrollo de nuevos métodos para sintetizar cátodos flexibles autoportantes, explorar mecanismos electrocatalíticos e identificar materiales adecuados para sintetizar cátodos flexibles con excelente desempeño catalítico. Como uno de los materiales catalizadores importantes para los ZAB, los catalizadores a base de carbono han atraído una atención significativa debido a su gran superficie específica, abundantes centros activos y buena conductividad eléctrica. Sin embargo, los materiales de carbono todavía adolecen de algunas desventajas, como la toxicidad incierta de los CNT, un costo más alto que otros materiales electrocatalizadores flexibles y una mala repetibilidad en diferentes sustratos; Los materiales de carbono derivados de biomateriales naturales tienen una flexibilidad y conductividad relativamente bajas, lo que limita el rendimiento de los dispositivos electrónicos portátiles en los que se aplican. Se espera que un estudio extenso sobre la microestructura del catalizador y el efecto del dopaje atómico, así como la relación interna entre la distribución electrónica del catalizador y su desempeño de reducción de oxígeno electrocatalítico, juegue un papel vital en la identificación efectiva de la función real de los iones metálicos. N, S y P, y otros elementos de dopaje en los sitios activos y profundizar la comprensión del proceso de ORR de electrocatálisis de catalizador de carbono. Esperábamos contribuir al desarrollo de catalizadores ORR de metales no nobles a base de carbono, asequibles y de alto rendimiento. Se han utilizado productos electrónicos flexibles a base de carbono para detectar el pulso y la frecuencia respiratoria humanos [97]. Se cree que en el futuro se comercializarán más dispositivos electrónicos flexibles multifuncionales basados en catalizadores ZAB flexibles basados en carbono.
Disponibilidad de datos y materiales
No aplica. Se han citado todas las imágenes del artículo.
Abreviaturas
- ZAB:
-
Baterías de zinc-aire
- ORR:
-
Reacción de reducción de oxígeno
- REA:
-
Reacción de desprendimiento de oxígeno
- CC:
-
Paño de carbón
- PEO:
-
Óxido de polietileno
- PAM:
-
Poliacrilamida
- PAA:
-
Ácido poliacrílico
- CNT:
-
Nanotubos de carbono
- TMP:
-
Fosfuros de metales de transición
- CFP:
-
Papel de fibra de carbono
- DFT:
-
Teoría funcional de la densidad
- DG:
-
Grafeno defectuoso
- VO:
-
Vacantes de oxígeno
- NiFe LDH:
-
Hidróxidos dobles en capas de NiFe
Nanomateriales
- Diseño higiénico para la industria alimentaria y de procesamiento
- Nanopartículas para la terapia del cáncer:avances y desafíos actuales
- Avances y desafíos de los nanomateriales fluorescentes para síntesis y aplicaciones biomédicas
- El diseño de la capa de emisión para multiplicadores de electrones
- Ingeniería del proceso de recubrimiento por inmersión y optimización del rendimiento para dispositivos electrocrómicos de tres estados
- Síntesis y propiedades electroquímicas de materiales de cátodo LiNi0.5Mn1.5O4 con dopaje compuesto Cr3 + y F− para baterías de iones de litio
- Preparación de micromateriales híbridos de MnO2 recubiertos de PPy y su rendimiento cíclico mejorado como ánodo para baterías de iones de litio
- Un diseño eficiente y eficaz de nanocables de InP para la máxima captación de energía solar
- Efecto de diferentes aglutinantes sobre el rendimiento electroquímico del ánodo de óxido metálico para baterías de iones de litio
- Síntesis y rendimiento in vitro de nanopartículas de hierro-platino recubiertas de polipirrol para terapia fototérmica e imágenes fotoacústicas
- Seis estrategias de cadena de suministro para petróleo y gas en la era del coronavirus



