Actividad imitadora de peroxidasa activada por electrones calientes de nanozimas ultrafinas de Pd
Resumen
Las nanozimas activadas por luz pueden brindar una gran cantidad de nuevas oportunidades para la industria química y la biotecnología. Sin embargo, los actuales sistemas catalíticos controlados a distancia distan mucho de ser satisfactorios. A continuación, presentamos un ejemplo interesante de la aplicación de nanohojas de Pd ultrafinas (Pd NS) como un imitador de peroxidasa controlable por luz. Dado que la mayoría de los átomos de Pd están expuestos en su superficie, las NS de Pd con un espesor de 1,1 nm poseen una alta actividad similar a la peroxidasa. Más importante aún, bajo excitación de luz, dicha actividad intrínseca puede activarse adicionalmente en casi 2,4 a 3,2 veces. Tal fenómeno se puede atribuir a la propiedad óptica única de los NS de Pd ultrafinos, que pueden capturar fotones de manera eficiente para generar electrones calientes a través del efecto de resonancia de plasmón superficial y así promover la descomposición in situ de H 2 O 2 en radicales de especies reactivas de oxígeno (O *). Esta catálisis mejorada también se puede utilizar para la detección colorimétrica de H2O2 en tiempo real y altamente sensible. Esperamos que nuestro trabajo pueda proporcionar información valiosa sobre el diseño racional de nanozimas artificiales con actividad controlable y eficiente en el diagnóstico biomédico, la administración de fármacos y la química ambiental.
Introducción
Las enzimas naturales son biocatalizadores exquisitos que pueden catalizar casi todas las transformaciones químicas de la vida [1, 2]. Sin embargo, todavía existen defectos inherentes, como una estabilidad deficiente y un coste elevado. Desde que se informó por primera vez sobre nanopartículas de magnetita con actividad intrínseca de imitación de la peroxidasa [3], el diseño y desarrollo de nanomateriales con actividades similares a las enzimas (nanozimas) ha atraído una creciente atención de la investigación [4]. Hasta ahora, se han utilizado una serie de nanomateriales a base de óxido [5,6,7], metal [8,9,10] y carbono [11,12,13] para imitar la peroxidasa de rábano picante (HRP). Entre ellos, los nanomateriales de metales nobles [8, 14,15,16,17,18,19], como la plata (Ag) [15], el oro (Au) [16, 17], el platino (Pt) [8], y se ha informado que el paladio (Pd) [18, 19] et al., poseen altas actividades miméticas de peroxidasa. Por otro lado, también se ha informado de la introducción de luz para activar la actividad de las nanozimas, lo que ofrece una gran cantidad de oportunidades para la industria química y biotecnológica [4, 20]. Sin embargo, los actuales sistemas catalíticos controlados a distancia distan mucho de ser satisfactorios.
Los nanomateriales metálicos plasmónicos pueden capturar o responder a la luz solar debido a la propiedad óptica única de la resonancia de plasmón superficial (SPR). Estos nanomateriales metálicos, que pueden capturar fotones para generar electrones calientes a través del efecto SPR, se han convertido en los materiales clave para mejorar la velocidad catalítica [21], promover la nueva detección óptica de biomoléculas [22], diseñar terapia fototérmica y utilizar la luz solar como energía renovable [ 23, 24]. Sin embargo, ninguno de ellos se centró en el efecto SPR de las nanoenzimas a base de metal plasmónico en sus actividades de imitación de enzimas. Por lo tanto, sería atractivo combinar nanozimas a base de metal plasmónico con efecto SPR para lograr una catálisis enzimática altamente activa y sintonizable a la luz.
En este documento, informamos por primera vez que las nanohojas ultrafinas de Pd (Pd NS) con un grosor de aproximadamente 1,1 nm pueden servir como un imitador de peroxidasa excelente y controlable por la luz. Se ha informado que los sistemas de nanoenzimas controlados por luz y nanozimas basados en Pd exhiben múltiples actividades miméticas de enzimas, incluidas la oxidasa, peroxidasa, catalasa y superóxido dismutasa [4, 18, 19]. Sin embargo, sus estructuras son generalmente partículas, bultos y varillas. Como todos sabemos, los NS ultrafinos de Pd tienen una alta energía de superficie, un tamaño lateral pequeño y una alta movilidad de electrones, lo que da como resultado una alta densidad de sitios de superficie activa [25]. Además, la mayoría de los átomos expuestos a nanoláminas ultrafinas pueden servir como una plataforma ideal para diseñar su rendimiento [26]. Inspirándonos en la estructura única de las nanohojas ultrafinas, presentamos una estrategia que no solo aprovecha al máximo los sitios activos de los átomos de Pd, sino que también inyecta electrones calientes en el proceso de catálisis enzimática. Como se muestra en el Esquema 1, la interacción de fotones con NS de Pd ultradelgados puede excitar la resonancia del plasmón de superficie que decae de forma no radiativa en electrones y huecos calientes, promoviendo así el H 2 O 2 Descomposición reductora in situ para generar radicales de especies de oxígeno (O *) con TMB oxidante bajo visible. Al introducir luz visible en la reacción enzimática, las NS de Pd exhiben actividades catalíticas significativamente más altas que las de las NS de Pd en condiciones de oscuridad.
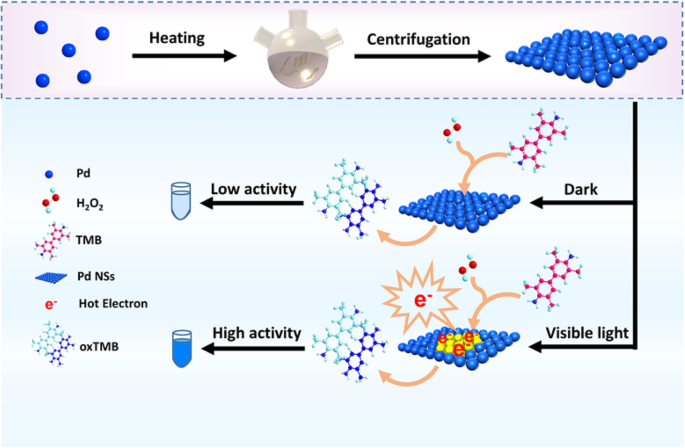
Ilustración esquemática de la estructura de Pd NS y la variación de la actividad de Pd NS bajo luz oscura y visible
Materiales y experimentales
Materiales y caracterizaciones
El ácido cítrico (CA); N, N-dimetilformamida (DMF); 3,3,5,5-tetrametilbencidina (TMB); y bromuro de cetiltrimetilamonio (CTAB) se adquirieron de Sigma Aldrich. Acetilacetonato de Pd (II), W (CO) 6 y polivinilpirrolidona (PVP) se obtuvieron de Macklin. Peróxido de hidrógeno (H 2 O 2 , 30% en peso) se compró a Beijing Chemicals (Beijing, China). Todos los químicos fueron usados sin purificación adicional. Durante todo el trabajo se utilizó agua experimental purificada por el sistema Millipore (18,2 MΩ; Millipore Co., EE. UU.).
Las estructuras de fase de los productos se caracterizaron por un difractómetro de rayos X PANalytical que utilizó radiación Cu Kα ( λ =1,5406 Å). Y los espectros de reflectancia difusa UV-vis (DRS) de las muestras se caracterizaron a temperatura ambiente utilizando el Lambda 750, PerkinElmer. Las concentraciones de catalizadores en soluciones fueron determinadas por ICP-AES (720, Agilent). Las imágenes de microscopía electrónica de transmisión (TEM) se registraron en un microscopio electrónico de transmisión JEM1400 plus operado a 100 kV. Se realizaron análisis TEM de alta resolución (HRTEM) en un microscopio electrónico de transmisión de emisión de campo (FE-TEM) JEM-2100F a 200 kV.
Síntesis de nanohojas de Pd
De acuerdo con el método informado [27], se sintetizaron Pd NS. Brevemente, acetilacetonato de Pd (II) (16 mg), PVP (PM =24.000, 30 mg), CA (150 mg) y CTAB (60 mg) se mezclaron en DMF (10 ml) y se agitaron en una atmósfera de nitrógeno durante 1 h. Cuando el color de la solución en el matraz (25 ml) cambia a una solución uniforme de color rojo anaranjado, 100 mg de W (CO) 6 se añadió a la solución bajo una N 2 atmósfera. A continuación, calentar el matraz a 80 ° C durante 1 h. Después de la reacción, el producto azul oscuro se separó por centrifugación (9000 rpm / min, 3 min) con una cantidad suficiente de acetona y luego se dispersó en etanol. Este proceso se repitió tres veces. Finalmente, las nanohojas de Pd se dispersaron en 10 ml de etanol para experimentos adicionales.
Medición fotocatalítica de imitación de peroxidasa
La actividad de imitación de peroxidasa de las nanozimas Pd NSs se evaluó midiendo la oxidación de TMB. Una lámpara Xe de 300 W (CEL-HXF300 / CEL-HXUV300, China education Au-light Co., Ltd., Beijing) sirvió como fuente de luz, y la adición de un filtro de vidrio habilita la luz visible ( λ ≥ 400 nm) para pasar. En un experimento típico, 12,6 μg mL −1 Se añadieron nanozimas de Pd NS (medidas por ICP-AES) a 1 ml de solución tampón de ácido fosfórico (0,1 M, pH 4) que contenía H 2 50 mM O 2 y TMB 0,7 mM a temperatura ambiente. Durante el tiempo diferente bajo irradiación, la actividad de imitación de la peroxidasa se determinó controlando el pico de absorción característico a 652 nm después de la centrifugación, lo que indica la concentración de productos de oxidación de TMB. El experimento de control tuvo las mismas condiciones a excepción de la iluminación.
Resultados y discusión
Diseño y caracterización de las nanozimas de Pd NS
Se preparó una síntesis típica de nanohojas de paladio a través de un método clásico (Fig. 1a) para construir una serie de nanozimas ultrafinas de sitios atómicos altamente activos que tienen sustratos inherentes y captura de fotones y características eficientes que imitan la enzima del peróxido. La Figura 1 b – d muestra una imagen típica de microscopía electrónica de transmisión (TEM) de bajo aumento de las NS de Pd sintetizadas, en la que se componen de nanohojas uniformes con dimensiones laterales de aproximadamente 10,0 nm (figura 1b, recuadro) y el grosor promedio de aproximadamente 1,1 nm (figura 1c, recuadro). Según el tamaño, el porcentaje de área de la superficie plana superior e inferior es superior al 90%. La microscopía electrónica de transmisión de alta resolución (HRTEM) se utiliza para confirmar aún más la morfología y la fase de las NS de Pd. La Figura 1g muestra los espaciamientos apropiados de ~ 0.22 y 0.256 nm para los planos de celosía (111) y (200) del paladio [27]. Para satisfacer las necesidades del experimento, el patrón XRD de Pd NS se caracterizó por la carga de carbono comercial. Como se muestra en la Fig. 1e, los picos de difracción alrededor de 40.11, 46.65 y 68.12 corresponden a los planos (111), (200) y (220) de NS de Pd cúbicos, lo cual es consistente con la observación de HRTEM. Además, no hay picos indicativos de fases cristalinas distintos de los picos asociados con el carbono comercial. El espectro de Pd 3d presenta dos picos (Fig. 1f) Pd 3d 5/2 y Pd 3d 3/2 (resultante de la división espín-órbita), ubicados respectivamente en 335,5 y 339,2 eV [25], lo que reveló que hay dos entornos químicos para el átomo de paladio.
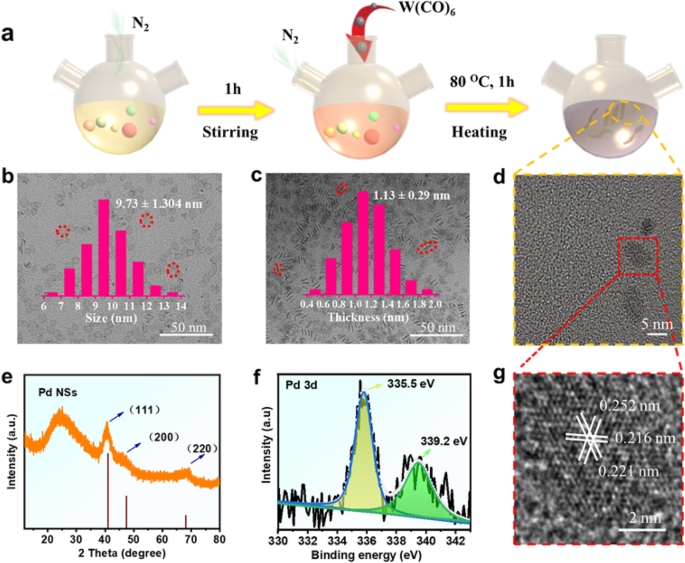
Caracterización de las nanozimas. un Mecanismo de crecimiento de nanozimas de Pd. b , c y d TEM. e Patrones XRD. f Espectro Pd 3d XPS de Pd NS. g Imagen HRTEM de Pd NS
Actividad fotocatalítica de imitación de peroxidasa
La actividad similar a la peroxidasa de las Pd NS se investigó utilizando TMB como un sustrato de peroxidasa típico. Dado que la mayoría de los átomos de Pd se expusieron en la superficie de las nanohojas ultradelgadas, razonamos que las NS ultrafinas de Pd poseen una alta densidad de sitios de superficie activa y, por lo tanto, dan como resultado una excelente actividad catalítica. Como era de esperar, en la coexistencia de H 2 O 2 , Las NS de Pd pueden catalizar eficazmente la oxidación del sustrato incoloro TMB al producto azul oxTMB, con la absorción característica a 652 nm (Fig. 2a, b). Sin embargo, sin la adición de H 2 O 2 , la actividad de las Pd NS puede despreciarse bajo la misma condición experimental, lo que reveló que la actividad similar a la peroxidasa jugó un papel importante durante la reacción. Al igual que las enzimas naturales y otras nanozimas, las nanozimas de Pd tienen una actividad peroxidasa dependiente del pH, la temperatura y la concentración (Fig. 2c y Fig. S1). En la condición del experimento, los Pd NS mostraron una actividad catalítica optimizada en la solución de ácido débil, y el pico de absorbancia característico de la solución de reacción fue el más alto a 35 ° C cuando la temperatura varió de 25 a 75 ° C (Fig. 2c). Sorprendentemente, con o sin irradiación de luz, se observó una diferencia significativa en la actividad de imitación de peroxidasa (Fig. 2d y Fig. S2). De acuerdo con el valor de absorción de la solución de reacción durante 60 min, la actividad de Pd NS bajo luz visible exhibió aproximadamente 2,4 ~ 3,2 veces mayor que la de Pd NS en condiciones de oscuridad (Fig. 2d y Fig. S2). De manera similar, la introducción de luz en el proceso de catálisis de otras nanopartículas metálicas plasmónicas también puede aumentar su actividad similar a la peroxidasa (Fig. S3-S5). Comparando estas nanozimas, encontramos que las NS de Pd mostraban el mayor rango de regulación de actividad. Este fenómeno se debe principalmente a la estructura única de la nanoplaca ultrafina. De estos resultados obtenidos, podemos inferir que la luz visible tiene un efecto directo sobre la actividad similar a la peroxidasa de todos los nanomateriales metálicos plasmónicos (Fig. 2e), y el efecto SPR puede jugar un papel esencial en el proceso catalítico.
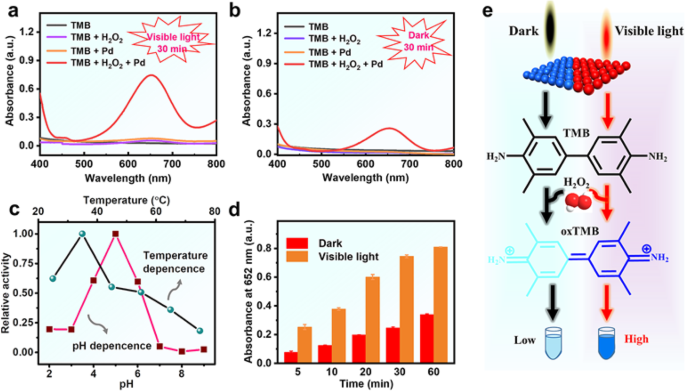
La actividad de imitación de peroxidasa de Pd NS. a-b Espectros de absorción UV-visible típicos de diferentes muestras en condiciones de luz y oscuridad visibles. c Efecto de la temperatura y el pH sobre la actividad imitadora de la peroxidasa. d Cursos de tiempo para la actividad imitadora de la peroxidasa. e El mecanismo similar a la peroxidasa de las Pd NS bajo luz oscura y visible. Condiciones experimentales:luz visible =λ ≥ 400 nm, TMB =0,7 mM, H 2 O 2 =50 mM, temperatura =25 ° C, Pd NSs =12,6 μg / mL y solución tampón de fosfato (0,1 M, pH 4)
Investigación cinética y del mecanismo de nanozimas de Pd
Para caracterizar el comportamiento enzimático de las NS de Pd, determinamos la teoría de la cinética de la enzima para la reacción. Sin embargo, dentro del rango de concentración adecuado de TMB, las NS de Pd presentan una curva típica de Michaelis-Menten (Fig. 3a). La constante de Michaelis (Km) y la velocidad máxima de reacción (Vmax) se obtuvieron utilizando la ecuación de Lineweaver Burk, como se muestra en la Tabla S1. En comparación con la peroxidasa de rábano picante (HRP), el valor de Km aparente de las NS de Pd con TMB se debilitó en 0,28 (Fig. 3a, by Tabla S1). Este resultado indica que la estructura de la hoja ultrafina de las Pd NS preparadas exhibe una alta afinidad por TMB, incluso más alta que la de la enzima natural HRP.
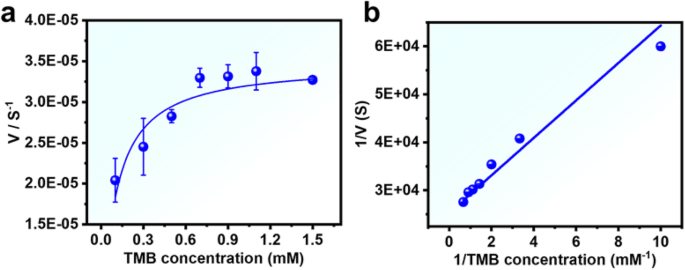
Ensayo cinético de estado estacionario y mecanismo catalítico de Pd NS (12,6 μg / mL). un La concentración de H 2 O 2 fue de 50 mM, y se varió la concentración de TMB (0,1-1,5 mM). b Gráficos recíprocos dobles para TMB
Dado que está claro que H 2 O 2 pueden descomponerse para formar especies reactivas de oxígeno con Pd NS, es crucial comprender qué especies se producen para proporcionar una función de oxidación. En principio, los metales nobles pueden catalizar la descomposición de H 2 O 2 para formar • OH, y los intermedios de reacción O * en condiciones de pH más bajas [28], cualquiera de las cuales puede ser la especie que proporciona la función de oxidación en las reacciones enzimáticas-miméticas. Para comprender el posible mecanismo catalítico de los Pd NS, primero usamos ácido tereftálico (TA) / H 2 O 2 sistema para probar si las características de tipo peroxidasa de las Pd NS están relacionadas con la formación de radicales • OH (Fig. 4a). Usando TA como sonda fluorescente, se produjo un producto altamente fluorescente mediante la reacción del ácido 2-hidroxitereftálico con • OH [29]. Como se muestra en la Fig. 4b, la intensidad de fluorescencia de la solución disminuye significativamente después de la adición de Pd NS. Los resultados concuerdan con la disminución de la intensidad de fluorescencia con el aumento de la concentración de Pd NS (Fig. S6). Estos resultados indican que los Pd NS pueden consumir radicales • OH en lugar de generarlos. Por lo tanto, de manera similar al comportamiento catalítico informado de las nanopartículas de ferritina-platino [30], el rendimiento catalítico de nuestros Pd NS fue independiente de la formación del radical • OH.
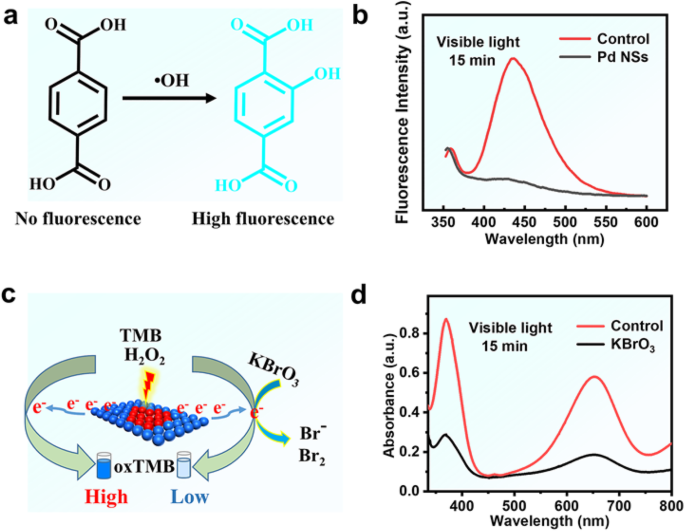
un Diagrama del mecanismo de captación de radicales hidroxilo (• OH) del ácido tereftálico (TA). Espectros de muestras que contienen tampón fosfato (0,1 M, pH 4), H 2 O 2 (50 mM) e iluminación de luz visible ( λ ≥ 400 nm, 15 min). b Los espectros de emisión de fluorescencia en presencia de Pd NS (12,6 μg / mL) y TA (66,7 μM). c Diagrama de mecanismo de KBrO 3 capturando electrónica caliente. d El espectro de absorción en presencia de Pd NS (12,6 μg / ml), KBrO 3 (0,3 mg / ml) y TMB (0,7 mM)
Para investigar si el mecanismo catalítico de las NS de Pd se relaciona con la formación de electrones calientes por la luz, también exploramos el experimento de captura de electrones calientes de especies activas durante la reacción fotocatalítica (Fig. 4c) [31]. Como se puede ver en la Fig. 4d, la capacidad catalítica de los Pd NS hacia la oxidación de TMB disminuye significativamente en 15 minutos mediante la adición de 0,3 mg / ml de KBrO 3 (un extintor de e - ). Una gran diferencia entre KBrO 3 El sistema de reacción y el sistema puro revelan que la presencia de electrones calientes podría ser crítica para la oxidación de TMB. Esto está de acuerdo con los resultados de la Fig. S7 de que las NS de Pd tienen un pico de absorción amplio a través del efecto SPR en el rango espectral de 500-1000 nm [25]. Además, una vez que los electrones calientes se alejan de la superficie de los Pd NS, quedan agujeros correspondientes en su superficie. Dado que estos orificios pueden oxidar el etanol para producir acetaldehído, también pueden tener una poderosa capacidad de oxidación hacia TMB. Como se esperaba, sin la adición de H 2 O 2 , se creó más oxTMB bajo la iluminación de luz visible.
A continuación, probamos si se formaron especies reactivas de oxígeno mediante la activación de O 2 bajo luz visible, incluido superóxido (O 2 - ). A la luz de esto, se realizaron experimentos controlados en diferentes atmósferas. Para la Fig. S8, el rendimiento catalítico de las enzimas miméticas no cambia significativamente cuando se introducen nitrógeno y oxígeno saturando el sistema de reacción, respectivamente, que no se ve afectado considerablemente por el O 2 para la actividad fotocatalítica de Pd NSs. Es esencial señalar que el rendimiento final de los Pd NS, incluso hasta 0,051 a.u./min durante 5 min bajo luz visible, fue 3,2 veces mayor que el de los catalizadores de Pd NS en la oscuridad (Fig. 2d). La actividad extremadamente alta de la nanozima de Pd bajo luz visible lleva a la hipótesis de que la existencia de electrones calientes por el efecto SPR de las NS de Pd que promueven la formación de intermediarios de reacción O * en lugar de radicales libres explica una actividad similar a la peroxidasa (Fig.5a ) [28]. En resumen, el experimento de captura de especies activas y el experimento de ventilación brindan un soporte sólido para el mecanismo enzimático mimético fotocatalítico de las Pd NS.
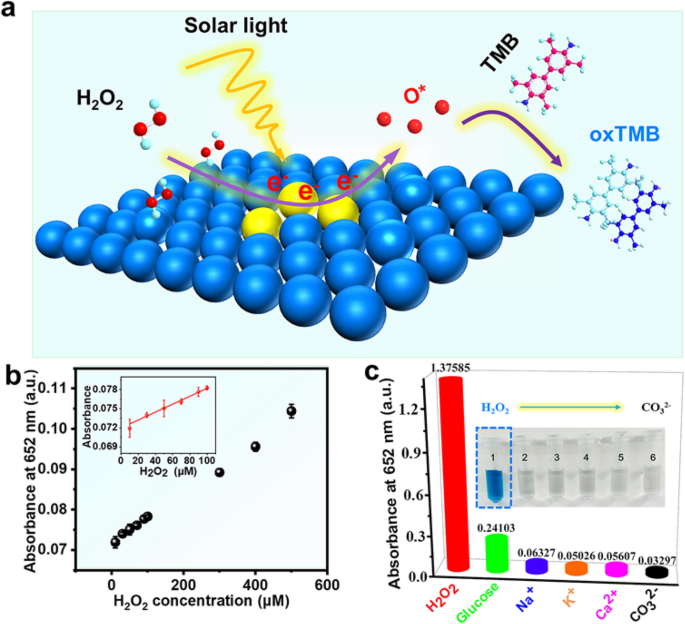
un Diagrama esquemático de un sensor para H 2 O 2 detección. b Curva dosis-respuesta de diferentes concentraciones de peróxido de hidrógeno. Condiciones experimentales:nanozima de Pd (25,2 μg / ml), tampón de fosfato (0,1 M, pH 4) e iluminación de luz visible de TMB (0,7 mM) ( λ ≥ 400 nm, 3 min). Recuadro:gráficos de calibración lineal. c Interferencia de otras impurezas en la absorbancia de H 2 O 2 sensor colorimétrico a 652 nm. Condiciones experimentales:nanozima de Pd (25,2 μg / ml), tampón de fosfato (0,1 M, pH 4), TMB (0,7 mM), iluminación de luz visible ( λ ≥ 400 nm, 15 min) e incluye 50 mM H 2 O 2 , Glucosa 200 mM, Na + , K + , Ca 2 + y CO 3 2− , y el recuadro muestra los cambios de color de las soluciones de reacción
Un nuevo sensor altamente sensible en tiempo real
Esto se demostró en varios estudios que la introducción de luz en el sensor como entrada de energía externa puede mejorar el rendimiento del sensor [22, 32, 33]. Por ejemplo, Ling et al. [32] encontró que O 2 detección de propiedades de los 10 at. % LaOCl-SnO 2 El sensor se mejoró significativamente mediante la iluminación con luz ultravioleta. Teniendo en cuenta la influencia significativa de la luz en el sensor y la excelente actividad de imitación de la peroxidasa de las Pd NS bajo luz visible en nuestros experimentos, un sensor colorimétrico eficaz y sensible H 2 O 2 fue construido. El mecanismo del sensor (Fig. 5a) muestra que los Pd NS pueden hacer un uso completo de su gran área de superficie específica para capturar fotones y generar una gran cantidad de electrones calientes. Después de eso, el electrón caliente promueve la descomposición de H 2 O 2 para producir intermedios de reacción O *, que pueden oxidar TMB a azul oxTMB. Finalmente, la detección eficiente de H 2 O 2 se realizó.
Como puede verse en el recuadro de la Fig. 5b, el rango lineal del H 2 construido O 2 sensor de nuestra parte fue de 10 a 100 μM, y el cálculo del límite de detección fue de 13,40 μM (LOD =3 s / k , donde s y k representan los bloques de calibración lineal de la desviación estándar relativa y la pendiente de ocho medidas de control paralelas, respectivamente. En este trabajo, s =2.97988 × 10 −4 , k =6,67 × 10 −5 ). Por lo tanto, el sensor de peróxido de hidrógeno basado en Pd NS fue superior a otros nanomateriales reportados bajo la condición de introducir luz. En la Tabla S2, se puede ver que con el mismo método colorimétrico para detectar peróxido de hidrógeno, nuestro sensor muestra un amplio rango de linealidad [34]. Y el límite de detección fue más bajo que muchos sensores basados en imitadores de peroxidasa basados en Fe o Co (Tabla S3) [35, 36]. Finalmente, llevamos a cabo H 2 O 2 y una serie de experimentos de control (Fig. 5c) con posibles interferencias como K + , glucosa, Na + , CO 3 2− y Ca 2+ . Como se muestra en el recuadro de la Fig. 5c, es obvio que la absorbancia de estas interferencias es débil a 652 nm y el color no cambia. Basándonos en nuestros resultados, se ha realizado con éxito un sensor de peróxido de hidrógeno altamente específico y eficiente basado en luz visible. Este sensor no solo hace un uso completo de la luz visible para mejorar su rendimiento de detección, sino que también proporciona un buen ejemplo para otros metales plasmónicos en el sensor.
Conclusiones
En resumen, demostramos un ejemplo emocionante de aplicación de nanohojas de Pd ultradelgadas (Pd NS) como un imitador de peroxidasa altamente eficiente y controlable por luz, debido a una alta densidad de sitios activos en la superficie de las nanohojas y la propiedad óptica única de SPR. Con la irradiación de luz visible, los electrones calientes generados a partir de nanohojas de Pd a través del efecto SPR pueden descomponer posteriormente H 2 O 2 para producir intermedios O *. Bajo irradiación con luz visible, tales nanozimas exhibieron una actividad similar a la peroxidasa mucho mayor que la de la oscuridad. Dicho sistema activado por luz se utilizó además para mejorar la biodetección de H 2 O 2 . El concepto básico que aquí se presenta, basado en la generación de electricidad caliente a través del efecto SPR sobre las nanozimas de Pd fotoactivadas, podría contribuir al diseño de sistemas enzimáticos artificiales inteligentes o más eficientes y ofrecer muchas nuevas oportunidades para la industria química y la biotecnología.
Disponibilidad de datos y materiales
Todos los datos generados o analizados durante este estudio se incluyen en este artículo publicado.
Abreviaturas
- Pd NSs:
-
Nanohojas de PD
- Ag:
-
Plata
- Au:
-
Oro
- Pt:
-
Platino
- Pd:
-
Paladio
- SPR:
-
Resonancia de plasmón superficial
- TEM:
-
Microscopía electrónica de transmisión
- HRTEM:
-
TEM de alta resolución
- XRD:
-
Difracción de rayos X
- HRP:
-
Peroxidasa de rábano picante
- Km:
-
Michaelis constante
- O 2 - :
-
Superóxido
Nanomateriales
- Actividad electrónica en reacciones químicas
- Nanozimas
- Predecir la toxicidad de desacoplamiento de los ácidos orgánicos
- Nanopartículas de FePO4 biocompatibles:administración de fármacos, estabilización de ARN y actividad funcional
- Preparación y actividad de hidrogenación catalítica mejorada de nanopartículas de Sb / Palygorskita (PAL)
- Efectos sinérgicos de nanopartículas de Ag / BiV1-xMoxO4 con actividad fotocatalítica mejorada
- Síntesis y actividad de oxidación del CO de óxido binario mixto 1D CeO2-LaO x catalizadores de oro soportados
- Síntesis en un solo recipiente de nanoplacas de Cu2ZnSnSe4 y su actividad fotocatalítica impulsada por la luz visible
- Fabricación, caracterización y actividad biológica de sistemas de nanoportación de avermectina con diferentes tamaños de partículas
- Actividad fotocatalítica de nanocompuesto ternario de atapulgita-TiO2-Ag3PO4 para la degradación de rodamina B bajo irradiación solar simulada
- Nanoadsorbente funcionalizado para la separación por afinidad de proteínas



