Puntos de nano-biomasa fluorescentes:extracción asistida por ultrasonidos y su aplicación como nanoprobe para la detección de Fe3 +
Resumen
La biomasa como recurso sostenible y renovable ha sido una de las fuentes de energía importantes para la vida humana. En este documento, se han extraído puntos luminiscentes de nanobiomasa (NBD) de la soja mediante un método ultrasónico, que confiere a la biomasa propiedades de fluorescencia. Los NBD preparados son de estructura amorfa con un diámetro medio de 2,4 nm y muestran una fluorescencia azul brillante con un rendimiento cuántico del 16,7%. Beneficiándose de las materias primas comestibles y del proceso de síntesis sin calentamiento, la prueba de citotoxicidad muestra que la viabilidad celular aún se mantiene al 100% incluso si la concentración de los NBD alcanza los 800 μg / ml, lo que indica la buena biocompatibilidad de los NBD. Además, la fluorescencia de los NBD es muy sensible al Fe 3+ , que se puede utilizar para Fe 3+ detección en términos de su superioridad en salud. El límite de detección (LOD) del sensor propuesto se determinó como 2,9 μM, que es más bajo que el nivel máximo permitido de Fe 3+ (5,37 μM) en agua potable.
Antecedentes
Los nanomateriales luminiscentes han logrado una amplia variedad de aplicaciones debido a sus propiedades ópticas únicas, especialmente en diodos emisores de luz, detectores, bioimagen y detección de iones metálicos [1, 2, 3, 4, 5, 6]. Se han informado varios nanomateriales luminiscentes hasta ahora, como puntos cuánticos semiconductores (QD), nanopuntos de carbono y QD de azufre, que han dado lugar a muchos avances en muchos campos [7,8,9,10,11,12] . Los QD como excelente representante de los nanomateriales luminiscentes se han utilizado en muchos campos debido a sus excelentes propiedades ópticas y eléctricas. A pesar de todo esto, la toxicidad de las QD todavía limita en gran medida sus aplicaciones [13, 14]. Siempre es de gran importancia encontrar nanomateriales con luminiscencia más ecológicos y sostenibles. La biomasa es una materia orgánica original que se puede producir mediante la fotosíntesis, y se destaca por sus propiedades sostenibles y renovables. Específicamente, la biomasa se define como la fracción biodegradable de productos, desechos y residuos de un organismo [15, 16]. En el contexto de la nanotecnología, la biomasa se suele utilizar como precursora, pudiendo convertirse en nanopuntos con determinadas propiedades ópticas tras un tratamiento especial. En comparación con los precursores químicos, los principales componentes de la biomasa, especialmente la comestible, son los azúcares y las proteínas, que son inocuos en los tratamientos posteriores. Por tanto, los puntos de nano-biomasa (NBDs) deben ser de alta biocompatibilidad, lo que asegure sus aplicaciones en campos biológicos y ambientales sin producir sustancias nocivas.
Hasta ahora, solo se han reportado nanopuntos de carbono fluorescentes derivados de la biomasa. Básicamente, parte de la biomasa natural, como las hojas, la clara de huevo y el jugo de limón, se trataron mediante un método hidrotermal para sintetizar nanopartículas de carbono de fluorescencia [17,18,19]. También hay otro tipo de nanopuntos de carbono que existen en los alimentos comestibles, que se producen en el procesamiento posterior de la biomasa natural [20, 21]. Todos ellos, sin excepción, implicaron procesos típicos de carbonización a alta temperatura. Este proceso puede implicar un tiempo prolongado y una temperatura elevada, y es difícil lograr una producción por lotes a gran escala [22]. En comparación con las altas temperaturas, la temperatura ambiente o las condiciones de baja temperatura son fáciles de realizar y mantienen las propiedades originales de la propia biomasa.
Nanoprobe es una de las aplicaciones importantes de los nanomateriales luminiscentes [23]. En vista de la fluorescencia brillante y la alta biocompatibilidad, los NBD se pueden utilizar como una especie de nanosensda en el campo de la biología y el medio ambiente. Fe 3+ es un ión metálico importante en el cuerpo humano por el que desempeñan un papel importante en la síntesis de hemoglobina y mioglobina [24]. Pero el exceso de Fe 3+ La acumulación en el cuerpo puede provocar daño tisular y fallo de órganos. Desarrollo de sistemas de detección eficaces y más ecológicos para la determinación cualitativa y cuantitativa de Fe 3+ es de gran importancia para las preocupaciones clínicas, médicas y ambientales. Esto nos permite considerar si la biomasa se puede adaptar en nanopuntos con propiedades deseables directamente de la biomasa comestible natural sin ningún procesamiento. Sin embargo, hasta donde sabemos, ninguno de estos NBD luminiscentes ha sido informado. Por lo tanto, buscar precursores de biomasa más naturales para obtener NBD con propiedades deseables y alta biocompatibilidad puede dar un paso hacia nanomateriales luminiscentes y Fe 3+ más ecológicos. detección.
Aquí, los puntos luminiscentes de nano-biomasa (NBD) se han demostrado mediante la estrategia de extracción ultrasónica (UES) de la soja por primera vez. El rendimiento cuántico de fotoluminiscencia (PL) (QY) de los NBD preparados puede alcanzar el 16,7%, y los NBD muestran una emisión brillante en estado sólido. La prueba de citotoxicidad muestra que los NBD tienen una alta biocompatibilidad. Además, los NBD se han empleado para Fe 3+ detección por su dependencia de la intensidad de fluorescencia linealmente en el Fe 3+ concentración, y el límite de detección (LOD) puede alcanzar 2,9 μM.
Métodos
Materiales
Variedades de soja del noreste de acuerdo con el Estándar Nacional de la República Popular de China ( GB1352-2009 ) se compraron en el supermercado local y se lavaron varias veces con agua destilada antes de su uso. Cloruro de calcio (CaCl 2 ), cloruro de manganeso (MnCl 2 ), cloruro cúprico (CuCl 2 ), cloruro de cobalto (CoCl 2 ), nitrato de plomo (Pb (NO 3 ) 2 ) y nitrato de cromo (Cr (NO 3 ) 3 ) se adquirieron en Aladdin Ltd. (Shanghai, China). Cloruro férrico (FeCl 3 ), cloruro ferroso (FeCl 2 ), cloruro de cadmio (CdCl 2 ), dicloruro de mercurio (HgCl 2 ), cloruro de sodio (NaCl) y cloruro de zinc (ZnCl 2 ) se obtuvieron de Sinopharm Chemical Reagent Co., Ltd. (Shanghai, China). Todos los productos químicos son de reactivo analítico (pureza> 99,0%) y se utilizan tal como se reciben sin purificación adicional.
Síntesis de NBD
En primer lugar, se lavaron 100 piezas de soja con una mezcla de alcohol y agua destilada durante 3 veces para eliminar la impureza. Luego, las semillas de soja se colocaron en un vaso de precipitados con 50 ml de agua destilada seguido de ultrasonidos durante 2 h. Durante este proceso, el color de la solución cambió de transparente a amarillo oscuro, lo que indica que la cáscara de la soja se adaptó a un tamaño nanométrico para formar NBD. Luego, la solución de color amarillo oscuro se transfirió a tubos de centrífuga y se centrifugó a 7000 rpm durante 3 minutos dos veces para eliminar las partículas de gran tamaño, después de eso, el sobrenadante se filtró a través de una membrana de 0,22 μM para eliminar más partículas grandes o aglomeradas. Posteriormente, la solución se colocó en un refrigerador seguido de un tratamiento congelado a - 5 ° C durante 6 h. Luego, se transfirió a un liofilizador a - 50 ° C durante 12 h para obtener los polvos. Los polvos congelados se dispersaron en agua para formar NBD para su posterior aplicación.
Caracterización
El patrón de difracción de rayos X (XRD) de los NBD se registró utilizando un difractómetro X 'Pert Pro, en el que los rayos X se generaron mediante una fuente de Cu-Kα. Se empleó un microscopio electrónico de transmisión (TEM) JEM-2010 para caracterizar el tamaño y la cristalinidad de los NBD. Los espectros de fluorescencia de los NBD se obtuvieron con un espectrofotómetro de fluorescencia F-7000. Los espectros de absorción de UV-Vis de los NBD se obtuvieron utilizando un espectrofotómetro UH4150. Los espectros de infrarrojos por transformada de Fourier (FTIR) de las muestras se registraron mediante un espectrómetro Thermo Scientific Nicolet iS10 FTIR. Los espectros de espectroscopía de fotoelectrones de rayos X (XPS) de las muestras se recogieron utilizando un espectrómetro Thermo Fisher Scientific ESCALAB 250Xi equipado con una fuente de radiación de rayos X Al-Kα.
Medición de rendimiento cuántico por fotoluminiscencia
El PL QY se probó utilizando un espectrofluorómetro F-9000 con esfera integradora. En primer lugar, la solución acuosa de NBD se diluyó hasta una intensidad de absorción por debajo de 0,1. Luego, esta solución acuosa se añadió a una cubeta de fluorescencia, se colocó en la esfera integradora y se excitó con luz monocromática de 370 nm. Los espectros de fluorescencia se recogieron en los rangos de 430 a 450 nm. Mientras tanto, también se registraron los mismos espectros de fluorescencia para agua pura en condiciones idénticas. Finalmente, el PL QY se calculó utilizando un software de fluorescencia basado en los espectros PL tanto de la muestra como del agua.
Prueba de toxicidad celular
La citotoxicidad de los NBD se evalúa mediante métodos MTT (3- (4,5) -dimetiltiahiazo (-z-y1) -3,5-di-fenitetra-zoliu-mromuro). Las células se cultivaron en RPMI-1640 normal con suero bovino fetal al 10% en CO 2 al 5% y 95% de aire a 37 ° C en una incubadora humidificada. Para las mediciones de la viabilidad celular, las células HeLa se colocaron en placas de 96 pocillos y luego se incubaron durante 72 h. Después de la incubación de células Hela con diversas concentraciones de NBD y CD durante 72 h, se registró la viabilidad celular.
Detección de Fe 3+
1 ml de solución con diferentes concentraciones de Fe 3+ se añadió a 1 ml de NBD con 3 g / l de solución antes de las mediciones de PL. Las soluciones se mezclaron a fondo y se dejaron reaccionar durante 1 min a temperatura ambiente, y luego se registraron los espectros de fluorescencia asociados. Las mediciones de PL se realizaron bajo excitación de 370 nm.
Resultados y discusión
Morfología y composición química
Los NBD se han preparado mediante métodos UES; todos los procesos se ilustran en el Esquema 1. Los tamaños y la morfología de los NBD se caracterizaron mediante microscopía electrónica de transmisión (TEM), como se muestra en la Fig. 1a y b. Las imágenes TEM muestran que los NBD tenían una forma casi esférica. Los diámetros de los NBD varían de 1 a 3 nm con un diámetro medio de 2,4 nm, y la distribución de tamaño correspondiente se enumera en la Fig. 1c. Las franjas de celosía de los NBD no se pueden observar a partir de la imagen TEM de alta resolución (recuadro de la Fig. 1b), lo que indica la naturaleza amorfa de los NBD. Las imágenes de microscopía electrónica de transmisión de barrido de campo oscuro anular de ángulo alto (HAADF-STEM) y el correspondiente mapeo elemental (carbono, nitrógeno y oxígeno) de los NBD se muestran en la figura 1d-g. Se puede ver que los elementos dominantes de los NBD son el carbono, el nitrógeno y el oxígeno. Además, el estado sólido 13 Las mediciones de resonancia magnética nuclear (RMN) C de los NBD se muestran en la Fig. 1h. Las señales varían entre 160 y 180 ppm, y los picos de 164 ppm y 170 ppm corresponden a enlaces C =O, que son indicativos de sp 2 átomos de carbono [25, 26].
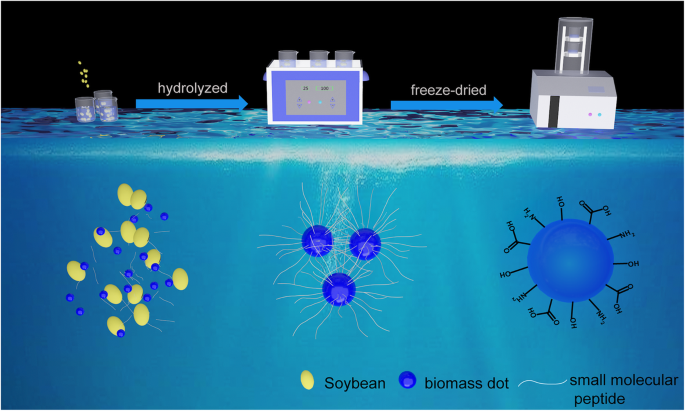
Ilustración esquemática del proceso de preparación de los NBD a partir de soja
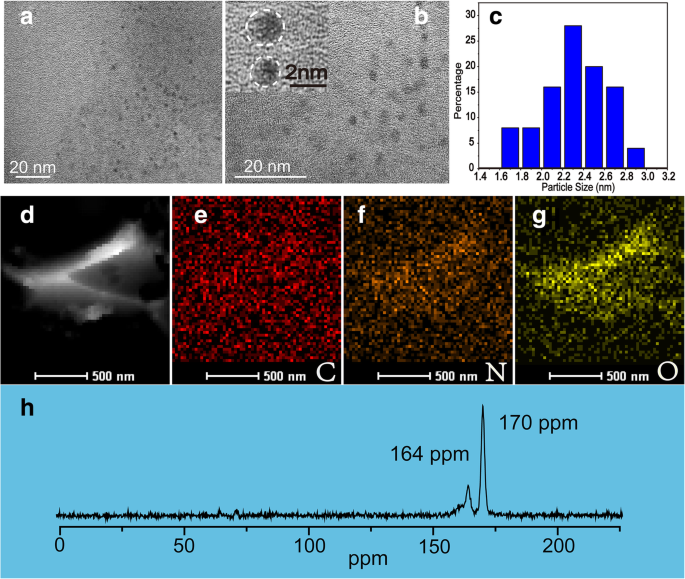
Imágenes TEM de los NBD ( a ) y ( b ). c La distribución del tamaño de partícula de los NBD. Imagen HAADF ( d ) y el correspondiente mapeo de distribución elemental de carbono ( e ), nitrógeno ( f ) y oxígeno ( g )
Para estudiar más a fondo las características estructurales de los NBD, se registró el patrón de difracción de rayos X (XRD). Como se muestra en la Fig. 2a, el patrón XRD típico muestra un pico ancho ubicado alrededor de 21,5 o y un pico de hombro alrededor de 41.0 o , que se puede atribuir a la fase de carbono amorfo [27]. Además, los picos de absorción característicos de la soja y los NBD se investigaron mediante espectroscopía de infrarrojos por transformada de Fourier (FTIR), como se muestra en la Fig. 2 (b). Las bandas de absorción alrededor de 3380 cm −1 se puede asignar a las vibraciones de estiramiento de O – H / –N – H, la banda alrededor de 2906 cm −1 a las vibraciones de estiramiento C – H, y la banda alrededor de 1650 cm −1 a las vibraciones de estiramiento C =O. Los picos a 1400 cm −1 y 1071 cm −1 corresponden a las vibraciones de flexión C – H y C – O, respectivamente [28]. Hay una diferencia obvia entre el espectro de la soja y los NBD de alrededor de 1750 cm −1 , que pertenece a las vibraciones de estiramiento de los enlaces C =O de los lípidos en la soja [29, 30]. Los lípidos insolubles en solución acuosa se separaron de la muestra cuando se remojaron en agua, lo que provocó la desaparición de los enlaces en el espectro FTIR de los NBD. Los enlaces C =O reducidos en la muestra provienen del grupo carboxilo en la proteína. El pico centrado a unos 1543 cm −1 También desapareció, lo que se puede atribuir a la proteólisis en el proceso de remojo de la soja. Al comparar todos los picos antes y después del proceso de ultrasonido, se puede observar la formación de grupos –OH, –C =O (amida I) y –NH en la superficie de los NBD [31]. Los resultados anteriores demuestran la existencia de grupos hidroxilo, amidógeno y carboxílico en la superficie de los NBD, y estos grupos funcionales juegan un papel importante en la hidrofilicidad y estabilidad de los NBD en solución acuosa. Se realizaron espectros de espectroscopía de fotoelectrones de rayos X (XPS) para dilucidar más los componentes de los NBD, como se muestra en la Fig. 2c. El espectro XPS muestra tres picos fuertes a 532.0, 401.1 y 286.1 eV, que pueden atribuirse a O 1s, N 1s (Fig. 2d) y C 1s (Fig. 2e), respectivamente [32]. Estos resultados indican que los NBD contienen principalmente C (64,33%), O (32,34%) y N (2,72%), así como una cantidad limitada de P, y el elemento P puede provenir del fosfolípido de la soja [33]. . En el espectro XPS de alta resolución, el espectro C 1s muestra tres picos a 287,6, 285,8 y 284,6 eV, que se pueden asignar a C =O, C – O / C – N y C – C / C =C grupos, como se muestra en la Fig. 2c. El enlace C =O es de los grupos carboxilo solubles [24]. El C – O / C =N y C – C / C =C son de los carbonos nitrosos y sp 2 / sp 3 carbonos, respectivamente [34]. El espectro de N 1s que se muestra en la Fig. 2d confirma dos bandas principales a 399,5 eV y 401,6 eV, revelando la existencia de N piridínico y N pirrólico, lo cual es consistente con el análisis FTIR. El espectro de O 1s presentado en la Fig. 2f tiene dos picos a 531,4 eV y 533,0 eV, que se pueden atribuir a los grupos C – OH / C – O – C y C =O, respectivamente [9].
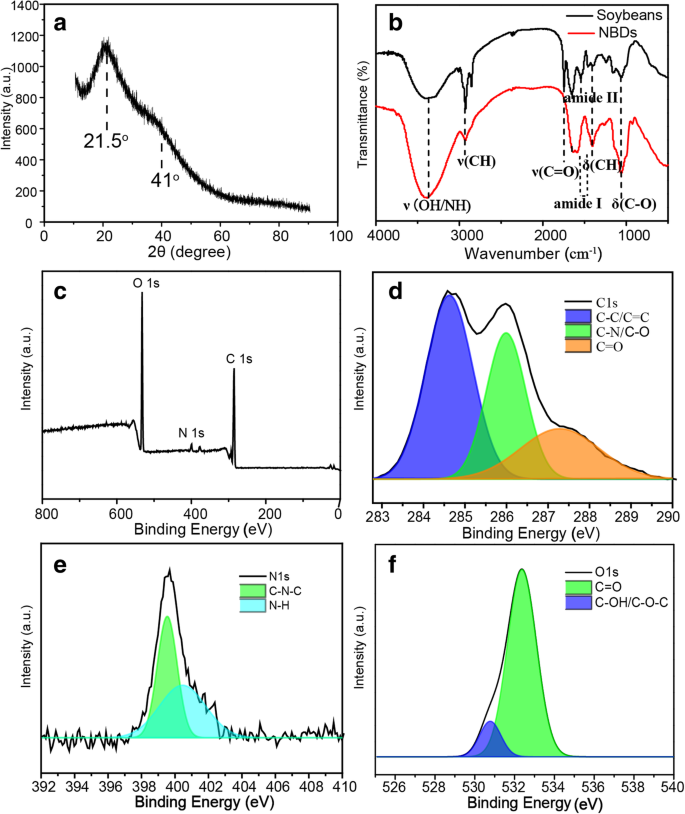
un Patrón XRD de los NBD. b Espectros FTIR de la soja y NBD. c Espectro de encuestas XPS de los NBD. Espectros XPS de alta resolución de C 1s ( d ), N 1s ( e ) y O 1s ( f )
Se propuso un posible mecanismo para la formación de NBD a partir de la soja con base en el análisis anterior. Primero, algunas partículas grandes de biomasa suspendidas en la solución se rompen en tamaño nanométrico por la conmoción cerebral ultrasónica. Los cambios en la solución antes y después del tratamiento de extracción ultrasónica se muestran en el archivo adicional 1:Figura S1. Luego, la proteína en las semillas de soja se hidrolizó a péptidos y aminoácidos de moléculas pequeñas en el proceso anterior, y muchas cadenas de péptidos de moléculas pequeñas se unen a la biomasa de tamaño nanométrico para formar puntos de biomasa altamente funcionalizados en la superficie. Los grupos funcionales en la superficie de los puntos de biomasa son los principales contribuyentes a la fluorescencia. De acuerdo con el mecanismo, el frijol mungo también se utilizó como precursores y también se obtuvieron NBD fluorescentes azules, como se muestra en el archivo adicional 1:Figura S2.
Propiedades ópticas
Los NBD muestran propiedades fluorescentes dependientes de la excitación, y cuando la longitud de onda de excitación varía de 320 a 520 nm, el pico de emisión se desplaza al rojo gradualmente, lo que indica que la emisión de los NBD se puede sintonizar cambiando la longitud de onda de excitación, como se muestra en la Fig. 3a. La solución acuosa de NBD es transparente bajo iluminación interior y muestra fluorescencia azul bajo iluminación UV, como se muestra en el recuadro de la Fig. 3b. El espectro de excitación por fotoluminiscencia (PLE) de los NBD se muestra en el archivo adicional 1:Figura S3, y la longitud de onda de excitación óptica está en el rango de 360 a 420 nm. Para explorar el origen PL de los NBD, se han registrado los espectros de absorción UV-Vis de los NBD con diferentes concentraciones a temperatura ambiente (la concentración de NBD de abajo hacia arriba es 0.03, 0.06, 0.13, 0.25, 0.25, 0.50, 0.50 , 0,75, 1,00 y 1,50 g / l), como se muestra en la Fig. 3b. Los espectros de absorción UV-Vis de los NBD exhiben dos picos de absorción claros a 270 nm y 330 nm, respectivamente. El primero se puede atribuir al π-π * transición de enlaces C – C / C =C, mientras que el último al n-π * transición de enlaces C =O / N [35, 36]. Estos grupos funcionales son los principales grupos cromogénicos que contribuyen a la fluorescencia de los NBD [37, 38]. Los espectros PL de la soja durante la extracción ultrasónica se muestran en el archivo adicional 1:Figura S4, y la intensidad PL aumenta con el tiempo y luego alcanza el máximo. La Figura 3c muestra los espectros PL de los NBD medidos de 80 a 300 K. Los NBD exhiben un comportamiento típico de extinción térmica, en el que todos los picos disminuyen monótonamente en intensidad al aumentar la temperatura. Este comportamiento de PL se puede atribuir al aumento de la recombinación no radiativa y la reducción de la recombinación de la radiación con el aumento de las temperaturas [39, 40]. Para evaluar la estabilidad de los NBD, se han caracterizado la fotoestabilidad y la termoestabilidad de los NBD, como se muestra en la Fig. 3d. Para la fotoestabilidad, la imagen de configuración de medición se muestra en el archivo adicional 1:Figura S5. Los valores de intensidad de fluorescencia se muestran en el archivo adicional 1:Figura S6 y S7. La intensidad de emisión de los NBD permanece por encima del 90% bajo la iluminación de la lámpara UV durante 6 h, lo que indica su buena fotoestabilidad. Para la termoestabilidad, las intensidades de fluorescencia de los NBD disminuyen poco cuando la temperatura varía de 20 a 80 ° C, revelando su alta estabilidad térmica.
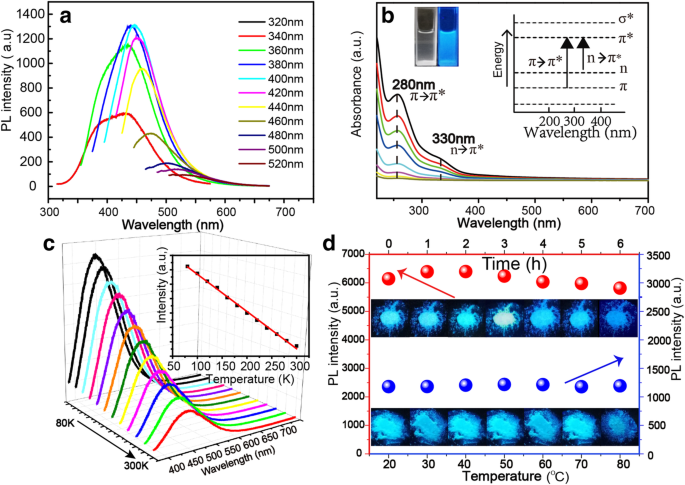
un Los espectros de fluorescencia de los NBD con cambios de longitud de onda de excitación de 320 a 520 nm. b Espectros de absorción UV-Vis de los NBD. c Espectros de fluorescencia de los NBD a diferentes temperaturas, el recuadro es el gráfico de la intensidad de fluorescencia de los NBD en función de la temperatura. d Intensidad de fluorescencia e imágenes de los polvos NBD bajo la iluminación de una lámpara de 365 nm de diferente duración y las de los polvos NBD a diferentes temperaturas de medición
Evaluación de citotoxicidad
Los ensayos MTT se utilizaron para evaluar la citotoxicidad de los NBD. Las viabilidades de las células HeLa incubadas con los NBD y otros dos tipos de CD sintetizados mediante el método hidrotermal, como se muestra en la figura 4. Como se indica en la figura, las viabilidades celulares disminuyen poco cuando se introduce la solución de NBD incluso cuando la concentración de la Los NBD alcanzan los 800 μg / ml. La tasa de supervivencia celular fue del 70% y del 67% cuando las células HeLa se incubaron con los otros dos tipos de CD a una concentración de 800 μg / ml. Obviamente, los NBD exhiben una biocompatibilidad superior que los CD preparados a partir de reactivos químicos.
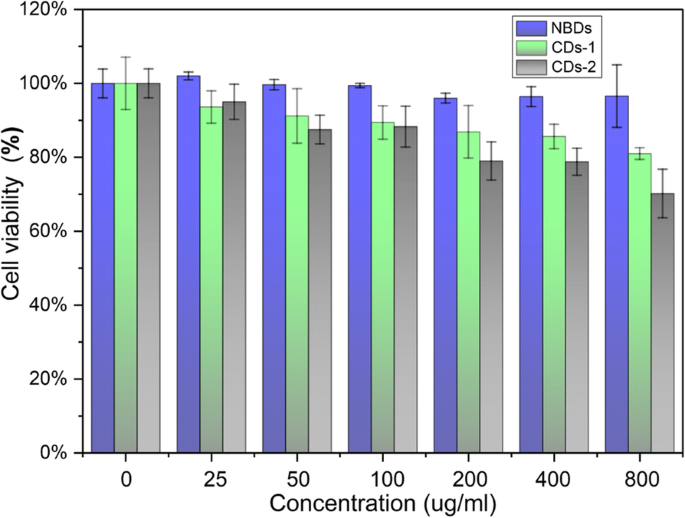
Viabilidad de las células HeLa después de 72 h de incubación con diferentes concentraciones de NBD y CD
Propiedades de detección de los NBD hacia Fe 3+
Curiosamente, la fluorescencia de los NBD se puede apagar eficazmente con Fe 3+ , como se muestra en la Fig. 5a, y la intensidad PL de los NBD disminuye significativamente con el aumento de Fe 3+ concentración. Además, se puede trazar una buena relación lineal entre F 0 / F y Fe 3+ concentración que varía de 0 a 30 μM ( R 2 =0,99), donde F 0 y F eran la intensidad PL de los NBD a ex / em de 370/445 nm en ausencia y presencia de Fe 3+ , como se muestra en la Fig. 5b. La eficiencia de enfriamiento fue ajustada por Stern-Volmer Eq:
$$ \ frac {{\ mathrm {F}} _ 0} {\ mathrm {F}} =1+ {K} _ {\ mathrm {SV}} \ left [Q \ right] $$ (1)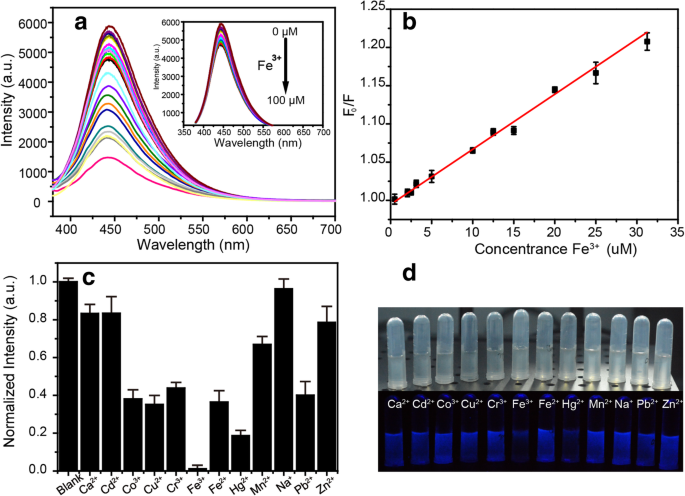
un Espectros PL de los NBD en presencia de diferentes concentraciones de Fe 3 + . b Curva de calibración del sensor en función de Fe 3 + concentración. c Intensidades de fluorescencia de los NBD en presencia de diferentes iones. d Imágenes fotográficas de la solución NBDs con diferentes iones metálicos bajo iluminación interior y UV
donde K sv es la constante de extinción de Stern-Volmer y [ Q ] es el Fe 3+ concentración. La ecuación de regresión lineal es Y =0,0072 X + 0,99479, R 2 =0,99. El límite de detección (LOD) del sensor propuesto se determinó como 2,9 μM, que es más bajo que el nivel máximo permitido de Fe 3+ (5,37 μM) en agua potable creada por la Agencia de Protección Ambiental de los Estados Unidos (USEPA) [24]. La selectividad es otro parámetro crítico para los sensores químicos. Por lo tanto, se ha investigado la respuesta de fluorescencia del sensor hacia varios iones metálicos interferentes, incluido el Ca 2+ , Cd 2+ , Co 2+ , Cu 2+ , Cr 3+ , Fe 3+ , Fe 2+ , Hg 2+ , Mn 2+ , Na + , Pb 2+ y Zn 2+ . Iones metálicos cada uno a una concentración de 10 −2 Se añadieron M a 1 ml de solución de NBD con una concentración de 3 g / l. En la Fig. 5c, se puede ver que la intensidad de fluorescencia de los NBD responde de manera más sensible al Fe 3+ que otros iones metálicos. Las fotografías de la Fig. 5d son las imágenes de los NBD con varios iones bajo iluminación interior y ultravioleta, y la concentración de iones metálicos fue de 100 µM. Obviamente, los NBD se apagan en presencia de Fe 3+ , lo que indica que se pueden utilizar para la detección visual.
Mecanismo de extinción
El mecanismo de extinción de los NBD en presencia de Fe 3+ se discutió sobre la base de los espectros de absorción UV-Vis y la vida útil de la fluorescencia de los NBD. A partir de los espectros de absorción UV-Vis que se muestran en el archivo adicional 1:Figura S8, no hay cambios en los picos de absorción a 270 nm y 340 nm con la introducción de Fe 3+ , lo que indica que el Fe 3+ no influye en la estructura de los NBD [41]. Además del espectro de absorción UV-Vis, el efecto de Fe 3+ sobre la vida útil del NBD también se estudió. En la Fig. 6a, la vida útil de la fluorescencia se acorta después de la adición de Fe 3+ , que puede implicar la transferencia parcial de electrones de los NBD al d orbital de Fe 3+ , disminuyen así la recombinación radiativa de los NBD [42]. El mecanismo de extinción de la fluorescencia de los NBD causados por Fe 3+ se muestra en la Fig. 6b. El sensible efecto de extinción de la fluorescencia de los NBD en presencia de Fe 3+ puede originarse de la fuerte interacción entre Fe 3+ y los grupos de superficie de los NBD. Fe 3+ tiene una afinidad de unión más fuerte y una cinética de quelación más rápida con grupos amino y carboxílicos en las superficies de los NBD. La coordinación especial entre Fe 3+ Los iones y los grupos hidroxilo / amina fenólicos de los NBD se han utilizado ampliamente para la detección de Fe 3+ iones o reacciones coloreadas en la química orgánica tradicional [43, 44]. Además, los potenciales redox de Fe 3+ / Fe 2+ ( Ф =0,77) se encuentran entre el orbital molecular desocupado más bajo (LUMO) y el orbital molecular ocupado más alto (HOMO) de los NBD, lo que provoca una transferencia de electrones fotoinducida de LUMO a los estados complejos de Fe 3+ [45]. Estos resultados demuestran que los NBD son muy sensibles al Fe 3+ sobre los otros iones metálicos.
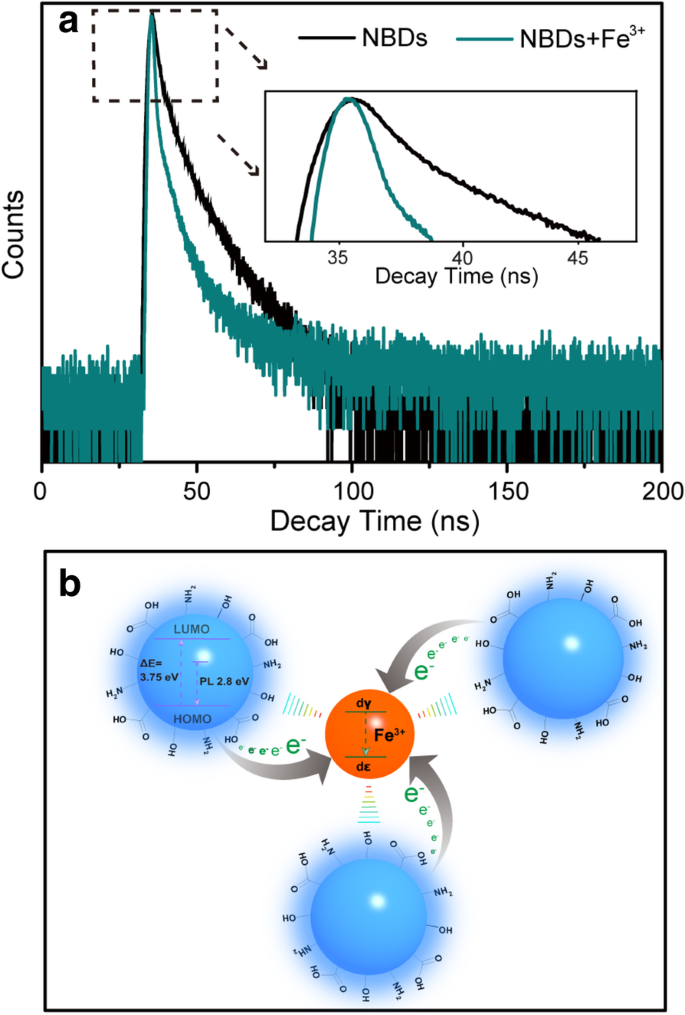
un Rastros de desintegración de fluorescencia de las ENT en ausencia y presencia de Fe 3 + bajo excitación a 370 nm y emisión a 445 nm. b Ilustración esquemática del posible mecanismo de extinción de la fluorescencia de los NBD en presencia de Fe 3 + iones
Conclusión
En resumen, los NBD luminiscentes se han preparado a partir de soja mediante un enfoque UES sin calentamiento. Los NBD muestran una fluorescencia azul brillante con PL QY del 16,7% y, beneficiándose de la biomasa comestible y el proceso de síntesis sin calentamiento, la viabilidad celular se mantiene al 100% incluso si la concentración de los NBD alcanza los 800 μg / ml. Además, la fluorescencia de los NBD muestra una sensibilidad específica al Fe 3+ , y el LOD puede alcanzar 2,9 μM. La baja toxicidad y el alto límite de detección indican que se espera que los NBD encuentren aplicaciones potenciales en sistemas biológicos y ambientales.
Abreviaturas
- FTIR:
-
Infrarrojos por transformada de Fourier
- HAADF-STEM:
-
Microscopía electrónica de transmisión de barrido de campo oscuro anular de alto ángulo
- LOD:
-
Límite de detección
- NBD:
-
Puntos de nano-biomasa
- RMN:
-
Resonancia magnética nuclear
- PL:
-
Fotoluminiscencia
- QD:
-
Puntos cuánticos
- QY:
-
Rendimiento cuántico
- TEM:
-
Microscopía electrónica de transmisión
- UES:
-
Estrategia de extracción ultrasónica
- USEPA:
-
Agencia de Protección Ambiental de Estados Unidos
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X
Nanomateriales
- Demostración de un biosensor flexible basado en grafeno para la detección rápida y sensible de células de cáncer de ovario
- Nanopartículas de oro multifuncionales para aplicaciones terapéuticas y diagnósticas mejoradas:una revisión
- Avances y desafíos de los nanomateriales fluorescentes para síntesis y aplicaciones biomédicas
- N, N-dimetilformamida reguladora de la fluorescencia de los puntos cuánticos de MXene para la determinación sensible de Fe3 +
- Síntesis de puntos cuánticos de tipo II / tipo I de ZnSe / CdS / ZnS con supresión de reabsorción y su aplicación para el ensayo inmunoabsorbente
- Un enfoque simple para sintetizar puntos cuánticos de carbono fluorescente de aguas residuales de tofu
- Síntesis de puntos cuánticos de sulfuro de antimonio solubles en agua y sus propiedades fotoeléctricas
- Una sonda fluorescente reanudable BHN-Fe3O4 @ SiO2 Nanoestructura híbrida para Fe3 + y su aplicación en bioimagen
- Síntesis fácil y respetuosa con el medio ambiente de nanocables de Co3O4 y su prometedora aplicación con grafeno en baterías de iones de litio
- Síntesis y caracterización de BiOCl modificado y su aplicación en la adsorción de tintes de baja concentración a partir de una solución acuosa
- Razones de la deformación de PCB y sus medidas preventivas



