Una microfibra de carbono dopada con nitrógeno altamente nanoporosa derivada de Bioresource como un nuevo tipo de electrocatalizador ORR
Resumen
La síntesis de electrocatalizadores a base de carbono sin metales para la reacción de reducción de oxígeno (ORR) para reemplazar los catalizadores convencionales a base de platino se ha convertido actualmente en un tema candente de investigación. Este trabajo propone una estrategia de carbonización asistida por activación para la fabricación de microfibras de carbono nanoporosas dopadas con nitrógeno (Me-CFZ-900) con una superficie BET alta (~ 929,4 m 2 g −1 ) mediante el uso de melamina como promotor / fuente de nitrógeno y residuos biológicos de carbono-bambú como fuente de carbono con la ayuda de un activador de cloruro de zinc. Las pruebas electroquímicas mostraron que el material Me-CFZ-900 ha exhibido una excelente actividad electrocatalítica de ORR y estabilidad a largo plazo, y también mostró una vía de ORR de casi cuatro electrones en un electrolito alcalino. También encontramos que el grafítico-N puede ser el sitio catalíticamente activo para la ORR, pero la formación de planar-N puede ayudar aún más a promover la actividad de la ORR para nuestros catalizadores. Los resultados abren un nuevo espacio y proporcionan una nueva idea para preparar valiosos materiales nanocarbonados porosos a partir de desechos sólidos carbonosos para la catálisis de una amplia gama de reacciones electroquímicas en el futuro.
Antecedentes
Los sistemas avanzados de energía electroquímica, como las pilas de combustible y las baterías de metal-aire, se consideran alternativas prometedoras para los combustibles fósiles tradicionales [1, 2]. La reacción de reducción de oxígeno (ORR) es una reacción importante en esas tecnologías energéticas, pero adolece de varias deficiencias, como un alto potencial excesivo, una cinética de ORR lenta y una diversidad de vías, lo que limita la mejora del rendimiento general y la eficiencia de conversión [3, 4 ]. En la actualidad, los catalizadores basados en Pt se han empleado ampliamente para mejorar la ORR en aplicaciones prácticas, pero el alto costo y los recursos restringidos de metal-Pt obstaculizan la comercialización [5, 6, 7]. Por lo tanto, la exploración de catalizadores de ORR libres de Pt baratos, activos y estables es importante para desarrollar rápidamente tecnologías de energía limpia.
Para buscar algunos sustitutos valiosos para los catalizadores de metal-Pt, se estudia popularmente el dopado de heteroátomos en alótropos de carbono como el grafeno [8], el grafeno [9] y el nanotubo de carbono [10] debido a sus estructuras físicas y electrónicas distintivas. Aunque se ha llevado a cabo una inmensa mejora en la fabricación controlada de los catalizadores de carbono dopado, el origen de la actividad catalítica de ORR aún no está claro, lo que se convierte en un cuello de botella técnico en este campo [11, 12]. Comúnmente, la mejora de la actividad de ORR de los catalizadores de carbono dopado se puede atribuir a la modulación de carga y la electroneutralidad rota causada por el dopaje de heteroátomos en el marco de carbono [13, 14]. Otras investigaciones también demostraron que la actividad de ORR de los catalizadores basados en carbono se origina en la ubicación y configuración adecuadas del dopaje [15, 16, 17]. Además, el dopaje de heteroátomos como el nitrógeno puede inducir la polarización de la superficie del carbono, lo que ayuda a formar nuevos sitios activos que contienen nitrógeno, favoreciendo así la adsorción de átomos e iones [18]. Por lo tanto, comprender la contribución de las estructuras de carbono ricas en N es importante para aclarar los sitios catalíticamente activos de ORR, lo que también puede allanar el camino para el diseño direccional de catalizadores de carbono dopado estables y activos de ORR.
El uso de biomasa natural (p. Ej., Soja [19], fibroína de seda [20], frijol [21] y hemoglobina [22]) y desechos biológicos animales (p. Ej., Escamas de pescado [23] y sangre animal [24]) como Se pensó que un precursor directo o la fuente de nitrógeno de los sitios activos de ORR catalíticamente era una vía eficaz para fabricar los catalizadores de carbono dopado. Más recientemente, Li et al. también sintetizó un catalizador de ORR dopado a base de carbono con una red porosa tridimensional mediante el uso de biomaterial de hemina como precursor de una sola fuente y el uso de cristales de cloruro de sodio autoensamblados como plantilla [25]. Jiang y col. [26] convirtió la enzima biológica de los centros sanguíneos en Fe – N x Sitios catalíticamente activos para electrocatálisis de ORR mediante la pirólisis de múltiples pasos de desechos biológicos de sangre. El electrocatalizador resultante muestra una actividad catalítica ORR superior, lo que indica que el Fe – N x La estructura del hemo en las células sanguíneas es beneficiosa en la formación de centros activos de ORR y, por lo tanto, puede promover el rendimiento de los catalizadores. Estos estudios pueden ser una aspiración de que se pueda preparar un nuevo tipo de catalizadores de carbono dopado de alto rendimiento controlando adecuadamente los procesos de pirólisis y eligiendo materiales de biomasa económicos como precursores.
Aquí, inspirados por el carbono dopado con heteroátomos derivado de residuos biológicos barato y fácilmente disponible para un rendimiento superior de ORR, desarrollamos una estrategia para sintetizar una microfibra de carbono nanoporoso dopada con N como un nuevo tipo de electrocatalizador de ORR (Me-CFZ-900) mediante pirólisis de tejidos de bambú-carbono desperdiciados con la activación de cloruro de zinc, combinada con el uso de melamina como promotora / fuente de nitrógeno. Hasta donde sabemos, no existen informes sobre el diseño de microfibras de carbono porosas como catalizador de ORR a través de la conversión fácil de residuos biológicos de bambú-carbono hasta ahora. Descubrimos que el catalizador Me-CFZ-900 preparado tiene una gran cantidad de mesoporos uniformes con un diámetro de poro promedio de 2.23 nm y un área de superficie alta (~ 929.4 m 2 g −1 ), que puede ser beneficioso para el transporte masivo de O 2 reducción electrocatalítica. Este estudio abre un nuevo espacio y proporciona una nueva idea para preparar valiosos materiales nanocarbonados porosos, que pueden funcionar como electrocatalizadores ORR prometedores al mejorar aún más las características de los poros y el contenido de especies de N activas.
Métodos
Síntesis de catalizadores ORR basados en carbono
Las microfibras de carbono nanoporosas dopadas con nitrógeno se prepararon mediante una pirólisis simple y fácil de dos pasos de tejidos de bambú y carbono desperdiciados (adquiridos de Fujian Hengan Group Co. Ltd., China) con la ayuda de la activación de cloruro de zinc. Por lo general, los tejidos desechados se trituraron en un despulpador y luego se carbonizaron a 350 ° C durante 1 h en un horno de tubo con una velocidad de calentamiento de 20 ° C min −1 bajo atmósfera de nitrógeno para eliminar algunas sustancias orgánicas residuales. Las microfibras de carbono obtenidas se etiquetan como CF350. Posteriormente, se mezclaron uniformemente 0,5 g de CF350, 1,0 g de melamina y 1,0 g de cloruro de zinc mediante una simple trituración en estado sólido durante 0,5 h en un mortero de ágata para obtener un nuevo precursor carbonoso (Me-CFZ). El precursor Me-CFZ se sometió a un tratamiento térmico adicional en un horno tubular a 900 ° C durante 2 h con una velocidad de calentamiento de 10 ° C min −1 debajo de N 2 atmósfera, dando como resultado una síntesis exitosa de Me-CFZ-900. La ilustración esquemática para la síntesis de Me-CFZ-900 mediante un método de carbonización asistida por activación se indica en la Fig. 1. Para comprobar el efecto de las temperaturas de pirólisis en el rendimiento de ORR de los catalizadores a base de carbono, también fabricamos otros Me-CFZ catalizadores a diferentes temperaturas, que se pueden marcar como Me-CFZ-700, Me-CFZ-800 y Me-CFZ-1000, respectivamente. Como control, se prepararon de manera similar CF-900 y CFZ-900 sin la adición de melamina. Todas las muestras se trataron adicionalmente sumergiéndolas en 0,5 mol l −1 Solución de HCl durante 2 h antes de que puedan usarse como electrocatalizador ORR. Para asegurar la reproducibilidad, preparamos todos los catalizadores ORR tres veces y sus errores se pueden controlar en el rango de 5.0%.

La ilustración esquemática para la síntesis de microfibras de carbono mesoporosas dopadas con nitrógeno para electrocatálisis de ORR mediante la carbonización asistida por activación de desechos biológicos de carbón de bambú
Caracterización física
Las pruebas de microscopía electrónica de barrido de alta resolución (SEM) y microscopía electrónica de transmisión (TEM) fueron adquiridas por Hitachi UHR S4800 (Japón) y el instrumento FEI Tecnai-G2 F30 con un voltaje de aceleración de 300 kV, respectivamente. La espectroscopia de fotoelectrones de rayos X (XPS) se realizó usando un espectrómetro Kratos XSAM800. Se aplicó un Micromeritics Analyzer (ASAP 2010) para probar N 2 -isotermas de adsorción / desorción a 77 K. El análisis de difracción de rayos X (XRD) se llevó a cabo utilizando un difractómetro de rayos X Shimadzu XRD-6000 (Japón) con Cu Ka 1 radiación ( λ =1,54178 Ǻ) a 4 ° min
- 1
. Los datos de espectroscopía Raman se registraron con el sistema Raman Horiba HR800 con una longitud de onda de excitación láser de 514,5 nm. La radiografía XR se realizó con un Shimadzu XRD-6000 ( λ =Difractómetro de rayos X (Japón) con Cu Ka 1 radiación  ).
).
Mediciones electroquímicas
El comportamiento electrocatalítico del catalizador ORR a base de carbono se evaluó en un bipotenciostato CHI760E (Shanghai Chenhua Instruments Co. Ltd., China). Un electrodo de disco de anillo de rotación de vidrio-carbono (GC-RRDE, Φ =5 mm, Pine Instrument Co.), un electrodo de calomelanos saturado (SCE) y una varilla de grafito ( Φ =0,5 cm) se utilizaron como electrodo de trabajo (WE), electrodo de referencia (RE) y electrodo auxiliar (AE), respectivamente. La fabricación de WE se refiere a nuestros informes anteriores [12]. Generalmente, 10 μl de 10 mg ml −1 La dispersión se pipeteó sobre la superficie de GC-RRDE y se secó naturalmente al aire. La carga de masa de catalizadores a base de carbono y catalizador comercial de Pt / C (20% en peso de Pt, Aladdin Industrial Co. Ltd.) se controló para que fuera ~ 600 μg cm −2 . Todos los potenciales (frente a SCE) se transformaron en potenciales frente al electrodo de hidrógeno reversible (RHE). Además, los espectros de impedancia electroquímica (EIS) se obtuvieron en presencia de 1 mmol l −1 K 3 [Fe (CN) 6 ] / K 4 [Fe (CN) 6 ] (relación molar =1:1) mezcla como una sonda redox en una solución de KCl 0,1 M. Para inducir suficientemente la descomposición completa del peróxido producida durante la prueba, el potencial del anillo se fijó en 0,5 V (frente a SCE) como se indica en otra parte. El% HO 2 - rendimiento y número de transferencia de electrones ( n ) durante la ORR se calcularon utilizando las siguientes ecuaciones [25]:
$$ \% {HO} _2 ^ {-} =100 \ times \ frac {2 {I} _ {\ mathrm {r}} / N} {I _ {\ mathrm {d}} + \ left ({I} _ {\ mathrm {r}} / N \ right)} $$ (1) $$ n =4 \ times \ frac {I _ {\ mathrm {d}}} {I _ {\ mathrm {d}} + {I } _ {\ mathrm {r}} / N} $$ (2)donde yo d es la corriente faradaica en el disco, I r es la corriente faradaica en el anillo, y N es la eficiencia de recolección del electrodo de anillo (0.38). n se calculó a partir de la ecuación de Koutecky-Levich [27]:
$$ 1 / {j} _d =1 / {j} _k + 1 / B {\ omega} ^ {1/2} $$ (3) $$ B =0.62 {nFC} _ {\ mathrm {O}} {D} _ {\ mathrm {O}} ^ {2/3} {\ nu} ^ {- 1/6} {\ omega} ^ {1/2} $$ (4)donde F es la constante de Faraday, C O es el O 2 concentración de saturación en el electrolito, D O es el O 2 coeficiente de difusión en el electrolito, ν es la viscosidad cinética del electrolito y ω es la velocidad de rotación del electrodo, y 0,62 es una constante cuando la velocidad de rotación se expresa en rpm.
Resultados y discusión
La Figura 2 muestra las imágenes SEM y TEM del catalizador Me-CFZ-900. Como se observa en estas imágenes SEM, el catalizador Me-CFZ-900 consta de microfibras de carbono irregulares dopadas con nitrógeno (Fig. 2a, b). Además, las imágenes TEM de Me-CFZ-900 (Fig. 2c, d) confirman aún más los resultados del análisis SEM. La formación de mesoporos dentro del catalizador Me-CFZ-900 se atribuye al papel de la activación del cloruro de zinc durante la pirólisis a alta temperatura que induce la deshidratación rápida y la deshidroxilación catalítica, lo que resulta en la liberación de hidrógeno y oxígeno en forma de H 2 O vapor. Este proceso de activación puede facilitar la producción de más mesoporos durante el proceso de dopaje con nitrógeno dentro del catalizador Me-CFZ-900. Además, también se pueden observar algunos defectos de los bordes expuestos gracias al dopaje N, que es beneficioso para promover la actividad catalítica de ORR.

El SEM ( a , b ) y TEM ( c , d ) imágenes de Me-CFZ-900
Se utilizaron isotermas de adsorción / desorción de nitrógeno para examinar el área de superficie específica de Brunauer-Emmett-Teller (BET) y las características de distribución de poros, como se muestra en la Fig. 3a y el archivo adicional 1:Figura S1. Se encuentra que un área de superficie BET alta (~ 929,4 m 2 g −1 ) de Me-CFZ-900 se puede atribuir a su superficie rugosa rica en defectos y características mesoporosas, que concuerda bien con los resultados de las mediciones de TEM. La distribución de tamaño de poro de BJH del catalizador Me-CFZ-900 se indica en el recuadro de la Fig. 3a. El volumen de poro total de Me-CFZ-900 con un diámetro de poro promedio de 2,3 nm es ~ 0,53 cm 3 g −1 , pero los mesoporos se centran principalmente en el diámetro de poro de 3,88 nm. Estas excelentes características pueden estar estrechamente relacionadas con la mejora de la actividad de la ORR. Las estructuras de carbono de diferentes catalizadores ORR basados en carbono se investigaron mediante patrones de difracción de rayos X en la Fig. 3b. No se pueden observar picos cristalinos, excepto por dos planos de carbono ((002) y (101)) ubicados en ~ 24 ° y ~ 43 ° respectivamente, lo que sugiere la estructura de carbono amorfo [19, 20]. El pico de difracción fuerte (002) puede atribuirse principalmente a los planos de la red de un carbono turboestrático típico [28]. Sin embargo, un pico 2-theta más alto de (002) y un pico 2-theta más bajo de (101) para Me-CFZ-900 en comparación con los de CF-900 y CFZ-900 pueden obtenerse debido a la ligera distorsión en el cristalino. regularidad a lo largo de la a o b dirección por el dopaje de átomos de nitrógeno en el sp 2 celosía de carbono. Además, todos los espectros Raman de CF-900, CFZ-900 y Me-CFZ-900 (Fig. 3c) han exhibido dos bandas de placa, ubicadas en ~ 1345 y ~ 1590 cm −1 , que se asignan a la sp 3 desordenada carbono (banda D) y grafito sp 2 carbono (banda G), respectivamente. La relación de intensidad ( I D / Yo G ) de la banda "D" a la banda "G" se utilizó para caracterizar los grados desordenados y grafíticos. El I correspondiente D / Yo G para CF-900, CFZ-900 y Me-CFZ-900 son aproximadamente 0,91, 0,91 y 0,92, respectivamente. Un I superior D / Yo G La proporción de Me-CFZ-900 representa una mayor eficiencia de dopaje con nitrógeno y una estructura más defectuosa, lo que facilita el aumento de la densidad del sitio activo y mejora la actividad electrocatalítica de ORR. El informe anterior también propuso que la conductividad eléctrica de los catalizadores de carbono dopado se puede mejorar mediante el dopado de más átomos de nitrógeno [25]. Por esta razón, probamos aún más la conductividad eléctrica (CE) de todos los catalizadores de carbono dopado mediante espectroscopia de impedancia electroquímica (EIS) en 1 mmol l −1 K 3 [Fe (CN) 6 ] / K 4 [Fe (CN) 6 ] (relación molar =1:1) solución de sonda, como se muestra en la Fig. 3d. Los resultados de Bode demuestran que Me-CFZ-900 ofrece una resistencia mucho menor para el transporte masivo, lo que sugiere una mejor conductividad general en comparación con CF-900 y CFZ-900. Además, una conductividad eléctrica más alta de Me-CFZ-900 puede ayudar a promover la capacidad de transporte de electrones, lo que resulta en una mejor actividad de ORR en medio alcalino.
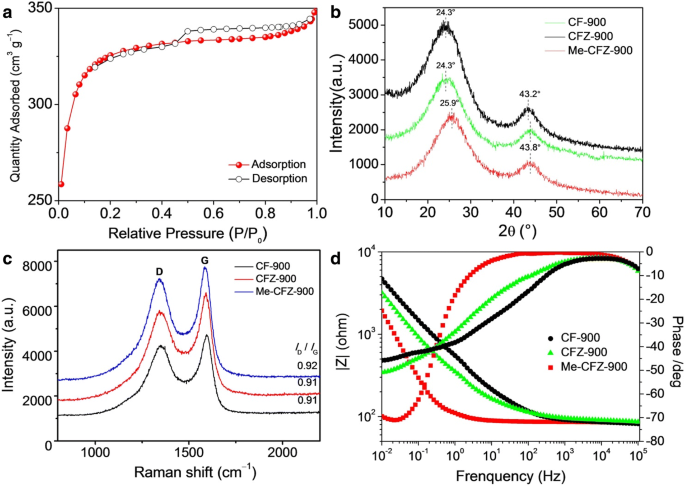
un N 2 -isotermas de absorción de Me-CFZ-900. b Patrones XRD de CF-900, CFZ-900 y Me-CFZ-900. c Espectros Raman de CF-900, CFZ-900 y Me-CFZ-900. d Espectros de Bode de CF-900, CFZ-900 y Me-CFZ-900 bajo una onda sinusoidal de 5.0 mV de amplitud en el rango de frecuencia de 100 kHz a 10 MHz
Los datos de la encuesta XPS (consulte el archivo adicional 1:Figura S2) indican que Me-CFZ-900 se compone principalmente de nitrógeno, carbono y oxígeno, respectivamente. La aparición del pico XPS de N1s sugiere el dopaje exitoso del nitrógeno en la estructura del carbono, lo cual se prueba adecuadamente mediante el análisis del pico C1s de Me-CFZ-900. Sin embargo, el pico N1 de CF-900 y CFZ-900 no se puede observar debido al bajo contenido de nitrógeno dentro de los desechos biológicos de bambú y carbono, como se muestra en el archivo adicional 1:Figura S1 y Tabla S1. Además, el contenido de N total de tres catalizadores de N dopado se determinó mediante análisis XPS de superficie. El contenido total de N de Me-CFZ-900 es 2,71 at.%, Pero el contenido total de N es sólo 0,91 at.% Para CF-900 y 0,94 at.% Para CFZ-900, respectivamente. Además, verificamos los espectros XPS de N1s de alta resolución de CF-900, CFZ-900 y Me-CFZ-900, como se muestra en la Fig. 4 (a – c). Los espectros XPS de N1s de CF-900 y CFZ-900 se pueden deconvolucionar en un pico con una energía de enlace (BE) de ~ 401,5 eV, correspondiente a las especies de N grafítico. Sin embargo, el espectro XPS de N1s de alta resolución de Me-CFZ-900 indica la existencia de cuatro tipos de grupos de nitrógeno:N piridínico a 398,3 eV, N pirrólico a 398,8 eV, N grafítico a 401,2 eV y N oxidado a 403,4 eV [29,30,31]. La formación de N piridínico y N pirrólico se deriva de la descomposición térmica de la melamina durante el proceso de activación-carbonización a altas temperaturas. Además, los espectros C1s de alta resolución (Fig. 4d y archivo adicional 1:Figura S3) de CF-900, CFZ-900 y Me-CFZ-900 se pueden deconvolucionar en cuatro picos a 284.5, 285.9, 287.0 y 293.0 eV, que se asignan a graphitic sp 2 carbono (C =C), carbono amorfo (C – C), sp 2 átomos de carbono unidos al nitrógeno (C – N) y sp 2 átomos de carbono unidos al oxígeno (C – O) [32], por separado. La proporción de estructura C – N aumenta de 7.8 at.% Para CF-900 a 12.2 at. % en Me-CFZ-900, lo que demuestra además que se han incorporado con éxito más átomos de nitrógeno en la estructura de carbono de Me-CFZ-900. Además, estos resultados muestran que la adición de melamina como promotor y fuente de nitrógeno durante la pirólisis a 900 ° C puede afectar el contenido de N total y dopado y luego ayudar a la formación de sitios más activos dentro de Me-CFZ-900, facilitando para mejorar la actividad catalítica de ORR durante las pruebas electroquímicas.
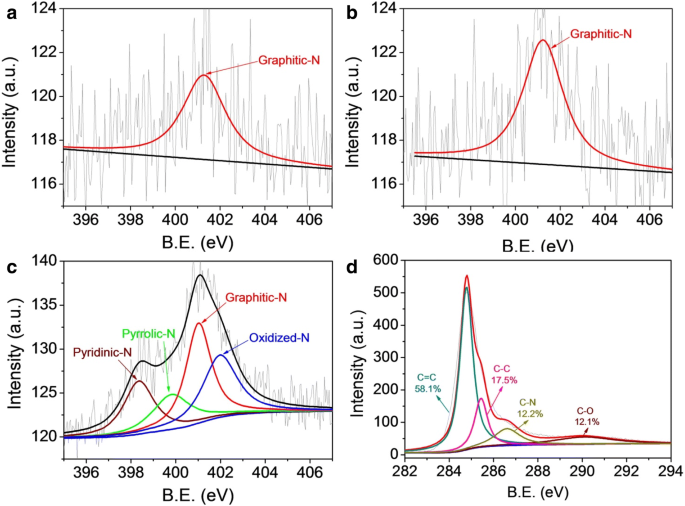
Espectros XPS N1s de alta resolución de CF-900 ( a ), CFZ-900 ( b ) y Me-CFZ-900 ( c ). (d ) Espectros XPS C1s de alta resolución de Me-CFZ-900 ( d )
Para evaluar la actividad electrocatalítica de ORR, se recubrieron tres catalizadores de ORR a base de carbono, respectivamente, en la superficie de GC-RRDE y se probaron mediante voltamperometría cíclica (CV) y voltamperometría de barrido lineal (LSV) en O 2 -saturado 0,1 mol l −1 Solución de KOH. Los resultados electroquímicos de la actividad ORR se indican en la Fig. 5a. Se puede encontrar que todas las curvas CV de CF-900, CFZ-900 y Me-CFZ-900 en O 2 Los electrolitos saturados muestran picos de ORR claros con potenciales de pico de 0,69, 0,84 y 0,91 V frente a RHE, respectivamente. Se encuentra que la actividad de ORR para tres catalizadores de carbono sigue el orden de Me-CFZ-900> CFZ-900> CF-900. Además, las curvas LSV (Fig. 5b) registradas en O 2 Se obtuvieron una solución saturada de KOH a una velocidad de rotación de 1600 rpm para comprender mejor las actividades catalíticas de CF-900, CFZ-900 y Me-CFZ-900. El electrodo catalizado por CFZ-900 muestra una mejor actividad de ORR con un potencial de media onda ( E 1/2 ) de 0,78 V en comparación con el electrodo catalizado por CF-900 con un E 1/2 de 0,65 V frente a RHE. Además, una E más alta 1/2 de ~ 0,86 V y una densidad de corriente limitada mayor a potenciales dados se puede obtener en el electrodo catalizado por Me-CFZ-900, que es comparable a los del catalizador comercial de Pt / C (20% en peso) (consulte el archivo adicional 1:Figura S4) y otros catalizadores de carbono informados en la literatura (ver Archivo adicional 1:Tabla S2). Estos resultados están de acuerdo con los resultados de las mediciones de CV, y muestran además la excelente actividad de ORR del Me-CFZ-900. Se sugiere que la activación del cloruro de zinc y la adición de una fuente de nitrógeno pueden mejorar la actividad catalítica de la ORR debido a la generación de estructuras mesoporosas y la mejora de la eficiencia del dopaje con N durante el proceso de pirólisis.
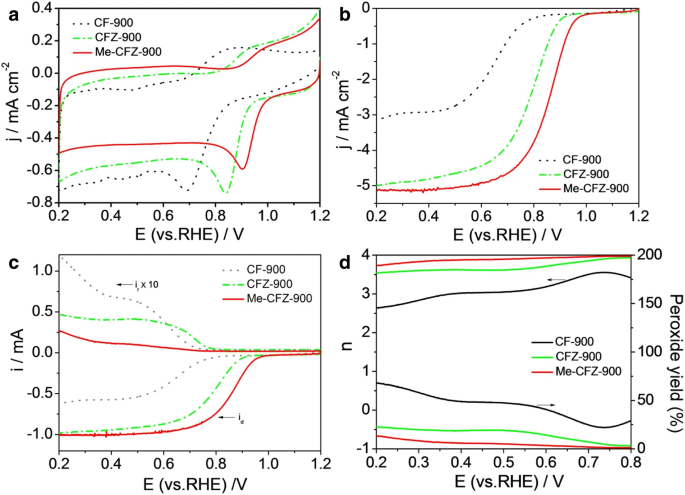
un Curvas CV de CF-900, CFZ-900 y Me-CFZ-900 en O 2 -saturado 0,1 mol l −1 Solución de KOH. b Curvas LSV para ORR de CF-900, CFZ-900 y Me-CFZ-900 y 20% en peso de Pt / C en O 2 -Solución de KOH 0,1 M saturada a una velocidad de rotación de 1600 rpm. c Corrientes de disco y anillo obtenidas con LSV en RRDE para CF-900, CFZ-900 y Me-CFZ-900 en O 2 -saturado 0,1 mol l −1 Solución de KOH. d El número de transferencia de electrones correspondiente y H 2 O 2 rendimiento de c
Se llevaron a cabo mediciones de RRDE para obtener información sobre la cinética de ORR de los catalizadores basados en carbono, como se muestra en la Fig. 5c. Además, según los datos de RRDE, el número de electrones correspondiente transferido ( n ) y especies de peróxido (H 2 O 2 %) producidos durante la ORR se calculan mediante el uso de las Ecs. (1) y (2), respectivamente. Los resultados del cálculo se muestran en la Fig. 5d. El H 2 O 2 El rendimiento (<14.0%) y el número de transferencia de electrones (3.45–3.95) en Me-CFZ-900 se pueden encontrar en el rango potencial de 0.2–0.8 V versus RHE, lo que indica una ruta de cuasi-cuatro electrones para que el proceso de ORR sea similar a la cinética de ORR del catalizador comercial de Pt / C (archivo adicional 1:Figura S3). Comparado con el Me-CFZ-900, mayor H 2 O 2 El rendimiento y el número de transferencia de electrones más pequeño se pueden observar tanto en CF-900 como en CFZ-900 en el mismo rango de potencial. Sin embargo, el H 2 O 2 el rendimiento en CFZ-900 es más alto que en Me-CFZ-900, pero el número de transferencia de electrones en CFZ-900 es similar al de Me-CFZ-900, lo que también sugiere una ruta de casi cuatro electrones para el proceso ORR. Desafortunadamente, CF-900 ha exhibido el número de transferencia de electrones más bajo (2.64–3.56) y el H 2 más alto O 2 rendimiento (22,2-68,2%), lo que implica que la ORR catalizada por CF-900 sigue principalmente una ruta mixta de procesos de dos y cuatro electrones. Estos resultados prueban que los catalizadores de carbono preparados por la activación de cloruro de zinc han exhibido una mayor eficiencia catalítica ORR y rendimiento electrocatalítico con o sin la adición de melamina. Combinado con el análisis de XPS y los datos de actividad de ORR, encontramos que solo las especies de N grafítico pueden existir en CF-900 y CFZ-900 pero exhiben actividad catalítica de ORR, lo que demuestra que el N grafítico puede ser uno de los sitios electrocatalíticamente activos que contribuyen a la Electrocatálisis ORR. Es notable que la adición de melamina al precursor puede promover la formación de especies de N piridínico y N pirrólico con estructuras planas, que pueden ser responsables de la mejora de la actividad de la ORR, respaldada por los resultados informados anteriormente [29]. Además, el excelente rendimiento de ORR de Me-CFZ-900 también se puede atribuir a otros aspectos:(1) el área de superficie BET alta y la estructura mesoporosa de Me-CFZ-900 pueden facilitar la adsorción y el transporte de la molécula de oxígeno y la exposición de más sitios activos; (2) una mayor conductividad eléctrica de Me-CFZ-900 puede impulsar eficazmente el transporte de electrones del proceso ORR; y (3) se incorporan más átomos de N en la estructura de carbono del Me-CFZ-900, que puede producir estructuras defectuosas y sitios activos más ricos en nitrógeno. Por lo tanto, la síntesis controlada de altos contenidos de especies de nitrógeno plano y grafítico es esencial para producir los catalizadores basados en carbón activo para ORR, pero la mejora adicional de la conductividad eléctrica, la eficiencia del dopaje con nitrógeno y las características mesoporosas es la cuestión clave para mejorar el catalizador de ORR. actividad.
Para comprender mejor el efecto de las temperaturas de pirólisis sobre la actividad de ORR, también preparamos otros tres catalizadores como Me-CFZ-700, Me-CFZ-800 y Me-CFZ-1000 mediante el mismo procedimiento de pirólisis. En la Fig. 6a, todos los catalizadores preparados han exhibido un pico de ORR obvio, pero el Me-CFZ-900 tiene el pico de corriente más grande y el potencial de pico más positivo. Las curvas de LSV registradas a una velocidad de rotación de 1600 rpm sugieren además que el Me-CFZ-900 ha exhibido un inicio más positivo y potenciales de media onda para ORR en comparación con otros catalizadores (Fig. 6b). Obviamente, la actividad catalítica ORR de nuestros catalizadores preparados depende en gran medida de la temperatura de pirólisis. La temperatura óptima es 900 ° C para nuestro sistema, ya que mayor o menor todavía producirá una actividad electrocatalítica de ORR inferior. Puede deberse a la densidad de los sitios activos y las características porosas dentro de los catalizadores controlados por la temperatura de pirólisis. Para comprender mejor el comportamiento cinético de ORR de diferentes catalizadores basados en carbono, también realizamos las pruebas RRDE para monitorear el H 2 O 2 rendimiento y número de transferencia de electrones (Fig. 6c, d). Se puede ver que la corriente del anillo ( i r ) de Me-CFZ-900 es obviamente más bajo que el de otros catalizadores en el rango de potencial de 0,2 a 0,8 V, lo que da como resultado el número de transferencia de electrones más alto y el H 2 más bajo O 2 rendimiento en Me-CFZ-900 basado en los datos RRDE. Estos resultados confirman además que la mejor actividad de ORR de los catalizadores preparados se puede obtener a 900 ° C.
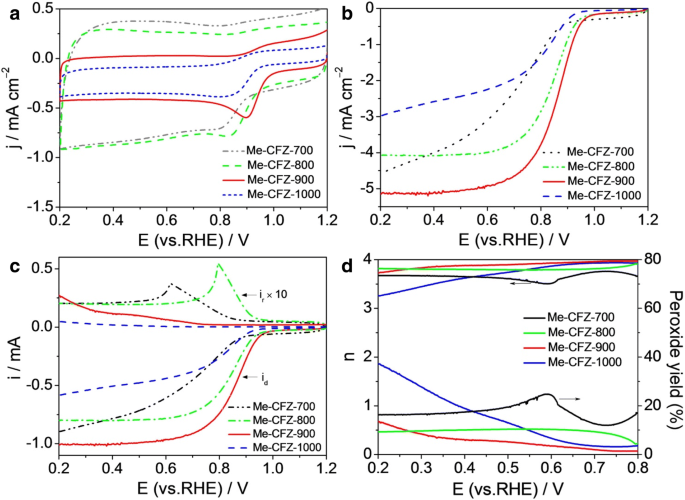
un CV y b Curvas LSV de Me-CFZ-700, Me-CFZ-800, Me-CFZ-900 y Me-CFZ-1000 en O 2 -saturado 0,1 mol l −1 Solución de KOH. c Corrientes de disco y anillo obtenidas con LSV en RRDE para Me-CFZ-700, Me-CFZ-800, Me-CFZ-900 y Me-CFZ-1000 en O 2 -saturado 0,1 mol l −1 Solución de KOH. d El número de transferencia de electrones correspondiente y H 2 O 2 rendimiento de c
El comportamiento de catálisis ORR de Me-CFZ-900 se evaluó adicionalmente mediante las curvas CV y las curvas LSV en N 2 versus O 2 -saturado 0,1 mol l −1 Soluciones de KOH (Fig. 7). En N 2 -electrolito saturado, a excepción de un CV capacitivo claro, no se puede observar ningún pico visible en la Fig. 7a, lo que indica que no tiene características. Por el contrario, cuando la prueba de CV se realiza en O 2 -electrolito saturado, se obtiene un pico ORR bien definido a ~ 0,90 V. Los resultados anteriores sugieren cualitativamente una actividad electrocatalítica de ORR de Me-CFZ-900 con un potencial de inicio de ORR de ~ 1.0 V acercándose al catalizador comercial de Pt / C (archivo adicional 1:Figura S4). Además, para revelar mejor el proceso de ORR de Me-CFZ-900, las mediciones de RDE se realizaron a una velocidad de escaneo de 5 mV s −1 con diferentes velocidades de rotación (400-2500 rpm), como se muestra en la Fig. 7b. La densidad de corriente de difusión limitante aumenta con el aumento de la velocidad de rotación, lo que demuestra que la corriente está controlada cinéticamente. Las tramas de Koutecky-Levich ( j −1 frente a ω −1/2 ) obtenidos a 0.2-0.6 V muestran buena linealidad y casi paralelismo (o superposición) (Fig. 7a), lo que indica números de transferencia de electrones similares para ORR a cinco potenciales (0.2-0.6 V). Se calcula que el número de transferencia de electrones promedio es ~ 3.84 a partir de la pendiente de los gráficos de Koutecky-Levich mediante el uso de las Ecs. (3) y (4), lo que confirma además que el ORR en Me-CFZ-900 sigue una ruta de reacción de cuatro electrones, siendo similar al catalizador Pt / C [33]. Este resultado concuerda bien con los resultados probados por RRDE. Además, la estabilidad de la electrocatálisis ORR es una de las principales preocupaciones en la tecnología actual de pilas de combustible alcalinas. Para este propósito, la estabilidad a largo plazo de Me-CFZ-900 se midió mediante una prueba de envejecimiento acelerado (AAT) en O 2 -Solución de KOH 0,1 M saturada. Antes de las pruebas de LSV para la catálisis de ORR nuevamente, el catalizador Me-CFZ-900 sufre mediciones continuas de CV entre 0.2 y 1.2 V frente a RHE durante 5000 ciclos a una velocidad de escaneo de 200 mV s −1 . Como se muestra en la Fig.7d, las curvas LSV de Me-CFZ-900 exhiben un cambio negativo de solo ~ 21 mV en el potencial de media onda y una disminución de aproximadamente 2.0% en la densidad de corriente de difusión limitada, pero no se observa una reducción notable en el potencial de inicio de ORR . Nuestros informes anteriores muestran que el catalizador comercial de Pt / C comúnmente muestra un cambio negativo de ~ 50 mV en el potencial de media onda de ORR después de la prueba de CV durante 5000 ciclos. Estos resultados electroquímicos sugieren una estabilidad a largo plazo prometedora de Me-CFZ-900, que es obviamente superior al catalizador comercial de Pt / C (archivo adicional 1:Figura S5). En resumen, podemos encontrar que el catalizador Me-CFZ-900 preparado en este trabajo es un candidato bastante prometedor para catalizadores ORR basados en Pt en medio alcalino.
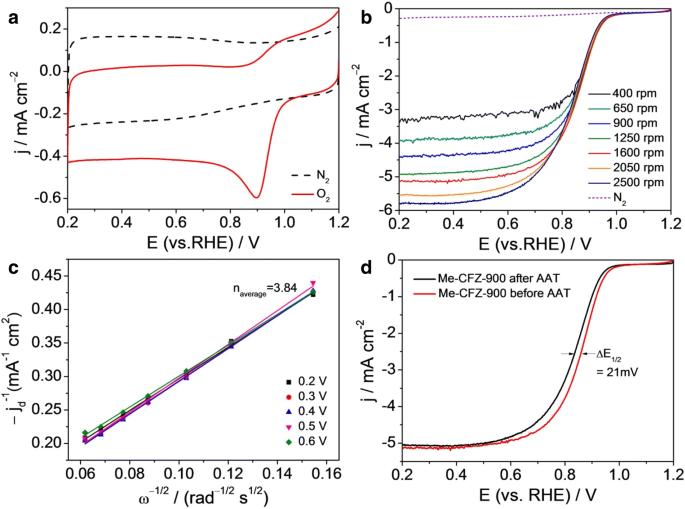
un Curvas CV de Me-CFZ-900 en 0,1 mol l −1 Solución de KOH saturada con N 2 versus O 2 . b Curvas LSV de Me-CFZ-900 en O 2 -saturado 0,1 mol l −1 Solución de KOH a diferentes velocidades de rotación (400–3600 rpm). c Gráficas de Koutecky-Levich de j d −1 frente a ω −1/2 obtenido de b a potenciales dados. d Curvas LSV de Me-CFZ-900 en O 2 -saturado 0,1 mol l −1 Electrolitos de KOH antes y después de la prueba AAT
Conclusiones
En resumen, desarrollamos un nuevo método para preparar microfibras de carbono nanoporosas dopadas con N (Me-CFZ-900) derivadas de residuos biológicos de bambú-carbono para la electrocatálisis de la reacción de reducción de oxígeno en medios alcalinos. El catalizador Me-CFZ-900 preparado exhibe la actividad electrocatalítica ORR con un potencial de media onda de ~ 0,86 V y un potencial máximo de ~ 0,91 V. El rendimiento de peróxido inferior al 14% y el número medio de transferencia de electrones de 3,84 son obtenido en Me-CFZ-900, que muestra además una vía de reacción de cuasi-cuatro electrones. An only 21 mV negative shift in half-wave potential and 2.0% decline in the limited current density are observed on Me-CFZ-900 after doing the accelerated aging test. Furthermore, high BET surface area (929.4 m 2 g −1 ) and mesoporous structure of Me-CFZ-900 can facilitate the adsorption and transportation of oxygen molecule. This work can help the researchers to build the high-performance carbon-based ORR electrocatalyst derived from biomass wastes and to understand the origin of the ORR electrocatalytic activity.
Abreviaturas
- AAT:
-
Accelerated aging test
- AE:
-
Auxiliary electrode
- APUESTA:
-
Brunauer-Emmett-Teller
- CF:
-
Carbon microfibers
- CV:
-
Voltamperometría cíclica
- E 1/2 :
-
Half-wave potential
- E ORR :
-
Onset potential
- E p :
-
Peak potential
- FE-SEM:
-
Microscopía electrónica de barrido por emisión de campo
- GC:
-
Glassy carbon
- HR-TEM:
-
Microscopía electrónica de transmisión de alta resolución
- LSV:
-
Voltamperometría de barrido lineal
- Me-CFZ-900:
-
Nitrogen-doped porous carbon microfibers
- ORR:
-
Oxygen reduction reaction
- Pt/C:
-
Platinum/carbon catalyst
- RDE:
-
Rotation disk electrode
- RE:
-
Reference electrode
- RHE:
-
Electrodo de hidrógeno reversible
- RRDE:
-
Rotation ring-disk electrode
- SCE:
-
Saturated calomel electrode
- WE:
-
Working electrode
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
Nanomateriales
- Nuevo folleto de dosificación y alimentación de Gericke
- Nuevos avances en FDM de Stratasys
- Un nuevo libro de Dominque Cardon
- Fibras de carbón activado con nanoestructura jerárquica derivada de guantes de algodón usados como electrodos de alto rendimiento para supercondensadores
- Microesferas de carbono magnéticas como adsorbente reutilizable para la eliminación de sulfonamidas del agua
- Un enfoque simple para sintetizar puntos cuánticos de carbono fluorescente de aguas residuales de tofu
- Carbón de alta porosidad autodopado con nitrógeno muy grafítico para la electrocatálisis de la reacción de reducción de oxígeno
- Síntesis y rendimiento del supercondensador de compuestos de carbono mesoporoso ordenados con polianilina / dopado con nitrógeno
- Electrocatalizadores de reducción de oxígeno Fe-N-C altamente activos y estables derivados de electrohilado y pirólisis in situ
- Síntesis fácil de esferas de carbono microporoso dopado con nitrógeno para supercondensadores simétricos de alto rendimiento
- Fácil preparación de nanocompuestos de nanotubos de carbono-Cu2O como nuevos materiales catalizadores para la reducción de p-nitrofenol



