Puntos de carbono dopados con N emisores multicolores derivados del ácido ascórbico y precursores de fenilendiamina
Resumen
En esta investigación, informamos el color verde, azul y naranja que emite puntos de carbono (CD) dopados con N, que se sintetizan a partir del ácido ascórbico y o - / m - / p -fenilendiamina ( o -PDA, m -PDA y p -PDA, respectivamente). Se han investigado sistemáticamente los efectos de la polaridad del disolvente y el pH de la solución sobre las propiedades de emisión de PL de los CD sintetizados. Se ha observado que la emisión de PL de los CD sintetizados disminuye con el aumento de la polaridad del disolvente debido a la mayor aglomeración. La carga superficial de los CD también muestra efectos prominentes sobre las propiedades de emisión de PL dependientes del pH.
Introducción
Recientemente, los puntos de carbono fluorescente (CD) han atraído una atención considerable debido a sus altos rendimientos cuánticos, baja toxicidad, excelente biocompatibilidad y procedimientos de preparación fáciles [1, 2, 3, 4]. Los CD se pueden utilizar ampliamente en aplicaciones de detección, visualización y bioimagen. La mayoría de los CD se emiten en una región azul o verde que limita su aplicación en la obtención de imágenes de tejidos vivos, ya que este proceso necesita una penetración profunda de la luz y la eliminación de la autofluorescencia, así como las limitaciones relacionadas con la dispersión de la luz de fondo. De ahora en adelante, la síntesis de CD que se emiten a mayor longitud de onda se ha vuelto importante. En este sentido, la síntesis química ecológica de CD emisores de varios colores es importante, ya que excluiría los peligros sintéticos asociados y los pasos críticos de separación [5].
El ajuste de la superficie de los CD mediante el dopado de heteroátomos, como los átomos de nitrógeno (N), boro (B) y azufre (S), se puede utilizar para modificar las propiedades de fluorescencia de los CD. Para este propósito, las moléculas orgánicas / inorgánicas con funcionalidades de heteroátomo podrían usarse como co-precursoras junto con la fuente de carbono o como precursoras [6, 7, 8]. Isómeros de fenilendiamina [ o -fenilendiamina ( o -PDA), m -fenilendiamina ( m -PDA) y p -fenilendiamina ( p -PDA)], con amina (–NH 2 ) funcionalidades, han demostrado ser una fuente de heteroátomos eficiente para la síntesis de CD dopados con N [3, 9, 10].
En este trabajo, los CD dopados con N que emiten color verde, azul y naranja se sintetizaron con éxito a partir del tratamiento hidrotermal de ácido ascórbico (AA) y m individual -PDA, o -PDA y p -PDA, respectivamente (A m -, A o - y A p -CD, respectivamente). Se investigaron sistemáticamente los efectos de las condiciones de reacción y los disolventes, y el pH de la solución sobre las propiedades de fluorescencia de cada tipo de CD. En particular, CD emisores de color verde sintetizados a partir de ácido ascórbico y m -PDA mostró un rendimiento cuántico (QY) muy alto en el disolvente de etanol.
Métodos experimentales
La información detallada sobre los materiales y el análisis instrumental se describen en el archivo adicional 1:Sección S1 y S2.
Síntesis de A m -, A o - y A p -CD
Para preparar A m -CD, ácido ascórbico (0,1 M, 0,8 mL) y m -fenilendiamina (0,1 M, 0,8 ml) (proporción de AA: m -PDA =1:1) se añadieron a 10,4 ml de agua desionizada y se agitaron durante 5 min. Luego, la mezcla se transfirió a un autoclave revestido con teflón de 50 ml y se calentó y mantuvo a 160ºC durante 6 h en un horno para una reacción adicional. Después de enfriar a temperatura ambiente (RT), el A m -Los CD se recogieron después de eliminar las partículas suspendidas mediante centrifugación a 10.000 rpm durante 20 min y se purificaron adicionalmente mediante un tubo de diálisis durante 6 h para eliminar los productos químicos residuales. La A m obtenida -La solución de CD se almacenó a 4 ° C para su posterior caracterización.
Para preparar A o -CD y A p -CD, todos los procedimientos experimentales fueron los mismos que los de A m -CD, excepto la relación de precursores. Para A o -CD, ácido ascórbico (0,1 M, 1,2 mL) y o -fenilendiamina (0,1 M, 0,8 ml) (proporción de AA: o -PDA =3:2); y para A p -CD, ácido ascórbico (0,1 M, 0,8 mL) y p -fenilendiamina (0,1 M, 0,4 ml) (proporción de AA: p -PDA =2:1), respectivamente.
Archivo adicional 1:la Fig. S1 muestra que la temperatura de reacción y la proporción de precursores se optimizaron para obtener la fluorescencia más alta para cada CD.
La Figura 1 muestra que la intensidad de emisión y la longitud de onda de los CD sintetizados son totalmente diferentes de las de los materiales precursores. La comparación general se resume en el archivo adicional 1:Tabla S1. Es interesante notar que la emisión de verde A m -Los CD se pueden obtener a partir de cian y azul que emiten AA y m -PDA, mientras que el color azul emite A o -Los CD se pueden obtener de cian y amarillo que emiten AA y o -PDA, que indica la nueva estructura conjugada formada a partir de la reacción entre AA y PDA.
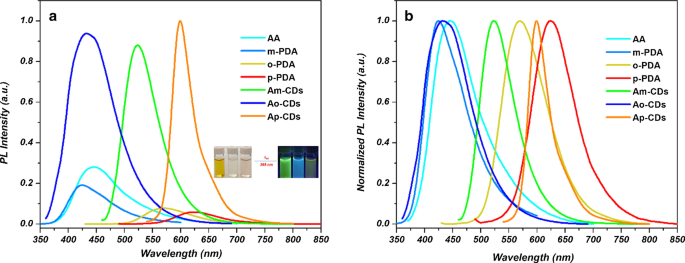
un Espectros de fluorescencia y b espectros de fluorescencia normalizados de A x -CD y materiales precursores diversos. Recuadro:Fotografías de A m -CD, A o -CD y A p -CDs dispersos en agua bajo luz natural (izquierda) y bajo irradiación UV ( λ ex =365 nm) (derecha)
Medición de rendimiento cuántico
Los rendimientos cuánticos (QY) de A m -, A o - y A p -Los CD se obtuvieron mediante un conocido método de pendiente relativa en RT utilizando varios tintes que hacen coincidir sus emisiones con las de cada CD [9]. Para A m -CD (longitud de onda de excitación de 450 nm), se seleccionó como referencia la rodamina 101 en etanol (QY =100%); para A o -CD (longitud de onda de excitación de 360 nm), sulfato de quinina (QS) en solución de ácido sulfúrico 0,1 M (QY =54%); y para A p -CD (longitud de onda de excitación de 514 nm), rodamina B en agua (QY =31%).
Para calcular los QY, se graficaron las intensidades PL integradas de la muestra y la referencia frente a la absorbancia a varias concentraciones, y se obtuvieron y compararon los gradientes.
Los QY de los tres CD se obtuvieron a partir de la siguiente ecuación:
$$ \ Phi _ {{\ text {s}}} =\ Phi _ {{\ text {r}}} * \ frac {{K _ {{\ text {s}}}}} {{K _ {{\ text { r}}}}} * \ frac {{\ eta _ {{\ text {s}}}}} {{\ eta _ {{\ text {r}}}}} $$ (1)donde Φ es el rendimiento cuántico relativo, K es la pendiente de la línea ajustada, y η es el índice de refracción del solvente. El subíndice "r" se refiere a la referencia y "s" a la muestra. Los valores del índice de refracción del agua y el etanol son 1,33 y 1,36, respectivamente.
Resultados y discusión
Caracterización de los CD como sintetizados
La morfología y el tamaño de A x -CD ( x = m , o y p ) se analizaron a partir de imágenes TEM. Las figuras 2, 3 y 4 muestran que los diámetros medios de A m -CD, A o -CD y A p -Los CD eran de 3,39 nm, 3,65 nm y 4,45 nm, respectivamente. Los espacios entre planos de A x -Los CD fueron de 0,23 nm, 0,21 nm y 0,35 nm analizados a partir de imágenes HR-TEM, respectivamente, que corresponden a los planos (100) y (002) del carbono de grafito [11].
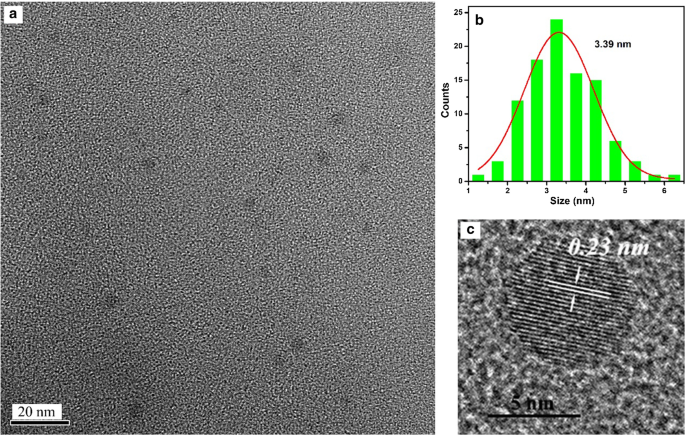
un Imágenes TEM de A m -CD, b los histogramas de distribución del tamaño de partícula, y c Imágenes HR-TEM
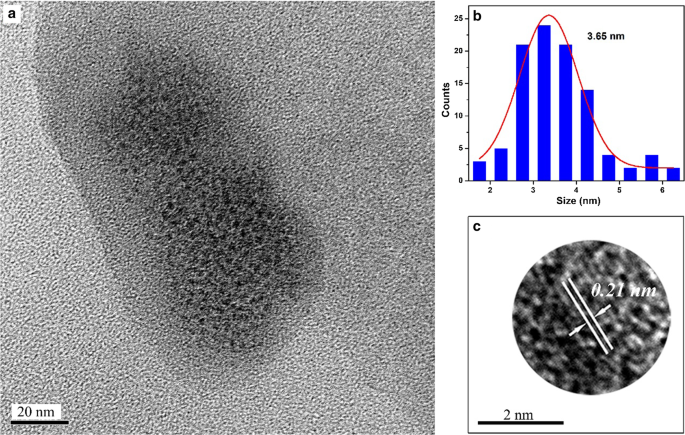
un Imágenes TEM de A o -CD, b los histogramas de distribución del tamaño de partícula, y c Imágenes HR-TEM
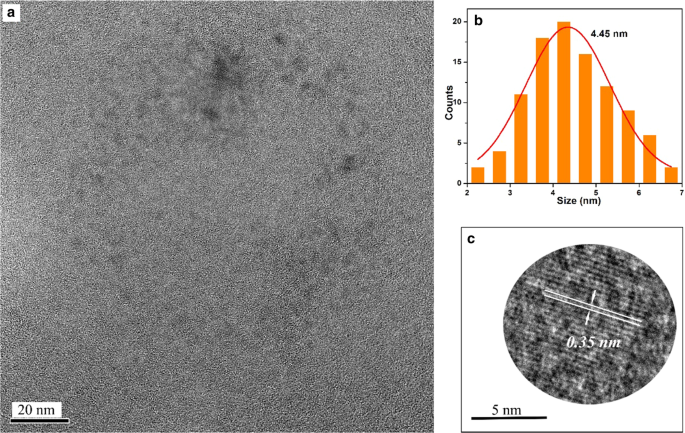
un Imágenes TEM de A p -CD, b los histogramas de distribución del tamaño de partícula, y c Imágenes HR-TEM
Las estructuras cristalinas de A x -Los CD fueron investigados por XRD. La Figura 5a muestra que los tres CD tienen un pico de difracción único amplio alrededor de 2 θ =21 ° –23 °, que se origina a partir de la estructura de carbono grafítico [3, 12].
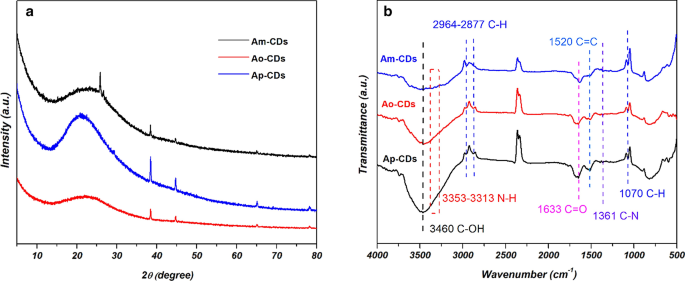
un Patrones XRD y b Espectros FTIR de A x -CD
Los enlaces químicos y los grupos funcionales superficiales de A x -Los CD se analizaron mediante espectros FT-IR. La Figura 5b muestra los picos en ~ 3460 y ~ 3313–3353 cm −1 que se puede atribuir a las vibraciones de estiramiento de O – H y N – H, respectivamente. La presencia de grupos hidrófilos puede mejorar la solubilidad de los CD en el disolvente polar mediante la formación de puentes de hidrógeno [13, 14]. Los picos en ~ 1070, ~ 2877 y ~ 2964 cm −1 puede asignarse a las vibraciones de estiramiento de C – H [8]. El pico fuerte observado a ~ 1633 cm −1 puede atribuirse a la vibración de estiramiento del enlace C =O en el grupo amida, lo que confirma la reacción de amidación entre los ácidos carboxílicos de AA y las aminas de PDA [15]. Los picos que aparecen a ~ 1520 cm −1 puede originarse a partir de la vibración de flexión de C =C [16]. Además, los picos observados a ~ 1361 cm −1 puede atribuirse a la vibración de estiramiento de C – N, que confirma la presencia de un átomo de nitrógeno en los CD sintetizados [10]. La casi identidad de los espectros FT-IR de las tres CD indica la presencia de enlaces químicos y grupos funcionales similares en las CD, independientemente de la posición del grupo amina en las especies de isómeros PDA.
Se utilizó XPS para analizar la composición elemental y los grupos funcionales de A x -CD. La Figura 6a muestra el espectro de levantamiento XPS de A m -CD, que indica la existencia de átomos de C, O y N en el A m sintetizado -CD. Archivo adicional 1:Figs. S2 y S3 muestran que los tres CD tienen composiciones elementales similares, como se resume en la Tabla 1. Los análisis de XPS también indican un estado de oxidación y funcionalidades similares en los tres CD. Figura 6 y archivo adicional 1:Figs. S2 y S3 muestran el C1 s de alta resolución Espectros XPS para A x -CD, que revelan que el carbono se puede deconvolucionar en varios picos centrados en ~ 284.0, ~ 285.2, ~ 286.9 y ~ 290.1 eV, que corresponden a C =C, C – C, C – O y N – C =O grupos, respectivamente. Los espectros de O1s de alta resolución pueden descomponerse en picos que se muestran a ~ 531,8 y ~ 532,8 eV que pueden atribuirse a los grupos C =O y C – O, respectivamente [17]. Los N1 s los espectros revelan la presencia de grupos N – H, C – N – C y N grafítico que se muestran a ~ 399,0, ~ 400,0 y ~ 401,4 eV, respectivamente [18].
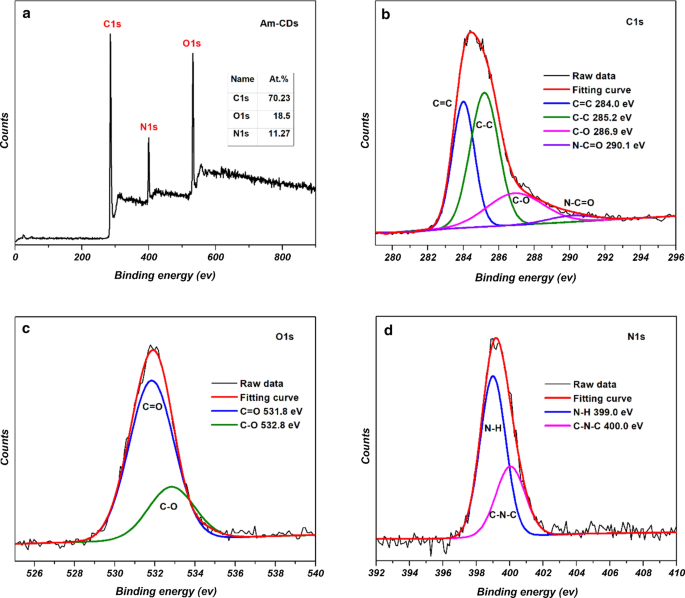
un Espectro de levantamiento XPS de A m -CD. La b de alta resolución C1 s , c O1 s y d N1 s Espectros XPS de A m -CD
Propiedades ópticas de A x -CD
Las propiedades ópticas del A x -Los CD fueron explorados por la absorción UV-Vis y los espectros PL. La Figura 7 muestra los espectros de absorción UV-Vis, excitación por fotoluminiscencia (PLE) y PL de A x -CD. Se observan dos picos de absorción centrados en 289 y 400 nm en la absorción UV-Vis de A m -CD (Fig. 7a), que corresponden al π - π * transiciones de la estructura C =C y n - π * transiciones de grupos C =O [15]. A o -CD y A p -Los CD mostraron dos picos en los espectros UV-Vis, sin embargo, las posiciones e intensidades de los picos fueron diferentes (Fig. 7c, e). Esta diferencia podría atribuirse a la diferente extensión de las transiciones electrónicas. Además, el pico de absorción amplio adicional que se muestra a ~ 510 nm se puede atribuir a la absorción superficial de la A p -CD, y sucesiva excitación de la emisión PL [19]. En consecuencia, los espectros PLE y PL son diferentes para los tres A x -CD. El A m -Los CD muestran una emisión en la región verde a 521 nm cuando se excitan a 450 nm. El A o -CD y A p -Los CD muestran picos de excitación a 360 y 580 nm y emiten en la región azul a 432 nm y la región naranja a 596 nm, respectivamente.
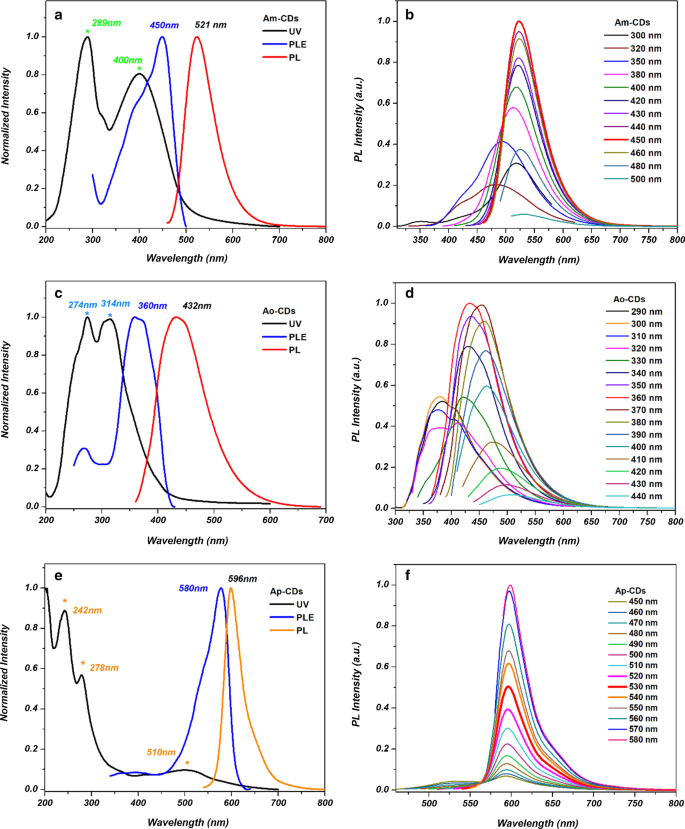
Los espectros de absorción UV-Vis normalizados, la excitación PL y los espectros de emisión PL del a A m -CD, c A o -CD y e A p -CD. Los espectros de emisión PL normalizados de b A m -CD, d A o -CD y f A p -CD a diferentes longitudes de onda de excitación
Las figuras 7b, d, f muestran que A m - y A o -Los CD muestran una emisión dependiente de la excitación mientras que A p -Los CD muestran una emisión independiente de la excitación. El comportamiento de emisión de PL dependiente de la longitud de onda de excitación podría originarse a partir del tamaño de CD no uniforme, y la presencia de varios defectos superficiales, y varios grupos funcionales de superficie en los CD [20, 21] . El comportamiento de emisión de PL independiente de la longitud de onda de excitación de A p -CD indica estados de emisión uniformes, que también dan como resultado un ancho de emisión estrecho. Las diferentes propiedades PL relacionadas con la longitud de onda de excitación entre las A x -Los CD implican los diferentes estados energéticos y su morfología [22, 23].
Efectos de los solventes y QY en las propiedades de emisión de PL
Los efectos del solvente, incluida el agua desionizada (H 2 O), metanol (MeOH), etanol (EtOH), alcohol isopropílico (IPA), acetona (ACE), acetonitrilo (ACN), N , N -Dimetilformamida (DMF) y dimetilsulfóxido (DMSO) sobre las propiedades de emisión de PL de la A x -Se investigaron los CD. Archivo adicional 1:La Fig. S4 muestra que la longitud de onda de emisión de PL cambia en diferentes disolventes. Esto muestra las propiedades solvatocrómicas típicas de los CD causadas por la interacción entre los grupos funcionales de la superficie de los CD y los solventes [21, 24].
Archivo adicional 1:la Fig. S5 muestra que la A m -Los CD poseían el QY más alto entre los tres CD. Además, el A x -Los CD en el solvente de etanol exhiben un QY más alto que los del agua, lo que puede explicarse por (1) un mayor grado de aglomeración de CD en solvente altamente polar, (2) mayor tasa de desintegración no radiativa durante la interacción entre solvente altamente polar y CD y (3) cambio morfológico inducido por el agua [25].
Efectos del pH en la emisión de fluorescencia de A x -CD
Las intensidades de emisión de PL del A m preparado -, A o - y A p -Las CD se controlaron en diversas condiciones de pH. La Figura 8 muestra que A m - y A o -Los CD exhiben un comportamiento de emisión de PL similar a medida que cambia el pH de la solución. La disminución de la emisión de PL a medida que aumenta el pH se puede atribuir a la desprotonación de los grupos funcionales superficiales del A m - y A o -CD, lo que resulta en la aglomeración de CD [26,27,28,29].
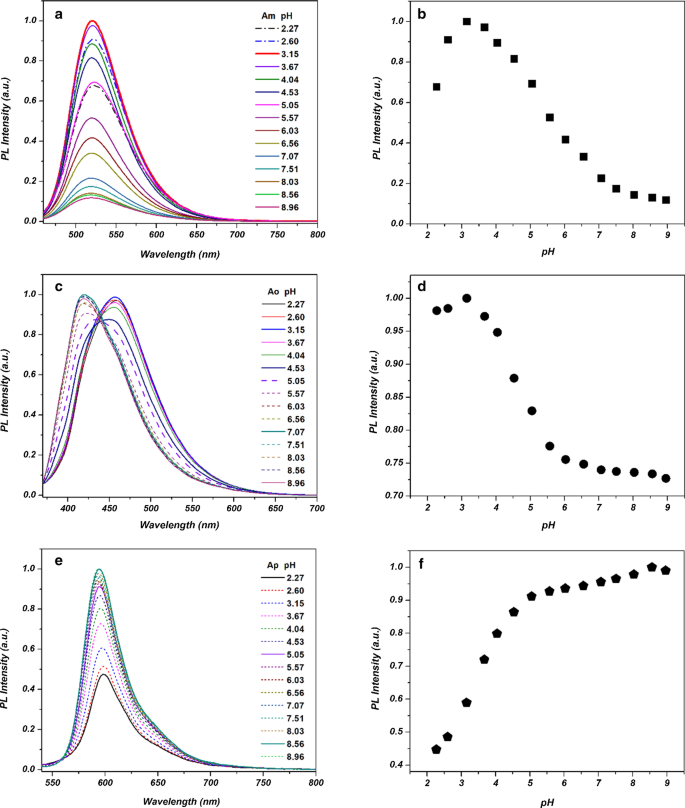
Emisión PL y cambio de intensidad de a , b A m -CD, c , d A o -CD y e , f A p -CD en varias condiciones de pH
Por otro lado, para A p -CD, la intensidad de PL aumenta a medida que aumenta el pH de la solución. Este fenómeno se puede atribuir a la diferente carga superficial de A p -CD de los otros CD.
Para investigar los diferentes comportamientos dependientes del pH entre A x -CD, se controló el potencial zeta a varios valores de pH. Como se muestra en la Fig.9, los potenciales zeta de A m - y A o -Los CD disminuyeron gradualmente al aumentar el pH, mientras que el potencial zeta de A p -Los CD aumentaron al aumentar el pH. Esto podría resultar en una menor aglomeración y mejorar la intensidad PL de A p -CD [30, 31].
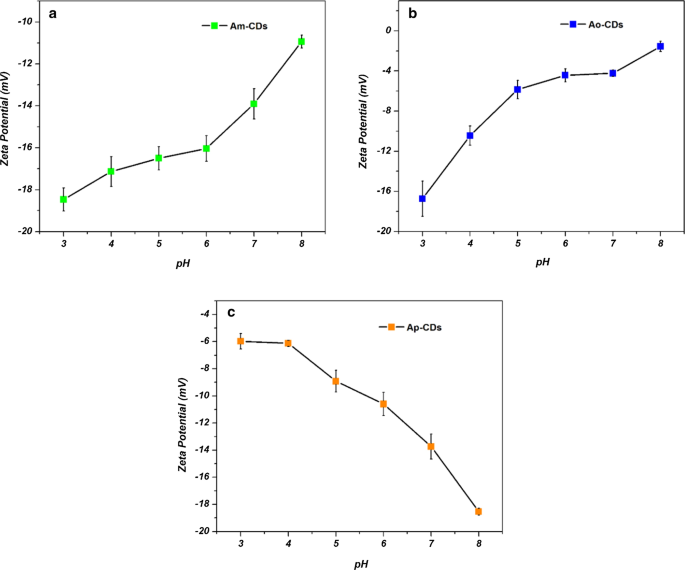
Potencial Zeta de a A m -CD, b A o -CD y c A p -CD con varios valores de pH, respectivamente
Conclusión
En este trabajo, los CD dopados con N que emiten color verde, azul y naranja se han sintetizado con éxito a partir de la reacción entre el ácido ascórbico (AA) y m -PDA, o -PDA y p -PDA, respectivamente. Para ello, se ha empleado un método sencillo de síntesis hidrotermal a baja temperatura. Las propiedades fotofísicas y ópticas de los tres CD se han investigado a fondo con diferentes disolventes y pH. La A x sintetizada -Los CD exhibieron QY más altos en etanol que en agua. La menor aglomeración, la tasa reducida de desintegración no radiativa y el menor cambio morfológico de las EC podrían ser la razón detrás de tal comportamiento. Además, la carga superficial de A x sintetizada -Los CD dieron como resultado diferentes propiedades de emisión de PL dependientes del pH. Estas propiedades únicas de los CD sintetizados permitirán sus aplicaciones en diferentes campos de imágenes y detección.
Disponibilidad de datos y materiales
Todos los datos generados o analizados durante este estudio se incluyen en este artículo y sus archivos de información complementaria.
Abreviaturas
- CD:
-
Puntos de carbono
- AA:
-
Ácido ascórbico
- m -PDA:
-
m -Fenilendiamina
- o -PDA:
-
o -Fenilendiamina
- p -PDA:
-
p -Fenilendiamina
- A x -CD:
-
x = m , o , Y p
- QY:
-
Rendimiento cuántico
- SI:
-
Información complementaria
- RT:
-
Temperatura ambiente
- QS:
-
Sulfato de quinina
- PLE:
-
Excitación por fotoluminiscencia
- H 2 O:
-
Agua desionizada
- MeOH:
-
Metanol
- EtOH:
-
Etanol
- IPA:
-
Alcohol isopropílico
- ACE:
-
Acetona
- ACN:
-
Acetonitrilo
- DMF:
-
N , N -Dimetilformamida
- DMSO:
-
Dimetilsulfóxido
- HR-TEM:
-
Microscopía electrónica de transmisión de alta resolución
- FT-IR:
-
Espectroscopía infrarroja por transformada de Fourier
- XRD:
-
Difracción de rayos X
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
Nanomateriales
- Creación y generación de imágenes de ciclocarbono
- Hilo de nanotubos de carbono, músculo y láminas transparentes
- Presentación de la estructura atómica y electrónica de las nanofibras de carbono de copa apilada
- Puntos de carbono luminiscentes azules independientes de excitación de alta eficiencia
- Compuestos de grafeno y polímeros para aplicaciones de supercapacitores:una revisión
- Síntesis de puntos cuánticos de tipo II / tipo I de ZnSe / CdS / ZnS con supresión de reabsorción y su aplicación para el ensayo inmunoabsorbente
- Fibras de carbón activado con nanoestructura jerárquica derivada de guantes de algodón usados como electrodos de alto rendimiento para supercondensadores
- Un enfoque simple para sintetizar puntos cuánticos de carbono fluorescente de aguas residuales de tofu
- Material y propiedades ópticas de los puntos cuánticos de carbono fluorescente fabricados a partir de jugo de limón mediante una reacción hidrotermal
- Electrocatalizadores de reducción de oxígeno Fe-N-C altamente activos y estables derivados de electrohilado y pirólisis in situ
- Síntesis sencilla en un solo recipiente de puntos de carbono de polidopamina para terapia fototérmica



