Material y propiedades ópticas de los puntos cuánticos de carbono fluorescente fabricados a partir de jugo de limón mediante una reacción hidrotermal
Resumen
Los puntos cuánticos de carbono fluorescentes solubles en agua (CQD) se sintetizan utilizando jugo de limón como recurso de carbono mediante una simple reacción hidrotermal. Los CQD obtenidos tienen un tamaño medio de 3,1 nm. Revelan una morfología uniforme y bien cristalinas y pueden generar una emisión de luz azul verdosa brillante bajo irradiación de luz ultravioleta o azul. Encontramos que la fluorescencia de estos CQD es inducida principalmente por la presencia de grupos que contienen oxígeno en la superficie y el borde de los CQD. Además, demostramos que las CQD preparadas se pueden aplicar a la obtención de imágenes de células vegetales. Este estudio está relacionado con la fabricación, investigación y aplicación de nanoestructuras de carbono desarrolladas recientemente.
Antecedentes
El punto cuántico de carbono (CQD) es una nueva clase de nanomaterial a base de carbono que normalmente tiene un tamaño espacial inferior a 20 nm, que fue descubierto por Xu et al. en 2004 [1]. Las nanopartículas de carbono fluorescentes fueron fabricadas por Sun et al. mediante ablación láser de polvo de grafito en 2006 [2] y desde entonces han sido nombrados como “puntos cuánticos de carbono (CQD)”. Los CQD fluorescentes tienen un gran potencial para ser aplicados en fotocatálisis, dispositivos optoelectrónicos, biomedicina, exhibición de película delgada, iluminación saludable y otras disciplinas de aplicaciones prácticas. En comparación con los puntos cuánticos tradicionales basados en semiconductores, los CQD se pueden obtener mediante técnicas de fabricación de bajo costo y tienen características fascinantes e importantes como buena biocompatibilidad, objetivo biológico preciso, baja toxicidad y un efecto de tamaño cuántico más fuerte. En los últimos años, los CQD fluorescentes han atraído una enorme atención [3, 4] debido a sus excelentes propiedades estructurales y ópticas [5]. Se han propuesto como materiales de sustitución de los puntos cuánticos de semiconductores convencionales en las áreas de aplicación que incluyen imágenes biológicas, etiquetado biológico, LED de puntos cuánticos (QLED), protección del medio ambiente y otros campos relacionados [6,7,8,9]. La investigación sobre CQD ha crecido rápidamente en física de materia condensada, ciencia de materiales, electrónica y optoelectrónica. Se han realizado extensivamente estudios fundamentales y de aplicación relacionados en todo el mundo [3, 4, 5, 6, 7, 8, 9].
En la actualidad, existen diversas técnicas [10, 11] para sintetizar CQD, como el enfoque hidrotermal [11, 12], el método de microondas [13], etc. Las CQD se han sintetizado a partir de varios precursores de carbono como la glucosa [14], el ácido cítrico [15] y el ácido ascórbico [16]. Sin embargo, la técnica para fabricaciones eficientes de CQD fluorescentes biocompatibles a gran escala de producción sigue siendo necesaria y se ha convertido en un desafío para las aplicaciones prácticas de los CQD. Se ha observado que la síntesis directa de los CQD a partir de productos alimenticios [17,18,19] y / o subproductos [20] es una de las estrategias más prometedoras y significativas. Se sintetizaron puntos de carbono emisores de rojo (R-CD) con un diámetro promedio de 4 nm y un alto rendimiento cuántico (QY) del 28% en agua [21] calentando una solución etanólica de jugo de limón sin pulpa. Un reductor fuerte NaBH 4 añadido a los R-CD se utilizó como un medio para aumentar la intensidad de la emisión de luz de los R-CD. Sin embargo, sabemos que NaBH 4 es tóxico. Muy recientemente, hemos fabricado los CQD que emiten verde y azul a partir de aguas residuales de tofu sin añadir sustancias tóxicas [22]. Los CQD elaborados a partir de productos alimenticios y / o subproductos se consideran seguros para aplicaciones biológicas porque casi no hay toxicidad conocida en estos recursos naturales de carbono. Recientemente, se han llevado a cabo varias investigaciones serias para sintetizar CQD a partir de recursos de carbono no tóxicos utilizando un enfoque de un solo paso y se ha logrado un progreso significativo en la síntesis, el estudio y la aplicación de estos CQD. Por ejemplo, el ajo se utilizó como fuente verde para sintetizar CQD [23]. Estudios detallados de estructura y composición demostraron [23] que el contenido de N y la formación de C – N y C =N son claves para mejorar la fotoluminiscencia (PL) QY. Además, los CQD exhiben una excelente estabilidad en un amplio rango de pH y altas concentraciones de NaCl, lo que los hace aplicables en condiciones complicadas y duras [23].
La principal motivación del presente trabajo es desarrollar un método experimental simple y eficiente para la fabricación de bajo costo de CQD a partir de jugo de limón mediante el uso de un tratamiento hidrotermal a temperaturas relativamente bajas y mediante un proceso que requiere menos tiempo. Se sabe que el jugo de limón se puede obtener fácil y económicamente y, por lo tanto, es una buena fuente de carbono para la fabricación de muestras y dispositivos basados en CQD. En comparación con el estudio anterior [21], las CQD no tóxicas obtenidas en nuestro trabajo son más adecuadas para la obtención de imágenes biológicas y marcadores celulares. En este estudio, también realizamos el examen del material básico y las propiedades ópticas de los CQD obtenidos a partir del jugo de limón y aplicamos los CQD para obtener imágenes de células vegetales.
Métodos
Materiales preliminares
En este estudio, los materiales precursores de carbono se obtienen del jugo de limón fresco. Los ingredientes principales y sus porcentajes se obtienen mediante la medición de cromatografía líquida de alto rendimiento (HPLC) como se muestra en la Tabla 1. Para la preparación de la muestra, el limón fresco tomado como fuente de carbono y la cebolla fresca utilizada para la obtención de imágenes celulares se compraron en el supermercado local. El etanol era analíticamente puro y se utilizó como agente dispersante. Se utilizó agua desionizada (18,25 MΩ cm) para los experimentos.
Síntesis de CQD
Los CQD se sintetizaron a partir del jugo de limón mediante un simple tratamiento hidrotermal a temperaturas relativamente bajas y mediante un proceso que requiere menos tiempo. Los procesos típicos de preparación de muestras se muestran en la Fig. 1. Se mezclaron ochenta mililitros de jugo de limón sin pulpa con 60 mL de etanol. Después, la mezcla se transfirió a un autoclave de acero inoxidable equipado con politetrafluoroetileno y se calentó a una temperatura constante a aproximadamente 120ºC durante 3 h. Después de la reacción, se obtuvo el producto de color marrón oscuro después de un enfriamiento natural a temperatura ambiente. La solución de color marrón oscuro se lavó con un exceso de diclorometano para eliminar los restos orgánicos que no reaccionaron y este paso se puede repetir 2-3 veces. Se añadió agua desionizada hasta que el volumen de la solución marrón aumentó hasta un tercio de la solución y se centrifugó a 10000 rpm durante 15 min para separar las partículas grandes. Así, las muestras de CQD pueden obtenerse por carbonización de jugo de limón, que contiene carbohidratos y ácidos orgánicos como glucosa, fructosa, sacarosa, ácido ascórbico, ácido cítrico, etc. como precursores de carbono. Nuestra fácil reacción hidrotermal se realiza a una temperatura más baja (120 ° C) y lleva menos tiempo (3 h), en comparación con el método informado [24].
Preparación de CQD a partir de jugo de limón mediante tratamiento hidrotermal
Caracterización
La morfología y microestructuras de las CQD obtenidas a partir de jugo de limón se analizaron mediante el microscopio electrónico de transmisión (JEM 2100, Japón) operado a 300 KV. La fase cristalina de los CQD se investigó mediante difracción de rayos X (Rigaku TTR-III, Japón) utilizando radiación Cu-Kα ( λ =0,15418 nm). El espectro de absorción de UV-Vis se midió mediante un espectrofotómetro de UV-Vis (Specord200). La emisión de luz inducida por fotones se examinó mediante un espectrofotómetro de fluorescencia (IHR320, HORIBA Jobin Yvon, EE. UU.) Para diferentes longitudes de onda de excitación que van desde 330 a 490 nm. Los espectros de espectroscopía de fotoelectrones de rayos X (XPS) se registraron mediante el espectrómetro de fotoelectrones PHI5000 Versa Probe II con Al Kα a 1486,6 eV.
Resultados y discusiones
Las imágenes del microscopio electrónico de transmisión (TEM) de los CQD se muestran en la Fig. 2. La imagen TEM de bajo aumento de las muestras preparadas indica que los CQD tienen una dispersión uniforme. Los CQD son de forma esférica con una distribución de tamaño estrecha que varía de 2,0 a 4,5 nm y con un tamaño medio de 3,1 nm que se muestra en la Fig. 2b, c. La Figura 2d muestra el espaciado de celosía de 0.215 nm que corresponde a la faceta [100] del carbono grafítico, y el correspondiente patrón de transformada rápida de Fourier (FFT) de los CQDs muestra además la estructura altamente cristalina, consistente con el informe anterior [25]. En comparación con los estudios previos [19, 21,22,23], como se muestra en la Fig. 2, las CQD obtenidas en nuestro trabajo no solo tienen buena calidad sino que también muestran una morfología mejor uniforme. Por lo tanto, los CQD con morfología redondeada uniforme y bien cristalinos se pueden fabricar mediante un proceso de tratamiento hidrotermal sencillo. El rendimiento de producción (PY) de CQD se puede calcular de acuerdo con la definición PY =( m / M ) × 100%, donde m es la masa de los CQD, y M es la masa de jugo de limón fresco. El rendimiento de producción de CQD preparados en este estudio es de aproximadamente 0,1% según los resultados de la medición, es decir, 100 g de líquido con 6,30% de ácido cítrico pueden obtener aproximadamente 0,1 g de CQD (ver Tabla 1).
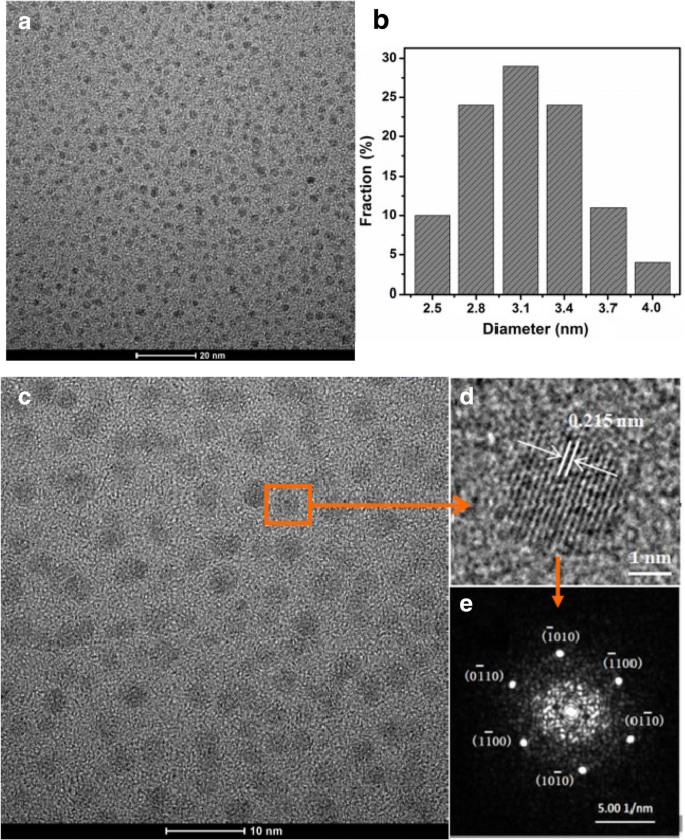
un , c , d Imagen TEM. b Distribución del tamaño de partícula de los CQD. e El patrón FFT correspondiente de CQD
La difracción de rayos X (XRD) típica y el perfil XPS de los CQD se muestran en la Fig. 3. Hay un pico amplio (002) centrado en 2 θ ~ 21,73 °, y el espaciado entre capas se calculó en 0,409 nm, correspondiente a la estructura del grafito, como se muestra en la Fig. 3a, que es similar a los devalores informados para CQD preparados por otros métodos [15, 26]. La variación de la distancia entre capas puede deberse a la introducción de más grupos que contienen oxígeno, como la presencia de –OH y –COOH en la superficie y el borde del CQD durante el procedimiento de reacción hidrotermal para la preparación de CQD. Se emplearon XPS y FTIR para detectar la composición de CQD. Como se muestra en la Fig. 3b, c, el espectro XPS muestra un pico de C1s grafítico dominante a 284,5 eV y un pico de O1s a 531,4 eV de CQD. El pico típico a 284,7, 286,5 y 288,9 eV en una exploración de alta resolución del espectro XPS de C1s (la figura 3c se atribuye a C =C / C – C, C – O y C =O / COOH, respectivamente. Indica claramente que los CQD se funcionalizaron con grupos hidroxilo, carbonilo y ácido carboxílico, que son beneficiosos para la modificación y funcionalización de la superficie, y también favorecen la solubilidad en agua. La figura 3d muestra el espectro de espectroscopía infrarroja por transformada de Fourier (FTIR) de CQDs. La presencia de funcionalidades de oxígeno de diferentes tipos en CQDs fue confirmada por picos a 3450 cm −1 (Vibraciones de estiramiento O – H), 2927 cm −1 , 1407 cm −1 (Vibraciones de estiramiento C – H), 1726 cm −1 (C =O vibraciones de estiramiento), 1639 cm −1 (C =C vibraciones de estiramiento), 1227 cm −1 (Vibraciones de estiramiento C – OH) y 1080 cm −1 (Vibraciones de estiramiento C – O). Se observa que el análisis FTIR está alineado con el resultado XPS anterior. Lo más importante es que el pico de C – O – C (epoxi) desapareció por completo a los 1290 cm −1 . Estos resultados implican el mecanismo de formación de CQD, con la ruptura de los grupos epoxi y la formación de los enlaces C – C subyacentes, posteriormente el sp 2 Los dominios se extrajeron de precursores de moléculas pequeñas como glucosa, fructosa, ácido ascórbico y ácido cítrico mediante deshidratación o carbonización adicional y finalmente para formar CQD. Por lo tanto, la escisión de enlaces de los grupos de oxígeno circundantes contribuye a la formación de los CQD [15, 27].
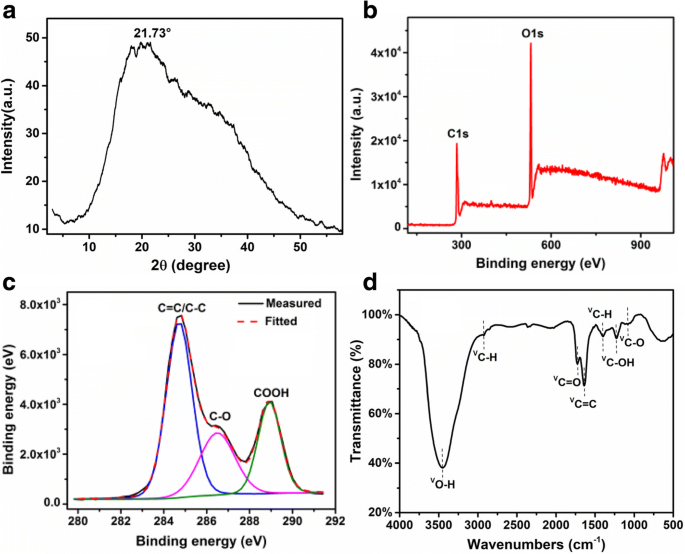
un Patrón XRD. b Espectros XPS de rango bajo. c Escaneo XPS de alta resolución de la región C1s. d Espectros FTIR de CQD
En la actualidad, se han propuesto y examinado los posibles mecanismos para la formación de CQD a partir de precursores de carbono mediante el método hidrotermal [28]. Sobre la base de estos resultados publicados, podemos comprender el mecanismo de síntesis de CQD a partir del jugo de limón. El jugo de limón sin pulpa se calienta y se deshidrata para formar el marco básico de C =C / C – C que se compone principalmente de CQD, y el resto de las moléculas llegan a la superficie del núcleo para producir un nuevo C =C / Enlace C – C y luego creció continuamente en esta forma. Con la extensión del tiempo de calentamiento, la morfología de las CQD se forma gradualmente. Al mismo tiempo, en el proceso de tratamiento hidrotermal de los CQD formados, la superficie y el borde de los CQD pueden contener una gran cantidad de hidroxilo (–OH), carboxilo (–COOH) y carbonilo (–C =O) u otro oxígeno- que contiene grupos funcionales; una porción del átomo de H y O en estos grupos podría eliminarse deshidratando en el ambiente hidrotermal.
Para examinar las propiedades ópticas de los CQD, se midieron los espectros de fotoluminiscencia (PL) y absorción ultravioleta-visible (UV-Vis) de los CQD en consecuencia. Como se muestra en la Fig. 4a, el pico de absorción óptica de los CQD se observó en la región ultravioleta con una absorción máxima a 283 nm, que se debe a n - π * transición de la banda C =O [29]. El espectro PL de la Fig. 4b muestra que la longitud de onda de emisión PL de los CQD alcanza el pico a 482 nm con una longitud de onda de excitación de 410 nm. La longitud de onda de emisión cambió de 430 a 530 nm cuando la longitud de onda de excitación se incrementó de 330 a 490 nm. Con el aumento de la longitud de onda de excitación, los picos emisores de fluorescencia se convierten en corrimiento al rojo, lo que se refiere a la reabsorción de fotones. El resultado revela que los CQD tienen una característica PL dependiente de la excitación [30]. Los CQD fluorescentes verdes también muestran un pico PL amplio que se desplaza con el cambio de longitud de onda de excitación, que está relacionado con el efecto de confinamiento cuántico y los defectos de borde. Con la medición PL estándar [22], el rendimiento cuántico de fluorescencia de los CQD es del 16,7% con una longitud de onda de excitación de 410 nm, donde se había utilizado sulfato de quinina como referencia. Este valor es significativamente mejor que el QY (8,95%) de CQD elaborados a partir de jugo de limón en el informe anterior [24]. Se sabe que la QY de los CQD se puede mejorar drásticamente después de la modificación o pasivación de la superficie [30]. La adición de etanol durante el proceso de síntesis puede introducir más grupos funcionales que pueden resultar en un mayor QY de CQD. Sin embargo, el QY de los CQD en este estudio es notablemente más bajo que el QY de los CQD sintetizados mediante el uso de ácido cítrico (CA) y etanolamina (EA) como moléculas modelo. Aquí, la pirólisis a 180 ° C resultó en un precursor molecular con un PL muy intenso y un QY alto del 50%, que se debe al dopaje N durante el proceso de síntesis [30].
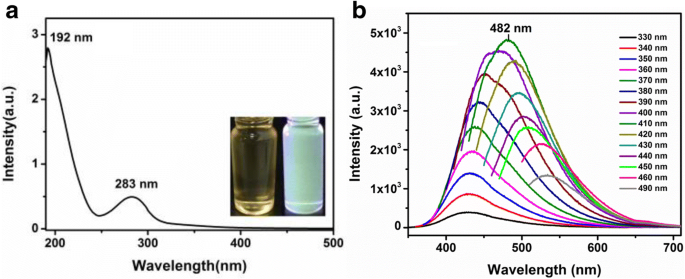
un Espectros de absorción UV-Vis de CQD, recuadro:imágenes ópticas bajo la luz del día (izquierda) y luz UV (derecha). b Espectros PL de CQD a diferentes longitudes de onda de excitación
Al ser no tóxicos y respetuosos con el medio ambiente, los CQD se consideran alternativas a los puntos cuánticos semiconductores para su aplicación en sistemas biológicos tanto in vitro como in vivo. Las CQD sintetizadas se aplicaron en una imagen óptica de células epidérmicas de cebolla como se muestra en la Fig. 5. La microscopía de fluorescencia revela que las paredes celulares y el núcleo celular de las células epidérmicas internas de la cebolla se pueden ver claramente, bien colocadas y bien colocadas. fuerte en sentido tridimensional. Los resultados muestran que la tinción y la formación de imágenes de puntos cuánticos de carbono son excelentes y no tienen ningún efecto adverso sobre los organismos y no se observan daños morfológicos de las células, lo que demuestra aún más CQD con baja citotoxicidad. La imagen confocal de la Fig. 5 indica que las CQD sintetizadas a partir del jugo de limón se pueden utilizar en la obtención de imágenes de células vegetales como indicadores fluorescentes, mostrando además las aplicaciones potenciales de las imágenes biológicas de las CQD.
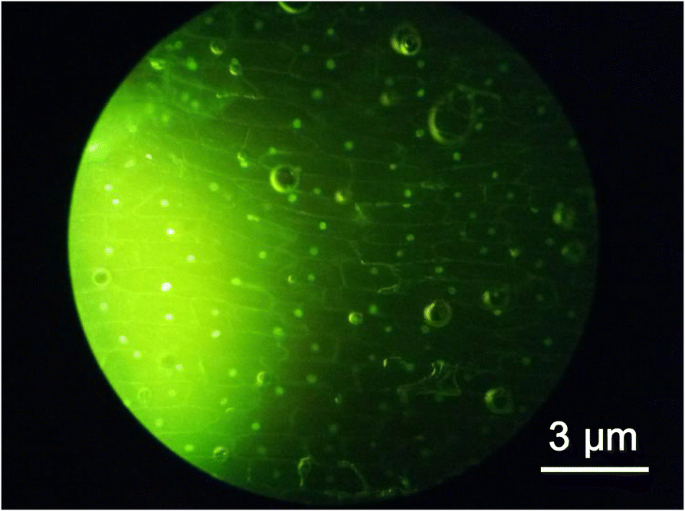
Una imagen óptica de células epidérmicas de cebolla teñidas con CQD iluminadas por una fuente de luz azul
Conclusiones
En este estudio, los puntos cuánticos de carbono fluorescentes solubles en agua se han sintetizado utilizando jugo de limón como recurso de carbono mediante una fácil reacción hidrotermal. Estos CQD tienen buenas propiedades ópticas y de material. Pueden emitir fluorescencia de color azul verdoso brillante bajo irradiación de luz ultravioleta o azul. Hemos demostrado que los CQD se pueden utilizar en la obtención de imágenes de células vegetales. Esperamos que estos hallazgos importantes y significativos puedan ayudarnos a obtener una comprensión profunda de las CQD y a explorar aplicaciones más prácticas de las nuevas nanoestructuras basadas en carbono.
Abreviaturas
- CQD:
-
Puntos cuánticos de carbono
- FFT:
-
Transformada rápida de Fourier
- HPLC:
-
Cromatografía líquida de alto rendimiento
- PL:
-
Fotoluminiscencia
- QLED:
-
LED de punto cuántico
- QY:
-
Rendimiento cuántico
- R-CD:
-
Puntos de carbono emisores de rojo
- TEM:
-
Microscopio electrónico de transmisión
- UV-Vis:
-
Ultravioleta visible
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X
Nanomateriales
- El reordenamiento atómico de múltiples pozos cuánticos basados en GaN en gas mixto H2 / NH3 para mejorar las propiedades estructurales y ópticas
- Modulación de las propiedades de anisotropía óptica y electrónica de ML-GaS por campo eléctrico vertical
- Síntesis fácil y propiedades ópticas de nanocristales y nanovarillas de selenio pequeños
- Síntesis de puntos cuánticos de carbono codopados N, S ricos en piridínicos como imitadores enzimáticos eficaces
- Características ópticas y eléctricas de los nanocables de silicio preparados por grabado electrolítico
- Un enfoque simple para sintetizar puntos cuánticos de carbono fluorescente de aguas residuales de tofu
- Síntesis de puntos cuánticos de sulfuro de antimonio solubles en agua y sus propiedades fotoeléctricas
- Síntesis sonoquímica de un solo paso y propiedades fotocatalíticas fáciles de compuestos de puntos cuánticos de grafeno / Ag3PO4
- Propiedades microestructurales, magnéticas y ópticas de las nanopartículas de perovskita manganita La0.67Ca0.33MnO3 sintetizadas mediante el proceso Sol-Gel
- Síntesis y propiedades de puntos cuánticos de CdTe de aleación de Mn emisor de azul soluble en agua
- Monocapa de g-GaN adsorbido por metales alcalinos:funciones de trabajo ultrabajo y propiedades ópticas



