Nueva detección de fluorescencia por inmunosensibilidad del fragmento de citoqueratina-19 de marcador tumoral (CYFRA 21-1) a través de nanocompuestos de óxido de zinc / puntos cuánticos de carbono
Resumen
La detección rápida de cáncer de pulmón en etapas tempranas utilizando el fragmento de antígeno citoqueratina-19 (CYFRA 21-1) como marcador tumoral en suero humano juega un papel importante en la supervivencia de los pacientes y en la reacción quirúrgica rápida. Este estudio tuvo como objetivo emplear el nanocompuesto de óxido de zinc conjugado con puntos cuánticos de carbono sintetizado verde como una solución inmunosensora de fluorescencia altamente sensible para la determinación rápida del antígeno CYFRA 21-1 en suero humano. El método sugerido se llevó a cabo aplicando un método hidrotermal para preparar puntos cuánticos de carbono utilizando Citrus lemon pericarpio. Los puntos cuánticos de carbono formados se utilizaron en la reducción y estabilización de acetato de zinc para sintetizar puntos cuánticos de carbono-nanocompuesto de óxido de zinc. Para formar un sistema inmunosensible anticuerpo-antígeno-anticuerpo de recubrimiento sándwich, se atrapó un antígeno CYFRA 21-1 inmovilizando un anticuerpo monoclonal no conjugado BM 19.21 en la superficie de nanocompuesto de puntos cuánticos de carbono-óxido de zinc y otro anticuerpo monoclonal KS 19.1, que se revistió sobre la superficie del pocillo de microtitulación. Este sistema tiene una característica de fluorescencia sintonizable registrada en la excitación y emisión de λ ex =470 y λ em =520 nm, respectivamente. El sistema de inmunosensibilidad de fluorescencia de nanocompuestos sugerido mostró una relación lineal de 0,01 a 100 ng mL −1 con un límite de detección de 0,008 ng mL −1 . El sistema de inmunosensibilidad sugerido basado en nanocompuestos de óxido de zinc y puntos cuánticos de carbono proporciona un enfoque prometedor para el diagnóstico rápido de cáncer de pulmón mediante la detección de CYFRA 21-1 en suero humano.
Introducción
El cáncer de pulmón es el tipo de cáncer más público y agresivo con grandes desafíos en el tratamiento médico. La recurrencia del tumor y la metástasis se consideran las principales causas de muerte en los pacientes con cáncer de pulmón [1]. El fragmento de citoqueratina 19 del marcador tumoral (CYFRA 21-1) es un fragmento que existe en muchas células epiteliales tanto normales como malignas [2]. Puede estimarse mediante un ensayo inmunorradiométrico tipo sándwich. Los primeros estudios aclararon que en las etapas malignas del cáncer de pulmón, CYFRA 21-1 se libera en la circulación sanguínea de los pacientes y se eleva en su suero [3]. Por lo tanto, es posible mejorar la supervivencia de los pacientes con cáncer de pulmón mediante la detección temprana y, en consecuencia, una rápida reacción quirúrgica [4].
Anteriormente se informaron pocas técnicas para la detección de CYFRA 21-1, incluido el inmunoensayo enzimático [5], el inmunoensayo de electroquimioluminiscencia [6] y el ensayo inmunorradiométrico [7] . Una estrategia ventajosa para aumentar y mejorar la sensibilidad de CYFRA 21-1 en el suero humano sigue siendo una preocupación.
En los últimos años, se han logrado importantes avances y un crecimiento explosivo de la nanotecnología en casi todos los campos de la vida [8]. Entre esos campos se encuentran los sistemas de administración de fármacos [9], el análisis farmacéutico [10], las reacciones de actividad catalítica [11], las aplicaciones medicinales [12], los marcadores tumorales de cáncer [13] y la obtención de imágenes de tejidos [14].
Hoy en día, las técnicas de detección basadas en fluorescencia (FL) han atraído a muchos investigadores debido a su diseño simple y excelente sensibilidad. Se han diseñado y sintetizado varios materiales sensoriales de FL para el seguimiento biológico. Los sistemas FL para la determinación biológica son altamente luminiscentes, dispersables en agua, químicamente estables y no tóxicos [15]. Existen varias sondas inmunosensibles basadas en fluorescencia para la detección de biomarcadores. El ensayo competitivo heterogéneo se realiza inmovilizando moléculas de captura en la superficie y luego se incuban con biomarcadores conjugados con fluoróforos. La competencia entre los biomarcadores libres y conjugados para unirse a las moléculas de captura disminuye la intensidad de la fluorescencia con la concentración de biomarcadores [16]. El ensayo sándwich heterogéneo se basa en la incubación de moléculas de captura y solución de interés formando un complejo con biomarcadores. En consecuencia, la intensidad de la fluorescencia aumenta con la concentración de biomarcadores [17].
En el ensayo competitivo homogéneo, dos moléculas de captura conjugadas con fluoróforo A diferentes conjugadas con biomarcadores conjugados con fluoróforo B y la solución aumenta la fluorescencia con concentraciones de biomarcadores [18]. Sin embargo, esas técnicas mostraron ciertos inconvenientes, incluido su largo tiempo experimental, la falta de detección multiplexada, la complejidad y, a veces, resultados relativamente falsos. Los avances en nanotecnología permitieron a los investigadores desarrollar nuevas sondas inmunosensibles de fluorescencia con características ópticas únicas [19]. Desde el primer uso de puntos cuánticos en la detección de biomoléculas, han ganado un gran interés ya que sus características ópticas proporcionan una gran flexibilidad en la selección de la longitud de onda adecuada, excelentes etiquetas para detección multiplexada, biocompatibilidad y capacidad de focalización [20].
Los puntos cuánticos de carbono (CQD) han demostrado excelentes propiedades químicas, físicas, ópticas, magnéticas y eléctricas. Las CQD se pueden sintetizar utilizando diferentes técnicas, incluidos los métodos hidrotermal, electrooxidación, ablación láser y microondas [21,22,23,24]. Debido a sus características de baja toxicidad, los investigadores científicos consideraron a los CQD como candidatos poderosos en muchas sondas fluorescentes. Además, tienen una gran capacidad para manipular a través de diferentes reacciones químicas controlables en diversas demandas, como sistemas bioquímicos, fotoquímicos, biosensores, de bioimagen y de administración de fármacos [25, 26, 27], así como en la detección de inmunoensayos [28]. Estudios anteriores sobre la síntesis de CQD revelaron ciertas desventajas al usar costosas fuentes de carbono, químicos y reactivos tóxicos, o al usar procesos no selectivos [29]. Para restringir esas desventajas, los investigadores comenzaron a utilizar jugos de frutas como una fuente nueva y barata de carbono [30]. Dado que el uso de zumos de frutas no proporciona el objetivo óptimo de utilizar los recursos, recientemente se obtuvieron CQD fluorescentes a partir de cáscaras de frutas [31]. El uso de cáscaras de frutas proporciona una ruta prometedora para la síntesis ecológica y ecológica de CQD.
El óxido de zinc (ZnO) es uno de los óxidos metálicos más importantes, potencialmente activos, estables y poco tóxicos que se utilizan ampliamente en dispositivos láser ultravioleta, campo biomédico, varios tipos de sensores y fotocatálisis [32,33,34,35]. Las nanopartículas de ZnO (ZnONP) mostraron propiedades fotoluminiscentes cerca de los rangos de espectro UV y Vis. Esto se puede atribuir a la emisión excitónica que se basa en la recombinación directa de pares de agujeros de electrones [36] o debido a la emisión verde-amarilla a 520 nm como resultado de la transición electrónica del borde de la banda de conducción a un nivel de trampa. [37].
Generalmente, los puntos de carbono son nanopartículas cuasi esféricas amorfas o nanocristalinas que contienen sp 2 y sp 3 carbono, grupos basados en O / N y grupos químicos modificados posteriormente. Además, los CQD tienen la capacidad de excitar con longitudes de onda más altas y pueden cambiar la eficacia de las superficies combinadas de los pares de agujeros de electrones y tratan la extinción en los sistemas analizados, lo que puede facilitar la determinación cuantitativa de biomoléculas [38]. Tienen la capacidad de ser decoradas con óxidos metálicos como TiO 2 y ZnO para formar nanocompuestos ópticamente activos que se pueden explotar en la detección de biomarcadores en suero humano. El ZnO es un material de banda prohibida amplia (3,37 eV), que puede ser luminiscente en las regiones ultravioleta y azul de la luz visible debido a la presencia de una gran densidad de niveles de defectos en la banda prohibida [39]. La formación de nanocompuestos de CQD / ZnO aumenta la absorción de luz visible debido a la hibridación de ZnO con CQD, y el cambio de azul en la absorción de luminiscencia a 520 nm puede atribuirse a la recombinación radiativa de vacantes de O ionizado. Además del aumento de la absorción de la luz visible, se puede considerar una mejor separación de los huecos de electrones y la reducción del tiempo de transferencia de electrones interfaciales para el mayor rendimiento óptico de las CQD hibridadas con nanopartículas de ZnO [40]. Además, el aumento significativo de radicales –OH *, generado a partir de nanocompuestos CQD / ZnO en la interfaz de agua, puede causar una elevación significativa en las señales de fluorescencia del sistema de análisis. Así, el nanocompuesto combinado de CQDs / ZnO mejora la modificación de las propiedades optoelectrónicas y fotoluminiscentes de la superficie de ZnO y produce un fuerte defecto superficial con fotoluminiscencia sintonizable [41]. Además, las CQD inmovilizadas con anticuerpos de bioreconocimiento que forman un sistema de detección de FL anticuerpo-antígeno-anticuerpo proporcionan una sonda viable con alta especificidad y sensibilidad para el analito diana [42].
El estudio sugerido propuso un nuevo sistema de detección de fluorescencia de inmunoensayo simple y ultrasensible basado en CQD decoradas con nanocompuesto de ZnO para determinar el marcador tumoral CYFRA 21-1 en suero humano. Se empleó pericarpio de limón cítrico como precursor de carbono para derivar CQD utilizando condiciones hidrotermales. Además, se utilizó como agente reductor y estabilizador para la síntesis de nanocompuestos de ZnO conjugado con CQD. El nanocompuesto de CQD / ZnO preparado se inmovilizó mediante un anticuerpo monoclonal (mAb) BM 19.21 no conjugado y los pocillos de microtitulación se recubrieron con otro anticuerpo monoclonal KS 19.1 para formar un sistema de inmunosensibilidad de taponado sándwich.
Métodos
Instrumentos
Los espectros espectrofotométricos tanto de CQD como de nanocompuestos de CQD / ZnO se registraron utilizando un espectrofotómetro Ultrospec 2100-Biochrom (Biochrom Ltd., Cambium, Cambridge, Reino Unido). La morfología de la superficie y la distribución del tamaño de partícula de los CQD sintetizados en verde y el nanocompuesto CQDS / Zn se evaluaron utilizando un microscopio electrónico de transmisión (TEM), un instrumento modelo JEOL 1200EX (JEOL Ltd., Freising, Alemania) y un microscopio electrónico de barrido (SEM) modelo JSM-7610F. (JEOL, Estados Unidos). Los espectros de fluorescencia y de infrarrojos por transformada de Fourier (FT-IR) del sistema de inmunosensibilidad sugerido se verificaron utilizando un lector multimodo Biotek Synergy H1 (Biotek, Tokio, Japón) y un espectrofotómetro Perkin Elmer FT-IR (PerkinElmer Ltd., Yokohama, Japón) , respectivamente. Los espectros Raman, la espectroscopía de fotoelectrones de rayos X (XPS) y el patrón de difracción de rayos X en polvo (XRD) se midieron utilizando un espectrómetro micro-Raman (CRAIC Technologies, CA, EE. UU.), El sistema de espectroscopía de rayos X Kratos Axis Ultra (Kratos Analytical Ltd. , Manchester, Reino Unido) y el difractómetro Siemens D-5000 (Siemens, Erfurt, Alemania), respectivamente.
Productos químicos y reactivos
Se utilizó el instrumento SG-2000-10090 (Barsbuttel, Alemania) para adquirir el agua desionizada utilizada en todos los experimentos. Los anticuerpos monoclonales no conjugados (mAb) de CYFRA 21-1 BM 19.21 y KS 19.1 para formar el sistema de inmunosensores de protección en sándwich se obtuvieron de Abcam (Cambridge, Reino Unido). Limón cítrico las frutas fueron abastecidas por los mercados locales. Se preparó solución salina tamponada con fosfato (PBS) de pH =7,4 usando cloruro de sodio, cloruro de potasio, hidróxido de sodio, fosfato monopotásico y fosfato disódico (BHD Ltd. Co. Poole, Reino Unido). Randox Laboratories (Irlanda del Norte-Reino Unido) proporcionó amablemente los sueros comerciales normales. Se recolectaron muestras de sangre al azar de voluntarios sanos y, antes de comenzar este estudio, se obtuvo un consentimiento informado. Además, Sigma-Aldrich (Hamburgo, Alemania) suministró un grado puro de clorhidrato de carbodiimida (EDC) y N-hidroxisuccinimida (NHS). El comité de ética de la investigación de la Universidad King Saud, KSA (KSU-REC-002-E, 2019) aprobó el estudio.
Preparación hidrotermal verde de puntos cuánticos de carbono (CQD)
Limón cítrico se empleó pericarpio para sintetizar CQD en condiciones hidrotermales. Aproximadamente 20 g de Citrus lemon Se transfirieron pericarpio y 200 mL de agua desionizada a un matraz redondeado y se sometieron a reflujo a 100 ° C bajo agitación magnética continua durante 6 h. Después de enfriar a temperatura ambiente, el extracto resultante se centrifugó a 3500 rpm y 20 ml de la solución extraída superior se esterilizó en autoclave y se calentó en condiciones hidrotermales en el rango de temperatura de 100 a 200 ° C para diferentes intervalos de 6 a 120 h. Después de enfriar a temperatura ambiente, el licor superior representa los CQD (esquema 1).
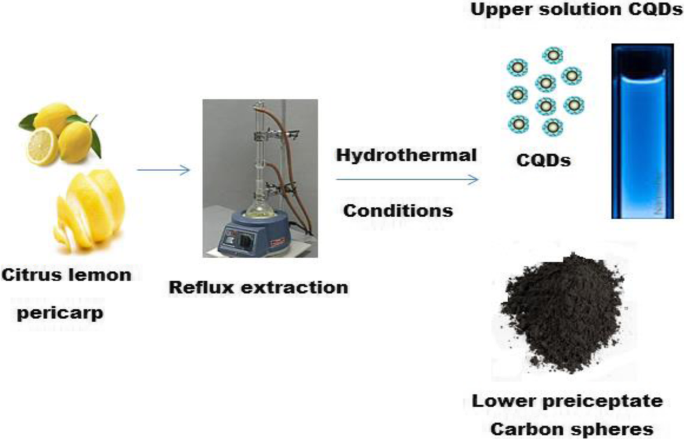
Síntesis verde de CQD utilizando Citrus lemon pericarpio a solución CQD fluorescente y esferas de carbono
Preparación de nanocompuesto de óxido de zinc y puntos cuánticos de carbono
Para preparar nanocompuestos de CQD / ZnO, se realizó una reacción de reducción química simple utilizando CQD como agente reductor y estabilizador. El nanocompuesto de CQD / ZnO se obtuvo agregando 20 mL de CQD a 50 mL de 5.0 × 10 −2 mol L −1 de acetato de zinc a 60 ° C con agitación continua durante 10 min. Cuando el color de la mezcla cambió de amarillento a cremoso, la mezcla se dejó a un lado durante 30 min para completar el proceso de reducción y se almacenó a 4 ° C. Para asegurar la estabilidad y comprobar la aglomeración del nanocompuesto de CQD / ZnO preparado, se empleó espectrometría UV-Vis para registrar la absorbancia en 20 días a 390 nm. Los resultados de los resultados revelaron una alta estabilidad y ningún cambio significativo en la absorbancia del nanocompuesto de CQD / ZnO.
Caracterización del nanocompuesto de óxido de zinc y puntos cuánticos de carbono
Para asegurar la formación de nanocompuestos CQDs / ZnO, se utilizaron diferentes técnicas microscópicas y espectroscópicas. La uniformidad y morfología de la superficie de CQD y nanocompuestos CQD / ZnO se estudiaron utilizando microscopio electrónico de transmisión de alta resolución (HRTEM) y SEM. Los espectros ópticos se estudiaron mediante espectroscopía UV-Vis, FT-IR, XPS y Raman. La estructura cristalina de las CQD preparadas se evaluó utilizando un patrón XRD.
Proceso de inmovilización
Se inmovilizó un anticuerpo monoclonal BM 19.21 no conjugado sobre la superficie del nanocompuesto de CQD / ZnO sintetizado mediante un enlace amida peptídico simple entre la amina y los grupos carboxílicos activos. El proceso de inmovilización se realizó agregando 5.0 mL de cada equimolar 3.0 × 10 −3 mol L −1 NHS y EDC a 5.0 mL de solución nanocompuesta CQDs / ZnO bajo agitación continua durante 1 h. Se disolvieron aproximadamente 5 mg de anticuerpo monoclonal BM 19.21 no conjugado en 1,0 ml de 0,01 mol de L −1 solución salina tamponada con fosfato (pH =7,4) y se añadió a la solución de detección anterior. El anticuerpo monoclonal BM 19.21 no conjugado se inmovilizó sobre la superficie de una solución de nanocompuesto de CQDs / ZnO después de la incubación a 37ºC durante 12 h (esquema 2). Se utilizó espectrofotometría para confirmar el éxito del proceso de inmovilización.
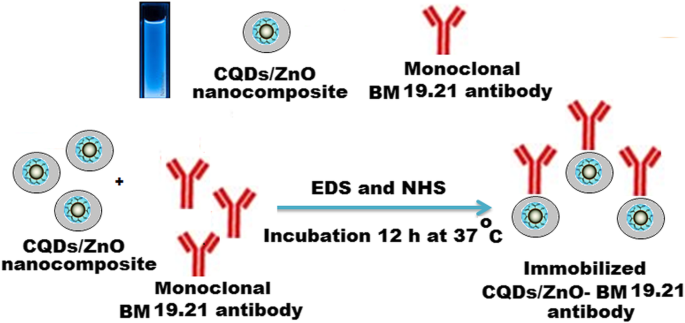
Inmovilización de anticuerpo monoclonal BM 19.21 en la superficie de nanocompuestos de CQD / ZnO
Principio general del método de inmunoensayo
Se obtuvo una reacción de taponamiento sándwich anticuerpo-antígeno-anticuerpo usando otro anticuerpo monoclonal KS 19.1 que recubre la superficie de los pocillos de microvaloración (esquema 3). En condiciones óptimas de inmunoensayo, la concentración de antígeno CYFRA 21-1 se determinó en función de un aumento en la intensidad de la señal de fluorescencia.
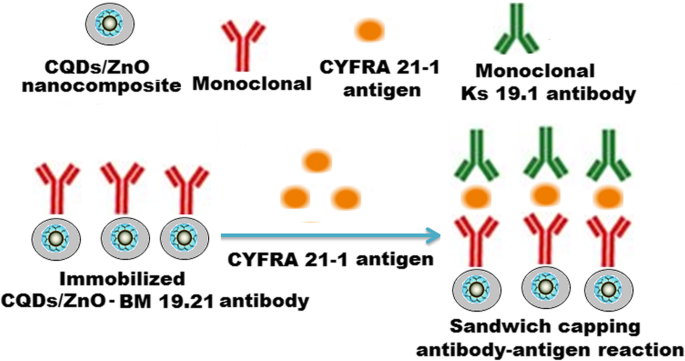
El esquema ilustrado representa una reacción anticuerpo-antígeno-anticuerpo inmunosensible que cubre un sándwich
El procedimiento de inmunosensibilidad
La colección de muestras de sueros humanos fue proporcionada por voluntarios al azar. Se aseguró la coagulación completa antes de la centrifugación a temperatura ambiente y se almacenó a 4 ° C. La técnica de adición se utilizó para preparar muestras estándar que contenían el antígeno CYFRA 21-1 en el rango de concentración de 0,01 a 500 ng ml −1 . Aproximadamente 50 μL de las muestras enriquecidas se dispensaron en pocillos de microvaloración y se mezclaron con 50 μL de anticuerpo monoclonal KS 19.1 recién diluido utilizando solución salina tamponada con fosfato de pH =7,4 durante 30 min y luego se incubaron sin cubrir la placa durante 1 ha 37 ° C. El contenido de los pocillos se agitó enérgicamente y los pocillos se enjuagaron tres veces con agua desionizada (300 μL) para cada pozo. Aproximadamente 50 μL de la solución de nanocompuesto CQDs / ZnO-BM 19.21 inmovilizados se agregaron a cada pocillo, se mezclaron suavemente y se incubaron durante 30 min a 37 ° C. Las muestras preparadas se sometieron a análisis de fluorescencia utilizando un lector de microtitulación para registrar las intensidades.
Resultados y discusión
Evaluación morfológica de puntos cuánticos de carbono y su nanocompuesto
Se utilizó un microscopio electrónico de transmisión (TEM) para caracterizar la morfología de la superficie y la distribución de CQD en las muestras. Para realizar el examen bajo TEM, aproximadamente 4 μL de la suspensión de CQD preparada se dejaron caer sobre la superficie de la rejilla de carbono de TEM. En la imagen HRTEM (Fig. 1a), los puntos negros uniformes observados con espaciado de celosía (0,36 nm) indicaron la formación de CQD. Se trazó un gráfico de distribución del tamaño de partícula y el tamaño medio de partícula varió de 1,5 ± 0,5 a 5,0 ± 0,5 nm (Fig. 1b). El tamaño de partícula obtenido demostró que los CQD formados son de hecho nanomateriales de tamaño cuántico. Además, se llevó a cabo una dispersión de luz dinámica (DLS) y se encontró que el tamaño medio de partícula era ~ 20 ± 0,2 nm. Se observó una diferencia entre las dos mediciones anteriores. Estudios anteriores revelaron que HRTEM no muestra la estructura de red cristalina de los CQD formados a mayores aumentos debido a su naturaleza amorfa [43]. De manera similar, en este estudio, el precursor natural del carbono es Citrus lemon el pericarpio y las CQD derivadas también exhibieron naturaleza amorfa. Por lo tanto, la diferencia en las mediciones del tamaño de las partículas se puede atribuir a la aglomeración de los CQD formados, la naturaleza amorfa de los puntos de carbono formados, el mecanismo involucrado en cada experimento y la dinámica de hidratación de las partículas.
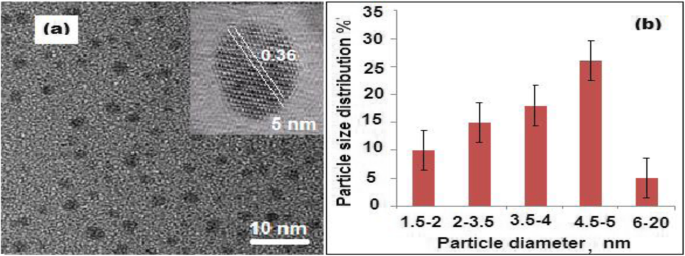
un Imagen de microscopio electrónico de transmisión de alta resolución (HRTEM) de CQD con un diámetro de 5 nm y b gráfico de distribución de tamaño de los CQD basado en el TEM
El nanocompuesto de CQDs / ZnO preparado se investigó usando TEM y SEM. En la imagen TEM (Fig. 2a), la presencia de partículas hexagonales unidas a CQD indica la formación de nanocompuestos CQD / ZnO. En SEM, la muestra de nanocompuesto se recubrió con oro para evitar la absorción de electrones por parte de la muestra y la acumulación de carga. El voltaje acelerado aplicado fue de 15 kV con un aumento de × 30.000 (Fig. 2b).

un y b representar las imágenes de microscopio electrónico de transmisión y microscopio electrónico de barrido de nanocompuestos de CQD / ZnO
Se estudiaron los espectros UV-Vis y de fluorescencia de CQD, y los espectros registrados mostraron dos picos significativos a 224 y 280 nm que se pueden atribuir a p ~ p * y n ~ P * transición de C =C y C =O, respectivamente. Además, el espectro de fluorescencia de los CQD mostró dos señales a un máximo de λ ex =360 y λ em =453 nm (Fig. 3a, b). Además, se estudió el espectro UV-Vis de los nanocompuestos de CQD / ZnO. Se observó un pico de absorción significativo a 370 nm que mostraba un desplazamiento azul verdoso (Fig. 4a). Se estudiaron las propiedades de fotoluminiscencia (PL) de los nanocompuestos de CQD / ZnO. El tamaño y los defectos superficiales de los CQD afectan en gran medida sus propiedades de luminiscencia. En función de la longitud de onda de excitación, se varió la emisión (PL) de CQD [38]. Además, las partículas nanométricas de ZnO exhibieron una emisión relacionada con defectos en la región visible de absorción de azul a verde [41]. Por lo tanto, los ZnONP decorados con CQD produjeron un excelente nanocompuesto para la emisión de PL. Como se muestra en la Fig. 4b, el espectro PL de CQDs / ZnO exhibió un desplazamiento al azul con un pico significativo a 520 nm después de una longitud de onda de excitación de 470 nm. El cambio observado se puede atribuir a la superposición entre las bandas de energía de CQD y ZnONP. El cambio azul mostrado estaba en el nivel de emisión de defectos 2.1 eV.
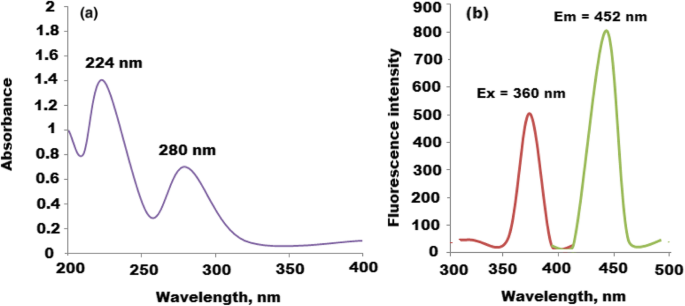
Espectros espectroscópicos de CQD ( a ) Espectro UV-Vis a 224 y 280 nm y ( b ) espectro de fluorescencia de CQD en λ ex =360 y λ em =452 millas náuticas
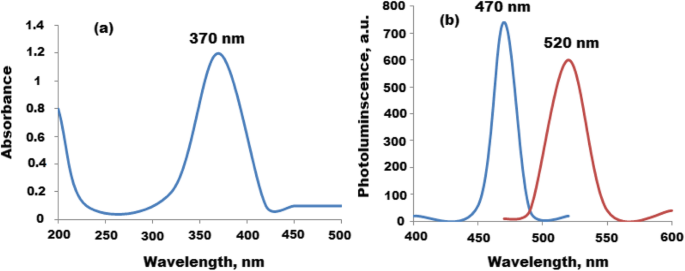
Espectros espectroscópicos de CQD / ZnONP a Espectro UV-Vis en el pico de absorción a 370 nm y b espectro de fotoluminiscencia de CQD / ZnONP en λ ex =470 y λ em =520 nm
Para confirmar la formación de nanocompuestos de CQD / ZnO y nanocompuestos de CQD / ZnO inmovilizados con anticuerpo monoclonal BM 19.21 no conjugado, se realizó un estudio comparativo FT-IR. El espectro FT-IR registrado de CQD reveló la presencia de diferentes picos distintos correspondientes a ciertos grupos funcionales, incluido el estiramiento de los picos vibratorios a 3462 cm −1 y 2932 cm −1 para los grupos C – OH y C – H, respectivamente. Además, se observaron tres bandas de absorción de vibraciones a 1749 cm −1 , 1375 cm −1 y 1246 cm −1 correspondiente a la presencia de grupos funcionales C =O, C – N y C – O – C, respectivamente (Fig. 5a). Un nuevo pico a 436 cm −1 correspondiente a un estiramiento de la banda de vibración de Zn – O se observó. Las propiedades reductoras y estabilizadoras de los CQD se obtuvieron de la presencia de grupos –OH y COOH en su superficie. Estos grupos funcionales actúan como donantes de electrones y tienen una fuerte afinidad hacia la formación de nanocompuestos de CQD / ZnO. Por lo tanto, los CQD redujeron y estabilizaron el nanocompuesto formado (Fig. 5b). Como se muestra en la Fig. 5c, se notó que se formaron dos nuevos picos a 3254 cm −1 y 1675 cm −1 . Estos picos se atribuyeron al estiramiento de la vibración de N – H y C =O, respectivamente, y confirmaron la inmovilización de CQD / ZnO-BM 19.21 a través de enlaces peptídicos.
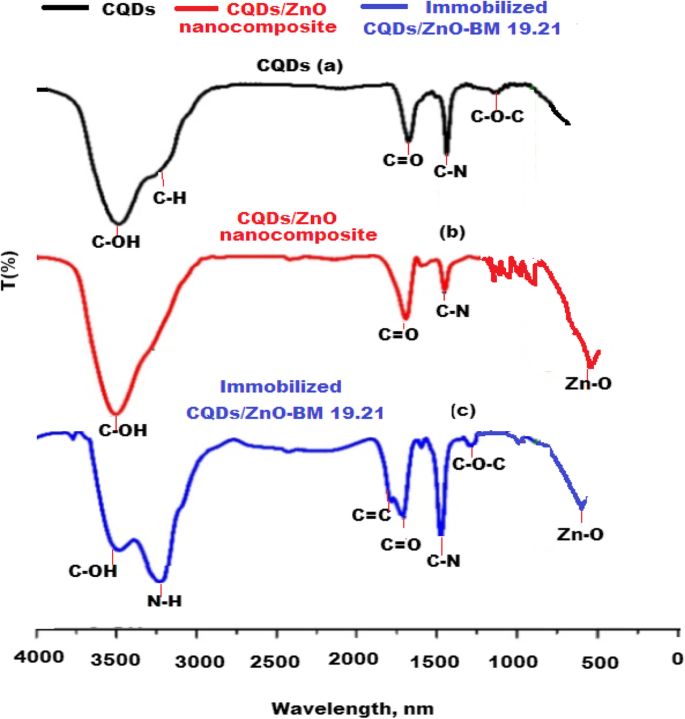
Espectros FT-IR de a CQD, b Nanocompuestos de CQD / ZnO y c CQD inmovilizados / nanocompuesto ZnO-BM 19.21
Se examinaron los espectros de espectroscopía de fotoelectrones de rayos X (XPS) de los CQD sintetizados en verde. El espectro obtenido de CQDs (Fig. 6a) mostró diferentes grupos funcionales a 288 y 286 eV para C =O y COOH, respectivamente. Además, se observaron dos picos de energía de enlace significativos a 1044,4 y 1021,5 eV para Zn 2p 1/2 y Zn 2p 3/2 , respectivamente (Fig. 6b). Además, el espectro XPS de alta resolución del nanocompuesto de CQD / ZnO confirmó la presencia de diferentes picos de energía de enlace a 560, 385, 350, 246 y 200 eV para O 1s, C 1s, Zn 3s, Zn 3p y Zn 3d. respectivamente (Fig. 6c). Todos los datos mencionados anteriormente demostraron la presencia de ZnO en la superficie de CQD que forman CQD / nanocompuesto de ZnO.
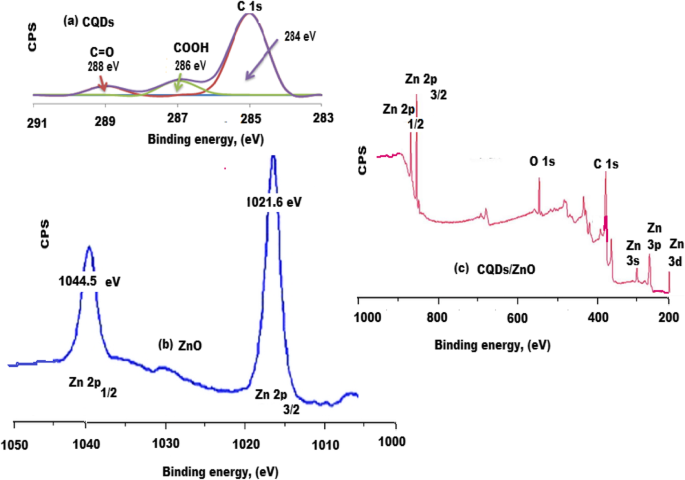
Espectros de espectroscopía de fotoelectrones de rayos X (XPS) de a CQD, b ZnO y c CQD / nanocompuesto de ZnO
Se realizó un estudio comparativo entre los patrones XRD de CQDs y CQDs / ZnO nanocomposite. Se observó un pico ancho a 20 ° (2Ɵ) para los puntos de carbono en el patrón XRD de los CQD (Fig. 7a). Sin embargo, se reconocieron diferentes picos agudos a 27 °, 32 °, 34 °, 45 °, 57 °, 64 °, 67 °, 70 °, 73 °, 78 ° y 80 ° (2Ɵ) para Zn (100), (002), (101), (102), (110), (103), (200), (112), (201), (004) y (202), respectivamente. Los picos observados reflejaron la distribución de ZnO en la superficie de los CQD que forman CQD / nanocompuesto de ZnO (Fig. 7b).
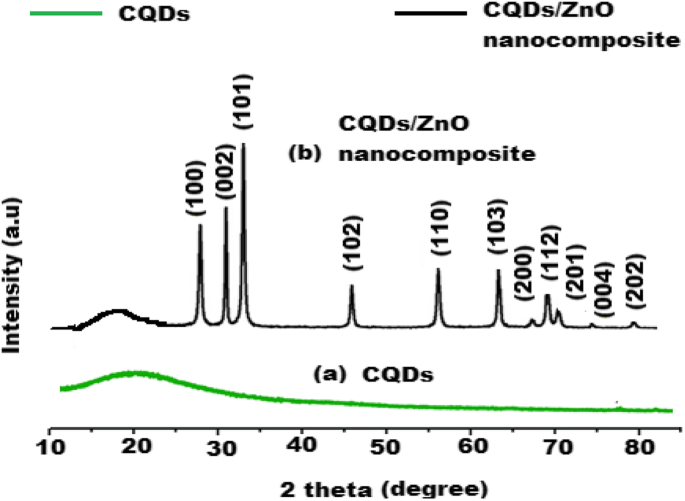
Patrón de difracción de rayos X de a CQD y b CQD / nanocompuesto de ZnO
Se estudiaron los espectros Raman de los CQD preparados, CQD / ZnO y nanocompuestos CQD / ZnO-BM 19.21 inmovilizados. Las señales Raman se utilizan comúnmente para estudiar la estructura cristalina y sus defectos. La Figura 8a, mostró dos bandas D y G típicas a 1300 y 1520 cm −1 para nanopartículas de carbono, respectivamente. Como se informó anteriormente, la banda D comúnmente representa sp 3 defectos, y la banda G es una característica de la vibración plana de sp 2 -carbonos enlazados [44]. El yo D / Yo G Se calculó la relación para los CQD preparados y se encontró que era 1,02 ± 0,03. Se observaron nuevos picos agudos a 440 y 520 cm −1 para nanopartículas de ZnO y los picos típicos de CQD se observaron a 1364 y 1595 cm −1 . La proporción de I D / Yo G se encontró que era 1,2 ± 0,01, lo que indica la formación de nanocompuestos de CQD / ZnO (Fig. 8b). El espectro Raman de nanocompuestos CQD / ZnO-BM 19.21 inmovilizados mostró numerosos picos que pueden reconocerse fácilmente como signos confirmatorios de estructuras secundarias y terciarias. Los picos observados en la región 1007–1128 cm −1 se asignaron para representar la estructura secundaria principal del anticuerpo monoclonal. El Raman alcanza un máximo de 550–682 cm −1 región se asignaron para representar conformaciones de disulfuro, mientras que 867-797 cm −1 se asignaron unos para representar el estado de enlace de hidrógeno de los residuos de tirosina. Además, el cambio significativo en el pico del espectro Raman a 1630 cm −1 puede atribuirse a la presencia de estructura terciaria del anticuerpo inmovilizado [45] (Fig. 8c). La proporción de I D / Yo G se incrementó a 1,4 ± 0,04 revelando una mejor estructura cristalina debido a la formación de CQD inmovilizados / nanocompuesto ZnO-BM 19.21.
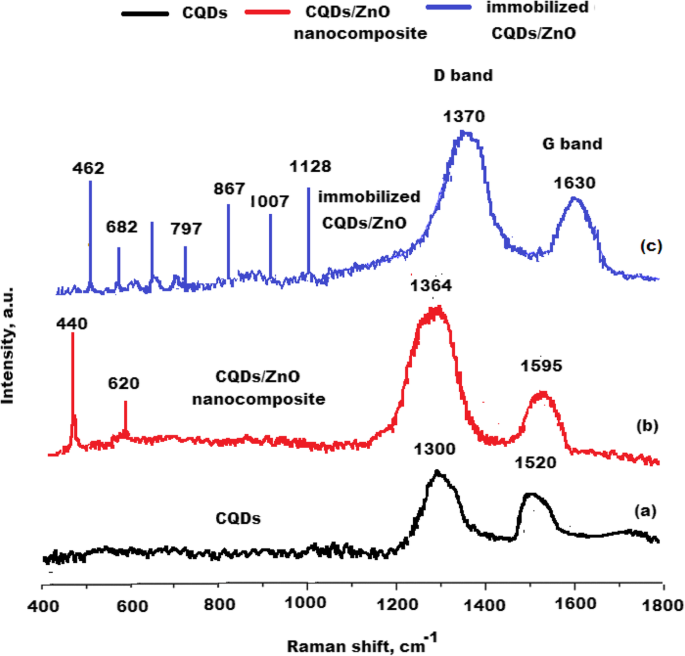
Desplazamiento del espectro Raman de a CQD, b Nanocompuestos de CQD / ZnO y c CQD inmovilizados / nanocompuesto ZnO-BM 19.21
Optimización de condiciones de inmunosensibilidad de fluorescencia
La selección y optimización de las condiciones de inmunosensibilidad de fluorescencia sugeridas se llevaron a cabo mediante el estudio de varios parámetros. Generalmente, la cantidad de nanocompuesto inmovilizado, el pH y la concentración del tampón usado, el tiempo de incubación entre el analito diana en las muestras de suero y los reactivos inmunosensibles deben investigarse y optimizarse. Para seleccionar la cantidad adecuada de nanocompuestos de CQD / ZnO-BM 19.21 inmovilizados, se probaron diferentes cantidades en el rango de 10 a 100 μl. La máxima intensidad de fluorescencia se observó añadiendo 50 μl del nanocompuesto CQD / ZnO-BM 19.21 inmovilizado (Fig. 9a). Se prepararon y probaron cuatro soluciones salinas tamponadas con fosfato con valores de pH de 7,2 a 7,5 y se analizaron en función de la intensidad de la fluorescencia. Se observó un ligero cambio en la intensidad de la señal de fluorescencia al cambiar los valores de pH. A pH 7,2 y 7,3, la señal de fluorescencia disminuyó debido a la inestabilidad química del nanocompuesto de CQD / ZnO inmovilizado. La señal de fluorescencia aumentó a un pH de 7,4 a 7,5 debido a la excelente interacción entre las moléculas monoclonales en la superficie del nanocompuesto (Fig. 9b). Se encontró que 7,4 es el valor de pH más adecuado para mantener la actividad del antígeno diana que puede descomponerse aumentando el pH más de 7,5. Por lo tanto, se seleccionó un pH de 7,4 para estudios adicionales.
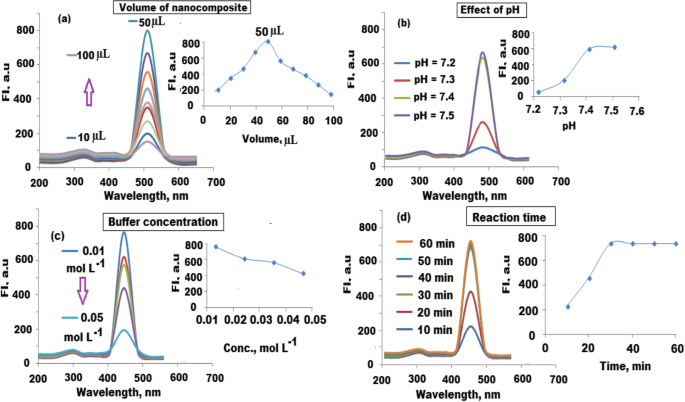
Optimización de la determinación de fluorescencia del antígeno CYFRA 21-1 en λ ex =470 y λ em =520 nm. un Efecto de CQD inmovilizados añadidos / nanocompuesto de ZnO-BM 19.21, b efecto de la solución salina tamponada con fosfato de pH entre 7,3 y 7,5, c efecto de la concentración de tampón usando PBS en el rango de concentración de 0.01–0.05 mol L −1 y d efecto del tiempo de inmunorreacción usando 10-60 min
La influencia de la concentración de solución salina tamponada con fosfato sobre la intensidad de la fluorescencia se estimó utilizando un rango de concentración de 0,01 a 0,05 mol L −1 . The maximum fluorescence intensity signal was obtained using the buffer concentration of 0.01 mol L −1 . At higher buffer concentrations, the immobilized CQDs/ZnO-BM 19.21 nanocomposite was aggregated, and the instability of the immunosensing solution may cause a decrease in fluorescence intensity (Fig. 9c). To calculate the immunoreaction time, the analytical procedure was repeated using reaction time ranging from 10 to 60 min. The maximum fluorescence intensity signal was observed by maintaining the reaction between the tested antigen and the immunosensing solution for at least 30 min (Fig. 9d).
Analytical Quantification
Under optimized conditions, the suggested immunoassay method was performed using 12 serum samples containing CYFRA 21-1 antigen in concentration range of 0.01–500 ng mL 1 . The outcome results were plotted to construct the calibration graph which was linear over a concentration range of 0.01–100 ng mL −1 with a detection limit of 0.008 ng mL −1 . The calculated equation was found to be I F = 7.933C + 181.24 (r 2 = 0.9992). After six repetitions, the percentage of the relative standard deviation (%RSD) was 1.3%. The acceptable results revealed a high sensitivity of the immunosensing fluorescence method for the quantification of CYFRA 21-1 antigen in serum samples.
System Suitability
System suitability was investigated by carrying out a comparative study between the suggested immobilized CQDs/ZnO-BM 19.21 immunosensing method and the previously addressed methods. The suggested fluorescence system provided significant advantages such as simplicity, eco-friendly, and easy to detect the target analyte in serum samples. The recorded results revealed high sensitivity with a wide linear detection range of 0.01–100 ng mL 1 and lower detection limit of 0.008 ng mL 1 (Table 1).
Accuracy, Precision, and Selectivity of the Immobilized Immunosensing System
To ensure the accuracy of the suggested immobilized CQDs/ZnO-BM 19.21 fluorescence immunosensing system for the determination of CYFRA 21-1 antigen in serum samples, 12 serum samples were tested. The outcome data were compared with another previously reported technique [6], which was based on electrochemiluminescence assay using tris 2,2′-bipyridyl ruthenium (II) complex to be excited by tripropylamine. Acceptable results were obtained as indicated in Table 2. Intra-day and inter-day assay were used to investigate the precision of the suggested method. The test was carried out using a serum sample containing 10 ng mL − 1 of CYFRA 21-1 antigen. The mean relative standard deviations were 1.1% and 1.3% for both intra- and inter-day assay, respectively, which revealed high precision. Furthermore, the selectivity of the suggested method towards the determination of CYFRA 21-1 antigen was evaluated using some possible interfering species such as amino acids (cysteine, lysine, serine, tyrosine, and glycine), some cations (K + , Na + , Ca 2+ , Mg 2+ , and Zn 2+ ) and some other bio-markers such as CA 15-3, CA 27-29, CA 19-9, and CA 125. The test was carried out under optimum conditions using human serum containing 10 ng mL −1 CYFRA 21-1 antigen in the presence of 10 ng mL −1 coexisting species. The outcome data were calculated as relative percentage error (Er%) and the corresponding result did not exceed ± 5% for each interfering species (Table 3). The calculated tolerance values (F-F 0 /F 0 ) were found to be with the tolerance limits (< 5%). Therefore, the suggested immobilized CQDs/ZnO-BM 19.21 immunosensing fluorescence system displayed high selectivity towards the determination of CYFRA 21-1 antigen in human serum.
Analysis of Real Specimens
In real human specimens, the suggested immunosensing fluorescence system based on immobilized CQDs/ZnO-BM 19.21 solution was exploiting to detect and quantify the percentage (%) recoveries of the tumor marker CYFRA 21-1 antigen. As previously mentioned in the immunosensing procedure, the suggested system was used to determine the CYFRA 21-1 antigen by finding the relationship between the fluorescence intensity and the concentration of CYFRA 21-1 antigen in serum samples. Certain amounts of the target antigen (0.5, 1.0, and 2.0 ng mL −1 ) were added to the estimated samples, and the increase in signal intensities was evaluated. After six determinations, the percentage relative standard deviations (%RSD) were calculated. The outcome percentage recoveries were found to be ranged from 96.7 ± 0.7 to 100.0 ± 1.3%. The calculated %RSD was in the range of 0.2–1.4%. The tested serum samples were analyzed using a previously reported method [6] and the percentage recoveries were found to be ranged from 96.1 ± 1.6 to 100.0 ± 0.4% with %RSD 0.3–1.7%. In order to ensure the suitability of the suggested immunosensing fluorescence technique using an immobilized CQDs/ZnO-BM 19.21 solution, a comparative statistical study using Student’s t test and F test [46] was carried out between the present results and those obtained by others from previously conducted methods (Table 4). The obtained t test and F test values were found to be ranged from 0.354 to 2.181 (2.228)* and 1.16 to 4.0 (5.05)* with respect to the tabulated values of P = 0.05, respectively. The results revealed good agreement between the suggested method and the previously published procedures. Also, all detected quantities of CYFRA 21-1 antigen in serum samples were within the normal limit indicating no lung cancer was diagnosed in the investigated serum samples.
Conclusion
The present study concerned with the preparation of green synthesis CQDs conjugated with ZnO nanocomposite using Citrus lemon as a precursor. The CQDs/ZnO nanocomposite was employed to form a new fluorescence immunosensing system by immobilizing a monoclonal BM 19.21 antibody through simple peptide bonds. The highly sensitive fluorescence system was used to determine the tumor marker of lung cancer (CYFRA 21-1) in human serum. CYFRA 21-1 antigen was determined via sandwich capping antibody-antigen-antibody reaction using another monoclonal antibody KS 19.1 coating the microtiter wells. The unique features and high sensitivity of the suggested system facilitate the determination of the target tumor marker with high stability and reproducibility. A comparative study was carried out and the outcome results confirmed the suitability and high sensitivity of the suggested immunosensing system, and the results were in agreement with a previously reported conventional technique.
Disponibilidad de datos y materiales
The only outcome data from this study was presented in the manuscript.
Abreviaturas
- %RSD:
-
Percentage relative standard deviation
- BM 19–21:
-
Specific monoclonal antibody
- CQD:
-
Puntos cuánticos de carbono
- CQDs/ZnO:
-
Carbon quantum dots/zinc oxide
- CYFRA-21-1:
-
Cytikeratin-19 fragment
- DLS:
-
Dispersión de luz dinámica
- EDC:
-
Carbodiimide hydrochloride
- eV:
-
Electron volt
- FT-IR:
-
Infrarrojos por transformada de Fourier
- HRTEM:
-
Microscopio electrónico de transmisión de alta resolución
- KS 19-1:
-
Monoclonal cytokeratin 19-specific antibody
- Ltd. Co:
-
Limited company
- mAb:
-
Monoclonal antibody
- NHS:
-
N-hidroxisuccinimida
- P:
-
Degree of confidence
- PBS:
-
Solución salina tamponada con fosfato
- SEM:
-
Microscopio electrónico de barrido
- TEM:
-
Microscopio electrónico de transmisión
- UK:
-
Unite Kingdom
- USA:
-
United States of America
- UV-Vis:
-
Ultravioleta visible
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X en polvo
- ZnO:
-
Óxido de zinc
- ϴ:
-
Theta degree
- λmax :
-
Wavelength
Nanomateriales
- Puntos de carbono luminiscentes azules independientes de excitación de alta eficiencia
- Síntesis de puntos cuánticos de carbono codopados N, S ricos en piridínicos como imitadores enzimáticos eficaces
- Nanodots de carbono como nanosensores de modo dual para la detección selectiva de peróxido de hidrógeno
- Puntos cuánticos de bismuto en pozos cuánticos de GaAsBi / AlAs recocidos
- Fabricación y caracterización de un nuevo catalizador anódico compuesto de nanofibras de carbono Tio2 para celdas de combustible de metanol directo mediante el método de electrohilado
- Un enfoque simple para sintetizar puntos cuánticos de carbono fluorescente de aguas residuales de tofu
- Síntesis de puntos cuánticos de sulfuro de antimonio solubles en agua y sus propiedades fotoeléctricas
- Material y propiedades ópticas de los puntos cuánticos de carbono fluorescente fabricados a partir de jugo de limón mediante una reacción hidrotermal
- Propiedades de las nanopartículas de óxido de zinc y su actividad contra los microbios
- Ajuste del modo de movimiento deslizante de los nanotubos de carbono mediante grupos de hidroxilo
- Síntesis y propiedades de puntos cuánticos de CdTe de aleación de Mn emisor de azul soluble en agua



