Aplicación multifuncional de nanocompuesto de óxido acoplado de Zn – Fe – Mn con ayuda de PVA
Resumen
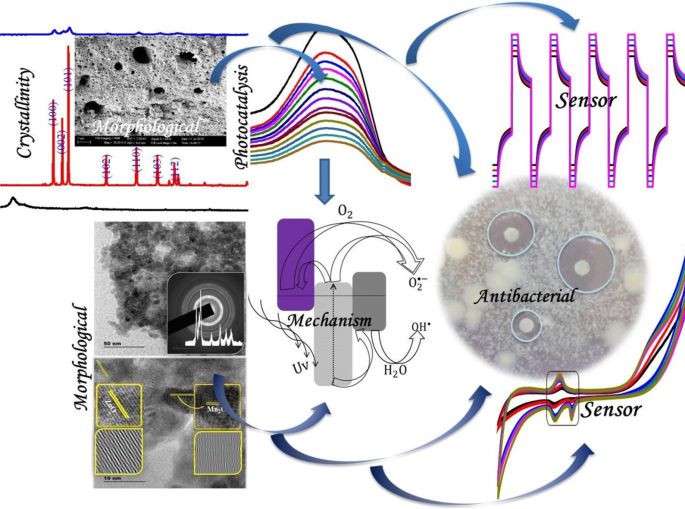
El óxido de zinc (ZnO) es un material semiconductor fascinante con muchas aplicaciones, como adsorción, fotocatálisis, sensores y actividades antibacterianas. Mediante el uso de un polímero de poli (alcohol vinílico) (PVA) como agente de remate y óxidos metálicos (hierro y manganeso) como pareja, se sintetizó el material nanocompuesto de óxido ternario de Zn / Fe / Mn asistido por PVA poroso (PTMO-NCM). Las propiedades térmicas, ópticas, de cristalinidad, de enlace químico, de porosidad, morfológicas y de transferencia de carga de los materiales sintetizados fueron confirmadas por DTG / DSC, UV-Vis-DRS, XRD, FT-IR, BET, SEM-EDAX / TEM-HRTEM- SAED, y CV / EIS / técnicas analíticas amperométricas, respectivamente. El PTMO-NCM mostró un área de superficie mejorada y capacidad de transferencia de carga, en comparación con ZnO. Usando el patrón XRD y el análisis de imagen TEM, se confirmó que el tamaño cristalino de los materiales estaba en el rango nanométrico. La porosidad y las capacidades superiores de transferencia de carga del PTMO-NCM se confirmaron a partir del análisis BET, HRTEM (IFFT) / SAED y CV / EIS. La cinética de adsorción (reacción de adsorción / difusión de adsorción) y la prueba de isoterma de adsorción confirmaron la presencia de un tipo de quimisorción de interacción adsorbato / colorante azul de metileno-adsorbente / PTMO-NCM. El rendimiento fotocatalítico se probó con los tintes rojo Congo y naranja ácido-8. La capacidad superior de detección de ácido ascórbico del material se entendió a partir del análisis CV y amperométrico. Las nobles actividades antibacterianas del material también se confirmaron en bacterias gramnegativas y grampositivas.
Introducción
Las nanopartículas de óxido de zinc (NP) se utilizan comúnmente en varios campos, como la adsorción [1], la fotocatálisis [2, 3], la conservación de alimentos [4] y el sensor de contaminantes [5]. Comparado con TiO 2 , el costo de producción de ZnO es aproximadamente un 75% menor y tiene una mayor eficacia de absorción en una gran fracción del espectro solar [6, 7]. La aplicación de óxido de un solo metal como fotocatalizador está restringida en la propiedad de transferencia del cargador debido a la recombinación fotogenerada de electrones / huecos. Esta recombinación, particularmente en el rango nanométrico, conduce a la disminución de su eficiencia cuántica y también puede conducir a la disipación de energía radiante al iniciar reacciones altamente deseables [8, 9]. Entre varios esfuerzos aplicados para reducir el problema de la recombinación de electrones y huecos, como el dopaje, la heterounión, la sensibilización del colorante, la deposición de metales nobles y no nobles, se encontró que la formación de materiales de heteroestructura es una de las preferencias nobles [10, 11, 12]. Se informó del acoplamiento de ZnO con otros óxidos metálicos para solucionar el problema de recombinación mencionado [8, 13,14,15,16]. Debido a su estabilidad y propiedades únicas, la hematita (α-Fe 2 O 3 ) [8, 14] y Mn 2 O 3 Se sugiere que [13] actúen como una pareja decente con ZnO.
Además, el polímero de PVA como agente estabilizador también tiene un gran uso para disminuir los problemas de recombinación entre electrones y huecos [17]. Como se informó [18, 19], 500 ° C es la temperatura óptima para eliminar las impurezas no deseadas, incluido el polímero PVA, después de actuar como agente de remate. También se ha informado de la modificación de los materiales sintetizados para que tengan una propiedad mesoporosa que permita un rápido proceso de transferencia de carga [20, 21]. Usando solo agua ambientalmente benigna como solvente y desarrollando un procedimiento de síntesis eficiente, también se pueden eliminar la toxicidad, la capacidad de causar cáncer y las propiedades mutagénicas de los solventes orgánicos.
Una pequeña variación en el nivel estándar de ácido ascórbico crea muchas enfermedades en los seres humanos [16]. Como se informó [22], el ácido ascórbico tiene un papel importante en el funcionamiento fisiológico normal de los organismos y también se utiliza como tratamiento para una enfermedad diferente. Por lo tanto, es importante desarrollar métodos novedosos que se utilicen para medir el nivel de ácido ascórbico. Hoy en día, los nanomateriales de óxido metálico se han utilizado en gran medida como aplicaciones de sensores [23]. Entre varias técnicas que se han realizado para mejorar las propiedades de detección del ZnO, se ha informado la formación de un compuesto con otros óxidos metálicos y la modificación de los materiales sintetizados para que tengan una propiedad mesoporosa que permita un rápido proceso de transferencia de carga [20, 21]. Además, las infecciones hospitalarias causadas por microorganismos se están convirtiendo en un problema mundial [24]. El ZnO también figura como agente antimicrobiano y material seguro para la conservación de alimentos de enfermedades transmitidas por los alimentos por la FDA de EE. UU. (21CFR182.8991) [4, 25].
Considerando todos los aspectos mencionados de agregación / aglomeración, relación superficie-volumen y toxicidad de solventes orgánicos, este trabajo sintetiza PTMO-NCM asistido por PVA usando un sol-gel simple seguido de técnicas de autopropagación accidental. El material sintetizado se caracterizó por técnicas analíticas DTG / DSC, XRD, BET, SEM – EDX / TEM / HRTEM / SAED y CV / EIS / amperométrica. Se ha logrado un área de superficie pronunciada y una mejora en la capacidad de transferencia de carga para PTMO-NCM, en comparación con ZnO. La aplicabilidad del PTMO-NCM acoplado sintetizado se probó en la adsorción y degradación de colorantes orgánicos, actividad antibacteriana y un sensor de ácido ascórbico.
Materiales y métodos
Los detalles instrumentales y los reactivos utilizados estaban presentes como material complementario (S). Los procedimientos detallados de síntesis de ZnO y PTMO-NCM también estuvieron presentes en trabajos anteriores del autor [1, 26, 27, 28]. Aproximadamente, el polímero de PVA se disolvió en agua destilada con agitación continua en un agitador magnético a ~ 115 ° C durante aproximadamente 15 min. Luego, los precursores de sal, Zn (NO 3 ) 2 .6H 2 O, Fe (NO 3 ) 3 .9H 2 O y MnSO 4 .H 2 O se mezclaron con una solución de polímero de PVA previamente disuelta y enfriada con agitación continua. Después de dos días de envejecimiento seguido de secado en un horno a aproximadamente 110 ° C, el producto se trituró suavemente para reducir el material autopropagado altamente amorfo. Finalmente, se calcinó a la temperatura de calcinación optimizada para DTG de 500 ° C durante 3 h. El proceso de calcinación a la temperatura optimizada ayuda a eliminar las impurezas no deseadas, así como el polímero PVA. El PTMO-NCM sintetizado se utilizó para la caracterización continua de muestras y las pruebas de aplicación. El experimento fotocatalítico se realizó con un 2 de 176,6 cm reactor de vidrio circular bajo una lámpara de vapor de mercurio de 125 W. Durante el experimento se utilizaron 20 ppm de 250 ml de colorantes rojo Congo (CR) y naranja ácido-8 (AO8) y 0,06 g de fotocatalizador PTMO-NCM. La prueba de adsorción se realizó utilizando los parámetros de adsorción optimizados experimentalmente [1], un tiempo de contacto adsorbato-adsorbente de 10 a 150 min y 1 a 35 mg L −1 concentraciones con una velocidad de agitación constante de 140 rpm. La prueba de actividad antibacteriana se había realizado utilizando tres concentraciones diferentes (75, 100 y 125 μg mL −1 ) de ZnO y PTMO-NCM. El experimento fue acompañado por un método de difusión en disco usando un estándar de 0.5 McFarland.
Resultados y discusión
Resultados de caracterización
Se determinó que la temperatura óptima de calcinación era de 500 ° C mediante el análisis de estabilidad DTG a 50 ° C min −1 caudal de nitrógeno gaseoso. Aproximadamente el 56% de la descomposición de la muestra tuvo lugar y quedó con ~ 42% de PTMO-NCM puro (Fig. 1a). A partir del gráfico de DSC (ver Fig. 1b), se supone que los dos picos exotérmicos se deben a la evaporación de componentes volátiles adsorbidos a 80 ° C y cambios conformacionales a 144 ° C. El tercer pico endotérmico que apareció a aproximadamente 210 ° C probablemente se deba a la transformación de fase de otras formas de óxidos de hierro o manganeso al Fe 2 estable. O 3 y Mn 2 O 3 fase. En comparación con el ZnO, la caída de alta reflectancia en la región visible para PTMO-NCM se observó a partir del análisis espectroscópico UV-Vis-DRS (archivo adicional 1:Fig. S1a). Este análisis óptico admite la reducción de la intensidad máxima del patrón XRD y la interpretación de la porosidad de la imagen SEM. Las gráficas de Kubelka-Munk [29, 30] mostraron la inexistencia de cambios en la banda prohibida entre ZnO y PTMO-NCM (archivo adicional 1:Fig. S1b).
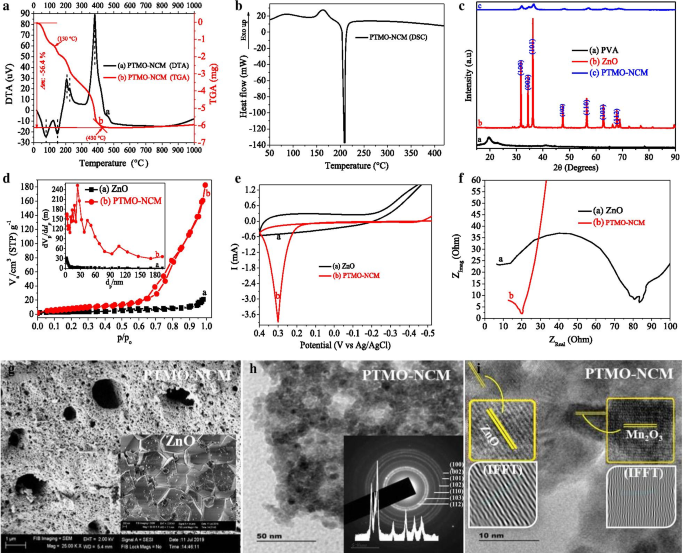
un DTG. b DSC. c XRD. d APUESTA. e CV. f Gráficos EIS. g SEM. h TEM. yo Imágenes HRTEM de ZnO simple y materiales nanocompuestos ternarios
La notable reducción del tamaño cristalino promedio aproximado (6x) se obtuvo para PTMO-NCM, en comparación con ZnO (Fig. 1c). Los picos del patrón XRD tanto de ZnO como de PTMO-NCM son consistentes con la fase hexagonal de ZnO (ICSD:00-036-1451, grupo espacial P63mc (# 186-1)). Esto probablemente se deba a los porcentajes más pequeños de óxidos de hierro (5%) y manganeso (5%). La ausencia de cambios de picos de PTMO-NCM en relación con ZnO también muestra la no aparición de distorsión estructural en la red de ZnO. Esto puede indicar la presencia de sólo una heterounión local entre los óxidos metálicos ternarios [8, 31, 32]. Los datos de XRD y el tamaño respectivo de las partículas se calcularon utilizando la fórmula de Debye-Scherrer ( D = Kλ / ( β cos ( θ )), donde λ es la longitud de onda de la radiación de rayos X (para Cu 0,15418 nm), K es constante cerca de la unidad, β es el ancho completo a la mitad del máximo (FWHM) en 2 θ escalas y θ es el ángulo de la reflexión de Bragg considerada [33, 34].
En comparación con el ZnO, la gran mejora del área de superficie para PTMO-NCM (15 ×) y la naturaleza porosa de PTMO-NCM se aprobaron a partir del análisis de imágenes BET y SEM, respectivamente (ver Fig.1d, g, (la imagen insertada en la Fig. .1g es para ZnO)). Según las clasificaciones de la IUPAC, entre seis tipos de isotermas de adsorción (I-VI) y cuatro tipos de bucles de histéresis, los gráficos BET de ZnO y PTMO-NCM parecen una isoterma IV típica y un bucle de histéresis H3. Se determinó que la distribución del tamaño de poro BJH promedio aproximado para ZnO y PTMO-NCM era 9 y 26, respectivamente, lo que es consistente con el rango mesoporoso de la clasificación IUPAC [35]. El mayor aumento de corriente en el análisis de CV [36] (Fig. 1e) y el diámetro de semicírculo más pequeño del gráfico de Nyquist en las técnicas de EIS [37] (Fig. 1f) confirman las capacidades mejoradas de transferencia de carga de PTMO-NCM sobre ZnO. El tamaño cristalino de rango nanométrico del PTMO-NCM se confirmó adicionalmente a partir de la imagen TEM (Fig. 1h). La composición predecible y la actualidad del PTMO-NCM se caracterizaron por EDX (ver archivo adicional 1:Fig. S2) y análisis HRTEM (Fig. 1i y sus recuadros), respectivamente. Los valores de espaciado d (0,2864, 0,2543, 0,1969, 0,1663, 0,1520, 0,1419 y 0,1104) que se determinaron a partir de anillos SAED (recuadro de 1h) también coinciden con el resultado del patrón XRD. Las fallas de apilamiento en la imagen HRTEM (IFFT) y la inexistencia de puntos de difracción en el anillo SAED que confirman la cristalinidad de los materiales [38] confirman aún más la naturaleza porosa del PTMO-NCM.
Adsorción de tinte azul de metileno
La dosificación optimizada de 0,02 g, pH de 8 y una velocidad de agitación constante de 140 rpm se utilizaron para los estudios de adsorción-reacción y de cinética de adsorción-difusión [1]. El coeficiente de determinación ( R 2 ) El valor y las ecuaciones utilizadas para calcular el parámetro de los modelos de cinética de adsorción se incluyeron en los gráficos respectivos como recuadro (Fig. 2). Entre los modelos de adsorción-reacción de pseudo-primer orden (PFO) (Fig.2b), pseudo-segundo orden (PSO) (Fig.2c) y Elovich (Fig.2d), el modelo de PSO que confirma los tipos de quimisorción de adsorción encaja bien. Además, el valor teórico (9,43 mg g −1 ) y experimental (9,91 mg g −1 ) los valores del modelo PSO tienen una estrecha relación a diferencia de la del PFO que tiene los valores experimentales de (3.64 mg g −1 ). El modelo de difusión intrapartícula (DPI) parece encajar bien (Fig. 2e); sin embargo, para decir que la reacción está bajo el control de adsorción-difusión, su gráfico lineal debe pasar por el origen. La trama IPD para este trabajo no pasa por el origen. A partir de esto, es posible concluir que la reacción está predominantemente bajo el control de la reacción de adsorción. Sin embargo, el buen ajuste del modelo de Bangham (Fig. 2f) indica la presencia de difusión de poros en el proceso de adsorción [39]. La presencia de esta difusión porosa también es consistente con las interpretaciones BET y SEM.
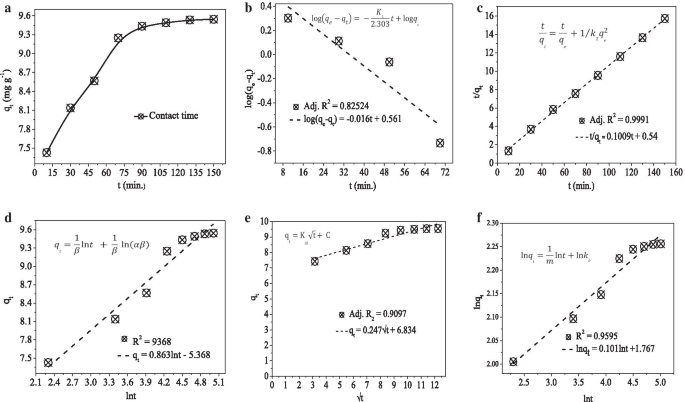
un Gráfico de la cinética de adsorción. b Pseudo-primer orden. c Pseudo-segundo orden. d Elovich. e Difusión intrapartícula. f Modelos de cinética de Bangham
La R 2 El valor y las ecuaciones utilizadas para calcular el parámetro de los modelos de isoterma de adsorción también se dieron en los gráficos respectivos como recuadro (Fig. 3). Dependiendo de la R 2 valores de los modelos de isoterma de adsorción (Langmuir (Fig. 2a), Freundlich (Fig. 2b), Dubinin-Radushkevich (D-RK) (Fig. 2c), Temkin (Fig. 2d), Flory-Huggins (FH) (Fig. . 2e) y Fowler-Guggenheim (FG) (Fig. 2f)), los modelos Langmuir y FH muestran un ajuste relativamente mejor. Del modelo de Langmuir, el factor de separación R L un valor entre 0 y 1 (0,05) indica la preferencia del proceso de adsorción. La favorabilidad del proceso de adsorción también se confirmó a partir del valor n (1,59) del modelo de Freundlich. El buen ajuste del modelo de Langmuir indica la presencia de una cobertura de colorante azul de metileno monocapa, que es consistente con la interpretación del modelo cinético de PSO. La capacidad máxima de adsorción del adsorbente que se determinó a partir del modelo de isoterma de Langmuir es de 7,75 mg g −1 . La indicación de la cobertura superficial característica y la espontaneidad de la reacción (- 3,8 kJ mol −1 ) también se dedujeron de la ecuación del modelo FH.
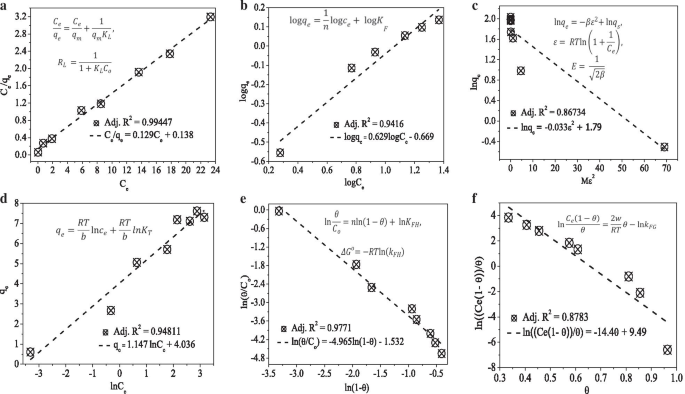
Gráficos de isotermas de adsorción de a Langmuir. b Freundlich. c Dubinin – Radushkevich. d Temkin. e Flory-Huggins. f Modelos Fowler – Guggenheim
Mecanismo y degradación del tinte rojo Congo y naranja ácida-8
Las capacidades de fotodegradación de PTMO-NCM se estudiaron en la decoloración de tintes CR y AO8 a una longitud de onda de absorción máxima de 494 y 484 nm (Fig. 4a, b), respectivamente. En los primeros 15 minutos, tuvo lugar aproximadamente el 17% del tinte CR y el 15% de la degradación del tinte AO8. A los 180 min, se estaba produciendo la degradación máxima del 70% para el tinte CR y del 68% para el tinte AO8. La constante de equilibrio obtenida k los valores para los tintes CR y AO8 fueron 0,007141 y 0,005627 min −1 , respectivamente. Desde el punto de contacto de 1 - C / C o versus t y C / C o versus t gráficos (ver Fig. 4c, d), el valor de vida media de degradación obtenido fue de aproximadamente 105 min para CR y 119 min para AO8. Consulte la ecuación cinética del PFO utilizada para estudiar la dinámica de reacción en el recuadro de la Fig. 4d.
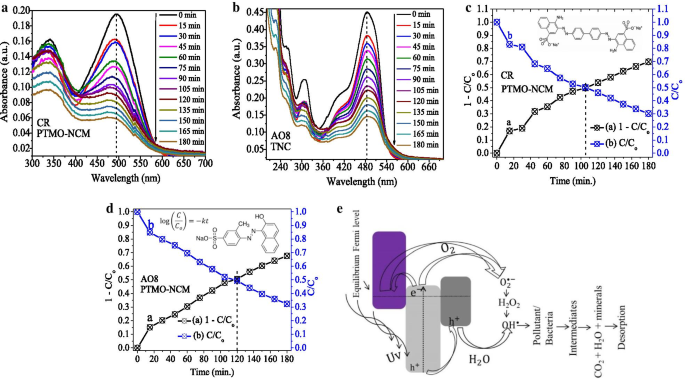
Actividades fotocatalíticas del PTMO-NCM: a , b gráficos de absorbancia frente a longitud de onda. c , d 1 - C / C o versus t y C / C o versus t parcelas de CR y AO8, respectivamente. e Mecanismo propuesto
La posición del borde de la banda de los óxidos metálicos depende en gran medida de la carga superficial. Para una reacción fotocatalítica eficaz, la parte inferior del CB debe ser más negativa que el potencial redox de H + / H 2 y la parte superior del VB debe ser más positiva que el potencial redox de O 2 / H 2 O [40, 41]. Como se informó [13], el CB de Mn 2 O 3 y ZnO están cerca uno del otro. Además, para confirmar la presencia de una heterounión apropiada y la realidad de la sinergia de transferencia de carga adecuada, el análisis mediante técnicas electroquímicas como CV y EIS es significativo [42]. Como se ve en el análisis de CV (Fig. 1e) y EIS (Fig. 1f), el PTMO-NCM muestra la presencia de una heterounión adecuada. Por lo tanto, se propuso el posible mecanismo fotocatalítico como se ve en la Fig. 4e. Durante la heterounión, hasta que el nivel de Fermi se iguala, la banda de energía de los óxidos metálicos comienza a moverse hacia arriba y hacia abajo transfiriendo electrones [8, 43] y conduce a la creación de una capa de agotamiento en la interfaz [44]. El nivel de Fermi del tipo p Mn 2 O 3 existe cerca de la VB. Durante la irradiación UV, los electrones fotogenerados tienen la probabilidad de localizarse en el CB de ZnO o de difundirse al VB del Mn 2 O 3 , y los agujeros se mueven al VB de Fe 2 O 3 . Por lo tanto, la recombinación de electrones y huecos disminuyó y resultó en una actividad fotocatalítica mejorada [8].
A partir del gráfico CV de PTMO-NCM (Fig. 5a), se observaron los picos de reacción de reducción. Como se informó [45], se indica que esta reacción redox rápida y reversible se debe a la naturaleza porosa de los materiales. Esto también es consistente con los resultados de la caracterización BET y SEM. La diferencia de potencial pico aproximada obtenida (Δ E a, c ) entre E pa (+ 0,401 V) y E pc (+ 0.323 V) pico es 0.078 V. Este Δ E más pequeño a, c El valor muestra la capacidad del material PTMO-NCM para ser más reversible. Con un aumento en la velocidad de exploración, los picos redox se desplazaron positivamente hacia los potenciales anódico y catódico. Como se ve en la gráfica de CV de la Fig. 5b y la gráfica de amperometría de la Fig. 5c, también se confirmó la novedad del PTMO-NCM como sensor de ácido ascórbico, ya que el aumento de la concentración de ácido ascórbico da como resultado un aumento de la corriente. La nobleza de detección del material también se confirmó a partir del análisis de amperometría, ya que el ciclo de detección se completó en unos pocos segundos. Los ciclos se repitieron para evaluar la estabilidad del electrodo durante 1 h. El resultado obtenido confirma la estabilidad y reproducibilidad del electrodo PTMO-NCM.
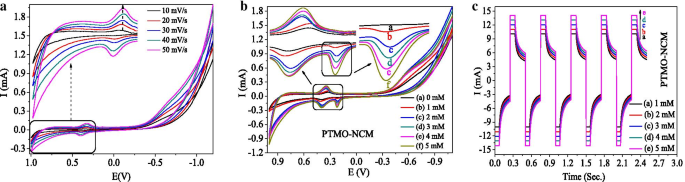
un Gráficos de CV a diferentes velocidades de escaneo. b Curva de detección de ácido ascórbico CV a diferentes concentraciones. c Gráfico de detección de ácido ascórbico amperométrico a diferentes concentraciones
La actividad antibacteriana de los óxidos metálicos depende en gran medida del tamaño de partícula [46] y de la capacidad de generación de ROS [47] de los materiales. Tomando diferentes porcentajes de precursor y cantidad de polímero de PVA [26], las actividades antibacterianas óptimas de PTMO-NCM hacia E. coli y S . aureus (Fig. 6a, b, respectivamente) se determinó que eran 50% ZnO, 25% Fe 2 O 3 y 25% Mn 2 O 3 . Las actividades antibacterianas mejoradas para PTMO-NCM se lograron en comparación con materiales basados en ZnO simple y binario [27]. El mecanismo de actividad antimicrobiana de las NP puede seguir tres mecanismos [48], que incluyen la liberación de iones antimicrobianos [25, 49], la interacción de las NP con microorganismos [50] y la formación de ROS por efecto de la radiación luminosa [51]. . Como se confirmó a partir del patrón XRD y los espectros UV-Vis-DRS, la distorsión estructural y el cambio de posición de la banda no se habían observado. La ausencia de esta distorsión y cambio se debe a la no intercalación de Fe 3+ / Mn 3+ iones. Esto indica que la actividad antimicrobiana debida a los iones puede no ser el mecanismo adecuado. Por lo tanto, las formas directas e indirectas de generación de ROS [52] se propusieron como un mecanismo de actividades antibacterianas, como se ve en la Fig. 6c.
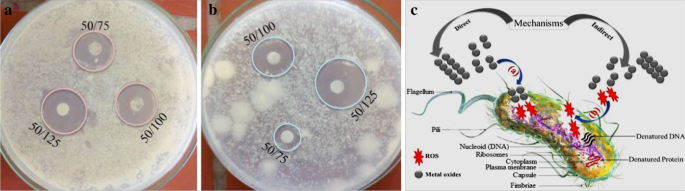
La actividad antibacteriana de PTMO-NCM hacia a E. coli. b S. aureus. c mecanismo antibacteriano (50/75:50 es el porcentaje de PTMO-NCM durante la síntesis, 75 es la cantidad utilizada en μg / mL durante la actividad antibacteriana)
Conclusiones
El PTMO-NCM que tiene alta porosidad, área de superficie mejorada y capacidad superior de transferencia de carga se sintetizó utilizando sol-gel seguido de técnicas de autopropagación. Usando el patrón XRD y el análisis de imagen TEM, se determinó que el tamaño cristalino promedio aproximado de PTMO-NCM estaba en el rango de 10 a 60 nm. El tamaño cristalino de PTMO-NCM es seis veces más pequeño que el ZnO desnudo. En comparación con el ZnO, se confirmó una mejora del área de superficie quince veces mayor para PTMO-NCM a partir del análisis BET. La naturaleza menos cristalina del PTMO-NCM se confirmó además a partir de las fallas de apilamiento presentes en la imagen HRTEM (IFFT) y la ausencia de puntos de difracción en el anillo SAED. El diámetro semicircular nueve veces más pequeño en el EIS y un aumento de corriente mejorado en CV indican la presencia de nuevas propiedades de transferencia de carga para PTMO-NCM, en comparación con ZnO. A partir del estudio de la cinética de adsorción y las isotermas de adsorción, se examinó la interacción adsorbato-adsorbente como un tipo de quimisorción. A partir del modelo de Langmuir, se determinó que la capacidad máxima de adsorción era de 7,75 mg g −1 . Se encontró que las constantes de equilibrio fotocatalítico eran 0.007141 min −1 y 0,005627 min −1 para tintes CR y AO8, respectivamente. También se verificaron la capacidad de detección superior y las actividades antibacterianas nobles de PTMO-NCM.
Disponibilidad de datos y materiales
Los conjuntos de datos utilizados y / o analizados durante el estudio actual están disponibles del autor correspondiente a solicitud razonable.
Abreviaturas
- PTMO-NCM:
-
Material nanocompuesto de óxido metálico ternario poroso
- UV - Vis-DRS:
-
UV - Espectroscopia de reflectancia difusa vis
- FT-IR:
-
Espectroscopía infrarroja por transformada de Fourier
- XRD:
-
Difracción de rayos X en polvo
- SEM:
-
Microscopía electrónica de barrido
- EDX:
-
Espectroscopia de rayos X de dispersión de energía
- TEM:
-
Microscopía electrónica de transmisión
- HRTEM:
-
Microscopía electrónica de transmisión de alta resolución
- SAED:
-
Difracción de electrones de área seleccionada
- APUESTA:
-
Brunauer – Emmett – Teller
- CV:
-
Voltamperometría cíclica
- EIS:
-
Espectroscopia de impedancia eléctrica
- FH:
-
Flory – Huggins
- FG:
-
Fowler – Guggenheim
- PFO:
-
Pseudoprimer orden
- PSO:
-
Pseudo-segundo orden
- IPD:
-
Difusión intrapartícula
- CR:
-
Rojo congo
- AO8:
-
Naranja ácida-8
- IFFT:
-
Transmisión rápida inversa de Fourier
- ROS:
-
Especies reactivas de oxígeno
- S. aureus :
-
Staphylococcus aureus
- E. coli :
-
Escherichia coli
Nanomateriales
- PBT resistente a la hidrólisis que también es transparente al láser brilla en aplicaciones exigentes de motores automotrices
- Una revisión sobre la aplicación de biosensores y nanosensores en los agroecosistemas
- Dirigirse a las células endoteliales con nanopartículas multifuncionales de GaN / Fe
- Crecimiento directo de estructuras de ZnO similares a plumas mediante una técnica de solución fácil para la aplicación de fotodetección
- Bioseguridad y capacidad antibacteriana del grafeno y el óxido de grafeno in vitro e in vivo
- Síntesis de nanocristales de ZnO y aplicación en células solares de polímero invertido
- Rendimiento fotocatalítico de luz visible de nanocompuestos de ZnO / g-C3N4 dopado con N
- Deposición de capa atómica de nanopelículas de óxido de indio para transistores de película delgada
- Fabricación y caracterización de nanoclips de ZnO mediante el proceso mediado por poliol
- Revisar la aplicación de silicio negro nanoestructurado
- Sensor de gas de hidrógeno de nanocables de óxido de cobre asistido por luz ultravioleta



