Carbón de alta porosidad autodopado con nitrógeno muy grafítico para la electrocatálisis de la reacción de reducción de oxígeno
Resumen
La producción a gran escala de catalizadores de carbono poroso activo y estable para la reacción de reducción de oxígeno (ORR) a partir de biomasa rica en proteínas se convirtió en un tema candente en la tecnología de celdas de combustible. Aquí, presentamos una estrategia fácil para la síntesis de nanocarbonos porosos dopados con nitrógeno por medio de un proceso de pirólisis simple de dos pasos combinado con la activación del cloruro de zinc y el proceso de tratamiento con ácido, en el que se adoptó preferentemente el frijol mediante carbonización a baja temperatura. como las únicas fuentes de carbono-nitrógeno. Los resultados muestran que este material de carbono exhibe una excelente actividad electrocatalítica de ORR y una mayor durabilidad y propiedad de tolerancia al metanol en comparación con el catalizador de Pt / C de última generación para el ORR, que se puede atribuir principalmente a un alto contenido de nitrógeno grafítico. , alta superficie específica y características porosas. Nuestros resultados pueden fomentar la síntesis de electrocatalizadores ORR basados en carbono de alto rendimiento derivados de biomasa natural ampliamente existente.
Antecedentes
Los materiales a base de platino (Pt), los catalizadores de última generación para las pilas de combustible, tienen un precio elevado, recursos limitados, durabilidad insuficiente y propiedades de tolerancia al metanol en el proceso de electrocatálisis de la reacción de reducción de oxígeno (ORR) [1] . Recientemente se han dedicado grandes esfuerzos a la búsqueda de alternativas altamente activas, duraderas y económicas a los electrocatalizadores ORR basados en Pt para este propósito [2]. Entre los diversos catalizadores que no son Pt, los carbonos porosos dopados con heteroátomos (HDPC) son un nuevo tipo de catalizadores libres de metales con alta actividad y durabilidad para ORR gracias a su bajo costo, no toxicidad y renovabilidad [3,4, 5,6], y por lo tanto, las investigaciones en profundidad se anticipan con impaciencia hasta la fecha. El HDPC generalmente se sintetiza mediante métodos químicos o plantillas naturales, pero no pueden cumplir con los requisitos de bajo costo, fácil síntesis y excelente rendimiento [7, 8]. Por lo tanto, la búsqueda de un método razonable y eficaz para sintetizar el material de HDPC sigue siendo un tema científico importante para realizar una catálisis altamente eficiente para la reducción de oxígeno.
Como se informó anteriormente, la biomasa enriquecida en proteínas (p. Ej., Nori [9], enredadera de boniato [10], piel de pomelo [11], hongo enoki [12], coprinus comatus [13] y Lemna minor [14]) se puede utilizar ampliamente como un precursor de una sola fuente para el catalizador de HDPC hacia el ORR. Recientemente, proponemos alguna estrategia para formar el catalizador HDPC con estructura de red porosa en 3D a través de la carbonización a alta temperatura de desechos biológicos a escala de pescado con un activador de cloruro de zinc [6]. Curiosamente, encontramos que el pretratamiento de la biomasa en el primer paso no solo puede ayudar a mejorar las características de la estructura del carbono del catalizador ORR final, sino que también aumenta su contenido de nitrógeno en la superficie y la eficiencia de dopaje de los átomos de nitrógeno en la estructura del carbono. Con base en este hallazgo, aquí presentamos primero una estrategia para fabricar carbonos porosos dopados con nitrógeno grafítico (KB350Z-900) mediante la conversión directa de biomasa de frijol blanco (KB) con un proceso de carbonización en dos pasos, seguido de cloruro de zinc. activación y proceso de tratamiento ácido. La biomasa KB, que es uno de los frijoles comestibles más famosos en la actualidad, se puede obtener de forma abundante y económica en varios países. El contenido total de proteína biológica en la biomasa de KB deshidratada es generalmente del 20 al 30%. Hasta donde sabemos, rara vez se informa sobre la actividad de ORR del catalizador de carbono dopado derivado de la biomasa de KB. El papel de ZnCl 2 en el proceso de activación puede estimular principalmente la deshidratación rápida y la deshidroxilación catalítica de la biomasa de KB de modo que el hidrógeno y el oxígeno dentro de la biomasa de KB se liberen en la formación de vapor de agua. Este proceso puede facilitar la formación de más micro / mesoporos, produciendo finalmente materiales de carbono de alta porosidad autodopados con nitrógeno. El catalizador a base de carbono obtenido exhibe una alta actividad electrocatalítica, durabilidad a largo plazo y propiedad de tolerancia al metanol, lo que puede ser una alternativa prometedora al catalizador a base de Pt hacia el ORR en medio alcalino.
Métodos
Primero, se lavó el frijol blanco (KB) con agua desionizada y se secó completamente a 80 ° C en un horno de secado al vacío. Posteriormente, KB se pretrató en Flow-N 2 atmósfera a 350 ° C durante 2 h para una descomposición eficaz de la proteína para producir el precursor KB350. Aunque la descomposición más rápida de la biomasa blanca de KB se produce a unos 300 ° C (archivo adicional 1:Figura S1), se eligió una temperatura de 350 ° C como la temperatura de carbonización de primer paso para superar la temperatura de descomposición de la tirosina (344 ° C), el más alto entre los aminoácidos de la bioproteína. KB350 y cloruro de zinc (ZnCl 2 ) se mezclaron mecánicamente mediante molienda de bolas a 500 rpm según una relación de masa de 1:1. La mezcla obtenida se pirolizó en un horno tubular a diferentes temperaturas (700, 800, 900 o 1000 ° C) durante 2 h con una velocidad de calentamiento de 10 ° C min - 1 . El nanocarbono producido se denomina en lo sucesivo KB350Z-X (X =700, 800, 900 o 1000). Como control, el KB-Z-900 se fabricó de manera similar pirolizando una mezcla mecánica de KB y ZnCl 2 con la misma relación de masa. Se utilizó la pirólisis directa de KB a 900 ° C durante 2 h para preparar el KB900. Todas las muestras preparadas se trataron posteriormente con 0,5 mol l - 1 Solución de HCl durante 2 h. El objetivo de la lixiviación ácida es eliminar eficazmente las especies de Zn y las impurezas metálicas antes de las pruebas electroquímicas.
Los datos de la espectroscopía Raman se probaron con una unidad inVia de Renishaw con un λ excitado de 514,5 nm. Las imágenes de microscopía electrónica de barrido de emisión de campo (FE-SEM) se obtuvieron mediante Hitachi UHR S4800 (Japón). Se realizó microscopía electrónica de transmisión de alta resolución (HR-TEM) en el instrumento FEI Tecnai F30 y el voltaje de aceleración es de 300 kV. La espectroscopia de fotoelectrones de rayos X (XPS) se llevó a cabo utilizando un espectrómetro Kratos XSAM800. Se aplicó un Micromeritics Analyzer (ASAP 2010) para medir N 2 isotermas de adsorción / desorción a 77 K.
Las mediciones electroquímicas se realizaron en una estación de trabajo Zennium-E (Alemania) con un sistema convencional de tres electrodos. Un electrodo de disco de rotación de vidrio-carbono (GC-RDE, Φ =4 mm, modelo 636-PAR), un electrodo de calomelanos saturado (SCE) y una varilla de grafito (Φ =0,5 cm) se utilizaron como electrodo de trabajo, electrodo de referencia, y electrodo auxiliar, respectivamente. La fabricación de electrodos de trabajo se refiere a nuestros informes anteriores [6]. Generalmente, 5,0 μl de 10 mg ml - 1 La dispersión se transfirió a la superficie de GC-RDE y se secó de forma natural. La carga de masa de todas las muestras analizadas se controló para que fuera de ~ 400 μg cm - 2 . Todos los potenciales (versus SCE) se transformaron en potenciales versus el electrodo de hidrógeno reversible (RHE).
Resultados y discusión
Primero probamos los espectros Raman de los catalizadores KB900, KB-Z-900 y KB350Z-900 para comprender sus diferencias de propiedades estructurales. Los espectros Raman se muestran en la Fig. 1a. La relación de intensidad (I D / I G ) de la banda "D" a la banda "G" se utilizó para caracterizar los grados desordenados y grafíticos. La I D / I G es 0.85 solo para KB350Z-900, pero el I D / I G es 0,94 para KB900 y 0,88 para KB-Z-900, respectivamente. Puede mostrar que se puede obtener un mayor grado de grafito en KB350Z-900 en comparación con los catalizadores basados en nitrógeno / carbono (NC) tal como se prepararon, lo que puede confirmarse directamente mediante la comparación de la intensidad Raman. Además, el uso de ZnCl 2 El activador en la síntesis de catalizadores basados en NC puede facilitar la mejora del grado grafítico durante el proceso de pirólisis debido a un I D más bajo / I G relación de KB350Z-900. El pretratamiento del primer paso de KB a 350 ° C puede mejorar aún más el grado grafítico de los catalizadores basados en NC, lo que puede ayudar a producir más estructuras de carbono dopadas con nitrógeno grafítico. N 2 Se utilizaron isotermas de adsorción-desorción para investigar los efectos de ZnCl 2 activador y pretratamiento de primer paso en el área de superficie específica y la distribución de poros de los catalizadores basados en NC. La Figura 1b muestra claramente una curva de isoterma de Langmuir IV con un bucle de histéresis de tipo H2, lo que demuestra que las estructuras mesoporosas también se incluyen en los catalizadores preparados (por ejemplo, KB-Z-900 y KB350Z-900). La superficie específica de BET es de unos 380 m 2 g - 1 para KB-Z-900 y 1132 m 2 g - 1 para KB350Z-900, respectivamente. Un volumen de poro total más alto de KB350Z-900 es ~ 0,62 m 3 g - 1 , y el área de mesoporos y macroporos de KB350Z-900 es ~ 664 m 2 g - 1 (recuadro de la Fig. 1b). El pretratamiento en el primer paso de KB a 350 ° C puede promover la formación de más mesoporos y macroporos y el aumento del área de superficie específica BET, lo que favorece la exposición de los sitios activos y la difusión de la molécula de oxígeno durante la prueba electroquímica. Las imágenes de microscopía electrónica de transmisión (TEM) (Fig. 1c, d) también confirman que en KB350Z-900 se puede observar un gran número de micro / macroporos y estructuras de carbono amorfo. Significativamente, se forman bordes defectuosos y expuestos en la nanoestructura de carbono debido a un mayor porcentaje de dopaje N, que también se supone que ofrece sitios reactivos de manera efectiva para el ORR [15].
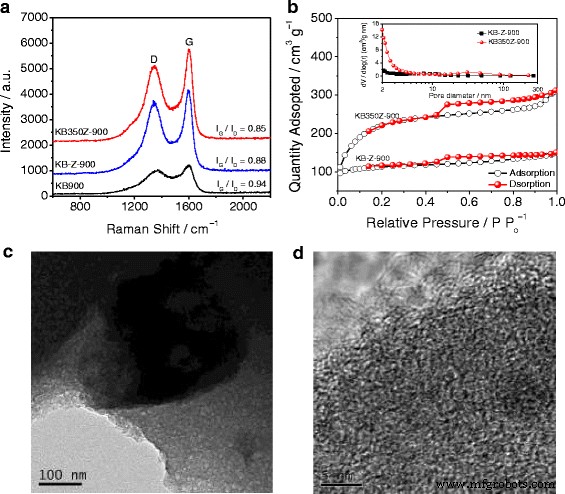
un Espectros Raman de KB900, KB-Z-900 y KB350Z-900. b Isotermas de adsorción-desorción de nitrógeno y distribuciones de tamaño de poro BJH correspondientes (recuadro) de KB-Z-900 y KB350Z-900. c Baja resolución y d Imágenes de microscopía electrónica de transmisión de alta resolución de KB350Z-900
La Figura 2a, b muestra que los átomos de nitrógeno se doparon con éxito en la estructura de carbono de tres tipos de catalizadores ORR. El contenido de nitrógeno superficial del análisis XPS es 1,23, 1,92 y 2,70 at.% Para KB-900, KB-Z-900 y KB350Z-900, respectivamente. Indica que la pérdida de nitrógeno puede disminuir debido a la activación de ZnCl 2 y proceso de carbonización en dos etapas [6]. Los espectros XPS de N1 s de KB-900 y KB-Z-900 se pueden ajustar a tres picos (consulte el archivo adicional 1:Figura S2), que se pueden atribuir a N piridínico, N grafítico y N oxidado [6, 7, 8, 12, 13], respectivamente. Sin embargo, el espectro XPS de N1 s de KB350Z-900 se puede ajustar en solo dos picos (ver archivo adicional 1:Figura S2), centrados en 398,5 y 401,1 eV, que se pueden asignar a piridínico-N y grafítico-N, respectivamente. En particular, la especie de N oxidado no se observa en el espectro XPS de N1 s de KB350Z-900, y el porcentaje de especies de N grafítico es de hasta 88,8% at. En el contenido total de nitrógeno. El contenido de especies de Graphitic-N sigue el orden de KB350Z-900> KB-Z-900> KB-900, lo que implica que el ZnCl 2 El proceso de activación puede ser fácil para facilitar el aumento del contenido de N grafítico dentro del material NC y el uso del precursor KB350 derivado del pretratamiento del material KB en el primer paso puede reducir efectivamente la formación de especies de N oxidado.
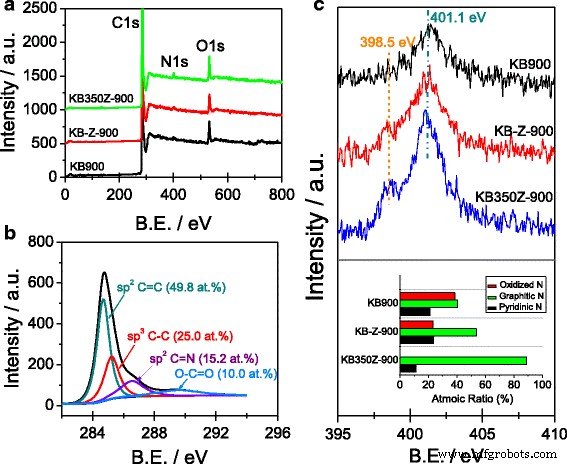
un Encuesta XPS de KB900, KB-Z-900 y KB350Z-900; b Espectro C1s XPS de KB350Z-900; c Espectros XPS de N1 s de KB900, KB-Z-900 y KB350Z-900
Curvas CV (ver Fig. 3a) obtenidas en N 2 versus O 2 Las soluciones saturadas de KOH demuestran que el KB350Z-900 exhibe la densidad de corriente máxima de ORR más alta y el potencial de pico más positivo (0,90 V) en comparación con KB-Z-900 y KB-900, lo que puede deberse al alto contenido de especies de N grafítico. en el interior del catalizador [13, 16]. Además, las curvas LSV (Fig. 3b) obtenidas en O 2 La solución saturada de KOH indica además que el potencial de media onda de ORR y la densidad de corriente limitada de KB350Z-900 se acercan a los del catalizador de primera clase al 20% en peso de Pt / C. Se utilizó el método Tafel para analizar las curvas de potencial actual (j-E) en el rango cinético. La densidad de corriente ORR es casi independiente de la velocidad de rotación del electrodo en el rango de potencial de 0,8 a 1,0 V (frente a RHE), lo que sugiere que la densidad de corriente en este rango de sobrepotencial bajo está dominada por la densidad de corriente cinética electroquímica. Las gráficas de Tafel de E en función de log (j) se muestran en (Archivo adicional 1:Figura S3). Una pendiente Tafel de 143 mV década - 1 se obtiene para KB350Z-900. La desviación de las pendientes de Tafel para el catalizador KB350Z-900 y Pt / C implica que su adsorción intermedia puede seguir un modelo diferente [17]. Las pendientes de Tafel más altas (valor absoluto) corresponden a un rápido aumento del sobrepotencial con la densidad de corriente, lo que probablemente conduce a una actividad catalítica de ORR relativamente inferior [18]. Sin embargo, la actividad electrocatalítica de ORR de KB350Z-900 puede ser más excelente en comparación con los catalizadores basados en carbono informados anteriormente derivados de otra biomasa o biomaterial [9,10,11,12,13,14]. El estudio del efecto de la temperatura de pirólisis en catalizadores NC a través del ZnCl 2 La activación también muestra que la actividad de la ORR sigue el orden de KB350Z-900> KB350Z-800> KB350Z-1000> KB350Z-700, lo que sugiere la mejor actividad electrocatalítica de KB350Z-900, ya que temperaturas más altas o más bajas harán que la actividad de la ORR sea peor. en medio alcalino [19]. Puede atribuirse principalmente a una razón valiosa de que la alta porosidad y el área de superficie específica, y el alto contenido de N en la superficie y el porcentaje de especies de N de KB350Z-900 pueden facilitar el transporte rápido de O 2 molécula y la exposición de sitios activos accesibles [6], que pueden ayudar a mejorar la actividad electrocatalítica hacia el ORR.
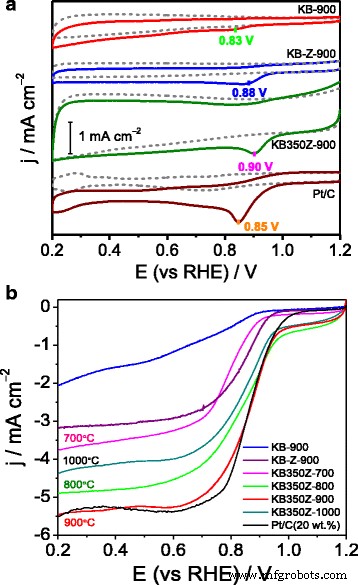
un Curvas CV de KB900, KB-Z-900 y KB350Z-900 en N 2 versus O 2 solución saturada de KOH; b Curvas LSV de los catalizadores preparados y el catalizador JM Pt / C
Además, las curvas LSV para ORR de KB-Z-900 y KB350Z-900 a diferentes velocidades de rotación (400-3600 rpm) se muestran en la Fig. 4a, b. La buena linealidad de los gráficos de Koutecky-Levich (Fig. 4c) indica la cinética de ORR de primer orden con respecto al O 2 disuelto concentración. El número medio de transferencia de electrones (n) de la ORR en KB-Z-900 y KB350Z-900 se estima en ~ 3,93 y ~ 3,98 (recuadro de la Fig. 4c), respectivamente, de acuerdo con la ecuación de Koutecky-Levich [20 ]. La ecuación de Koutecky-Levich es la siguiente:
$$ 1 / {j} _d =1 / {j} _k + 1 / B {\ omega} ^ {1/2} $$ $$ \ mathrm {B} =0.62 \ mathrm {nF} {\ mathrm {C }} _ {\ mathrm {O}} {\ mathrm {D}} _ {\ mathrm {O}} ^ {2/3} {\ nu} ^ {- 1/6} {\ upomega} ^ {1 / 2} $$donde F es la constante de Faraday, C O es el O 2 concentración de saturación en el electrolito, D O es el O 2 coeficiente de difusión en el electrolito, ν es la viscosidad cinética del electrolito y ω es la velocidad de rotación del electrodo y 0,62 es una constante cuando la velocidad de rotación se expresa en rpm. Sugiere que el proceso de ORR en KB-Z-900 y KB350Z-900 sigue principalmente una vía de transferencia directa de cuatro electrones para producir H 2 O (por ejemplo, O 2 + 2 H 2 O + 4e - → 4 OH - ), que es muy similar a la ORR catalizada por un catalizador de Pt / C [21].
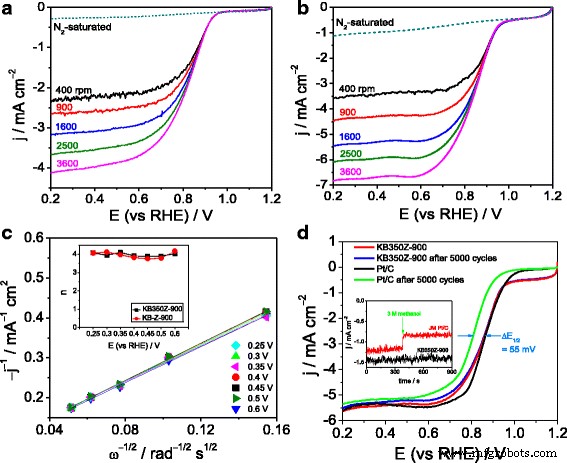
un Curvas LSV de KB-Z-900 en N 2 versus O 2 solución saturada de KOH a diferentes velocidades de rotación; b Curvas LSV de KB350Z-900 en N 2 versus O 2 solución saturada de KOH a diferentes velocidades de rotación; c Gráficas de Koutecky-Levich de j d - 1 versus ω - 1/2 obtenido de ( b ) a los potenciales dados (0,25-0,6 V). El recuadro son las gráficas de n frente al potencial obtenido de ( a ) y ( b ); d Curvas LSV de KB350Z-900 y JM Pt / C antes y después de CV durante 5000 ciclos en O 2 solución saturada de KOH; El recuadro son curvas i-t amperométricas a 0,9 V frente a RHE para pruebas de tolerancia al metanol
Aquí, utilizamos la prueba de envejecimiento acelerado (AAT) por barrido continuo de CV durante 5000 ciclos en un rango de potencial de 0,2 a 1,2 V frente a RHE para evaluar la estabilidad electroquímica de KB350Z-900 y catalizador Pt / C en un O 2 -Electrolito de KOH saturado. Después de la prueba de CV, el potencial de media onda del ORR en el electrodo catalizado por KB350Z-900 se desplaza negativamente en solo 2 mV, pero el potencial de media onda reducido del ORR en el electrodo catalizado por JM Pt / C es de aproximadamente 55 mV (figura 4d). Además, también se encuentra una mayor degradación en la densidad de corriente limitada para el catalizador de Pt / C, lo que indica una estabilidad electrocatalítica más excelente de KB350Z-900 hacia el ORR. Curvas amperométricas i-t a 0,9 V en O 2 El electrolito KOH saturado (recuadro de la Fig. 4d) confirma que la reacción de electrooxidación del metanol 3 M apenas se produce en KB350Z-900, lo que sugiere un buen rendimiento tolerante al metanol de KB350Z-900 y las aplicaciones prometedoras en pilas de combustible de metanol alcalino.
Conclusiones
En este documento, desarrollamos un método fácil y sencillo para la producción a gran escala de carbonos de alta porosidad dopados con nitrógeno fuertemente grafítico a partir de la pirólisis en dos pasos de la biomasa de frijol combinado con la activación del cloruro de zinc y el proceso de tratamiento ácido, que puede ser funcionó como un electrocatalizador de reducción de oxígeno en medio alcalino. Primero, encontramos que una gran área de superficie BET (~ 1132 m 2 g - 1 ) se puede obtener en KB350Z-900 con un volumen de poro alto de ~ 0,62 m 3 g - 1 . En segundo lugar, el proceso de pirólisis de dos pasos con activación de cloruro de zinc puede ayudar a aumentar significativamente el contenido de nitrógeno grafítico dentro del catalizador a base de carbono. También observamos que la actividad catalítica de la ORR de este material de carbono puede compararse favorablemente con la del catalizador comercial de 20% en peso de Pt / C de última generación, pero también la estabilidad de la electrocatálisis de la primera a la ORR y el rendimiento tolerante al metanol. son mejores, lo que sugiere aplicaciones prometedoras en pilas de combustible alcalinas. El excelente rendimiento de ORR de KB350Z-900 puede deberse principalmente al alto contenido de nitrógeno grafítico, la alta superficie específica y las características porosas. Nuestros resultados pueden promover aún más la producción a gran escala de electrocatalizadores ORR basados en carbono altamente activos y estables derivados de biomasa natural ampliamente existente.
Nanomateriales
- Los científicos de IBM inventan un termómetro para nanoescala
- Los nanotubos de carbono superan el límite de la electrónica flexible
- Imagen de carbono oceánico en escala atómica
- Cómo la industria aeroespacial utiliza la fibra de carbono para sus necesidades
- 5 consejos para encontrar el mejor fabricante de piezas de fibra de carbono
- El diseño de la capa de emisión para multiplicadores de electrones
- Saponinas Platycodon de Platycodi Radix (Platycodon grandiflorum) para la síntesis verde de nanopartículas de oro y plata
- Reacción de reducción de oxígeno en nanocatalizador de PtCo:Envenenamiento por aniones (bi) sulfato
- Electrocatalizadores de reducción de oxígeno Fe-N-C altamente activos y estables derivados de electrohilado y pirólisis in situ
- Fácil preparación de nanocompuestos de nanotubos de carbono-Cu2O como nuevos materiales catalizadores para la reducción de p-nitrofenol
- Deposición de capas atómicas de capas amortiguadoras para el crecimiento de matrices de nanotubos de carbono alineadas verticalmente



