(La0.97RE0.01Yb0.02) Nanophosphors 2O2S convertidos de hidroxil sulfato en capas e investigación de fotoluminiscencia de conversión ascendente (RE =Ho, Er)
Resumen
Fase pura (La 0.97 RE 0.01 Yb 0.02 ) 2 O 2 Se recocieron nanofosforos de conversión ascendente (UC) (tamaño medio de cristalito ~ 45 nm; RE =Ho, Er) de sus precursores de hidroxilsulfato en capas cristalizados hidrotermalmente en un flujo de hidrógeno a 1200 ° C durante 1 h, con vapor de agua como único escape. Bajo excitación láser de 978 nm (hasta 2,0 W), el Ho 3+ -el fósforo dopado exhibió emisiones de color verde (medio), rojo (débil) e infrarrojo cercano (fuerte) a ~ 546 ( 5 F 4 → 5 Yo 8 ), 658 ( 5 F 7 → 5 Yo 8 ) y 763 nm ( 5 F 4 → 5 Yo 7 ), respectivamente, y tiene las coordenadas de cromaticidad estable de aproximadamente (0.30, 0.66) en la región de luz visible (400-700 nm). El Er 3+ fósforo UC dopado, por otro lado, mostró un verde débil (~ 527/549 nm, 2 H 2/11 , 4 S 3/2 → 4 Yo 15/2 ), rojo débil (~ 668/672 nm, 4 F 2/9 → 4 Yo 15/2 ) e infrarrojo cercano intenso (~ 807/58 nm, 4 Yo 2/9 → 4 Yo 15/2 ) luminiscencia, cuyo color de emisión en la región visible pasó de verde amarillento [(0.36, 0.61)] a verde [(0.32, 0.64)] con una potencia de excitación creciente. El análisis de la luminiscencia UC dependiente de la potencia encontró procesos de tres y dos fotones para RE =Ho y Er, respectivamente, y se propusieron los posibles mecanismos UC.
Antecedentes
El fósforo de conversión ascendente (UC) está atrayendo una atención considerable debido a su capacidad única para convertir la radiación de longitud de onda más larga en fluorescencia de longitud de onda más corta [1, 2] y está encontrando amplias aplicaciones en los campos de los láseres de estado sólido [3], pantallas multicolores [ 4], administración de fármacos [5], marcadores biológicos fluorescentes [6], convertidores de longitud de onda para células solares [7], etc. Un fósforo UC se forma comúnmente dopando una red del anfitrión con un par de sensibilizador / activador, donde el sensibilizador suele ser Yb 3+ y el activador suele ser Ho 3+ , Er 3+ o Tm 3+ . Esto se debe a que Yb 3+ puede absorber eficientemente la excitación de láser de infrarrojo cercano de 980 nm y los tres tipos de activadores tienen niveles de energía en forma de escalera que son beneficiosos para la absorción secuencial de fotones y la transferencia de energía [8]. Los fundamentos de la luminiscencia UC y la transferencia de energía en la conversión ascendente de lantánidos se pueden encontrar en los artículos de revisión de Auzel [9] y Dong et al. [10], respectivamente. Gai y col. [8] compiló recientemente el progreso reciente logrado en microcristales / nanocristales de tierras raras para conversión descendente (DC) y UC, incluida la síntesis química blanda, propiedades luminiscentes y aplicaciones biomédicas. Wang y col. [11], por otro lado, resumió ampliamente en su artículo de revisión la aplicación de fósforos UC y DC dopados con iones de tierras raras en termometría óptica. La propiedad de un fósforo UC se ve significativamente afectada por el tipo de red del huésped, combinación de sensibilizador / activador, concentración de dopante, morfología de partículas / cristalitos, cristalinidad, poder de excitación y el sitio de la red real donde reside el ion dopante [8,9,10 , 11,12,13]. Por ejemplo, se identificaron dos sitios cristalográficos activados por Gd no equivalentes en un Er 3+ -dopado Na hexagonal 1,5 Gd 1.5 F 6 fósforo, y mediante espectroscopía de resolución temporal, se demostró que las dos emisiones verdes del 4 S 3/2 nivel de Er 3+ se originan por separado de los sitios cristalográficos de Gd1 (540 nm) y Na2 / Gd2 (550–555 nm), mientras que la emisión roja de 657 nm de los 4 F 2/9 El nivel solo se origina en el sitio de Na2 / Gd2 [12]. Un estudio reciente de la novela Er 3+ -dopado Sr transparente 0.69 La 0.31 F 2.31 La cerámica de vidrio, por otro lado, ilustró que la división del espectro, la relación de extinción térmica, la estabilidad de la población y la sensibilidad a la temperatura de los tres niveles de energía acoplados térmicamente (TCL) de 2 H 2/11 / 4 S 3/2 , 4 F 9/2 (1) / 4 F 2/9 (2) y 4 Yo 2/9 (1) / 4 Yo 2/9 (2) dependen de la potencia de bombeo del láser de 980 nm, y se desarrolló un nuevo método de ajuste para establecer la relación entre las relaciones de intensidad de fluorescencia y la temperatura [13]. Haluros de tierras raras (RE) (como NaYF 4 :Yb / Er) son actualmente los fósforos UC más eficientes debido a sus bajas energías de fonón (ℏω <400 cm −1 ) [8, 10, 11, 14], aunque las materias primas tóxicas implicadas en la síntesis y la sensibilidad del aire de muchos haluros limitan su aplicación y producción. Otro tipo de fósforos UC ampliamente investigados es RE 2 O 3 (como Y 2 O 3 :Yb / Er), cuya energía fonónica relativamente alta (ℏω ~ 600 cm −1 ; ~ 591 cm −1 para Y 2 O 3 y 612 cm −1 para Lu 2 O 3 ) [15], sin embargo, reduce la eficiencia de la luminiscencia UC debido al acoplamiento fotón-fonón. Desde el punto de vista de la biocompatibilidad, Li et al. [16] Yb sintetizado 3+ - y Ho 3+ -cristales de fluorapatito copiado (nanovarillas de 16 por 286 nm) mediante reacción hidrotermal y luminiscencia UC de Ho 3+ a 543 y 654 nm se logró mediante un proceso de dos fotones bajo excitación láser de 980 nm. Los cristales también exhibieron imágenes de células fluorescentes claras después de que las superficies fueran injertadas con dextrano hidrófilo [16].
RE 2 O 2 El sulfuro de sodio es una familia importante de compuestos en el campo del fósforo y puede ser ventajoso sobre el óxido para aplicaciones luminiscentes. Por ejemplo, la aparición de S 2− → Eu 3+ transición de transferencia de carga en Eu 3+ -activado RE 2 O 2 S extiende significativamente la longitud de onda de excitación efectiva a ~ 400 nm [17,18,19], lo que hace que el fósforo sea útil como componente rojo en LED blancos excitados por UV cercano (365–410 nm) según lo revisado por Ye et al. [20]. La técnica más madura para sintetizar RE 2 O 2 S es una reacción de estado sólido, que tiene las ventajas de alto rendimiento y conveniencia, pero la alta temperatura de reacción, la morfología incontrolable del producto y especialmente el empleo de fuentes de azufre nocivas para el medio ambiente son defectos evidentes [21,22,23]. Sulfuración de RE 2 O 3 por H 2 S o CS 2 gas a una temperatura elevada [24,25,26] es otra estrategia de uso frecuente para producir RE 2 O 2 S. Dado que la metodología para la síntesis controlada de RE 2 O 3 es rico y está bien desarrollado, RE 2 O 2 Por lo tanto, se ha producido S con diversas morfologías de partículas a través de la ruta de sulfuración, aunque los procedimientos complicados son menos factibles para la producción industrial. Otras técnicas para RE 2 O 2 La síntesis de S puede incluir precipitación [27], reacción hidrotermal [28], termólisis de polímero en gel en solución en dos pasos [29], síntesis con plantilla de gelatina [30], termólisis en gel [31], síntesis solvotérmica de alivio de presión [32], y combustión [33]. La participación de fuentes o subproductos de azufre nocivos (como C 2 S, H 2 S, y tiourea) es, sin embargo, todavía difícil de evitar. La aparición de hidróxido de tierras raras en capas de tipo sulfato (RE 2 (OH) 4 SO 4 ∙ 2H 2 Oh, entonces 4 2− -LREH) en 2010 [34] brindó una oportunidad única para resolver los problemas antes mencionados, ya que este grupo de compuestos tiene exactamente la misma relación molar RE / S de RE 2 O 2 S. Hidrólisis homogénea de RE 2 (SO 4 ) 3 · 8H 2 O en presencia de Na 2 SO 4 y hexametilentetramina (C 6 H 12 N 4 ) es la técnica clásica para producir SO 4 2− -LREH, pero se limita a RE =Pr – Tb en la familia de los lantánidos [34]. Ampliamos el grupo de compuestos a RE =La – Dy mediante la reacción de soluciones acuosas de RE (NO 3 ) 3 · n H 2 O y (NH 4 ) 2 SO 4 en condiciones hidrotermales [17, 18, 19] y posteriormente manifestó que RE 2 O 2 S se puede producir fácilmente mediante termólisis de SO 4 2− -LREH en atmósfera reductora [17,18,19]. RE 2 O 2 Recientemente se identificó que S tiene una energía de fonón relativamente baja (ℏω ~ 500 cm −1 ) [1], buena estabilidad química y una eficiencia UC particularmente alta comparable a los haluros [35, 36], pero el estudio de este tipo de fósforos UC prometedores está lejos de ser suficiente [8, 10, 11, 37, 38]. La 3+ no ha desocupado 4 f suborbital y es ópticamente inerte y, por tanto, sus compuestos son redes de hospedadores adecuadas para la luminiscencia. Así sintetizamos en este trabajo La 2 O 2 Fósforos S:Yb / RE UC (RE =Ho, Er) mediante el recocido del SO 4 cristalizado hidrotermalmente 2− -LREH en H 2 que fluye , y las propiedades luminiscentes y los procesos UC se elaboraron en detalle.
Métodos
Los materiales de partida de RE (NO 3 ) 3 · 6H 2 O (RE =La, Ho, Er e Yb;> 99,99% de pureza), (NH 4 ) 2 SO 4 (> 99,5% puro) y NH 3 · H 2 La solución de O (28%, pureza ultra alta) se adquirió de Kanto Chemical Co., Inc. (Tokio, Japón) y se utilizó tal como se recibió. Yb 3+ / Ho 3+ - y Yb 3+ / Er 3+ -dopado La 2 (OH) 4 SO 4 · 2H 2 O se sintetizó por separado mediante una reacción hidrotermal. El contenido de dopante es 2 at.% Para Yb 3+ y 1 at.% para Ho 3+ y Er 3+ según la literatura [39]. En una síntesis típica [17], 6 mmol de (NH 4 ) 2 SO 4 se disolvió en 60 ml de una solución acuosa de tierras raras (0,1 mol / L para RE 3+ total ), seguido de la adición gota a gota de NH 3 · H 2 O hasta pH =9. Después de agitar continuamente durante 15 min, la suspensión resultante se transfirió a un autoclave revestido con teflón de 100 ml de capacidad para 24 h de cristalización hidrotermal en un horno eléctrico precalentado a 100ºC. El producto resultante se recogió mediante centrifugación, se lavó con agua filtrada tres veces y con etanol una vez y finalmente se secó al aire a 70 ° C durante 24 h. La 2 O 2 A continuación, se recocieron los fósforos S:Yb / RE UC de su SO 4 2− -Precursores de LREH en el flujo de H 2 (200 mL / min) a 1200 ° C durante 1 h, con una velocidad de calentamiento de 5 ° C / min en la etapa de rampa.
La identificación de fase se realizó mediante difractometría de rayos X (XRD; Modelo RINT2200, Rigaku, Tokio, Japón) bajo 40 kV / 40 mA, utilizando Cu- K filtrado con níquel radiación α (λ =0,15406 nm) y una velocidad de exploración de 1 ° / min. Los parámetros de estructura de los productos se derivaron de los datos XRD utilizando el software TOPAS [40]. La morfología de las partículas se observó mediante microscopía electrónica de barrido de emisión de campo (FE-SEM; Modelo S-5000, Hitachi, Tokio) bajo un voltaje de aceleración de 10 kV. Los espectros de luminiscencia UC se obtuvieron a temperatura ambiente utilizando un espectrofotómetro fluorado FP-6500 (JASCO, Tokio) con excitación láser de infrarrojo cercano de 978 nm de los fósforos con un diodo láser de longitud de onda continua (CW) (Modelo KS3-12322-105, BWT Beijing Ltd., Beijing, China). La relación señal / ruido (S / N) del espectrómetro es ≥ 200, y la sensibilidad se estableció en un valor bajo debido a la fuerte luminiscencia UC de los fósforos. La configuración experimental se puede encontrar en el archivo adicional 1:Figura S1.
Resultados y discusión
La Figura 1 muestra los patrones de XRD de los productos hidrotermales, donde se ve que en cada caso, todos los picos de difracción pueden indexarse bien con el compuesto estratificado de La 2 (OH) 4 SO 4 · 2H 2 O [17, 18]. En una solución acuosa que contiene SO 4 2− , los cationes de tierras raras (RE) sufrirían hidratación e hidrólisis parcial para formar los iones complejos de [RE (OH) x (H 2 O) y (SO 4 ) z ] 3- x -2 z [17,18,19]. Una temperatura más alta o el pH de la solución promoverán RE 3+ hidrólisis, que conduce a más OH - mientras que menos SO 4 2− (SO 4 más pequeño 2− / OH - relación molar) en el ion complejo. En las condiciones hidrotermales optimizadas de 100 ° C y pH =9 [17,18,19], el ion complejo puede tener un SO 4 adecuado 2− / OH - relación molar, y por lo tanto, el objetivo de SO 4 2− El compuesto -LREH se puede cristalizar mediante reacciones de condensación. Los parámetros de estructura de los productos hidrotermales se resumen en la Tabla 1. Está claro que (La 0.97 Ho 0.01 Yb 0.02 ) 2 (OH) 4 SO 4 · 2H 2 O tiene constantes de celosía más grandes ( a , b , c ) y volumen celular ( V ) que (La 0.97 Er 0.01 Yb 0.02 ) 2 (OH) 4 SO 4 · 2H 2 O. Esto es comprensible en vista de que Ho 3+ (1.072 Å para CN =9) es mayor que Er 3+ (1,062 Å para CN =9). Ambos productos tienen constantes de celda y volumen de celda más pequeños que el La 2 sin dopar. (OH) 4 SO 4 · 2H 2 O (SO 4 2− -LLaH), de acuerdo con el hecho de que La 3+ es el más grande (1.216 Å para CN =9) entre los cuatro tipos de iones RE. Los diferentes parámetros de la celda proporcionaron evidencia directa de la formación de una solución sólida.
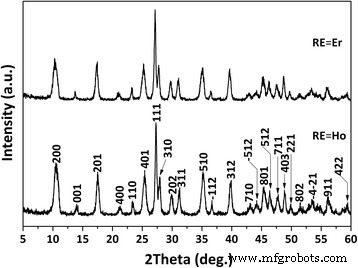
Patrones XRD del (La 0.97 RE 0.01 Yb 0.02 ) 2 (OH) 4 SO 4 · 2H 2 Compuestos en capas de O obtenidos mediante reacción hidrotermal a 100 ° C y pH =9 durante 24 h
La Figura 2 muestra los patrones XRD de los productos recocidos de su SO 4 2− -Precursores de LREH a 1200 ° C durante 1 h en flujo de H 2 . Los picos de difracción se pueden indexar completamente con la estructura hexagonal La 2 O 2 S en cada caso (grupo espacial: P- 3 m 1; Tarjeta JCPDS no. 00-075-1930). SO 4 2− -LLaH se descompondría en La 2 O 2 SO 4 hasta 1200 ° C en el aire a través de las reacciones de La 2 (OH) 4 SO 4 · 2H 2 O → La 2 (OH) 4 SO 4 + 2H 2 O (deshidratación) y La 2 (OH) 4 SO 4 → La 2 O 2 SO 4 + 2H 2 O (deshidroxilación) [17]. En un H 2 atmósfera, el S 6+ en SO 4 2− se reduciría a S 2− siguiendo la reacción de La 2 O 2 SO 4 + 4H 2 → La 2 O 2 S + 4H 2 O, y así, La 2 O 2 S puede resultar con vapor de agua como único subproducto [17]. Los parámetros de la red y el volumen de la celda de (La 0.97 RE 0.01 Yb 0.02 ) 2 O 2 S se muestran en la Tabla 2 junto con los de La 2 O 2 S [17]. La dimensión de la celda decreciente hacia un RE 3+ más pequeño indica la formación exitosa de una solución sólida.
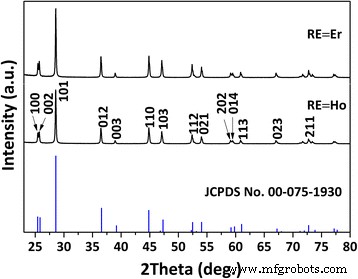
Patrones XRD del (La 0.97 RE 0.01 Yb 0.02 ) 2 O 2 Fósforos de conversión ascendente calcinados a partir de sus precursores estratificados en el flujo de H 2 (200 ml / min) a 1200 ° C durante 1 h. Las difracciones estándar de La 2 O 2 S se incluyen como barras para comparar
La Figura 3 muestra la morfología de las partículas de los precursores estratificados y los fósforos UC resultantes. Se ve que el SO 4 2− -LREH cristalizó como nanoplacas de ~ 150–550 nm de tamaño lateral y ~ 20–30 nm de espesor. Las nanoplacas sufrieron una desintegración significativa tras la calcinación a 1200 ° C para producir partículas redondeadas. El tamaño medio de cristalito se evaluó con la ecuación de Scherrer de ~ 45 nm para los fósforos UC.

Morfologías de partículas FE-SEM del (La 0.97 Ho 0.01 Yb 0.02 ) 2 (OH) 4 SO 4 · 2H 2 O ( a ) y (La 0.97 Er 0.01 Yb 0.02 ) 2 (OH) 4 SO 4 · 2H 2 O ( b ) precursores en capas y el (La 0.97 Ho 0.01 Yb 0.02 ) 2 O 2 S ( c ) y (La 0.97 Er 0.01 Yb 0.02 ) 2 O 2 S ( d ) fósforos de conversión ascendente
La Figura 4a muestra los espectros de luminiscencia UC del (La 0.97 Ho 0.01 Yb 0.02 ) 2 O 2 Fósforo S bajo excitación láser de 978 nm. Las emisiones a ~ 546, 658 y 763 nm se atribuyen a los 5 F 4 → 5 Yo 8 , 5 F 7 → 5 Yo 8 y 5 F 4 → 5 Yo 7 transiciones de Ho 3+ , respectivamente [36], predominando la emisión NIR de 763 nm. El efecto sensibilizador de Yb 3+ es significativa, y ~ 15 y 20 veces más fuertes emisiones verdes (546 nm) y NIR (763 nm, no sensibles a los ojos humanos), respectivamente, se produjeron mediante la codificación de 2 at.% Yb 3+ (Archivo adicional 1:Figura S2a). Bajo un bombeo láser de 50 mW, se observó una emisión verde intensa y vívida para el (La 0.97 Ho 0.01 Yb 0.02 ) 2 O 2 S fósforo a simple vista, como se muestra en el inserto de la Fig. 4a. A pesar de la potencia de excitación, las coordenadas de color CIE calculadas a partir de los espectros de emisión en la región de luz visible (400-700 nm) son estables en aproximadamente (0.30, 0.66), típico de un color verde vivo (Archivo adicional 1:Tabla S1 y Figura S3).
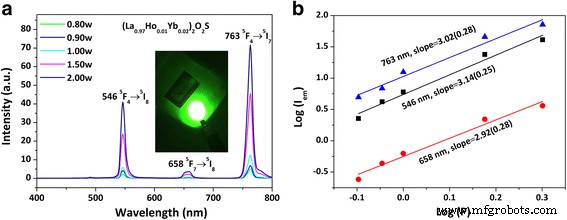
Espectros de luminiscencia de conversión ascendente ( a ) y la relación entre log ( I em ) y log ( P ) ( b ) para el (La 0.97 Ho 0.01 Yb 0.02 ) 2 O 2 S fósforo, donde I em y P son la intensidad de emisión y la potencia de excitación (en vatios), respectivamente. El recuadro en a es una fotografía que muestra la aparición de una fuerte emisión de UC por debajo de 50 mW de excitación láser de 978 nm
En general, el número de fotones necesarios para poblar el estado de emisión superior en condiciones insaturadas se puede obtener de la relación I em ∝ P n [41], donde I es la intensidad de luminiscencia, P la potencia de bombeo, y n el número de fotones láser. La Figura 4b muestra el registro ( I em ) -log ( P ) gráfica de la relación anterior, de la cual n El valor se determinó a partir de la pendiente del ajuste lineal en ~ 3.02, 3.14 y 2.92 (aproximadamente 3) para las emisiones de UC que alcanzaron un máximo de ~ 546, 658 y 763 nm, respectivamente. Por lo tanto, los resultados sugieren que se involucró un proceso de tres fotones para generar la luminiscencia de UC observada.
En principio, tres mecanismos básicos de población, a saber, absorción de estado excitado (AEE), transferencia de energía (ET) y avalancha de fotones, pueden estar implicados en un proceso de CU [8,9,10]. Dado que no se observó ningún umbral de potencia en el rango de este estudio, el mecanismo de avalancha de fotones puede despreciarse. El diagrama de energía de Yb 3+ / Ho 3+ en La 2 O 2 S rara vez se ha informado y no está disponible para nuestra comparación. No obstante, la luminiscencia UC que involucra tres fonones se vio en el trabajo anterior en Yb 3+ / Ho 3+ -sistemas de otros materiales codopados [42, 43]. Por lo tanto, el diagrama de energía y el proceso UC de (La 0.97 Ho 0.01 Yb 0.02 ) 2 O 2 S se construyeron en la Fig.5 haciendo referencia a estos estudios previos y se detallan a continuación:(1) excitación de Yb 3+ por fotones láser [ESA; 2 F 7/2 (Yb 3+ ) + hν (978 nm) → 2 F 5/2 (Yb 3+ )]; (2) población de los 5 Yo 6 nivel de energía de Ho 3+ después de Yb 3+ absorbiendo el primer fotón láser y transfiriendo energía a Ho 3+ [ET1; 2 F 5/2 (Yb 3+ ) + 5 Yo 8 (Ho 3+ ) → 2 F 7/2 (Yb 3+ ) + 5 Yo 6 (Ho 3+ )]; (3) relajación no radiativa (NR) a los 5 Yo 7 nivel de Ho 3+ [NR; 5 Yo 6 (Ho 3+ ) ~ 5 Yo 7 (Ho 3+ )]; (4) excitación de Ho 3+ desde el 5 Yo 7 a 5 F 5 nivel después de Yb 3+ absorbiendo el segundo fotón láser y transfiriendo energía a Ho 3+ [ET2; 2 F 5/2 (Yb 3+ ) + 5 Yo 7 (Ho 3+ ) → 2 F 7/2 (Yb 3+ ) + 5 F 5 (Ho 3+ )]; (5) Relajación NR al 5 Yo 5 nivel de Ho 3+ [ 5 F 5 (Ho 3+ ) ~ 5 Yo 5 (Ho 3+ )]; (6) excitación de Ho 3+ desde el 5 Yo 5 a 5 F 4 / 5 S 2 nivel después de Yb 3+ absorbiendo el tercer fotón láser y transfiriendo energía a Ho 3+ [ET3; 2 F 5/2 (Yb 3+ ) + 5 Yo 5 (Ho 3+ ) → 2 F 7/2 (Yb 3+ ) + 5 F 4 / 5 S 2 (Ho 3+ )]; y (7) retroceso de los electrones excitados de los 5 poblados F 4 / 5 S 2 nivel al 5 Yo 8 estado fundamental para producir la emisión verde (~ 546 nm; 5 F 4 , 5 S 2 → 5 Yo 8 ). Los electrones también pueden relajarse hasta los 5 F 5 y 5 Yo 4 niveles a través de procesos NR, de los cuales el rojo (~ 658 nm; 5 F 5 → 5 Yo 8 ) e infrarrojo cercano (~ 763 nm; 5 Yo 4 → 5 Yo 8 ) se produjeron emisiones. La fuerte emisión de UC en el infrarrojo cercano a ~ 763 nm puede implicar que la relajación de NR en 5 Yo 8 el nivel de energía es significativo.
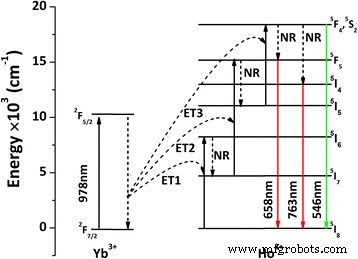
Una ilustración esquemática de los niveles de energía y los procesos de UC para el (La 0.97 Ho 0.01 Yb 0.02 ) 2 O 2 Fósforo
El 2 F 5/2 → 2 F 7/2 transición de emisión de Yb 3+ y el 4 Yo 15/2 → 4 Yo 2/11 transición de excitación de Er 3+ tienen energías que combinan bien, lo que hace que Yb 3+ / Er 3+ el par activador / sensibilizador más ampliamente investigado para la luminiscencia de UC en varios tipos de redes de acogida [8,9,10,11,12,13]. Similar a Ho 3+ , la emisión de UC de Er 3+ también se mejoró drásticamente con Yb 3+ codoping (Archivo adicional 1:Figura S2b). Tomando la emisión verde de 527 nm, por ejemplo, 2 at.% De Yb 3+ mejorado el Er 3+ luminiscencia por un factor de ~ 14. Bajo excitación láser de 978 nm, el (La 0.97 Er 0.01 Yb 0.02 ) 2 O 2 El fósforo S UC exhibe bandas de emisión en las regiones verde (~ 527 y 549 nm), rojo (~ 668 y 672 nm) e infrarrojo cercano (~ 807 y 858 nm) (Fig. 6a), que surgen de la 2 H 2/11 / 4 S 3/2 → 4 Yo 15/2 , 4 F 2/9 → 4 Yo 15/2 y 4 Yo 2/9 → 4 Yo 15/2 transiciones de Er 3+ , respectivamente [32]. Las coordenadas de color determinadas para la luminiscencia UC en la región de luz visible (400-700 nm) derivaron de la región verde amarillenta [(0.36, 0.61)] a verde [(0.32, 0.64)] en el diagrama de cromaticidad CIE junto con el aumento potencia de excitación de 0,7 a 2,0 W (Archivo adicional 1:Figura S3b y Tabla S2). El cambio de color también concuerda bien con la relación de intensidad gradualmente mayor de las emisiones de verde a rojo ( I 549 / Yo 668 y yo 527 / Yo 668 , Archivo adicional 1:Tabla S3) bajo una mayor potencia de excitación. Ajuste del color de emisión dependiente de la potencia de excitación del Yb 3+ / Er 3+ par se observó previamente en Y 2 O 2 S [44]. El número de fotones de bombeo necesarios para poblar los estados emisores se derivó de la pendiente del registro ( I em ) -log ( P ) parcela (Fig. 6b), y se encontró que los tres grupos de emisiones tenían n similares valores de ~ 2. Esto indica que un proceso de dos fonones es en gran parte responsable de la luminiscencia UC observada.
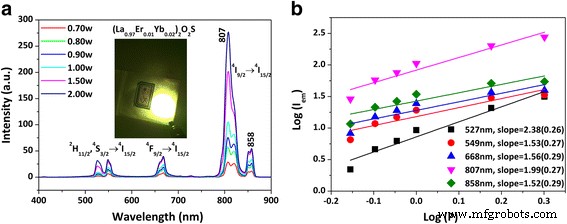
Espectros de luminiscencia de conversión ascendente ( a ) y la relación entre log ( I em ) y log ( P ) ( b ) para el (La 0.97 Er 0.01 Yb 0.02 ) 2 O 2 S fósforo, donde I em y P son la intensidad de emisión y la potencia de excitación (en vatios), respectivamente. El recuadro en a es una fotografía que muestra la fuerte emisión de UC de (La 0.97 Er 0.01 Yb 0.02 ) 2 O 2 S por debajo de 50 mW de excitación láser de 978 nm
El diagrama de energía y el proceso de fotones que conducen a la luminiscencia UC de (La 0.97 Er 0.01 Yb 0.02 ) 2 O 2 S se muestran esquemáticamente en la Fig. 7. Absorción en estado excitado e Yb 3+ → Er 3+ La excitación de transferencia de energía está implicada principalmente en el mecanismo de CU, siendo este último el dominante [8,9,10,11,12,13,14,39,43]. Tras la excitación con láser de 978 nm, el 2 F 7/2 electrones en estado fundamental de Yb 3+ son bombeados al 2 F 5/2 estado excitado (ESA). Desde el 2 F 5/2 nivel de Yb 3+ y el 4 Yo 2/11 nivel de Er 3+ se combinan bien entre sí, la transferencia de energía de Yb 3+ a Er 3+ se lleva a cabo fácilmente. El Er 3+ De este modo, los electrones pueden excitarse a partir de los 4 Yo 15/2 estado fundamental al 4 Yo 2/11 nivel con la energía transferida desde Yb 3+ (un fotón, ET1). La sección transversal de absorción de Er 3+ es más pequeño que el de Yb 3+ a ~ 980 nm [42, 45], por lo que la transferencia de energía (ET) domina la excitación real de Er 3+ . La energía de excitación en el 4 Yo 2/11 El nivel puede relajarse de forma no radiativa (NR) al 4 Yo 13/2 nivel, desde el cual los electrones pueden excitarse hasta 4 F 7/2 estado por ET de un segundo fotón láser (ET2). Después de los procesos de NR, los tres grupos de emisiones (Fig. 6a) se pueden producir mediante las transiciones electrónicas que se muestran en la Fig. 7. Las reacciones de fotones de todo el proceso de UC se pueden presentar de la siguiente manera:(1) 2 F 7/2 (Yb 3+ ) + hν (978 nm) → 2 F 5/2 (Yb 3+ ) y 4 Yo 15/2 (Er 3+ ) + h ν (978 nm) → 4 Yo 2/11 (Er 3+ ); (2) 2 F 5/2 (Yb 3+ ) + 4 Yo 15/2 (Er 3+ ) → 2 F 7/2 (Yb 3+ ) + 4 Yo 2/11 (Er 3+ ); (3) 4 Yo 2/11 (Er 3+ ) ~ 4 Yo 13/2 (Er 3+ ); (4) 2 F 5/2 (Yb 3+ ) + 4 Yo 13/2 (Er 3+ ) → 2 F 7/2 (Yb 3+ ) + 4 F 7/2 (Er 3+ ); (5) 4 F 7/2 (Er 3+ ) ~ 2 H 2/11 / 4 S 3/2 (Er 3+ ), 4 F 2/9 (Er 3+ ) y 4 Yo 2/9 (Er 3+ ); y (6) 2 H 2/11 / 4 S 3/2 (Er 3+ ) → 4 Yo 15/2 (Er 3+ ) + hν (~ 527 y 549 nm), 4 F 2/9 (Er 3+ ) → 4 Yo 15/2 (Er 3+ ) + hν (~ 668 y 672 nm) y 4 Yo 2/9 (Er 3+ ) → 4 Yo 15/2 (Er 3+ ) + hν (~ 807 y 858 nm). El cambio de color de emisión mencionado anteriormente puede sugerir una población más eficiente de 4 F 7/2 (Er 3+ ) nivel de energía bajo una mayor potencia de excitación, y el 4 F 7/2 (Er 3+ ) ~ 2 H 2/11 / 4 S 3/2 (Er 3+ ) El proceso NR se vuelve sucesivamente más fuerte que 4 F 7/2 (Er 3+ ) ~ 4 F 2/9 (Er 3+ ).
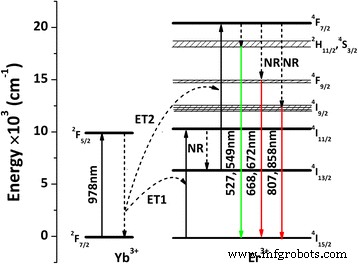
A schematic illustration of the energy levels and UC processes for (La0.97 Er0.01 Yb0.02 )2 O2 S phosphor
Conclusiones
(La0.97 RE0.01 Yb0.02 )2 O2 S upconversion (UC) nanophosphors (RE=Ho, Er) were successfully produced via thermal decomposition of their layered hydroxyl sulfate precursors in flowing H2 at 1200 °C, with water vapor as the only exhaust. The precursors crystallized as nanoplates with the lateral sizes of ~ 150–550 nm and thicknesses of ~ 20–30 nm, which disintegrated into rounded nanoparticles (average crystallite size:~ 45 nm) upon thermal decomposition. The oxysulfide phosphors exhibit strong UC luminescence under 978-nm laser excitation, through a three-photon process for Ho 3+ and a two-photon process for Er 3+ . For the UC luminescence in the visible region (400–700 nm), the chromaticity coordinates of (La0.97 Ho0.01 Yb0.02 )2 O2 S are stable at around (0.30, 0.66), while those of (La0.97 Er0.01 Yb0.02 )2 O2 S changed from about (0.36, 0.61) to (0.32, 0.64) along with the excitation power increasing from 0.7 to 2 W.
Nanomateriales
- Ajuste del rendimiento tribológico de nanoplaquetas de fosfato de circonio en capas en aceite mediante modificaciones de la superficie y de la capa intermedia
- Preparación de nanoesferas poliméricas impresas con iones de paladio (II) y su eliminación del paladio (II) de la solución acuosa
- Síntesis y caracterización de BiOCl modificado y su aplicación en la adsorción de tintes de baja concentración a partir de una solución acuosa
- Dependencia de la temperatura de fonones E2g en el plano con actividad Raman en grafeno en capas y escamas de h-BN
- Saponinas Platycodon de Platycodi Radix (Platycodon grandiflorum) para la síntesis verde de nanopartículas de oro y plata
- Evolución de la fotoluminiscencia, Raman y la estructura de los microalambres de perovskita CH3NH3PbI3 bajo exposición a la humedad
- Mejora de la absorción de banda ancha y multibanda de grafeno monocapa en frecuencias ópticas a partir de resonancias magnéticas dipolo múltiples en metamateriales
- Electrocatalizadores de reducción de oxígeno Fe-N-C altamente activos y estables derivados de electrohilado y pirólisis in situ
- Síntesis e investigación de nanocables de CuGeO3 como materiales anódicos para baterías avanzadas de iones de sodio
- Crecimiento propio de MOCVD y fotoluminiscencia mejorada espectacularmente de nanocables de núcleo-carcasa de InGaAs / InP
- Evaluación de la toxicidad de las nanopartículas de PEG-PCCL e investigación preliminar sobre su efecto antitumoral de la carga de paclitaxel



