Preparación de nanoesferas poliméricas impresas con iones de paladio (II) y su eliminación del paladio (II) de la solución acuosa
Resumen
Se utilizaron tres tipos de monómeros funcionales, 4-vinilpridina (4-VP), ácido 2- (aliltio) nicotínico (ANA) y ácido 2-acetamidoacrílico (AAA), para sintetizar nanoesferas poliméricas (Pd (II) IIPs) mediante el método de precipitación-polimerización con el fin de estudiar los efectos de diferentes monómeros funcionales sobre las propiedades de adsorción de materiales impresos con iones. Los resultados de los espectros UV para estudiar la interacción entre el ion plantilla PdCl 4 2− y los monómeros funcionales mostraron que hubo grandes diferencias en la estructura después de que la plantilla reaccionó con tres monómeros funcionales, 4-VP y ANA causaron un gran cambio estructural, mientras que AAA básicamente no cambió. Otros resultados sobre el rendimiento de adsorción de Pd (II) IIP en Pd (II) confirmaron que 4-VP era el candidato más prometedor para la síntesis de Pd (II) IIP con una capacidad de adsorción de 5.042 mg / g en comparación con ANA y AAA . Se investigó la influencia de los parámetros operativos en el rendimiento de Pd (II) IIP sobre la adsorción de Pd (II). Hubo un aumento en la capacidad de adsorción de Pd (II) IIP a mayor pH, temperatura y concentración inicial de Pd (II). Los resultados de los experimentos de adsorción competitiva de múltiples metales mostraron que los Pd (II) IIP tenían selectividad por Pd (II). Se pudo alcanzar un equilibrio de adsorción a los 180 min. El análisis cinético mostró que los datos de la prueba de adsorción se ajustaban mejor al modelo cinético de pseudo-segundo orden, y la capacidad de adsorción en equilibrio teórico era de aproximadamente 5,085 mg / g. Las isotermas de adsorción de Pd (II) por Pd (II) IIP concordaron bien con la ecuación de Freundlich, lo que sugiere una reacción de adsorción favorable en condiciones óptimas. Estos resultados mostraron que los Pd (II) IIP tienen una aplicación potencial en la eliminación de Pd (II) de soluciones acuosas y pueden proporcionar cierta información para la selección de monómeros funcionales en la preparación de Pd (II) IIP.
Antecedentes
El paladio con propiedades físicas y químicas únicas se usa ampliamente en materiales de galvanoplastia, catalizadores, aleaciones dentales y aleaciones de soldadura fuerte [1, 2]. Con la aplicación cada vez mayor de paladio en varios campos, se puede producir una cantidad considerable de aguas residuales que contienen paladio. La descarga de aguas residuales que contienen paladio no solo puede causar un grave desperdicio de recursos, sino que también puede causar una gran contaminación al medio ambiente y dañar la salud humana [3, 4, 5, 6]. En algunos estudios, la separación y el enriquecimiento pueden resolver estos problemas; los métodos habituales de enriquecimiento y separación incluyen la coprecipitación [7], la adsorción [8] y el intercambio iónico [9], la extracción líquido-líquido [10] y la extracción en fase sólida [11] , extracción de micro-líquidos [12] y extracción del punto de enturbiamiento [13]. Hay muchos estudios sobre el enriquecimiento y la separación del paladio [14,15,16,17,18]; entre ellos, el método de adsorción se usa ampliamente de muchas maneras porque es simple, conveniente y eficiente. El rendimiento de los adsorbentes comunes incluye carbón activado, sin embargo, no es altamente selectivo para secuestrar iones de paladio de soluciones acuosas que contienen varios metales. Por lo tanto, el desarrollo de material de separación de paladio con alta selectividad para la eliminación, recuperación y reciclaje de iones de paladio de la solución de desecho es de gran importancia.
Las nanoesferas poliméricas impresas con iones con alta selectividad para la separación de metales de una solución acuosa en comparación con otros adsorbentes comunes se han convertido en uno de los puntos calientes de la investigación en los últimos años [19,20,21,22,23]. En la preparación de nanoesferas poliméricas impresas con iones, la estabilidad de los quelatos formados por monómeros funcionales con diferentes grupos funcionales e ión metálico por enlace iónico o enlace de coordinación depende de la fuerza de interacción entre el monómero funcional y los iones metálicos, cuanto más fuerte es la interacción, cuanto más fuerte es la capacidad del polímero con impresión de iones para quelar los iones metálicos y mayor es el rendimiento de adsorción. Por eso es importante seleccionar monómeros funcionales [24].
Muchos estudios utilizaron 4-VP como monómero funcional en la preparación de Pd (II) IIP, mientras que pocos estudios han incluido la comparación de 4-VP con otros monómeros funcionales [25,26,27,28,29,30]. En este estudio, se utilizaron dos tipos de monómeros funcionales poco comunes ANA y AAA para compararlos con 4-VP comunes. La interacción entre PdCl 4 2− y el monómero funcional se analizó mediante barrido UV de longitud de onda completa. Luego, se seleccionó el mejor monómero funcional comparando el efecto de adsorción de Pd (II) IIP correspondientes a tres monómeros funcionales en paladio (II). A través de experimentos de adsorción por lotes, se evaluó el rendimiento de adsorción de Pd (II) IIP para iones de paladio (II) en soluciones acuosas. Se utilizaron varios medios de caracterización de FTIR, SEM y TGA para explorar más a fondo el mecanismo correspondiente de adsorción de Pd (II) en Pd (II) IIP.
Métodos
Materiales
Los siguientes productos químicos K 2 PdCl 4 , Se adquirieron 4-vinil piridina (4-VP, 96%), ácido 2-alil sulfhidril nicotínico (ANA, 98%), ácido 2-acetamidoacrílico (AAA, 99%) y dimetacrilato de etilenglicol (EGDMA, 98%) de la empresa Alfa en EE. UU. Se adquirió azo isobutironitrilo (AIBN, 99%) de Shanghai zhongfugang Co. Ltd. La solución estándar de elemento único de paladio se adquirió de la red nacional de materiales estándar de China. Todos los productos químicos estaban en grados de reactivo analítico y se usaron sin más modificaciones. Se utilizó agua ultrapura para preparar todas las soluciones. Todo el material de vidrio se limpió y enjuagó con agua Milli-Q y luego se secó en un horno durante la noche antes de usarlo.
Preparación de nanoesferas poliméricas impresas con iones de paladio (II)
Las nanoesferas poliméricas impresas con iones de paladio (II) se sintetizaron mediante el método de precipitación-polimerización. En el procedimiento de precipitación, se prepararon Pd (II) IIP de acuerdo con la proporción de plantilla (PdCl 4 2− ), monómeros funcionales (4-VP, ANA, AAA) y monómero de reticulación a 1:4:40. En el procedimiento de polimerización, se usó etilenglicoldimetacrilato (EGDMA) como monómero de reticulación, la mezcla de polimerización también incluyó 2,2-azobisisobutironitrilo (AIBN, iniciador) y metanol (Porogen). La operación detallada es la siguiente:
En primer lugar, 0,1 mmol K 2 PdCl 4 se disolvió en 20 mL de metanol en un matraz de vidrio de 50 mL, luego se añadió 0,4 mmol de 4-VP y se agitó en un oscilador termostático a 25 ° C durante 3 h. En segundo lugar, se añadieron 4 mmol de EGDMA y 36,13 mg de AIBN al matraz de vidrio y la solución obtenida se transfirió a botellas a presión de pared gruesa. El oxígeno de la solución de muestra se eliminó burbujeando gas nitrógeno a través de la muestra durante 10 min. La polimerización se realizó en un baño de agua a 60 ° C durante 24 h con agitación a 180 rpm. El polímero preparado se lavó varias veces con 1:4 ( v / v ) metanol / agua para eliminar los materiales que no han reaccionado y luego los iones de paladio (PdCl 4 2− ) se lixivió del material polimérico agitando con 4 x 50 ml de HCl 1:1 durante 24 h hasta que la solución de lavado estuvo libre de iones paladio. Finalmente, se lavó con agua desionizada hasta alcanzar un pH neutro. Los polímeros se secaron al vacío en un desecador. De la misma manera, se prepararon los polímeros no impresos (NIP) pero sin dopar iones de paladio.
Caracterizaciones
Se utilizó un espectrofotómetro ultravioleta visible (UV-2600, Shimadzu, Japón) para analizar la interacción entre PdCl 4 2− y monómero funcional. Se utilizó un microscopio electrónico de barrido de emisión de campo (SU8040, Hitachi, Japón) para observar los cambios morfológicos del polímero con impresión de iones antes y después de la elución y el polímero sin impresión de iones. Los espectros de infrarrojos por transformada de Fourier (FTIR) de los IIP de Pd (II) antes y después de la elución, y los NIP se analizaron con un espectrómetro FTIR (Nicolet 6700, Thermo-Nicolet, EE. UU.) Con gránulos de KBr en el rango de 4000 ~ 400 cm −1 . Se utilizó la prueba de Brunauer, Emmett, Teller (BET, TriStarII3020) para analizar el área de superficie específica. El análisis de termogravimetría (TGA) se realizó utilizando Netzsch STA-409PC (Alemania) de 313 a 873 K bajo una atmósfera de nitrógeno seco, y la velocidad de calentamiento fue de 10 K / min.
Experimentos de adsorción por lotes
La concentración de Pd (II) se determinó mediante espectrofotometría de absorción atómica de llama (FAAS, TAS-990, Persee, China). Todos los experimentos de adsorción por lotes se realizaron usando un oscilador termostático a 180 rpm con 10 mg de adsorbente en un tubo de centrífuga de plástico de 50 ml que contenía 10 ml de solución metálica. Se tomaron muestras por triplicado para todos los experimentos por lotes. El efecto de la temperatura sobre la adsorción de Pd (II) sobre Pd (II) IIP se evaluó a 15, 25, 35, 45 y 55 ° C. Se eligieron cuatro iones metálicos interferentes que incluyen Pt (II), Zn (II), Cu (II) y Ni (II) con una concentración inicial de 10 mg / L para estudiar el efecto de múltiples metales sobre la adsorción de Pd (II) .
Se llevaron a cabo experimentos de adsorción de isotermas con una dosis constante de adsorbentes y una concentración variable de Pd (II) en el rango de 1 ~ 80 mg / L a 25 ° C (pH 2). Los experimentos cinéticos de adsorción se llevaron a cabo recolectando la solución a intervalos de tiempo predeterminados (el tiempo de muestreo se estableció en 5, 8, 10, 15, 20, 25, 30, 40, 60, 120, 180, 240 y 300 min) y analizando la concentración de metales en las soluciones acuosas.
El porcentaje de eliminación de Pd (II) y la capacidad de adsorción de los Pd (II) IIP para iones Pd (II) se pueden calcular de acuerdo con las siguientes ecuaciones:
$$ r =\ left ({c} _0- {c} _e \ right) / {c} _0 \ times 100 \% $$ (1) $$ q =\ left ({c} _0- {c} _e \ right) \ times V / m $$ (2)en el que r (%) es la eficiencia de eliminación de Pd (II), q (mg / g) es la capacidad del Pd (II) adsorbido en el adsorbente de Pd (II) IIP, c e (mg / L) es la concentración de Pd (II) en solución en equilibrio, c 0 (mg / L) es la concentración inicial de Pd (II) en solución, V (mL) es el volumen de la solución de Pd (II) y m (mg) es la masa de adsorbente.
Los modelos de isotermas de Langmuir (ecuación 3) y Freundlich (ecuación 4) se pueden representar matemáticamente mediante las siguientes ecuaciones:
$$ \ frac {c_e} {q_e} =\ frac {1} {bq_m} + {c} _e \ frac {1} {q_m} $$ (3) $$ \ ln {q} _e =\ ln {K } _f + \ frac {1} {n} \ veces \ ln {c} _e $$ (4)donde q e es la cantidad de Pd (II) adsorbida en los adsorbentes en equilibrio (mg / g), q m es la capacidad de adsorción máxima teórica de los adsorbentes en determinadas condiciones (mg / g), c e es la concentración de Pd (II) en soluciones acuosas en equilibrio (mg / L), b es la constante de Langmuir conectada a la afinidad entre el Pd (II) y los adsorbentes (L / mg), K f es la constante de Freundlich relacionada con la capacidad de adsorción de los adsorbentes, y 1 / n es el factor de heterogeneidad que va de 0 a 1.
Con el fin de aclarar aún más la dinámica y el mecanismo de control de la velocidad para el proceso de adsorción, se utilizaron dos modelos cinéticos de uso común, es decir, la cinética de pseudo primer orden y la cinética de pseudo-segundo orden, para simular los datos experimentales de adsorción. La cinética de pseudo primer orden (Ec. 5) y la cinética de pseudo-segundo orden (Ec. 6) se pueden expresar matemáticamente como:
$$ {q} _t ={q} _e \ left (1- {e} ^ {\ left (- {k} _1t \ right)} \ right) $$ (5) $$ {q} _t =\ frac {q_e ^ 2 {k} _2t} {1+ {q} _e {k} _2t} $$ (6)donde q e es la cantidad de Pd (II) adsorbida en los adsorbentes en equilibrio (mg / g), t es el tiempo de contacto durante el proceso de adsorción, q t es la cantidad de Pd (II) adsorbida en los adsorbentes en cualquier momento t (mg / g), k 1 es la constante de velocidad del modelo de pseudo primer orden (min −1 ) y k 2 es la constante de velocidad del modelo de pseudo segundo orden (g / mg min).
Resultados y discusión
La optimización del monómero funcional
Los espectros UV de PdCl 4 2− y 4-VP, y ANA y AAA en metanol antes y después de la interacción se muestran en la Fig. 1. Se puede ver en la figura que PdCl 4 2− tiene dos picos de absorción a 219,4 y 242,4 nm, y los picos de absorción se desplazan cuando se añaden diferentes monómeros funcionales. Cuando se dosifica el monómero funcional de 4-VP (Fig. 1a), hay un efecto hipocrómico sobre el PdCl 4 2− apareció a 219,4 y 242,4 nm, y se formó un nuevo pico de absorción alrededor de 275 nm como resultado del efecto hipercrómico en comparación con el de 219,4 nm, lo que sugiere los cambios obvios en la estructura de PdCl 4 2− y 4-VP en las proximidades de 275 nm. Cuando se agregó ANA en PdCl 4 2− solución de metanol como monómero funcional (Fig. 1b), PdCl 4 2− apareció un fenómeno de desplazamiento hacia el rojo a 219,4 y 242,4 nm, y dos nuevos picos de absorción surgieron en las proximidades de 285 y 347 nm en comparación con el pico de absorción a 219,4 nm, los dos picos recién formados se pueden atribuir al efecto hipocrómico, lo que indica que ambos PdCl 4 2− y ANA tienen alguna diferencia en sus estructuras en la vecindad de 285 y 347 nm. Puede verse en la Fig. 1c que la adición de AAA no produce ningún desplazamiento hacia el rojo ni hacia el azul en el pico de absorción de PdCl 4 2− a 219,4 y 242,4 nm, y no hay un nuevo pico de absorción, lo que indica un cambio insignificante en la estructura de PdCl 4 2− y AAA.
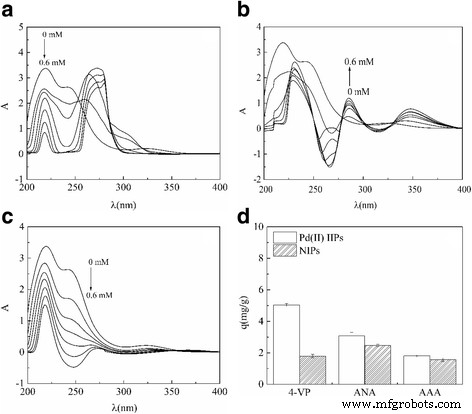
Espectros ultravioleta de las interacciones entre PdCl 4 2− y ( a ) 4 vicepresidente, ( b ) ANA, ( c ) AAA en metanol y ( d ) propiedades de adsorción de Pd (II) IIP sintetizadas por diferentes monómeros de función
Con el fin de estudiar más a fondo el efecto de adsorción de Pd (II) en Pd (II) IIP y NIP preparados por 4-VP, ANA y AAA, se midió la adsorción de Pd (II) en cada material. Como se muestra en la Fig. 1d, la cantidad de iones Pd (II) adsorbidos en los IIP de Pd (II) fue mayor que en los NIP correspondientes. Además, según el método BET, se calculó la superficie de las PII y las NIP (Tabla 1):la superficie de las PII preparadas por 4-VP es de 23,74 m 2 / g superan los NIP (0,46 m 2 /gramo). Significa que se produjo una especie de nanoesferas poliméricas Pd (II) IIP con una superficie más grande después de agregar el ión impreso. Esta observación se puede interpretar por las diferencias significativas en la estructura espacial de Pd (II) IIP y NIP con el mismo tipo de monómeros funcionales. En el proceso de formación de Pd (II) IIP, debido a la adición del ion Pd (II) impreso, el monómero funcional y el ion Pd (II) formaron un complejo de coordinación con las cavidades de impresión y el orificio del Pd (II) ) presenta una "memoria", que conduce a una mayor cantidad de adsorción de iones Pd (II) en Pd (II) IIP que en NIP. Además, la Tabla 1 mostró que la capacidad de adsorción de Pd (II) de los tres tipos de polímeros aumentó con un orden de 4-VP> ANA> AAA, lo que indica que los IIP de Pd (II) preparados por 4-VP eran los mejores. Los resultados fueron causados por el par solitario de electrones de los átomos de N en la estructura de 4-VP que no solo se pueden quelar con iones metálicos, sino que también forman enlaces de hidrógeno con grupos funcionales como los grupos carboxilo e hidroxilo. Además, los grupos vinilo en la estructura pueden reaccionar con el agente de reticulación de modo que el átomo de N cuelga de la cadena del polímero para formar un polielectrolito alcalino débil.
Al comparar la estructura de estos tres tipos de monómeros funcionales (Fig.2) y los resultados de la prueba de adsorción, encontramos que el efecto de adsorción de heterociclos de nitrógeno que contienen 4-VP fue el mejor, seguido por ANA que contiene tanto heterociclos de nitrógeno como grupos carboxilo, y lo peor fue AAA que contenía grupos carboxilo. Por lo tanto, especulamos que la unión de los iones Pd (II) y los monómeros funcionales que contienen heterociclos de nitrógeno son más fuertes que los que contienen grupos carboxilo, y la presencia de grupos carboxilo puede debilitar la unión de los iones Pd (II) y los monómeros funcionales que contienen ambos heterociclos de nitrógeno. y grupos carboxilo.
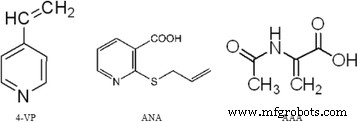
Fórmula estructural de tres monómeros funcionales
Todos los Pd (II) IIP mencionados en los siguientes estudios se prepararon utilizando 4-VP como monómero funcional.
Características de Pd (II) IIP y NIP
Se observó la morfología microscópica de Pd (II) IIP lixiviados, Pd (II) IIP no lixiviados y NIP. Puede verse en la Fig. 3a, d que no hay cambios en la morfología de las IIP de Pd (II) no lixiviadas ni de las IIP de Pd (II) lixiviadas; Además, el método BET mostró que la superficie específica de Pd (II) IIP lixiviada (23,74 m 2 / g) fue similar con los IIP de Pd (II) no lixiviados (22,49 millones 2 / g), la pequeña diferencia puede ignorarse, por lo que se puede concluir que la elución no tiene ningún efecto sobre la morfología de los Pd (II) IIP. La superficie del polímero se vuelve relativamente rugosa después de la adición del PdCl 4 2− plantilla, que se debe a la formación de agujeros impresos. En comparación, los NIP exhiben una superficie más lisa (Fig.3e) con un tamaño de partícula mucho mayor de 2 μm que el de los IIP de Pd (II) no lixiviados y los IIP de Pd (II) lixiviados (alrededor de 200 nm) con el mismo aumento. Este hallazgo indicó que la adición de la plantilla PdCl 4 2− ejerce una gran influencia en las propiedades morfológicas del polímero con impresión de iones de paladio (II).

SEM de ( a ) 4-VP - PII lixiviados, ( b ) ANA:Pd (II) PII lixiviados, ( c ) IIP Pd (II) lixiviados con AAA, ( d ) 4-VP - PII sin depurar, ( e ) 4-VP - NIP lixiviados. (Todas las imágenes con el mismo aumento en 20.000X)
Se puede observar un comportamiento de descomposición diferente a partir de las curvas termogravimétricas de Pd (II) IIP no lixiviado, Pd (II) IIP lixiviado y NIP (Fig. 4a). A temperaturas más bajas de 40 ~ 100 ° C, la tasa de descomposición térmica es relativamente baja. La pérdida de peso se atribuye principalmente a la evaporación de moléculas de agua libres y / o unidas. La composición principal de las muestras aún no ha comenzado a descomponerse a una temperatura de 100 ~ 250 ° C. A una temperatura superior a 250 ° C, las muestras comienzan a perder peso rápidamente; esto se debe principalmente a la descomposición de materias orgánicas en los polímeros con el aumento de temperatura. A medida que la temperatura se eleva por encima de 440 ° C, las materias orgánicas de los polímeros se han descompuesto por completo, alcanzando un estado de estabilidad térmica. Cuando la temperatura sube a 600 ° C, el porcentaje en masa de residuos de Pd (II) IIP sin lixiviar llega a alrededor del 6%. Se supone que las materias residuales están compuestas principalmente de paladio inorgánico.
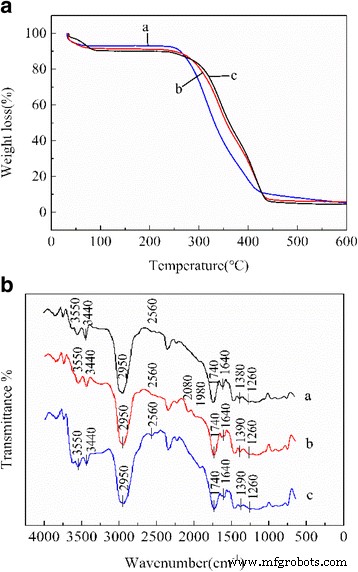
un Curvas TGA de a:Pd (II) IIP no lixiviado, b:Pd (II) lixiviado IIP, c:NIP; ( b ) Espectros FTIR de a:Pd (II) IIP no lixiviados, b:Pd (II) IIP lixiviados, c:NIP
Con base en los picos y bandas de absorción en los espectros FTIR, se pueden representar y caracterizar muchos grupos funcionales en la superficie del material absorbente para Pd (II) IIP no lixiviados, Pd (II) IIP lixiviados y NIP (Fig. 4b). Se puede ver en la figura que las bandas observadas a 3440 y 1640 cm −1 se asignan a la frecuencia de vibración de estiramiento de C-N y -CONH- en amida, respectivamente. Los picos a 3550, 2950, 2560, 2350, 1740 y 1260 cm −1 se atribuyen a la frecuencia de vibración de estiramiento de −OH, C-H, S-H, C =O en ésteres y C-O, respectivamente. No hay cambio entre estos picos de absorción vibratoria en las tres curvas FTIR debido a la falta de coordinación. Como se muestra en la curva by la curva c, el pico atribuido a C-N pasó de 1390 a 1380 cm −1 después de añadir el ión plantilla Pd (II), lo que indica que se produjo la coordinación entre el ión plantilla Pd (II) y el monómero funcional. Además, aparecieron nuevos picos de absorción a 2080 y 1980 cm −1 en la curva b puede ser causado por el proceso de elución de Pd (II) que puede conducir a algunos cambios en los grupos.
Experimentos de adsorción por lotes
El efecto de la concentración inicial de iones Pd (II) sobre la capacidad de adsorción de Pd (II) IIP se muestra en la Fig. 5a. Cuando se fija la dosis de Pd (II) IIP, la capacidad de adsorción de Pd (II) IIP para iones Pd (II) aumenta con el aumento de la concentración inicial de iones adsorbato, mientras que la eficiencia de eliminación disminuye en consecuencia. Esto se debe a los sitios de adsorción limitados proporcionados por Pd (II) IIP en solución. A una concentración más baja de Pd (II), la cantidad de sitios de adsorción activos es abundante para absorber la mayoría de los iones de Pd (II) en solución. Sin embargo, a medida que aumenta la concentración inicial de iones Pd (II), el número disponible de sitios de adsorción activa está limitado por la dosis fija de adsorbente. No hay más sitios activos para combinar el exceso de iones Pd (II) en una concentración más alta. Acompañado por la saturación gradual de la capacidad de adsorción de Pd (II) IIP, hay una disminución constante en la eficiencia de eliminación de Pd (II).
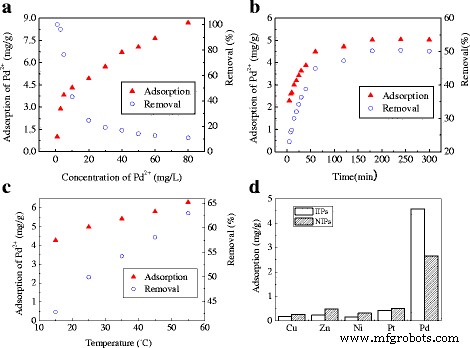
Efectos de ( a ) concentración inicial, ( b ) tiempo de contacto, ( c ) temperatura y ( d ) múltiples metales en la adsorción de Pd (II) en Pd (II) IIP
El efecto del tiempo de contacto sobre la capacidad de adsorción y la eficiencia de eliminación de Pd (II) IIP para iones Pd (II) se muestra en la Fig. 5b. En el período de prueba inicial de 60 minutos, tanto la capacidad de adsorción como la eficiencia de eliminación de Pd (II) IIP para Pd (II) aumentan rápidamente a medida que se alarga el tiempo de contacto de la reacción. Al comienzo de la reacción, hay una gran cantidad de sitios de unión disponibles en Pd (II) IIP para la adsorción de Pd (II) junto con la concentración relativamente alta de iones de Pd (II), existe una fuerte fuerza impulsora para promover la masa transferencia de iones de adsorbato de la solución a granel a los sitios de unión desocupados. Como consecuencia, es propicio para que los Pd (II) IIP actúen como un adsorbente eficiente para eliminar metales pesados de las aguas residuales en las primeras 3 h. Sin embargo, a medida que se extiende el tiempo de contacto, la mayoría de los sitios activos de Pd (II) IIP combinados con iones Pd (II) y los sitios activos disponibles disminuyeron. Después de 180 min, la capacidad de adsorción y la eficiencia de eliminación de Pd (II) IIP permanece sin cambios y alcanza un estado de equilibrio. Por lo tanto, se estableció 180 minutos como el tiempo de contacto óptimo para el proceso de adsorción.
La Figura 5c representa el efecto de la temperatura de funcionamiento sobre la capacidad de adsorción y la eficiencia de eliminación de Pd (II) IIP para Pd (II). Encontramos que la capacidad de adsorción y la eficiencia de eliminación de Pd (II) IIP para Pd (II) aumenta con el aumento de temperatura, lo que indica un proceso endotérmico para la reacción de adsorción. Una temperatura más alta es beneficiosa para promover la capacidad de adsorción de los absorbentes. En general, a una temperatura de ingeniería normal entre 25 y 35 ° C, los IIP de Pd (II) pueden tener un buen rendimiento en la aplicación práctica.
La influencia de múltiples metales sobre la adsorción de Pd (II) por Pd (II) IIP y NIP se muestra en la Fig. 5d. En el sistema coexistente de múltiples metales, la capacidad de adsorción de Pd (II) IIP y sus correspondientes NIP en Pd (II) es la más grande, seguida de Pt, Zn, Ni y Cu. La capacidad de adsorción de Pd (II) IIP en Pd (II) fue 26,7, 21,5, 31,8 y 10,4 veces mayor que la de Cu (II), Zn (II), Ni (II) y Pt (II), respectivamente. . Los resultados indicaron que los Pd (II) IIP eran altamente eficientes y selectivos para Pd (II). La capacidad de adsorción de Pd (II) IIP en Pt (II) fue mayor que la de Cu (II), Zn (II) y Ni (II), lo que puede deberse a la similitud química del Pt (II) con el Pd ( II) y sitios de adsorción competitivos en comparación con otros metales. La capacidad de adsorción de los NIP en Cu (II), Zn (II), Ni (II) y Pt (II) fue mayor que la de Pd (II) IIP, mientras que Pd (II) es exactamente lo contrario, lo que indica que mejor El efecto de adsorción de Pd (II) IIP en Pd (II) que el de NIP no es causado por un área específica grande sino por la formación de los sitios de adsorción de reconocimiento para Pd (II) en el proceso de preparación.
Estudios isotérmicos y cinéticos
Para explorar la capacidad de adsorción de Pd (II) IIP, se utilizaron dos modelos de isotermas de adsorción típicos, es decir, los modelos de isotermas de adsorción de Langmuir y Freundlich (Fig. 6a), para investigar el mecanismo de adsorción. A continuación, los datos experimentales se ajustan con los modelos cinéticos de pseudo primer orden y pseudo-segundo orden (Fig. 6b). Los parámetros isotérmicos y cinéticos de los respectivos modelos se resumen en la Tabla 2.
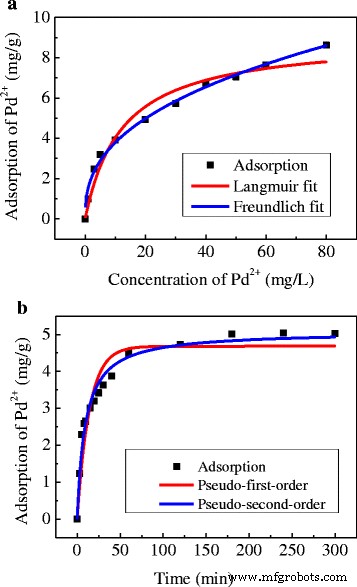
un Adsorción isotérmica y ( b ) curvas de ajuste cinético de Pd (II) en Pd (II) IIP
En el estudio de isotermas, el coeficiente de correlación del modelo de isotermas de Freundlich ( R ^ 2 =0.991) está mucho más cerca de 1 en comparación con el modelo de Langmuire ( R ^ 2 =0,946), lo que sugiere que el modelo de isoterma de Freundlich es más adecuado para describir el proceso de adsorción de iones Pd (II) en Pd (II) IIP. El modelo de Freundlich es una ecuación empírica, generalmente se cree que el recíproco de la constante de Freundlich n se correlaciona negativamente con el rendimiento de adsorción [27]. Cuando 1 / n está entre 0,1 ~ 0,5, es fácil de adsorber; cuando 1 / n es mayor que 2, es difícil de adsorber. El 1 / n El valor obtenido de este experimento es de aproximadamente 0,39, lo que indica que los iones Pd (II) son fáciles de adsorber por los Pd (II) IIP.
En el estudio cinético, el resultado de ajuste concuerda mejor con el modelo cinético de pseudo-segundo orden ( R 2 =0,971) que con el modelo cinético de pseudo primer orden ( R 2 =0,896). Con una capacidad de adsorción de equilibrio teórico de 5.085 mg / g, que está más cerca del valor experimental de 5.042 mg / g, la adsorción de iones Pd (II) en Pd (II) IIP se considera más de acuerdo con el pseudo-segundo -orden modelo cinético. El modelo cinético de pseudo-segundo orden asume que los pasos de control de la velocidad son principalmente procesos de adsorción química entre iones de metales pesados y los sitios de adsorción en absorbentes [31]. Por lo tanto, la adsorción de iones Pd (II) en Pd (II) IIP se debe principalmente a reacciones químicas, lo que confirma la formación de sitios de reconocimiento impresos.
Conclusión
Los estudios sobre tres tipos de monómeros funcionales durante la síntesis de Pd (II) IIP mostraron efectos de impresión significativamente diferentes. Los espectros UV mostraron que 4-VP y ANA causaron un gran cambio estructural después de que la plantilla reaccionó con tres monómeros funcionales, mientras que AAA básicamente no cambió. Según los experimentos de adsorción por lotes, 4-VP se comportó como el monómero funcional candidato más prometedor con una capacidad de adsorción de Pd (II) más alta que ANA y AAA. La formación de sitios de reconocimiento impresos, que fue beneficiosa para la adsorción de Pd (II) IIPs para iones Pd (II), fue evidenciada por los espectros FTIR. En condiciones óptimas de trabajo, se obtuvo una capacidad de adsorción de equilibrio teórico de 5.085 mg / g para los iones Pd (II) mediante los Pd (II) IIP sintetizados. En comparación con Cu (II), Zn (II), Ni (II) y Pt (II), los Pd (II) IIP mostraron una alta selectividad por los iones Pd (II). Los resultados isotérmicos sugirieron que el modelo de isoterma de Freundlich demostró un mejor ajuste para el proceso de adsorción de Pd (II) en Pd (II) IIP que el modelo de isoterma de Langmuir. Los estudios cinéticos revelaron que el proceso de adsorción podría describirse mejor mediante el modelo cinético de pseudo segundo orden.
Abreviaturas
- 4-VP:
-
4-vinilpridina
- AAA:
-
Ácido 2-acetamidoacrílico
- ANA:
-
Ácido 2- (aliltio) nicotínico
- APUESTA:
-
(Brunauer, Emmett, prueba de Teller)
- FAAS:
-
Espectrofotometría de absorción atómica de llama
- FTIR:
-
Espectroscopia infrarroja por transformada de Fourier
- NIP:
-
Nanoesferas poliméricas sin impresión de iones
- Pd (II) IIP:
-
Nanoesferas poliméricas impresas con iones de paladio (II)
- SEM:
-
Microscopio electrónico de barrido por emisión de campo
- TGA:
-
Análisis de termogravimetría
- UV:
-
Ultravioleta visible
Nanomateriales
- Eliminación por adsorción de iones de cobre (II) de una solución acuosa utilizando un nano-adsorbente de magnetita de residuos de cascarilla de molino:síntesis, caracterización, adsorción y mode…
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- Hacia los nanofluidos de TiO2:Parte 1:Preparación y propiedades
- Preparación de nanobarras de alúmina a partir de lodos de alúmina que contienen cromo
- La preparación de la nanoestructura yema-cáscara de Au @ TiO2 y sus aplicaciones para la degradación y detección del azul de metileno
- Preparación y rendimiento fotocatalítico de fotocatalizadores LiNb3O8 de estructura hueca
- Síntesis y caracterización de BiOCl modificado y su aplicación en la adsorción de tintes de baja concentración a partir de una solución acuosa
- Preparación de NP de Ag encapsulado de silicalita-1 poroso jerárquico y su rendimiento catalítico para la reducción de 4-nitrofenol
- Eliminación de antibióticos del agua con una membrana de nanofiltración 3D totalmente de carbono
- Una síntesis hidrotermal de nanopartículas híbridas de Fe3O4 @ C y rendimiento de adsorción magnética para eliminar iones de metales pesados en una solución acuosa
- Preparación de liposomas de ácido glicirretínico mediante el método de solución monofásica de liofilización:preformulación, optimización y evaluación in vitro



