Preparación de nanobarras de alúmina a partir de lodos de alúmina que contienen cromo
Resumen
Se prepararon nanobarras de alúmina a partir de lodos de alúmina que contienen cromo y se investigaron los efectos de los elementos dopantes, como Cr, Fe y Mg. Los resultados muestran que la transformación cristalina de la alúmina está restringida por el Cr dopado y facilitada por el Fe y el Mg dopados, que se transforma de θ -Al 2 O 3 a α -Al 2 O 3 en el proceso de calcinación. Mientras tanto, la transformación cristalina de la alúmina está fuertemente restringida por elementos codopados del lodo de alúmina que contiene cromo. Los elementos dopados cambian el curso de la transformación de la estructura de fase y transforman ligeramente el enlace químico de las nanovarillas de alúmina. Los elementos impuros se dopan en el cristal de alúmina y restringen el crecimiento cristalino de las nanovarillas de alúmina de acuerdo con las reglas. En la muestra preparada a partir de lodo de alúmina que contiene cromo, se dopan más Cr y Mg pero menos Fe, y la mayoría del Cr existe como Cr (III). Es posible que el dopaje con Fe esté limitado por la competencia de Cr y Mg. Además, la imperfección reticular de la alúmina es causada por iones dopados, como Cr, Fe y Mg, y el estado químico de O y Al se ve afectado. Los hallazgos de estos experimentos proporcionan información esencial para eliminar la contaminación y promover la utilización integral del lodo de alúmina que contiene cromo.
Antecedentes
La nanoalúmina de baja dimensión, como las nanofibras de alúmina [1, 2, 3] y las nanovarillas de alúmina [4], tiene propiedades superiores de alta resistencia, alto módulo elástico, estabilidad química, buen rendimiento de aislamiento térmico y baja conductividad térmica [5, 6,7,8,9], por lo que se aplicó ampliamente en varios campos, como el refuerzo para compuestos de matriz cerámica y compuestos de matriz metálica y catalizador, portador de catalizador, adsorbentes, reactores de membrana, revestimientos y materiales de ánodos [4, 10, 11,12,13,14,15]. Sin embargo, el alto costo de producción ha limitado su aplicación. Algunos autores han informado con éxito sobre métodos de síntesis de nanoalúmina de baja dimensión, que incluyen principalmente el método de fase sólida, el método de fase de vapor [16] y el método de fase líquida [17, 18]. Entre ellos, el método en fase líquida se aplica ampliamente por su condición de reacción suave, productos homogéneos y bajo costo de producción. Hubo muchos informes sobre la preparación de nanoalúmina mediante el método sol-gel [5, 19,20,21], el método de microemulsión [22], el método hidrotermal [23], el método de precipitación [23], la deposición química de vapor [16], y electrohilado [1, 3, 24, 25]. Sin embargo, el método de precipitación es adecuado para laboratorios e industrias debido a su bajo consumo de energía, homogeneidad del producto y tamaño y forma controlable.
El lodo de alúmina que contiene cromo es un tipo de residuo sólido peligroso, que se produce en el proceso de producción de productos de cromo mediante un método de tostado sin calcio. Se generan siete mil kilogramos de lodo de alúmina que contiene cromo a partir de cada tonelada de producto de cromo. Está compuesto de 55 ~ 65% de Al 2 O 3 , 7 ~ 13% de cromo y pocos compuestos de silicio, hierro, magnesio y sodio. Los componentes del lodo de alúmina que contiene cromo se muestran en la Tabla 1, que son proporcionados por el fabricante (CITIC Jinzhou Metal Co., Ltd., China).
Como principal sustancia peligrosa, el cromo existe en forma de Cr (III) o Cr (VI) en los lodos de alúmina que contienen cromo, y el Cr (VI) se considera el contaminante dominante debido a su carcinogenicidad [26]. En la actualidad, la contaminación de la solución del lodo de alúmina que contiene cromo se desintoxica y utiliza principalmente. El primero transforma el Cr (VI) en Cr (III) de baja toxicidad y lo almacena como residuo de desecho. Zhang Dalei [27] señaló un método de pirólisis para transformar Cr (VI) en Cr (III) utilizando paja. Duan Suhua [28] señaló que la escoria que contiene cromo podría tratarse con alcohol industrial. Sin embargo, los métodos mencionados anteriormente no solo ocupan tierra, sino que también causan un gran desperdicio de recursos. Además, la contaminación secundaria puede ocurrir inesperadamente. El último método consiste en separar y utilizar los componentes útiles del lodo de alúmina que contiene cromo. Xue Wendong [29] informó que el lodo de alúmina que contiene cromo podría usarse para preparar refractario. Sin embargo, el método anterior puede verse limitado debido a su escaso valor añadido. En consecuencia, se deben proponer algunos métodos nuevos para eliminar la contaminación y promover la utilización integral de los lodos de alúmina que contienen cromo, que no solo pueden resolver los problemas ambientales sino también traer grandes beneficios económicos.
En este artículo, las nanovarillas de alúmina se preparan a partir del lodo de alúmina que contiene cromo mediante el método de precipitación-calcinación. Mientras tanto, con el fin de investigar la influencia del ión de dopaje simple en las nanovarillas de alúmina, se preparan y caracterizan las nanovarillas de alúmina con iones de dopaje simple o sin dopaje. Los resultados proporcionarán apoyo técnico para eliminar la contaminación y promover la utilización integral de los lodos de alúmina que contienen cromo.
Métodos
Materiales
Los reactivos (p. Ej., Octadecahidrato de sulfato de aluminio, sulfato de cromo, sulfato férrico, sulfato de magnesio, hidróxido de sodio, ácido sulfúrico y dodecilbencenosulfonato de sodio) utilizados en este estudio fueron productos químicos analíticamente puros. El lodo de alúmina que contiene cromo fue proporcionado por CITIC Jinzhou Metal Co., Ltd. (China). Todas las soluciones se prepararon con agua desionizada.
Tratamiento del lodo de alúmina que contiene cromo
Al principio, el lodo de alúmina que contiene cromo se lavó y filtró con agua desionizada de acuerdo con la relación sólido-líquido de 1:5 (g / mL). Como resultado, la mayoría de Cr 6+ los compuestos se separaron del lodo de alúmina que contenía cromo. Luego, la torta de filtración se disolvió con ácido sulfúrico de acuerdo con la relación sólido-líquido de 1:3 (g / mL), y luego, el H 2 O 2 se utilizó para transformar el Cr 6+ residual a Cr 3+ . Por último, se obtuvo con éxito la solución ácida de lodo de alúmina que contiene cromo y los componentes se analizaron mediante titulación química y espectrofotómetro de luz visible (VIS, 721N, Varian, América) que se muestra en la Tabla 2.
Síntesis de nanovarillas de alúmina
Se agregaron lentamente dos moles por litro de solución de NaOH y solución de dodecil benceno sulfonato en 0,25 mol / L de Al 2 (SO 4 ) 3 solución bajo agitación magnética a 85 ° C, y el valor de pH de la solución mezclada se ajustó a 9,0 con NaOH o H2 2 SO 4 solución. Después de agitar durante 5 h y envejecer durante 20 h, los precipitados se separaron y lavaron varias veces con agua desionizada y alcohol etílico. Posteriormente, las muestras se secaron al vacío a 40 ° C durante 15 h, y luego se prepararon los precursores. Finalmente, las muestras se calcinaron a 250 ° C por 1 h, 400 ° C por 1 h, 770 ° C por 1 h, 900 ° C por 1 h, y 1050 ° C por 2 h de manera continua, y luego se recolectaron las muestras. para usar. La alúmina sin dopar se preparó a partir de Al 2 puro (SO 4 ) 3 solución, y las muestras dopadas con iones se prepararon mediante el mismo método que el anterior. Mientras tanto, los cloratos de Cr, Fe y Mg se agregaron en el Al 2 (SO 4 ) 3 se preparó una solución de acuerdo con el contenido de elemento dopante en el lodo de alúmina que contiene cromo (Tabla 2), y la alúmina dopada con Cr, dopada con Fe y dopada con Mg. Usando la solución ácida de lodo de alúmina que contiene cromo como materia prima, se nombró la alúmina que se preparó a partir del lodo de alúmina que contiene cromo.
Caracterización de varillas de nanoalúmina
Las fases cristalinas de las muestras se caracterizaron por difracción de rayos X en polvo (XRD) utilizando un difractómetro de rayos X D / MAX-RB (Rigaku, Japón) con radiación Cu K en el rango 2θ de 10 ° -70 ° en un escaneo. velocidad de 2 ° / min. Los espectros infrarrojos de transformada de Fourier (FT-IR) de las muestras se caracterizaron utilizando el espectrómetro Scimitar 2000 Near FT-IR (Thermo electron, EE. UU.), Y los espectros se registraron en el rango de 4000 a 400 cm -1 . La estabilidad térmica del precursor se examinó mediante un analizador termogravimétrico (TG-DSC, STA449F3, NETZSCH, Alemania) con una velocidad de flujo de 30 ml / min en atmósfera de aire y una temperatura de 15-1200 ° C con una velocidad de calentamiento de 10 °. C / min. Las morfologías, la estructura cristalina y la distribución de elementos de las muestras se examinaron mediante microscopía electrónica de transmisión de emisión de campo (FETEM, Jem-2100F, JEOL, Japón). Los espectros de espectroscopía de fotoelectrones de rayos X (XPS) de las muestras se registraron en XPS (ESCAMABMKLL, VG, Reino Unido) equipado con un analizador de electrones hemisférico y un Al Kα Fuente de rayos X.
Resultados y discusión
Caracterización XRD de los nanorods de alúmina
Se registraron patrones de XRD para confirmar la estructura cristalina de las muestras, como se muestra en la Fig. 1. Para las nanovarillas de alúmina sin dopar, los resultados de XRD muestran la existencia de diferentes estructuras cristalinas de alúmina, incluido el corindón ( α -Al 2 O 3 , syn) (JCPDS No. 46-1212) y óxido de aluminio ( θ -Al 2 O 3 , JCPDS No. 35–0121) y los picos de difracción de θ -Al 2 O 3 son más débiles (Fig. 1 (a)). En general, la alúmina se transforma desde el estado de transición θ -Al 2 O 3 a estado estable α -Al 2 O 3 a 1000 ~ 1200 ° C. En comparación con la muestra sin dopar, las nanovarillas de alúmina dopadas con Cr tienen picos relativamente más fuertes de θ -Al 2 O 3 y picos relativamente más débiles de α -Al 2 O 3 (Figura 1 (b)). Significa que la transición cristalina está restringida por el Cr dopado en el proceso de calcinación, por lo que menos θ -Al 2 O 3 se transforma en α -Al 2 O 3 después de calcinado a 1050 ° C. En la Fig. 1 (c), se puede ver que los picos de α -Al 2 O 3 son más fuertes y nítidos que los de (a) y (b), lo que sugiere un tamaño de cristal más grande y una mejor cristalinidad. Mientras tanto, los picos de θ -Al 2 O 3 son aún más débiles, lo que indica que la transición cristalina es facilitada por el Fe dopado. Puede ser porque más θ -Al 2 O 3 se transforma en α -Al 2 O 3 después de la calcinación. La figura 1 (d) muestra que las nanovarillas de alúmina dopadas con Mg tienen picos de α relativamente más fuertes y más nítidos -Al 2 O 3 y picos relativamente más débiles de θ -Al 2 O 3 . Se sugiere que la muestra contenga más α -Al 2 O 3 y menos θ -Al 2 O 3 , lo que puede deberse a que el Mg dopado promueve la transición cristalina de la alúmina en el proceso de calcinación. Para las nanovarillas de alúmina preparadas a partir de lodos de alúmina que contienen cromo, los picos de α -Al 2 O 3 casi desaparecen, mientras que los picos de θ -Al 2 O 3 se vuelven más fuertes pero no lo suficientemente afilados (Fig. 1 (e)). Se indica que el θ -Al 2 O 3 tiene poca cristalinidad y un tamaño de cristal más pequeño. Esto podría deberse a que más elementos de impurezas del lodo de alúmina que contiene cromo están dopados en la alúmina, y la transición cristalina de la alúmina está restringida en el proceso de calcinación. Entonces, el θ -Al 2 O 3 rara vez se transforma en α -Al 2 O 3 .
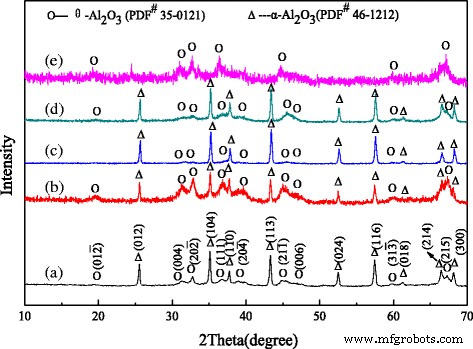
Patrones XRD de nanobarras de alúmina dopadas con diferentes iones: a alúmina sin dopar, b Alúmina dopada con Cr, c Alúmina dopada con Fe, d Alúmina dopada con magnesio y e la alúmina preparada a partir del lodo de alúmina que contiene cromo
Espectros FT-IR de los nanorods de alúmina
Espectros FT-IR de nanobarras de alúmina en el rango de 4000 a 400 cm −1 se muestran en la Fig. 2 [27]. La absorción alcanza su punto máximo a 3500-3300 y 1635 cm −1 que aparecen en todos los espectros se atribuyen a la vibración de estiramiento de la asociación de enlaces no químicos de los grupos OH y las vibraciones de flexión H – O – H, respectivamente, lo que indica que el agua de los poros y el agua adsorbida existen en las muestras [30]. Los picos a 2360 cm −1 se atribuyen a la presencia de dióxido de carbono. La Figura 2 (2) muestra la región de huellas dactilares de los espectros FT-IR de las muestras. Como se muestra en la Fig.2 (2a), para la muestra sin dopar, los picos a 829, 589 y 449 cm −1 se atribuyen a AlO 6 vibraciones, que indican la formación de α -Al 2 O 3 [1]. Mientras tanto, los picos a 762 cm −1 se atribuyen a la vibración de flexión de Al – O – Al, y las de 663 y 488 cm −1 se atribuyen a las vibraciones de estiramiento y flexión de Al – O, respectivamente, lo que indica la formación de θ -Al 2 O 3 . La Figura 2 (2b) muestra que los picos de α -Al 2 O 3 son más débiles que los de la figura 2 (2a), lo que indica que el dopado con Cr evita la formación de α -Al 2 O 3 en el proceso de calcinación. Para la alúmina dopada con Fe y Mg, los picos de θ -Al 2 O 3 se vuelven más débiles, y los picos de α -Al 2 O 3 tienen muy pocos cambios (Fig. 2 (2c, d)). En comparación con la Fig. 2 (2a), los picos se han desplazado al rojo o al azul levemente, lo que ilustra que el Fe y el Mg dopados se benefician del crecimiento de α -Al 2 O 3 y transformar ligeramente el enlace químico de las nanovarillas de alúmina. La Fig. 2 (2e) es la región de la huella dactilar de los espectros FT-IR de las nanovarillas de alúmina preparadas a partir del lodo de alúmina que contiene cromo. Los picos por debajo de 500 cm −1 desaparecen, lo que indica que no hay α -Al 2 O 3 en las muestras. Además, los picos a 900-500 cm −1 están dispersos, lo que podría ser el resultado de vibraciones de M – O y M – O – M (M es Al o el elemento dopado de alúmina del lodo de alúmina que contiene cromo). Los resultados anteriores están de acuerdo con los resultados de XRD.
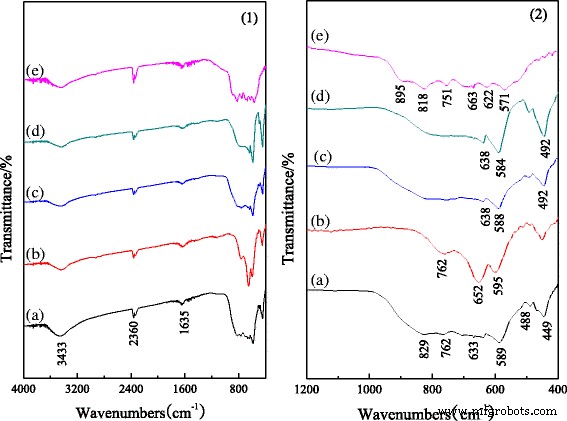
Espectros FT-IR de varillas de nanoalúmina dopadas con diferentes iones: a alúmina sin dopar, b Alúmina dopada con Cr, c Alúmina dopada con Fe, d Alúmina dopada con magnesio y e la alúmina preparada a partir del lodo de alúmina que contiene cromo
TG-DSC de nanorods de alúmina
El analizador termogravimétrico (TG) y las curvas de calorimetría diferencial de barrido (DSC) de los precursores de nanovarillas de alúmina se muestran en la Fig. 3. Los resultados de XRD indican que el precursor de nanovarillas de alúmina es AlO (OH) (JCPDS No. 49-0133). Como se muestra en la Fig. 3a, en el aire, solo se pueden ver tres etapas en la muestra sin dopar. Por debajo de 250 ° C, aproximadamente el 40% de pérdida de masa en la curva TG y los picos endotérmicos correspondientes a 50 y 150 ° C en la curva DSC están asociados con la evaporación de humedad y la desorción de agua adsorbida. La segunda etapa está entre 250 y 730 ° C, con una pérdida de masa total de aproximadamente 35% y dos picos endotérmicos están a 320 y 694 ° C. A la temperatura de 320 ° C, el pico endotérmico se debe a la transformación de AlO (OH) en Al 2 amorfo. O 3 . Mientras tanto, el pico endotérmico débil a 694 ° C se atribuye a la transformación de Al 2 amorfo O 3 a θ -Al 2 O 3 . En la tercera etapa por encima de 730 ° C, hay una pequeña pérdida de masa y un fuerte pico endotérmico a 980 ° C, que es principalmente el resultado de la transformación de θ -Al 2 O 3 a α -Al 2 O 3 . En comparación con la muestra sin dopar, el dopaje con iones metálicos hace que los picos endotérmicos se desplacen. La Figura 3b-e muestra que los picos endotérmicos se desplazan a temperaturas más altas y se ensanchan. Puede deberse a que los iones dopados cambian el curso de la transformación de la estructura de fase, por lo que el grado de transformación de θ -Al 2 O 3 a α -Al 2 O 3 es diferente para cada muestra. Los resultados concuerdan con los de XRD y FT-IR.
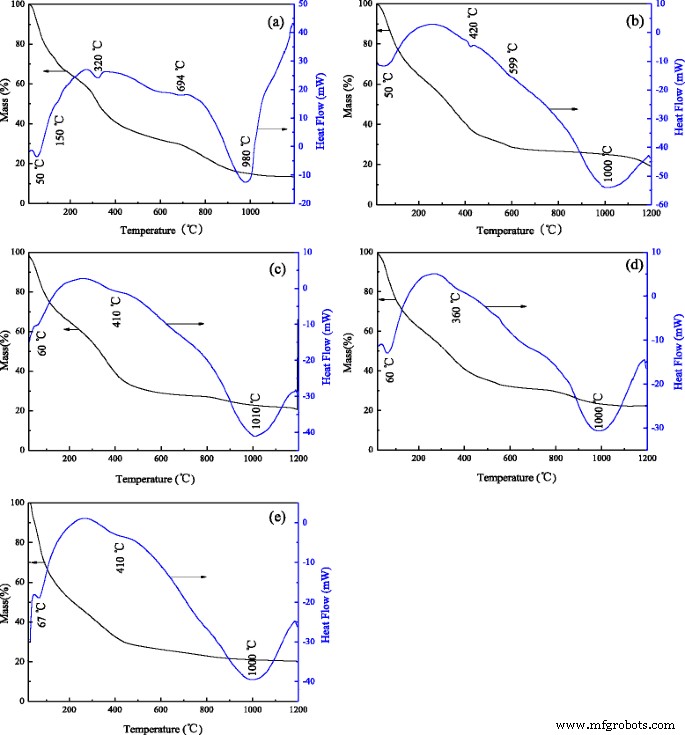
TG y DSC de los precursores de varillas de nanoalúmina dopados con diferentes iones: a alúmina sin dopar, b Alúmina dopada con Cr, c Alúmina dopada con Fe, d Alúmina dopada con magnesio y e La alúmina preparada a partir del lodo de alúmina que contiene cromo
Imágenes TEM, SAED y HRTEM de nanorods de alúmina
La Figura 4 muestra los resultados de TEM, difracción electrónica de área seleccionada (SAED) y microscopía electrónica de transmisión de alta resolución (HRTEM). Como se muestra en la Fig. 4 (a1-a3), la alúmina sin dopar son nanobarras dispersivas con un diámetro de 4 a 6 nm y una longitud de 20 a 60 nm. Mientras tanto, los planos (215), (006), (21 \ (\ overline {1} \)) y (20 \ (\ overline {4} \)) están de acuerdo con θ -Al 2 O 3 (JCPDS No. 35–0121), y los planos (300), (214), (113) y (104) están asociados con α -Al 2 O 3 (JCPDS No. 46-1212). Además, la distancia interplanar observada de 0.273 y 0.284 nm podría asignarse a los planos (20 \ (\ overline {2} \)) y (004) de θ -Al 2 O 3 , y el espaciado de celosía de 0.255 y 0.348 nm podría corresponder a los planos (104) y (012) de α -Al 2 O 3 . En comparación con la muestra sin dopar, la muestra dopada con Cr son nanobarras con un diámetro de 4 a 6 nm y una longitud de 50 a 120 nm (Fig. 4 (b1)). La Figura 4 (b2) muestra que los planos (215), (21 \ (\ overline {1} \)), (20 \ (\ overline {2} \)) y (111) están de acuerdo con θ -Al 2 O 3 , y los planos (300), (214), (113) y (104) están de acuerdo con α -Al 2 O 3 . Como se muestra en la Fig. 4 (b3), la distancia interplanar de 0.202 nm, 0.273 nm, 0.284 nm y 0.454 nm se asignan a (21 \ (\ overline {1} \)), (20 \ (\ overline { 2} \)), (004) y (10 \ (\ overline {2} \)) planos de θ -Al 2 O 3 , y la distancia interplanar de 0.209 y 0.238 nm se asignan a los planos (113) y (110) de α -Al 2 O 3 . La Figura 4 (c1) muestra que la muestra dopada con Fe es la mezcla de nanobarras con un diámetro de 5 a 10 nm y una longitud de 30 a 100 nm y nanopartículas de aproximadamente 10 nm. La Figura 4 (c2) muestra que los planos (20 \ (\ overline {2} \)) están de acuerdo con θ -Al 2 O 3 , y los planos (300), (214), (024), (113), (104) y (116) están de acuerdo con α -Al 2 O 3 , está de acuerdo con los resultados de XRD. Mientras tanto, la distancia interplanar observada de 0.284 y 0.454 nm se asigna a los planos (004) y (10 \ (\ overline {2} \)) de θ -Al 2 O 3 , y la distancia interplanar de 0.238 y 0.255 nm se asignan a los planos (110) y (104) de α -Al 2 O 3 (Figura 4 (c3)).
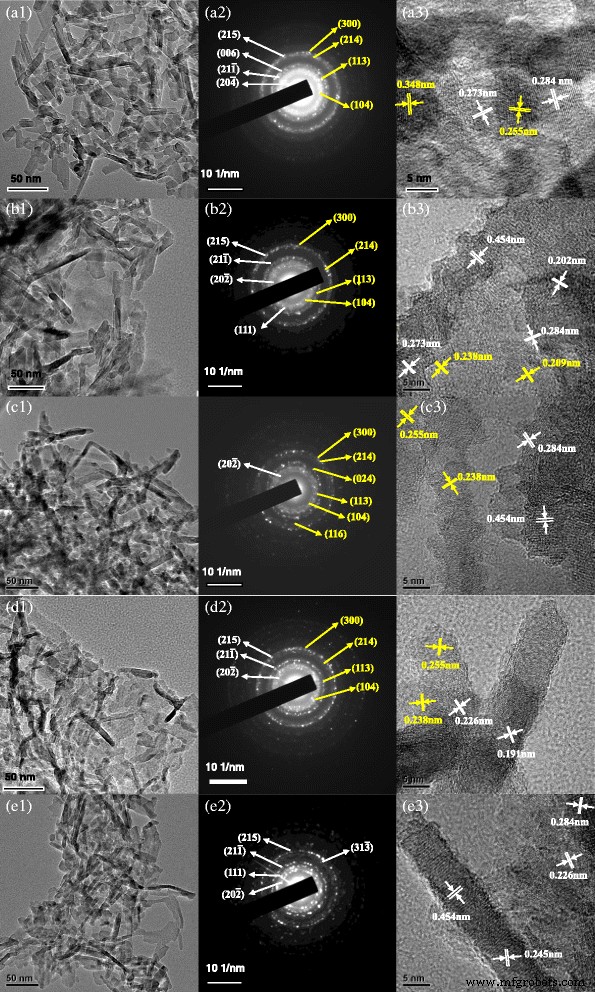
TEM, SAED y HRTEM de nanobarras de alúmina dopadas con diferentes iones: a alúmina sin dopar, b Alúmina dopada con Cr, c Alúmina dopada con Fe, d Alúmina dopada con magnesio y e la alúmina preparada a partir del lodo de alúmina que contiene cromo. (1) TEM; (2) SAED; (3) HRTEM
Como se muestra en la Fig. 4 (d1 – d3), la muestra dopada con Mg son nanobarras bien dispersas con un diámetro de 5–10 nm y una longitud de 20–50 nm, y existen nanopartículas de aproximadamente 10 nm simultáneamente. Los resultados de SAED muestran que los planos (215), (21 \ (\ overline {1} \)) y (20 \ (\ overline {2} \)) están de acuerdo con θ -Al 2 O 3 , y los planos (300), (214), (113) y (104) están de acuerdo con α -Al 2 O 3 . Los resultados de HRTEM muestran que la distancia interplanar observada de 0.226 y 0.191 nm se asigna a los planos (20 \ (\ overline {4} \)) y (006) de θ -Al 2 O 3 , y la distancia interplanar de 0.255 y 0.238 nm se asignan a los planos (104) y (110) de α -Al 2 O 3 . La Figura 4 (e1-e3) muestra que la muestra preparada a partir de lodo de alúmina que contiene cromo es nanobarras bien dispersas con un diámetro de 4 a 6 nm y una longitud de 50 a 100 nm, y que existen nanopartículas de aproximadamente 5 a 10 nm simultáneamente. Los resultados de SAED y HRTEM muestran que (215), (111), (21 \ (\ overline {1} \)), (31 \ (\ overline {3} \)) y (20 \ (\ overline {2 } \)) los planos están de acuerdo con θ -Al 2 O 3 , y la distancia interplanar observada de 0.226, 0.245, 0.284 y 0.454 nm se asignan a (20 \ (\ overline {4} \)), (111), (004) y (10 \ (\ overline {2 } \)) planos de la misma. Sin embargo, no hay planos de acuerdo con α -Al 2 O 3 . Como resultado, las nanovarillas de alúmina sin dopar son bien dispersas que las otras y las partículas tienen una forma regular. Puede ser que los elementos de impureza estén dopados en el cristal de alúmina y frenen el crecimiento cristalino de nanobarras de alúmina de acuerdo con las reglas. Por lo tanto, las formas y dispersibilidades de las nanovarillas de alúmina se ven afectadas por los elementos dopados.
Caracterización por EDS del precursor de nanovarillas de alúmina dopado con diferentes iones
Los resultados de EDS revelan que Cr, Fe y Mg están dopados en el precursor de nanobarras de alúmina con una cantidad molar de 2,06, 0,99 y 0,58%, respectivamente (Tabla 3). Esta cantidad de dopaje está cerca de la dosis de adición del elemento de impureza (Tabla 2), lo que indica que la mayoría de los elementos de impureza están dopados en el precursor de nanovarillas de alúmina. Mientras tanto, para la muestra preparada a partir de lodo de alúmina que contiene cromo, la cantidad molar dopada de Cr, Fe y Mg son 2,11, 0,14 y 0,96%, respectivamente. Los resultados sugieren que la mayor parte del Cr y Mg está dopado en la muestra, pero una pequeña cantidad de Fe está dopado en ella. Es posible que el dopaje de Fe esté limitado por la competencia de Cr y Mg.
Caracterización XPS de fibras de alúmina nanométricas dopadas con diferentes iones
La Figura 5 muestra los espectros XPS de O1 s y Al 2 p . Como se muestra en la Fig.5a, los picos a 531.90, 531.85, 531.15, 531.20 y 532.00 eV se atribuyen a las nanovarillas de alúmina sin dopar, dopadas con Cr, dopadas con Fe y dopadas con Mg y la muestra preparada a partir de las nanovarillas de alúmina que contienen cromo. lodos de alúmina, respectivamente. Los picos se asignan a O 2− del Al 2 O 3 [31]. La figura 5b muestra los picos a 74,00, 74,25, 74,75, 74,38 y 73,90 eV de Al 2 p se atribuyen a las muestras anteriores, respectivamente. Los picos se atribuyen a Al 3+ del Al 2 O 3 . Mientras tanto, las buenas simetrías de la curva se prueban mediante ajuste gaussiano, lo que indica que se forman menos oxígeno y aluminio en las muestras. Los O1 s La energía de unión (BE) de las nanovarillas de alúmina no dopadas y dopadas con Cr y la muestra preparada a partir del lodo de alúmina que contiene cromo son casi y son más altas que las de las muestras dopadas con Fe y dopadas con Mg. El orden de los O1s BE más pequeños es el siguiente:nanobarras de alúmina dopadas con Fe, dopadas con Mg, dopadas con Cr, sin dopar y la muestra preparada a partir del lodo de alúmina que contiene cromo. Sin embargo, el Al 2p BE está en contraste. Los resultados de XRD muestran que el estado más transitorio θ -Al 2 O 3 están en las nanovarillas de alúmina sin dopar y dopadas con Cr y la muestra preparada a partir del lodo de alúmina que contiene cromo, y más α -Al 2 O 3 están en las nanobarras de alúmina dopadas con Fe y con Mg. Debido al formulario de coordinación [AlO 4 ] para θ -Al 2 O 3 y [AlO 6 ] para α -Al 2 O 3 , es posible que el O1 s BE de [AlO 6 ] es mayor y Al 2 p BE es más pequeño que el de [AlO 4 ]. Además, las imperfecciones de la red de Al 2 O 3 son causados por iones Cr, Fe y Mg que entran en Al 2 O 3 enrejado. Entonces, los estados químicos de O y Al se ven afectados por el defecto de la red y la energía de enlace cambia.
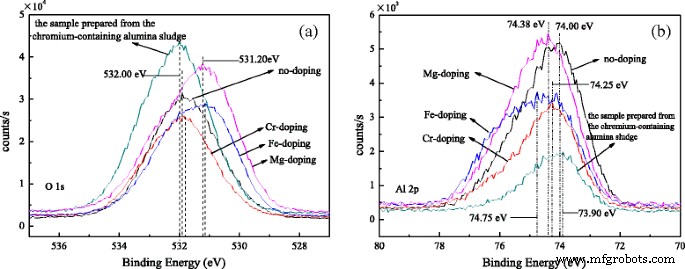
Espectros XPS de a O1 s y b Al 2 p para nanobarras de alúmina dopadas con diferentes iones
La Figura 6 presenta los espectros XPS del ion dopante. Como se muestra en la Fig. 6a, los picos en 589,80 y 578,52 eV se asignan a Cr 2p 1/2 y Cr 2p 3/2 de Cr (VI), y los picos en 587.53 y 577.39 eV se asignan a Cr 2p 1/2 y Cr 2p 3/2 de Cr (III). Muestra que el Cr existe en las nanovarillas de alúmina dopadas con Cr como Cr (VI) y Cr (III). Sin embargo, la mayor parte del Cr existe como Cr (III) en la muestra preparada a partir del lodo de alúmina que contiene cromo. Indica que la parte de Cr (III) se oxida en el proceso de calcinación en la muestra dopada con Cr, pero se oxida menos Cr (III) en las muestras preparadas a partir del lodo de alúmina que contiene cromo. Para las muestras preparadas a partir del lodo de alúmina que contiene cromo, debido a que se forma la combinación de enlaces químicos de Cr-O y el elemento metálico de impureza, el potencial de electrodo de Cr 6+ / Cr 3+ aumenta a alta temperatura, por lo tanto, poco Cr (VI) en la muestra. Como se muestra en la Fig. 6b, los picos a 724,45 y 711,30 eV se asignan a Fe 2p 1/2 y Fe 2p 3/2 de Fe 2 O 3 , y 722.38 y 710.44 eV se asignan a Fe 2p 1/2 y Fe 2p 3/2 de Fe 3 O 4 . Los resultados muestran que existen Fe en la muestra de dopaje con Fe como Fe (II) y Fe (III). Se sugiere que el elemento Fe se introduzca en la red del precursor de alúmina y tenga lugar en la red de aluminio durante la síntesis. En el proceso de calcinación subsiguiente, un poco de Fe (III) se reduce a Fe (II) al reducir la sustancia en el aire. Sin embargo, no hay picos de Fe en la muestra preparada a partir del lodo de alúmina que contiene cromo, debido a la poca cantidad de Fe en la muestra (Tabla 3). Como se muestra en la Fig. 6c, los picos de 50,20 a 50,34 eV se asignan a Mg 2 p de MgO, lo que sugiere que Mg existe en la muestra dopada con Mg como MgO. Sin embargo, el pico de Mg 2p es muy débil en la muestra preparada a partir del lodo de alúmina que contiene cromo. Es posible que el contenido de Mg sea raro. Los resultados coinciden con la EDS. De acuerdo con los resultados de XRD, FT-IR y XPS, se ilustra que la imperfección de la red de muestras de dopaje de un solo elemento se forma debido a las impurezas del elemento metálico que entran en la red de alúmina. Sin embargo, debido a la competencia de múltiples elementos, se ingresa más Cr en la red de alúmina preparada a partir del lodo de alúmina que contiene cromo, y se ingresan pocos elementos de Fe y Mg.
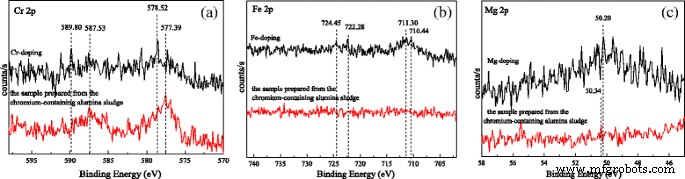
Espectros XPS de a Cr 3+ 2 p , b Fe 3+ 2 p y c Mg 2+ 2 p
Conclusiones
En resumen, los elementos de impureza se doparon en nanobarras de alúmina, como Cr, Fe y Mg. La transformación cristalina de la alúmina está restringida por el Cr dopado y facilitada por el Fe y el Mg dopados, que se transforma de θ -Al 2 O 3 a α -Al 2 O 3 en el proceso de calcinación. Además, la transformación cristalina de la alúmina está fuertemente restringida por elementos codopados del lodo de alúmina que contiene cromo. El curso de la transformación de la estructura de fase, el enlace químico, la microestructura y el estado químico de O y Al de las nanobarras de alúmina se ven afectados por los elementos dopados. En la muestra preparada a partir de lodo de alúmina que contiene cromo, el dopaje con Fe está limitado por la competencia de Cr y Mg. Este estudio sugiere que se pueden preparar nanobarras de alúmina a partir de lodos de alúmina que contienen cromo para reducir costos y eliminar la contaminación.
Abreviaturas
- BE:
-
Energía vinculante
- DSC:
-
Análisis de calorimetría diferencial de barrido
- EDS:
-
Espectrómetro de dispersión de energía
- FETEM:
-
Microscopía electrónica de transmisión por emisión de campo
- FT-IR:
-
Espectros infrarrojos de transformada de Fourier
- HRTEM:
-
Microscopía electrónica de transmisión de alta resolución
- SAED:
-
Difracción de electrones de área seleccionada
- TEM:
-
Microscopía electrónica de transmisión
- TG:
-
Analizador termogravimétrico
- XPS:
-
Espectroscopia de fotoelectrones de rayos X
- XRD:
-
Difracción de rayos X en polvo
Nanomateriales
- Preparación de renio en polvo
- Métodos de preparación de polvo de tantalio
- Conversión de numeración decimal
- De eléctrico a electrónico
- 3 razones para realizar la transición de C a C ++
- Nanocelulosa de algas verdiazules
- Nanorods de oro recubiertos con BSA para la terapia fototérmica NIR-II
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- Hacia los nanofluidos de TiO2:Parte 1:Preparación y propiedades
- Dispersión en ángulos pequeños de fractales gordos a nanoescala
- De la interfaz de usuario a la IA:un viaje de automatización



