Eliminación de tinte catiónico fotocatalíticamente mejorada con hidróxidos dobles en capas de Zn-Al
Resumen
Se estudiaron los hidróxidos dobles estratificados (LDH) de Zn-Al calcinados y organomodificados como adsorbentes y fotocatalizadores para la eliminación de colorantes catiónicos, como el azul de metileno (MB) . Se obtuvieron LDH de Zn-Al con una relación catiónica de 2:4 mediante el método de coprecipitación. Las muestras tal como se sintetizaron se calcinaron a diferentes temperaturas y las transformaciones de fase se investigaron mediante los métodos XRD, TG / DTG y UV-vis-DR. La actividad de las LDH de Zn-Al calcinadas y sintetizadas bajo luz ultravioleta se atribuyó a la presencia de la fase ZnO. La cantidad de ZnO en las LDH se puede regular variando la relación Zn / Al y la temperatura de calentamiento. Se observó predominante el impacto de la relación Zn / Al sobre la actividad fotocatalítica de las LDH. Las LDH de Zn-Al calcinadas demostraron una baja adsorción de MB. La modificación de las LDH de ZnAl por dodecilsulfato de sodio se realizó mediante un método de reconstrucción. Los nanohíbridos organo / LDH demostraron una alta capacidad de adsorción a MB. La eliminación de MB de soluciones con LDH de organo / Zn-Al se mejoró mediante el uso de luz ultravioleta debido a la fotodestrucción de MB.
Antecedentes
La eliminación de colorantes orgánicos peligrosos de las aguas residuales y la remediación de contaminantes en las aguas superficiales y subterráneas es un problema importante en el mundo. Se conocen varios métodos tradicionales que incluyen adsorción, coagulación, floculación, ozonización, filtración por membrana, intercambio iónico, oxidación y precipitación química para el tratamiento de efluentes que contienen colorantes [1, 2]. La adsorción es una técnica económica que no requiere ninguna configuración especial. En los últimos años, se desarrollaron y utilizaron muchos tipos de adsorbentes con función catalítica para eliminar nitratos, metales pesados y contaminantes orgánicos del agua [3, 4, 5].
Se ha explorado el uso de hidróxidos de doble capa (LDH) como materiales alternativos para la eliminación de tintes orgánicos de medios acuosos [6, 7, 8]. Las LDH se conocen como arcillas aniónicas y materiales similares a la hidrotalcita. Su estructura básica se asemeja a la de la brucita, Mg (OH) 2 , cuando una fracción x de cationes divalentes es reemplazado isomorfamente por cationes trivalentes, dando capas con carga positiva. La composición química de las LDH se expresa mediante la fórmula general [M 2+ 1 − x M 3+ x (OH) 2 ] [A n− ] x / n · ZH 2 O, donde M 2+ puede ser común; Mg 2+ , Zn 2+ o Ni 2+ y M 3+ puede ser común; Al 3+ , Ga 3+ , Fe 3+ o Mn 3+ . Un anión orgánico o inorgánico de compensación de carga sin estructura (CO 3 2− , Cl - , SO 4 2− , RCO 2 - ) está firmado como A n− ; x normalmente está entre 0,2-0,4. Las capas de LDH obtienen una carga positiva por sustitución isomorfa de M 3+ para M 2+ , que se compensa con aniones de capa intermedia y agua [9].
El tratamiento térmico de LDH conduce a la pérdida de moléculas de agua fisisorbidas y entre capas, OH - grupos de capas y aniones de equilibrio de carga. La estructura en capas colapsa y se forma una solución sólida de óxido de metal mixto. Los óxidos mixtos típicamente poseían grandes áreas de superficie específicas, estabilidad térmica e interacciones sinérgicas entre los diferentes componentes metálicos. Por lo tanto, los productos de calcinación de LDH han encontrado numerosas aplicaciones en varios procesos catalíticos [10,11,12].
Debido a su capacidad de intercambio aniónico, las LDH son adecuadas para la intercalación y sorción de tintes aniónicos, pero no son aplicables para los catiónicos. La modificación de la superficie de LDH con tensioactivos aniónicos permite obtener composites capaces de adsorber diferentes tipos de moléculas orgánicas [13, 14]. Las LDH modificadas con dodecil sulfato de sodio (DS) demostraron una absorción extremadamente alta de colorantes catiónicos como la safranina [15], el azul de metileno [16] y el azul básico [17].
Recientemente, las LDH se han investigado intensamente como fotocatalizadores heterogéneos prometedores debido a sus características intrínsecas de foto-respuesta, su bajo costo y su fácil preparación y modificación [18]. Las LDH como fotocatalizadores mostraron una gran eficiencia de conversión de energía como resultado de la alta dispersión de especies activas en una matriz estratificada, lo que facilita la separación de cargas. Los óxidos mixtos con propiedades semiconductoras se obtienen mediante calcinación de LDH que contienen metales de transición apropiados. Una amplia variedad de cationes metálicos, como Zn 2+ y Ti 4+ , se puede introducir en las capas [19, 20]. Sus proporciones relativas se pueden variar en una amplia gama, lo que permite la posibilidad de preparar óxidos semiconductores con propiedades sintonizables. Las aplicaciones fotocatalíticas de las LDH son un campo emergente interesante. Se han estudiado varios óxidos mixtos semiconductores derivados de LDH, como Zn-Al [20], Zn-Ce, ZnFe, Zn-Cr [21], Mg-Zn-Al [22] y Zn-Ga [23]. para la degradación fotocatalítica de contaminantes.
Además del color indeseable, los productos de degradación de los tintes también presentan un efecto mutagénico o cancerígeno en los seres humanos y su ingestión puede causar daños graves a los organismos. El cloro y el ácido hipocloroso, que se generan durante la degradación, son oxidantes tóxicos fuertes. Pueden oxidar materias orgánicas y al mismo tiempo se reducen a cloruro [24]. Como tinte básico importante utilizado para estampar calicó, teñir algodón y cuero, el MB podría causar varios efectos nocivos como quemaduras en los ojos, irritación del tracto gastrointestinal y de la piel. [25].
Se demostró la alta capacidad de adsorción de las capas intermedias de Zn-Al modificadas con DS para el azul de metileno (MB) [26]. La presencia de un componente fotoactivo en el adsorbente puede aumentar la eficiencia de los materiales basados en Zn-Al LDH para eliminar el tinte catiónico mediante el uso de irradiación UV. Así, en el presente trabajo se determinaron las condiciones óptimas para la preparación de LDH de Zn-Al para la remoción de colorantes catiónicos, como el MB por adsorción y fotodestrucción.
Métodos
Síntesis de LDH de Zn-Al
Todos los productos químicos eran de calidad analítica y se utilizaron sin purificación adicional. Las LDH de Zn-Al con carbonato como anión de capa intermedia, con [Zn]:[Al] =1:2 se sintetizaron mediante el método de coprecipitación a un pH constante similar a [9]. La primera solución que contiene Na 2 CO 3 (0,5 M) y se obtuvo NaOH (1,5 M). La segunda solución que contiene una mezcla de nitratos metálicos de Zn (NO 3 ) 2 ∙ 6H 2 O y Al (NO 3 ) 3 ∙ 9H 2 Se preparó O (la concentración total de metal fue 0,6 M, la relación molar de Zn / Al 2:1, 3:1, 4:1) y se añadió gota a gota a la primera solución con agitación. El pH se ajustó a 10 mediante la adición de NaOH. Una vez que se completó la adición, la temperatura se elevó a 85 o C y la suspensión se mantuvo durante 6 ha esta temperatura con agitación continua. Después de eso, la suspensión se enfrió a temperatura ambiente en varias horas. El producto se aisló por filtración y se lavó con agua desionizada hasta pH 7 varias veces. Posteriormente, el sólido se secó a 100 ° C. Las muestras se etiquetaron como ZnAl 21 LDH, ZnAl 31 LDH y ZnAl 41 LDH.
Las LDH de Zn-Al sintetizadas anteriormente se calcinaron a 450 ° C durante 2 hya 600 ° C durante 1, 2 y 5 h en aire. Las muestras se etiquetaron como ZnAl 21 -450, ZnAl 31 -450, ZnAl 41 -450, ZnAl 21 -600-1, ZnAl 31 -600-1, ZnAl 41 -600-1, ZnAl 21 -600-2, ZnAl 31 -600-2, ZnAl 41 -600-2, ZnAl 21 -600-5, ZnAl 31 -600-5, ZnAl 41 -600-5.
Las LDH de Zn-Al se modificaron con dodecilsulfato de sodio CH 3 (CH 2 ) 11 SO 4 Na por método de reconstrucción. Las suspensiones de 1 g de LDH calcinadas y 50 ml de soluciones acuosas de DS 0,05 M se agitaron durante 24 ha temperatura ambiente. Los compuestos obtenidos se etiquetaron como ZnAl 21 -450 / DS, ZnAl 31 -450 / DS, ZnAl 41 -450 / DS, ZnAl 21 -600-1 / DS ZnAl 31 -600-1 / DS ZnAl 41 -600-1 / DS.
Caracterización
Los patrones de XRD de las muestras se registraron con un difractómetro DRON-4-07 (Burevestnik Inc., San Petersburgo, Rusia), (CuK α radiación). El análisis termogravimétrico (TGA) y el análisis térmico diferencial (DTA) se llevaron a cabo utilizando un aparato Derivatograph Q-1500 D (MOM, Hungría) operado en flujo de aire a una velocidad de calentamiento de 10 ° min −1 . Los espectros de reflectancia difusa se obtuvieron con un espectrómetro Lambda 35 UV-Vis (Perkin Elmer, Alemania) equipado con un Labsphere RSA-PR-20 integrador en el rango de longitud de onda 200-1000 nm. Los espectros UV-visible de las soluciones se registraron utilizando un espectrómetro Lambda 35 UV-Vis (Perkin Elmer, Alemania).
Experimento fotocatalítico
Se dispersaron 0,020 g de Zn-Al LDH en 40 ml de 9 × 10 -5 M (para LDH calcinadas) y 10 -4 M (para LDH modificadas con DS) Solución acuosa de MB en el reactor de cuarzo. Antes de la iluminación, las suspensiones se agitaron durante 1 h (LDH calcinadas) y 24 h (LDH modificadas con DS) en la oscuridad para alcanzar un equilibrio de adsorción-desorción entre el fotocatalizador y las moléculas de MB. Luego, la solución se irradió durante 3 h con lámpara de vapor de mercurio (λ max =365 nm) bajo agitación magnética. En determinados intervalos de tiempo, la solución se analizó midiendo los espectros de absorción utilizando una espectrometría UV-Vis.
Resultados y discusiones
Caracterización
El patrón XRD para las LDH de Zn – Al sintetizadas con los diferentes Zn 2+ / Al 3+ relación catiónica se presentan en la Fig. 1a. La estructura similar a hidrotalcita se formó para todas las proporciones catiónicas. Los patrones XRD exhiben los reflejos característicos relacionados con los hidróxidos dobles en capas. Una fase adicional de ZnO estaba presente en el ZnAl 41 LDH como lo indican los patrones XRD. Los picos 2θ a 31,9 °, 34 ° y 36,2 ° pertenecen a la fase de ZnO formada en la superficie de las hojas similares a brucita. Todos los reflejos son nítidos, lo que indica un material altamente cristalino.
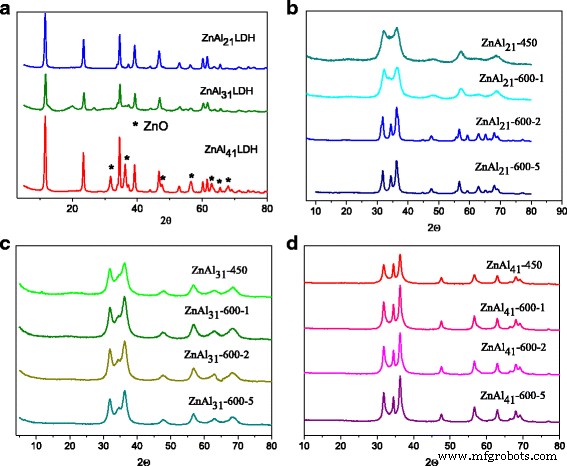
Patrones de difracción de rayos X de LDH de Zn-Al sintetizadas ( a ) y calcinado:ZnAl 21 LDH ( b ), ZnAl 31 LDH ( c ), ZnAl 41 LDH ( d )
El análisis de los patrones de XRD de los derivados calcinados mostró que la estructura estratificada de las LDH originales se destruyó por completo, lo que sugiere una descomposición casi total de las LDH originales y la eliminación de la mayoría de los aniones de carbonato entre capas y el agua (Fig. 1b-d). Todos los reflejos podrían indexarse perfectamente como la estructura hexagonal de wurtzita ZnO. Sin reflejos característicos correspondientes a Al 2 O 3 Se observaron fases en los patrones XRD. Debe tenerse en cuenta que el grado más alto de cristalinidad de ZnO se mejoró con el aumento de Zn 2+ / Al 3+ proporción catiónica.
Se sabe que la hidratación de las LDH de Zn-Al calcinadas en suspensión acuosa provocó la reconstrucción de la fase hidrotalcita [9]. Se pudo ver que la estructura en capas se restauró bajo hidratación de LDH de Zn-Al calcinadas en soluciones acuosas de DS (Fig. 2). La aparición de patrones de difracción en ángulos pequeños puso de manifiesto la presencia de LDH intercaladas por DS. Todas las LDH de Zn-Al modificadas con DS reconstruidas contenían también fase intercalada de carbonato. Cabe señalar que la reconstrucción completa de la estructura en capas se observó solo para ZnAl 21 -450 / DS LDH (figura 2a). Los patrones XRD de ZnAl 31 -450 / DS y ZnAl 41 -450 / DS LDH contenían reflejos de ZnO (Fig. 2a). Según [27], la hidratación de óxidos mixtos de Zn-Al con una relación Zn / Al 1:5 dio como resultado la formación de una estructura de hidrotalcita con Zn / Al =2, independientemente de la relación inicial Zn / Al. Entonces, ZnAl 31 -450 / DS, ZnAl 41 -450 / DS LDH contenían una menor cantidad de fase intercalada DS. Los patrones de XRD de todas las LDH modificadas con DS obtenidas a partir de óxidos mixtos de Zn-Al calcinados a 600 ° C contenían reflejos de la fase ZnO (Fig. 2b). Evidentemente, que la liberación continua de Zn 2+ de la fase de óxido amorfo condujo a la formación de más nanopartículas de ZnO con el aumento de la temperatura de calcinación.
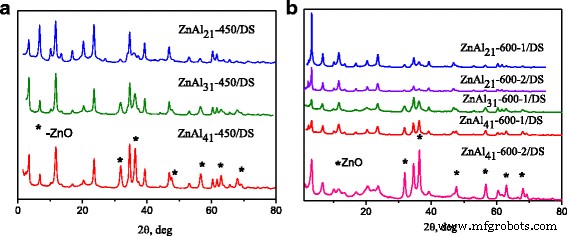
Patrones de difracción de rayos X de LDH de Zn-Al modificados con DS obtenidos mediante la reconstrucción de LDH calcinadas a 450 ° C ( a ) y 600 ° C ( b )
Las trazas termogravimétricas registradas para las LDH de Zn-Al fueron muy similares para todas las relaciones Zn / Al. Las curvas TG, DTA y DTG para las muestras con Zn / Al =4:1 se presentan en la Fig. 3. La gráfica TGA para LDH-carbonato (Fig. 3a) mostró la pérdida de masa en los rangos de temperatura de 60-190, 190–300 y 300–500 ° C. La pérdida de masa en el primer paso es una característica común de la hidrotalcita relacionada con la liberación de agua fisisorbida y entre capas. La segunda pérdida de masa se atribuyó al primer paso de deshidroxilación y eliminación de iones carbonato de la capa intermedia. En este rango de temperatura, la hidrotalcita experimentó reacciones de descarbonatación y deshidroxilación que dieron como resultado la formación de óxidos metálicos. En el tercer paso de la pérdida de masa que se produjo a más de 500 ° C, la pérdida de masa se reconoció como la deshidroxilación total y un colapso de la estructura debido a la eliminación de los aniones intercalares restantes [28]. La pérdida de masa insignificante observada a 500 - 1000 ° C puede atribuirse a la pérdida de algunos aniones de carbonato que están fuertemente adsorbidos en los cristalitos de óxidos mixtos [29].
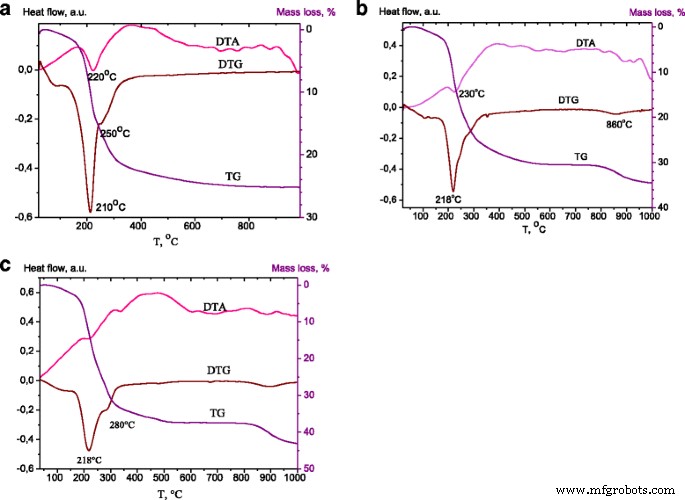
Curvas TG, DTA y DTG de ZnAl 41 LDH ( a ), ZnAl 41 -450 / DS ( b ), ZnAl 41 -600-1 / DS ( c )
Las etapas de descomposición térmica para todas las LDH de Zn-Al estudiadas se presentan en la Tabla 1. La pérdida de masa total disminuye al aumentar la relación Zn / Al en las LDH de ZnAl, ya que los materiales con menor densidad de carga contienen menos aniones carbonato. Además, como ZnAl 31 LDH y ZnAl 41 LDH contenía la fase de ZnO, la menor cantidad de hidróxidos metálicos e iones de carbonato entre capas estaba presente en las muestras. Entonces, los procesos de deshidroxilación y descarboxilación para ZnAl 31 LDH y ZnAl 41 LDH no fueron tan intensivos como para ZnAl 21 LDH.
Las trazas termogravimétricas registradas para ZnAl 41 -450 / DS presentado en la Fig. 3b. El primer paso de la descomposición térmica se atribuyó a la pérdida de agua entre capas. El segundo paso de la descomposición, la deshidroxilación de las láminas similares a la brucita, estuvo acompañada de la destrucción del DS. La descomposición de los iones DS tuvo lugar en el rango de 210–250 ° C [30, 31] y, por lo tanto, se observó una mayor pérdida por debajo de 200 ° C. La pérdida de masa de LDH modificadas por DS a 300-500 ° C se atribuyó a la deshidroxilación total y al colapso de la estructura en capas. El aumento de la pérdida de masa en esta etapa se debió a la carga de DS, cuya descomposición se reflejó en la pérdida de masa en 400–900 ° C. La pérdida de masa entre 800 y 900 ° C podría reconocerse como SO 3 evolución debido a la descomposición de (Zn, Al) sulfato formado por descomposición de DS durante la segunda etapa de pérdida de masa [32].
Las pérdidas de masa totales para ZnAl 31 -450 / DS y ZnAl 41 -450 / DS fueron menores en comparación con ZnAl 21 -450 / DS apuntó al menor contenido de fases intercaladas de DS- en las muestras con una relación Zn / Al 3:1 y 4:1. La presencia de reflejos de ZnO en los patrones de estas LDH indicó la reconstrucción incompleta de LDH bajo rehidratación de óxidos dobles mixtos en una solución acuosa de DS (Fig. 2a). Según [33], las extrafases coexisten en las LDH. Las LDH de Zn-Al sintetizadas y rehidratadas (Zn:Al =2:1) contenían aproximadamente 25 y 23% en peso de una fase amorfa [33]. Los autores encontraron que las muestras rehidratadas contenían aproximadamente 3 wt adicionales. El% de la fase de ZnO (zincita) resultó de la segregación de Zn de las capas similares a la brucita. Probablemente la modificación de ZnAl 21 Las LDH con DS provocaron la formación adicional de la fase de hidróxido de zinc amorfa. Como se sugiere en [27], hubo una reacción preliminar de rehidratación en una etapa temprana de reconstrucción de la fase de hidróxido de zinc amorfo y luego una rehidratación de los óxidos de Zn-Al durante el proceso de reconstrucción. Posiblemente, la rehidratación de la fase amorfa dio como resultado la formación de una fase intercalada de carbonato. La rehidratación de óxidos de Zn-Al en soluciones de DS provocó la formación de la fase intercalada de DS. Las pérdidas de masa de ZnAl 21 -600-1 / DS, ZnAl 31 -600-1 / DS, ZnAl 41 -600-1 / DS fueron significativamente diferentes. Obviamente, las LDH de Zn-Al calcinadas a 600 ° C contenían menos fase amorfa.
La presencia de ZnO fotoactivo amplía la gama de aplicaciones para LDH y compuestos basados en LDH, particularmente como fotocatalizadores, filtros UV, células solares sensibilizadas con colorante. Se examinó el efecto de las transformaciones de fase sobre la capacidad de las LDH de Zn-Al para absorber la luz ultravioleta. Los espectros de absorción óptica de las LDH de Zn-Al sintetizadas, las LDH de Zn-Al calcinadas y las LDH de Zn-Al modificadas con DS para muestras con Zn:Al =2:1 se muestran en la Fig. 4a, b. La reconstrucción de óxidos mixtos calcinados a 450 y a 600 ° C durante 1 hora promovió la formación de una cantidad adicional de ZnO cristalino, lo que resultó en el desplazamiento hacia el rojo de la banda de absorbancia de ZnAl 21 -450 / DS y ZnAl 21 -600-1 / DS (Fig. 4a, b). La banda de absorbancia de ZnAl 21 -600-2 se cambió a luz visible en aproximadamente 35 nm. No hubo cambios en la absorbancia de óxidos mixtos con Zn:Al =2:1 obtenido por calcinaciones de LDH durante 5 h (Fig. 4b).
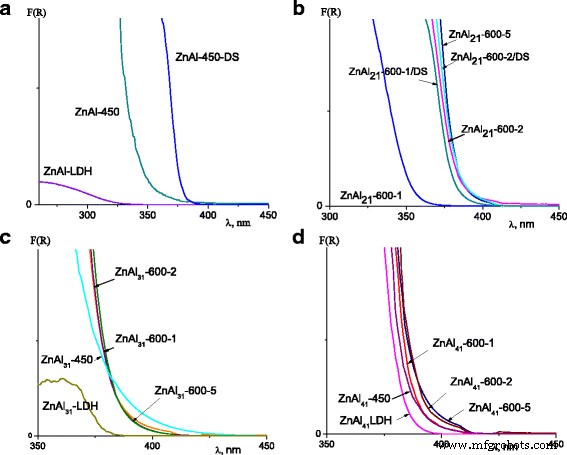
Espectros UV-Vis de LDH de Zn-Al con relación Zn / Al:2:1 ( a , b ), 3:1 ( c ), 4:1 ( d )
La posición de la banda de absorbancia de óxidos mixtos con Zn:Al =3:1 fue casi similar para las muestras tratadas a 450 y 600 ° C y fue independiente de la duración del tratamiento térmico (Fig. 4c). Para LDH de Zn-Al y óxidos mixtos con Zn:Al =4:1, las bandas de absorción se situaron a 382-390 nm (Fig. 4d).
Dado que Al 2 O 3 es un material con banda prohibida amplia (5,55 eV), cuya absorción de luz en el rango UV es causada por el ZnO presente en las muestras, cuya banda prohibida es de 3,37 eV [34]. Los valores de la energía de la banda prohibida (E g ) de las muestras se calcularon a partir de la intersección de los espectros UV-vis utilizando la ecuación:E g =1240 / λ [35] (Cuadro 3). Entre las LDH de Zn-Al calcinadas, el valor más bajo de energía de banda prohibida se observó para la muestra con el mayor contenido de Zn (Tabla 3).
Estudio fotocatalítico
Para evaluar el rendimiento fotocatalítico de Zn-Al LDH, la degradación de 2 * 10 -5 acuosos Se llevó a cabo una solución de MB M bajo luz ultravioleta. La escasa capacidad de absorción de luz de las LDH con una relación Zn / Al 2:1 y 3:1 provocó su baja actividad bajo irradiación (Tabla 2).
ZnAl 41 que contiene ZnO Las LDH entre las otras LDH demostraron la mayor actividad fotocatalítica en la destrucción de MB. La actividad fotocatalítica mejoró mucho cuando las muestras se calcinaron a 450 y 600 ° C debido a las mayores cantidades de fase de ZnO formada. Las curvas de fotodegradación de MB para las LDH de Zn-Al calcinadas a 600 ° C se presentan en la Fig. 5a. Dado que la diferencia en el rendimiento fotocatalítico de las LDH de Zn-Al calcinadas fue causada por la fase ZnO, las LDH con una relación Zn / Al 4:1 demostraron los mejores resultados en la fotodestrucción de MB.
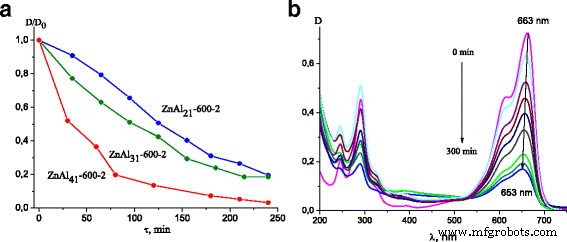
Curvas de degradación de MB sobre LDH de Zn-Al calcinadas bajo irradiación de luz ultravioleta ( a ); Cambios de absorción de 2 * 10 -5 Solución de M MB durante el proceso de fotodegradación sobre ZnAl 31 -600-1 ( b )
Los cambios en los espectros de absorbancia de la solución de MB durante diferentes tiempos de irradiación en presencia de ZnAl 31 -600-1 se puede ver en la Fig. 5b. Los picos a 610 y 663 nm se asignaron a la absorción del sistema π conjugado, mientras que los picos cercanos a 300 nm se asignaron a la absorción del anillo aromático [36]. Se pudo ver que la intensidad de los picos originales disminuyó con el aumento del tiempo de irradiación. Además, también se pudo observar una disminución paralela en las intensidades y un ligero desplazamiento al azul de las bandas ubicadas a 663 nm. Fue causado por la N-desmetilación de la fenotiazina y su degradación concomitante [37]. Se observaron cambios similares en los espectros de absorbancia óptica de MB para los sistemas fotocatalíticos con todas las LDH.
La modificación de DS de Zn-Al LDH aumentó su afinidad por MB debido a interacciones hidrófobas entre los tensioactivos y las moléculas de colorante [26]. ZnAl 41 -600-1 / DS demostró el mejor resultado en la adsorción de MB (Tabla 3). La actividad fotocatalítica de las LDH de organo / Zn-Al fue comparable con las LDH de Zn-Al calcinadas (Tabla 3). El mayor nivel de degradación de MB se observó para ZnAl 41 -450 / DS. Los valores de eliminación de MB con LDH de Zn-Al modificado con DS por adsorción fueron más altos que los de por fotodestrucción . Por lo tanto, la eliminación por adsorción de MB con LDH de organo / Zn-Al podría mejorarse mediante la aplicación de irradiación de luz.
Probablemente, la fotodestrucción del tinte se ha producido en la superficie de las LDH de Zn-Al modificadas con DS que no se fijaron en las condiciones experimentales. Después de lograr el equilibrio, las LDH de Zn-Al modificadas por DS con MB adsorbido tenían un color azul intenso.
Conclusiones
En este trabajo, se prepararon las LDH de Zn-Al as-sintetizadas y calcinadas con diferentes proporciones catiónicas. Los materiales obtenidos se caracterizaron y utilizaron para la eliminación del tinte catiónico MB de soluciones acuosas. Los estudios de fotodestrucción de MB bajo luz ultravioleta sobre LDH y LDH calcinadas indican que:
La actividad fotocatalítica de las LDH de Zn-Al se originó a partir de la presencia de la fase ZnO. La formación de la fase ZnO en las LDH podría estar regulada por el aumento de la relación Zn / Al en las LDH y con el tratamiento de temperatura de las LDH.
La influencia de la relación Zn / Al sobre la actividad fotocatalítica de las LDH fue predominante. La fotodegradación de MB en el presente del ZnAl sintetizado 41 LDH y ZnAl 41 La LDH a 600 ° C fue 72 y 95%, respectivamente. Para calcinado a 600 ° C ZnAl 31 LDH y ZnAl 21 LDH, la fotodegradación de MB fueron 76 y 74%, respectivamente.
Las LDH de organo / Zn-Al mostraron una alta capacidad de adsorción al tinte catiónico MB. También demostraron las actividades fotocatalíticas en la destrucción de MB. Por lo tanto, la eliminación por adsorción de MB de soluciones con LDH de Zn-Al modificadas con DS podría mejorarse mediante el uso de irradiación UV.
Nanomateriales
- Actividades fotocatalíticas mejoradas por nanopartículas au-plasmónicas en un fotoelectrodo de nanotubos de TiO2 recubierto con MoO3
- Un nuevo fotocatalizador de heterounión Bi4Ti3O12 / Ag3PO4 con rendimiento fotocatalítico mejorado
- Efectos sinérgicos de nanopartículas de Ag / BiV1-xMoxO4 con actividad fotocatalítica mejorada
- Nuevos conocimientos sobre la adsorción de CO2 en nanomateriales basados en hidróxido doble en capas (LDH)
- Eficiencia de conversión de energía mejorada de células solares de perovskita con un material de conversión ascendente de Er3 + -Yb3 + -Li + TiO2 tri-dopado
- Eliminación de antibióticos del agua con una membrana de nanofiltración 3D totalmente de carbono
- Rendimiento energético mejorado basado en la integración con los nanolaminados de Al / PTFE
- Propiedades fotovoltaicas mejoradas en la celda solar de heterounión plana Sb2S3 con un enfoque de selección rápida
- Rendimiento fotovoltaico de células solares de matriz de nanoconos de unión de clavijas con absorción óptica eficaz mejorada
- La respuesta fotocorriente extremadamente mejorada en nanohojas de aislante topológico con alta conductividad
- Nanoesferas de caolinita de estructura jerárquica con propiedades de adsorción notablemente mejoradas para el azul de metileno



