Estudio comparativo del efecto antimicrobiano de nanocompuestos y compuestos basados en poli (adipato-co-tereftalato de butileno) utilizando nanopartículas de Cu y Cu / Cu2O y CuSO4
Resumen
Se sintetizaron nanocompuestos y un compuesto a base de poli (adipato-co-tereftalato de butileno) (PBAT) utilizando nanopartículas de cobre comerciales (Cu-NP), nanopartículas de cobre / óxido cuproso (Cu | Cu 2 O-NPs) y sulfato de cobre (CuSO 4 ), respectivamente. El Cu | Cu 2 Las O-NP se sintetizaron mediante reducción química y se caracterizaron por difracción de rayos X (XRD) y microscopía electrónica de transmisión (TEM). La síntesis de Cu | Cu 2 Los O-NP produjeron una mezcla de Cu y Cu 2 O, con metal Cu que tiene una morfología esférica de aproximadamente 40 nm de diámetro y Cu 2 O con un diámetro de 150 nm. Para preparar los nanocomposites (NC) y el material compuesto (MC), los NP y el CuSO 4 La sal se incorporó a la matriz de PBAT en concentraciones de 1, 3 y 5% p / p mediante un método ex situ. La espectroscopia infrarroja por transformada de Fourier (FTIR), una prueba de tracción, calorimetría diferencial de barrido (DSC), análisis termogravimétrico (TGA) y ensayos de difusión en agar se utilizaron para la caracterización estructural, termomecánica y antimicrobiana. Los resultados mostraron que los refuerzos no modificaron la estructura química del PBAT y solo aumentaron ligeramente el porcentaje de cristalización. Las propiedades mecánicas y térmicas del PBAT no cambiaron mucho con la adición de cargas, excepto por un ligero aumento en la resistencia a la tracción y la estabilidad térmica, respectivamente. Los ensayos antimicrobianos de difusión en agar mostraron que los NC y los MC tenían buenas respuestas inhibidoras contra las cepas no resistentes Enterococcus faecalis , Streptococcus mutans y Staphylococcus aureus . Los MC basados en CuSO 4 tuvo el mayor efecto biocida, incluso contra la bacteria resistente Acinetobacter baumannii .
Introducción
La mayoría de los materiales plásticos se producen a partir de combustibles fósiles y son prácticamente no degradables, lo que genera preocupaciones sobre la sostenibilidad económica y medioambiental [1, 2]. Así, el desarrollo y síntesis de materiales biodegradables de otra fuente ha recibido mucha atención por parte de la comunidad científica con el objetivo de reducir la producción de plásticos derivados del petróleo [3,4,5]. Los polímeros biodegradables han comenzado a jugar un papel fundamental en la solución de estos problemas como una opción prometedora a los combustibles fósiles junto con una nueva clase de materiales conocidos como bionanocomposites, que a través de la nanotecnología han llegado a poseer mejores propiedades [6,7,8,9 , 10].
Los bionanocomposites consisten en una matriz orgánica en la que se dispersan nanomateriales inorgánicos [8, 11,12,13]. Las diferentes morfologías y tamaños de los componentes inorgánicos, como nanopartículas, nanotubos, nanoláminas, nanocables y nanoarcillas, tienen un efecto considerable sobre las propiedades de la matriz polimérica. Las propiedades ópticas, térmicas, mecánicas, magnéticas y optoelectrónicas se mejoran debido a la sinergia entre el área de la superficie, la alta reactividad de la superficie, la excelente estabilidad térmica y la alta resistencia mecánica de los componentes inorgánicos y la matriz polimérica [14,15,16]. . Una amplia gama de innovaciones en química de polímeros y técnicas de micro y nanofabricación han impulsado la investigación en bionanocomposites de polímeros, no solo para la producción de estructuras mejoradas, sino también para la preparación de nuevos materiales funcionales con propiedades interesantes y aplicaciones altamente sofisticadas [17,18 , 19]. Se han estudiado ampliamente varios biopolímeros de origen natural o sintético, como el ácido poliláctico (PLA) [20] y el poli (adipato-co-tereftalato de butileno) (PBAT) [21, 22].
Un polímero que se utiliza actualmente como matriz en nanocompuestos es el PBAT [23]. Este biopolímero sintético es un poliéster biodegradable alifático lineal basado en los monómeros 1,4-butanodiol, ácido adípico y ácido tereftálico en la cadena del polímero [24]. Sus propiedades son similares a las del polietileno de baja densidad debido a su alto peso molecular y su estructura molecular ramificada de cadena larga, lo que lo hace flexible [24,25,26]. La principal limitación del PBAT es su escasa resistencia mecánica; sin embargo, con la adición de cargas nanométricas, esta desventaja se puede superar dotando a este material de propiedades multifuncionales como mejores propiedades termomecánicas [6, 27].
Actualmente, también existe una necesidad urgente de desarrollar bionanocomposites que puedan controlar o prevenir la colonización microbiana incorporando nanopartículas con actividad antibacteriana conocida o mejorando las propiedades antibacterianas que ya posee la matriz polimérica. En este último caso, la mejora sustancial de la capacidad biocida de la matriz polimérica se ha asociado con la sinergia entre los dos componentes del bionanocompuesto [28, 29]. Por lo tanto, el polímero no solo proporciona una matriz de soporte para las nanopartículas, sino que también puede mejorar el desempeño antibacteriano y extender las posibles aplicaciones del bionanocompuesto para cumplir con varios requisitos para aplicaciones biomédicas o dispositivos médicos como tubos endotraqueales y catéteres vasculares y urinarios [30 , 31,32]. Sin embargo, el uso de PBAT en dispositivos médicos no se ha estudiado ampliamente; solo unos pocos artículos han informado de la posibilidad de su uso en algunas aplicaciones clínicas [1].
Varias investigaciones han informado del uso de nanopartículas metálicas como agente antimicrobiano. La propiedad biológica intrínseca de estos materiales depende de varios factores, como el metal involucrado, el tamaño de partícula, la estructura y el área de la superficie. Todas las posibles combinaciones de estos factores pueden retrasar la resistencia a los antibacterianos [33]. La mayoría de los estudios antimicrobianos de nanocompuestos se han centrado en el envasado de alimentos y la actividad biocida siempre se ha dirigido a las mismas bacterias. No es seguro si las bacterias se vuelven resistentes a las nanopartículas biocidas de la misma manera que lo hacen a los medicamentos. Así, uno de los objetivos de este trabajo fue evaluar la actividad antimicrobiana de nanocomposites que contienen PBAT con diferentes concentraciones de Cu-NPs para su potencial uso en la fabricación de implementos dentales. Además, realizamos un estudio comparativo completo sobre las propiedades termomecánicas y antimicrobianas de los materiales basados en PBAT. Los nanocompuestos de PBAT se prepararon con nanopartículas de Cu en tres concentraciones diferentes. Del mismo modo, los nanocomposites se prepararon utilizando Cu | Cu 2 O-NPs como carga. Finalmente, un CuSO 4 Se preparó material compuesto a base de las mismas concentraciones que se utilizaron para preparar los nanocomposites. Se evaluó la actividad biocida de los nanocompuestos y el compuesto PBAT frente a Staphylococcus aureus , que es responsable de infecciones cutáneas como foliculitis, furunculosis y conjuntivitis; Streptococcus mutans , que es en parte responsable de la placa dental y la biopelícula dental; y Enterococcus faecalis y Acinetobacter baumannii , que puede causar infecciones que comprometen a los humanos, especialmente en el entorno hospitalario.
Materiales y métodos
Materiales
El PBAT (Ecoflex) utilizado para la preparación de nanocomposites fue suministrado por BASF (Ludwigshafen, Alemania). Su estructura molecular se muestra en el archivo adicional 1:Figura S1 (material complementario). Las nanopartículas de Cu de metal puro al 99,99% (Sigma-Aldrich, St. Louis, MO, EE. UU.) Tenían entre 100 y 200 nm de diámetro. Para la síntesis de Cu | Cu 2 O-NP, CuSO 4 se utilizó como precursor, ácido ascórbico (C 6 H 8 O 6 ) como agente reductor e hidróxido de sodio (NaOH) como controlador de pH. Además, CuSO 4 (Sigma-Aldrich) se utilizó para preparar el material compuesto.
Síntesis de nanopartículas por reducción química
Un método de síntesis propuesto por Khan et al. [34] se utilizó para obtener Cu | Cu 2 O-NPs. La síntesis comenzó disolviendo CuSO 4 × 5H 2 O en agua destilada para obtener 120 mL de solución 0.1 M. A continuación, los 120 mL de CuSO 4 se añadió a un matraz sumergido en un baño de propilenglicol, seguido de la adición rápida de 50 ml de C 6 H 8 O 6 solución. La mezcla se agitó vigorosamente a aproximadamente 390 rpm durante 30 min mientras se aumentaba la temperatura a 80ºC, tras lo cual se añadieron gota a gota 30 ml de solución de NaOH y la solución se agitó continuamente durante 2 h. Se dejó sedimentar la solución final durante la noche y luego se eliminó el líquido sobrenadante. El concentrado se centrifugó y se lavó con agua destilada y etanol. Finalmente, las partículas se dispersaron utilizando un equipo de ultrasonido, se colocaron en placas de Petri y se secaron en el horno a 60 ° C durante la noche (consulte el archivo adicional 1:Figura S2).
Síntesis de nanocompuestos
Para preparar los nanocomposites y el material compuesto, Cu-NPs, Cu | Cu 2 O-NP y CuSO 4 La sal se incorporó a la matriz de PBAT en concentraciones de 1, 3 y 5%. Primero, se fundió el PBAT y luego se agregaron los NP y se mezclaron en un reómetro de torque (modelo 835205, Brabender GmbH &Co. KG, Duisburg, Alemania) durante 7 min a 60 rpm y una temperatura de trabajo de 140 ° C ( Archivo adicional 1:Figura S4). La carga máxima fue del 5% porque cargas más altas produjeron efectos de fluorescencia en los espectros Raman (Archivo adicional 1:Figura S3).
Caracterización
Los nanocomposites y materiales compuestos obtenidos se caracterizaron para estudiar sus diferencias con respecto al polímero PBAT. Asimismo, estudiamos cómo las diferentes concentraciones de Cu-NP, Cu | Cu 2 O-NP y CuSO 4 dentro del polímero afectó sus propiedades mecánicas, térmicas, morfológicas, estructurales y bactericidas.
Cu-NP y Cu | Cu 2 Las O-NP se caracterizaron mediante difracción de rayos X (XRD) y microscopía electrónica de transmisión (TEM). Nanocompuestos PBAT con Cu-NP (NCs-PBAT / Cu) y Cu | Cu 2 O-NP (NC-PBAT / Cu | Cu 2 O) y el material compuesto PBAT con CuSO 4 (MC-PBAT / CuSO 4 ) se caracterizaron mediante análisis termogravimétrico (TGA), calorimetría diferencial de barrido (DSC), microscopía electrónica de barrido (SEM), espectroscopia infrarroja por transformada de Fourier (FTIR), XRD, pruebas de tracción y ensayo de actividad antimicrobiana mediante difusión en agar. Se preparó una muestra en forma de placa de 100 mm x 100 mm x 1 mm de cada nanocompuesto de modo que las muestras homogeneizadas en cada análisis tuvieran el mismo tamaño. Para obtener la forma de la placa, NCs-PBAT / Cu, NCs-PBAT / Cu | Cu 2 O y MCs-PBAT / CuSO 4 se moldearon utilizando una prensa hidráulica Labtech (modelo LP-20B; Labtech Engineering Co., Ltd., Samutprakarn, Tailandia) a 160 ° C y 110 bares durante 5 min. Los tiempos de precalentamiento y enfriamiento fueron de 15 min y 1 min, respectivamente (Archivo adicional 1:Figura S4).
Propiedades morfológicas y estructurales
Verificar la escala nanométrica de las nanopartículas y que los polvos sintetizados fueran una mezcla de Cu y Cu 2 O nanopartículas, se realizó un análisis estructural mediante XRD y un análisis morfológico mediante TEM.
Micrografías TEM de Cu | Cu 2 Los O-NP se obtuvieron con un microscopio electrónico de transmisión JEM 1200 EX II (JEOL, Ltd., Tokio, Japón) a un voltaje de 120 kV. Se preparó una muestra colocando una gota de nanopartículas diluidas en etanol sobre una rejilla de cobre recubierta de carbono de malla 200. Además, las nanopartículas se analizaron mediante un patrón de difracción de electrones.
Espectros XRD de Cu-NP, Cu | Cu 2 Se obtuvieron O-NP, nanocomposites y material compuesto utilizando un difractómetro Bruker Endeavour (modelo D4 / MAX-B; Bruker, Billerica, MA, EE. UU.). El barrido de 2θ fue de 4 a 80 ° con un paso de 0.02 ° y un tiempo de conteo de 1 s. El difractómetro se hizo funcionar a 20 mA y 40 kV con una lámpara de cátodo de cobre ( λ =1,541 Å).
Los espectros FTIR de los nanocomposites se obtuvieron utilizando un espectrómetro FTIR Spectrum Two (× 1720) (PerkinElmer, Waltham, MA, EE. UU.) Con la función de reflexión total atenuada (ATR). Cada espectro se obtuvo mediante exploraciones consecutivas en el rango de 4000 a 500 cm −1 con una resolución de 1 cm −1 .
Propiedades mecánicas (prueba de tracción)
Las pruebas de tracción, basadas en la norma ASTM D638, se llevaron a cabo en una máquina de prueba universal smarTens (modelo 005; Emmeram Karg Industrietechnik, Krailling, Alemania) a una velocidad de prueba de 50 mm / min y una celda de carga de 1 kN. Las probetas tipo V se fabricaron por compresión a temperaturas de moldeo de 160 ° C. Los tiempos de precalentamiento, prensado y enfriamiento fueron de 7, 5 y 1 min, respectivamente. Se fabricaron cinco muestras de cada NC y MC en estudio y se obtuvieron la resistencia a la tracción, el porcentaje de alargamiento final y el módulo.
Propiedades térmicas
La TGA se llevó a cabo utilizando una termomicrobalanza TG 209 FI Iris® (NETZSCH-Gerätebau GmbH, Selb, Alemania). Las muestras, que iban de 3 a 10 mg, se colocaron en crisoles de aluminio, que luego se cargaron en el instrumento. El cambio de masa en función de la temperatura se midió calentando las muestras de 20 a 600 ° C a una velocidad de 10 ° C / min bajo una N 2 atmósfera.
El análisis de DSC se realizó utilizando un calorímetro de barrido diferencial NETZSCH (modelo DSC 204 F1). Se colocaron muestras de nanocompuestos (5 a 10 mg) en crisoles de aluminio sellados, que se calentaron de 25 a 200 ° C a una velocidad de 10 ° C / min bajo una constante N 2 caudal de 20 mL / min. La temperatura de fusión ( T m ) se obtuvo a partir de este análisis DSC.
Ensayos de actividad antimicrobiana de NC y CM mediante difusión de agar
La actividad antibacteriana de los nanocomposites y el material compuesto a base de Cu-NPs, Cu | Cu 2 O-NP y CuSO 4 se determinó mediante el método de cinética de crecimiento por difusión en agar. El análisis se realizó en dos etapas siguiendo el protocolo de Jaramillo et al. [35]. Se utilizaron cuatro cepas de bacterias:dos cepas clínicas, A. baumannii (ABA 538) aislado de una infección intrahospitalaria y E. faecalis (6.4) de una infección oral, y dos cepas de colección, S. aureus (ATCC) y S. mutans (ATCC 25175).
La primera etapa consistió en una evaluación cualitativa de la actividad antibacteriana para seleccionar cuál de las tres concentraciones de nanocomposites y material compuesto usar para realizar las pruebas cuantitativas para reducir el diseño experimental porque usar tres concentraciones de carga sería muy costoso. Después de las pruebas de evaluación, se seleccionó la muestra con el porcentaje de carga que presentó la mejor inhibición de contacto. Para realizar las pruebas cualitativas, A. baumannii (ABA 538), E. faecalis (6,4), S. aureus (ATCC) y S. mutans (ATCC 25175) se sembraron por separado en un agar tripticasa de soja (TSA) y se incubaron durante la noche a 37 ° C. Después del cultivo, se seleccionó una colonia bien aislada y se transfirió a un tubo que contenía 4 a 5 ml de caldo TSA utilizando un asa de inoculación. El caldo se incubó de nuevo durante la noche a 37 ° C hasta que alcanzó o excedió la turbidez de 0,5 en la escala de McFarland. A continuación, se ajustó la turbidez del inóculo con solución salina hasta 0,5 en la escala de McFarland utilizando un turbidímetro. La suspensión preparada contenía aproximadamente 1 × 10 8 UFC / mL, que se diluyó a 1:10 para obtener una concentración final de inóculo de 10 7 UFC / mL. Las placas de TSA se sembraron uniformemente con cada inóculo. Luego, hojas (10 × 10 mm 2 ) de los nanocompuestos y el material compuesto en concentraciones de 1, 3 y 5%, más un control de PBAT, se colocaron en la superficie de las placas de TSA y se verificaron para asegurarse de que se adhirieran bien. Finalmente, las placas se colocaron en un horno y se incubaron a 37 ° C durante 24 h para observar la inhibición de las muestras de PBAT.
La segunda etapa del método de cinética de crecimiento consistió en pruebas cuantitativas realizadas solo en aquellos nanocompuestos y material compuesto donde la inhibición por contacto era evidente en la prueba cualitativa. Para mantener la esterilidad, las pruebas se llevaron a cabo utilizando una cabina de seguridad biológica tipo A2 Serie 1200 (ThermoFisher Scientific, Waltham, MA, EE. UU.). Primero, las muestras se acondicionaron previamente colocándolas dentro de placas de Petri estériles y llevándolas a la cabina de bioseguridad donde se expusieron a la luz ultravioleta durante 15 minutos en cada lado. A continuación, los cultivos bacterianos de 24 h de cada cepa se ajustaron a una turbidez de 0,5 en la escala de McFarland para crear posteriormente seis diluciones en serie (1, 2, 3, 4, 5 y 6). Se realizó un recuento inicial en las diluciones 4, 5 y 6 (por triplicado) para determinar el recuento en el tiempo cero.
Se prepararon cámaras húmedas, una para cada tiempo de evaluación (2, 4, 6 y 8 h) y para cada cepa, colocando una gasa estéril humedecida con agua destilada estéril en placas de Petri estériles. Luego, se colocó un portaobjetos estéril dentro de cada cámara húmeda de manera que el lado superior no tocara la gasa húmeda. A continuación, tres 2 de 1 × 1 cm Se colocaron en las cámaras láminas de los nanocomposites y material compuesto, y láminas de PBAT como controles, con la ayuda de una pinza estéril. Se depositó la dilución (20 μL) en cada hoja cuadrada y las cámaras se incubaron a 37 ° C durante 2, 4, 6 y 8 h.
Después de la incubación, se extrajeron las cámaras húmedas y cada hoja de polímero se depositó dentro de un tubo Falcon con 1 mL de agua destilada estéril. Los tubos se agitaron con vórtex durante 2-5 min [35]. Se hicieron tres diluciones del producto en los tubos Falcon. Las placas de Petri que contenían TSA se dividieron en cuatro partes. Aproximadamente de tres a cinco gotas (correspondientes a 20 μL) de cada una de las tres diluciones y una gota del contenido del tubo Falcon sin diluir se colocaron en los cuadrantes. Las placas de agar tenían que estar completamente secas para que las gotas se absorbieran casi instantáneamente. A continuación, las placas se incubaron a 37 ° C durante 24 h seguido de un recuento de colonias con un contador de colonias. Los datos obtenidos se multiplicaron por el factor de dilución utilizado y se trazaron en gráficos utilizando la función logarítmica o porcentaje de supervivencia.
Resultados y discusión
La reometría se utiliza para obtener medidas dinámicas de las propiedades reológicas de los nanocompuestos en condiciones cercanas a las condiciones reales en las que se procesaron los nanocompuestos. Para ello, se realizaron medidas para controlar los cambios de viscosidad durante el mezclado en estado fundido. Los resultados de estas mediciones se muestran en el archivo adicional 1:Figura S5. El aumento del par motor está relacionado con la viscosidad de fusión del polímero [21, 36], y los valores comienzan a ser constantes después de 4 min de mezclado. Esto confirma que el tiempo de mezclado de 7 min establecido en este trabajo fue suficiente para lograr un mezclado completo.
Los valores de torque para la matriz PBAT y NCs-PBAT / Cu 1% fueron de alrededor de 19,86 N m. Las curvas (Archivo adicional 1:Figura S5) indican que la concentración del 1% de Cu-NP tuvo poco efecto sobre las propiedades mecánicas de la matriz, pero se obtuvieron valores de torque de equilibrio más bajos de 18,4 y 17,4 N m para NCs-PBAT / Cu 3 % y NCs-PBAT / Cu 5%, respectivamente. Estos resultados implican claramente que la procesabilidad de NCs-PBAT / Cu mejoró con respecto a la matriz PBAT [37]. Se obtuvieron resultados similares con la mezcla de NCs-PBAT / Cu | Cu 2 O, donde el valor del par de equilibrio disminuyó con el aumento del porcentaje de carga al 3%, pero la carga del 5% arrojó un valor muy cercano al de la carga al 1% de Cu | Cu 2 O-NPs. Los valores de par de equilibrio fueron 19,39, 19,07 y 19,37 Nm para 1, 3 y 5%, respectivamente. Para MCs-PBAT / CuSO 4 mezcla, los valores de par de equilibrio aumentaron a medida que la carga de CuSO 4 aumentado, es decir, 18,71 N m para 1%, 19,16 N m para 3% y 19,79 N m para 5% de carga. Este comportamiento se puede atribuir al tamaño del CuSO 4 cristales. Simultáneamente, archivo adicional 1:La figura S5 muestra que el par de equilibrio de todos los nanocomposites y material compuesto fue estable con el aumento del tiempo de mezcla, lo que indica que la descomposición térmica no ocurrió en el mezclador, probablemente porque las nanopartículas disminuyen las fuerzas de cohesión entre las cadenas de polímero y lo más probable es que realice una autolubricación en el proceso de mezcla [37].
Propiedades morfológicas y estructurales
Primero, se analizaron las nanopartículas obtenidas por reducción química. Los resultados de la síntesis de Cu | Cu 2 Los O-NP se muestran en la Fig. 1b. La micrografía TEM muestra una mezcla de partículas esféricas y partículas poliédricas. El diámetro medio de las nanopartículas esféricas fue de 26 nm (Fig. 1c), mientras que el diámetro de las nanopartículas poliédricas osciló entre 80 y 160 nm. La composición de estas nanopartículas se determinó mediante difracción de electrones de área seleccionada (SAED) (Fig. 1c), que encontró fases correspondientes al metal Cu y Cu 2 O. Este hallazgo fue corroborado por el difractograma que se muestra en la Fig. 1a. Se observaron claramente seis picos de difracción a 2θ =36,3 °, 42,17 °, 43,42 °, 50,63 °, 61,47 ° y 74,37 °. Porque las nanopartículas se sintetizaron reduciendo químicamente CuSO 4 a CuO, los picos de difracción fueron verificados por los datos de Cu en la base de datos X’Pert HighScore de patrones de difracción de rayos X en polvo. Observamos que los picos en 2θ =43,2 °, 50,63 ° y 74,37 ° pertenecen a los planos de difracción de Cu metálico (111), (200) y (220). Los otros tres picos muestran que las nanopartículas sintetizadas contenían más de una sustancia, por lo que el patrón de difracción es una combinación de ambas. Wijesundera [38] analizó películas delgadas de Cu 2 O usando XRD y mostró que los planos difractados a 2θ =36,3 °, 42,17 ° y 61,47 ° corresponden a los índices de Miller (111), (200) y (220). Estos índices pertenecen a una estructura cúbica centrada en las caras (FCC) que corresponde a una parte del área central de una estructura antifluorita, que concuerda con la estructura de Cu 2 O, de acuerdo con los hallazgos del análisis SAED.
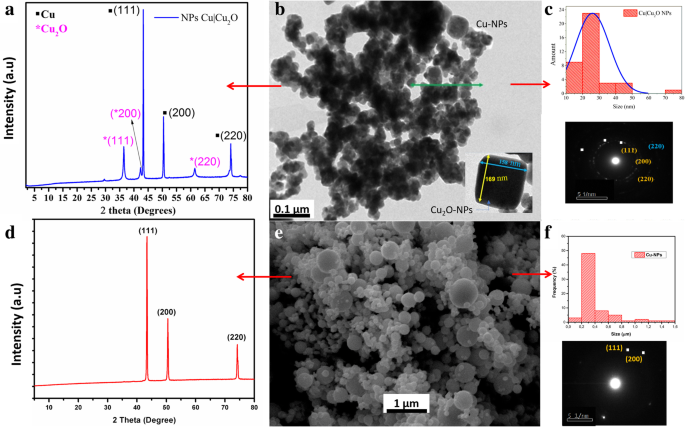
un XRD de nanopartículas de Cu y CuO2 sintetizadas. b , c Imagen TEM, distribución de tamaño y patrón de difracción de las nanopartículas sintetizadas. d XRD de nanopartículas de Cu. e , f Imagen TEM, distribución de tamaño y patrón de difracción de nanopartículas de Cu
Wang y col. [39] encontró que durante la síntesis de Cu-NP por reducción química, el tamaño de las partículas variaba entre 100 y 150 nm. Usaron C 6 H 8 O 6 como agente reductor y poli (vinilpirrolidona) (PVP) como tensioactivo. Las caras no correspondían a las de Cu 2 O porque el PVP ayudó a estabilizar las semillas en crecimiento, evitando así su oxidación. Sin embargo, el objetivo de nuestra investigación fue sintetizar Cu 2 O NP, que se puede lograr mediante reducción química sin el uso de un agente estabilizador como PVP.
Las Cu-NP utilizadas en la preparación del nanocompuesto eran esféricas con un diámetro que variaba entre 100 y 200 nm (Fig. 1e, f). En el patrón XRD para Cu-NP que se muestra en la Fig. 1d, los tres picos claramente observados a 43,60 °, 50,72 ° y 73,95 ° corresponden a los planos cristalinos (111), (200) y (220), respectivamente. La estructura cristalina cúbica con un grupo espacial Fm3m (JCPDS No.85-1326) [55] está de acuerdo con la estructura encontrada por el análisis SAED (Fig. 1d).
Las partículas metálicas utilizadas en nuestro estudio se obtuvieron mediante un sistema de trituración mecánica, según el proveedor. La desventaja de este método es que un pequeño porcentaje de partículas (~ 10%) son mayores de 500 nm. Sin embargo, esto no afectó negativamente a los objetivos de nuestra investigación. A continuación, demostramos cómo esta dispersión afectó las propiedades termomecánicas de la matriz PBAT. Es importante destacar que los métodos de trituración mecánica no utilizan precursores ni estabilizadores, como es el caso de los métodos de síntesis húmeda, que se conocen como métodos de reducción química. Por lo tanto, la superficie de las Cu-NP obtenidas por trituración no se pasiva por la adsorción de moléculas ni de un estabilizador ni de un subproducto de reacción. Por tanto, estas Cu-NP, aunque no mejoran sustancialmente las propiedades mecánicas del polímero, tampoco las degradan. Sin embargo, las propiedades antimicrobianas deben mejorarse debido a la migración de Cu 2+ se facilita en superficies no pasivadas.
La Figura 2 presenta los espectros XRD de NCs-PBAT / Cu (Fig. 2a), NCs-PBAT / Cu | Cu 2 O (Fig. 2b) y MCs-PBAT / CuSO 4 (Figura 2c). La Figura 2c se preparó en tres concentraciones (1, 2 y 3% w / w ). Estos difractogramas se compararon con los de la matriz de polímero PBAT para demostrar el efecto de las cargas sobre la estructura del polímero. El difractograma PBAT mostró un patrón de difracción con cinco picos de difracción en 2θ =16.1 °, 17.3 °, 20.2 °, 23.1 ° y 25 °, correspondientes a los planos (011), (010), (101), (100) y (111), respectivamente. Este análisis reveló la existencia de cristalinidad en la matriz del polímero. La caracterización de PBAT por Arruda et al. [40] utilizando XRD también encontró los mismos cinco picos de difracción en los mismos ángulos que los encontrados en esta investigación, correspondientes a los mismos planos.
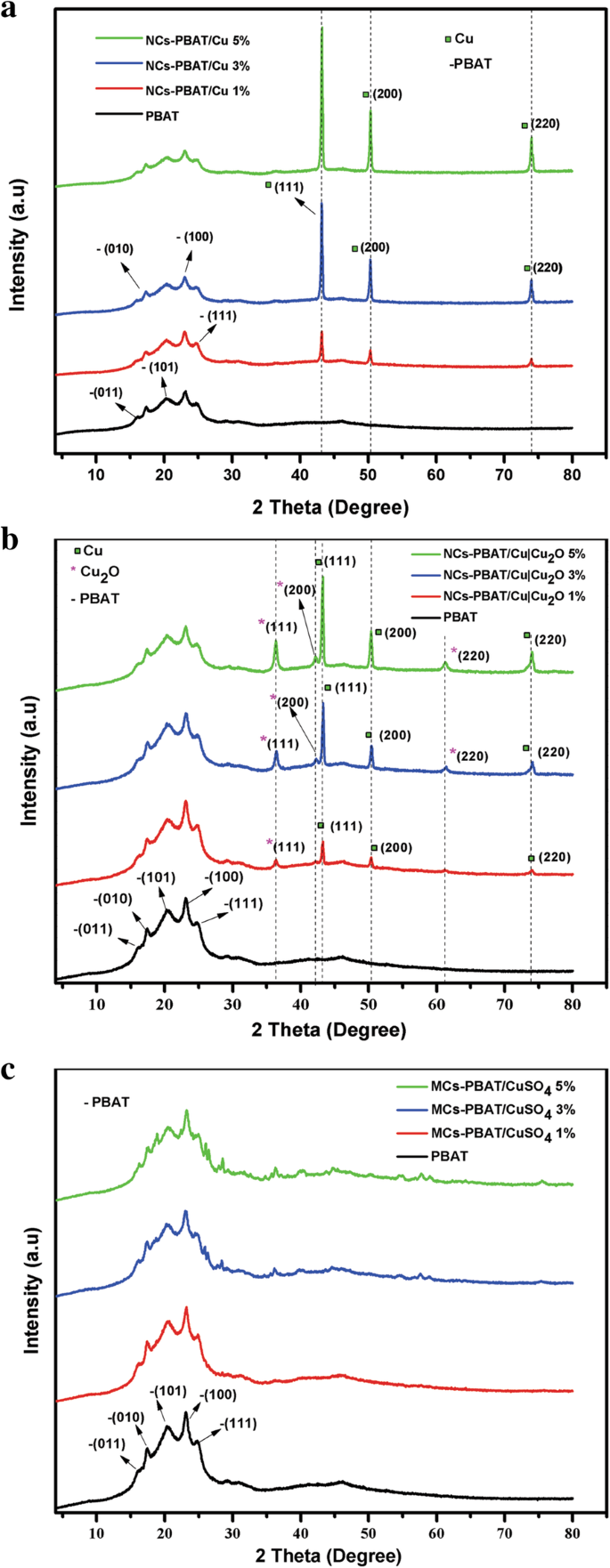
Difractograma de PBAT, NCs-PBAT / Cu, NCs-PBAT / Cu | Cu 2 O y MCs-PBAT / CuSO 4
Los difractogramas de los nanocompuestos con cargas de Cu-NP se muestran en la Fig. 2a. Las señales 2θ a 43 °, 50 ° y 74 ° son características de los planos (111), (200) y (220) de la estructura FCC de Cu con un grupo espacial Fm3m (JCPDS No.85-1326) [ 41]. Sin fases correspondientes a CuO o Cu 2 Se observaron O en el difractograma de NCs-PBAT / Cu, por lo que concluimos que las nanopartículas no se oxidaron durante la síntesis del nanocompuesto. Además, los difractogramas muestran que las nanopartículas no afectaron ni modificaron la estructura del PBAT y que la intensidad de los picos es directamente proporcional al porcentaje de carga de las Cu-NP. Los difractogramas de NCs-PBAT / Cu | Cu 2 O tiene seis picos característicos a 2θ =36,4 °, 43 °, 42,4 °, 50 °, 61,5 ° y 74 ° (Fig. 2b). Según la literatura y el análisis de las nanopartículas, solo tres corresponden al metal Cu y los picos a 36,4 °, 42,4 ° y 61,5 ° pertenecen al Cu 2 O, según el espectro de este tipo de nanopartículas que se muestra en la Fig. 1a [35].
Los picos de difracción correspondientes a Cu | Cu 2 Los refuerzos de O-NP se volvieron más intensos a medida que aumentaba la concentración dentro de la matriz, pero los picos pertenecientes a la zona cristalina del polímero disminuían levemente en intensidad con la incorporación de cargas. Chivrac y col. [42] informó resultados similares en un estudio que utilizó cargas de nanoarcillas en PBAT. Sugirieron que no había una transcristalinidad significativa en la interfaz carga-polímero y, por lo tanto, no hubo cambios en la estructura cristalina del polímero. Sin embargo, la disminución de la intensidad de los picos de difracción del PBAT con el aumento de la concentración de cargas en la matriz indica una caída en la cristalinidad del PBAT. Por tanto, las cargas dificultan el crecimiento cristalino del PBAT. Esto podría explicar la leve disminución de los picos de difracción pertenecientes al PBAT con el aumento de Cu | Cu 2 O-NP.
La Figura 2c muestra los espectros XRD de MC-PBAT / CuSO 4 para las tres concentraciones de CuSO 4 de 1, 3 y 5%. La adición del 1% CuSO 4 La carga no generó cambios en el polímero. El 3 y 5% CuSO 4 Las curvas de carga muestran solo un aumento mínimo en la intensidad de los picos en 2θ =36,4 °, 40,25 °, 43,94 °, 57,9 ° y 75,7 °, que pertenecen al Cu y Cu 2 O presente, lo que indica que una fracción del Cu 2 SO 4 se redujo y oxidó durante el proceso de mezcla. En cuanto a la zona cristalina del PBAT, el aumento de la concentración del CuSO 4 Los refuerzos disminuyeron la intensidad de los picos de difracción en PBAT, como ocurrió para NCs-PBAT / Cu y NCs-PBAT / Cu | Cu 2 O. Así, la incorporación de CuSO 4 en la matriz de polímero disminuyó su capacidad de cristalización, probablemente porque CuSO 4 dificulta el crecimiento de cristalitos. Porque no hay información adicional sobre los espectros XRD de CuSO 4 en materiales compuestos, tendremos que investigar su comportamiento en polímeros biodegradables. El grado de cristalinidad de la matriz se calculó como:
$$ {X} _ {\ mathrm {c}} =\ frac {I _ {\ mathrm {c}}} {I _ {\ mathrm {c}} + {I} _ {\ mathrm {a}}} $$ (1)donde yo c es el área de los picos de la fase cristalina y I c + yo a es el área total debajo del difractograma. Los valores de grado de cristalinidad para cada material se dan en la Tabla 1. Estos resultados muestran que el porcentaje de cristalinidad aumenta a medida que la concentración de Cu-NP y Cu | Cu 2 Los O-NPs aumentan en la matriz PBAT, lo que se evidencia con el aumento de la intensidad de los picos en los respectivos difractogramas.
Por otro lado, los difractogramas muestran que las nanopartículas no afectaron ni modificaron la estructura del PBAT y que la intensidad de los picos es directamente proporcional al porcentaje de carga de los Cu-NPs y Cu | Cu 2 O-NPs. Además, la adición de CuSO 4 La sal precursora disminuyó la cristalinidad del polímero en comparación con la del polímero en su estado puro. Esta condición se produjo porque la adición de concentración de cargas en los nanocompuestos aumentó el porcentaje relativo de cristalinidad pero disminuyó la cristalinidad del PBAT, resultado que, en general, se informó como un ligero aumento en el porcentaje total de cristalinidad. El MCs-PBAT / CuSO 4 las cargas no presentaron picos cristalinos en sus espectros XRD. Por tanto, no contribuyeron al aumento de la cristalinidad, pero provocaron una disminución de la cristalinidad en la cadena del polímero, lo que explica la disminución del porcentaje total de cristalinidad en el material compuesto. Some studies have shown that metal nanoparticles act as centers of nucleation in the orientation of the polymer chains, which in turn increases the crystallinity of the polymer [43].
The FTIR (Additional file 1:Figure S6) spectra show that the characteristic peaks at different load concentrations are at the same frequency but have different intensities. The spectra show that as the concentration of nanoparticles in the polymer matrix increased, the intensity of the peaks corresponding to NCs-PBAT/Cu and NCs-PBAT/Cu|Cu2 O increased with respect to the PBAT. Therefore, there was no effective interaction between the chains of the PBAT and the nanoparticles. Had there been interaction, some of the signals in the FTIR spectrum would have been displaced as a result of the interaction of the functional groups of the polymer with the surface of the PBAT [40].
Mechanical Properties (Tensile Test)
To give multifunctionality to biopolymers, nanomaterials that provide special properties to a nanocomposite are usually incorporated. Their inclusion will change the mechanical properties of the material and the intensity of the changes is directly related to the union of the nanostructure with the polymer network [44]. We conducted tensile tests on the nanocomposites and the composite material. The tensile strength and maximum deformation values are summarized in Table 2.
Figure 3 shows the average curves of the tensile tests on the nanocomposites and composite material. As the permanent deformation of the material began, the effect of the concentration of the nanoparticles in the polymer could be distinguished. Figure 3a shows the results for NCs-PBAT/Cu. The results show that the inclusion of nanostructures did not considerably affect the elastic range but there were noticeable changes in the yield strength. As the concentration of the Cu-NPs increased, maximum resistance increased and maximum elongation decreased. These changes clearly indicate that the nanostructures harden the PBAT. At 3% concentration of Cu-NPs, the tensile strength slightly increased but the elongation percentage in the fracture decreased between 30 and 35%.
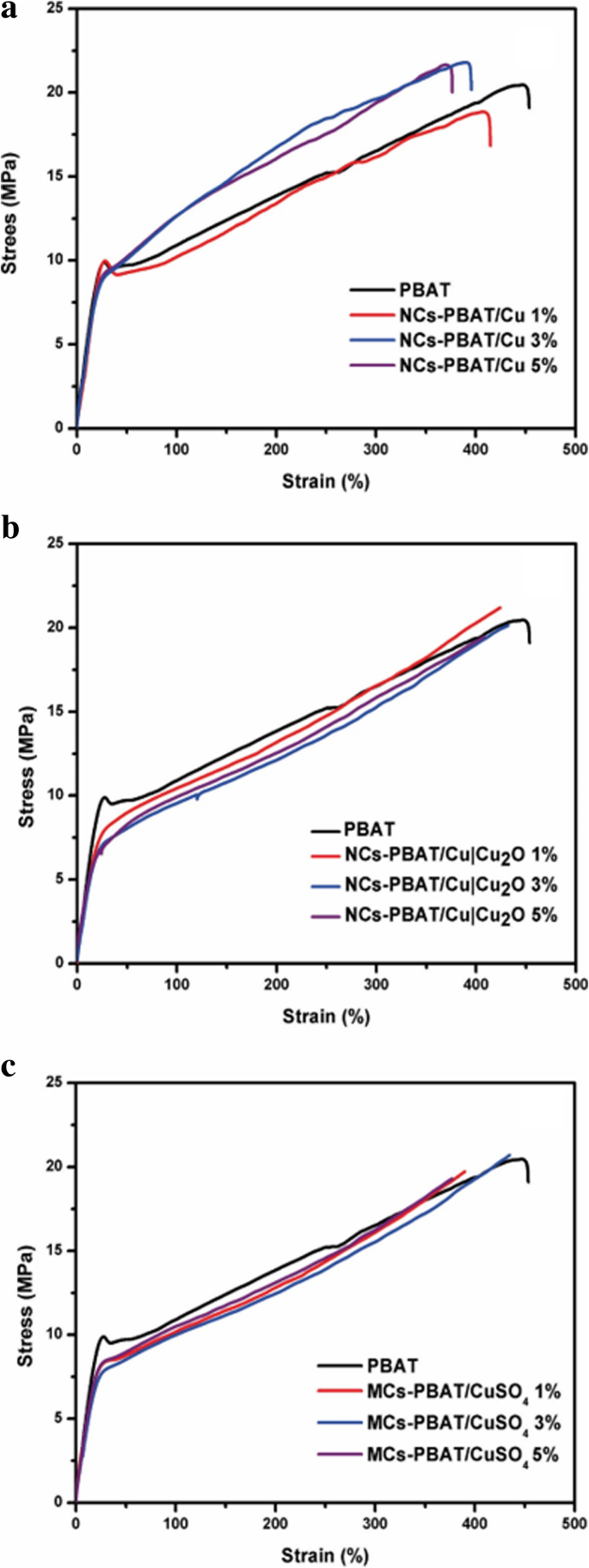
Stress and strain of PBAT, NCs-PBAT/Cu, NCs-PBAT/Cu|Cu2 O, and MCs-PBAT/CuSO4
Figure 3b shows the results of the tensile tests on the NCs-PBAT/Cu|Cu2 O. The 1% load nanocomposite clearly showed an increase in tensile strength and elongation with respect to the PBAT. There was no appreciable effect on the elastic range, but it did appear to be above the yield stress. In addition, the curve for the 3% load NCs-PBAT/Cu|Cu2 O shows there was no significant difference with respect to the PBAT. The same behavior is seen with curve for the 5% load NCs-PBAT/Cu|Cu2 O. The curves for MCs-PBAT/CuSO4 (Fig. 3c) show that the yield stress decreased for the three concentrations of CuSO4 with respect to the PBAT.
From the results, we can conclude that the reinforcements did not significantly change the mechanical properties of the PBAT. Venkatesan and Rajeswari [45] showed a significant increase in mechanical properties by incorporating ZnO nanoparticles in a PBAT matrix with respect to that of the PBAT. Similar results with some improvements were obtained by Chen and Yang [46]. They elaborated a PBAT nanocomposite with montmorillonite nanoparticles using melt blending.
Our investigation found that the NCs-PBAT/Cu|Cu2O 3 and 5% and MCs-PBAT/CuSO4 1 and 5% had slightly decreased tensile strength, that is, there were no significant variations in the mechanical properties. However, the NCs-PBAT/Cu|Cu2 O 1% and MCs-PBAT/CuSO4 3% had slightly increased tensile strength. Therefore, no reinforcement at any concentration in the matrix caused remarkable variations in the mechanical properties of the PBAT. In addition, as the concentration of Cu-NPs increased, their mechanical properties increased the resistance of the PBAT but elongation could not be maintained. The results of the tensile tests showed that the commercial Cu nanoparticles improved the tensile strength of the PBAT slightly more than did the Cu|Cu2 O nanoparticles and the CuSO4 partículas. The difference between the tensile properties found in our investigation and those in the literature could be attributed to load dispersion because the agglomerated particles act as stress concentrators [47]. Finally, the variations in the test values were explained by the preparation conditions of the test samples, the degree of crystallinity of the PBAT, the molecular mass, the degree of interaction at the polymer-reinforcement interface, and the load dispersion because the agglomerates in the matrix could act as stress concentrators.
Thermal Properties
One of the disadvantages of the PBAT is its low thermal stability because the fusion process can degrade its polymer chains [48]. Therefore, the effect of nanometric and micrometric loads on the decomposition of this biopolymer must be investigated. TGA of NCs-PBAT/Cu, NCs-PBAT/Cu|Cu2 O, and MCs-PBAT/CuSO4 was carried out to observe the changes in the thermal stability of the PBAT caused by the presence of Cu nanoparticles in the matrix. The TGA results are shown in Fig. 4, and the initial (T di ) and final (T df ) decomposition temperatures of the analyzed samples are summarized in Table 3. The thermograms show that the polymer without any load had a weight loss of 1% at 420.77 °C, while the nanocomposites NCs-PBAT/Cu 1, 3, and 5% presented a weight loss of around 3% (Fig. 4a). This suggests that the presence of Cu-NPs at concentrations of 3 and 5% slightly increases the thermal stability of the nanocomposites compared to that of the unloaded polymer. After the final thermal decomposition, the degradation percentages, at around 420–427 °C, of the PBAT matrix and nanocomposites NCs-PBAT/Cu 1, 3, and 5% were 98.9, 97.5, 95.4, and 96.8%, respectively. The residues were higher for Cu-NPs-incorporated nanocomposite samples. Similar results have been reported for PBAT nanocomposites with different loads of Ag-NPs [49].
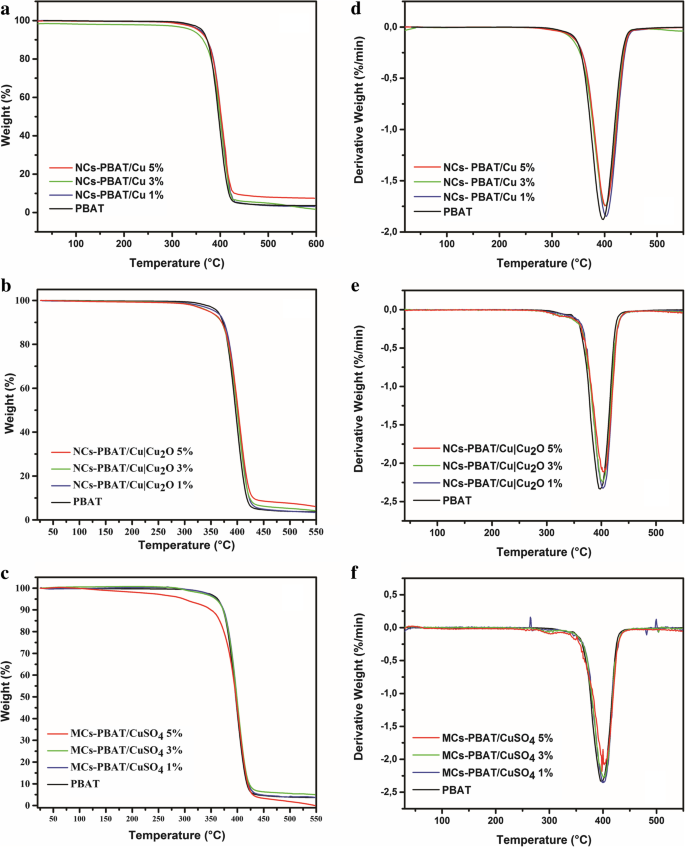
TGA of a PBAT and NCs-PBAT/Cu, b NCs-PBAT/Cu|Cu2 O, and c MCs-PBAT/CuSO4 , DTG of d PBAT and NCs-PBAT/Cu, e NCs-PBAT/Cu|Cu2 O, f MCs-PBAT/CuSO4
Although no significant change is seen among the curves in Fig. 4b for the NCs-PBAT/Cu|Cu2 O, the results show that as the Cu|Cu2 O-NPs increased in the polymer structure, T di increased and T df decreased with respect to the initial and final degradation temperatures of PBAT; in addition, the total mass loss decreased. By calculating the derivative of the mass with respect to the temperature, we obtained the curves in Fig. 4d–f for the indicated peaks of the nanocomposite with Cu|Cu2 O-NPs and found that T df , at which the maximum decomposition occurs, was between 402 and 403 °C (Table 3).
The CuSO4 loads incorporated into the polymer matrix, i.e., MCs-PBAT/CuSO4 , yielded the same behavior as that of the NCs-PBAT/Cu|Cu2 O, with an increase in T di and a decrease in T df with respect to the PBAT polymer. The T di values of the NCs-PBAT/Cu|Cu2 O and the MCs-PBAT/CuSO4 were greater than that of the NCs-PBAT/Cu, but the T df and degradation percentage values were less than those of the nanocomposites with Cu-NPs loads.
This enhancement of the thermal stability of the PBAT is attributed to the barrier effect of the loads. The loads were also supposed to have a shielding effect on the matrix to slow the rate of mass loss of the decomposition product [50]. The data obtained by our analysis were compared with published results to verify that the indicated behavior is usual for this type of polymer. Sinha Ray et al. [51] found by thermal analysis of PBAT reinforced with nanoclays that the degradation temperatures of the nanocomposites were greater than or at least equal to that of the PBAT. In general, the reinforcements improve the thermal stability of the polymer matrix because they act as a heat barrier, which improves the total thermal stability of the system. However, the studies of Sinha Ray et al. and this investigation showed that the thermal stability of the nanocomposite and PBAT compounds only slightly improved. To explain the relatively low improvement in the thermal stability of some nanocomposites, Sinha Ray et al. assumed that in the early stages of thermal decomposition, the reinforcements displace the decomposition to higher temperatures, but in a second stage, the clay layers accumulate heat and then act as a source of heat. This heat source, along with the heat flow supplied by the external heat source, promotes the acceleration of decomposition. This could explain the behavior of the reinforcements in the NCs-PBAT/Cu|Cu2 O and MCs-PBAT/CuSO4 . Thus, we conclude that the thermal properties of the nanocomposites and the composite material slightly improve but not significantly. On the other hand, the results of DSC (Additional file 1:Figure S7 and Table S1) indicated that the addition of reinforcements to the matrix slightly hindered the kinetics and degree of crystallization of the PBAT. The addition of clays increased the crystallization temperature from 1 to 10 °C and the melting temperature from 1 to 5 °C. These phenomena were probably due to an increase in the viscosity of the polymer with the addition of clays, which reduced the mobility of the macromolecular chains against the growth of crystals.
Comparative Evaluation of the Antimicrobial Activity of NCs-PBAT/Cu, NCs-PBAT/Cu|Cu2 O, and MCs-PBAT/CuSO4
Qualitative Test
After the experimental procedure was performed, we wanted to observe whether bacterial colonies were inhibited by each PBAT sample, i.e., NCs-PBAT/Cu 1, 3, and 5%; NCs-PBAT/Cu|Cu2 O 1, 3, and 5%; and MCs-PBAT/CuSO4 1, 3, and 5%. We decided to use the 3% concentrations because the 1% concentrations did not produce enough bacterial inhibition and the 5% concentration produced behavior similar to that of the 3% concentration, the minimum percentage with activity that avoided toxicity in the polymer.
Quantitative Test
The study was carried out at different contact times using four bacterial strains and the PBAT samples NCs-PBAT/Cu 3%, NCs-PBAT/Cu|Cu2 O 3%, and MCs-PBAT/CuSO4 3%. The times and colony-forming unit counts (CFU/mL) are presented in Table 4, and the bacterial activity and colony count for each Petri dish are shown in Fig. 5. In addition, a graphical analysis is shown in Fig. 6, where images of bacterial growth are also presented. The statistical analysis of the data is summarized in Table 5.
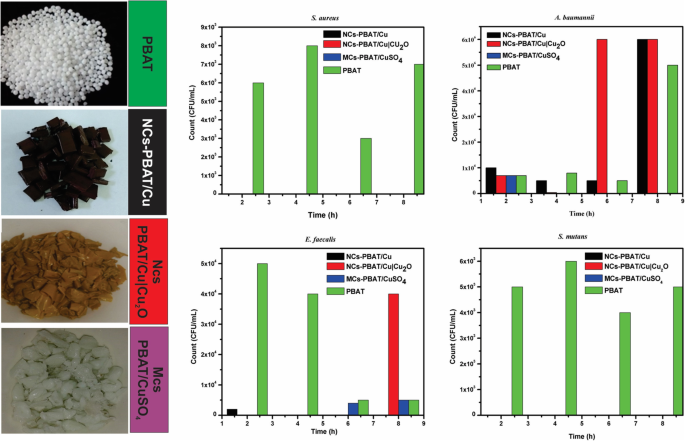
Bacterial activity and colonization count PBAT, NCs-PBAT/Cu-3%, NCs-PBAT/Cu|Cu2 O 3%, and MCs-PBAT/CuSO4 3% for each strain of bacteria. Staphylococcus aureus , Acinetobacter baumanni , Enterococcus faecalis , Streptococcus mutans
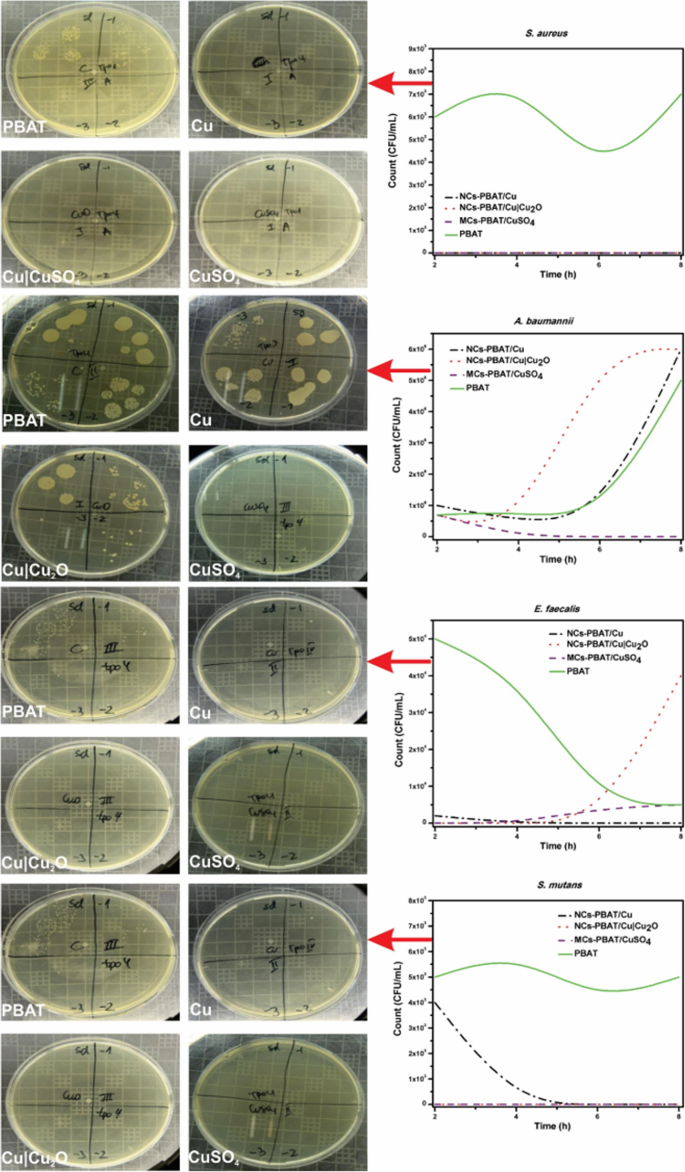
Graphical analysis of colony count (CFU/mL) vs time (h) of PBAT, NCs-PBAT/Cu-3% NCs-PBAT/Cu|Cu2 O 3%, and MCs-PBAT/CuSO4 3% for each strain of bacteria. Enterococcus faecalis , Acinetobacter baumanni , Streptococcus mutans , Staphylococcus au reus
The study of A. baumannii found that the colonies grew in all periods (2, 4, 6, and 8 h) in the samples containing Cu-NPs, Cu|Cu2 O-NPs, and PBAT. High bactericidal activity occurred with the sample containing CuSO4 during exposure times of 4, 6, and 8 h, decreasing from 7 × 10 5 to 0 CFU/mL. The sample containing Cu-NPs showed a significant increase in the growth of bacterial colonies from 1 × 10 5 to 6 × 10 6 CFU/mL, with an average of 2 × 10 6 CFU/mL. The bacterial colonies in the sample containing Cu|Cu2 O-NPs grew from 7 × 10 5 in time I to 6 × 10 6 in time IV, with an average growth of 3.19 × 10 6 CFU/mL. Bacterial growth in the PBAT reached an average of 1.75 × 10 6 CFU/mL.
The study of E. faecalis found good bactericidal activity by the samples containing Cu-NPs, Cu|Cu2 O-NPs, and CuSO4 , with average colony growth of 5 × 10 2 , 1 × 10 4 , and 2.2 × 10 3 CFU/mL, respectively, while the PBAT did not show bactericidal activity and the colonies grew at all times. Colony growth in the sample containing Cu-NPs was 2 × 10 3 CFU/mL at 2 h then dropped to zero at 4, 6, and 8 h, whereas the samples containing Cu|Cu2 O-NPs had 0 CFU/mL at times I, II, and III, but 4 × 10 4 CFU/mL at time IV. Samples containing CuSO4 prevented the growth of bacteria in times I and II with growth activity of 0 CFU/mL, but colonies grew to 4 × 10 3 and 5 × 10 3 CFU/mL for times III and IV, respectively. PBAT did not show bactericidal activity against E. faecalis .
The study of S. mutans found no colony growth in the samples containing Cu|Cu2 O-NPs and CuSO4 . The sample containing Cu-NPs showed very good bactericidal activity except at time I, at which colony growth was 4 × 10 3 CFU/mL, making the average growth for the four times 8 × 10 2 CFU/mL. PBAT without reinforcement showed no bactericidal activity against S. mutans . The samples containing Cu-NPs, Cu|Cu2 O-NPs, and CuSO4 in contact with S. aureus showed an excellent bactericidal response. They completely inhibited the growth of colonies, while PBAT did not show any bactericidal activity against S. aureus , which grew an average of 6 × 10 3 CFU/mL.
In general, the antibacterial effectiveness of polymer-and-metal nanocomposites improves with a high surface/volume ratio, which increases the number of ions released from the nanoparticles into the polymer. The mechanism of the corrosion of Cu in aqueous solutions and the resulting Cu species vary with pH. In general, the species Cu2 O and CuO are formed and can be dissolved in Cu ions. Elemental metal particles require the presence of water and oxygen molecules to release a small amount of ions. Therefore, retention of water and oxygen within the polymer is crucial for the release of Cu ions. Some properties of polymer-and-metal nanocomposites such as the crystallinity and polarity of the matrix, which constitute a barrier for the diffusion of water molecules and ions during their propagation, can affect the rate of release. Shankar and Rhim [49] prepared films composed of PBAT and Ag nanoparticles (PBAT/Ag-NPs) that showed strong antibacterial activity against E. coli and Listeria monocytogenes compared with that of PBAT films without Ag-NPs. Similar results were obtained by Venkatesan and Rajeswari [45] when they evaluated the antimicrobial activity of ZnO-NPs incorporated in a PBAT matrix. The PBAT compound, which was used as a control matrix, showed no antimicrobial activity compared to the PBAT/ZnO-NPs nanocomposite films. The results showed that the films had high bactericidal activity against the pathogens tested (E. coli y S. aureus ), with increased inhibition of bacterial growth as the ZnO load concentration increased from 1 to 10% by weight. This ability of Cu, Zn, and Ag nanoparticles to inhibit bacterial growth is mainly due to the irreparable damage to the membrane of the bacterial cells caused by the interaction between the surface of the bacteria and these oxides and metals [52, 53]. Compared with the works discussed above, our investigation found significant antimicrobial activity against inpatient and oral-resistant strains.
To complement this investigation, we performed water absorption tests using three different media and following point 7.4, “Long-Term Immersion”, in ASTM D570-98. The results of these tests are reported in the supplementary material, Additional file 1:Table S2–S4 and Figure S8, with their respective analysis. Analysis showed that sulfate-based composite materials absorb large amounts of water, even in acidic and basic environments. This phenomenon greatly affects the mechanical properties of these materials; however, resistant bacteria, such as A. baumannii , require an immediate Cu + distribution to control them. This explains the antimicrobial power of CuSO4 within the PBAT matrix.
Conclusiones
Using XRD and TEM, we determined that the synthesis of nanocomposites and material composites based on PBAT using chemical reduction and a mixture of metal Cu nanoparticles with CuO2 , where Cu had a spherical morphology and Cu2 O had a polyhedral morphology. The structural characterization of the NCs and MCs by FTIR and XRD showed that the Cu-NPs, Cu|Cu2 O-NPs, and CuSO4 reinforcements did not modify the structure of the PBAT. However, they did slightly alter the percentage of its crystallinity, which increased with NPs and decreased with CuSO4 . On the other hand, the mechanical properties of the PBAT for both the NCs and MCs did not vary significantly with the addition of reinforcements, meaning that the PBAT maintained its mechanical properties. From the thermal tests, we concluded that reinforcing the PBAT did not fundamentally improve its thermal properties, it only increased its thermal stability a few degrees Celsius, which is not significant. Antimicrobial analyses showed that the Cu|Cu2 O-NPs within the PBAT generated antibacterial activity against E. faecalis y S. mutans and excellent bactericidal properties against S. aureus . CuSO 4 had a good bactericidal response against A. baumannii , E. faecalis , and S mutans and an exceptional response against S. aureus . The PBAT without loads did not present bactericidal properties when in contact with the bacterial strains. In general, the addition of loads into the PBAT generates bactericidal activity that the polymer does not possess by itself. The addition of CuSO4 yielded the best antimicrobial response against the four strains used in this investigation. In the search for new applications for bionanocomposites, it will be essential to evaluate their antimicrobial response in food containers, medical devices, packaging, and other products; analyze their biocidal effects against other bacteria against which only NPs have antibacterial characteristics; and justify the expense associated with their synthesis.
Abreviaturas
- Cu|Cu2 O-NPs:
-
Copper/cuprous oxide nanoparticles
- Cu-NPs:
-
Nanopartículas de cobre
- CuSO4 :
-
Copper sulfate
- DSC:
-
Calorimetría diferencial de barrido
- FTIR:
-
Espectroscopia infrarroja por transformada de Fourier
- MC:
-
Composite material
- MCs-PBAT/CuSO4 :
-
Composite materials of poly(butylene adipate-co-terephthalate) with copper sulfate
- NC:
-
Nanocomposites
- NCs-PBAT/Cu:
-
Nanocomposites of poly(butylene adipate-co-terephthalate) with copper nanoparticles
- NCs-PBAT/Cu|Cu2 O:
-
Nanocomposites of poly(butylene adipate-co-terephthalate) with copper/cuprous oxide nanoparticles
- PBAT:
-
Poly(butylene adipate-co-terephthalate)
- TEM:
-
Microscopía electrónica de transmisión
- TGA:
-
Análisis termogravimétrico
- XRD:
-
Difracción de rayos X
Nanomateriales
- Preparación y propiedades magnéticas de nanopartículas de espinela de FeMn2O4 dopadas con cobalto
- El efecto del plasma de no equilibrio por contacto sobre las propiedades estructurales y magnéticas de Mn Х Fe3 - X О4 Espinelas
- Formación y propiedades luminiscentes de Al2O3:nanocompuestos de SiOC en la base de nanopartículas de alúmina modificadas por feniltrimetoxisilano
- Propiedades paramagnéticas de nanomateriales derivados del fullereno y sus compuestos poliméricos:efecto de bombeo drástico
- Efecto sinérgico del grafeno y los MWCNT en la microestructura y las propiedades mecánicas de los nanocompuestos de Cu / Ti3SiC2 / C
- Nanocompuestos magnéticos de poli (N-isopropilacrilamida):efecto del método de preparación sobre las propiedades antibacterianas
- Efecto catalítico de los clústeres de Pd en la combustión de poli (N-vinil-2-pirrolidona)
- Una metodología de dos pasos para estudiar la influencia de la agregación / aglomeración de nanopartículas en el módulo de Young de nanocompuestos poliméricos
- Dependencias de temperatura y presión de las propiedades elásticas de los cristales individuales de tantalio bajo una carga de tracción <100>:un estudio de dinámica molecular
- Estudio comparativo de las propiedades electroquímicas, biomédicas y térmicas de nanomateriales naturales y sintéticos
- Síntesis verde de nanopartículas de metal y óxido de metal y su efecto sobre el alga unicelular Chlamydomonas reinhardtii



