Efecto catalítico de los clústeres de Pd en la combustión de poli (N-vinil-2-pirrolidona)
Resumen
El Pd (0) es capaz de catalizar reacciones que involucran oxígeno debido a su capacidad para convertir oxígeno molecular en una forma atómica muy reactiva. En consecuencia, la inclusión de una pequeña cantidad de agrupaciones de Pd (0) en fases poliméricas puede aprovecharse tecnológicamente para mejorar la cinética de incineración de estos polímeros. El efecto de la nanoestructuración sobre la actividad catalítica de Pd (0) en la reacción de incineración del polímero se ha estudiado utilizando poli ( N -vinil-2-pirrolidona) (\ (\ overline {Mw} \) =10,000 gmol −1 ) como sistema de modelo polimérico. Se encontró experimentalmente un cambio en el mecanismo cinético de incineración de PVP con un aumento significativo en la velocidad de reacción. La cinética de la combustión catalizada por Pd (0) se ha estudiado mediante análisis termogravimétrico isotérmico. Después de un corto tiempo de inducción, la combustión en presencia de grupos de Pd (0) cambió a una cinética de orden cero desde un control cinético de segundo orden, que está operativo en la reacción de combustión de PVP pura. Además, la energía de activación resultó mucho más baja en comparación con el caso de incineración de PVP puro (de 300 a 260 kJ / mol).
Antecedentes
A escala nanoscópica, los metales nobles muestran propiedades catalíticas anormalmente aumentadas, lo que se conoce como "efecto supercatalítico" [1, 2]. No solo aumenta el número de sitios catalíticos con la disminución del diámetro del cristal, debido al aumento de la relación superficie / volumen (la relación superficie / volumen para una partícula esférica es 3 / R), sino también la naturaleza del sitio catalítico (es decir, La acidez de Lewis) se ve fuertemente afectada [1]. En particular, la acidez de Lewis de los sitios catalíticos aumenta con la disminución del tamaño debido a que cambia la abundancia relativa de diferentes sitios catalíticos. Según modelos teóricos, como por ejemplo el “modelo cúbico” [3], la distribución de los diferentes tipos de sitios (es decir, sitios de plano basal, borde y esquina) en un cristal de metal noble se revoluciona al disminuir el diámetro del cristal [1 ]. De hecho, en algunos polvos de micras, los planos basales cristalinos son los más abundantes, mientras que los sitios de borde y / o esquina prevalecen en un sistema de cristal nanoscópico [2]. Debido al menor número de coordinación de estos sitios, sigue una actividad catalítica diferente. Además, como también la actividad, la selectividad y especificidad de los sitios catalíticos se modifican [4, 5].
La incineración de polímeros es un proceso químico tecnológicamente relevante, que involucra oxígeno y tiene lugar a temperaturas relativamente altas [6, 7]. El PVP es un polímero común, explotado industrialmente en varios campos (cosmético, biomédico, como excipiente en fármacos, etc.), por lo que fue seleccionado como el “polímero modelo” a estudiar. Además, la incineración de PVP es tecnológicamente relevante en sinterización de cerámica [8], fabricación de sensores de cerámica [8, 9], fabricación de electrodos de batería [6], destrucción de desechos [10, 11], desarrollo de propulsores sólidos [12, 13], etc. .
Aquí, hemos descubierto que el proceso de incineración de PVP puede beneficiarse de la presencia de un catalizador de metal noble de tamaño nanométrico, probablemente porque es capaz de convertir cuantitativamente el oxígeno molecular (O 2 ) a los átomos de oxígeno más agresivos (O ·) [14, 15]. Todos los tipos de combinaciones de metales nobles / PVP se pueden sintetizar fácilmente, en una forma muy homogénea, utilizando la técnica de proceso de poliol muy común [16,17,18,19,20,21,22]. En este estudio, el Pd ha sido seleccionado como un metal catalítico ya que se puede lograr en un tamaño extremadamente pequeño mediante este esquema de reacción simple [21, 22].
La incineración de polímeros se puede estudiar fácilmente mediante el análisis termogravimétrico (TGA) [7]. En particular, para este análisis cinético se han utilizado pruebas de TGA isotérmicas, realizadas a temperaturas superiores a la temperatura de ignición de PVP. Las pruebas de TGA isotérmica se realizaron a cuatro temperaturas diferentes ligeramente por encima de 370 ° C, que corresponde a la temperatura de inicio de degradación en un termograma de TGA dinámico. No se investigaron temperaturas superiores a 440 ° C porque la velocidad de reacción resultó demasiado alta para una monitorización de TGA satisfactoria. Para establecer el mecanismo de combustión involucrado, (i) el orden de reacción, (ii) la constante cinética, (iii) y los valores de energía de activación se han valorado a partir de los datos de TGA isotérmicos de las combustiones de PVP puro y nano-Pd / PVP.
Experimental
Las muestras se prepararon de acuerdo con un método de la bibliografía [22]. En particular, poli ( N -vinil-2-pirrolidona) (PVP, Aldrich, \ (\ overline {Mw} \) =10,000 gmol −1 ) se disolvió en etilenglicol seco (EG, Aldrich, 99,8%) y la solución se colocó en un baño termostático a 90 ° C en aire, hasta su completa disolución. En una preparación típica, se disolvieron 24 g de polvo de PVP en 70 ml de EG. Por separado, un volumen menor (10 ml) de una solución concentrada de tetracloropalladato de potasio (II) (K 2 PdCl 4 , Aldrich, 99,99%) en EG (0,35% en peso de sal) y se inyectó rápidamente en la solución PVP / EG caliente agitada vigorosamente. La concentración de PVP en EG fue 30 mM y la relación molar Pd (II):PVP fue 1:10. Después de calentar durante 120 min, la solución se vertió en una gran cantidad de acetona para flocular el sistema nano-Pd / PVP. El producto se secó al aire y se almacenó a temperatura ambiente en un desecador. También se preparó un segundo tipo de muestras de nano-Pd / PVP dispersando un polvo comercial de Pd (0) de tamaño micrométrico (Pd, Aldrich, tamaño de partículas <1 μm, 99,9%) en PVP que tiene el mismo peso molecular. La concentración de dispersión fue similar a la utilizada para el Pd de tamaño nanométrico en muestras de PVP (0,3% en peso).
La morfología de los grupos de Pd se investigó en una forma incrustada en PVP mediante el uso de microscopía electrónica de transmisión (TEM, aparato FEI Tecnai G2 Spirit gemelo) operado a 120 kV, y después del proceso de combustión, se obtuvieron imágenes del producto residual usando microscopía electrónica de barrido ( Aparato SEM, FEI QUANTA 200 FEG).
Según la literatura [23, 24], las propiedades de combustión del poli ( N puro) -vinil-2-pirrolidona) (PVP) y muestras de nano-Pd / PVP se investigaron mediante análisis termogravimétrico (TGA, Q5000, TA Instruments) en atmósfera oxidativa (aire en movimiento) en condiciones de presión estándar. El proceso de combustión se investigó quemando muestras de PVP y nano-Pd / PVP en ambas dinámicas (desde temperatura ambiente hasta 600 ° C, a una velocidad de calentamiento de 10 ° C min −1 ) y condiciones isotérmicas, bajo flujo de aire (25 mL min −1 ). La temperatura de las pruebas isotérmicas de TGA se tomó por encima de la temperatura de ignición (inicio) determinada por el escaneo dinámico de TGA. Se registraron datos isotérmicos para todas las muestras hasta una pérdida de peso completa.
Resultados y discusión
En la Fig. 1a se muestra una micrografía TEM representativa de muestras de nano-Pd / PVP. Los grupos de Pd sin contacto, que tienen un tamaño de 2.8 ± 0.2 nm (ver Fig. 1b), parecen estar uniformemente dispersos en la matriz de PVP.
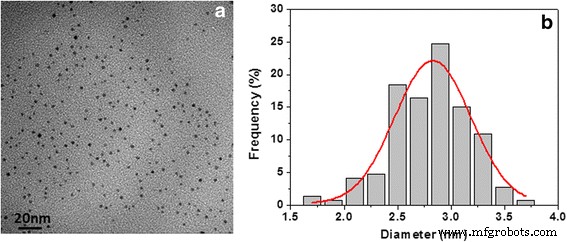
Micrografía TEM de una muestra de nano-Pd / PVP ( a ) y distribución del tamaño de partícula ( b )
La micrografía SEM mostrada en la Fig. 2 evidencia que, en presencia del catalizador de Pd (0), la combustión de PVP resultó completa. De hecho, el producto de combustión constaba únicamente de racimos de Pd agregados, sin trazas de ningún residuo orgánico. En particular, esta muestra de nano-Pd / PVP se quemó en una balanza termogravimétrica, en condiciones dinámicas (es decir, de temperatura ambiente a 600 ° C, a una velocidad de calentamiento de 10 ° C min −1 ), usando aire de flujo (25 ml min −1 ). La estructura metálica continua ha sido generada por la sinterización de racimos adyacentes de Pd (0) después de la remoción de PVP.

Micrografía SEM del producto TGA residual (polvo de paladio)
Los procesos de combustión para muestras de PVP puro y nano-Pd / PVP se estudiaron mediante análisis termogravimétrico dinámico e isotérmico (TGA). La TGA dinámica permitió determinar a qué temperatura comienza la combustión (es decir, la temperatura de ignición) y finaliza, y brindó información general sobre la cinética de reacción y otros parámetros que caracterizan el comportamiento de la combustión. En la figura 3 se presenta un análisis comparativo de las curvas TGA (índice de pérdida de peso) y DTG (índice de pérdida de peso) para muestras de PVP puro y nano-Pd / PVP. La forma de las curvas indica que la mayor pérdida de peso se produce entre 400 y 500 ° C. Las muestras de PVP puro y nano-Pd / PVP difieren en reactividad, como lo demuestran claramente las desviaciones en la tasa de descomposición máxima y la tendencia de la curva de pérdida de peso de nano-Pd / PVP, que en general es más rápida en comparación con la de PVP puro. De hecho, la presencia de una cantidad muy pequeña de catalizador de Pd afecta la degradación térmica del polímero tanto antes como después de la ignición (ver Fig. 3a). Además, una pérdida de peso residual de aprox. 0.3%, debido al contenido de catalizador de Pd, es claramente visible en el nano-Pd / PVP TGA. Las curvas DTG de muestras de PVP puro y nano-Pd / PVP exhiben una tasa de descomposición máxima de aprox. 420 ° C (ver Fig. 3b). Además, la curva nano-Pd / PVP muestra un segundo pico que se anticipa visiblemente en comparación con el PVP puro (470 ° C en lugar de 540 ° C).
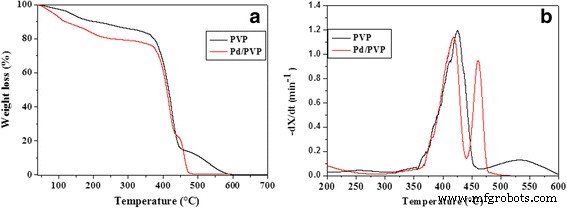
Pérdida de peso ( a ) y tasa de pérdida de peso ( b ) correspondiente a la combustión de PVP puro (negro) y nano-Pd / PVP (rojo), realizada a una velocidad de calentamiento de 10 ° C min −1
El análisis isotérmico de TGA se utilizó para estudiar la cinética de combustión del PVP catalizado por Pd (0). La Figura 4 muestra la fracción de pérdida de peso isotérmica, X ( t ), en función del tiempo durante el proceso de combustión para muestras de PVP puro y nano-Pd / PVP a temperaturas ligeramente superiores a la temperatura de ignición. La fracción de pérdida de peso se define como X ( t ) = w ( t ) / w 0 , donde w 0 y w ( t ) se refieren al peso inicial y al peso en el momento t , respectivamente. El análisis termogravimétrico isotérmico se realizó a cuatro temperaturas diferentes:400, 420, 430 y 440 ° C.
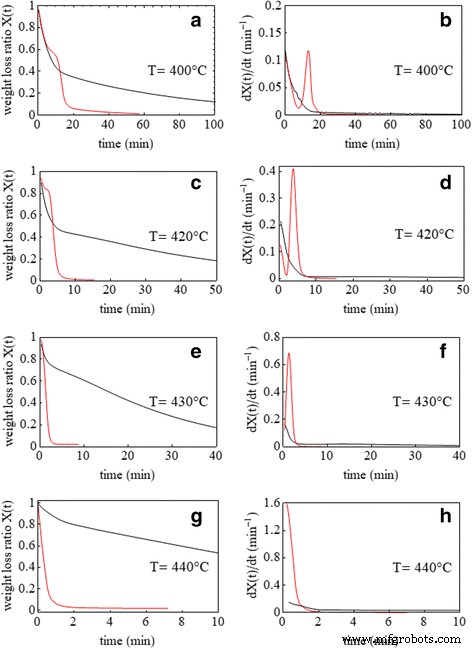
Relación de pérdida de peso isotérmica en función del tiempo durante la combustión de PVP puro (curvas negras) y nano-Pd / PVP (curvas rojas) a 400 ° C ( a ), 420 ° C ( c ), 430 ° C ( e ) y 440 ° C ( g ) y las correspondientes curvas derivadas ( b , d , f , h )
Dos etapas de combustión son visibles en los termogramas (ver Fig. 4):en la primera etapa, se encuentra un comportamiento de pérdida de peso similar, caracterizado por curvas perfectas que se superponen, tanto para muestras de PVP puro como para muestras de nano-Pd / PVP. Esta etapa tiende a acortarse con el aumento de temperatura. En la segunda etapa, la curva de pérdida de peso de nano-Pd / PVP disminuye muy rápidamente y luego se nivela para volverse asintótica con respecto al contenido residual de Pd. Estas dos etapas están vinculadas entre sí a través de un breve intervalo de tiempo en el que la pérdida de peso se mantiene casi constante.
Este comportamiento probablemente pueda atribuirse al tiempo necesario para saturar la superficie de Pd con oxígeno molecular [9]. El catalizador de Pd es capaz de convertir cuantitativamente el oxígeno molecular de baja reactividad (O 2 ) a una especie de oxígeno atómico muy reactivo. Por lo tanto, en la primera etapa, común a la combustión de PVP y nano-Pd / PVP, solo el oxígeno molecular juega el papel dominante en la reacción, mientras que el oxígeno atómico juega un papel importante en la segunda etapa de la combustión de nano-Pd / PVP.
La curva de pérdida de peso de la PVP pura alcanza su valor asintótico solo después de un tiempo muy largo y, según el análisis de regresión aplicado, sigue un comportamiento cinético de segundo orden. De manera diferente, las curvas nano-Pd / PVP caen rápidamente a sus valores asintóticos (ver Fig. 4) siguiendo un comportamiento lineal, lo que sugiere un control cinético de orden cero para esta segunda etapa de combustión. En particular, un factor de correlación de R 2 =0,98 se encontró para todas las curvas. Los valores estimados de las constantes cinéticas tanto en presencia como en ausencia del catalizador Pd (0) se dan en la Tabla 1 para cada temperatura de combustión.
Para determinar la energía de activación para la etapa rápida del proceso de combustión de nano-Pd / PVP, el k =A · exp (−E a / RT) La ecuación de Arrhenius se ha utilizado para ajustar las constantes cinéticas a diferentes temperaturas. La constante A es el factor de frecuencia, E a es la energía de activación, y R es la constante del gas. La gráfica de Arrhenius (ln (k) vs. 1 / T) se muestra en la Fig. 5. La línea continua es el ajuste lineal de las constantes cinéticas experimentales, y su pendiente depende de la energía de activación ( E a ). El factor preexponencial calculado, A , fue 1,7 × 10 19 min −1 (ln (A) =44,3) y la energía de activación ( E a ) fue ca. 260 kJ / mol. A modo de comparación, la Fig. 5 muestra también el gráfico de Arrhenius de las constantes cinéticas para la combustión de PVP puro. El factor preexponencial calculado A fue 7,7 × 10 21 min −1 (ln (A) =50,4) y la energía de activación ( E a ) fue ca. 300 kJ / mol, determinado a partir de la pendiente del ajuste lineal a las constantes cinéticas (puntos negros) de la combustión PVP.
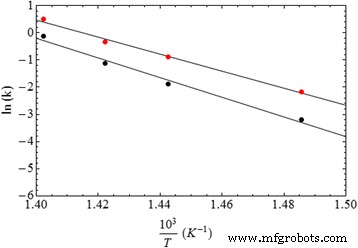
Gráfico de Arrhenius para muestras de PVP puro (puntos negros) y nano-Pd / PVP (puntos rojos)
Según la Fig.5 y los datos mostrados en la Tabla 1, la presencia del catalizador de paladio tiene el efecto global de disminuir la energía de activación de la combustión del polímero, permitiendo que la reacción se acelere (valores de constante cinética más altos).
El conocimiento de la energía de activación, E a , ayuda a desarrollar hipótesis sobre el mecanismo de reacción. De hecho, al comparar E a con los valores tabulados de las energías de enlace, se puede determinar cuál es el paso limitante de la velocidad en la reacción de combustión que se investiga. La energía de activación calculada, E a =260 kJ / mol, es aproximadamente la mitad de la energía del doble enlace del oxígeno molecular (498,36 ± 0,17 kJ / mol) [25]. Dado que la energía de enlace simple del oxígeno está bastante cerca de la energía de activación medida, se puede concluir que la formación de oxígeno atómico (O 2 → 2O) tiene lugar en la superficie del racimo de paladio y es el paso limitante de la velocidad de combustión de nano-Pd / PVP. De hecho, en condiciones de flujo de oxígeno (concentración constante de oxígeno), el orden cinético de este proceso elemental es como cero. Otros procesos elementales involucrados en el mecanismo de combustión catalizada, que pueden indicarse esquemáticamente como PVP + O → productos gaseosos , debería tener lugar en una escala de tiempo mucho más rápida que el paso de formación de oxígeno atómico.
La nanoestructuración de la fase de paladio juega un papel importante en este proceso de combustión catalítica. De hecho, la incrustación de un polvo micrónico de Pd (0) en la fase PVP, utilizando la misma cantidad de muestras de nano-Pd / PVP sintetizadas (0,3% en peso), no afecta la cinética de la reacción (ver Fig.6) . En dicha figura, se comparan la fracción de pérdida de peso de la PVP pura, de la muestra de Pd / PVP preparada usando un polvo micrónico y de la muestra de nano-Pd / PVP sintetizada. Las comparaciones se realizan a temperaturas de 420 ° C (Fig. 6a) y 440 ° C (Fig. 6b), respectivamente. El efecto catalítico mejorado del Pd de tamaño nanométrico en comparación con el polvo de Pd micrométrico es visualmente evidente. La actividad catalítica del Pd de tamaño nanométrico aumenta; gracias a su alta superficie específica y a la reactividad mejorada del sitio catalítico.
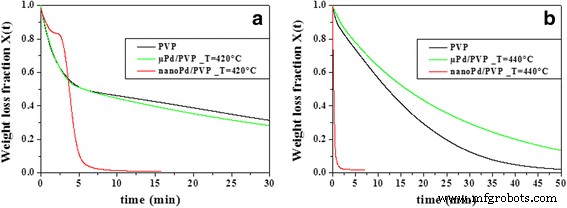
Relación de pérdida de peso isotérmica en función del tiempo durante la combustión de PVP puro (curvas negras), μ-Pd / PVP (curvas verdes) y nano-Pd / PVP (curvas rojas) a 420 ° C ( a ) y 440 ° C ( b )
Como consecuencia de dicho mecanismo cinético (formación de oxígeno atómico como un paso limitante de la velocidad), también podría esperarse un efecto del catalizador de Pd de tamaño nanométrico en la combustión de otros polímeros. Por lo tanto, el catalizador de Pd de tamaño nanométrico podría explotarse industrialmente en la incineración de polímeros.
Conclusiones
En este artículo, hemos investigado el efecto catalítico de los racimos de paladio en la reacción de incineración de PVP. Se seleccionó PVP como el "polímero modelo" para estudiar la incineración en presencia de una cantidad catalítica (0,3% en peso) de racimos de Pd (0) de tamaño nanométrico (diámetro de aproximadamente 2,8 nm). Hemos encontrado que la incineración de polímeros realizada en presencia de racimos de Pd de tamaño nanométrico es promovida por la acción de los átomos de oxígeno, que son más reactivos que la forma molecular. Después de un breve tiempo de inducción, se demostró que la presencia de catalizador nanoscópico de Pd (0) determinaba una combustión casi instantánea de la PVP. Los datos de TGA isotérmicos de la reacción de combustión de nano-Pd / PVP se han elaborado para determinar el mecanismo de combustión, las constantes cinéticas, el orden de reacción y la energía de activación. Según el análisis cinético, se ha propuesto un mecanismo de reacción que implica la formación catalítica de oxígeno atómico como un paso limitante de velocidad de orden cero. Los grupos de Pd de tamaño nanométrico han demostrado exhibir un efecto supercatalítico en comparación con el polvo micrométrico de Pd en la incineración de PVP. Este efecto catalítico del Pd de tamaño nanométrico podría ser de interés para la incineración de otros polímeros.
Nanomateriales
- Comprender el efecto del flujo de caja de los robots
- ¿Qué es el efecto piel?
- El efecto Nike:el ciclo de innovación de la Industria 4.0 en la práctica
- El efecto de las temperaturas criogénicas en los materiales plásticos
- El efecto del pH en los tintes amarillos del jardín
- El efecto de una pequeña cantidad de SiO2 en la cinética de sinterización de nanopolvos tetragonales de zirconia
- El efecto de los aniones sulfato en la nucleación de titania ultrafina
- El efecto del plasma de no equilibrio por contacto sobre las propiedades estructurales y magnéticas de Mn Х Fe3 - X О4 Espinelas
- Efecto del tratamiento de recocido in situ sobre la movilidad y morfología de transistores de efecto de campo orgánico basados en TIPS-pentaceno
- Efecto del polietilenglicol en el fotocátodo de NiO
- Nanocompuestos magnéticos de poli (N-isopropilacrilamida):efecto del método de preparación sobre las propiedades antibacterianas



